文档内容
2024 年江西省新高考化学试卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项符合题目要求。
1. 景德镇青花瓷素有“国瓷”的美誉。是以黏土为原料,用含钴、铁的颜料着色,上釉后一次性高温烧制而
成的青蓝色彩瓷。下列关于青花瓷说法正确的是
A. 青蓝色是由于生成了单质钴 B. 表面的釉属于有机高分子膜
的
C. 主要成分为铝硅酸盐 D. 铁元素 存在形式只有Fe O
2 3
2. 科学家发现宇宙中存在100多种星际分子。下列关于星际分子说法正确的是
A. 分子的极性:SiH>NH B. 键的极性:H—Cl>H—H
4 3
C. 键角:HO>CH D. 分子中三键的键长:HC≡N>HC≡CH
2 4
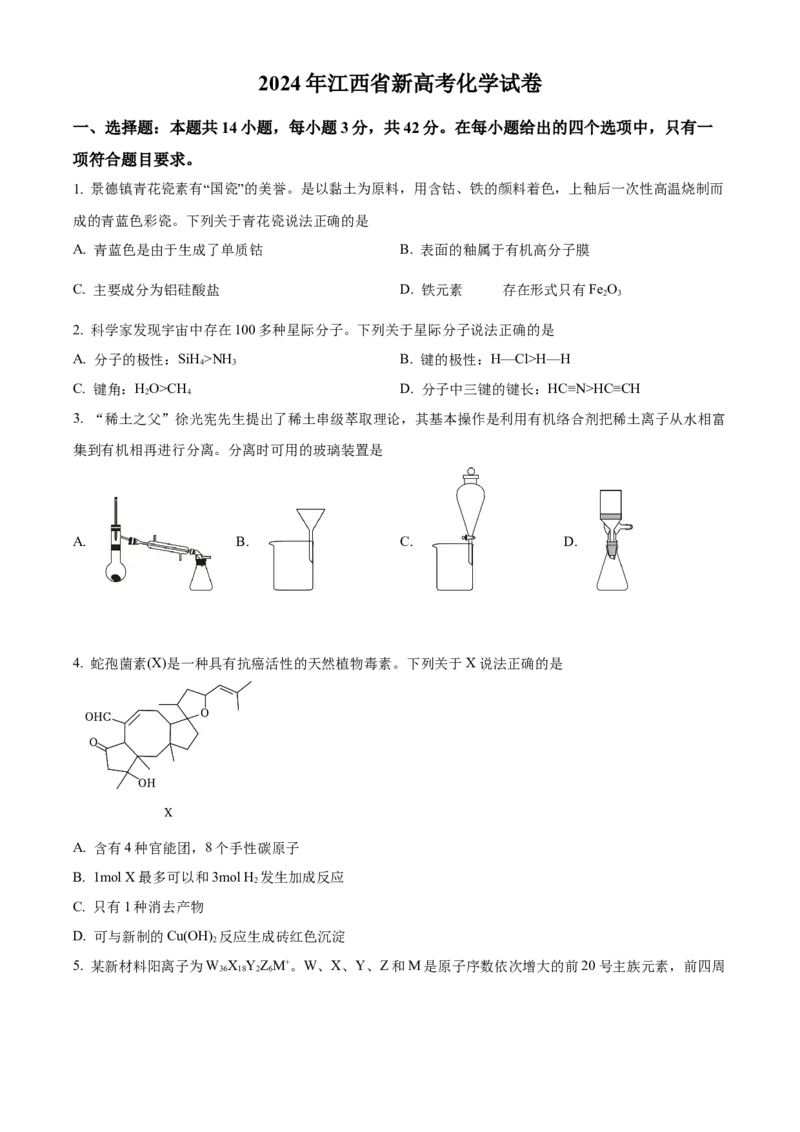
3. “稀土之父”徐光宪先生提出了稀土串级萃取理论,其基本操作是利用有机络合剂把稀土离子从水相富
集到有机相再进行分离。分离时可用的玻璃装置是
A. B. C. D.
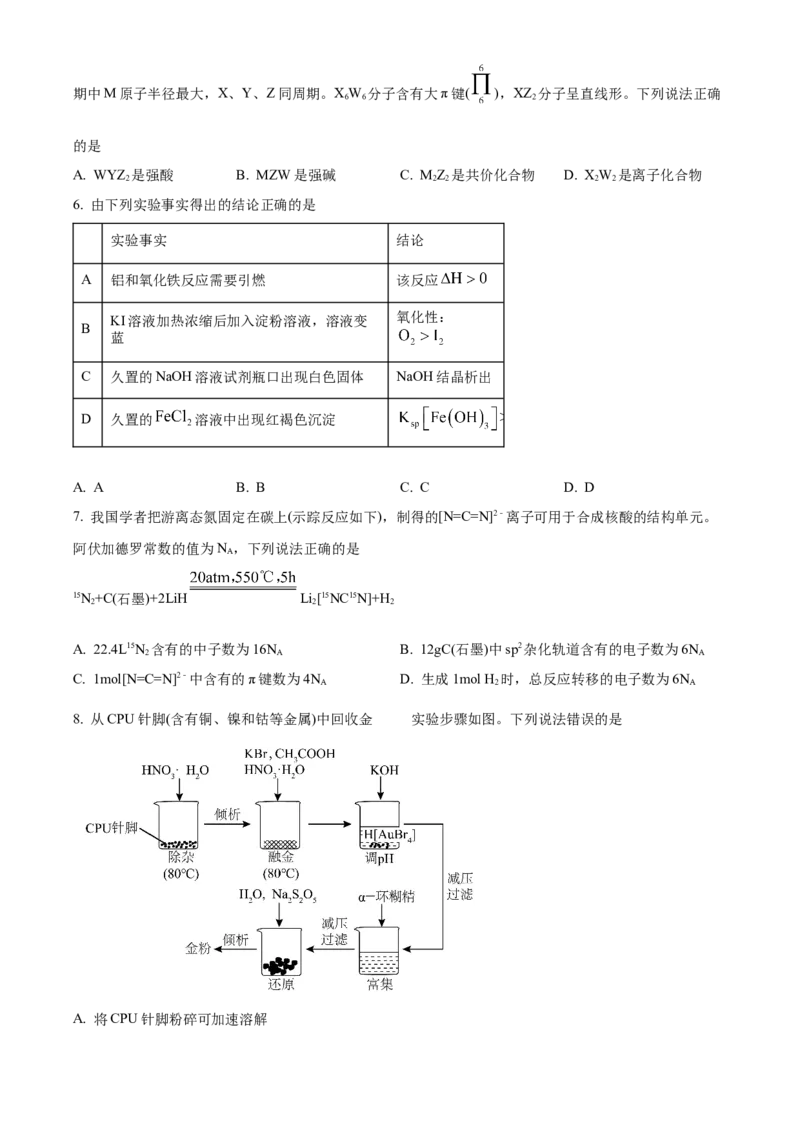
4. 蛇孢菌素(X)是一种具有抗癌活性的天然植物毒素。下列关于X说法正确的是
A. 含有4种官能团,8个手性碳原子
B. 1mol X最多可以和3mol H 发生加成反应
2
C. 只有1种消去产物
D. 可与新制的Cu(OH) 反应生成砖红色沉淀
2
5. 某新材料阳离子为W X YZM+。W、X、Y、Z和M是原子序数依次增大的前20号主族元素,前四周
36 18 2 6期中M原子半径最大,X、Y、Z同周期。XW 分子含有大π键( ),XZ 分子呈直线形。下列说法正确
6 6 2
的是
A. WYZ 是强酸 B. MZW是强碱 C. MZ 是共价化合物 D. XW 是离子化合物
2 2 2 2 2
6. 由下列实验事实得出的结论正确的是
实验事实 结论
A 铝和氧化铁反应需要引燃 该反应
KI溶液加热浓缩后加入淀粉溶液,溶液变 氧化性:
B
蓝
C 久置的NaOH溶液试剂瓶口出现白色固体 NaOH结晶析出
D 久置的 溶液中出现红褐色沉淀
A. A B. B C. C D. D
7. 我国学者把游离态氮固定在碳上(示踪反应如下),制得的[N=C=N]2﹣离子可用于合成核酸的结构单元。
阿伏加德罗常数的值为N ,下列说法正确的是
A
15N+C(石墨)+2LiH Li[15NC15N]+H
2 2 2
A. 22.4L15N 含有的中子数为16N B. 12gC(石墨)中sp2杂化轨道含有的电子数为6N
2 A A
C. 1mol[N=C=N]2﹣中含有的π键数为4N D. 生成1mol H 时,总反应转移的电子数为6N
A 2 A
的
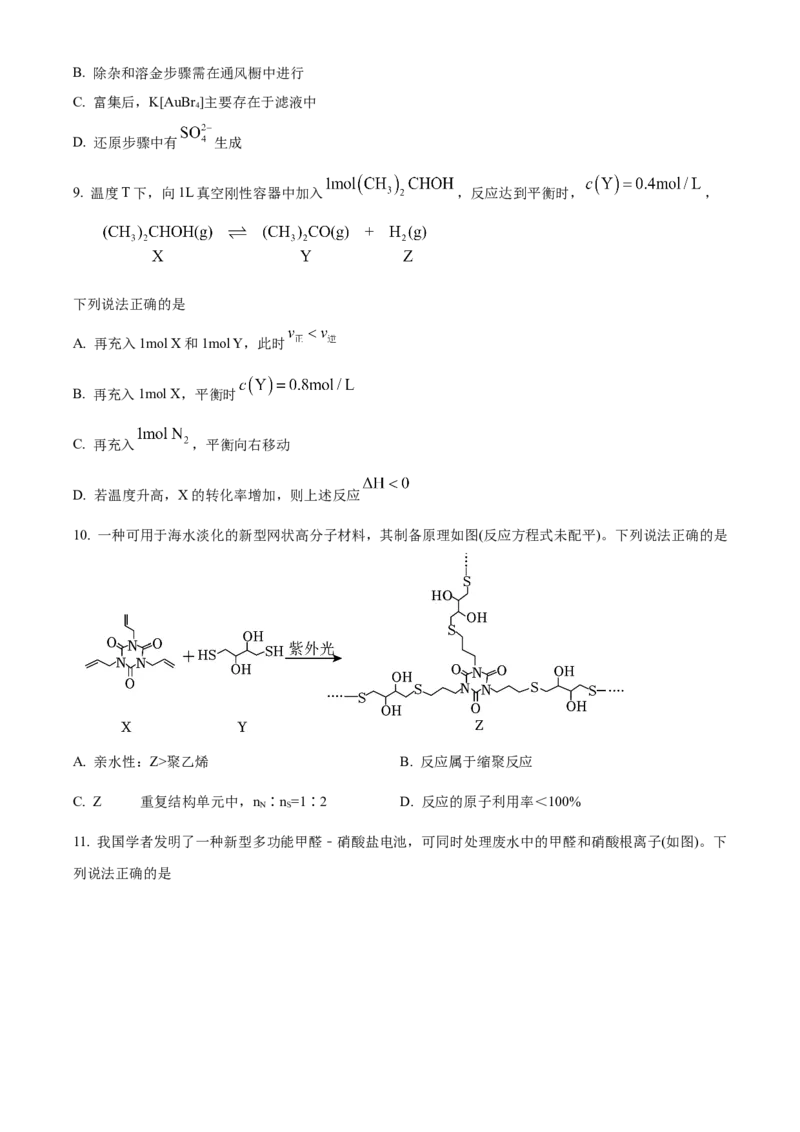
8. 从CPU针脚(含有铜、镍和钴等金属)中回收金 实验步骤如图。下列说法错误的是
A. 将CPU针脚粉碎可加速溶解B. 除杂和溶金步骤需在通风橱中进行
C. 富集后,K[AuBr ]主要存在于滤液中
4
D. 还原步骤中有 生成
9. 温度T下,向1L真空刚性容器中加入 ,反应达到平衡时, ,
下列说法正确的是
A. 再充入1mol X和1mol Y,此时
B. 再充入1mol X,平衡时
C. 再充入 ,平衡向右移动
D. 若温度升高,X的转化率增加,则上述反应
10. 一种可用于海水淡化的新型网状高分子材料,其制备原理如图(反应方程式未配平)。下列说法正确的是
A. 亲水性:Z>聚乙烯 B. 反应属于缩聚反应
的
C. Z 重复结构单元中,n ∶n =1∶2 D. 反应的原子利用率<100%
N S
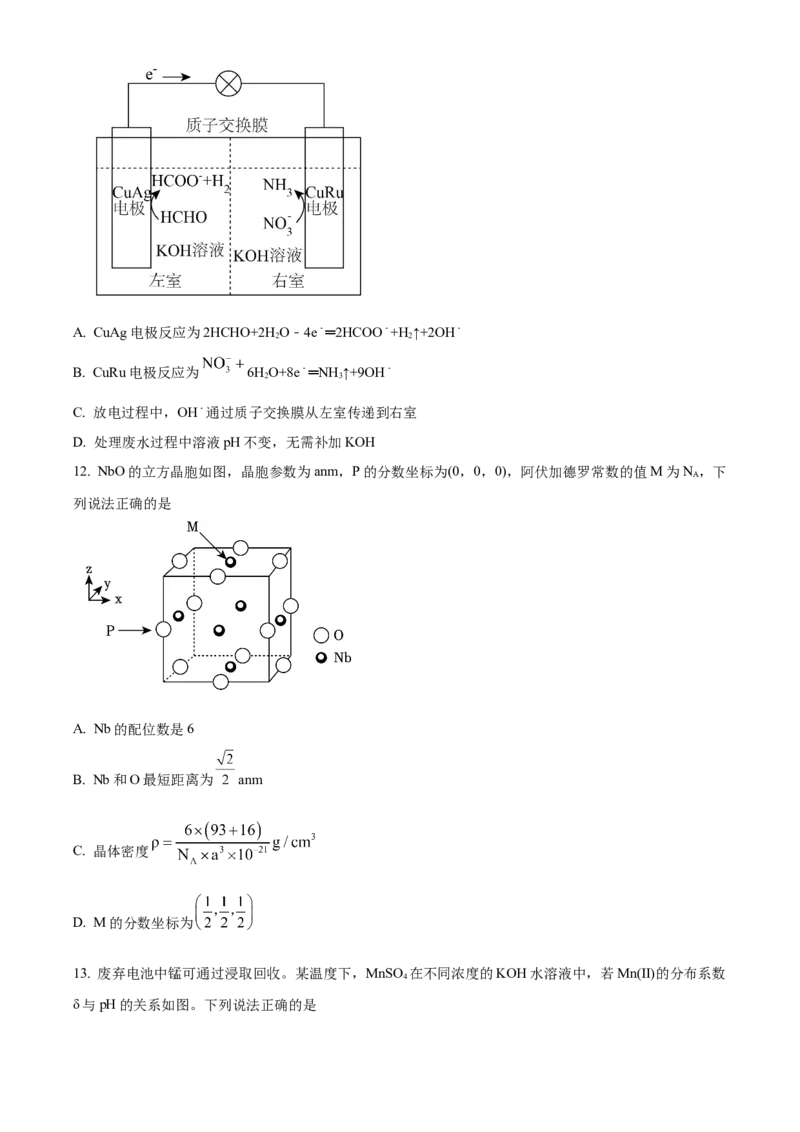
11. 我国学者发明了一种新型多功能甲醛﹣硝酸盐电池,可同时处理废水中的甲醛和硝酸根离子(如图)。下
列说法正确的是A. CuAg电极反应为2HCHO+2H O﹣4e﹣═2HCOO﹣+H ↑+2OH﹣
2 2
B. CuRu电极反应为 6HO+8e﹣═NH ↑+9OH﹣
2 3
C. 放电过程中,OH﹣通过质子交换膜从左室传递到右室
D. 处理废水过程中溶液pH不变,无需补加KOH
12. NbO的立方晶胞如图,晶胞参数为anm,P的分数坐标为(0,0,0),阿伏加德罗常数的值M为N ,下
A
列说法正确的是
A. Nb的配位数是6
B. Nb和O最短距离为 anm
C. 晶体密度
D. M的分数坐标为
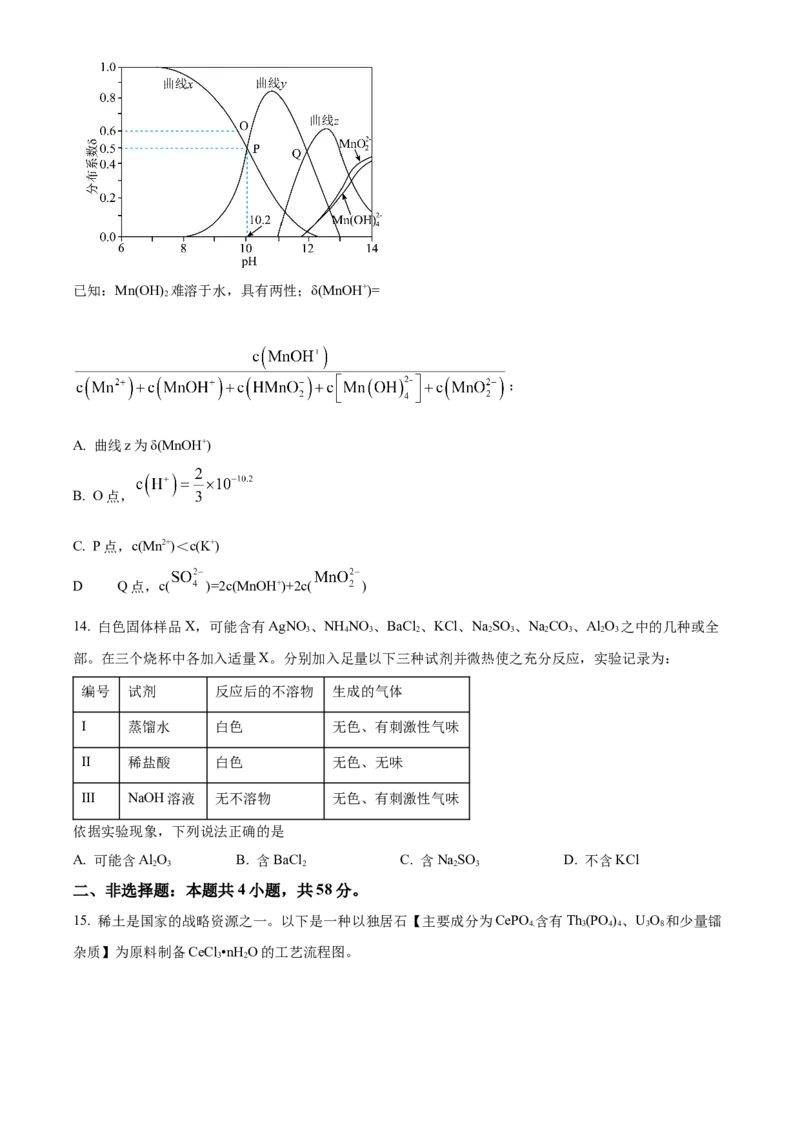
13. 废弃电池中锰可通过浸取回收。某温度下,MnSO 在不同浓度的KOH水溶液中,若Mn(Ⅱ)的分布系数
4
δ与pH的关系如图。下列说法正确的是已知:Mn(OH) 难溶于水,具有两性;δ(MnOH+)=
2
;
A. 曲线z为δ(MnOH+)
B. O点,
C. P点,c(Mn2+)<c(K+)
.
D Q点,c( )=2c(MnOH+)+2c( )
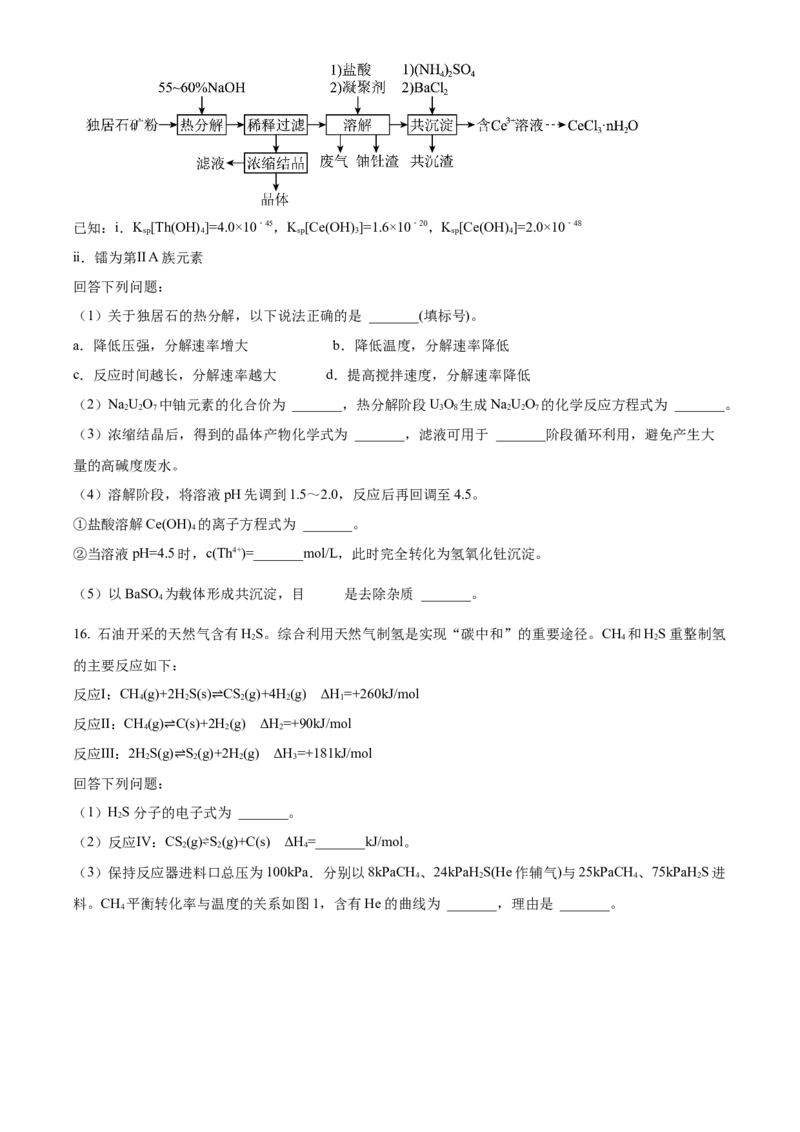
14. 白色固体样品X,可能含有AgNO、NH NO 、BaCl 、KCl、NaSO 、NaCO、Al O 之中的几种或全
3 4 3 2 2 3 2 3 2 3
部。在三个烧杯中各加入适量X。分别加入足量以下三种试剂并微热使之充分反应,实验记录为:
编号 试剂 反应后的不溶物 生成的气体
Ⅰ 蒸馏水 白色 无色、有刺激性气味
Ⅱ 稀盐酸 白色 无色、无味
Ⅲ NaOH溶液 无不溶物 无色、有刺激性气味
依据实验现象,下列说法正确的是
A. 可能含Al O B. 含BaCl C. 含NaSO D. 不含KCl
2 3 2 2 3
二、非选择题:本题共4小题,共58分。
15. 稀土是国家的战略资源之一。以下是一种以独居石【主要成分为CePO 含有Th(PO )、UO 和少量镭
4. 3 4 4 3 8
杂质】为原料制备CeCl •nH O的工艺流程图。
3 2已知:ⅰ.K [Th(OH) ]=4.0×10﹣45,K [Ce(OH) ]=1.6×10﹣20,K [Ce(OH) ]=2.0×10﹣48
sp 4 sp 3 sp 4
ⅱ.镭为第ⅡA族元素
回答下列问题:
(1)关于独居石的热分解,以下说法正确的是 _______(填标号)。
a.降低压强,分解速率增大 b.降低温度,分解速率降低
c.反应时间越长,分解速率越大 d.提高搅拌速度,分解速率降低
(2)NaUO 中铀元素的化合价为 _______,热分解阶段UO 生成NaUO 的化学反应方程式为 _______。
2 2 7 3 8 2 2 7
(3)浓缩结晶后,得到的晶体产物化学式为 _______,滤液可用于 _______阶段循环利用,避免产生大
量的高碱度废水。
(4)溶解阶段,将溶液pH先调到1.5~2.0,反应后再回调至4.5。
①盐酸溶解Ce(OH) 的离子方程式为 _______。
4
②当溶液pH=4.5时,c(Th4+)=_______mol/L,此时完全转化为氢氧化钍沉淀。
的
(5)以BaSO 为载体形成共沉淀,目 是去除杂质 _______。
4
16. 石油开采的天然气含有HS。综合利用天然气制氢是实现“碳中和”的重要途径。CH 和HS重整制氢
2 4 2
的主要反应如下:
反应Ⅰ:CH(g)+2HS(s) CS(g)+4H(g) ΔH =+260kJ/mol
4 2 2 2 1
反应Ⅱ:CH
4
(g) C(s)+2⇌H
2
(g) ΔH
2
=+90kJ/mol
反应Ⅲ:2H
2
S(g⇌) S
2
(g)+2H
2
(g) ΔH
3
=+181kJ/mol
回答下列问题:⇌
(1)HS分子的电子式为 _______。
2
(2)反应Ⅳ:CS(g)⇌S(g)+C(s)ㅤΔH=_______kJ/mol。
2 2 4
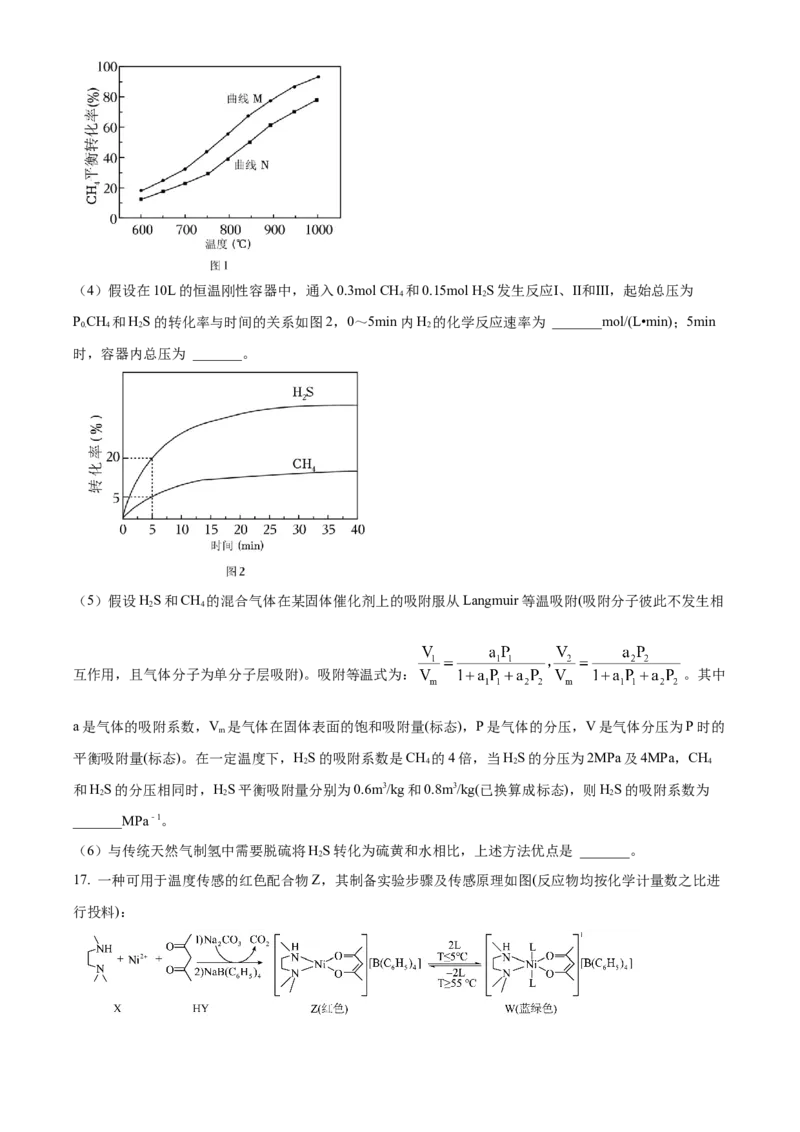
(3)保持反应器进料口总压为100kPa.分别以8kPaCH、24kPaHS(He作辅气)与25kPaCH、75kPaHS进
4 2 4 2
料。CH 平衡转化率与温度的关系如图1,含有He的曲线为 _______,理由是 _______。
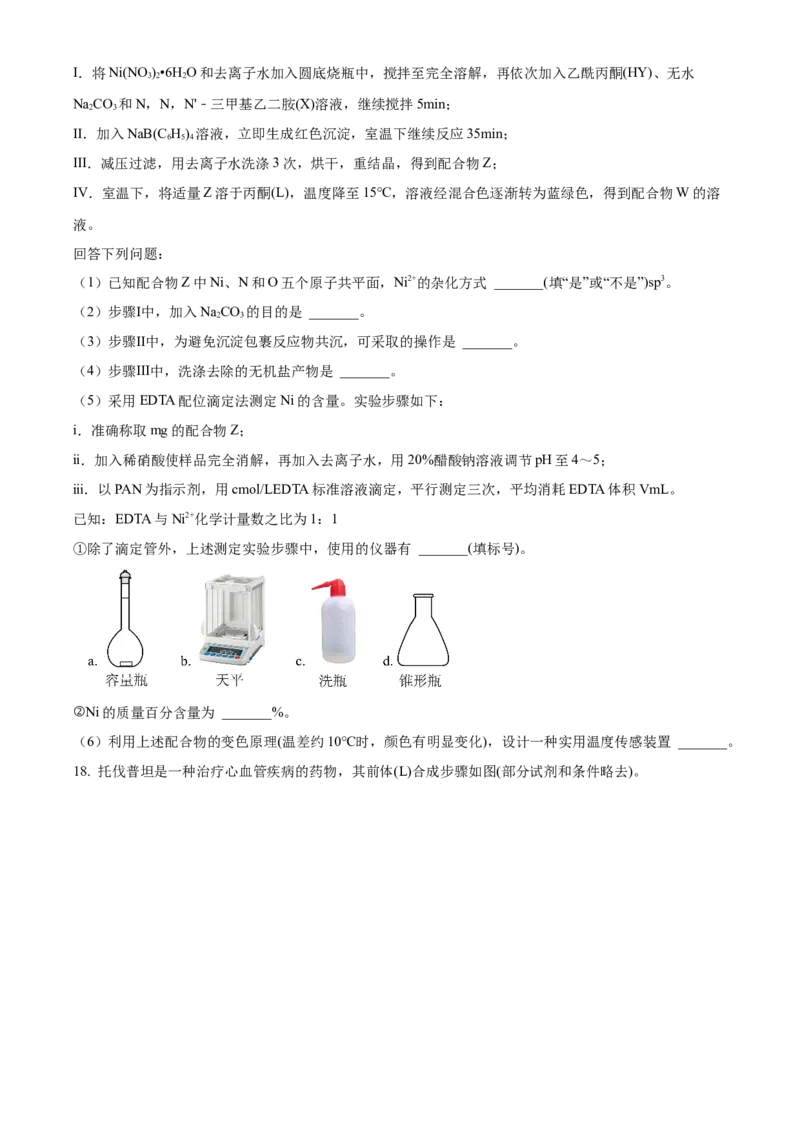
4(4)假设在10L的恒温刚性容器中,通入0.3mol CH 和0.15mol H S发生反应Ⅰ、Ⅱ和Ⅲ,起始总压为
4 2
P CH 和HS的转化率与时间的关系如图2,0~5min内H 的化学反应速率为 _______mol/(L•min);5min
0. 4 2 2
时,容器内总压为 _______。
(5)假设HS和CH 的混合气体在某固体催化剂上的吸附服从Langmuir等温吸附(吸附分子彼此不发生相
2 4
互作用,且气体分子为单分子层吸附)。吸附等温式为: 。其中
a是气体的吸附系数,V 是气体在固体表面的饱和吸附量(标态),P是气体的分压,V是气体分压为P时的
m
平衡吸附量(标态)。在一定温度下,HS的吸附系数是CH 的4倍,当HS的分压为2MPa及4MPa,CH
2 4 2 4
和HS的分压相同时,HS平衡吸附量分别为0.6m3/kg和0.8m3/kg(已换算成标态),则HS的吸附系数为
2 2 2
_______MPa﹣1。
(6)与传统天然气制氢中需要脱硫将HS转化为硫黄和水相比,上述方法优点是 _______。
2
17. 一种可用于温度传感的红色配合物Z,其制备实验步骤及传感原理如图(反应物均按化学计量数之比进
行投料):Ⅰ.将Ni(NO )•6H O和去离子水加入圆底烧瓶中,搅拌至完全溶解,再依次加入乙酰丙酮(HY)、无水
3 2 2
NaCO 和N,N,N'﹣三甲基乙二胺(X)溶液,继续搅拌5min;
2 3
Ⅱ.加入NaB(C H) 溶液,立即生成红色沉淀,室温下继续反应35min;
6 5 4
Ⅲ.减压过滤,用去离子水洗涤3次,烘干,重结晶,得到配合物Z;
Ⅳ.室温下,将适量Z溶于丙酮(L),温度降至15℃,溶液经混合色逐渐转为蓝绿色,得到配合物W的溶
液。
回答下列问题:
(1)已知配合物Z中Ni、N和O五个原子共平面,Ni2+的杂化方式 _______(填“是”或“不是”)sp3。
(2)步骤Ⅰ中,加入NaCO 的目的是 _______。
2 3
(3)步骤Ⅱ中,为避免沉淀包裹反应物共沉,可采取的操作是 _______。
(4)步骤Ⅲ中,洗涤去除的无机盐产物是 _______。
(5)采用EDTA配位滴定法测定Ni的含量。实验步骤如下:
ⅰ.准确称取mg的配合物Z;
ⅱ.加入稀硝酸使样品完全消解,再加入去离子水,用20%醋酸钠溶液调节pH至4~5;
ⅲ.以PAN为指示剂,用cmol/LEDTA标准溶液滴定,平行测定三次,平均消耗EDTA体积VmL。
已知:EDTA与Ni2+化学计量数之比为1:1
①除了滴定管外,上述测定实验步骤中,使用的仪器有 _______(填标号)。
②Ni的质量百分含量为 _______%。
(6)利用上述配合物的变色原理(温差约10℃时,颜色有明显变化),设计一种实用温度传感装置 _______。
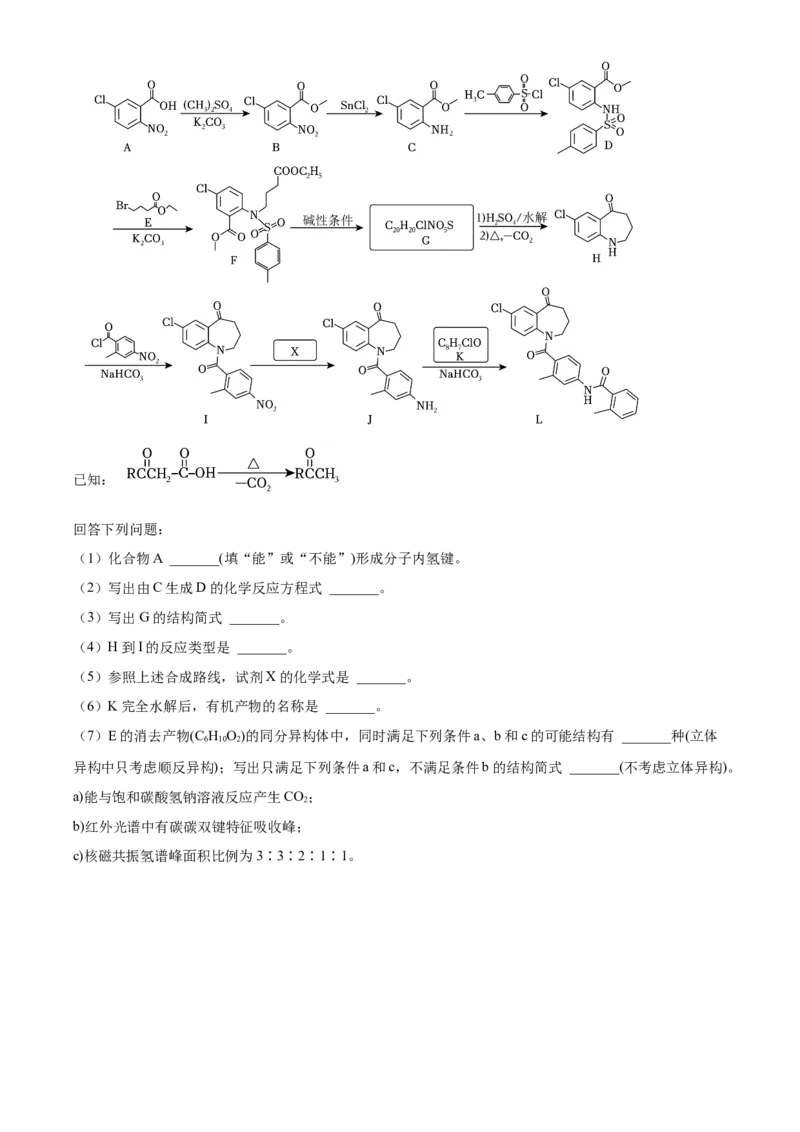
18. 托伐普坦是一种治疗心血管疾病的药物,其前体(L)合成步骤如图(部分试剂和条件略去)。已知:
回答下列问题:
(1)化合物A _______(填“能”或“不能”)形成分子内氢键。
(2)写出由C生成D的化学反应方程式 _______。
(3)写出G的结构简式 _______。
(4)H到I的反应类型是 _______。
(5)参照上述合成路线,试剂X的化学式是 _______。
(6)K完全水解后,有机产物的名称是 _______。
(7)E的消去产物(C H O)的同分异构体中,同时满足下列条件a、b和c的可能结构有 _______种(立体
6 10 2
异构中只考虑顺反异构);写出只满足下列条件a和c,不满足条件b的结构简式 _______(不考虑立体异构)。
a)能与饱和碳酸氢钠溶液反应产生CO;
2
b)红外光谱中有碳碳双键特征吸收峰;
c)核磁共振氢谱峰面积比例为3∶3∶2∶1∶1。