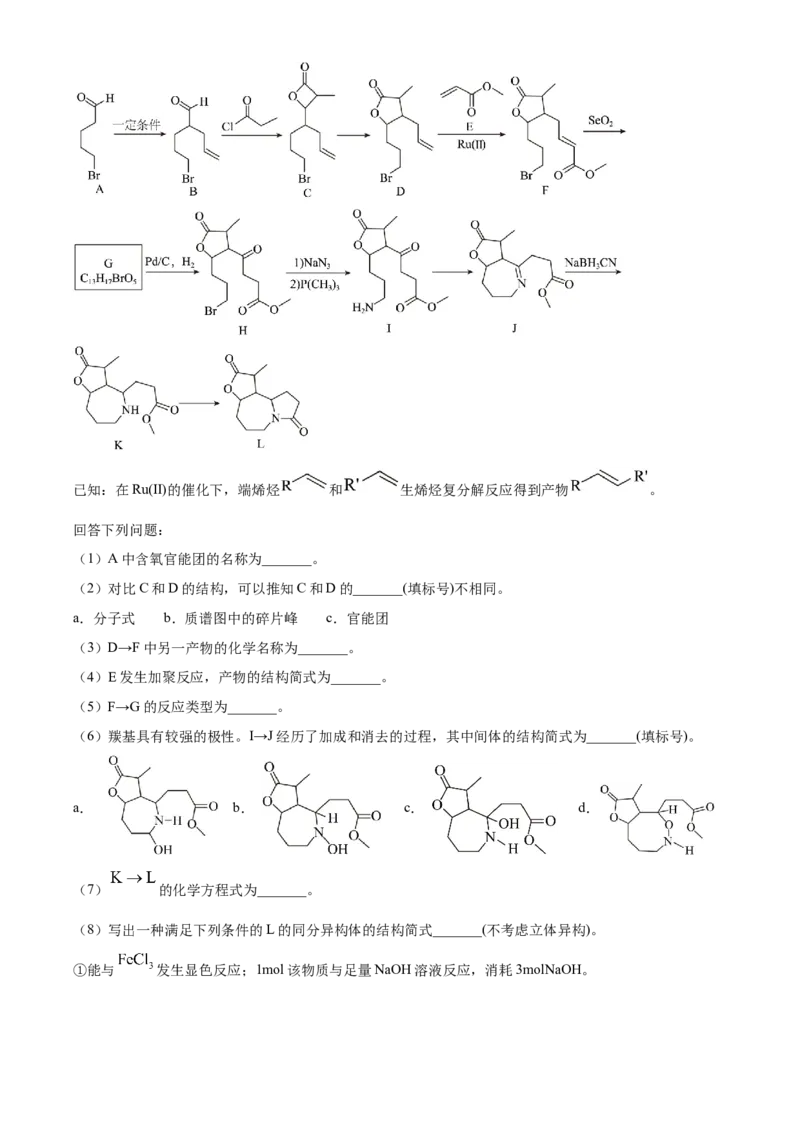
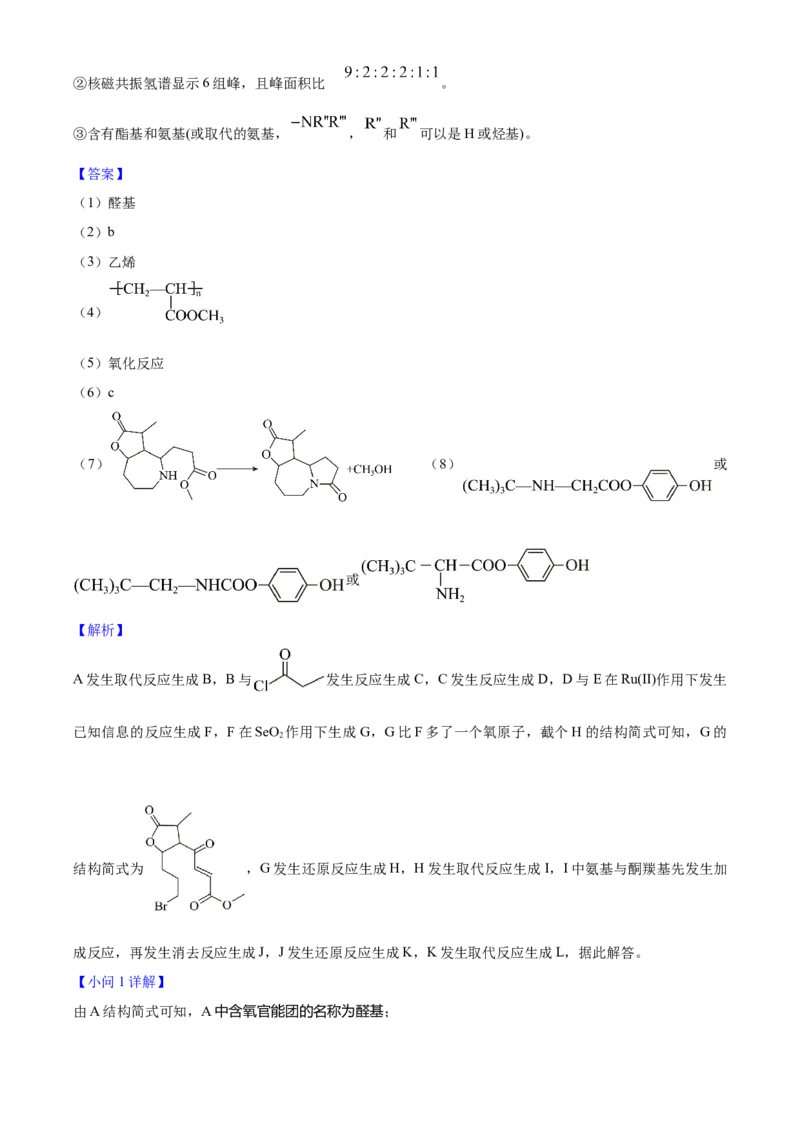
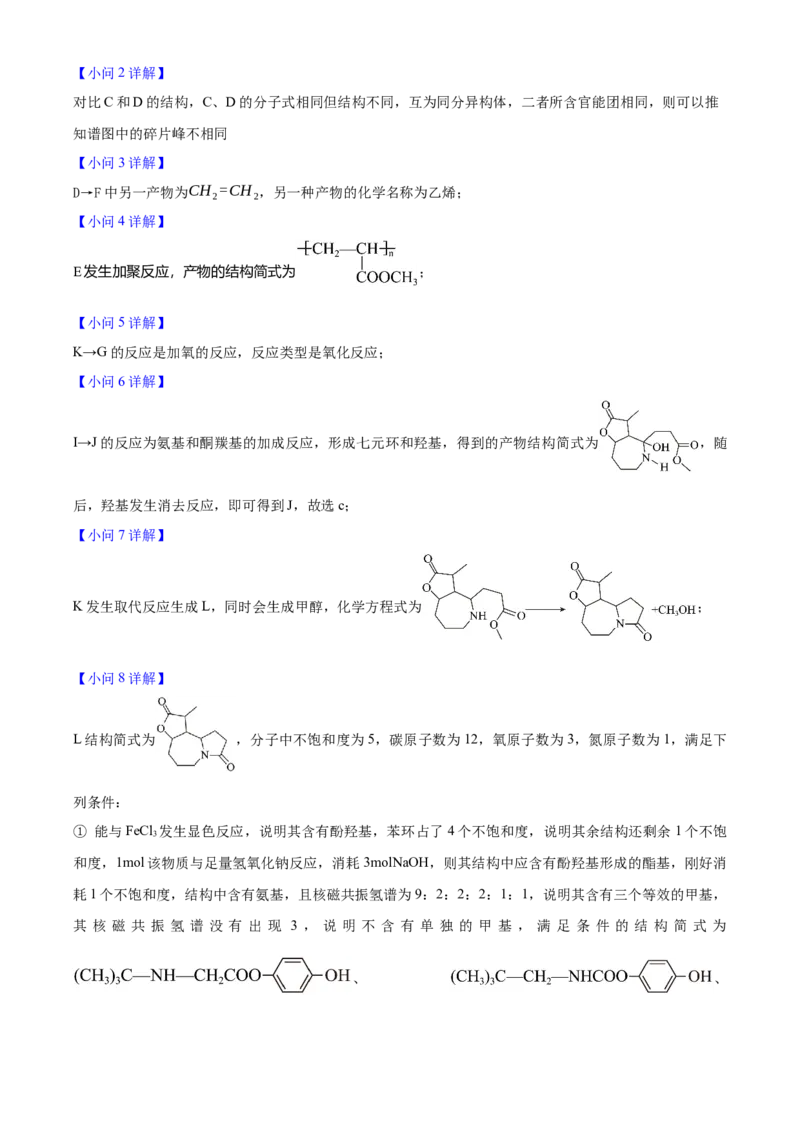
文档内容
2025 年云南省普通高等学校招生统一考试
化学
注意事项:
1.答卷前,考生务必用黑色碳素笔将自己的姓名、准考证号、考场号、座位号填写在答题卡
上,并认真核准条形码上的姓名、准考证号、考场号、座位号及科目,在规定的位置贴好条
形码。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,用黑色碳素笔将答案写在
答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 F 19 Na 23 S 32 Cl 35.5
Mn 55 Fe 56 Cu 64 Sb 122
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 画中有“化”,多彩中华。下列叙述正确的是
A. 岩彩壁画颜料所用贝壳粉,主要成分属于硅酸盐
B. 油画颜料调和剂所用核桃油,属于有机高分子
C. 竹胎漆画颜料赭石的主要成分氧化铁,耐酸、碱
D. 水墨画墨汁的主要成分碳,常温不易被氧化
【答案】D
【解析】
A.贝壳粉的主要成分是碳酸钙,属于碳酸盐,A错误;
B.核桃油属于油脂,分子量较小,不属于有机高分子,B错误;
C.氧化铁(Fe O)能与酸反应,不耐酸,C错误;
2 3
D.碳在常温下化学性质稳定,不易被氧化,D正确;
故选D。
2. 下列化学用语或图示表示正确的是
A. 的VSEPR模型:B. 的电子式:
C. Cl的原子结构示意图:
D. 溶于水的电离方程式:
【答案】A
【解析】
1
A.N H 分子中N原子的价层电子对数为3+ (5−3)=4,含有1对孤电子对,其VSEPR模型为四面体,
3 2
即 ,故A正确;
B.Na S由Na+ 和S2− 构成,其电子式为 ,B错误;
2
C.氯是第17号元素,Cl原子结构示意图为: ,C错误;
D.Al (SO ) 是强电解质,溶于水的电离方程式:Al (SO ) =2Al3++3SO2− ,故D错误;
2 4 3 2 4 3 4
故选A。
3. 下列化学方程式错误的是
A. 煤制水煤气:
B. 供氧:
C. 覆铜板制作印刷电路板:
D. 铅酸蓄电池放电:
【答案】C【解析】
A.煤制水煤气的反应为C+H O(g)¿+H ,该反应是将煤转化为水煤气的常见反应,化学方程式正确。
2 2
B.Na O 可作供氧剂,与CO 反应生成Na CO 和O ,化学方程式2Na O +2CO =2Na CO +O
2 2 2 2 3 2 2 2 2 2 3 2
正确,可用于潜水艇等环境中提供氧气。
C.覆铜板制作印刷电路板时,FeCl 与Cu反应,生成的是FeCl 而不是Fe,正确的化学方程式应为
3 2
2FeCl +Cu=2FeCl +CuCl ,该选项错误。
3 2 2
D.铅酸蓄电池放电时,Pb、PbO 与H SO 反应生成PbSO 和H O,化学方程式
2 2 4 4 2
Pb+PbO +2H SO =2PbSO +2H O正确,体现了铅酸蓄电池的工作原理。
2 2 4 4 2
故选C。
4. 为阿伏加德罗常数的值。下列说法正确的是
A. 中原子的数目为
B. 所含中子的数目为
C. 粉和足量S完全反应,转移电子的数目为
D. 盐酸与足量 反应,生成 的数目为
【答案】B
【解析】
A.未指明CH 所处的状态(如标准状况),不能用标准状况下的气体摩尔体积(222.4L/mol)来计算
4
其物质的量,也就无法确定原子数目,A 错误。
B.18O的中子数为18-8=10,1mol18O含10mol中子,数目为10N ,B正确;
A
C.28g Fe(0.5mol)与S反应生成FeS,Fe的氧化态为+2,转移电子数为0.5×2=1mol=1N ,而非1.5N ,
A A
C错误;
D.MnO 与浓盐酸反应,随着反应进行,盐酸浓度降低变为稀盐酸,稀盐酸与MnO 不反应,所以盐酸
2 2
不能完全反应,生成Cl 的物质的量小于0.3mol,生成Cl 的数目小于0.3N ,D 错误。
2 2 A
故选B。
5. 下列装置(省略部分夹持装置)或操作正确的是B.配制 溶
A.制备
液
C.探究Na与 反应 D.探究温度对化学平衡的影响
A. A B. B C. C D. D
【答案】D
【解析】
A. 和 固体混合物加热制取氨气,试管口要略向下倾斜,A错误;
B.配制 溶液,应在烧杯中溶解KCl固体,B错误;
C.金属钠与水反应剧烈,不能在试管中进行,应在烧杯中进行,且烧杯不能盛满水,C错误;
D.两个烧杯中分别盛有热水和冰水,可以通过观察气体的颜色深浅来探究温度对2NO (红棕色)
2
NO(无色)平衡的影响,D正确;
2 4
故选D。
6. 化合物Z是某真菌的成分之一,结构如图。下列有关该物质说法错误的是
A. 可形成分子间氢键B. 与乙酸、乙醇均能发生酯化反应
C. 能与 溶液反应生成
D. 与 的 溶液反应消耗
【答案】D
【解析】
A. 分子中的醇羟基能形成分子间氢键,故A正确;
B. 分子中含有醇羟基,所以能和乙酸发生酯化反应,分子中含有羧基,所以能和乙醇发生酯化反应,故 B
正确;
C. 分子中含有—COOH,所以能和碳酸氢氧化钠溶液反应生成CO ,故C正确;
2
D. 碳碳碳双键和溴以1:1发生加成反应,分子在含有 2根碳碳碳双键,所以1 mol该物质最多消耗2
mol溴的四氯化碳溶液,故D错误;
答案选D。
7. 稻壳制备纳米Si的流程图如下。下列说法错误的是
A. 可与NaOH溶液反应
B. 盐酸在该工艺中体现了还原性
C. 高纯Si可用于制造硅太阳能电池
D. 制备纳米Si:
【答案】B
【解析】
稻壳在一定条件下制备纳米SiO ,纳米SiO 和Mg在650℃发生置换反应生成MgO和纳米Si,加盐酸将
2 2
MgO转化为MgCl ,过滤、洗涤、干燥得到纳米Si。
2
A.SiO 属于酸性氧化物,可与NaOH溶液反应,A正确;
2
B.盐酸参与的反应为:MgO+2HCl=MgCl +H O,该反应是非氧化还原反应,盐酸体现酸性,没有体现还
2 2
原性,B错误;
C.高纯硅可作半导体材料,故可用于硅太阳能电池中,C正确;
D.SiO 和 Mg 在 650℃条件下发生置换反应得到 MgO 和纳米 Si,反应的化学方程式为
2,D正确;
答案选B。
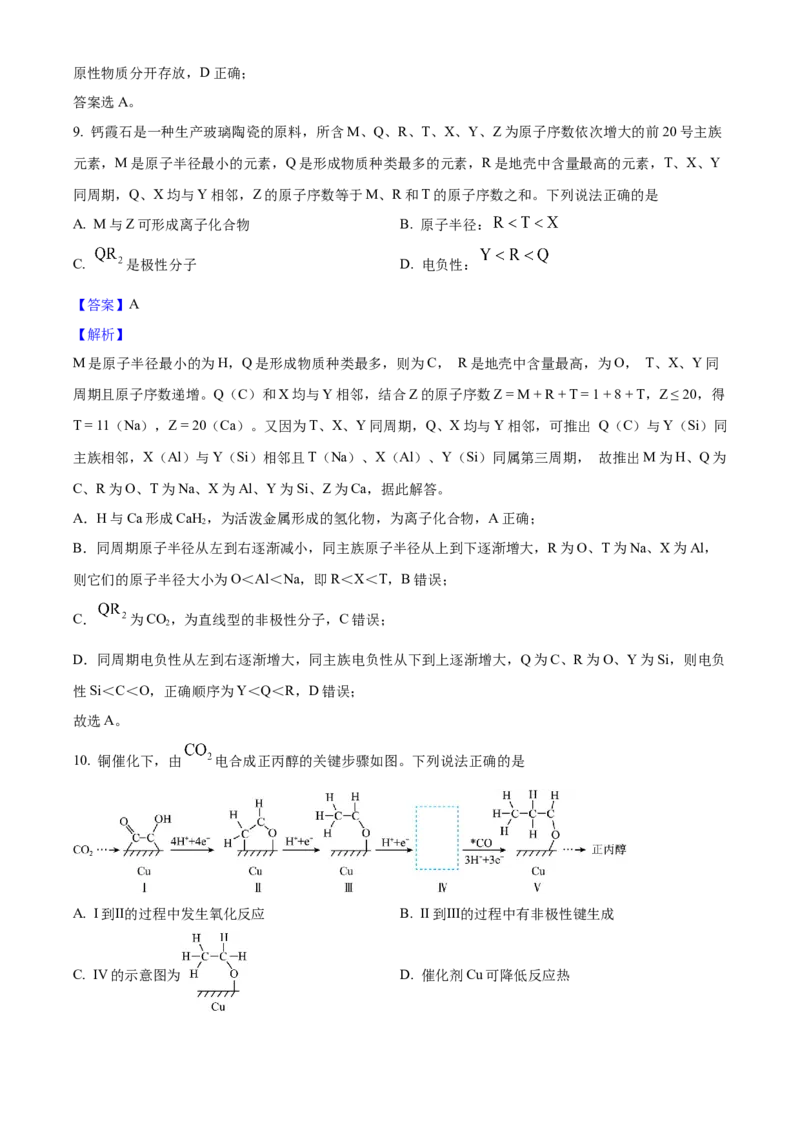
8. 某化学兴趣小组设计如下实验装置,通过测定反应前后质量的变化,验证 固体在酒精灯加热条
件下,受热分解的气态产物。
实验步骤:先缓慢通入Ar气,排尽装置内空气;关闭Ⅰ左侧阀门,点燃酒精灯;一段时间后,Ⅱ中灼热的
铜网变黑,熄灭酒精灯甲;再次缓慢通入Ar气……
下列说法错误的是
A. 实验步骤中,点燃酒精灯的顺序为甲、乙、丙
B. 整个过程中,若Ⅲ中灼热的铜网未变黑,则说明生成的 在Ⅱ中反应完全
C. 实验结束后,若Ⅰ中减少的质量等于Ⅱ中增加的质量,则分解的气态产物只有
D. 应远离热源、可燃物,并与还原性物质分开存放
【答案】A
【解析】
先缓慢通入Ar气,排尽装置内空气,防止对实验造成干扰,关闭Ⅰ左侧阀门,先后点燃乙、丙、甲处酒精
灯,一段时间后,Ⅰ中灼热的铜网变黑,说明NaNO 分解产生了O ,熄灭酒精灯甲,再次缓慢通入Ar气,
3 2
使NaNO 分解产生的气态产物全部排尽,浓硫酸用于防止空气中的水蒸气进入装置干扰实验。
3
A.一段时间后,Ⅰ中灼热的铜网变黑,说明NaNO 分解产生了O ,为确保能准确测定产生的氧气的质量,
3 2
应先点燃乙处酒精灯,再点燃丙处酒精灯,最后点燃甲处酒精灯,A错误;
B.Ⅱ、Ⅲ中Cu均能和氧气反应生成黑色的CuO,整个过程中,若Ⅱ中灼热的铜网未变黑,则说明生成的
O 在Ⅱ中反应完全,B正确;
2
C.Ⅱ中的Cu只能吸收O ,实验结束后,若Ⅰ中减少的质量等于Ⅰ中增加的质量,则分解的气态产物只有
2
O,C正确;
2
D.由该实验可知NaNO 受热易分解产生氧化剂、助燃性气体O,故NaNO 应远离热源、可燃物,并与还
3 2 3原性物质分开存放,D正确;
答案选A。
9. 钙霞石是一种生产玻璃陶瓷的原料,所含M、Q、R、T、X、Y、Z为原子序数依次增大的前20号主族
元素,M是原子半径最小的元素,Q是形成物质种类最多的元素,R是地壳中含量最高的元素,T、X、Y
同周期,Q、X均与Y相邻,Z的原子序数等于M、R和T的原子序数之和。下列说法正确的是
A. M与Z可形成离子化合物 B. 原子半径:
C. 是极性分子 D. 电负性:
【答案】A
【解析】
M是原子半径最小的为H,Q是形成物质种类最多,则为C, R是地壳中含量最高,为O, T、X、Y同
周期且原子序数递增。Q(C)和X均与Y相邻,结合Z的原子序数Z = M + R + T = 1 + 8 + T,Z ≤ 20,得
T = 11(Na),Z = 20(Ca)。又因为T、X、Y同周期,Q、X均与Y相邻,可推出 Q(C)与Y(Si)同
主族相邻,X(Al)与Y(Si)相邻且T(Na)、X(Al)、Y(Si)同属第三周期, 故推出M为H、Q为
C、R为O、T为Na、X为Al、Y为Si、Z为Ca,据此解答。
A.H与Ca形成CaH,为活泼金属形成的氢化物,为离子化合物,A正确;
2
B.同周期原子半径从左到右逐渐减小,同主族原子半径从上到下逐渐增大,R为O、T为Na、X为Al,
则它们的原子半径大小为O<Al<Na,即R<X<T,B错误;
C. 为CO,为直线型的非极性分子,C错误;
2
D.同周期电负性从左到右逐渐增大,同主族电负性从下到上逐渐增大,Q为C、R为O、Y为Si,则电负
性Si<C<O,正确顺序为Y<Q<R,D错误;
故选A。
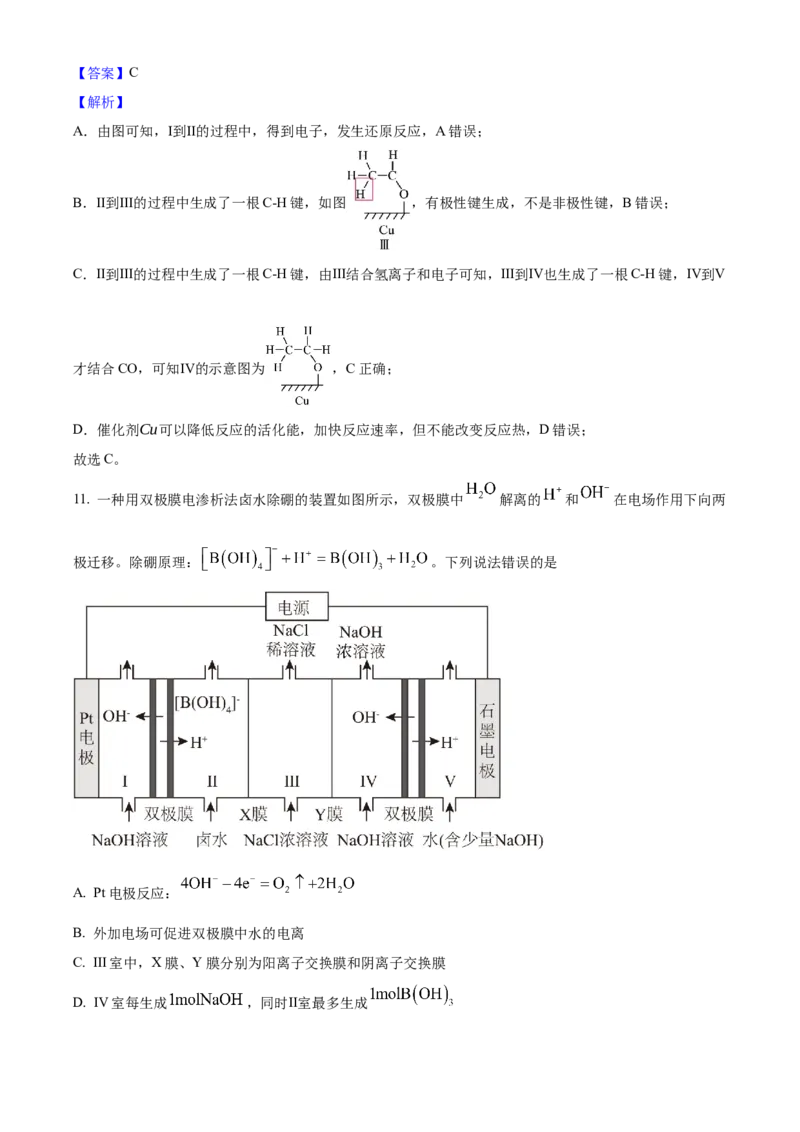
10. 铜催化下,由 电合成正丙醇的关键步骤如图。下列说法正确的是
A. Ⅰ到Ⅱ的过程中发生氧化反应 B. Ⅱ到Ⅲ的过程中有非极性键生成
C. Ⅳ的示意图为 D. 催化剂Cu可降低反应热【答案】C
【解析】
A.由图可知,Ⅰ到Ⅱ的过程中,得到电子,发生还原反应,A错误;
B.Ⅱ到Ⅲ的过程中生成了一根C-H键,如图 ,有极性键生成,不是非极性键,B错误;
C.Ⅱ到Ⅲ的过程中生成了一根C-H键,由Ⅲ结合氢离子和电子可知,Ⅲ到Ⅳ也生成了一根C-H键,Ⅳ到Ⅴ
才结合CO,可知Ⅳ的示意图为 ,C正确;
D.催化剂Cu可以降低反应的活化能,加快反应速率,但不能改变反应热,D错误;
故选C。
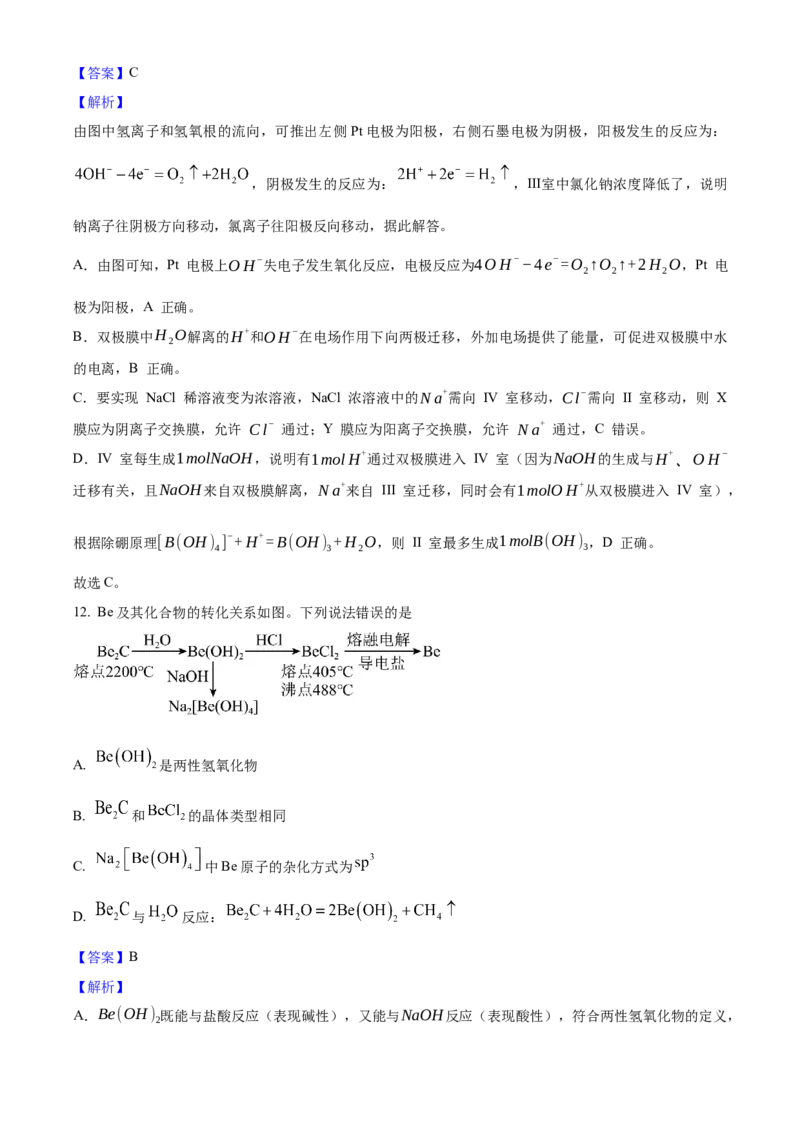
11. 一种用双极膜电渗析法卤水除硼的装置如图所示,双极膜中 解离的 和 在电场作用下向两
极迁移。除硼原理: 。下列说法错误的是
A. Pt电极反应:
B. 外加电场可促进双极膜中水的电离
C. Ⅲ室中,X膜、Y膜分别为阳离子交换膜和阴离子交换膜
D. Ⅳ室每生成 ,同时Ⅱ室最多生成【答案】C
【解析】
由图中氢离子和氢氧根的流向,可推出左侧Pt电极为阳极,右侧石墨电极为阴极,阳极发生的反应为:
,阴极发生的反应为: ,Ⅲ室中氯化钠浓度降低了,说明
钠离子往阴极方向移动,氯离子往阳极反向移动,据此解答。
A.由图可知,Pt 电极上OH−失电子发生氧化反应,电极反应为4OH−−4e−=O ↑O ↑+2H O,Pt 电
2 2 2
极为阳极,A 正确。
B.双极膜中H O解离的H+和OH−在电场作用下向两极迁移,外加电场提供了能量,可促进双极膜中水
2
的电离,B 正确。
C.要实现 NaCl 稀溶液变为浓溶液,NaCl 浓溶液中的Na+需向 IV 室移动,Cl−需向 II 室移动,则 X
膜应为阴离子交换膜,允许 Cl− 通过;Y 膜应为阳离子交换膜,允许 Na+ 通过,C 错误。
D.IV 室每生成1molNaOH,说明有1molH+通过双极膜进入 IV 室(因为NaOH的生成与H+ 、OH−
迁移有关,且NaOH来自双极膜解离,Na+来自 III 室迁移,同时会有1molOH+从双极膜进入 IV 室),
根据除硼原理[B(OH) ] −+H+=B(OH) +H O,则 II 室最多生成1molB(OH) ,D 正确。
4 3 2 3
故选C。
12. Be及其化合物的转化关系如图。下列说法错误的是
A. 是两性氢氧化物
B. 和 的晶体类型相同
C. 中Be原子的杂化方式为
D. 与 反应:
【答案】B
【解析】
A.Be(OH) 既能与盐酸反应(表现碱性),又能与NaOH反应(表现酸性),符合两性氢氧化物的定义,
2所以Be(OH) 是两性氢氧化物,A 正确。
2
B.Be C熔点为2200∘C,熔点很高,属于离子晶体;BeCl 熔点405∘C、沸点488∘C,熔点较低,属
2 2
于分子晶体,二者晶体类型不同,B 错误。
C.在Na [Be(OH) ]中,Be 原子的配位数为 4,其杂化方式为sp3杂化,C 正确。
2 4
D.类比CaC 与水的反应,Be C与H O反应生成Be(OH) 和CH ,反应方程式为
2 2 2 2 4
Be C+4H O=2Be(OH) +CH ↑,D 正确。
2 2 2 4
综上所述,本题选B。
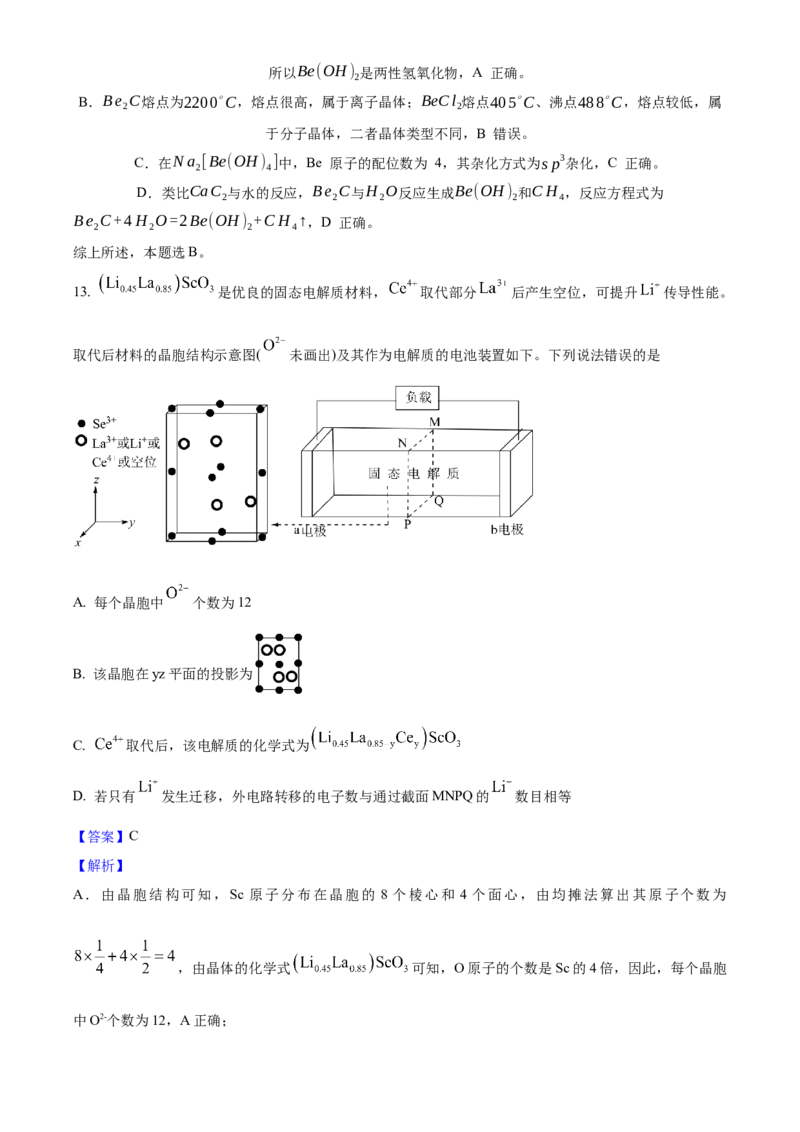
13. 是优良的固态电解质材料, 取代部分 后产生空位,可提升 传导性能。
取代后材料的晶胞结构示意图( 未画出)及其作为电解质的电池装置如下。下列说法错误的是
A. 每个晶胞中 个数为12
B. 该晶胞在yz平面的投影为
C. 取代后,该电解质的化学式为
D. 若只有 发生迁移,外电路转移的电子数与通过截面MNPQ的 数目相等
【答案】C
【解析】
A.由晶胞结构可知,Sc 原子分布在晶胞的 8 个棱心和 4 个面心,由均摊法算出其原子个数为
,由晶体的化学式 可知,O原子的个数是Sc的4倍,因此,每个晶胞
中O2-个数为12,A正确;B.由晶胞结构可知,该晶胞在yz平面的投影就是其前视图 ,B正确;
C.Ce4+ 取代La3+后,Li+数目减小并产生空位,因此,根据化合价的代数和为0可知,取代后该电解质的
化学式为 ,C错误;
D.Li+与电子所带的电荷数目相同,只是电性不同,原电池中内电路和外电路通过的电量相等,因此,若
只有Li+发生迁移,外电路转移的电子数与通过截面MNPQ的Li+数目相等,D正确;
综上所述,本题选C 。
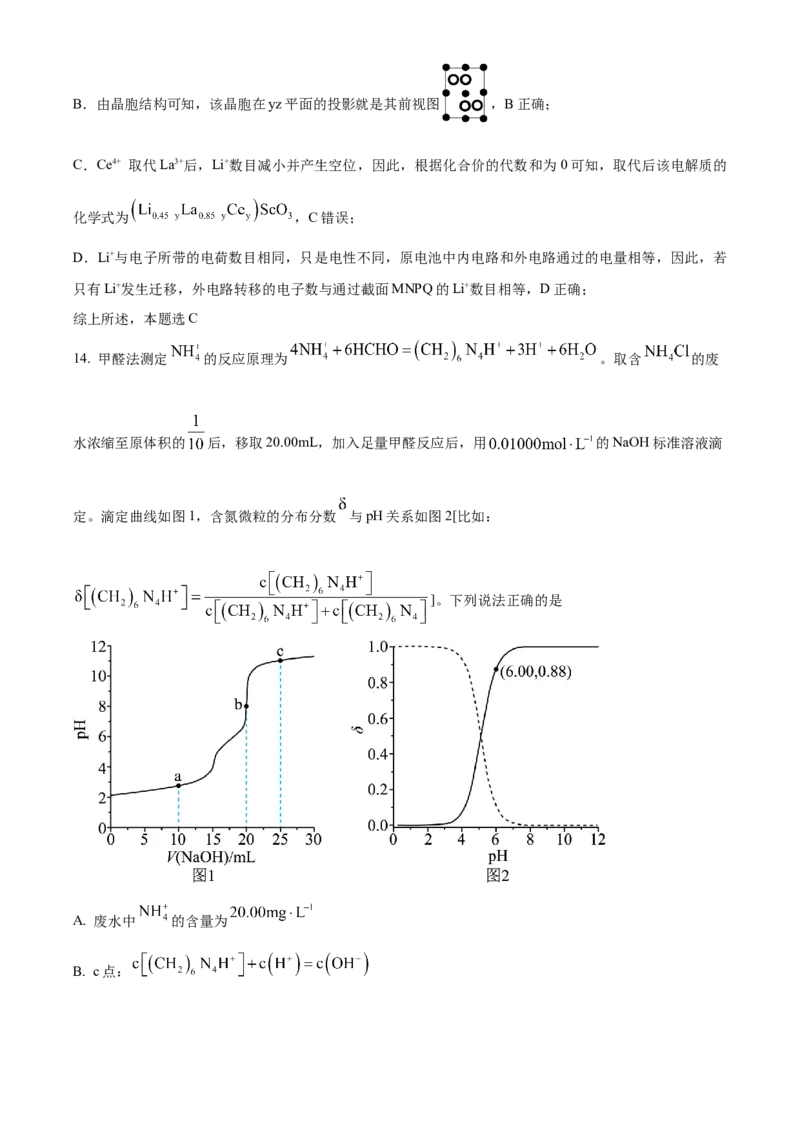
14. 甲醛法测定 的反应原理为 。取含 的废
水浓缩至原体积的 后,移取20.00mL,加入足量甲醛反应后,用 的NaOH标准溶液滴
定。滴定曲线如图1,含氮微粒的分布分数 与pH关系如图2[比如:
]。下列说法正确的是
A. 废水中 的含量为
B. c点:C. a点:
D. 的平衡常数
【答案】D
【解析】
A.CH 、N H+ 、H+均能与NaOH反应,关系式为N H+NaOH,即n(N H+ )=n(NaOH),由图可
2 4 4 4
知,加入20mLNaOH溶液时达到滴定终点,可得浓缩废水中c(N H+ )=0.010000mol/L,则原废水中
4
c(N H+ )=0.001000mol/L,即废水中N H+ 的含量为18.00mg⋅L−1,故 A 错误;
4 4
B . c点 溶 液 中 含 有 NaCl、 NaOH, 且 c(Cl− )=0.8c(Na+ ), 电 荷 守 关 系 为
c(CH ) N H++c(H+ )+c(Na+ )=c(OH− )+c(Cl− ),则c(CH ) N++c(H+ )