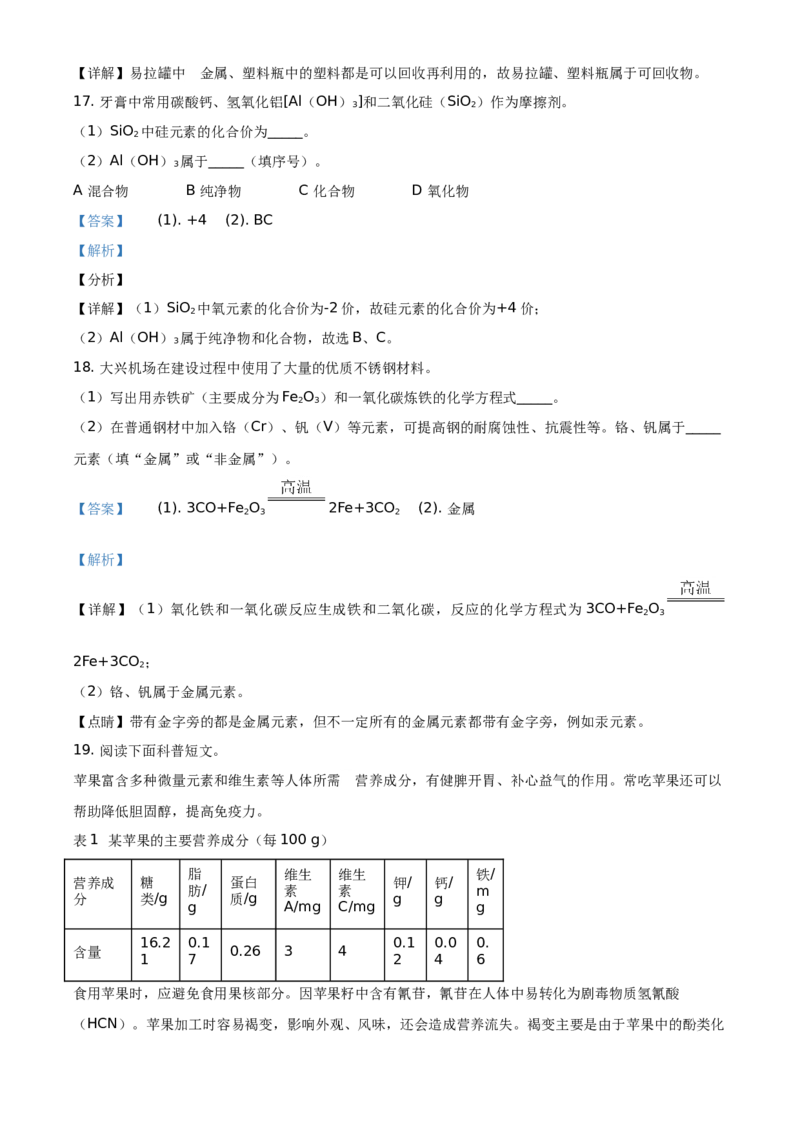文档内容
丰台区 2019~2020 学年度第一学期期末暨毕业练习
初三化学
相对原子质量:H-1 C-12 O-16
第一部分 选择题(共15分)
(每小题只有1个选项符合题意。共15个小题,每小题1分)
1. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
【答案】A
【解析】
【详解】空气的成分按体积计算,大约是:氮气占78%、氧气占21%、稀有气体占0.94%、二氧化碳占
0.03%、其它气体和杂质占0.03%。
2. 下列物质与水混合,不能形成溶液的是
A. 食盐 B. 蔗糖 C. 花生油 D. 白醋
【答案】C
【解析】
【详解】A、食盐能与水形成均一、稳定的溶液,不符合题意;
B、蔗糖能与水形成均一、稳定的溶液,不符合题意;
C、花生油不能与水不互溶,无法形成均一、稳定的溶液,符合题意;
D、白醋能与水形成均一、稳定的溶液,不符合题意。
故选C。
3. 一些物质的pH范围如下,其中呈碱性的是
A. 油污净(12~13) B. 西瓜汁(5~6) C. 洁厕灵(1~2) D. 橘子汁(3~4)
【答案】A
【解析】
【分析】溶液的pH大于7,溶液显碱性;pH=7,显中性;pH小于7 ,显酸性;
【详解】A、油污净的pH=12~13,大于7,故溶液呈碱性,故正确;
B、西瓜汁的pH=(5~6),故显酸性,故错误;
C、洁厕灵pH=(1~2),小于7,故显酸性,故错误;
D、橘子汁pH=(3~4),小于7 ,故选酸性,故错误。故选A。
4. 下列人体所必需的元素中,缺乏会引起贫血的是A. 铁 B. 钙 C. 碘 D. 锌
【答案】A
【解析】
【详解】人体必须的元素中,缺铁容易引起贫血,缺少钙元素会引起骨质疏松症;缺少碘元素会造成甲状
腺肿大;缺少锌元素会发育迟缓,食欲不振;故答案选择A。
5. 氢氧化钙可用于改良酸性土壤,其俗称是( )
A. 小苏打
B. 熟石灰
C. 生石灰
D. 纯碱
【答案】B
【解析】
【详解】试题分析:氢氧化钙可用于改良酸性土壤,其俗称是熟石灰。故选B.
考点:物质的名称
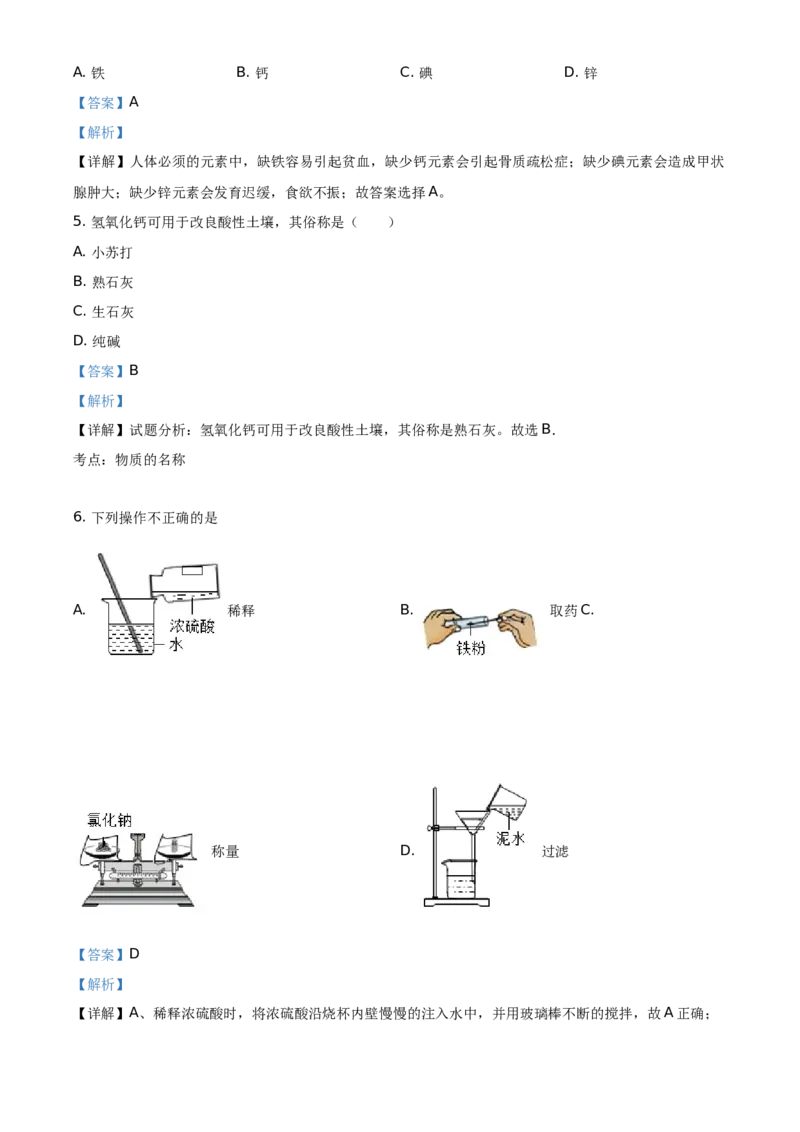
6. 下列操作不正确的是
A. 稀释 B. 取药C.
称量 D. 过滤
【答案】D
【解析】
【详解】A、稀释浓硫酸时,将浓硫酸沿烧杯内壁慢慢的注入水中,并用玻璃棒不断的搅拌,故A正确;B、取用固体药品时,试管要先平放,将药品慢慢的送人试管中底部,在将试管直立,故正确;
C、称量固体药品时,要做到左物右码,故正确;
D、该过滤装置中缺少玻璃棒的引流,故错误。故选D。
7. 下列物质中,含有氧分子的是
A. O B. MnO C. CO D. H O
2 2 2 2 2
【答案】A
【解析】
【详解】A、O 是氧气,由氧分子构成,则含有氧分子,故A正确;
2
B、MnO 不含有氧气,则不含有氧分子,故B错误;
2
C、CO 不含有氧气,则不含有氧分子,故C错误;
2
D、H O 不含有氧气,则不含有氧分子,故D错误;
2 2
故选A.
【点评】本题考查了物质微观构成微粒的知识,完成此题,可以依据已有的知识进行.
8. 三位科学家在锂电池发展上做出了突出贡献,获得了2019年诺贝尔化学奖。已知一种锂原子的原子核
内有3个质子和4个中子。该锂原子的核外电子数为
A. 4 B. 1 C. 7 D. 3
【答案】D
【解析】
【详解】核内质子数与核外电子数相等,故该锂原子的核外电子数为3,故选D。
9. 明代用“烧坊遍地,满城飘香”来形容酿酒业的发达。香飘满城的原因是
A. 分子的质量很小 B. 分子间有间隔
C. 分子在不断运动 D. 分子由原子构成
【答案】C
【解析】
【详解】香飘满城的原因是分子是在不断运动的,所以香味才可以传播,故选C。
10. 电解水实验如图。下列说法正确的是
A. 试管2中得到H
2B. 与试管1相连的电极是负极
C. 产生H 与O 的质量比约为2∶1
2 2
D. 该实验说明水由H 和O 组成
2 2
【答案】B
【解析】
【详解】A、试管1与负极相连,产生氢气;试管2与正极相连,产生氧气,选项错误;
B、由电解水实验图可以看出试管1与电源的负极相连,选项正确;
C、产生氢气和氧气的体积比为2:1,质量比为1:8,选项错误;
D、电解水实验说明水是由氢元素和氧元素组成的,选项错误。
故选B。
11. 下列物质的用途中,利用其物理性质的是
A. 干冰用作冷冻剂 B. 硫酸用于处理碱性废液
C. 氧气用于气焊 D. 生石灰用作干燥剂
【答案】A
【解析】
【详解】试题分析:干冰用于冷冻剂,是利用干冰能够升华吸收热量,过程中没有产生新的物质,属于物
理变化,此性质属于物理性质。故选A.
考点:物质的性质
12. 农业上常用质量分数为16%的NaCl溶液选种。实验室欲配制100 g该浓度的溶液,下列说法不正确
的是
A. 需称量NaCl的质量为16 g
B. 需量取水的体积为100 mL
C. 溶解时用玻璃棒搅拌可以加速溶解
D. 装试剂瓶时有液体洒出,不影响溶液浓度
【答案】B
【解析】
【详解】A、溶液质量为100g,NaCl质量分数为16%,故需称量NaCl的质量为100×16%=16g,正
确,不符合题意;
B、溶液质量为100g,NaCl质量为16g,故需水的质量为100g-16g=84g,错误,符合题意;
C、溶解时用玻璃棒搅拌可以加速溶解,正确,不符合题意;
D、溶液是均一的,稳定的混合物,故装试剂瓶时有液体洒出,不影响溶液浓度,正确,不符合题意。
故选B。13. 英国化学家戴维将光气与氨作用合成尿素,该反应的化学方程式为:COCl + 4NH =2X + CO
2 3
(NH ) ,其中X的化学式为
2 2
A. H B. HCl C. NH Cl D. Cl
2 4 2
【答案】C
【解析】
【详解】反应的化学方程式左边有1个C原子,1个O原子,2个Cl原子,4个N原子和12个H原子;
方程式右边有1个C原子,1个O原子,2个N原子,4个H原子和2X;故2X中含有2个N原子,2个
Cl原子和8个H原子,故X中含有1个N原子,4个H原子和1个Cl原子,X的化学式为NH Cl,故选
4
C。
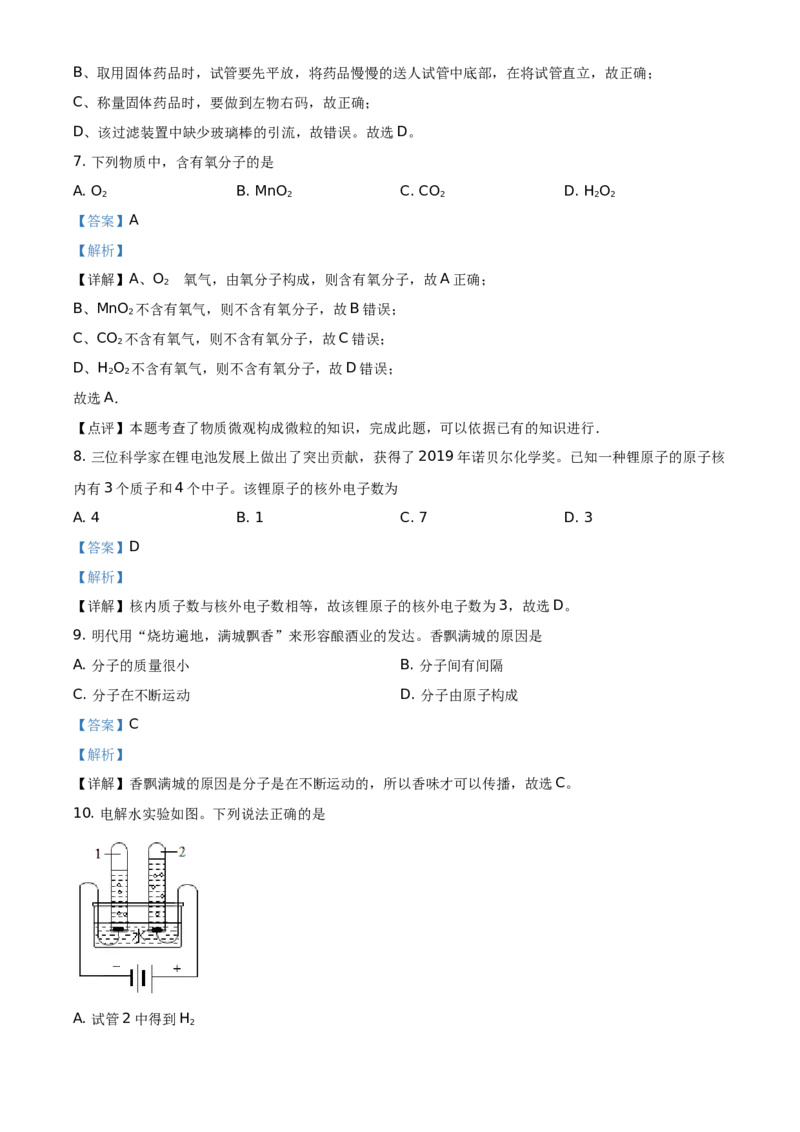
14. 下列不能达到实验目的的是
选
A B C D
项
实
验证甲烷
验 除去粗盐中的 测定空气中氧 除去CO中
燃烧产生
目 难溶性杂质 气含量 的CO
水 2
的
实
验
装 将粗盐研碎、
置 溶解、
或 过滤、蒸发
操
作
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A、除去粗盐中的难溶性杂质,将粗盐研碎、溶解、过滤可除去不溶性杂质,再蒸发可以得到较
纯的盐,可以达到目的,不符合题意;
B、用红磷燃烧来测定空气中氧气含量,水可以从烧杯中流入瓶内,通过瓶内的刻度可以显示空气中氧气
的含量,可以达到目的,不符合题意;
C、验证甲烷燃烧产生水,将产物通入干冷的烧杯,可观察到烧杯内壁有水生成,可以达到目的,不符合
题意;
D、二氧化碳与浓硫酸不能发生反应,无法除去二氧化碳,不能达到目的,符合题意。
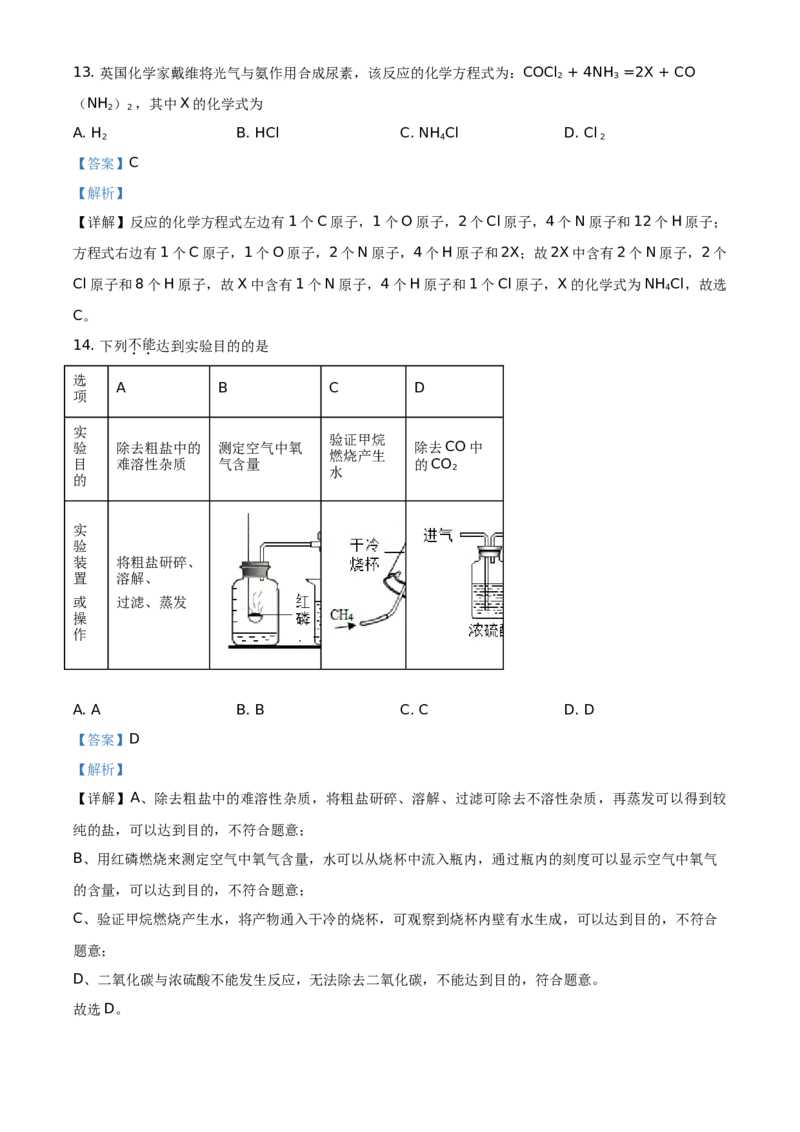
故选D。15. 我国科研人员提出了由CO 和CH 转化为CH COOH的催化反应,该反应的微观示意图如下。下列
2 4 3
说法不正确的是
A. 甲中碳、氢元素的质量比为1∶4 B. 16 g甲完全反应至少需要44 g乙
C. 丙含有三种元素 D. 反应中,甲、乙、丙的分子个数比为1∶1∶1
【答案】A
【解析】
【详解】A、甲是CH ,甲中碳、氢元素的质量比为12:4=3:1;错误,符合题意;
4
B、CO 和CH 转化为CH COOH的催化反应的反应方程式为 ,故16 g
2 4 3
甲完全反应至少需要44 g乙,正确,不符合题意;
C、丙的化学式为CH COOH,含有C、H、O三种元素,正确,不符合题意;
3
D、CO 和CH 转化为CH COOH 的催化反应的反应方程式为 ,故反应中
2 4 3
甲、乙、丙的分子个数比为1∶1∶1,正确,不符合题意。
故选A。
第二部分 非选择题(共35分)
16. 垃圾分类,人人有责。易拉罐、塑料瓶属于 _____ (填序号)。
【答案】C
【解析】【详解】易拉罐中 的金属、塑料瓶中的塑料都是可以回收再利用的,故易拉罐、塑料瓶属于可回收物。
17. 牙膏中常用碳酸钙、氢氧化铝[Al(OH) ]和二氧化硅(SiO )作为摩擦剂。
3 2
(1)SiO 中硅元素的化合价为_____。
2
(2)Al(OH) 属于_____(填序号)。
3
A 混合物 B 纯净物 C 化合物 D 氧化物
【答案】 (1). +4 (2). BC
【解析】
【分析】
【详解】(1)SiO 中氧元素的化合价为-2价,故硅元素的化合价为+4价;
2
(2)Al(OH) 属于纯净物和化合物,故选B、C。
3
18. 大兴机场在建设过程中使用了大量的优质不锈钢材料。
(1)写出用赤铁矿(主要成分为Fe O )和一氧化碳炼铁的化学方程式_____。
2 3
(2)在普通钢材中加入铬(Cr)、钒(V)等元素,可提高钢的耐腐蚀性、抗震性等。铬、钒属于_____
元素(填“金属”或“非金属”)。
【答案】 (1). 3CO+Fe O 2Fe+3CO (2). 金属
2 3 2
【解析】
【详解】(1)氧化铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为3CO+Fe O
2 3
2Fe+3CO ;
2
(2)铬、钒属于金属元素。
【点睛】带有金字旁的都是金属元素,但不一定所有的金属元素都带有金字旁,例如汞元素。
19. 阅读下面科普短文。
苹果富含多种微量元素和维生素等人体所需 的营养成分,有健脾开胃、补心益气的作用。常吃苹果还可以
帮助降低胆固醇,提高免疫力。
表1 某苹果的主要营养成分(每100 g)
脂 维生 维生 铁/
营养成 糖 蛋白 钾/ 钙/
肪/ 素 素 m
分 类/g 质/g g g
g A/mg C/mg g
16.2 0.1 0.1 0.0 0.
含量 0.26 3 4
1 7 2 4 6
食用苹果时,应避免食用果核部分。因苹果籽中含有氰苷,氰苷在人体中易转化为剧毒物质氢氰酸
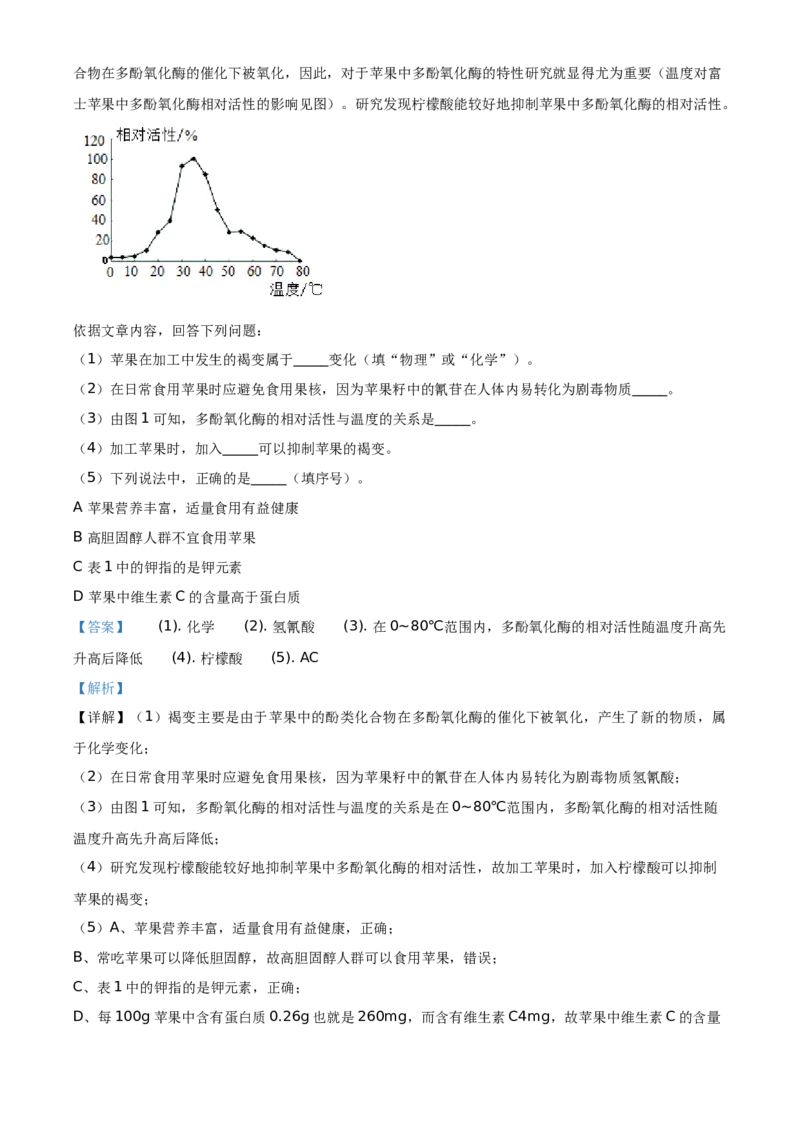
(HCN)。苹果加工时容易褐变,影响外观、风味,还会造成营养流失。褐变主要是由于苹果中的酚类化合物在多酚氧化酶的催化下被氧化,因此,对于苹果中多酚氧化酶的特性研究就显得尤为重要(温度对富
士苹果中多酚氧化酶相对活性的影响见图)。研究发现柠檬酸能较好地抑制苹果中多酚氧化酶的相对活性。
依据文章内容,回答下列问题:
(1)苹果在加工中发生的褐变属于_____变化(填“物理”或“化学”)。
(2)在日常食用苹果时应避免食用果核,因为苹果籽中的氰苷在人体内易转化为剧毒物质_____。
(3)由图1可知,多酚氧化酶的相对活性与温度的关系是_____。
(4)加工苹果时,加入_____可以抑制苹果的褐变。
(5)下列说法中,正确的是_____(填序号)。
A 苹果营养丰富,适量食用有益健康
B 高胆固醇人群不宜食用苹果
C 表1中的钾指的是钾元素
D 苹果中维生素C的含量高于蛋白质
【答案】 (1). 化学 (2). 氢氰酸 (3). 在0~80℃范围内,多酚氧化酶的相对活性随温度升高先
升高后降低 (4). 柠檬酸 (5). AC
【解析】
【详解】(1)褐变主要是由于苹果中的酚类化合物在多酚氧化酶的催化下被氧化,产生了新的物质,属
于化学变化;
(2)在日常食用苹果时应避免食用果核,因为苹果籽中的氰苷在人体内易转化为剧毒物质氢氰酸;
(3)由图1可知,多酚氧化酶的相对活性与温度的关系是在0~80℃范围内,多酚氧化酶的相对活性随
温度升高先升高后降低;
(4)研究发现柠檬酸能较好地抑制苹果中多酚氧化酶的相对活性,故加工苹果时,加入柠檬酸可以抑制
苹果的褐变;
(5)A、苹果营养丰富,适量食用有益健康,正确;
B、常吃苹果可以降低胆固醇,故高胆固醇人群可以食用苹果,错误;
C、表1中的钾指的是钾元素,正确;
D、每100g苹果中含有蛋白质0.26g也就是260mg,而含有维生素C4mg,故苹果中维生素C的含量低于蛋白质,错误。
故选A、C。
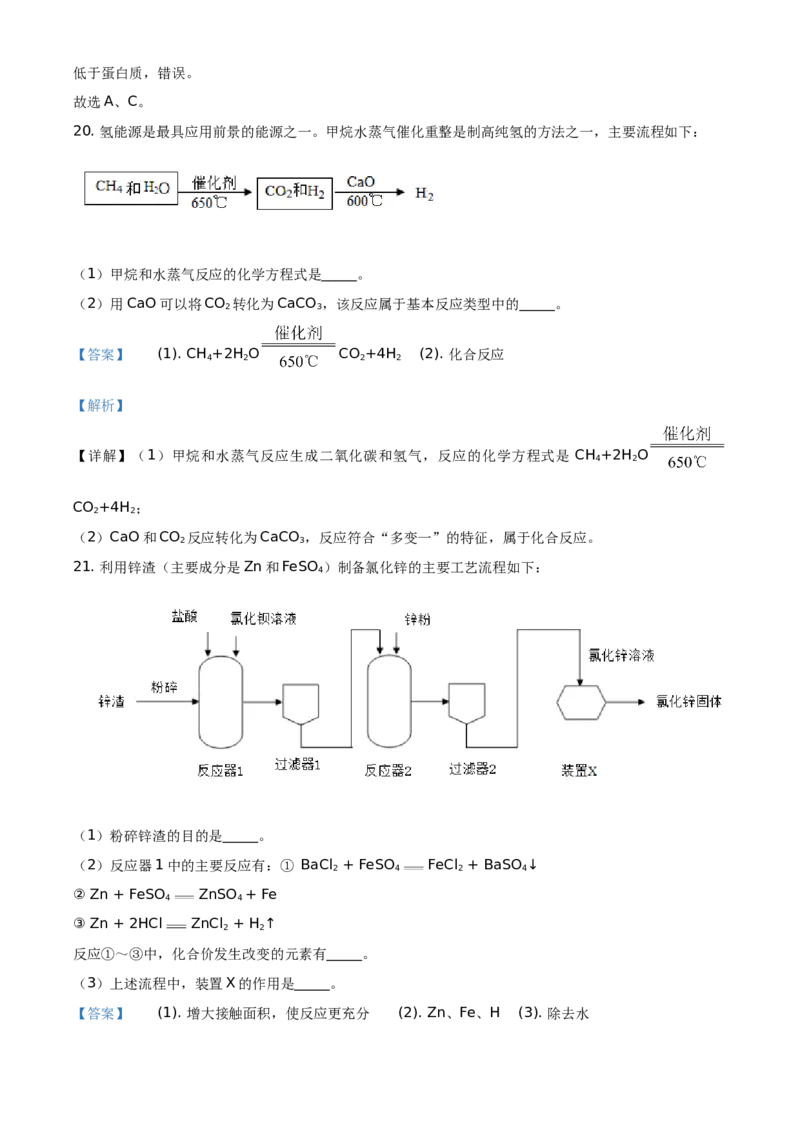
20. 氢能源是最具应用前景的能源之一。甲烷水蒸气催化重整是制高纯氢的方法之一,主要流程如下:
(1)甲烷和水蒸气反应的化学方程式是_____。
(2)用CaO可以将CO 转化为CaCO ,该反应属于基本反应类型中的_____。
2 3
【答案】 (1). CH +2H O CO +4H (2). 化合反应
4 2 2 2
【解析】
【详解】(1)甲烷和水蒸气反应生成二氧化碳和氢气,反应的化学方程式是 CH +2H O
4 2
CO +4H ;
2 2
(2)CaO和CO 反应转化为CaCO ,反应符合“多变一”的特征,属于化合反应。
2 3
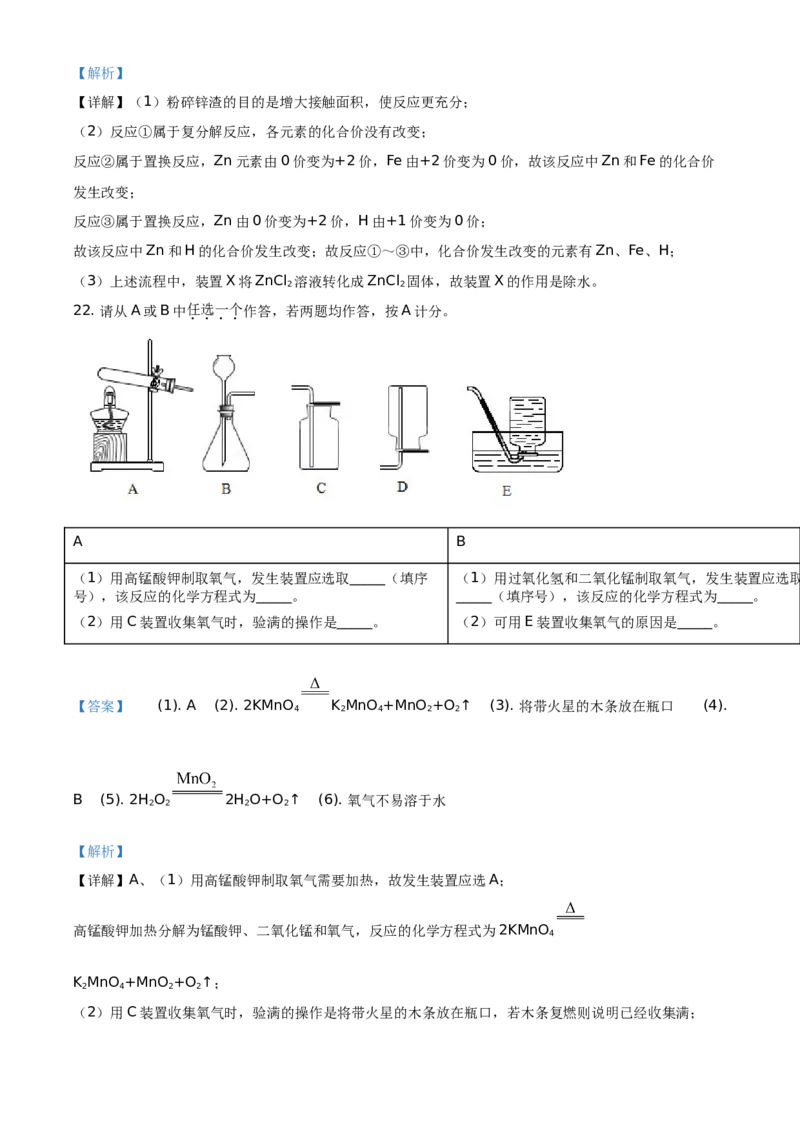
21. 利用锌渣(主要成分是Zn和FeSO )制备氯化锌的主要工艺流程如下:
4
(1)粉碎锌渣的目的是_____。
(2)反应器1中的主要反应有:① BaCl + FeSO FeCl + BaSO ↓
2 4 2 4
② Zn + FeSO ZnSO + Fe
4 4
③ Zn + 2HCl ZnCl + H ↑
2 2
反应①~③中,化合价发生改变的元素有_____。
(3)上述流程中,装置X的作用是_____。
【答案】 (1). 增大接触面积,使反应更充分 (2). Zn、Fe、H (3). 除去水【解析】
【详解】(1)粉碎锌渣的目的是增大接触面积,使反应更充分;
(2)反应①属于复分解反应,各元素的化合价没有改变;
反应②属于置换反应,Zn元素由0价变为+2价,Fe由+2价变为0价,故该反应中Zn和Fe的化合价
发生改变;
反应③属于置换反应,Zn由0价变为+2价,H由+1价变为0价;
故该反应中Zn和H的化合价发生改变;故反应①~③中,化合价发生改变的元素有Zn、Fe、H;
(3)上述流程中,装置X将ZnCl 溶液转化成ZnCl 固体,故装置X的作用是除水。
2 2
22. 请从A或B中任选一个作答,若两题均作答,按A计分。
A B
(1)用高锰酸钾制取氧气,发生装置应选取_____(填序 (1)用过氧化氢和二氧化锰制取氧气,发生装置应选取
号),该反应的化学方程式为_____。 _____(填序号),该反应的化学方程式为_____。
(2)用C装置收集氧气时,验满的操作是_____。 (2)可用E装置收集氧气的原因是_____。
【答案】 (1). A (2). 2KMnO K MnO +MnO +O ↑ (3). 将带火星的木条放在瓶口 (4).
4 2 4 2 2
B (5). 2H O 2H O+O ↑ (6). 氧气不易溶于水
2 2 2 2
【解析】
【详解】A、(1)用高锰酸钾制取氧气需要加热,故发生装置应选A;
高锰酸钾加热分解为锰酸钾、二氧化锰和氧气,反应的化学方程式为2KMnO
4
K MnO +MnO +O ↑;
2 4 2 2
(2)用C装置收集氧气时,验满的操作是将带火星的木条放在瓶口,若木条复燃则说明已经收集满;B、(1)用过氧化氢和二氧化锰制取氧气不需要加热,发生装置应选B;
过氧化氢在二氧化锰催化下生成水和氧气,反应的化学方程式为2H O 2H O+O ↑;
2 2 2 2
(2)可用E装置的排水法收集氧气的原因是氧气不易溶于水。
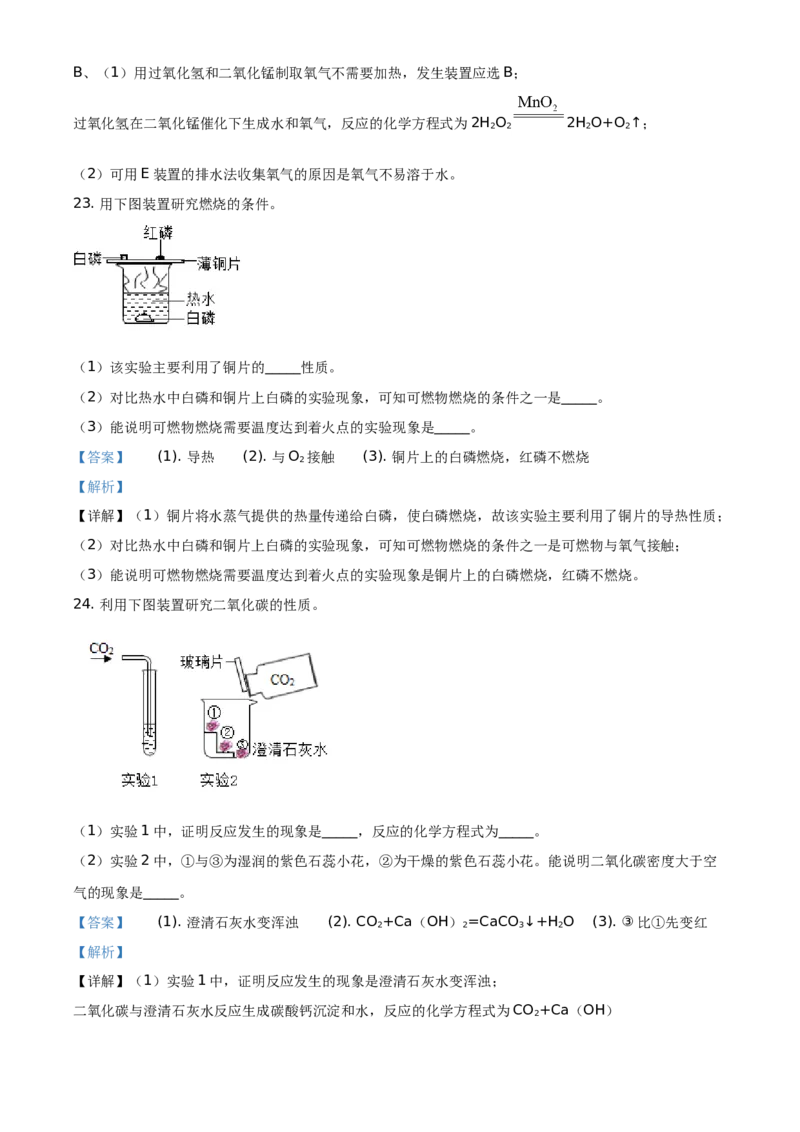
23. 用下图装置研究燃烧的条件。
(1)该实验主要利用了铜片的_____性质。
(2)对比热水中白磷和铜片上白磷的实验现象,可知可燃物燃烧的条件之一是_____。
(3)能说明可燃物燃烧需要温度达到着火点的实验现象是_____。
【答案】 (1). 导热 (2). 与O 接触 (3). 铜片上的白磷燃烧,红磷不燃烧
2
【解析】
【详解】(1)铜片将水蒸气提供的热量传递给白磷,使白磷燃烧,故该实验主要利用了铜片的导热性质;
(2)对比热水中白磷和铜片上白磷的实验现象,可知可燃物燃烧的条件之一是可燃物与氧气接触;
(3)能说明可燃物燃烧需要温度达到着火点的实验现象是铜片上的白磷燃烧,红磷不燃烧。
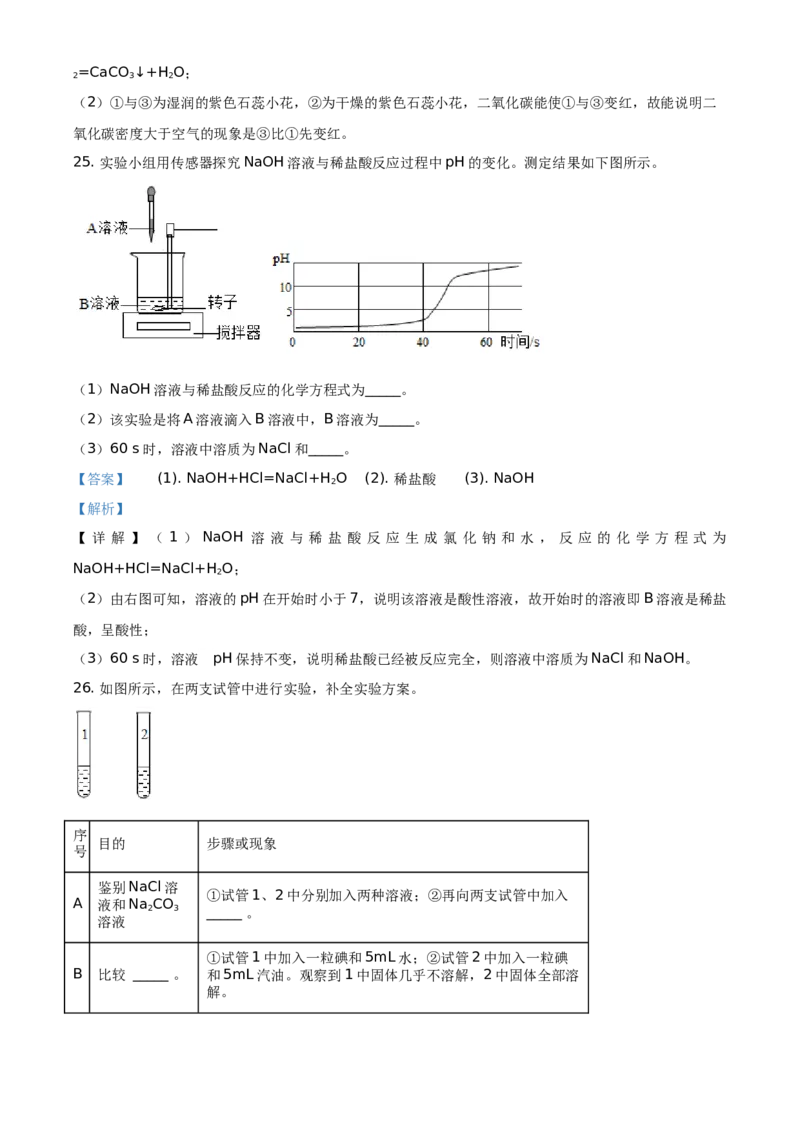
24. 利用下图装置研究二氧化碳的性质。
(1)实验1中,证明反应发生的现象是_____,反应的化学方程式为_____。
(2)实验2中,①与③为湿润的紫色石蕊小花,②为干燥的紫色石蕊小花。能说明二氧化碳密度大于空
气的现象是_____。
【答案】 (1). 澄清石灰水变浑浊 (2). CO +Ca(OH) =CaCO ↓+H O (3). ③比①先变红
2 2 3 2
【解析】
【详解】(1)实验1中,证明反应发生的现象是澄清石灰水变浑浊;
二氧化碳与澄清石灰水反应生成碳酸钙沉淀和水,反应的化学方程式为CO +Ca(OH)
2=CaCO ↓+H O;
2 3 2
(2)①与③为湿润的紫色石蕊小花,②为干燥的紫色石蕊小花,二氧化碳能使①与③变红,故能说明二
氧化碳密度大于空气的现象是③比①先变红。
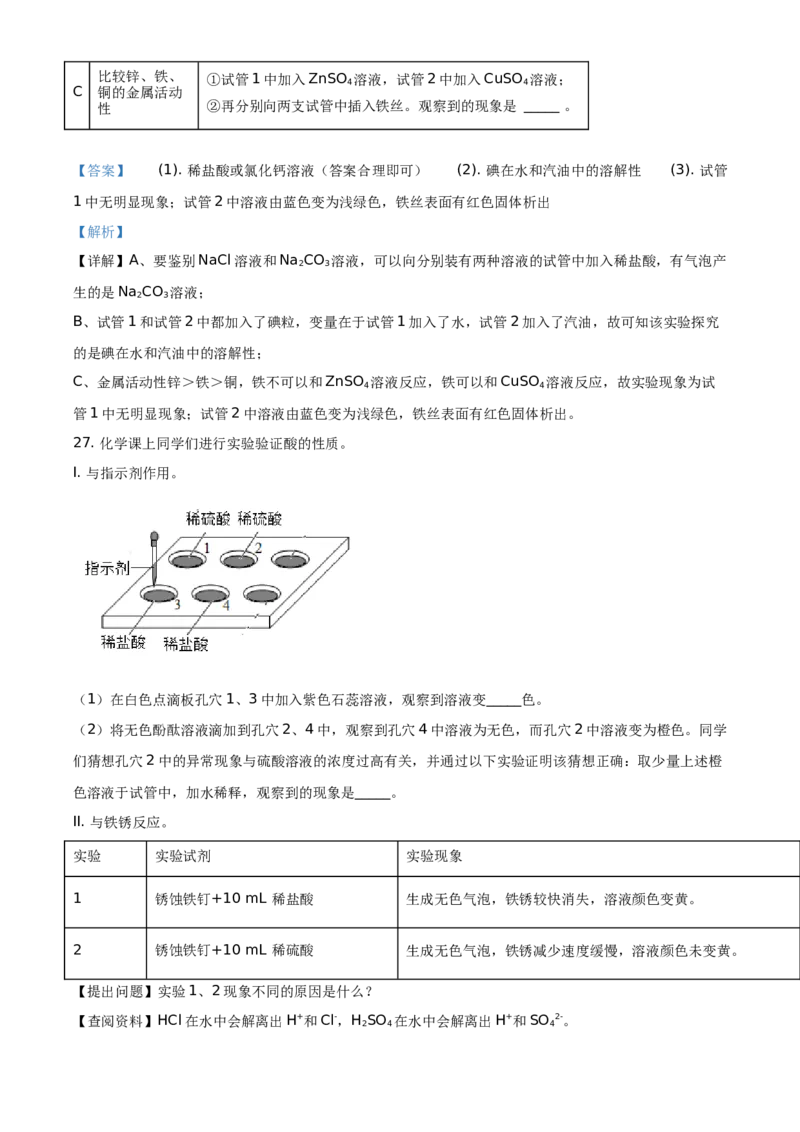
25. 实验小组用传感器探究NaOH溶液与稀盐酸反应过程中pH的变化。测定结果如下图所示。
(1)NaOH溶液与稀盐酸反应的化学方程式为_____。
(2)该实验是将A溶液滴入B溶液中,B溶液为_____。
(3)60 s时,溶液中溶质为NaCl和_____。
【答案】 (1). NaOH+HCl=NaCl+H O (2). 稀盐酸 (3). NaOH
2
【解析】
【 详 解 】 ( 1 ) NaOH 溶 液 与 稀 盐 酸 反 应 生 成 氯 化 钠 和 水 , 反 应 的 化 学 方 程 式 为
NaOH+HCl=NaCl+H O;
2
(2)由右图可知,溶液的pH在开始时小于7,说明该溶液是酸性溶液,故开始时的溶液即B溶液是稀盐
酸,呈酸性;
(3)60 s时,溶液 的pH保持不变,说明稀盐酸已经被反应完全,则溶液中溶质为NaCl和NaOH。
26. 如图所示,在两支试管中进行实验,补全实验方案。
序
目的 步骤或现象
号
鉴别NaCl溶
①试管1、2中分别加入两种溶液;②再向两支试管中加入
A 液和Na CO
2 3 _____ 。
溶液
①试管1中加入一粒碘和5mL水;②试管2中加入一粒碘
B 比较 _____ 。 和5mL汽油。观察到1中固体几乎不溶解,2中固体全部溶
解。比较锌、铁、 ①试管1中加入ZnSO 溶液,试管2中加入CuSO 溶液;
4 4
C 铜的金属活动
性 ②再分别向两支试管中插入铁丝。观察到的现象是 _____ 。
【答案】 (1). 稀盐酸或氯化钙溶液(答案合理即可) (2). 碘在水和汽油中的溶解性 (3). 试管
1中无明显现象;试管2中溶液由蓝色变为浅绿色,铁丝表面有红色固体析出
【解析】
【详解】A、要鉴别NaCl溶液和Na CO 溶液,可以向分别装有两种溶液的试管中加入稀盐酸,有气泡产
2 3
生的是Na CO 溶液;
2 3
B、试管1和试管2中都加入了碘粒,变量在于试管1加入了水,试管2加入了汽油,故可知该实验探究
的是碘在水和汽油中的溶解性;
C、金属活动性锌>铁>铜,铁不可以和ZnSO 溶液反应,铁可以和CuSO 溶液反应,故实验现象为试
4 4
管1中无明显现象;试管2中溶液由蓝色变为浅绿色,铁丝表面有红色固体析出。
27. 化学课上同学们进行实验验证酸的性质。
I. 与指示剂作用。
(1)在白色点滴板孔穴1、3中加入紫色石蕊溶液,观察到溶液变_____色。
(2)将无色酚酞溶液滴加到孔穴2、4中,观察到孔穴4中溶液为无色,而孔穴2中溶液变为橙色。同学
们猜想孔穴2中的异常现象与硫酸溶液的浓度过高有关,并通过以下实验证明该猜想正确:取少量上述橙
色溶液于试管中,加水稀释,观察到的现象是_____。
II. 与铁锈反应。
实验 实验试剂 实验现象
1 锈蚀铁钉+10 mL 稀盐酸 生成无色气泡,铁锈较快消失,溶液颜色变黄。
2 锈蚀铁钉+10 mL 稀硫酸 生成无色气泡,铁锈减少速度缓慢,溶液颜色未变黄。
【提出问题】实验1、2现象不同的原因是什么?
【查阅资料】HCl在水中会解离出H+和Cl-,H SO 在水中会解离出H+和SO 2-。
2 4 4【假设猜想】可能和溶液中阴离子不同有关。
【进行实验】
实验 实验试剂 实验现象
3 锈蚀铁钉+10 mL稀硫酸 + _A_ 生成无色气泡,铁锈减少速度比实验2快,溶液颜色变黄。
4 锈蚀铁钉+10 mL稀盐酸 + Na SO 生成无色气泡,铁锈减少速度比实验1慢,溶液颜色变黄。
2 4
【解释和结论】
(3)铁锈(主要成分为Fe O )和盐酸反应的化学方程式是_____。
2 3
(4)实验1中产生的无色气体是_____。
(5)实验3中,物质A是_____。
(6)结合实验1~4,得出的结论是_____。
【答案】 (1). 红 (2). 溶液由橙色变为无色 (3). Fe O +6HCl=2FeCl +3H O (4). H
2 3 3 2 2
(5). NaCl (6). 稀硫酸、稀盐酸与锈蚀铁钉反应的现象不同与溶液中阴离子不同有关
【解析】
【详解】(1)紫色石蕊试液遇酸变红,故在白色点滴板孔穴1、3中加入紫色石蕊溶液,观察到溶液变红;
(2)取少量上述橙色溶液于试管中,加水稀释,硫酸的浓度降低,故观察到的现象是溶液由橙色变为无
色;
(3)铁锈(主要成分为Fe O )和盐酸反应生成氯化铁和水,反应的化学方程式为
2 3
Fe O +6HCl=2FeCl +3H O;
2 3 3 2
(4)铁和稀盐酸反应产生氢气,故实验1中产生的无色气体是氢气;
(5)实验3和实验4是对比实验,是为了探究Cl-和SO 2-对反应的影响,实验4加了Na SO 溶液,则
4 2 4
实验3应该加入NaCl溶液;
(6)结合实验1~4,得出的结论是稀硫酸、稀盐酸与锈蚀铁钉反应的现象不同与溶液中阴离子不同有关。本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635