文档内容
泰州市二○○九年初中毕业、升学统一考试
化学试题
(考试时间:90分钟 满分:100分)
请注意:l.本试卷分为选择题和非选择题两个部分。
2.所有试题的答案均填写在答题卡上,答案写在试卷上无效。
可能用到的相对原子质量:
H一1 C一12 N一14 O一16 Na一23 Mg一24 S一32 Ca一40
第一部分 选择题(共40分)
一、(本题包括l5小题,每小题2分,共30分。每小题只有一个选项符合题意)
1.下列性质属于化学性质的是
A.沸点 B.硬度 C.还原性 D.溶解性
2.下列变化属于化学变化的是
A.瓦斯爆炸 B.海水晒盐 C.潮涨潮落 D.干冰升华
3.下列物质的俗名与化学式一致的是
A.水银Ag B.纯碱NaHCO C.酒精CHO D.烧碱NaOH
3 4
4.吸烟有害健康,其原因是吸烟时会产生多种有害物质,污染环境,害人害己。香烟燃烧产生
的烟气中,最容易与人体血红蛋白结合的物质是
A.一氧化碳 B.尼古丁 C.二氧化硫 D.二氧化碳
5.下列物质由离子构成的是
A.铜 B.氯化钠 C.氧气 D.金刚石
6.下列材料中属于天然纤维的是
A.塑料 B.铁丝 C.玻璃丝 D.棉花
7.下列混合物中不属于溶液的是
A.食盐水 B.泥水 C.碘酒 D.澄清石灰水
8.结构示意图 表示的微粒是
+11 28
A.原子 B.分子 C.阳离子 D.阴离子
9.下列气体通入高锰酸钾酸性溶液中,能使溶液紫红色褪去的是
A.SO B.CO C.N D.O
2 2 2 2
10.2009年春夏之际,世界上多个国家和地区出现了甲型HlNl流感。甲型HINl流感与普
通流感一样“可防可治”。甲型HlNl流感病毒属于
A.淀粉 B.蛋白质 C.油脂 D.葡萄糖
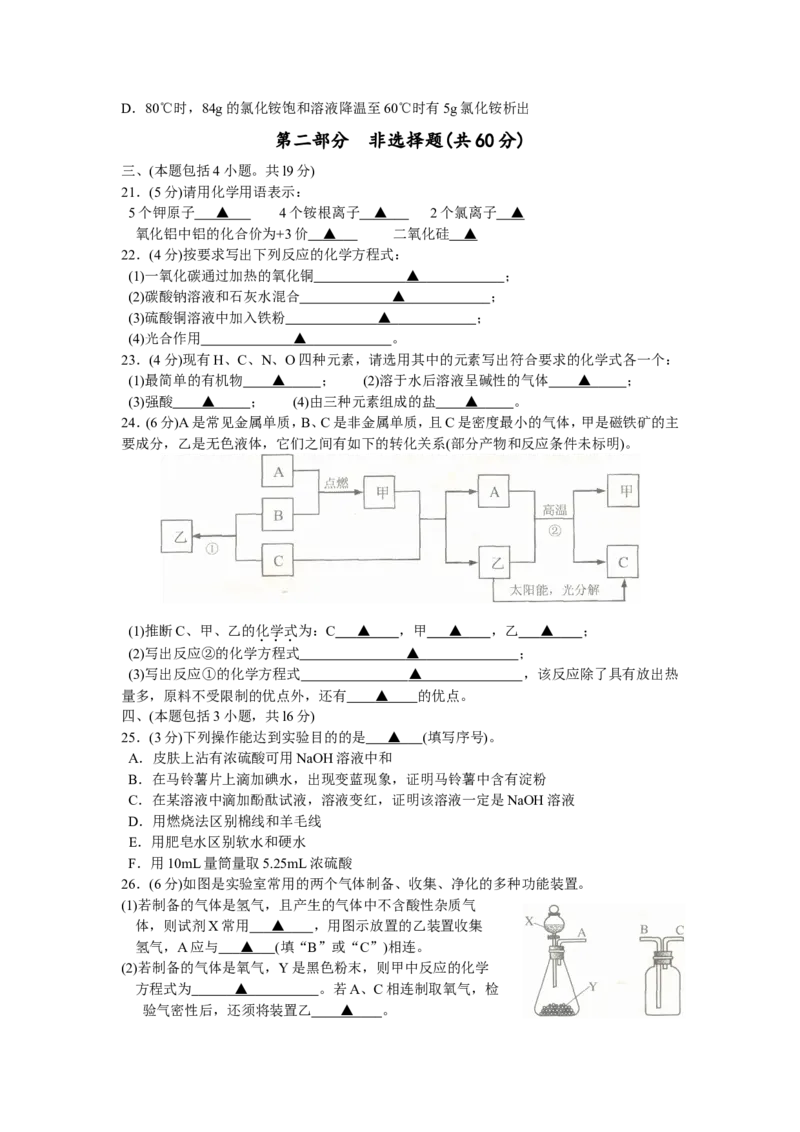
11.下列实验操作正确的是
A B C D12.“人离不开水,没有水就没有生命”。在生产自来水的过程中不能加入或通入的物质是
A.明矾 B.漂白粉 C.臭氧 D.硫酸铜
13.不用其他试剂,可以鉴别石蕊、盐酸、氢氧化钙、氢氧化钠、碳酸钠五种溶液,第二个被鉴
别出来的物质是
A.盐酸 B.氢氧化钙 C.氢氧化钠 D.碳酸钠
14.煤油中含有噻吩,噻吩(用X表示)有令人不愉快的气味,其燃烧的化学方程式可表示为:
X+6O 4CO+SO+2H O,则噻吩X的化学式为
2 2 2 2
A.CHS B.C HS C.C HS D.C HS
4 2 6 4 4 6 6
15.A、B、C、D是四种金属单质,A能从B的硝酸盐溶液中置换出B,但A不能与稀盐酸反应。
相同条件下,C、D能与稀盐酸反应产生H,且D比C反应剧烈。则四种金属的活动性由强到
2
弱的顺序是
A.A、B、C、D B.B、A、C、D C.D、C、A、B D.D、C、B、A
二、(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意。若正确答案
包括一个选项。多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,
选两个且都正确的给2分,但只要选错一个,该小题为0分)
16.下列说法正确的是
A.pH越小,溶液的酸性越强
B.pH小于5.6的雨水是酸雨
C.胃酸过多的病人在空腹时最好多喝一些柠檬汁
D.用pH试纸伸入某溶液中测定其pH
17.人类只有一个地球,为了社会可持续发展,必须解决环境保护问题,化学在这方面可以发
挥重要的作用。下列处理不符合这一思想的是
A.增加污水处理工厂 B.向燃煤中加生石灰固硫
c.大量使用含磷酸钠(Na PO)的洗衣粉 D.垃圾的分类回收和处理
3 4
18.β胡萝卜素(C H )是一种天然的植物色素,它广泛存在于黄绿色蔬菜和水果中,一定条
40 56
件下在人体内能够转化为维生素A(C H O)。下列有关说法正确的是
20 30
A.维生素A中碳、氢、氧三种元素的质量比为20:30:1
B.维生素A的相对分子质量为286g
C.维生素不是人体必需的营养物质
D.β一胡萝卜素在植物油中的溶解度比在水中大
19.为了除去物质中的杂质(括号内物质为杂质),所选用试剂和操作方法都正确的是
物 质 选用试剂(过量) 操作方法
A CO(CO) O 点燃
2 2
B Cu(Fe) 稀盐酸 加入稀盐酸充分反应后过滤、洗涤
C CuSO溶液(H SO) 氧化铜 加入氧化铜粉末充分反应后过滤
4 2 4
D 盐酸(H SO) 硝酸钡溶液 加入硝酸钡溶液充分反应后过滤
2 4
20.下表是氯化铵在不同温度时的溶解度
温度/℃ 20 40 60 80
溶解度/g 40 50 58 68
据此数据,判断下列说法正确的是
A.20℃时,氯化铵饱和溶液中氯化铵的质量分数是25%
B.20℃时,70g氯化铵的饱和溶液升温至40℃得到不饱和溶液
C.40℃时,75g氯化铵的饱和溶液中加入25g水后氯化铵的质量分数为30%D.80℃时,84g的氯化铵饱和溶液降温至60℃时有5g氯化铵析出
第二部分 非选择题(共60分)
三、(本题包括4小题。共l9分)
21.(5分)请用化学用语表示:
5个钾原子 ▲ 4个铵根离子 ▲ 2个氯离子 ▲
氧化铝中铝的化合价为+3价 ▲ 二氧化硅 ▲
22.(4分)按要求写出下列反应的化学方程式:
(1)一氧化碳通过加热的氧化铜 ▲ ;
(2)碳酸钠溶液和石灰水混合 ▲ ;
(3)硫酸铜溶液中加入铁粉 ▲ ;
(4)光合作用 ▲ 。
23.(4分)现有H、C、N、O四种元素,请选用其中的元素写出符合要求的化学式各一个:
(1)最简单的有机物 ▲ ; (2)溶于水后溶液呈碱性的气体 ▲ ;
(3)强酸 ▲ ; (4)由三种元素组成的盐 ▲ 。
24.(6分)A是常见金属单质,B、C是非金属单质,且C是密度最小的气体,甲是磁铁矿的主
要成分,乙是无色液体,它们之间有如下的转化关系(部分产物和反应条件未标明)。
(1)推断C、甲、乙的化学式为:C ▲ ,甲 ▲ ,乙 ▲ ;
(2)写出反应②的化学方程式 ▲ ;
(3)写出反应①的化学方程式 ▲ ,该反应除了具有放出热
量多,原料不受限制的优点外,还有 ▲ 的优点。
四、(本题包括3小题,共l6分)
25.(3分)下列操作能达到实验目的的是 ▲ (填写序号)。
A.皮肤上沾有浓硫酸可用NaOH溶液中和
B.在马铃薯片上滴加碘水,出现变蓝现象,证明马铃薯中含有淀粉
C.在某溶液中滴加酚酞试液,溶液变红,证明该溶液一定是NaOH溶液
D.用燃烧法区别棉线和羊毛线
E.用肥皂水区别软水和硬水
F.用10mL量筒量取5.25mL浓硫酸
26.(6分)如图是实验室常用的两个气体制备、收集、净化的多种功能装置。
(1)若制备的气体是氢气,且产生的气体中不含酸性杂质气
体,则试剂X常用 ▲ ,用图示放置的乙装置收集
氢气,A应与 ▲ (填“B”或“C”)相连。
(2)若制备的气体是氧气,Y是黑色粉末,则甲中反应的化学
方程式为 ▲ 。若A、C相连制取氧气,检
验气密性后,还须将装置乙 ▲ 。(3)若X是稀盐酸、Y是石灰石,用甲、乙两装置组成发生、 甲 乙
净化、收集CO 气体的系列装置。若乙中放入饱和NaHCO 溶液,该溶液的作用是除去
2 3
▲ ;若乙中放入浓硫酸,浓硫酸的作用是 ▲ 。
27.(7分)化学试剂的等级分为实验纯(LR)、化学纯(CP)、分析纯(AR)等。化学纯试剂厂泛
应用于化学实验中。现由市售大理石(假设杂质均不参加反应,且不溶于水)制备化学纯碳
酸钙,某化学活动小组设计了两个方案:
方案一:市售大理石 煅 烧 固体 水 物质X 气 体 甲 沉淀→过滤、洗涤、晾干
① ② ③
方案二:市售大理石 混合物 Y溶液 沉淀→过滤、洗涤、晾干
盐酸 试剂乙
回答下列问题: ④ ⑤
(1)气体甲的化学式是 ▲ ,试剂乙的名称是 ▲ ;
▲
(2)反应类型:①属于 ▲ 反应,④属于 ▲ 反应;
(3)对方案二制得的碳酸钙进行分析,确认其达到化学纯等级。将 ▲
所得的固体粉末装入广口瓶中,需要贴上标签,请在右边的标签
上注明相关信息。 ▲
(4)经检测方案一制得的碳酸钙没有达到化学纯等级,请你分析原因 ▲ (只
需要回答一个方面)。
五、(本题包括2小题,共l7分)
28.(6分)南宋诗人赵师秀有诗“黄梅时节家家雨,青草池塘处处蛙。有约不来过夜半,闲敲
棋子落灯花。”诗中“灯花”是蜡烛不完全燃烧产生的炭附着在蜡烛芯上的现象。
(1)制造蜡烛的原料是石蜡,石蜡属于 ▲ (填序号)。
A.无机物 B.有机物 C.纯净物 D.混合物
(2)家用石油液化气与石蜡属于同类别物质,欲使其燃烧不产生“灯
花”现象的条件是 ▲ 。
(3)如图是小李同学从点燃的蜡烛火焰中引出一缕“白烟”的实验
装置。小李同学认为“白烟”的成分是水蒸气,小王同学认为“白
烟”的成分是蜡烛蒸汽。请你参与探究,确定“白烟”成分。验证小
李同学猜想所用的方法是 ▲ ;支持小王同学猜想
的方法是 ▲ 。
29.(11分)钢铁、铝合金、铜制品等是应用广泛的金属材料。据估计,每年全世界被腐蚀损耗
的钢铁材料,约占全年钢产量的十分之一。某校化学兴趣小组的同学探究金属腐蚀的原因,
设计如下实验:
(1)如图,取一根约10cm的光亮铁钉放在自来水中,观察A、B、C三处的变化。
几天后,他们会发现 ▲ 处最先出现铁锈,大家结合书本知识知道,铁在空
气中生锈实际是铁和 ▲ 、 ▲ 等物质相互作用发生一系列复杂的
化学反应的过程。
(2)一同学联想到家里铜制餐具上有一层绿色物质,认为铜在空气中也会生锈。
他们上网查阅资料,知道这种绿色物质的化学成分为Cu (OH) CO(铜绿)。他们从铜绿组成和
2 2 3
空气的成分大胆猜测,铜生锈除了与铁生锈条件相同外,还应该有CO 参加反应。
2
请写出铜在空气中生成铜绿的化学方程式 ▲ 。
(3)【查阅资料】孔雀石的主要成分是Cu (OH) CO,也可以表示成CuCO·Cu(OH) 。
2 2 3 3 2
与孔雀石相似,还有许多矿物可用xCuCO·yCu(OH) (x、y都是正整数)表示,石青
3 2
就是其中的一种。【实验探究】为了验证石青的组成成分,他们设计了如下实验,请你共同参与探究。
实验操作 实验现象 结论
取少量石青样品置于大(1)产生大量气体 (1)石青中含有 ▲ 离子
步骤l
试管中加入足量稀硫酸 (2)溶液呈蓝色 (2)石青中含有 ▲ 离子
取少量石青样品置于大(1)残留固体呈 ▲ 色
步骤2 石青加热易分解
试管中加热 (2)大试管内壁 ▲
【反思与拓展】
①确定步骤1中产生气体成分的实验方法是 ▲ 。
②根据以上探究,只要测定出参加反应的石青的质量、生成的氧化铜的质量和 ▲ 的质
量,就可确定石青的化学式(即确定x、y的值)。
③防止金属锈蚀的方法很多,如制成不锈钢、在金属表面 ▲ (任写一种方法)。
六、(本题包括l小题,共8分)
30.(8分)某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫
酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
稀硫酸用量 剩余固体质量
第一次加入10g mg
第二次加入10g 2.0g
第三次加入10g 1.5g
第四次加入10g 1.0g
第五次加入10g 0.6g
第六次加入10g 0.6g
(1)测定过程中发生反应的化学方程式为 ▲ ;
(2)从以上数据可知,最后剩余的0.6g固体的成分是 ▲ ;这六次实验中,第 ▲ 次
加入稀硫酸时样品中的镁已经完全反应;表格中,m= ▲ 。
(3)计算合金样品中镁的质量分数。
(4)计算所用稀硫酸中HSO 的质量分数。
2 4
泰州市二○○九年初中毕业、升学统一考试化学试题参考答案
一、(本题包括l5小题,每小题2分,共30分。每小题只有一个选项符合题意)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C A D A B D B C A B C D A C C
二、
题号 16 17 18 19 20
答案 AB C D BC BD
三、(本题包括4小题。共l9分)
21.5K 4NH + 2Cl- SiO
4 2
22.(1) CO+CuO =△==Cu+CO
2(2) NaCO+Ca(OH) =CaCO ↓+2NaOH
2 3 2 3
(3) Fe+CuSO =Cu+FeSO
4 4
(4) 6CO 2 +6H 2 O 光 C 6 H 12 O 6 +6O 2
叶绿素
23.CH NH HNO NH NO
4 3 3 4 3
24.(1) H Fe O HO (2) 3Fe+4HO 高=温== Fe O+4H
2 3 4 2 2 3 4 2
(3) 2H
2
+O
2
点=燃== 2H
2
O 产物无污染
四、(本题包括3小题,共l6分)
25.BDE
MnO
26.(1) 稀硫酸 C (2) 2HO ===2= 2HO+ O↑ 装满水或倒立
2 2 2 2
(3) 除氯化氢气体 干燥气体或除去水蒸气
27.(1) CO 碳酸钠或碳酸钾 (2) 分解 复分解 (3) 化学纯或CP 碳酸钙
2
CaCO (4) 通入CO 前没有过滤或石灰石锻烧不完全或水不多或气体甲不纯或气体甲的
3 2
量少
五、(本题包括2小题,共l7分)
28.(1) D (2) 调节风门,保证有足够的空气或要充分燃烧 (3) 让白烟通过无水硫酸铜或
用干冷的烧杯罩在白烟上方 将白烟用火柴点燃或将白烟冷却得到白色的蜡状固体
29.(1) B O 或氧气 HO或水 (2) 2Cu+O+HO+CO ===Cu (OH) CO
2 2 2 2 2 2 2 3
(3) 【查阅资料】CO2- Cu2+ 黑 有水珠
3
【反思与拓展】
①将产生的气体通入足量的澄清石灰水中
②水或二氧化碳
③涂油、漆等
六、(本题包括l小题,共8分)
30.(1) Mg+HSO =MgSO +H↑ (2) Cu 5 2.5 (3) 80% (4) 20.4%
2 4 4 2