文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【大单元复习】2024 年中考化学一轮复习备考学案(人教版)
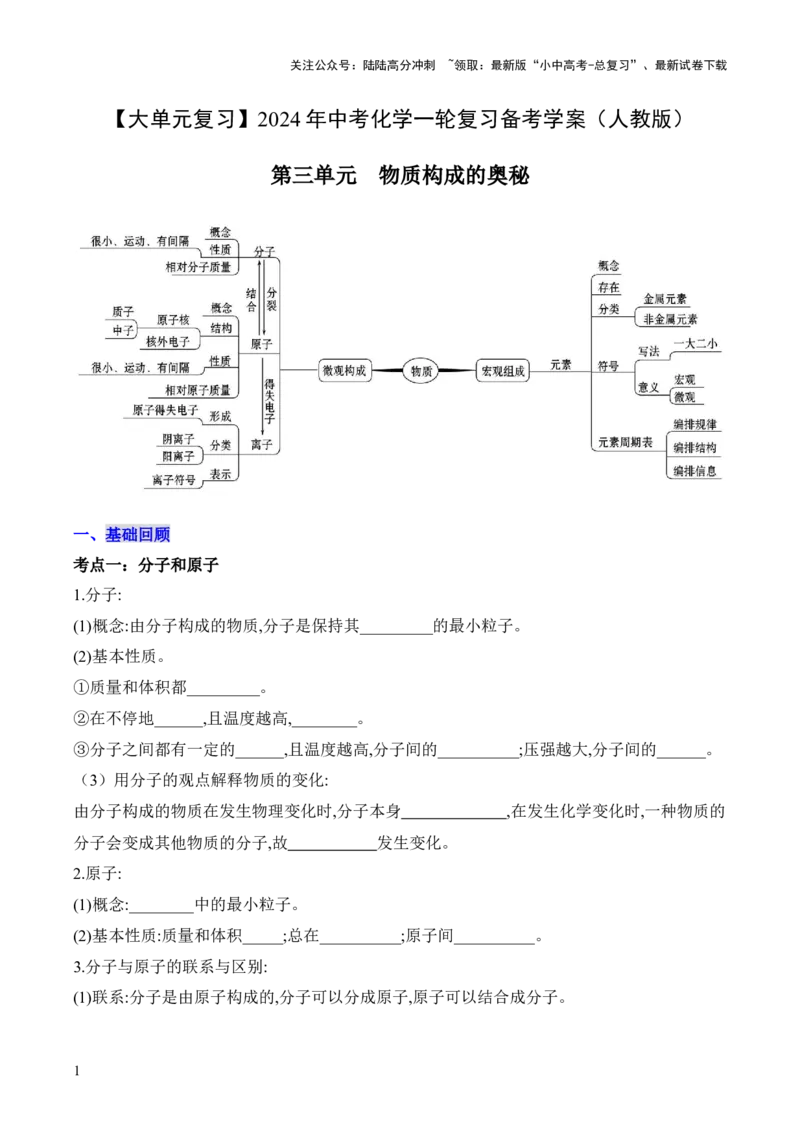
第三单元 物质构成的奥秘
一、基础回顾
考点一:分子和原子
1.分子:
(1)概念:由分子构成的物质,分子是保持其_________的最小粒子。
(2)基本性质。
①质量和体积都_________。
②在不停地______,且温度越高,________。
③分子之间都有一定的______,且温度越高,分子间的__________;压强越大,分子间的______。
(3)用分子的观点解释物质的变化:
由分子构成的物质在发生物理变化时,分子本身 ,在发生化学变化时,一种物质的
分子会变成其他物质的分子,故 发生变化。
2.原子:
(1)概念:________中的最小粒子。
(2)基本性质:质量和体积_____;总在__________;原子间__________。
3.分子与原子的联系与区别:
(1)联系:分子是由原子构成的,分子可以分成原子,原子可以结合成分子。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)区别: 。
4.化学变化的实质:化学变化中,反应物的分子首先分成 , 重新结合成
_________。
考点二:原子的结构
(一)原子的构成:
1.
2. 构 成原子的粒子之
间的关系
(1)位置关系:原子核居于 ,决定原子的 。
(2)数量关系:在原子中, _______数= 数 =_________数=_________数
(3)电性关系:质子和电子所带电量_________,电性_________,故原子 电
性。
(4)原子的种类与质子数关系: ;
(5)元素的化学性质与外层电子数关系: 。
(二)原子核外电子的排布:
1.原子结构示意图。
2.原子结构与元素化学性质的关系:
元素分类 原子最外层电子数 结构的稳定性 化学性质
金属元素 通常不超过_____个 不稳定 易
非金属元素 通常多于____个 不稳定 易
稀有气体元素 ____个(He 为____个) 稳定 不易
3.相对原子质量:
(1)概念:以_____________为标准,其他原子的质量与它相比较所得到的比。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)计算公式。
相对原子质量=_______________________。
(3)近似计算。
相对原子质量≈质子数+中子数。
4.离子:
(1)概念:带电的_________。
(2)分类:①阳离子:带______的原子(质子数_____核外电子数)
②阴离子:带____的原子(质子数_____核外电子数)
③离子符号表示的意义。
④原子和离子的相互转化关系:
考点三:元素与元素周期表
1.概念:_________数(即_____________)相同的一类_________的总称。
2.在地壳中的含量:居前四位的元素为____________________(由多到少的顺序)。
3.生物细胞中的含量:居前三位的元素为_____________(由多到少的顺序),最多的金属元素为
_______。
4.元素符号的意义:
(1)宏观:表示____________。
(2)微观:表示_______________________。
(3)若元素符号前面加上化学计量数,该符号只能表示_________________。
5.元素的分类:
元素分为_________元素、___________元素和稀有气体元素。
元素的化学性质由_________________决定。
元素的种类由_______________决定。
6.元素周期表:
(1)编排结构。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①每一横行:周期表中每一横行为一个_________,共有7个周期。
②每一纵列:每个纵列为一个_______(8、9、10三个纵列共同组成一个族),共有16个族。
③排列规律:同周期元素,原子的___________数相同;最外层电子数由1增加至8,由_________
元素过渡到__________元素,以稀有气体元素结尾;周期表中同一纵列的元素,原子的
_____________________相同,自上而下电子层数逐渐增多。
(2)每一格信息(以碳元素为例)。
二、基础达标
1.豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指( )
A.原子 B.分子 C.元素 D.单质
2.关于分子、原子的说法错误的是( )
A.分子和原子总在不断地运动 B.同种原子可能构成不同分子
C.分子的质量一定大于原子的质量 D.化学变化中分子可分、原子不可分
3.铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有 58个质子和82个中子,该原
子的核外电子数为( )
A.24 B.58 C.82 D.140
4.列对于宏观现象的微观解释中,错误的是 ( )
A.水通直流电分解,是因为水分子被破坏,形成新的分子
B.“酒香不怕巷子深”,是因为分子在不停地运动
C.10 mL水与10 mL酒精混合后体积小于20 mL,是因为水分子的体积减小
D.CO和CO2具有不同的化学性质,是因为构成它们的分子不同
5.下面是几种微粒结构示意图,请用相应微粒代号填空。
(1)属于金属元素原子的是______;
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)具有相对稳定结构的是________;
(3)属于同种元素的是_________;
(4)表示离子的是______。
6.元素周期表是学习科学的重要工具。下表是元素周期表的一部分,请回答下列问题:
(1)不同种元素之间最本质的区别是______不同。
A.相对原子质量 B.质子数 C.中子数
(2)第3号元素属于_________(选填“金属”或“非金属”)元素。
(3)第12号元素和第17号元素组成化合物的化学式是_________。
三、能力提升
7.下列化学符号中的数字表示的意义不正确的是( )
A.NO :“2”表示一个二氧化氮分子含有两个氧原子
2
B.2Na:“2”表示两个钠元素
C. :“+2”表示镁元素的化合价为+2价
D.2OH﹣:“2”表示两个氢氧根离子
8.苏州的“碧螺春”享誉全国。“碧螺春”茶叶中的单宁酸具有抑制血压上升、清热解毒、
抗癌等功效,其化学式为C H O .下列说法错误的是( )
76 52 46
A.单宁酸由碳、氢、氧三种元素组成
B.一个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成
C.单宁酸中碳、氧元素的质量比为57:23
D.单宁酸中氢元素的质量分数最小
9.下列符号中,既表示一个原子,又表示一种元素,还能表示一种物质的是( )
A.He B.N C.H D.2O
2 2
10.下列物质中含有氧分子的是( )
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.O B.H O C.H CO D.SO
2 2 2 2 3 2
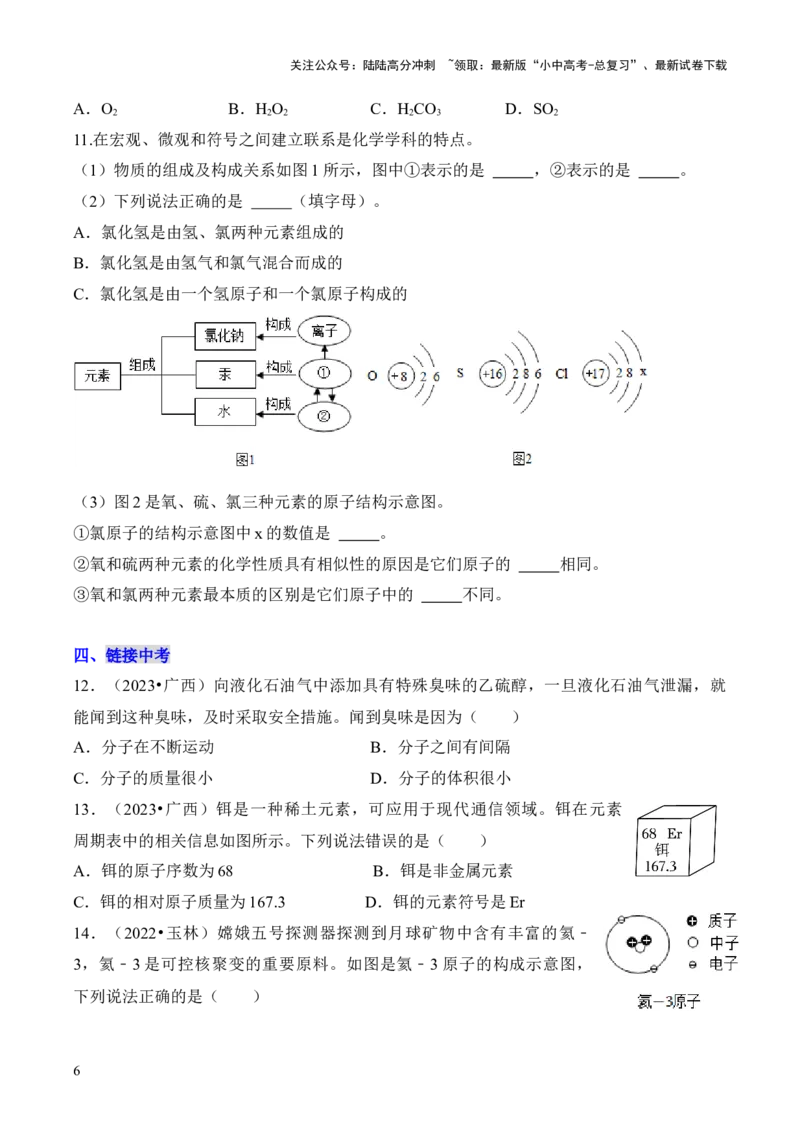
11.在宏观、微观和符号之间建立联系是化学学科的特点。
(1)物质的组成及构成关系如图1所示,图中①表示的是 ,②表示的是 。
(2)下列说法正确的是 (填字母)。
A.氯化氢是由氢、氯两种元素组成的
B.氯化氢是由氢气和氯气混合而成的
C.氯化氢是由一个氢原子和一个氯原子构成的
(3)图2是氧、硫、氯三种元素的原子结构示意图。
①氯原子的结构示意图中x的数值是 。
②氧和硫两种元素的化学性质具有相似性的原因是它们原子的 相同。
③氧和氯两种元素最本质的区别是它们原子中的 不同。
四、链接中考
12.(2023•广西)向液化石油气中添加具有特殊臭味的乙硫醇,一旦液化石油气泄漏,就
能闻到这种臭味,及时采取安全措施。闻到臭味是因为( )
A.分子在不断运动 B.分子之间有间隔
C.分子的质量很小 D.分子的体积很小
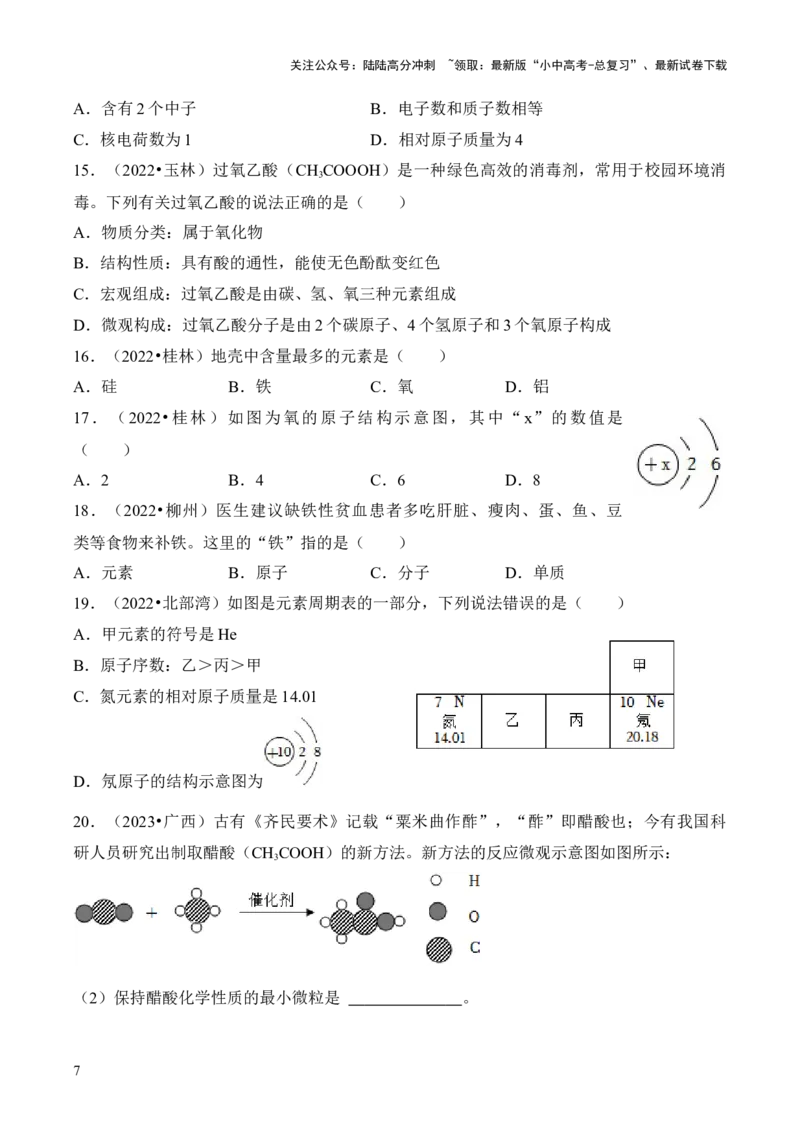
13.(2023•广西)铒是一种稀土元素,可应用于现代通信领域。铒在元素
周期表中的相关信息如图所示。下列说法错误的是( )
A.铒的原子序数为68 B.铒是非金属元素
C.铒的相对原子质量为167.3 D.铒的元素符号是Er
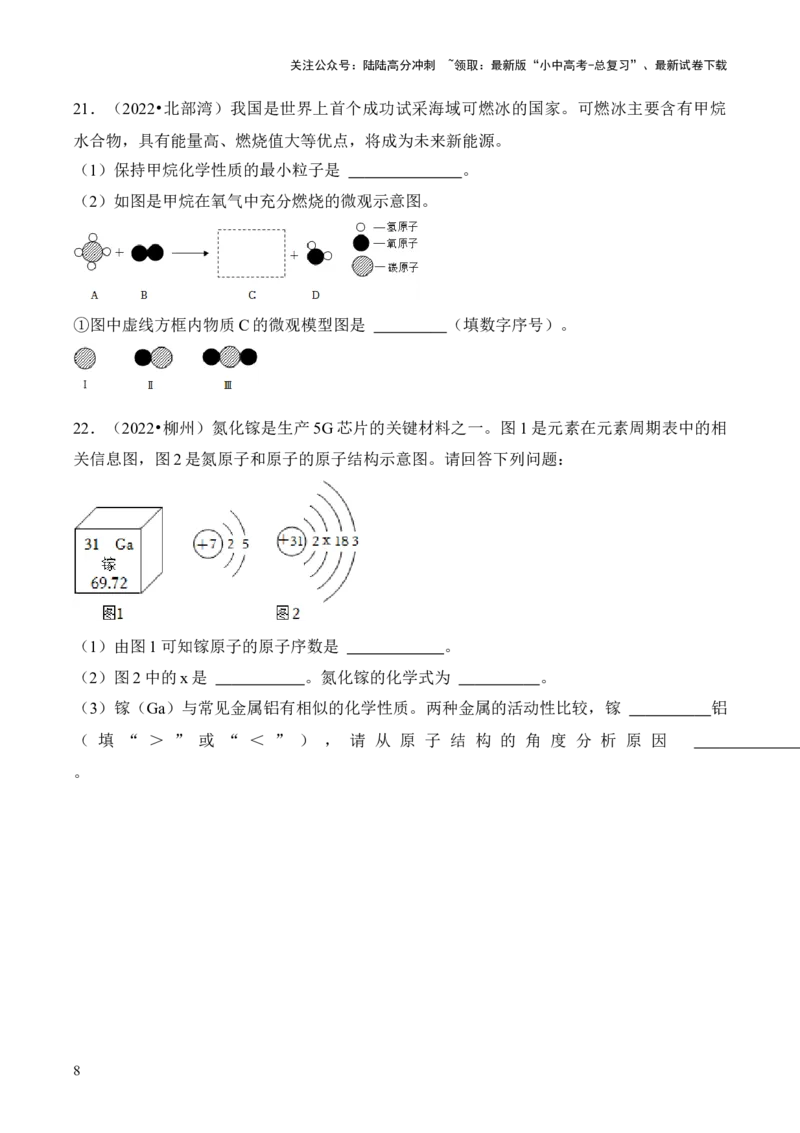
14.(2022•玉林)嫦娥五号探测器探测到月球矿物中含有丰富的氦﹣
3,氦﹣3是可控核聚变的重要原料。如图是氦﹣3原子的构成示意图,
下列说法正确的是( )
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.含有2个中子 B.电子数和质子数相等
C.核电荷数为1 D.相对原子质量为4
15.(2022•玉林)过氧乙酸(CH COOOH)是一种绿色高效的消毒剂,常用于校园环境消
3
毒。下列有关过氧乙酸的说法正确的是( )
A.物质分类:属于氧化物
B.结构性质:具有酸的通性,能使无色酚酞变红色
C.宏观组成:过氧乙酸是由碳、氢、氧三种元素组成
D.微观构成:过氧乙酸分子是由2个碳原子、4个氢原子和3个氧原子构成
16.(2022•桂林)地壳中含量最多的元素是( )
A.硅 B.铁 C.氧 D.铝
17.(2022•桂林)如图为氧的原子结构示意图,其中“x”的数值是
( )
A.2 B.4 C.6 D.8
18.(2022•柳州)医生建议缺铁性贫血患者多吃肝脏、瘦肉、蛋、鱼、豆
类等食物来补铁。这里的“铁”指的是( )
A.元素 B.原子 C.分子 D.单质
19.(2022•北部湾)如图是元素周期表的一部分,下列说法错误的是( )
A.甲元素的符号是He
B.原子序数:乙>丙>甲
C.氮元素的相对原子质量是14.01
D.氖原子的结构示意图为
20.(2023•广西)古有《齐民要术》记载“粟米曲作酢”,“酢”即醋酸也;今有我国科
研人员研究出制取醋酸(CH COOH)的新方法。新方法的反应微观示意图如图所示:
3
(2)保持醋酸化学性质的最小微粒是 。
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
21.(2022•北部湾)我国是世界上首个成功试采海域可燃冰的国家。可燃冰主要含有甲烷
水合物,具有能量高、燃烧值大等优点,将成为未来新能源。
(1)保持甲烷化学性质的最小粒子是 。
(2)如图是甲烷在氧气中充分燃烧的微观示意图。
①图中虚线方框内物质C的微观模型图是 (填数字序号)。
22.(2022•柳州)氮化镓是生产5G芯片的关键材料之一。图1是元素在元素周期表中的相
关信息图,图2是氮原子和原子的原子结构示意图。请回答下列问题:
(1)由图1可知镓原子的原子序数是 。
(2)图2中的x是 。氮化镓的化学式为 。
(3)镓(Ga)与常见金属铝有相似的化学性质。两种金属的活动性比较,镓 铝
( 填 “ > ” 或 “ < ” ) , 请 从 原 子 结 构 的 角 度 分 析 原 因
。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
参考答案
一、基础回顾
考点一:
(一)分子和原子
1.(1)化学性质。 (2)①很小②运动;运动越快 ③间隔;间隔越大;间隔越小
(4)没有发生变化;分子种类会
2.(1)化学变化 (2)都很小;不停运动;存在间隔
3.(2)在化学变化中,分子可以再分,而原子不可再分
4.原子; 原子 ;新的分子
考点二:原子的结构
(一)原子的构成:
1.原子核;质子;正;中子;电子;负
2.(1)中心 ;质量 (2)核电荷; 质子;核外电子;原子序;相等;相反;不显
(3) 质子数决定原子的种类 ,质子数相同的一类原子属于同种元素;
(4)最外层电子数决定元素的化学性质,最外层电子数相同,元素的化学性质相似
(二)原子核外电子的排布:
2.
元素分类 原子最外层 结构的 化学性质
电子数 稳定性
金属元素 通常不超过 不稳定 易失去最外层电子
___4___个
非金属元素 通常多于__4__个 不稳定 易得到电子
稀有气体元素 8 个(He 稳定 不易得失电子
为___2___个)
3. (1)一种碳原子质量的1/12
(2)
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
4.(1)原子(2)①正电;大于②负电;小于
考点三:元素与元素周期表
1. 质子;核电荷数;原子
2. 氧、硅、铝、铁
3.氧、碳、氢;钙
4.(1)一种元素 (2)这种元素的一个原子(3)该原子的个数5.元素的分类:
金属;非金属。最外层电子数。 核内质子数。
6.(1)①周期 ②族③电子层金属;非金属;最外层上的电子数
二、基础达标
1.C 2.C 3.B 4.C 5.(1)①; (2)④⑤; (3)③⑤; (4)⑤。 6.(1)B (2)金属 (3)MgCl
2
三、能力提升
7.B 8.C 9.A 10.A 11.(1)①原子;②分子;(2)A;(3)①7;②最外层电子数;
③质子数。
四、链接中考
12.A 13.B 14.B 15.C 16.C 17.D 18.A 19.B
20.(2)醋酸分子 21.(1)甲烷分子(2)① Ⅲ 22.(1) 31 (2) 8 ;
GaN
(3) > ; 铝原子的核外有3个电子层,镓原子有4个电子层,且铝原子与镓原子的最
外层电子数相同,因此镓原子的原子核对最外层电子的吸引能力较弱,更容易失去最外层的
三个电子 。
10