文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点提分训练(十七)中和反应
一、选择题
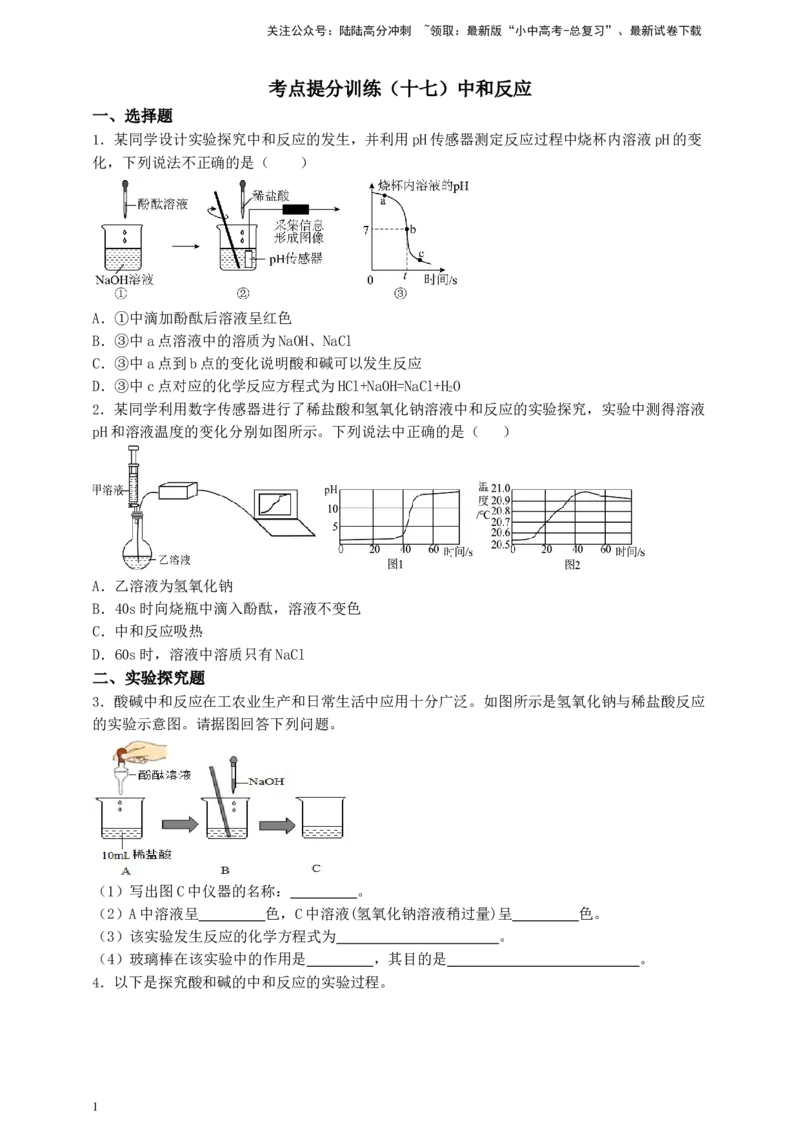
1.某同学设计实验探究中和反应的发生,并利用pH传感器测定反应过程中烧杯内溶液pH的变
化,下列说法不正确的是( )
A.①中滴加酚酞后溶液呈红色
B.③中a点溶液中的溶质为NaOH、NaCl
C.③中a点到b点的变化说明酸和碱可以发生反应
D.③中c点对应的化学反应方程式为HCl+NaOH=NaCl+HO
2
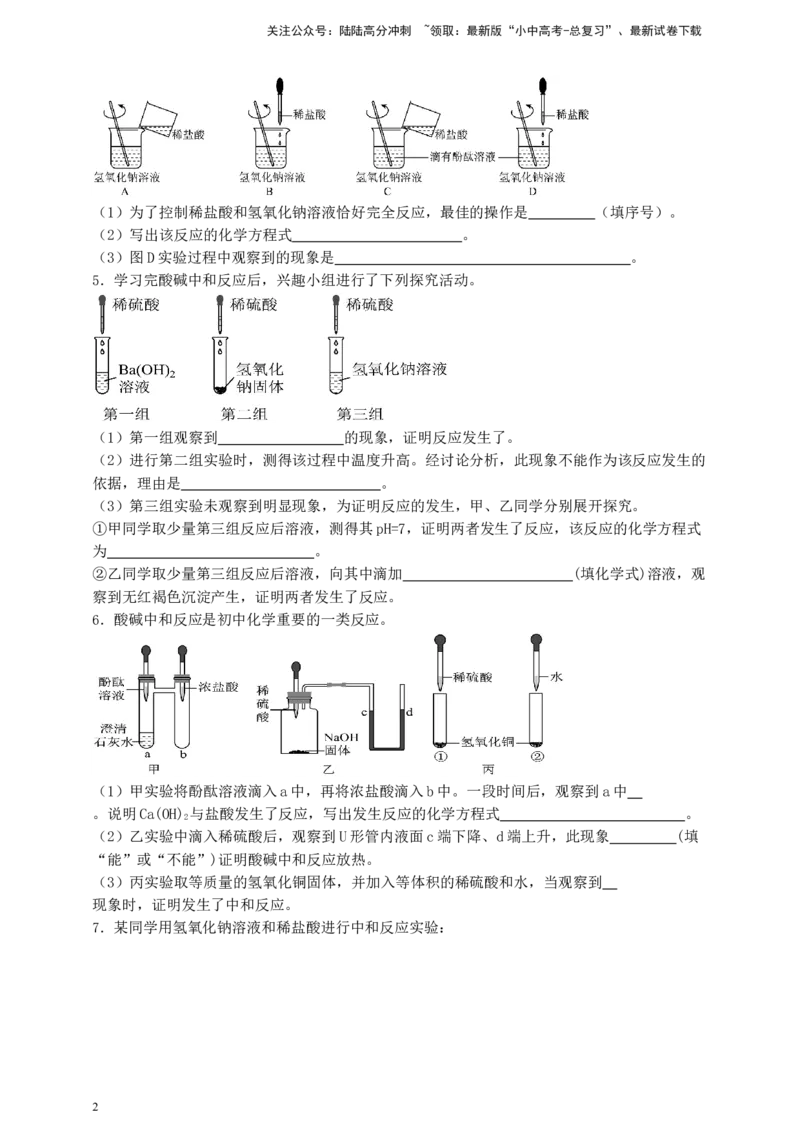
2.某同学利用数字传感器进行了稀盐酸和氢氧化钠溶液中和反应的实验探究,实验中测得溶液
pH和溶液温度的变化分别如图所示。下列说法中正确的是( )
A.乙溶液为氢氧化钠
B.40s时向烧瓶中滴入酚酞,溶液不变色
C.中和反应吸热
D.60s时,溶液中溶质只有NaCl
二、实验探究题
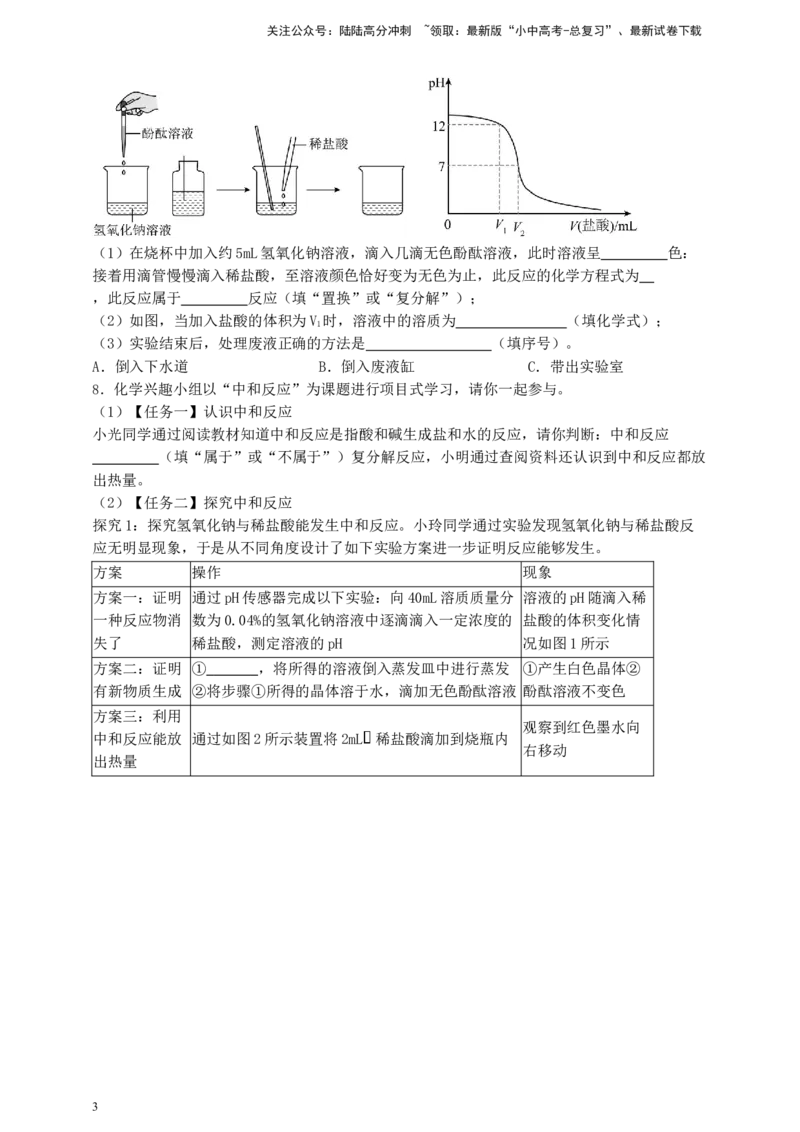
3.酸碱中和反应在工农业生产和日常生活中应用十分广泛。如图所示是氢氧化钠与稀盐酸反应
的实验示意图。请据图回答下列问题。
(1)写出图C中仪器的名称: 。
(2)A中溶液呈 色,C中溶液(氢氧化钠溶液稍过量)呈 色。
(3)该实验发生反应的化学方程式为 。
(4)玻璃棒在该实验中的作用是 ,其目的是 。
4.以下是探究酸和碱的中和反应的实验过程。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)为了控制稀盐酸和氢氧化钠溶液恰好完全反应,最佳的操作是 (填序号)。
(2)写出该反应的化学方程式 。
(3)图D实验过程中观察到的现象是 。
5.学习完酸碱中和反应后,兴趣小组进行了下列探究活动。
(1)第一组观察到 的现象,证明反应发生了。
(2)进行第二组实验时,测得该过程中温度升高。经讨论分析,此现象不能作为该反应发生的
依据,理由是 。
(3)第三组实验未观察到明显现象,为证明反应的发生,甲、乙同学分别展开探究。
①甲同学取少量第三组反应后溶液,测得其pH=7,证明两者发生了反应,该反应的化学方程式
为 。
②乙同学取少量第三组反应后溶液,向其中滴加 (填化学式)溶液,观
察到无红褐色沉淀产生,证明两者发生了反应。
6.酸碱中和反应是初中化学重要的一类反应。
(1)甲实验将酚酞溶液滴入a中,再将浓盐酸滴入b中。一段时间后,观察到a中
。说明Ca(OH) 与盐酸发生了反应,写出发生反应的化学方程式 。
2
(2)乙实验中滴入稀硫酸后,观察到U形管内液面c端下降、d端上升,此现象 (填
“能”或“不能”)证明酸碱中和反应放热。
(3)丙实验取等质量的氢氧化铜固体,并加入等体积的稀硫酸和水,当观察到
现象时,证明发生了中和反应。
7.某同学用氢氧化钠溶液和稀盐酸进行中和反应实验:
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈 色:
接着用滴管慢慢滴入稀盐酸,至溶液颜色恰好变为无色为止,此反应的化学方程式为
,此反应属于 反应(填“置换”或“复分解”);
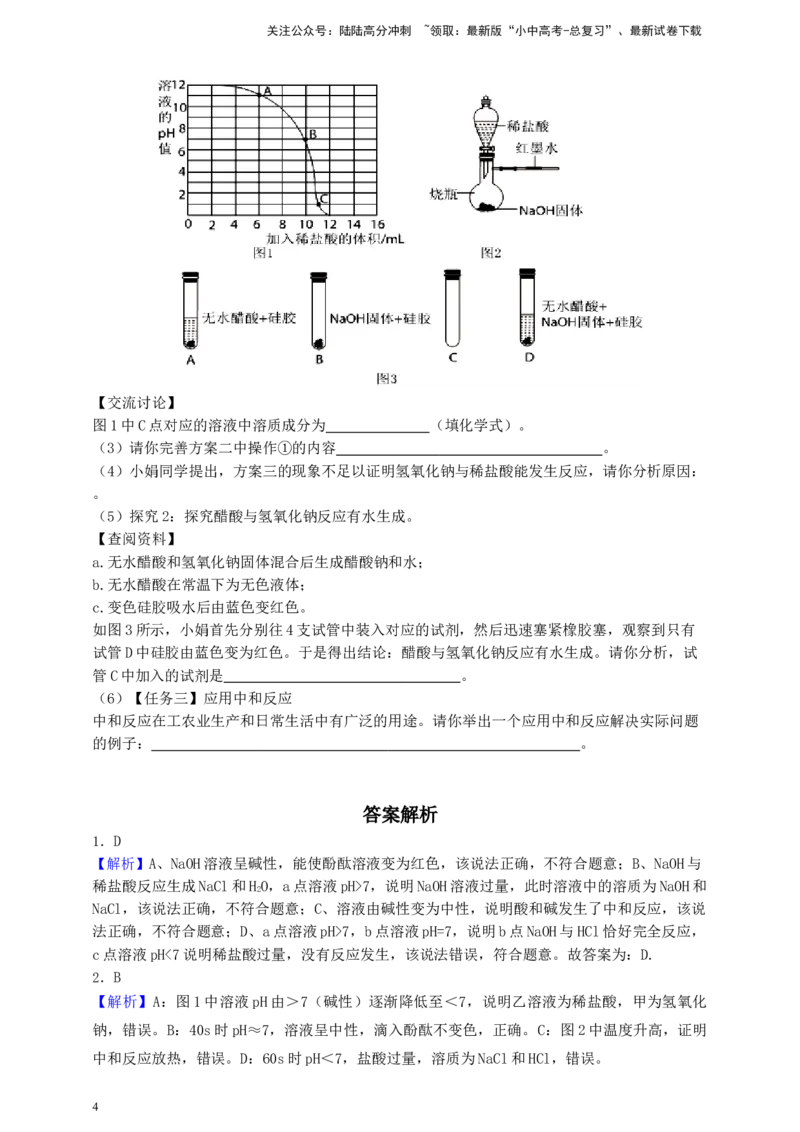
(2)如图,当加入盐酸的体积为V 时,溶液中的溶质为 (填化学式);
1
(3)实验结束后,处理废液正确的方法是 (填序号)。
A.倒入下水道 B.倒入废液缸 C.带出实验室
8.化学兴趣小组以“中和反应”为课题进行项目式学习,请你一起参与。
(1)【任务一】认识中和反应
小光同学通过阅读教材知道中和反应是指酸和碱生成盐和水的反应,请你判断:中和反应
(填“属于”或“不属于”)复分解反应,小明通过查阅资料还认识到中和反应都放
出热量。
(2)【任务二】探究中和反应
探究1:探究氢氧化钠与稀盐酸能发生中和反应。小玲同学通过实验发现氢氧化钠与稀盐酸反
应无明显现象,于是从不同角度设计了如下实验方案进一步证明反应能够发生。
方案 操作 现象
方案一:证明 通过pH传感器完成以下实验:向40mL溶质质量分 溶液的pH随滴入稀
一种反应物消 数为0.04%的氢氧化钠溶液中逐滴滴入一定浓度的 盐酸的体积变化情
失了 稀盐酸,测定溶液的pH 况如图1所示
方案二:证明 ① ,将所得的溶液倒入蒸发皿中进行蒸发 ①产生白色晶体②
有新物质生成 ②将步骤①所得的晶体溶于水,滴加无色酚酞溶液 酚酞溶液不变色
方案三:利用
观察到红色墨水向
中和反应能放 通过如图2所示装置将2mL 稀盐酸滴加到烧瓶内
右移动
出热量
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【交流讨论】
图1中C点对应的溶液中溶质成分为 (填化学式)。
(3)请你完善方案二中操作①的内容 。
(4)小娟同学提出,方案三的现象不足以证明氢氧化钠与稀盐酸能发生反应,请你分析原因:
。
(5)探究2:探究醋酸与氢氧化钠反应有水生成。
【查阅资料】
a.无水醋酸和氢氧化钠固体混合后生成醋酸钠和水;
b.无水醋酸在常温下为无色液体;
c.变色硅胶吸水后由蓝色变红色。
如图3所示,小娟首先分别往4支试管中装入对应的试剂,然后迅速塞紧橡胶塞,观察到只有
试管D中硅胶由蓝色变为红色。于是得出结论:醋酸与氢氧化钠反应有水生成。请你分析,试
管C中加入的试剂是 。
(6)【任务三】应用中和反应
中和反应在工农业生产和日常生活中有广泛的用途。请你举出一个应用中和反应解决实际问题
的例子: 。
答案解析
1.D
【解析】A、NaOH溶液呈碱性,能使酚酞溶液变为红色,该说法正确,不符合题意;B、NaOH与
稀盐酸反应生成NaCl和HO,a点溶液pH>7,说明NaOH溶液过量,此时溶液中的溶质为NaOH和
2
NaCl,该说法正确,不符合题意;C、溶液由碱性变为中性,说明酸和碱发生了中和反应,该说
法正确,不符合题意;D、a点溶液pH>7,b点溶液pH=7,说明b点NaOH与HCl恰好完全反应,
c点溶液pH<7说明稀盐酸过量,没有反应发生,该说法错误,符合题意。故答案为:D.
2.B
【解析】A:图1中溶液pH由>7(碱性)逐渐降低至<7,说明乙溶液为稀盐酸,甲为氢氧化
钠,错误。B:40s时pH≈7,溶液呈中性,滴入酚酞不变色,正确。C:图2中温度升高,证明
中和反应放热,错误。D:60s时pH<7,盐酸过量,溶质为NaCl和HCl,错误。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3.(1)烧杯
(2)无;红
(3)NaOH+HCl=NaCl+HO
2
(4)搅拌;使盐酸与氢氧化钠充分反应
【解析】(1)图中仪器a的名称是烧杯;(2)根据稀盐酸中加入酚酞溶液是无色的,加入氢
氧化钠,当稀盐酸被消耗完,溶液是碱性的,溶液变为红色;(3)根据氢氧化钠和稀盐酸反应
生成氯化钠和水,化学方程式为 NaOH+HCl=NaCl+HO ;(4)氢氧化钠和稀盐酸反应过程中,
2
利用玻璃棒搅拌,目的是 使盐酸与氢氧化钠充分反应 ;
4.(1)D
(2)NaOH+HCl=NaCl+HO
2
(3)加了酚酞后溶液先变红,继续滴加稀盐酸后,红色逐渐褪去,最终溶液变为无色
5.(1)产生白色沉淀
(2)氢氧化钠固体溶于水放热
(3)H SO +2NaOH=Na SO +2H O
2 4 2 4 2
;FeCl 或Fe(NO) 或Fe(SO)
3 3 3 2 4 3
6.(1)溶液由红色变无色;2HCl+Ca(OH) =CaCl +2H O
2 2 2
(2)不能
(3)试管①中固体溶解,溶液变蓝色,试管②中固体不溶解
7.(1)红;NaOH+HCl=NaCl+HO;复分解
2
(2)NaCl、NaOH
(3)B
8.(1)属于
(2)NaCl和HCl
(3)取少量氢氧化钠溶液加入足量稀盐酸,振荡
(4)氢氧化钠溶于水放热也会使瓶内的压强增大,红色墨水向右移动;稀盐酸加入烧瓶中,瓶
内气体被压缩,压强增大,红色墨水也会向右移动(合理即可)
(5)醋酸钠和硅胶
(6)服用氢氧化铝治疗胃酸过多(或用熟石灰改良酸性土壤)(合理即可)
【解析】(1)两种化合物相互交换成分生成另外两种化合物的反应是复分解反应,中和反应是
酸与碱反应生成盐和水的反应属于复分解反应;(2)方案一向40mL溶质质量分数为0.04%的氢
氧化钠溶液中逐滴滴入一定浓度的稀盐酸,氢氧化钠和稀盐酸反应生成氯化钠和水,图1中C
点溶液的pH小于7,显酸性,说明此时盐酸过量,则对应溶液中的溶质成分为氯化钠和氯化
氢;(3)方案二证明有新物质生成,根据实验现象①产生白色晶体,②白色晶体溶于水,滴加
无色酚酞溶液,酚酞溶液不变色,根据无色酚酞溶液与酸性或中性溶液不变色,碱性溶液变
红,则步骤①为取少量氢氧化钠溶液,加入足量稀盐酸,振荡,将所得溶液倒入蒸发皿中进行
蒸发,②将步骤①所得晶体溶于水滴加无色酚酞溶液;(4)由于氢氧化钠溶于水放热,也会使
瓶内的压强增大,红墨水向右移动,稀盐酸加入烧瓶中占据部分体积,瓶内气体被压缩,压强
增大,红墨水也会向右移动,所以方案三的现象不足以证明氢氧化钠与盐酸能发生反应;(5)
分别向4支试管中加入对应的试剂,然后迅速塞紧橡胶塞,观察到只有试管D中硅胶由蓝色变
为红色,于是得出结论,醋酸与氢氧化钠反应有水生成,无水醋酸和氢氧化钠固体混合后生成
醋酸钠和水,A试管为无色醋酸和硅胶不变色,B试管为氢氧化钠固体和硅胶,不变色,D试管
为无色醋酸,氢氧化钠固体和硅胶,变色,则C试管中应该是醋酸钠和硅胶,A、B、C中固体不
变色说明无水醋酸,氢氧化钠固体,醋酸钠固体中不含水,D中固体由蓝色变红色,说明无水
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
醋酸和氢氧化钠固体反应生成了水,可以得出的结论是醋酸与氢氧化钠反应有水生成;(6)中
和反应是指酸和碱反应生成盐和水的反应,日常生活中服用氢氧化铝治疗胃酸过多或者用熟石
灰改良酸性土壤等,均是中和反应的实际应用。
6