文档内容
单元检测一 物质的组成、性质和分类 离子反应
一、选择题(本题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.下列说法正确的是( )
A.气溶胶是一种以气体为分散剂的分散系,分散质粒子直径大多在纳米级别
B.长征五号B运载火箭首飞成功,“胖五”的助推剂为液氧和煤油,二者均为纯净物
C.ECMO人工肺利用了半透膜的原理,血浆与氧气均不能通过半透膜
D.“雨过天晴云破处,这般颜色做将来”描述的是汝窑的典型特征,其颜色来自于氧化
铁
2.分类法是学习和研究化学的一种常用的科学方法。下列分类合理的是( )
①Fe O、CaO、NaO 都是碱性氧化物
2 3 2 2
②NaCO 是正盐,NaHCO 是酸式盐
2 3 3
③HSO 与KHSO 均含相同的元素氢,故KHSO 也可以称为酸
2 4 4 4
④洁净的空气、纯净的盐酸都是混合物
⑤根据分散系能否产生丁达尔效应将分散系分为胶体、溶液和浊液
A.只有①③⑤ B.只有②④
C.只有①②④ D.只有②③⑤
3.新冠肺炎传播途径主要为直接传播、接触传播和气溶胶传播。气溶胶传播是指飞沫混合
在空气中,形成气溶胶,吸入后导致感染,而气溶胶是胶体的一种。胶体区别于其他分散
系的本质特征是( )
A.胶体是稳定的分散系
B.胶体是纯净物,其他分散系是混合物
C.能产生丁达尔效应
D.分散质粒子直径在10-9~10-7 m之间
4.朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,
高处丛生的灌木,落下参差的斑驳的黑影。”结合这段文字及所学的化学知识判断下列说
法不正确的是( )
A.荷塘上方的薄雾是气溶胶
B.月光通过薄雾时产生了丁达尔效应
C.薄雾是一种较稳定的分散系
D.“大漠孤烟直”中“孤烟”的组成成分和这种薄雾的组分相同
5.下列表格中各项分类都正确的一组是( )
类别
纯净物 混合物 电解质 非电解质
选项
A 生理盐水 明矾 液态KNO 蔗糖
3B CaO 海水 铜 乙醇
C 胆矾 铝合金 AgCl CO
2
D 氢氧化钠 空气 NaSO 溶液 食醋
2 4
6.下列指定反应的离子方程式正确的是( )
A.向漂白液中滴入过量醋酸:ClO-+H+===HClO
B.铝与烧碱溶液反应产生氢气:Al+2OH-===AlO+H↑
2
C.向澄清石灰水中滴加少量碳酸氢钠溶液:Ca2++OH-+HCO===CaCO ↓+HO
3 2
D.向明矾溶液中加入Ba(OH) 使Al3+刚好沉淀完全:Al3++3OH-===Al(OH) ↓
2 3
7.某溶液中含有Ba2+、Cu2+、Ag+。学习小组的同学现用NaOH溶液、盐酸和NaSO 溶
2 4
液将这三种离子逐一沉淀分离,实验流程如图所示。下列说法正确的是( )
A.试剂A为NaSO 溶液
2 4
B.沉淀3的化学式可能是BaSO
4
C.生成沉淀1的离子方程式为Cu2++2OH-===Cu(OH) ↓
2
D.生成沉淀2的离子方程式为Ag++Cl-===AgCl↓
8.下列各组离子一定能大量共存的是( )
A.在无色溶液中:NH、Fe2+、SO、CO
B.在含大量Ba2+的溶液中:NH、Na+、Cl-、OH-
C.在强碱性溶液中:Na+、K+、SO、HCO
D.在强酸性溶液中:K+、Fe2+、Cl-、SO
9.某研究性学习小组做了一个如图所示的实验,在导管口点燃氢气后,发现烧杯中酸性
KMnO 溶液褪色,若将烧杯中的溶液换成含有少量KSCN的FeCl 溶液,溶液显红色。下
4 2
列判断正确的是( )
A.该条件下H 燃烧放出的热量使冰分解产生了O
2 2
B.该条件下H 被冷却为液态氢,液氢的水溶液具有还原性
2C.该条件下H 燃烧的产物中可能含有一定量的HO
2 2 2
D.该条件下生成的水分子的化学性质比较活泼
10.Pd/Al O 催化H 还原CO 的机理示意图如下。下列说法不正确的是( )
2 3 2 2
A.H—H的断裂需要吸收能量
B.①→②,CO 发生加成反应
2
C.④中,CO被氧化为CH
4
D.生成CH 的总反应方程式是CO+4H=======CH+2HO
4 2 2 4 2
11.某工业废气中的SO 经如图中的两个循环可分别得到S和HSO 。下列说法正确的是(
2 2 4
)
A.循环Ⅰ中,反应1中的氧化产物为ZnFeO
3.5
B.循环Ⅰ中,反应2中的还原产物为ZnFeO
4
C.Mn可作为循环Ⅱ中电解过程中的阳极材料
D.循环Ⅰ和循环Ⅱ中消耗同质量的SO ,理论上得到S和HSO 的质量之比为16∶49
2 2 4
12.(2022·浙江模拟)下列“类比”合理的是( )
A.由O +2HS===S+2HO,说明非金属性:O>S,推测:2C+SiO=====Si+2CO,非
2 2 2 2
金属性:C>Si
B . 由 CO + Ca(ClO) + HO===CaCO ↓ + 2HClO , 推 测 : SO + Ca(ClO) +
2 2 2 3 2 2
HO===CaSO↓+2HClO
2 3
C.Fe与S在加热条件下反应生成FeS,推测:Cu与S在加热条件下生成CuS
D.由NaSO +2HCl===2NaCl+HO+SO ↑,推测:NaSO +HSO ===NaSO +HO+
2 3 2 2 2 3 2 4 2 4 2
SO ↑
2
13.已知电离平衡常数:HCO>HClO>HCO,氧化性:HClO>Cl >Br >Fe3+>I 。下列有关
2 3 2 2 2
离子反应或离子方程式的叙述正确的是( )
A.常温下,中性溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存B.向含有0.4 mol FeI 的溶液中通入0.3 mol Cl 充分反应:4Fe2++2I-+3Cl===4Fe3++
2 2 2
6Cl-+I
2
C.向NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO+HO===HClO+HCO
2 2
D.向FeBr 溶液中滴加少量氯水,再加入CCl 溶液振荡,静置,有机层呈橙色
2 4
14.根据下列实验操作和现象所得到的实验结论正确的是( )
选项 实验操作和现象 实验结论
向某溶液中加入氯化钡溶液有白色沉
A 原溶液中一定有SO
淀产生,再加盐酸,沉淀不消失
向某溶液中加入碳酸钠溶液产生白色
B 原溶液中一定有Ba2+
沉淀,再加盐酸,沉淀消失
向某溶液中加入氢氧化钠溶液,将湿
C 润红色石蕊试纸置于试管口,试纸不 原溶液中一定无NH
变蓝
向某黄色溶液中加入淀粉-KI溶液,
D 溶液中可能含Br
2
溶液呈蓝色
15.通过卤素间的反应实验,可以比较出卤素单质氧化性的强弱。实验如下:
下列说法不正确的是( )
A.CCl 起到萃取、富集I 的作用
4 2
B.Ⅰ中发生反应的离子方程式为Br +2I-===I+2Br-
2 2
C.依据a、b中的现象,可以证明Cl 的氧化性比Br 强
2 2
D.b中下层变无色,说明I 转化为I-
2
二、非选择题(本题包括5小题,共55分)
16.(10分)物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、
提高学习效率、解决问题都有着重要的意义。
请回答下列问题:
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观。
①图中所示所属的分类方法为______________________________________________。②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两
种物质归为一类的是________(填字母)。
A.具有还原性 B.属于氧化物
C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如
下部分药品,实验室新购进一些晶体碘,应该将它存放在________________________(填字
母)。
药品柜 甲柜 乙柜 丙柜 丁柜
活性炭、红 锌粒、铜
药品 乙醇、乙酸 氯化钠、氯化钾
磷 片
A.甲柜 B.乙柜
C.丙柜 D.丁柜
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、碳酸钠)”能发生反应。将一定量的稀
硫酸逐滴滴入氢氧化钠和碳酸钠的混合溶液中,边滴加边搅拌,直至有少量气泡产生,此
过程中共发生的离子反应有________个。
(2)含铁元素的物质有很多,在生产、生活中应用广泛。取少量某油漆的原料Fe O(红棕色
2 3
粉末),加入适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入
NaOH 溶 液 , 可 观 察 到 有 沉 淀 生 成 , 生 成 沉 淀 的 离 子 方 程 式 为
_________________________________,
另在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入2 mL上述棕黄色溶液,
继续加热至液体呈______色,停止加热,证明所得分散系类型的实验方法的名称是
___________。
17.(12分)请回答鉴定(认定)某白色固体样品(可能为NH HCO 、NaHCO 、NaCO 和NaCl
4 3 3 2 3
中的一种)的下列问题。
(1)甲同学经分析后,认为以Ba(OH) 试液滴加到样品溶液中(必要时可加热),通过产生的
2
现象即可完成实验。你认为该同学实验方案的设计______________(填“可行”或“不可
行”)。
(2)乙同学选用了试管、玻璃棒、酒精灯、试管夹;蒸馏水、pH试纸,通过合理、全面的
实验步骤,给出了鉴定(认定)。
①为保证实验方案的顺利实施,乙同学在给固体样品加热时,正确的操作方法是
____________
________________________________________(使用酒精灯和试管夹的方法不必叙述)。
②乙在实验中可能要两次使用玻璃棒和pH试纸。第一次是将一小块试纸用蒸馏水润湿后
粘在玻璃棒的一端,以便通过玻璃棒将试纸对准加热的试管附近;第二次(测试溶液的pH)
的正确方法是__________________________________。
③完成下表中空格部分的填写。固体试样 判断依据(要点) 有关化学方程式(或离子方程式)
碳酸氢铵 NH HCO =====NH ↑+CO↑+HO
4 3 3 2 2
pH试纸显示有酸 2NaHCO =====NaCO+CO↑+HO
3 2 3 2 2
碳酸氢钠
性气体产生 CO+HOHCO
2 2 2 3
碳酸钠
氯化钠 NaCl===Na++Cl-
18.(11分)十九大报告提出“要像对待生命一样对待生态环境”,对硫、氮元素形成的有
毒、有害物质进行处理成为科学研究热点。
(1)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是
____________(填字母)。
a.碳氧化物 b.硫氧化物
c.氮氧化物
(2)H S是严重危害环境的气体,可采取多种方法减少HS的排放并加以资源利用。
2 2
① 用 Fe (SO ) 吸 收 HS , 发 生 反 应 的 离 子 方 程 式 为
2 4 3 2
____________________________________。
②HS与CO 在高温下反应可生成氧硫化碳(COS),氧硫化碳分子中所有原子均满足最外层
2 2
8电子稳定结构,其结构式为________________________。
(3)ClO 氧化吸收法可用于处理氮氧化物。ClO 可将NO氧化为NO ,并进一步将NO 氧化
2 2 2 2
为HNO,ClO 则被还原为Cl-。吸收时,ClO 溶液从吸收器顶部喷淋,氮氧化物从吸收器
3 2 2
底部通入(如图1所示),氮氧化物去除率与吸收器内碎瓷片填料的高度关系如图2所示。
①NO 和ClO 反应的离子方程式为________________________________________________。
2 2
② 随 着 吸 收 器 内 填 料 高 度 增 加 , NO 去 除 率 升 高 的 原 因 是
x
______________________________。
(4)用碱液吸收氮氧化物(NO):NO+NO +2NaOH===2NaNO +HO、2NO +
x 2 2 2 2
2NaOH===NaNO +NaNO +HO。根据上述原理判断,将下列气体通入过量NaOH溶液中,
2 3 2
反应结束后一定有剩余的是________(填字母)。
A.1 mol O 和4 mol NO
2 2
B.1 mol NO和4 mol NO
2
C.1 mol O 和7 mol NO
2D.6 mol NO和4 mol NO
2
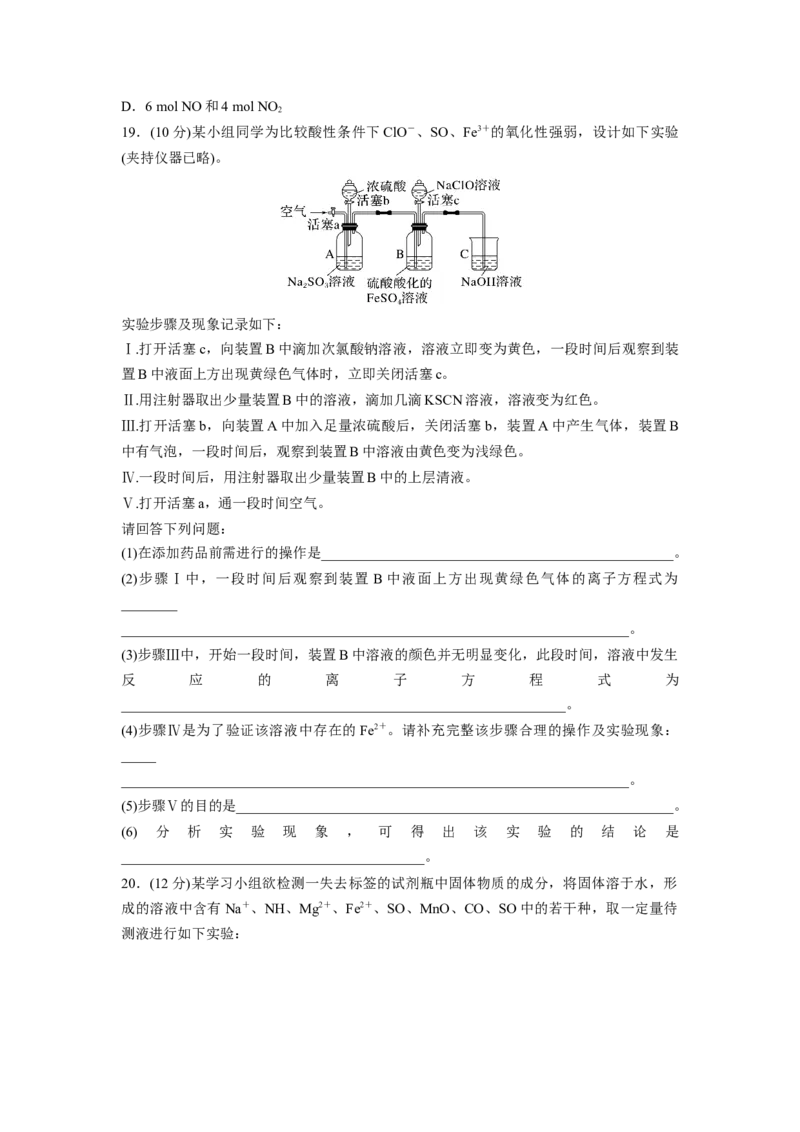
19.(10分)某小组同学为比较酸性条件下ClO-、SO、Fe3+的氧化性强弱,设计如下实验
(夹持仪器已略)。
实验步骤及现象记录如下:
Ⅰ.打开活塞c,向装置B中滴加次氯酸钠溶液,溶液立即变为黄色,一段时间后观察到装
置B中液面上方出现黄绿色气体时,立即关闭活塞c。
Ⅱ.用注射器取出少量装置B中的溶液,滴加几滴KSCN溶液,溶液变为红色。
Ⅲ.打开活塞b,向装置A中加入足量浓硫酸后,关闭活塞b,装置A中产生气体,装置B
中有气泡,一段时间后,观察到装置B中溶液由黄色变为浅绿色。
Ⅳ.一段时间后,用注射器取出少量装置B中的上层清液。
Ⅴ.打开活塞a,通一段时间空气。
请回答下列问题:
(1)在添加药品前需进行的操作是__________________________________________________。
(2)步骤Ⅰ中,一段时间后观察到装置 B 中液面上方出现黄绿色气体的离子方程式为
________
________________________________________________________________________。
(3)步骤Ⅲ中,开始一段时间,装置B中溶液的颜色并无明显变化,此段时间,溶液中发生
反 应 的 离 子 方 程 式 为
_______________________________________________________________。
(4)步骤Ⅳ是为了验证该溶液中存在的Fe2+。请补充完整该步骤合理的操作及实验现象:
_____
________________________________________________________________________。
(5)步骤Ⅴ的目的是______________________________________________________________。
(6) 分 析 实 验 现 象 , 可 得 出 该 实 验 的 结 论 是
___________________________________________。
20.(12分)某学习小组欲检测一失去标签的试剂瓶中固体物质的成分,将固体溶于水,形
成的溶液中含有Na+、NH、Mg2+、Fe2+、SO、MnO、CO、SO中的若干种,取一定量待
测液进行如下实验:回答下列问题:
(1)该待测液中一定含有的离子是______________;无法确定是否含有的离子是
__________________。
(2)沉淀B的成分及物质的量为_______________________________________(物质写化学式)。
(3)生成无色气体X时的离子方程式为______________________________________________。
(4)生成沉淀C时的离子方程式为__________________________________________________。
(5)在催化剂、加热条件下气体X与气体Y可以反应转化为对环境无害的物质,该反应的化
学方程式为_____________________________________________________________________,
所得氧化产物与还原产物的质量之比为__________________。
单元检测一 物质的组成、性质和分类 离子反应答案解
析
1.答案 A
解析 分散质粒子直径在1~100 nm之间的分散系是胶体,气溶胶是一种以气体为分散剂
的分散系,分散质粒子直径大多在纳米级别,故 A正确;煤油是混合物,故 B错误;
ECMO人工肺利用了半透膜的原理,血浆是胶体,不能通过半透膜,但氧气不是胶体,能
透过半透膜,故C错误;“雨过天晴云破处,这般颜色做将来”描述的是汝窑的典型特征,
其颜色是青色的,而氧化铁是红色的,故D错误。
2.答案 B
解析 NaO 与水反应产生NaOH和O ,属于过氧化物,不属于碱性氧化物,①错误;
2 2 2
KHSO 电离产生K+、H+和SO,阳离子不完全是H+,因此不能称为酸,③错误;洁净的
4
空气(含有氧气、氮气等)、纯净的盐酸(溶质为氯化氢)都是混合物,④正确;根据分散质粒
子直径的大小,将分散系分为胶体、溶液和浊液,⑤错误,故B正确。
3.答案 D
解析 胶体区别于其他分散系的本质特征是胶体粒子的直径在 1~100 nm(10-9~10-7 m)之
间,溶液的分散质粒子直径小于1 nm,浊液的分散质粒子直径大于100 nm。
4.答案 D
解析 薄雾是空气中的小液滴,是一种胶体,微粒直径在1~100 nm之间,A正确;薄雾是胶体,具有丁达尔效应,B正确;薄雾的微粒直径在1~100 nm之间,是一种较稳定的
分散系,C正确;“大漠孤烟直中”的“孤烟”是固体小颗粒,薄雾是液态小液滴,二者
组分不同,D错误。
5.答案 C
解析 A项,生理盐水是氯化钠的水溶液,为混合物,明矾是结晶水合物,为纯净物,液
态硝酸钾电离能导电,属于电解质,蔗糖不能电离,为非电解质,错误;B项,铜为金属
单质,既不是电解质也不是非电解质,错误;D项,氢氧化钠为纯净物,空气由不同物质
组成,为混合物,硫酸钠溶液和食醋均为混合物,不是电解质也不是非电解质,错误。
6.答案 C
解析 醋酸是弱酸,离子方程式中要用化学式表示:ClO-+CHCOOH===HClO+CHCOO
3 3
-,故A项错误;电荷不守恒,故B项错误;没有考虑同时生成硫酸钡沉淀,故D项错误。
7.答案 B
解析 Cu2+、Ag+均与NaOH溶液反应生成沉淀,Ba2+、Ag+均与NaSO 溶液反应生成沉
2 4
淀,只有Ag+与Cl-反应生成沉淀,则这三种离子逐一沉淀分离时,A为盐酸,沉淀1为
AgCl,B为NaOH或NaSO ,C为NaSO 或NaOH。由上述分析可知,A是盐酸,故A错
2 4 2 4
误;若B为NaOH,C为NaSO ,沉淀3是BaSO ,故B正确;生成沉淀1的离子方程式
2 4 4
为 Ag++Cl-===AgCl↓,故 C 错误;生成沉淀 2 的离子方程式为 Cu2++2OH-
===Cu(OH) ↓或Ba2++SO===BaSO↓,故D错误。
2 4
8.答案 D
解析 Fe2+为有色离子,且Fe2+、CO之间发生反应,在溶液中不能大量共存,故A错误;
NH、OH-之间发生反应,在溶液中不能大量共存,故 B错误;HCO与OH-反应,在强碱
性溶液中不能大量共存,故C错误;强酸性溶液中存在大量H+,K+、Fe2+、Cl-、SO之
间不反应,在溶液中能够大量共存,故D正确。
9.答案 C
解析 该条件下H 燃烧放出的热量不能使冰分解产生氧气,水在很高的温度下才分解,A
2
项错误;实验结果表明氢气已经燃烧,被冷却的氢气不能使酸性高锰酸钾溶液褪色,也不
能氧化亚铁离子,B项错误;烧杯中酸性KMnO 溶液褪色,说明H 燃烧的产物中可能有
4 2
还原性物质,若将烧杯中的溶液换成含有少量 KSCN的FeCl 溶液,溶液呈红色,说明有
2
Fe3+生成,因此说明H 燃烧的产物中可能有氧化性物质,由此说明H 燃烧的产物中可能既
2 2
有还原性又有氧化性的物质,可能为HO ,C项正确;同种物质的性质相同,该条件下生
2 2
成的水分子的化学性质与普通的水的性质一样,D项错误。
10.答案 C
解析 断裂化学键要吸收能量,H—H的断裂需要吸收能量,故A正确;①→②,CO 中碳
2
氧双键断裂,与羟基发生加成反应,故B正确;④中,CO被还原为CH ,故C错误;根
4据质量守恒,生成CH 的总反应方程式是CO+4H=======CH+2HO,故D正确。
4 2 2 4 2
11.答案 D
解析 反应1为2ZnFeO +H=====2ZnFeO +HO,氧化产物为HO,故A错误;反应2
4 2 3.5 2 2
为4ZnFeO +SO =====4ZnFeO +S,还原产物为S,故B错误;循环Ⅱ中电解时,阳极上
3.5 2 4
Mn2+放电生成MnO ,若Mn作为循环Ⅱ中电解过程中的阳极材料,则阳极上Mn放电,得
2
不到MnO ,故C错误;根据S元素守恒,循环Ⅰ和循环Ⅱ中消耗同质量的SO ,理论上得
2 2
到S和HSO 的物质的量之比为1∶1,质量之比为16∶49,故D正确。
2 4
12.答案 D
解析 可以通过非金属元素之间的置换反应说明元素非金属性强弱,但反应物中的非金属
单质必须表现出氧化性,推测化学方程式中非金属元素C表现出还原性,A错误;SO 具
2
有还原性、Ca(ClO) 具有氧化性,因此会发生氧化还原反应,B错误;Fe与S发生氧化还
2
原反应生成FeS,说明S的氧化性可使变价金属生成低价态,因此推测应该生成 Cu S,C
2
错误;利用强酸制弱酸的原理,D正确。
13.答案 C
解析 Fe3+只存在于强酸性溶液中,在中性溶液中 Fe3+已沉淀完全,A项错误;依据还原
性强弱,I-优先反应,其次才是Fe2+。依据离子方程式:2I-+Cl===I +2Cl-,溶液中0.8
2 2
mol I-完全反应需消耗0.4 mol Cl ,而现在只通入0.3 mol Cl ,所以Fe2+没有参与反应,离
2 2
子方程式为2I-+Cl===I +2Cl-,B项错误;从题给信息可知次氯酸的酸性大于HCO,所
2 2
以向NaClO溶液中通入少量二氧化碳的离子方程式为ClO-+CO +HO===HClO+HCO,
2 2
C项正确;氯气先与Fe2+反应,再与Br-反应,所以滴加少量的氯水,并不会生成溴单质,
而是发生反应:2Fe2++Cl===2Fe3++2Cl-,D项错误。
2
14.答案 D
解析 能和氯化钡溶液反应生成白色不溶于盐酸的沉淀的可能是Ag+或SO,所以原溶液中
不一定含有硫酸根离子,故A错误;向某溶液中加入碳酸钠溶液产生白色沉淀,再加盐酸,
沉淀消失,存在的阳离子可能是Ba2+或Ca2+,所以原溶液中不一定含有钡离子,故B错误;
氨气极易溶于水,稀溶液中,铵根离子与氢氧根离子反应生成一水合氨,不加热,一水合
氨不能分解,没有氨气逸出,故不能说明原溶液中是否含有 NH,故C错误;向某黄色溶
液中加入淀粉-KI溶液,溶液呈蓝色,该黄色溶液可能是碘水;也可能是该溶液有氧化性,
能把碘离子氧化成碘,则该溶液中可能含有溴,也可能含有铁离子,故D正确。
15.答案 D
解析 I 在水中溶解度较小,易溶于CCl ,故CCl 起到萃取、富集I 的作用,A正确;在
2 4 4 2
KI溶液中加溴水,溴单质与I-发生置换反应,故Ⅰ中发生反应的离子方程式为Br +2I-
2
===I +2Br-,B正确;依据现象可知,氯水能继续氧化碘单质,而溴单质不能,故依据
2
a、b中现象,可以证明Cl 的氧化性比Br 强,C正确;继续滴加氯水,可以将I 氧化为
2 2 2IO(无色),D错误。
16.答案 (1)①树状分类法 ②D ③B ④3
(2)Fe3++3OH-===Fe(OH) ↓ 红褐 丁达尔效应
3
解析 (1)②A项,碳和一氧化碳具有还原性;B项,一氧化碳和二氧化碳属于氧化物;C
项,二氧化碳和碳酸氢钠中碳元素化合价相同;D项,只有碳酸氢钠属于电解质,故选D
项。
③晶体碘属于非金属单质,故选B项。④将一定量的稀硫酸逐滴滴入氢氧化钠和碳酸钠的
混合溶液中,边滴加边搅拌,直至有少量气泡产生,此过程中共发生的离子反应有 OH-+
H+===HO、H++CO===HCO、HCO+H+===HO+CO↑。(2)棕黄色FeCl 溶液中滴入
2 2 2 3
NaOH溶液会产生Fe(OH) 沉淀,即Fe3++3OH-===Fe(OH) ↓,在小烧杯中加入20 mL蒸
3 3
馏水,加热至沸腾后,向沸水中滴入2 mL棕黄色氯化铁溶液,继续加热可以获得红褐色的
氢氧化铁胶体,氢氧化铁胶体具有丁达尔效应。
17.答案 (1)不可行 (2)①试管口略向下倾斜,加热前先将试管外壁擦干,加热时应先使
试管在酒精灯上移动,使试管均匀受热 ②取一小块pH试纸放在玻璃片(或表面皿)上,用
洁净的玻璃棒蘸取待测液点在试纸的中部,观察试纸颜色的变化并跟标准比色卡比较,即
可确定溶液的pH ③pH试纸显示有碱性气体产生 加热时无气体产生,溶液呈碱性 CO
+HOHCO+OH- 加热时无气体产生、溶液呈中性
2
解析 (1)NaHCO 、NaCO 与Ba(OH) 溶液均能生成白色沉淀,所以该方案不可行。(2)①
3 2 3 2
给试管里的固体药品加热时,往往有水汽产生,因此试管口必须略向下倾斜。加热前需先
将试管外壁擦干,以防止加热时试管炸裂。加热时应先使试管在酒精灯上移动,使试管均
匀受热。②用pH试纸测溶液pH的操作是取一小块pH试纸放在玻璃片或表面皿上,用洁
净的玻璃棒蘸取待测液点在试纸的中部,观察试纸颜色的变化并跟标准比色卡比较,即可
确定溶液的pH。(3)碳酸氢铵受热分解生成碱性气体NH ,通过检验NH 即可判断碳酸氢铵
3 3
存在;碳酸钠和氯化钠受热无气体放出,但碳酸钠溶液由于水解而呈碱性:CO+
HOHCO+OH-,所以只要加热时无气体产生、溶液呈碱性,即可判断碳酸钠存在;氯
2
化钠溶液呈中性,所以只要加热时无气体产生、溶液呈中性,即可判断氯化钠存在。
18.答案 (1)bc
(2)①2Fe3++HS===2Fe2++S↓+2H+
2
②O==C==S
(3)①5NO +3HO+ClO ===5NO+6H++Cl- ②填料高度增加,使气体和吸收液能够充分
2 2 2
接触反应
(4)CD
解析 (1)酸雨包括硫酸型酸雨和硝酸型酸雨,主要与硫的氧化物和氮的氧化物的排放有关,
与碳的氧化物无关,故b、c符合题意。(2)①用Fe (SO ) 吸收HS,发生氧化还原反应,
2 4 3 2
生成亚铁离子和硫单质,反应的离子方程式为2Fe3++HS===2Fe2++S↓+2H+。(3)①NO
2 2和ClO 反应生成硝酸和氯离子(盐酸),根据原子守恒和化合价升降守恒,可得离子方程式
2
为5NO +3HO+ClO ===5NO+6H++Cl-。②随着吸收器内填料高度增加,NO 去除率升
2 2 2 x
高的原因是填料高度增加,使气体和吸收液能够充分接触反应。(4)1 mol O 和4 mol NO 可
2 2
以恰好反应生成4 mol HNO ,HNO 与NaOH溶液完全反应,无气体剩余,A错误;根据
3 3
题给信息可知,当n(NO)≤n(NO )时,气体可以被完全吸收,B错误;1 mol O 和2 mol NO
2 2
反应生成2 mol NO ,2 mol NO 与2 mol NO被NaOH溶液恰好吸收后,NO还剩余3 mol,
2 2
不能被完全吸收,C正确;4 mol NO和4 mol NO 被NaOH溶液恰好吸收后,NO还剩余2
2
mol,不能被完全吸收,D正确。
19.答案 (1)检查装置气密性 (2)Cl-+ClO-+2H+===Cl↑+HO (3)SO +Cl +
2 2 2 2
2HO===4H++SO+2Cl- (4)滴加K[Fe(CN) ]溶液,出现蓝色沉淀 (5)将装置中残留的
2 3 6
SO 、Cl 排入装置C中,被NaOH溶液吸收,防止污染环境 (6)酸性条件下,氧化性:
2 2
ClO->Fe3+>SO
解析 (1)该实验涉及二氧化硫气体的制备,实验在添加药品前需进行的操作是检查装置气
密性。
(2)步骤Ⅰ中,一段时间后观察到装置B中液面上方出现黄绿色气体,说明Cl-被ClO-氧化
为氯气,反应的离子方程式为Cl-+ClO-+2H+===Cl↑+HO。
2 2
(3)步骤Ⅲ中,开始一段时间,装置B中溶液的颜色并无明显变化,说明Fe3+没反应,氯气
与SO 发生氧化还原反应,反应的离子方程式是SO +Cl+2HO===4H++SO+2Cl-。
2 2 2 2
(4)验证该溶液中存在Fe2+的方法是向用注射器取出的上层清液中滴加K[Fe(CN) ]溶液,出
3 6
现蓝色沉淀,则含有Fe2+。
(5)打开活塞a,通一段时间空气的目的是将装置中残留的 SO 、Cl 排入装置C中,被
2 2
NaOH溶液吸收,防止污染环境。
(6)向装置B中滴加次氯酸钠溶液,溶液立即变为黄色,说明Fe2+被ClO-氧化为Fe3+,氧
化性:ClO->Fe3+;步骤Ⅲ中一段时间后,观察到装置B中溶液由黄色变为浅绿色,说明
Fe3+把SO 氧化为SO,氧化性:Fe3+>SO。所以可得出该实验的结论是酸性条件下,氧化
2
性:ClO->Fe3+>SO。
20.答案 (1)NH、Fe2+、Mg2+、SO 无 (2)0.3 mol Fe(OH) 、0.1 mol Mg(OH)
3 2
(3)3Fe2++NO+4H+===2HO+3Fe3++NO↑ (4)Ba2++CO +2OH-===BaCO ↓+HO
2 2 3 2
(5)4NH +6NO=====5N+6HO 2∶3
3 2 2
解析 待测液中加入过量的稀盐酸,无明显现象,溶液中一定没有 SO、CO,加入过量的
硝酸钡溶液,生成标准状况下2.24 L的无色气体X,则溶液中含有Fe2+,发生反应的离子
方程式是3Fe2++4H++NO===3Fe3++NO↑+2HO,生成的一氧化氮的物质的量是 0.1
2
mol,则Fe2+的物质的量是0.3 mol,高锰酸根离子具有氧化性,与亚铁离子不能共存,则
溶液中不含有MnO,一定含有SO,SO的物质的量是=0.5 mol,向滤液Ⅰ中加入过量的氢氧化钠溶液,生成无色气体,则溶液中一定含有NH,NH的物质的量是=0.2 mol,滤液Ⅰ
中含有铁离子,根据原子守恒生成氢氧化铁的质量是0.3 mol×107 g·mol-1=32.1 g,而沉
淀B是37.9 g,则有5.8 g的氢氧化镁,其物质的量是=0.1 mol,则溶液中一定含有0.1 mol
的Mg2+,依据电荷守恒:n(Na+)+2n(Mg2+)+2n(Fe2+)+n(NH)=2n(SO),把数据代入得,
n(Na+)=0,则溶液中不含有Na+,据此回答问题。
(4)滤液Ⅱ中含有钡离子、氢氧根离子,通入少量二氧化碳,生成沉淀 C是碳酸钡,反应的
离子方程式为Ba2++CO +2OH-===BaCO ↓+HO。(5)一氧化氮和氨气反应生成氮气和
2 3 2
水,反应的化学方程式是4NH +6NO=====5N +6HO;由方程式可知,4 mol氨气被氧化
3 2 2
生成
2 mol氮气,6 mol一氧化氮被还原生成3 mol氮气,则所得氧化产物与还原产物的质量之
比为2∶3。