文档内容
第1讲 原子结构与性质
[考纲要求]
1.了解原子核外电子的运动状态、能级分布和排布原理,能正确书写1~36号元素原子
核外电子、价电子的电子排布式和轨道表达式。
2.了解电离能的含义,并能用以说明元素的某些性质。
3.了解电子在原子轨道之间的跃迁及其简单应用。
4.了解电负性的概念,并能用以说明元素的某些性质。
考点一 原子结构
1知识梳理
1.能层与能级
(1)能层(n)
在多电子原子中,核外电子的____是不同的,按照电子的____差异将其分成不同能层。
通常用__________表示相应的第一、二、三、四、五、六、七……能层,能量依次升高。
(2)能级
同一能层的电子的____也可能不同,又将其分成不同的能级,通常用________等表示,
同一能层里,各能级的能量按________的顺序升高,即__________。
2.原子轨道
(1)原子轨道:表示电子在原子核外的一个空间运动状态。电子云轮廓图给出了电子在
________________的区域。
原子轨道 轨道形状 轨道个数
s 球形 ____
p 哑铃形 ____
(2)能量关系
①相同能层上原子轨道能量的高低:____________。
②形状相同的原子轨道能量的高低:____________。
③同一能层内形状相同而伸展方向不同的原子轨道的能量相等,如np、np、np 轨道的
x y z
能量相等。
3.基态原子的核外电子排布原理
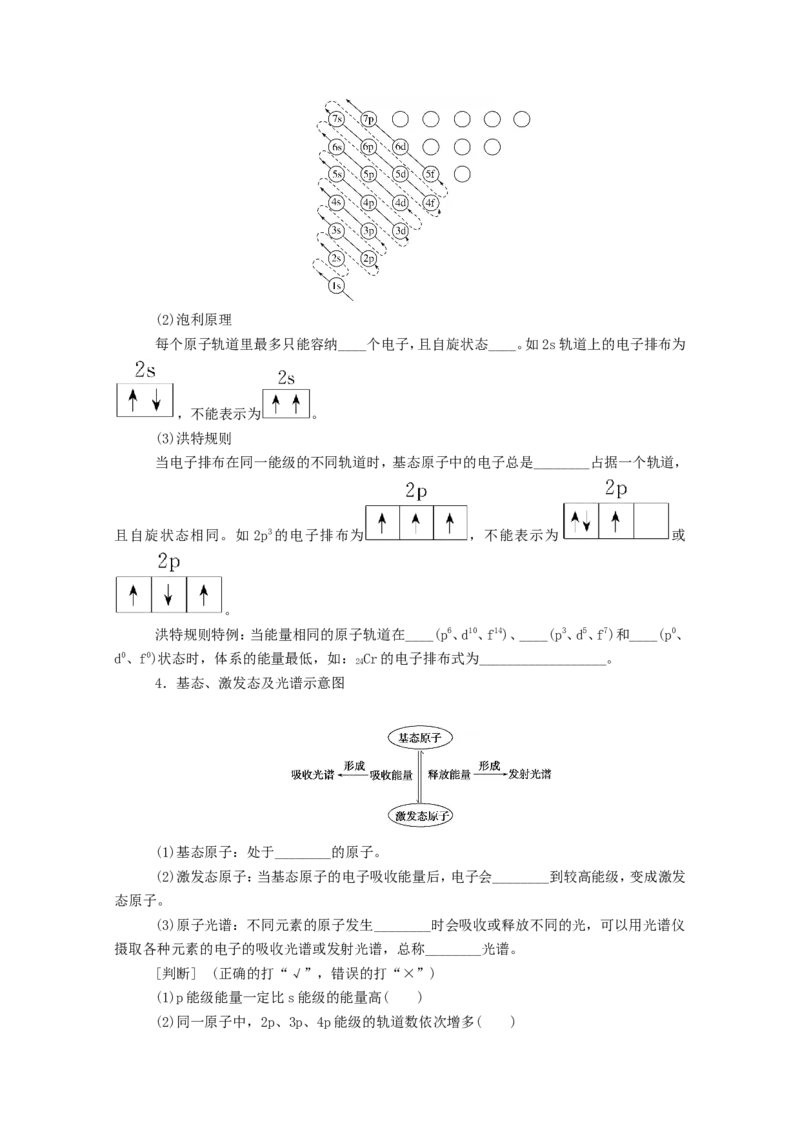
(1)能量最低原理:即电子尽可能地先占有能量低的轨道,然后进入能量高的轨道,使整
个原子的能量处于最低状态。
下图为构造原理示意图,即基态原子核外电子原子轨道排布顺序图:(2)泡利原理
每个原子轨道里最多只能容纳____个电子,且自旋状态____。如2s轨道上的电子排布为
,不能表示为 。
(3)洪特规则
当电子排布在同一能级的不同轨道时,基态原子中的电子总是________占据一个轨道,
且自旋状态相同。如 2p3的电子排布为 ,不能表示为 或
。
洪特规则特例:当能量相同的原子轨道在____(p6、d10、f14)、____(p3、d5、f7)和____(p0、
d0、f0)状态时,体系的能量最低,如: Cr的电子排布式为__________________。
24
4.基态、激发态及光谱示意图
(1)基态原子:处于________的原子。
(2)激发态原子:当基态原子的电子吸收能量后,电子会________到较高能级,变成激发
态原子。
(3)原子光谱:不同元素的原子发生________时会吸收或释放不同的光,可以用光谱仪
摄取各种元素的电子的吸收光谱或发射光谱,总称________光谱。
[判断] (正确的打“√”,错误的打“×”)
(1)p能级能量一定比s能级的能量高( )
(2)同一原子中,2p、3p、4p能级的轨道数依次增多( )(3)2p和3p轨道形状均为哑铃形,能量也相等( )
(4)钠元素的基态原子的电子排布式为1s22s22p62d1( )
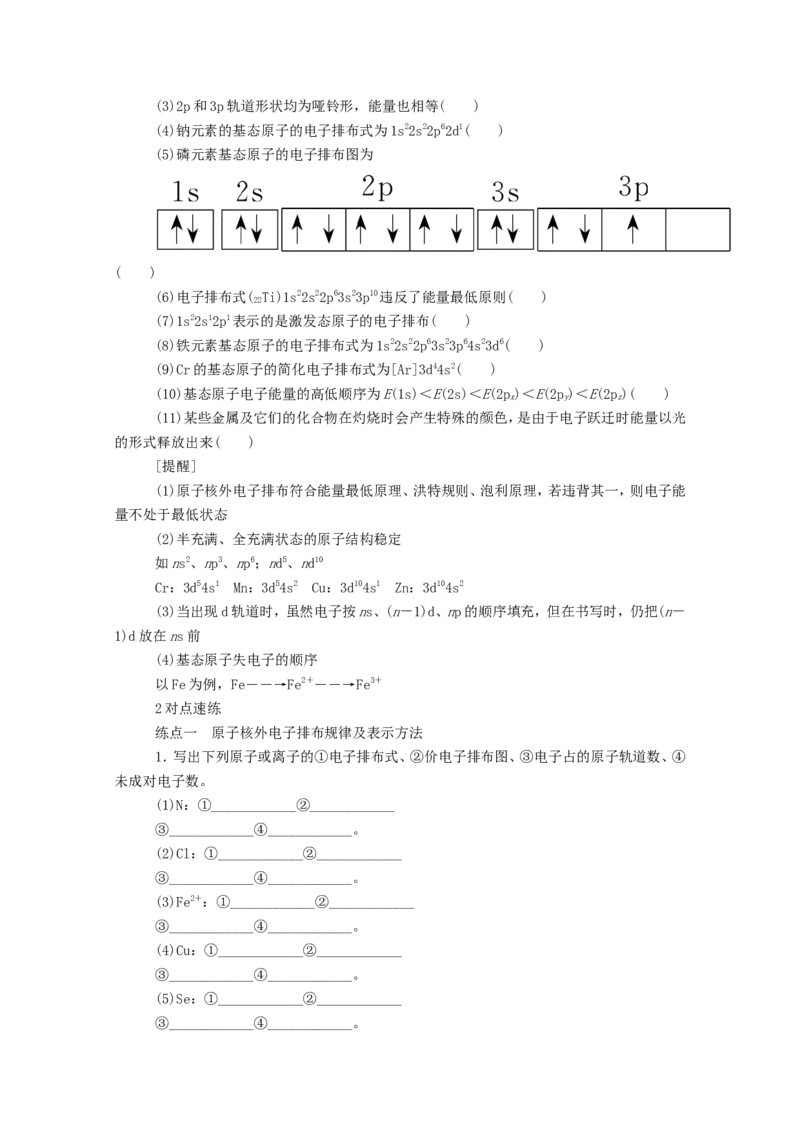
(5)磷元素基态原子的电子排布图为
( )
(6)电子排布式( Ti)1s22s22p63s23p10违反了能量最低原则( )
22
(7)1s22s12p1表示的是激发态原子的电子排布( )
(8)铁元素基态原子的电子排布式为1s22s22p63s23p64s23d6( )
(9)Cr的基态原子的简化电子排布式为[Ar]3d44s2( )
(10)基态原子电子能量的高低顺序为E(1s)<E(2s)<E(2p)<E(2p)<E(2p)( )
x y z
(11)某些金属及它们的化合物在灼烧时会产生特殊的颜色,是由于电子跃迁时能量以光
的形式释放出来( )
[提醒]
(1)原子核外电子排布符合能量最低原理、洪特规则、泡利原理,若违背其一,则电子能
量不处于最低状态
(2)半充满、全充满状态的原子结构稳定
如ns2、np3、np6;nd5、nd10
Cr:3d54s1 Mn:3d54s2 Cu:3d104s1 Zn:3d104s2
(3)当出现d轨道时,虽然电子按ns、(n-1)d、np的顺序填充,但在书写时,仍把(n-
1)d放在ns前
(4)基态原子失电子的顺序
以Fe为例,Fe――→Fe2+――→Fe3+
2对点速练
练点一 原子核外电子排布规律及表示方法
1.写出下列原子或离子的①电子排布式、②价电子排布图、③电子占的原子轨道数、④
未成对电子数。
(1)N:①____________②____________
③____________④____________。
(2)Cl:①____________②____________
③____________④____________。
(3)Fe2+:①____________②____________
③____________④____________。
(4)Cu:①____________②____________
③____________④____________。
(5)Se:①____________②____________
③____________④____________。(6)Br-:①____________②____________
③____________④____________。
2.下列电子排布式或轨道表示式正确的是( )
①C原子的轨道表示式:
②Cr原子的电子排布式:1s22s22p63s23p63d44s2
③O原子的轨道表示式:
④Br原子的外围电子排布式:3d104s24p5
⑤B原子的轨道表示式:
A.①②③ B.②③④
C.①②④⑤ D.只有③
反思归纳
在写基态原子的电子排布图时,常出现以下错误:
练点二 核外电子排布中的能量变化
3.气态电中性基态原子的原子核外电子排布发生如下变化,吸收能量最多的是( )
A.1s22s22p63s23p2→1s22s22p63s23p1
B.1s22s22p63s23p3→1s22s22p63s23p2
C.1s22s22p63s23p4→1s22s22p63s23p3
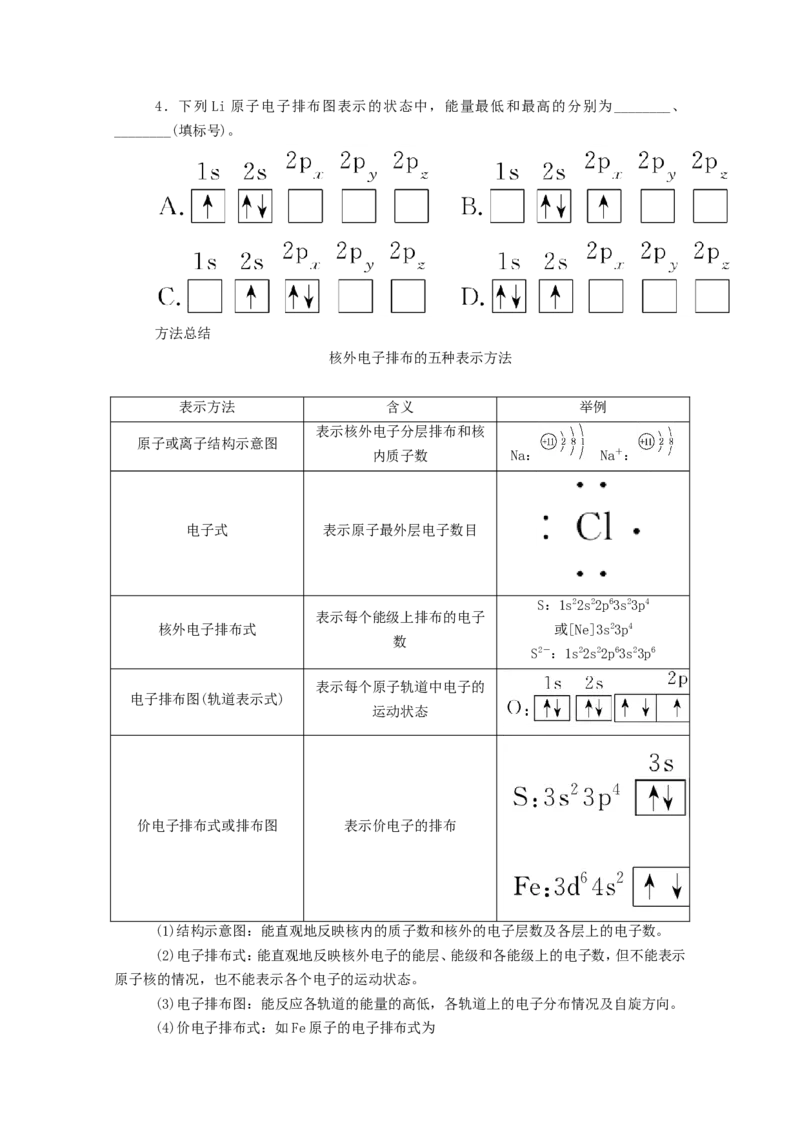
D.1s22s22p63s23p63d104s24p2→1s22s22p63s23p63d104s24p14.下列 Li原子电子排布图表示的状态中,能量最低和最高的分别为________、
________(填标号)。
方法总结
核外电子排布的五种表示方法
表示方法 含义 举例
表示核外电子分层排布和核
原子或离子结构示意图
内质子数 Na: Na+:
电子式 表示原子最外层电子数目
S:1s22s22p63s23p4
表示每个能级上排布的电子
核外电子排布式 或[Ne]3s23p4
数
S2-:1s22s22p63s23p6
表示每个原子轨道中电子的
电子排布图(轨道表示式)
运动状态
价电子排布式或排布图 表示价电子的排布
(1)结构示意图:能直观地反映核内的质子数和核外的电子层数及各层上的电子数。
(2)电子排布式:能直观地反映核外电子的能层、能级和各能级上的电子数,但不能表示
原子核的情况,也不能表示各个电子的运动状态。
(3)电子排布图:能反应各轨道的能量的高低,各轨道上的电子分布情况及自旋方向。
(4)价电子排布式:如Fe原子的电子排布式为1s22s22p63s23p63d64s2,价电子排布式为3d64s2。价电子排布式能反映基态原子的能层数
和参与成键的电子数以及最外层电子数。
考点二 原子结构与元素性质
1知识梳理
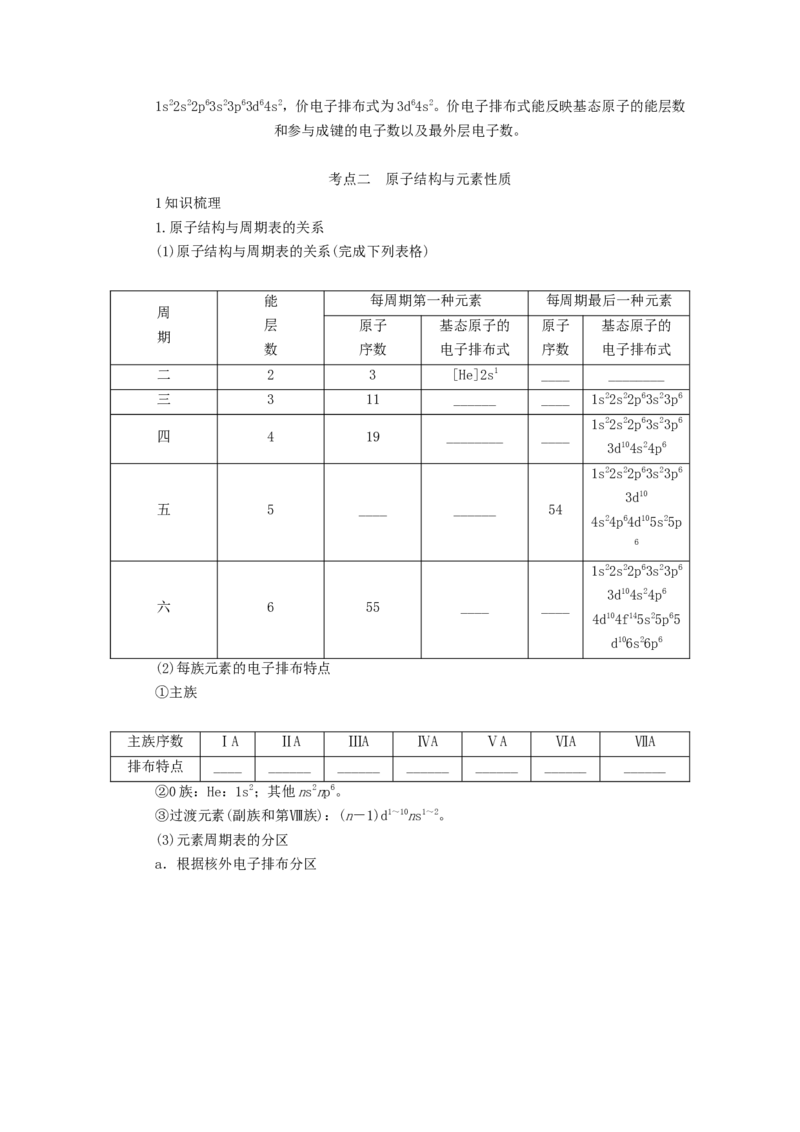
1.原子结构与周期表的关系
(1)原子结构与周期表的关系(完成下列表格)
能 每周期第一种元素 每周期最后一种元素
周
层 原子 基态原子的 原子 基态原子的
期
数 序数 电子排布式 序数 电子排布式
二 2 3 [He]2s1 ____ ________
三 3 11 ______ ____ 1s22s22p63s23p6
1s22s22p63s23p6
四 4 19 ________ ____
3d104s24p6
1s22s22p63s23p6
3d10
五 5 ____ ______ 54
4s24p64d105s25p
6
1s22s22p63s23p6
3d104s24p6
六 6 55 ____ ____
4d104f145s25p65
d106s26p6
(2)每族元素的电子排布特点
①主族
主族序数 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
排布特点 ____ ______ ______ ______ ______ ______ ______
②0族:He:1s2;其他ns2np6。
③过渡元素(副族和第Ⅷ族):(n-1)d1~10ns1~2。
(3)元素周期表的分区
a.根据核外电子排布分区b.各区元素化学性质及原子最外层电子排布特点
分区 元素分布 外围电子排布 元素性质特点
除氢外都是活泼金属元
s区 ⅠA族、ⅡA族 ns1~2 素;通常是最外层电子参
与反应
通常是最外层电子参与反
p区 ⅢA族~ⅦA族、0族 ns2np1~6(He除外)
应
ⅢB族~ⅦB族、Ⅷ族(除 d轨道可以不同程度地参
d区 (n-1)d1~9ns1~2(除钯外 )
镧系、锕系外) 与化学键的形成
ds区 ⅠB族、ⅡB族 (n-1)d10ns1~2 金属元素
镧系元素化学性质相近,
f区 镧系、锕系 (n-2)f0~14(n-1)d0~2ns2
锕系元素化学性质相近
2.元素性质的规律性变化
(1)电离能
①含义
第一电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的______,
符号____,单位________。
②规律
a.同周期:第一种元素的第一电离能____,最后一种元素的第一电离能____,总体呈现
从左至右逐渐____的变化趋势。
b.同族元素:从上至下第一电离能逐渐____。
c.同种原子:逐级电离能越来越______(即I____I____I…)。
1 2 3
(2)电负性
①含义:不同元素的原子在化合物中____________能力的标度。元素的电负性越大,表
示其原子在化合物中____________的能力越____。
②标准:以最活泼的非金属氟的电负性为____和锂的电负性为1.0作为相对标准,计算
得出其他元素的电负性(稀有气体元素未计)。
③变化规律
a.金属元素的电负性一般________,非金属元素的电负性一般________,而位于非金属
三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右,它们既有金属又有非金属性。b.在元素周期表中,同周期从左至右,元素的电负性逐渐____,同主族从上至下,元素的
电负性逐渐____。
[思考]
按要求回答下列问题
(1) 第 三 周 期 所 有 元 素 的 第 一 电 离 能 (I) 大 小 顺 序 为
1
__________________________________________(用元素符号表示)。
(2)Na的逐级电离能中有________次突跃。分别是哪级电离能发生突跃?________、
________。
(3)F、Cl、Br、I的第一电离能由大到小的顺序为________________,电负性由大到小的
顺序为________________。
[判断] (正确的打“√”,错误的打“×”)
(1)共价化合物中,成键元素电负性大的表现为负价( )
(2)根据元素周期表,氮与氧相比,后者的第一电离能大( )
(3)过渡元素中含有非金属元素( )
(4)s区全部是金属元素( )
(5)电负性越大,非金属性越强,第一电离能也越大( )
(6)价电子排布为4s24p3的元素位于第四周期ⅤA族,是p区元素( )
(7)价电子排布为5s25p1的元素位于第五周期ⅠA族,是s区元素( )
[提醒]
(1)金属活动性顺序与元素相应的电离能大小顺序不完全一致,故不能根据金属活动性
顺序表判断电离能的大小。
(2)第二、三、四周期的同周期主族元素,第ⅡA(ns2np0)和第ⅤA族(ns2np3),因p轨道处
于全空或半充满状态,比较稳定,所以其第一电离能大于同周期相邻的第ⅢA族和第ⅥA族元
素,如第一电离能:Mg>Al,P>S。
(3)不能将电负性1.8作为划分金属和非金属的绝对标准。
2对点速练
练点一 原子结构与元素性质基础判断
1.下列说法中正确的是( )
A.第三周期所有元素中钠的第一电离能最小
B.钠的第一电离能比镁的第一电离能大
C.在所有元素中,氟的第一电离能最大
D.钾的第一电离能比镁的第一电离能大
2.电负性的大小也可以作为判断元素金属性和非金属性强弱的尺度。下列关于电负性
的变化规律正确的是( )
A.元素周期表从左到右,元素的电负性逐渐变大
B.元素周期表从上到下,元素的电负性逐渐变大
C.电负性越大,金属性越强
D.电负性越小,非金属性越强3.现有三种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是( )
A.最高正化合价:③>②>①
B.原子半径:③>②>①
C.电负性:③>②>①
D.第一电离能:③>②>①
4.回答下列问题:
(1)已知铁是26号元素,写出Fe的价层电子排布式________;在元素周期表中,该元素
在________区(填“s”“p”“d”“f”或“ds”)。
(2)写出与N同主族的As的基态原子的核外电子排布式:________。从原子结构的角度
分析B、N和O的第一电离能由大到小的顺序为________。
(3)写出Fe2+的核外电子排布式:________。
(4)Zn2+的核外电子排布式为________。
练点二 原子结构与元素性质综合应用
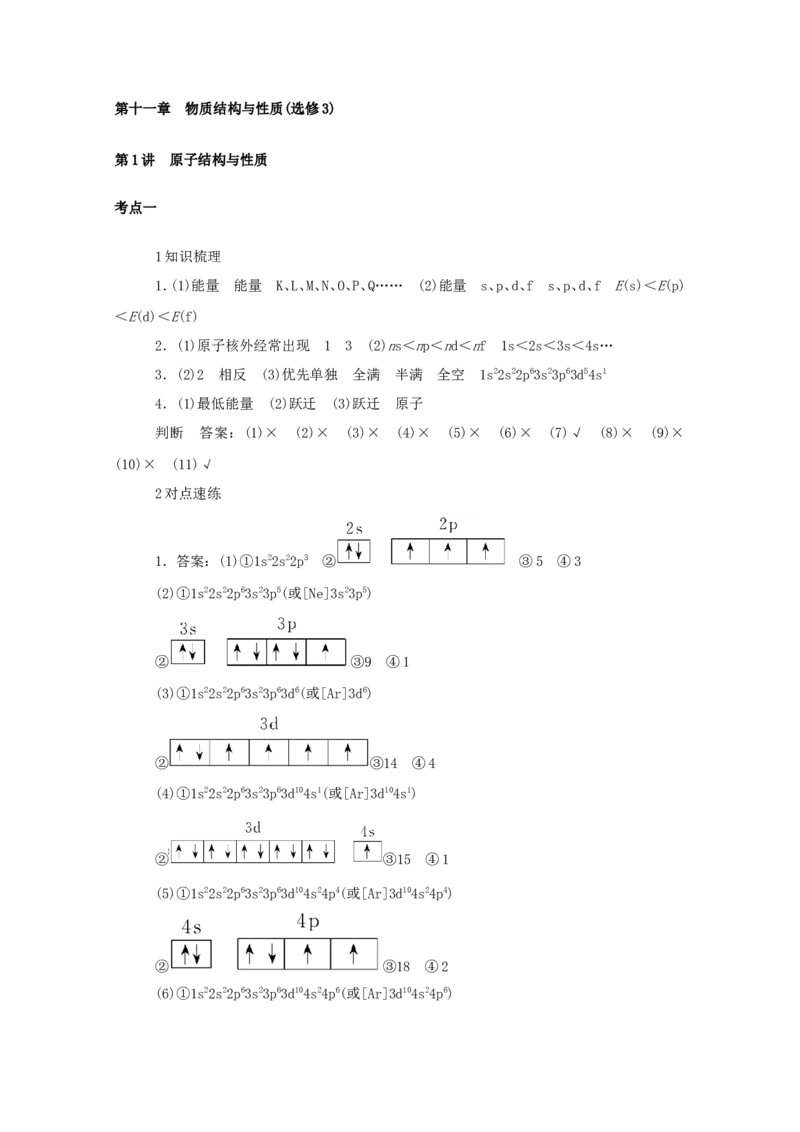
5.根据信息回答下列问题:
A.第一电离能I是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)
1
所需的最低能量。下图是部分元素原子的第一电离能I随原子序数变化的曲线图(其中12号
1
至17号元素的有关数据缺失)。
B.不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一
般认为:如果两个成键原子间的电负性差值小于1.7,原子之间通常形成离子键,如果两个成键
原子间的电负性差值小于1.7,通常形成共价键。下表是某些元素的电负性值。
元素
Li Be B C O F Na Al Si P S Cl
符号
电负
1.0 1.5 2.0 2.5 3.5 4.0 0.9 1.5 1.8 2.1 2.5 3.0
性值
(1)认真分析信息A图中同周期元素第一电离能的变化规律,推断第三周期Na~Ar这几
种元素中,Al的第一电离能的大小范围为________X>Y>Z
B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z
D.氢化物水溶液的酸性:Y>W
2.[2020·天津卷,8]短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列
说法正确的是( )
A.元素电负性:ZCl>Br>I F>Cl>Br>I
判断 答案:(1)√ (2)× (3)× (4)× (5)× (6)√ (7)×
2对点速练
1.解析:C项,在所有元素中,He的第一电离能最大。
答案:A
2.解析:利用同周期从左至右元素电负性逐渐增大,同主族从上至下元素电负性逐渐减
小的规律来判断。电负性越大,金属性越弱,非金属性越强。
答案:A
3.解析:根据核外电子排布可知①是S,②是P,③是F。F无最高正价,A错误;同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则原子半径:②>①>③,B错误;
非金属性越强,电负性越大,则电负性:③>①>②,C错误;非金属性越强,第一电离能越大,但P
的3p轨道电子处于半充满状态,稳定性强,第一电离能强于S,则第一电离能:③>②>①,D正
确。
答案:D
4.解析:B、N、O元素同周期,在第一电离能逐渐增大的趋势中出现了I(N)>I(O)的曲折。
1 1
答 案 : (1)3d64s2 d (2)1s22s22p63s23p63d104s24p3 或 [Ar]3d104s24p3 N>O>B
(3)1s22s22p63s23p63d6 (4)1s22s22p63s23p63d10
5.解析:(1)由信息所给的图可以看出,同周期的ⅠA族元素的第一电离能最小,而第
ⅢA族元素的第一电离能小于第ⅡA族元素的第一电离能,故NaMg>Ca,最小范围
应为0.9~1.5。
(5)AlCl 中Al与Cl的电负性差值为1.5,根据信息,电负性差值若小于1.7,则形成共
3
价键,所以AlCl 为共价化合物,离子化合物在熔融状态下以离子形式存在,可以导电,但共价
3
化合物不能导电。
答案:(1)Na Mg
(2)第五 第ⅠA
(3)两 Be(OH)+2H+===Be2++2HO、
2 2
Be(OH)+2OH-===Be +2HO
2 2
(4)0.9~1.5
(5)Al元素和Cl元素的电负性差值为1.5(<1.7),所以形成共价键,为共价化合物;判断
方法:将氯化铝加热到熔融态,进行导电性实验,如果不导电,说明是共价化合物本讲真题研练
1.解析:根据Z与X可形成淡黄色化合物ZX,即该化合物为NaO,结合原子序数关系
2 2 2 2
可知,X为O元素,Z为Na元素;基态O原子核外有8个电子,是最高能级2p上排布的电子数的
2倍;由原子序数关系可知Y为F元素,则与其同主族的W为Cl元素。根据第一电离能递变规
律,可知其相对大小顺序为:F>O>Cl>Na,A项错误;根据非金属性:F >O>Cl,可知简单离子的还
原性:Cl->O2->F-,B项错误;根据离子半径的变化规律,可知简单离子半径:Cl->O2->F->Na+,
C项正确;氢化物水溶液的酸性:HF< HCl,D项错误。
答案:C
2.解析:本题考查物质性质与元素推断,考查的化学学科核心素养是宏观辨识与微观探
析。从Z的最高价氧化物的水化物的化学式和W的最高价氧化物的水化物的pH可知,Z、W是磷、
硫元素,结合X、Y的最高价氧化物水化物的0.1 mol·L-1溶液的pH,可知X、Y是氮、钠元素。
电负性:P Na+,B项错误;磷的3p轨道为半满稳定状态,其第一电
离能大于硫,C项错误;NH 分子间存在氢键,导致其沸点高于PH,D项错误。
3 3
答案:A
3.解析:(全国卷Ⅰ):(1)A表示基态镁原子的第二电离能,B表示基态镁原子的第一电
离能,则电离能:A>B;C表示激发态镁原子的第一电离能,则电离能:A>C;D表示激发态镁原子
的第二电离能,则电离能:A>D。
(全国卷Ⅱ):(2)金属原子变为阳离子,首先失去最外层电子。
(3)F-与O2-具有相同电子层结构,F原子序数较大,离子半径较小。
(全国卷Ⅲ):(1)根据对角线原则,Li与Mg的化学性质最相似。基态时Mg原子的两个M
层电子处于3s轨道上,且自旋方向相反。
答案:(全国卷Ⅰ):(1)A
(全国卷Ⅱ):(2)4s 4f5 (3)小于
(全国卷Ⅲ):(1)Mg 相反
4.解析:(全国卷Ⅰ):(2)Li+和H-的电子层结构相同,而具有相同电子层结构的离子半
径大小与核电荷数有关,核电荷数越大,离子半径越小。
(全国卷Ⅱ):(1)基态Fe原子核外有26个电子,按照构造原理,其核外电子排布式为
[Ar]3d64s2,按照洪特规则,价层电子3d上6个电子优先占据5个不同轨道,故价层电子的电子排布图为 。
基态S原子的核外电子排布式为1s22s22p63s23p4,电子占据最高能级为3p,p能级的电子
云轮廓图为哑铃(纺锤)形。
(全国卷Ⅲ):(1)Zn原子核外有30个电子,其电子排布式为[Ar]3d104s2。
(2)Cu原子的外围电子排布式为3d104s1,4s能级处于半充满状态,而Zn原子的4s能级
处于全充满状态,Zn原子更不易失去1个电子,所以Zn原子的第一电离能较大。
答案:(全国卷Ⅰ):
(2)Li+核电荷数较大
(全国卷Ⅱ):
(1) 哑铃(纺锤)
(全国卷Ⅲ):
(1)[Ar]3d104s2
(2)大于 Zn核外电子排布为全充满稳定结构,较难失电子
5.解析:(全国卷Ⅰ):(1)赤橙黄绿青蓝紫,波长逐渐减小。
(2)K原子位于第四周期,原子结构示意图 ,核 外电子排布式为
1s22s22p63s23p64s1,最高能层为N层,第4电子层为4s原子轨道,为球形。K原子半径大,且价
电子数少(K原子价电子数为1,Cr原子价电子排布为3d54s1,价电子数为6),金属键弱,熔沸点
低。
(全国卷Ⅱ):(1)N原子位于第二周期第ⅤA族,价电子是最外层电子,即电子排布图是
。
(2)根据图(a),电子亲和能增大(除N外),同周期从左向右非金属性增强,得电子能力
增强,因此同周期自左向右电子亲和能增大;氮元素的p能级达到半满状态,原子相对稳定,不
易得到1个电子。(全国卷Ⅲ):(1)Co 为 27 号元素,Co 的基态原子核外电子排布式为:
1s22s22p63s23p63d74s2或[Ar]3d74s2;金属性越强,第一电离能越小,而金属性:Mn>O,故第一电
离能较大的为O。Mn原子的价电子排布式为3d54s2,根据洪特规则,有5个未成对电子,而O原
子的价电子排布式为2s22p4,仅有2个未成对电子,故基态原子核外未成对电子数较多的是
Mn。
答案:(全国卷Ⅰ):
(1)A
(2)N 球形 K原子半径较大且价电子数较少,金属键较弱
(全国卷Ⅱ):
(1)
(2)同周期元素随核电荷数依次增大,原子半径逐渐变小,故结合一个电子释放出的能
量依次增大 N的p能级处于半充满状态,具有稳定性,故不易结合一个电子
(全国卷Ⅲ):
(1)1s22s22p63s23p63d74s2或[Ar]3d74s2 O Mn