文档内容
第2讲 离子反应
[考纲要求]
1.了解电解质的概念,了解强电解质和弱电解质的概念。
2.了解电解质在水溶液中的电离,以及电解质溶液的导电性。
3.了解离子反应的概念、离子反应发生的条件。
4.能正确书写离子方程式。
5.掌握常见离子的检验方法。
6.正确判断常见离子在溶液中能否大量共存。
考点一 电解质的电离
1知识梳理
1.电解质和非电解质、强电解质和弱电解质
2.电解质的电离
电离是指电解质在________________状态下,离解成自由移动离子的过程。
3.电离方程式的书写
(1)强电解质的电离方程式中,用“____”连接,弱电解质(包括弱酸的酸式酸根)的电
离方程式中,用“____”连接。
如NaSO:______________________,HClO:__________________________。
2 4
(2)多元弱酸的电离分步书写,多元弱碱的电离一步写完。
如:HCO :______________________,____________________________;Fe(OH) :
2 3 3
__________________________。
(3)酸式盐的电离
多元强酸酸式盐与多元弱酸酸式盐的阴离子电离情况不同。
如NaHSO 溶液中:__________________________;
4NaHCO 溶液中:______________________、________________________。
3
[判断] (正确的打“√”,错误的打“×”)
(1)强电解质溶液的导电性比弱电解质溶液的导电性强( )
(2)弱电解质溶液中存在两种或两种以上共价化合物分子( )
(3)强电解质都是离子化合物,弱电解质都是共价化合物( )
(4)CaO是强电解质,是因为它的水溶液能导电( )
(5)Cl 的水溶液能导电,所以Cl 是电解质( )
2 2
(6)NaHCO
的电离方程式为NaHCO===Na++H++CO2−
( )
3 3 3
(7)NaHSO
溶于水:NaHSO===Na++HSO−
( )
4 4 4
(8)Al(OH) 碱式电离:Al(OH)===Al3++3OH-( )
3 3
(9)H
2
SO
3
在水溶液中电离:H
2
SO 32H++SO
3
2−( )
(10)HBr在水溶液中电离:HBrH++Br-( )
强、弱电解质与物质类别的关系
2对点速练
练点一 基本概念的判断
1.下列说法正确的是( )
A.酸、碱、盐都是电解质
B.电解质都是易溶于水的物质
C.氧化物都是电解质
D.氢化物都不是电解质2.今有12种物质:①Al ②稀硝酸 ③HNO ④液氨
3
⑤CO ⑥空气 ⑦NaCl ⑧CaCO ⑨NaHCO ⑩酒精 ⑪AlO ⑫石墨
2 3 3 2 3
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
序号 符合的条件 物质的序号
(1) 混合物
(2) 电解质,但熔融状态下并不导电
(3) 电解质,熔融状态能导电
(4) 电解质,但难溶于水
(5) 非电解质
(6) 既不是电解质,也不是非电解质,但本身能导电
练点二 电离方程式的书写与判断3.写出下列典型物质在水中的电离方程式
(1)HSO____________________________________________________________________
2 4
____。
(2)HCO____________________________________________________________________
2 3
____。
(3)Ca(OH)_________________________________________________________________
2
_______。
(4)Fe(OH)_________________________________________________________________
3
_______。
(5)NH·HO_________________________________________________________________
3 2
_______。
(6)NaCl____________________________________________________________________
____。
(7)BaSO___________________________________________________________________
4
_____。
(8)NaHSO__________________________________________________________________
4
______。
(9)NaHCO__________________________________________________________________
3
______。
(10)CHCOOH________________________________________________________________
3
________。练后归纳
书写电离方程式的两个基本判断
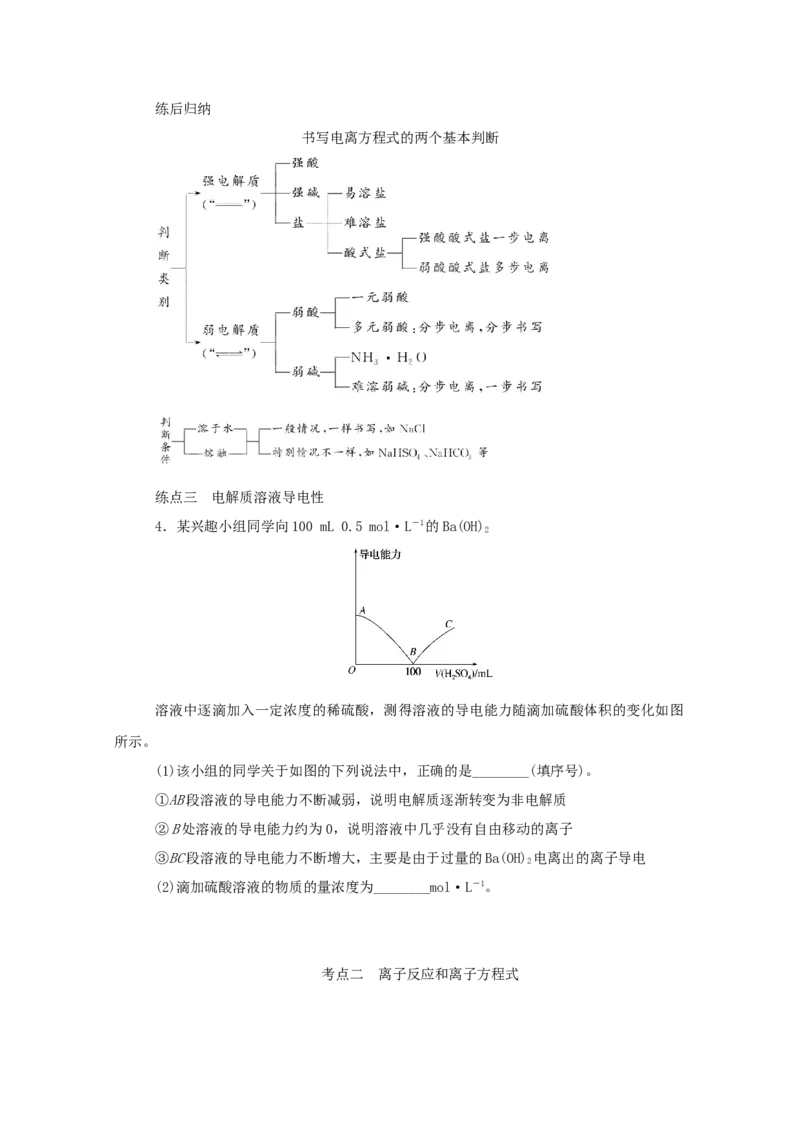
练点三 电解质溶液导电性
4.某兴趣小组同学向100 mL 0.5 mol·L-1的Ba(OH)
2
溶液中逐滴加入一定浓度的稀硫酸,测得溶液的导电能力随滴加硫酸体积的变化如图
所示。
(1)该小组的同学关于如图的下列说法中,正确的是________(填序号)。
①AB段溶液的导电能力不断减弱,说明电解质逐渐转变为非电解质
②B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
③BC段溶液的导电能力不断增大,主要是由于过量的Ba(OH) 电离出的离子导电
2
(2)滴加硫酸溶液的物质的量浓度为________mol·L-1。
考点二 离子反应和离子方程式1知识梳理
1.离子反应
(1)概念:指____________________的化学反应。
(2)本质:反应物中某些离子的________减小。
(3)发生条件
①复分解反应类型。
②氧化还原反应类型。
如FeCl 溶液与Cu反应的离子方程式为________________________________。
3
2.离子方程式
(1)离子方程式:用______________________来表示反应的式子。
(2)离子方程式的意义
离子方程式不仅可以表示____________________,还可以表示__________________。
3.离子方程式的书写步骤
书写步骤(以CaCO 与盐酸的反应为例)
3
[判断] (正确的打“√”,错误的打“×”)
(1)向水中加入一小块钠:Na+2HO===Na++2OH-+H↑( )
2 2(2)NaO固体与水反应:O2-+HO===2OH-( )
2 2
(3)醋酸溶液与水垢中的CaCO 反应:CaCO+2H+===Ca2++HO+CO↑( )
3 3 2 2
(4)Fe(OH) 和稀硫酸的反应:OH-+H+===HO( )
3 2
(5)硫酸铜溶液跟氢氧化钡溶液反应:Ba2++S ===BaSO↓( )
O2− 4
4
(6)澄清石灰水与稀盐酸反应:H++OH-===HO( )
2
(7)Fe和稀盐酸反应:2Fe+6H+===2Fe3++3H↑( )
2
(8)向NHCl溶液中滴入烧碱溶液并加热:N +OH-=====NH·HO( )
4 H+ 3 2
4
(9)向NaClO溶液中通入少量SO:2ClO-+SO+HO===2HClO+S ( )
2 2 2 O2−
3
[提醒]
书写离子方程式时特殊情况的处理
特殊情况 处理方式 举例
澄清石灰水和盐酸反应:
微溶性反应物呈澄清溶液形式 拆写成离子符号
OH-+H+===HO
2
用石灰乳制漂白粉的反应:
微溶性生成物或反应物呈悬浊液
形式 写化学式 Ca(OH) 2 +Cl 2 ===Ca2++Cl-+ClO-
+HO
2
硫酸铝溶液中加入氨水:
氨水为反应物和不加热的稀溶液
写成NH·HO Al3++3NH·HO===Al(OH)↓+
中的生成物 3 2 3 2 3
3NH+
4
氨水为加热条件或浓溶液中的生 浓NaOH溶液中加入硫酸铵固体并
成物 写成NH 3 ↑+H 2 O 加热OH-+NH+ =====NH↑+HO
4 3 2
2对点速练
练点一 单一反应离子方程式的书写
1.完成下列反应的离子方程式
(1)MnO 与浓盐酸反应制Cl:
2 2
_________________________________________。
(2)NaS水溶液在空气中被氧化变质:
2
_________________________________________。
(3)明矾溶于水产生Al(OH) 胶体:
3
_________________________________________。(4)NaO 溶于水:
2 2
_________________________________________。
(5)浓盐酸与铁屑反应:
_________________________________________。
(6)钠与CuSO 溶液反应:
4
_________________________________________。
练点二 多重反应离子方程式的书写
2.完成下列反应的离子方程式
(1)Ba(OH) 溶液与(NH)SO 溶液混合:
2 4 2 4
__________________________________________。
(2)CuSO 溶液与Ba(OH) 溶液混合:
4 2
__________________________________________。
(3)NHHCO 与过量NaOH溶液混合:
4 3
__________________________________________。
(4)Ba(OH) 与HSO 两稀溶液混合:
2 2 4
__________________________________________。
(5)Fe(OH) 溶于HI溶液中:
3
__________________________________________。
练点三 “限定条件”离子方程式的书写
3.(1)Ca(HCO) 溶液与NaOH溶液反应
3 2
①NaOH不足:___________________________________;
②NaOH过量:___________________________。
(2)NaHCO 溶液与Ca(OH) 溶液反应
3 2
①NaHCO 不足:____________________________;
3
②NaHCO 过量:___________________________。
3
(3)Ba(OH) 溶液与NaHSO 溶液的反应
2 4
①溶液呈中性时:___________________________;
②溶液呈碱性时:___________________________。
4.(1)①FeBr 溶液中通入少量Cl:
2 2
___________________________;
②FeBr 溶液中通入与其等物质的量的氯气:
2___________________________;
③FeBr 溶液中通入足量Cl:
2 2
___________________________。
(2)①少量铁粉加入到足量稀硝酸中:
___________________________;
②n(Fe)∶n[HNO(稀)]=1∶3:
3
___________________________;
③足量铁粉加入到少量稀硝酸中:
___________________________。
练点四 “信息型”离子方程式的书写
5.利用硫酸渣(主要含FeO 、FeO,杂质为AlO 和SiO 等)生产铁基颜料铁黄(FeOOH)
2 3 2 3 2
的制备流程如下:
(1)“酸溶”时,FeO 与硫酸反应的化学方程式为______________________________。
2 3
(2)滤渣Ⅰ的主要成分是FeS 、S和________(填化学式);Fe3+被FeS 还原的离子方程
2 2
式为________________。
(3)“ 氧 化 ” 中 , 生 成 FeOOH 的 离 子 方 程 式 为
________________________________________。
(4)滤液Ⅱ中溶质是Al(SO) 和________(填化学式):“洗涤”时,检验铁黄表面已
2 4 3
洗涤干净的操作是________________________________________________。
练点五 离子方程式正误判断
6.下列指定反应的离子方程式正确的是 ( )
A.钠与水反应:Na+2HO===Na++2OH-+H↑
2 2
B.电解饱和食盐水获取烧碱和氯气: 2Cl-+2HO=====H↑+Cl↑+2OH-
2 2 2
C.向氢氧化钡溶液中加入稀硫酸: Ba2++OH-+H++S ===BaSO↓+HO
O2− 4 2
4
D.向碳酸氢铵溶液中加入足量石灰水: Ca2++H +OH-===CaCO↓+HO
O− 3 2
3
7.下列表示对应化学反应的离子方程式正确的是( )A.向稀HNO 中滴加NaSO 溶液:S +2H+===SO↑+HO
3 2 3 O2− 2 2
3
B.向NaSiO 溶液中通入过量SO:Si +SO+HO===HSiO↓+S
2 3 2 O2− 2 2 2 3 O2−
3 3
C.向Al(SO) 溶液中加入过量NH·HO:Al3++4NH·HO===[Al(OH)]-+4
2 4 3 3 2 3 2 4 H+
4
D.向CuSO 溶液中加入NaO:2NaO+2Cu2++2HO===4Na++2Cu(OH)↓+O↑
4 2 2 2 2 2 2 2
8.下列指定反应的离子方程式正确的是( )
A.向KCO 溶液中通入过量SO:
2 3 2
C +2SO+HO===CO+2HS
O2− 2 2 2 O−
3 3
B.Fe与稀醋酸反应:Fe+2H+===Fe2++H↑
2
C.在强碱溶液中NaClO与FeCl 反应生成NaFeO:
3 2 4
3ClO-+2Fe3++5HO===2Fe +3Cl-+10H+
2 O2−
4
D.用新制Cu(OH) 悬浊液检验乙醛中的醛基:
2
CHCHO+Cu(OH)+OH-――→CHCOO-+Cu+2HO
3 2 3 2
练后归纳
离子方程式正误判断的审题要点本讲真题研练
1.[2020·全国卷Ⅲ,11]对于下列实验,能正确描述其反应的离子方程式是( )
A.用NaSO 溶液吸收少量Cl:3S +Cl+HO===2HS +2Cl-+S
2 3 2 O2− 2 2 O− O2−
3 3 4
B.向CaCl 溶液中通入CO:Ca2++HO+CO===CaCO↓+2H+
2 2 2 2 3
C.向HO 溶液中滴加少量FeCl:2Fe3++HO===O↑+2H++2Fe2+
2 2 3 2 2 2
D.同浓度同体积NHHSO 溶液与NaOH溶液混合:N +OH-===NH·HO
4 4 H+ 3 2
4
2.[2020·江苏卷,7]下列指定反应的离子方程式正确的是( )
A.Cl
2
通入水中制氯水:Cl
2
+H
2
O2H++Cl-+ClO-
B.NO 通入水中制硝酸:2NO+HO===2H++N +NO
2 2 2 O−
3
C.0.1 mol·L-1 NaAlO 溶液中通入过量CO:Al +CO+2HO===Al(OH)↓+HC
2 2 O− 2 2 3 O−
2 3
D.0.1 mol·L-1 AgNO 溶液中加入过量浓氨水:Ag++NH+HO===AgOH↓+N
3 3 2 H+
4
3.[2020·浙江7月,13]能正确表示下列反应的离子方程式是( )
A.(NH)Fe(SO) 溶液与少量Ba(OH) 溶液反应:S +Ba2+===BaSO↓
4 2 4 2 2 O2− 4
4
B.电解MgCl 水溶液:2Cl-+2HO=====2OH-+Cl↑+H↑
2 2 2 2
C.乙酸乙酯与NaOH溶液共热:CHCOOCHCH+OH-――→CHCOO-+CHCHOH
3 2 3 3 3 2
D.CuSO 溶液中滴加稀氨水:Cu2++2OH- ===Cu(OH)↓
4 2
4.[2019·全国卷Ⅰ,10]固体界面上强酸的吸附和离解是多相化学在环境、催化、材
料科学等领域研究的重要课题。下图为少量 HCl气体分子在253 K冰表面吸附和溶解过程的
示意图。下列叙述错误的是( )A.冰表面第一层中,HCl以分子形式存在
B.冰表面第二层中,H+浓度为5×10-3mol·L-1(设冰的密度为0.9 g·cm-3)
C.冰表面第三层中,冰的氢键网络结构保持不变
D.冰表面各层之间,均存在可逆反应HClH++Cl-
5.[2019·天津卷,2]下列离子方程式能用来解释相应实验现象的是( )
实验现象 离子方程式
A
向氢氧化镁悬浊液中滴加氯化铵溶 Mg(OH)+2NH+
===Mg2++2NH·HO
液,沉淀溶解 2 4 3 2
向沸水中滴加饱和氯化铁溶液得到红
B Fe3++3HO===Fe(OH)↓+3H+
褐色液体 2 3
3SO+2MnO− +4H+===3SO2− +2Mn2++
C 二氧化硫使酸性高锰酸钾溶液褪色 2 4 4
2HO
2
D 氧化亚铁溶于稀硝酸 FeO+2H+===Fe2++HO
2
6.[2019·江苏卷,7]下列指定反应的离子方程式正确的是( )
A.室温下用稀NaOH溶液吸收Cl:Cl+2OH-===ClO-+Cl-+HO
2 2 2
B.用铝粉和NaOH溶液反应制取少量H:Al+2OH-===Al +H↑
2 O− 2
2
C.室温下用稀HNO 溶解铜:Cu+2N +2H+===Cu2++2NO↑+HO
3 O− 2 2
3
D.向NaSiO 溶液中滴加稀盐酸:NaSiO+2H+===HSiO↓+2Na+
2 3 2 3 2 3
7.[2019·浙江4月,13]不能正确表示下列变化的离子方程式是( )
A.二氧化硫与酸性高锰酸钾溶液反应:5SO+2HO+2Mn ===2Mn2++5S +4H+
2 2 O− O2−
4 4
B.酸性碘化钾溶液中滴加适量双氧水:2I-+2H++HO===I+2HO
2 2 2 2
C.硅酸钠溶液和盐酸反应:Si +2H+===HSiO↓
O2− 2 3
3
D.硫酸铜溶液中加少量的铁粉:3Cu2++2Fe===2Fe3++3Cu
第2讲 离子反应
考点一
1知识梳理1.水溶液中 熔融状态下 强电解质 弱电解质
2.水溶液中或熔融
3.(1)=== NaSO===2Na++S
⇌ 2 4 O2−
4
HClO H++ClO-
⇌
(2)HCO H++HC
2 3⇌ O−
3
HC H++C
O−⇌ O2−
3 3
Fe(OH) Fe3++3OH-
3⇌
(3)NaHSO===Na++H++S
4 O2−
4
NaHCO===Na++HC
3 O−
3
HC H++C
O−⇌ O2−
3 3
判断 答案:(1)× (2)√ (3)× (4)× (5)× (6)× (7)× (8)× (9)×
(10)×
2对点速练
1.答案:A
2.答案:(1)②⑥ (2)③ (3)⑦⑧⑨⑪ (4)⑧⑪ (5)④⑤ 10 (6)①⑫
3.答案:(1)HSO===2H++S
2 4 O2−
4
(2)HCO H++HC 、HC H++C
2 3⇌ O− O−⇌ O2−
3 3 3
(3)Ca(OH)===Ca2++2OH-
2
(4)Fe(OH) Fe3++3OH-
3⇌
(5)NH·HO N +OH-
3 2 ⇌ H+
4
(6)NaCl===Na++Cl-
(7)BaSO===Ba2++S
4 O2−
4
(8)NaHSO===Na++H++S
4 O2−
4(9)NaHCO===Na++HC 、HC H++C
3 O− O−⇌ O2−
3 3 3
(10)CHCOOH CHCOO-+H+
3 ⇌ 3
4.答案:(1)② (2)0.5
考点二
1知识梳理
1.(1)在溶液中有离子参加 (2)浓度 (3)难溶 难电离 挥发性 2Fe3++Cu===2Fe2
++Cu2+
2.(1)实际参加反应的离子符号 (2)某一个具体的化学反应 同一类型的离子反应
3.CaCO +2HCl===CaCl +HO+CO↑ CaCO +2H++2Cl-===Ca2++2Cl-+HO+CO↑
3 2 2 2 3 2 2
CaCO+2H+===Ca2++HO+CO↑ 原子
3 2 2
判断 答案:(1)× (2)× (3)× (4)× (5)× (6)√ (7)× (8)× (9)×
2对点速练
1.答案:(1)MnO+4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(2)2S2-+O+2HO===2S↓+4OH-
2 2
(3)Al3++3HO Al(OH)(胶体)+3H+
2 ⇌ 3
(4)2NaO+2HO===4Na++4OH-+O↑
2 2 2 2
(5)Fe+2H+===Fe2++H↑
2
(6)2Na+Cu2++2HO===Cu(OH)↓+2Na++H↑
2 2 2
2.答案:(1)Ba2++2OH-+2N +S ===BaSO↓+2NH·HO
H+ O2− 4 3 2
4 4
(2)Cu2++S +Ba2++2OH-===BaSO↓+Cu(OH)↓
O2− 4 2
4
(3)N +HC +2OH-===NH·HO+C +HO
H+ O− 3 2 O2− 2
4 3 3
(4)Ba2++2OH-+2H++S ===BaSO↓+2HO
O2− 4 2
4
(5)2Fe(OH)+6H++2I-===2Fe2++6HO+I
3 2 2
3.答案:(1)①Ca2++HC +OH-===CaCO↓+HO
O− 3 2
3
②Ca2++2HC +2OH-===CaCO↓+2HO+C
O− 3 2 O2−
3 3(2)①HC +OH-+Ca2+===CaCO↓+HO
O− 3 2
3
②Ca2++2OH-+2HC ===CaCO↓+C +2HO
O− 3 O2− 2
3 3
(3)①Ba2++2OH-+2H++S ===BaSO↓+2HO
O2− 4 2
4
②S +H++OH-+Ba2+===BaSO↓+HO
O2− 4 2
4
4.答案:(1)①2Fe2++Cl===2Fe3++2Cl-
2
②2Fe2++2Br-+2Cl===2Fe3++Br+4Cl-
2 2
③2Fe2++4Br-+3Cl===2Fe3++2Br+6Cl-
2 2
(2)①Fe+4H++N ===Fe3++NO↑+2HO
O− 2
3
②4Fe+12H++3N ===3Fe2++Fe3++3NO↑+6HO
O− 2
3
③3Fe+8H++2N ===3Fe2++2NO↑+4HO
O− 2
3
5.解析:(2)硫酸渣加硫酸酸溶,得Fe3+、Fe2+、Al3+的溶液,加FeS 还原Fe3+,
2
SiO 不溶于酸,滤渣Ⅰ中还有SiO 。反应物为Fe3+、FeS(硫显-1价,铁显+2价),生成物
2 2 2
有Fe2+(Fe3+被还原为Fe2+)、S(滤渣Ⅰ成分之一),根据得失电子守恒配平。(3)滤液Ⅰ中主
要含Fe2+、Al3+,通入空气氧化Fe2+为Fe3+,加氨水调节pH 3~4,沉淀Fe3+。反应物为Fe2
+、O 、NH·HO,生成物有 FeOOH、N ,根据得失电子守恒有:4Fe2++NH·HO+
2 3 2 H+ 3 2
4
O―→4FeOOH↓+N ,根据电荷守恒配N :4Fe2++8NH·HO+O―→4FeOOH↓+8N ,
2 H+ H+ 3 2 2 H+
4 4 4
根据原子守恒补水。(4)由(3)中反应可判断滤液Ⅱ中溶质为Al(SO) 、(NH)SO 。由滤液Ⅱ
2 4 3 4 2 4
成分可知铁黄表面可溶性杂质是Al(SO)、(NH)SO,若洗涤干净,则洗涤液中无S 。
2 4 3 4 2 4 O2−
4
答案:(1)FeO+3HSO===Fe(SO)+3HO
2 3 2 4 2 4 3 2
(2)SiO 2Fe3++FeS===3Fe2++2S
2 2
(3)4Fe2++8NH·HO+O===4FeOOH↓+8N +2HO
3 2 2 H+ 2
4
(4)(NH)SO 取最后一次洗涤液,先加入稀盐酸酸化,再加入 BaCl 溶液,若无白色
4 2 4 2沉淀,说明已洗涤干净
6.解析:A项,电荷不守恒,正确的为:2Na+2HO===2Na++2OH-+H↑,错误;C项,
2 2
正确的为:Ba2++2OH-+2H++S ===BaSO↓+2HO;D项,Ca(OH) 过量,N 也反应,正
O2− 4 2 2 H+
4 4
确的为:N +HC +Ca2++2OH-===CaCO↓+NH·HO+HO。
H+ O− 3 3 2 2
4 3
答案:B
7.解析:稀硝酸有强氧化性,会将S 氧化,A错误;因通入的SO 过量,故生成的
O2− 2
3
是HS ,不是S ,B错误;Al(OH) 不溶于NH·HO,C中正确的离子方程式应为Al3++
O− O2− 3 3 2
3 3
3NH·HO===Al(OH)↓+3N ,C错误;向CuSO 溶液中加入NaO ,先发生反应的离子方程
3 2 3 H+ 4 2 2
4
式为 2NaO +2HO===4Na++4OH-+O↑,再发生反应的离子方程式为 Cu2++2OH-
2 2 2 2
===Cu(OH)↓,整理后可得出D中的离子方程式,D正确。
2
答案:D
8.解析:A项,SO 过量,生成HS ,正确;B项,醋酸是弱酸,不能拆成离子形式,
2 O−
3
错误;C项,碱性溶液,不能生成H+,错误;D项,醛基将Cu(OH) 还原为CuO,不是Cu,错
2 2
误。
答案:A
本讲真题研练
1.解析:设少量Cl 为1 mol,根据得失电子守恒可知,1 mol Cl 消耗1 mol S
2 2 O2−
3
:Cl+S +HO===2Cl-+S +2H+,由于S 过量,继续消耗产生的H+生成HS ,故
2 O2− 2 O2− O2− O−
3 4 3 3
总反应的离子方程式为3S +Cl +HO===2HS +2Cl-+S ,A项正确;将离子方程式
O2− 2 2 O− O2−
3 3 4
写为化学方程式,可知是HCO 制得HCl,不符合强酸制弱酸规律,B项错误;加入的少量Fe3
2 3
+对HO 的分解起催化作用,催化机理为2Fe3++HO===O↑+2H++2Fe2+和HO+2Fe2++2H+
2 2 2 2 2 2 2===2Fe3++2HO,C项错误;由电离方程式NHHSO===N +H++S 可知,OH-先与H+反应,
2 4 4 H+ O2−
4 4
再与N 反应,故同浓度同体积两种溶液混合,发生的反应为H++OH-===HO,D项错误。
H+ 2
4
答案:A
2.解析:本题考查离子方程式的正误判断,考查的化学学科核心素养是变化观念与平
衡思想。HClO为弱电解质,在离子方程式中不能拆开,A项错误;B项电荷不守恒,正确的
离子方程式为3NO +HO===2H++2N +NO,B项错误;CO 过量,生成HC ,C项正确;
2 2 O− 2 O−
3 3
AgOH不能稳定存在,正确的离子方程式为Ag++2NH===[Ag(NH)]+,D项错误。
3 3 2
答案:C
3.解析:本题考查离子方程式的书写,考查的化学核心素养是宏观辨识与微观探析。
硫酸亚铁铵与少量氢氧化钡反应的离子方程式为 Fe2++S +Ba2++2OH-===Fe(OH)↓+
O2− 2
4
BaSO↓,A项错误;电解MgCl 水溶液的离子方程式为Mg2++2Cl-+2HO=====Mg(OH)↓+
4 2 2 2
H↑+Cl↑,B项错误;乙酸乙酯在氢氧化钠条件下水解得到乙酸钠和乙醇,C项正确;一水
2 2
合氨是弱碱,书写离子方程式时不能拆写,应为Cu2++2NH·HO===Cu(OH)↓+2N ,D项
3 2 2 H+
4
错误。
答案:C
4.解析:由图可知,在冰表面第一层氯化氢以分子形式存在,在第二层氯化氢以离子
形式存在,而第三层只有水分子,则在第一、二层之间存在可逆反应:HCl H++Cl-,A、C
⇌
项正确,D项错误:1 L冰中水的物质的量为0.9 g·cm-3×1 000 mL=50 mol,第二层
18 g·mol-1
n(Cl−)
中,n(Cl-)∶n(HO)=10-4∶1,n(Cl-)=5×10-3 mol,则c(H+)=c(Cl-)= =
2
V
5×10-3 mol
=5×10-3 mol·L-1,B项正确。
1 L
答案:D
5.解析:本题涉及离子方程式的书写及正误判断,通过实验现象分析发生的反应,考查分析和解决化学问题的能力,体现证据推理与模型认知的学科核心素养。
A项,悬浊液中存在平衡:Mg(OH)(s) Mg2+(aq)+2OH-(aq),加入NHCl溶液后,N
2 ⇌ 4
与OH-结合成NH·HO,平衡正向移动而使沉淀逐渐溶解,正确;B项,红褐色液体是
H+ 3 2
4
Fe(OH) 胶体,不是沉淀,错误;C项,得失电子不守恒,电荷不守恒,错误;D项,稀硝酸
3
具有强氧化性,可将Fe2+氧化为Fe3+,错误。
答案:A
6.解析:本题涉及的考点有离子方程式的正误判断、元素及其化合物的性质,通过离
子方程式正误判断的形式考查了学生对知识的识记、再现、辨认能力,体现了以宏观辨识与
微观探析为主的学科核心素养。
A项,Cl 能与NaOH溶液反应生成NaCl、NaClO和水,离子方程式为Cl +2OH-===ClO-
2 2
+Cl-+HO,正确;B项,铝粉能与 NaOH溶液反应制取 H ,离子方程式为 2Al+2OH-+
2 2
2HO===2Al +3H↑,错误;C项,铜与稀硝酸反应生成NO,离子方程式为3Cu+8H++2N
2 O− 2
2
===3Cu2++2NO↑+4HO,错误;D 项,NaSiO 易溶于水,应用离子符号表示,故向
O− 2 2 3
3
NaSiO 溶液中滴加稀盐酸发生反应的离子方程式为Si +2H+===HSiO↓,错误。
2 3 O2− 2 3
3
答案:A
7.解析:硫酸铜溶液中加少量的铁粉:Cu2++Fe===Fe2++Cu,D错误。
答案:D