文档内容
第4讲 铜及其化合物 金属资源
[考纲要求]
1.掌握铜及其重要化合物的主要性质及其应用。
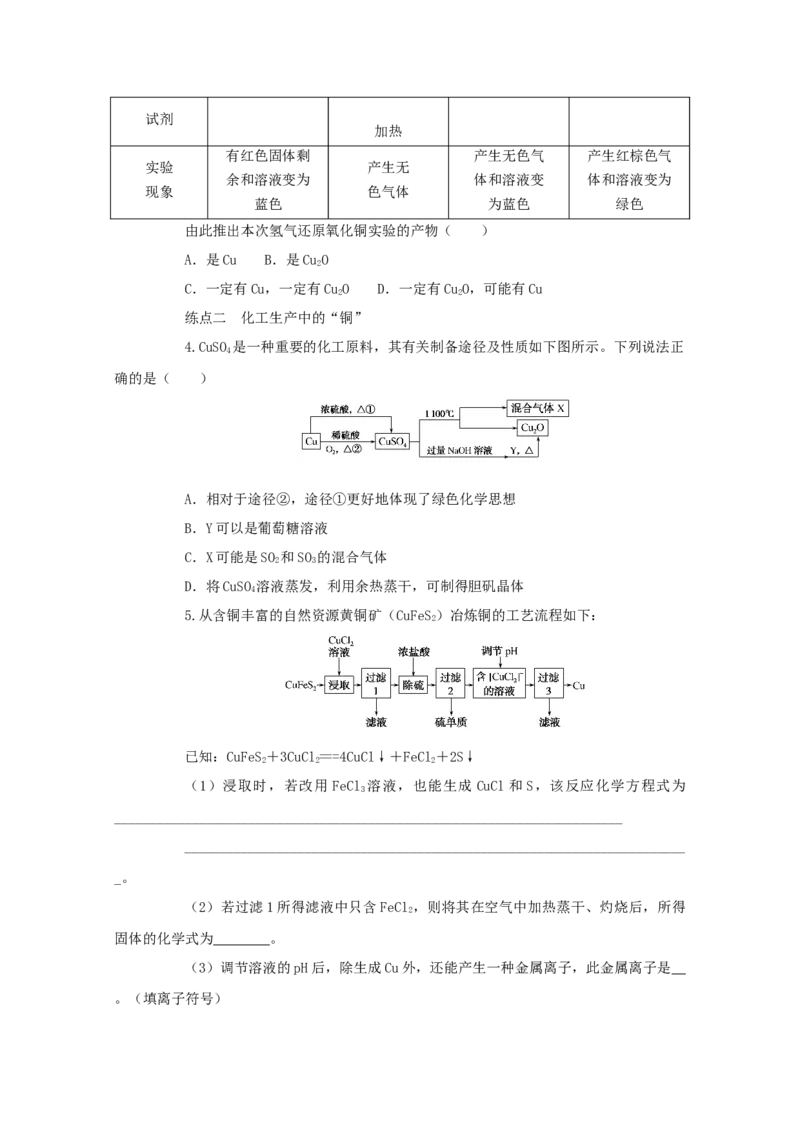
2.了解常见金属活动顺序。
3.了解合金的概念及其重要应用。
考点一 铜及其重要化合物
知识梳理
1.铜的性质
(1)物理性质:铜是 色金属,具有良好的 性、 性和延
展性。
(2)化学性质
写出图中有关反应的化学方程式或离子方程式:
①化学方程式: ( 固体)。
②化学方程式: 。
③与氧化性酸
a.与浓硫酸共热: ;
b. 与 稀 硝 酸 反 应 的 离 子 方 程 式 :
;
c . 与 浓 硝 酸 反 应 的 离 子 方 程 式 :
。
2.氧化铜和氧化亚铜
名称 氧化铜 氧化亚铜
颜色 黑色 砖红色
与酸反
CuO+2H+===Cu2++Cu+HO
2 2
应(H+)与H 反应
2
转化关系
3.氢氧化铜
(1)物理性质: 色 溶于水的固体。
(2)化学性质及应用
4.铜盐
(1)铜盐溶液有毒,主要是因为Cu2+作为一种重金属离子能与蛋白质作用,使
蛋白质变性失去生理活性,因此可将胆矾、熟石灰、水配成波尔多液,用来杀灭植物的病毒。
(2)CuSO·5HO俗称 。
4 2
可发生CuSO4·5H2O CuSO4+5HO,无水CuSO 遇水变蓝色,可用于检验
2 4
水的存在。
(3)Cu(OH)CO:名称为 ,是铜绿、孔雀石的主要成分。
2 2 3
[判断] (正确的打“√”,错误的打“×”)
(1)过量的铜与浓硝酸反应一定没有一氧化氮生成( )
(2)利用无水硫酸铜遇水变成蓝色这一性质,来检验水的存在( )
(3)将铁片置于 CuSO 溶液中,铁片上有红色物质析出,说明铁比铜活泼
4
( )
(4)铜在干燥的空气中性质稳定,但是在潮湿的环境中则易被锈蚀,生成铜绿(
)
(5)铜与氯气、氧气、硫分别反应,得到的产物中铜的化合价均为+2 价
( )
(6)湿法炼铜和火法炼铜的反应中,铜元素都发生了还原反应( )
(7)CuO是黑色固体,与水反应可生成Cu(OH)( )
2(8)CuO遇硝酸会被氧化成Cu2+( )
2
(9)Cu(OH)CO 是铜锈的主要成分,在干燥的空气中不易生成( )
2 2 3
(10)无水硫酸铜生成CuSO·5HO属于物理变化( )
4 2
(11)铜绿在灼烧条件下会分解生成氢氧化铜和二氧化碳( )
[提醒]
1.铜及其化合物的颜色
物质 颜色 物质 颜色
Cu 紫红色 CuSO 白色
4
CuO 黑色 CuSO·5HO 蓝色
4 2
CuO 砖红色 Cu(OH)CO 绿色
2 2 2 3
CuS 黑色 Cu(OH) 蓝色
2 2
2.无水CuSO 只能作为水的检验试剂,但不能作为水蒸气的吸收试剂用于除杂。
4
对点速练
练点一 铜及其化合物的性质
1.我国晋代《抱朴子》中描述了大量的化学反应,其中有:①“丹砂(HgS)烧之
成水银,积变又还成丹砂”;②“以曾青涂铁,铁赤色如铜”。下列有关叙述正确的是(
)
A.①中描述的化学反应是可逆反应
B.“曾青”是含有Cu2+的溶液,如硫酸铜溶液
C.“积变又还成丹砂”中的“还”可理解为“被还原”
D.水银能跟曾青发生置换反应生成单质铜
2.某同学通过系列实验,探究Cu及其化合物的性质,下列操作正确且能达到目的
的是( )
A.将铜粉和硫粉混合均匀加热以制取CuS
B.将Cu片放入过量浓硫酸中,一段时间后加水以观察CuSO 溶液的颜色
4
C.向CuSO 溶液中加入NaOH溶液,过滤洗涤并收集沉淀,加热以制取CuO
4
D.设计Cu-Al-浓硝酸原电池,以证明金属活动性:Cu