文档内容
第1讲 化学能与热能
[考纲要求]
1.了解化学反应中能量转化的原因,能说出常见的能量转化形式。
2.了解化学能与热能的相互转化。了解吸热反应、放热反应、反应热等概念。
3.了解热化学方程式的含义,能正确书写热化学方程式。
4.了解焓变与反应热的含义。了解ΔH=H(反应产物)-H(反应物)表达式的含义。
5.理解盖斯定律,并能运用盖斯定律进行有关反应焓变的计算。
6.了解能源是人类生存和社会发展的重要基础。了解化学在解决能源危机中的重要作
用。
考点一 反应热和热化学方程式
1知识梳理
1.化学反应中的能量变化
(1)化学反应中的两大变化:____变化和____变化。
(2)化学反应中的两大守恒:____守恒和____守恒。
(3)化学反应中的能量转化形式:____、光能、电能等。通常主要表现为____的变化。
2.反应热、焓变
(1)反应热
在化学反应过程中__________________通常叫做反应热。
(2)焓变
生成物与反应物的焓值差。
恒压条件下,化学反应的______等于焓变。
(3)符号:____。
(4)单位:______或________。
3.吸热反应和放热反应
(1)从能量高低角度理解
ΔH<0,放热反应 ΔH>0,吸热反应(2)从化学键角度理解
ΔH=E(反应物键能)-E(生成物键能)
1 2
若EE,ΔH>0,吸热反应
1 2
4.热化学方程式概念及意义
(1)表示参加反应________和______关系的化学方程式。
(2)热化学方程式的意义
表明了化学反应中的________变化和________变化。
如:C(s)+O(g)===CO(g) ΔH=-393.5 kJ·mol-1
2 2
表示在 25 ℃,101 kPa 时,__________________生成____________,同时放出
____________。
5.热化学方程式书写步骤
[判断] (正确的打“√”,错误的打“×”)
(1)物质发生化学变化都伴有能量的变化( )
(2)放热反应不需要加热就能反应,吸热反应不加热就不能反应( )
(3)同温同压下,反应H(g)+Cl(g)===2HCl(g)在光照和点燃条件下的ΔH不同( )
2 2
(4)可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关( )
(5)C(石墨,s)===C(金刚石,s) ΔH>0,说明石墨比金刚石稳定( )
(6)2HO(l)===2H(g)+O(g)的焓变ΔH>0( )
2 2 2
1
(7)H(g)+ O(g)===HO(l) ΔH和2H(g)+O(g)===2HO(l) ΔH中的ΔH=ΔH(
2 2 2 2 1 2 2 2 2 1 2)
1 1
(8)H(g)+ O(g)===HO(g) ΔH和HO(g)===H(g)+ O(g) ΔH中的ΔH=ΔH(
2 2 2 2 1 2 2 2 2 2 1 2
)
[提醒]
常见的放热反应和吸热反应
1.放热反应:①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟酸的
置换反应;⑤物质的缓慢氧化等。
2.吸热反应:①大多数分解反应;②盐的水解和弱电解质的电离;③ Ba(OH)·8HO
2 2
与NHCl反应;④碳和水蒸气、C和CO 的反应等。
4 2
2对点速练
练点一 化学反应历程与能量变化
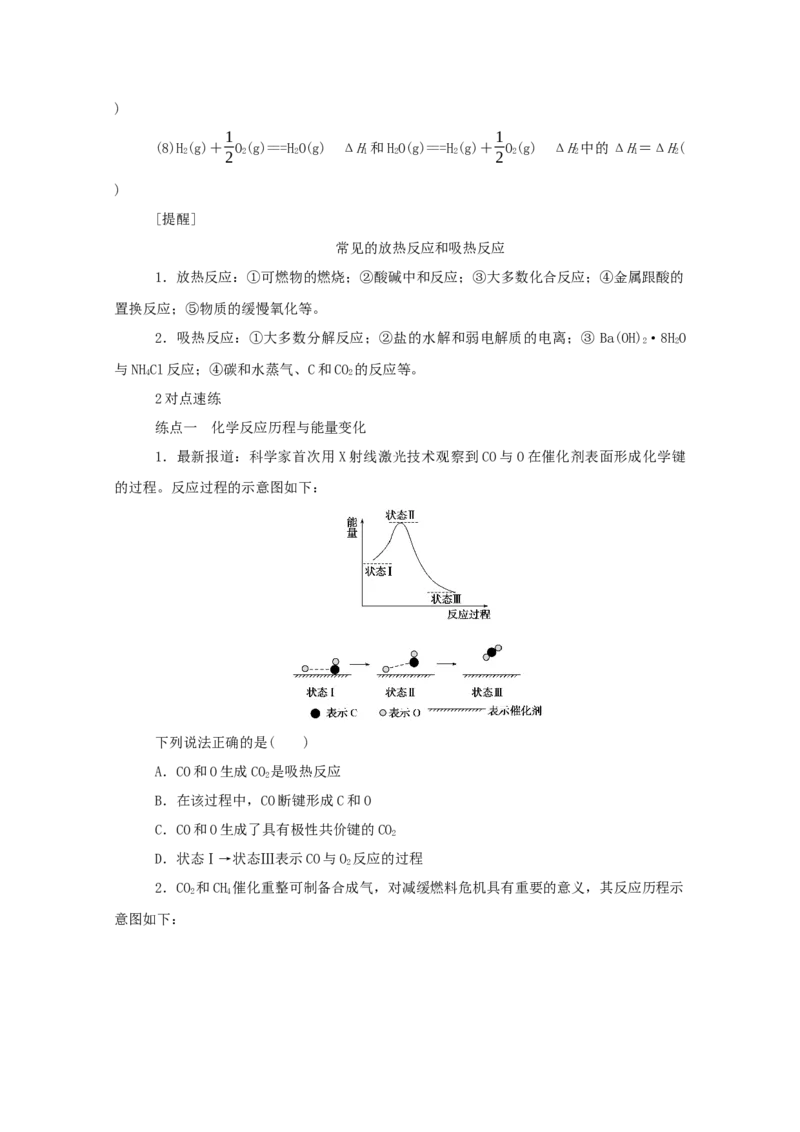
1.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键
的过程。反应过程的示意图如下:
下列说法正确的是( )
A.CO和O生成CO 是吸热反应
2
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO
2
D.状态Ⅰ→状态Ⅲ表示CO与O 反应的过程
2
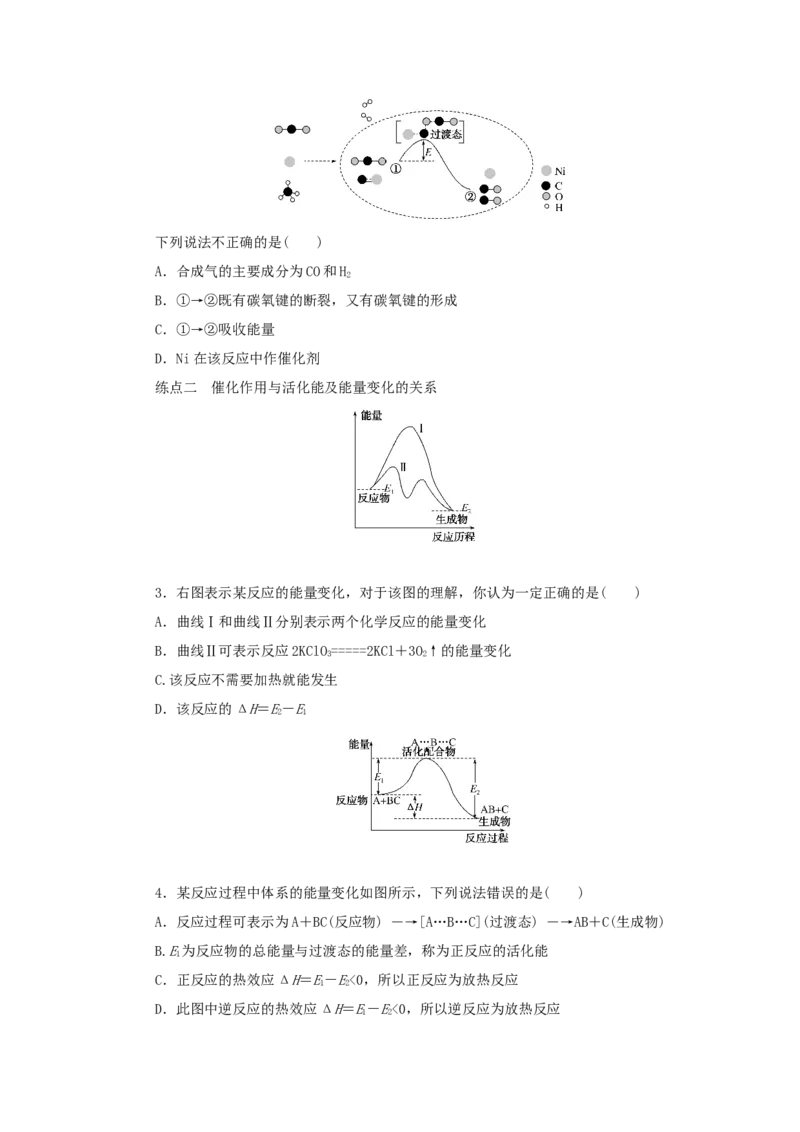
2.CO 和CH 催化重整可制备合成气,对减缓燃料危机具有重要的意义,其反应历程示
2 4
意图如下:下列说法不正确的是( )
A.合成气的主要成分为CO和H
2
B.①→②既有碳氧键的断裂,又有碳氧键的形成
C.①→②吸收能量
D.Ni在该反应中作催化剂
练点二 催化作用与活化能及能量变化的关系
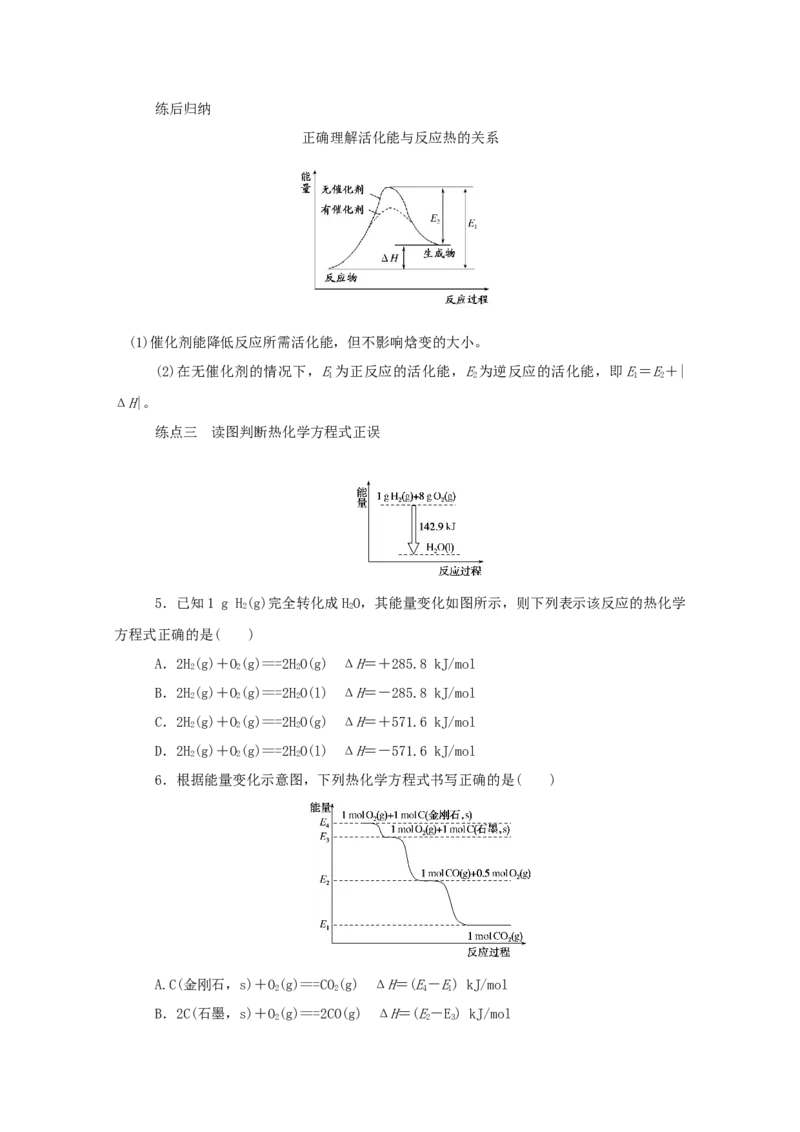
3.右图表示某反应的能量变化,对于该图的理解,你认为一定正确的是( )
A.曲线Ⅰ和曲线Ⅱ分别表示两个化学反应的能量变化
B.曲线Ⅱ可表示反应2KClO=====2KCl+3O↑的能量变化
3 2
C.该反应不需要加热就能发生
D.该反应的ΔH=E-E
2 1
4.某反应过程中体系的能量变化如图所示,下列说法错误的是( )
A.反应过程可表示为A+BC(反应物) ―→[A…B…C](过渡态) ―→AB+C(生成物)
B.E为反应物的总能量与过渡态的能量差,称为正反应的活化能
1
C.正反应的热效应ΔH=E-E<0,所以正反应为放热反应
1 2
D.此图中逆反应的热效应ΔH=E-E<0,所以逆反应为放热反应
1 2练后归纳
正确理解活化能与反应热的关系
(1)催化剂能降低反应所需活化能,但不影响焓变的大小。
(2)在无催化剂的情况下,E为正反应的活化能,E为逆反应的活化能,即E=E+|
1 2 1 2
ΔH|。
练点三 读图判断热化学方程式正误
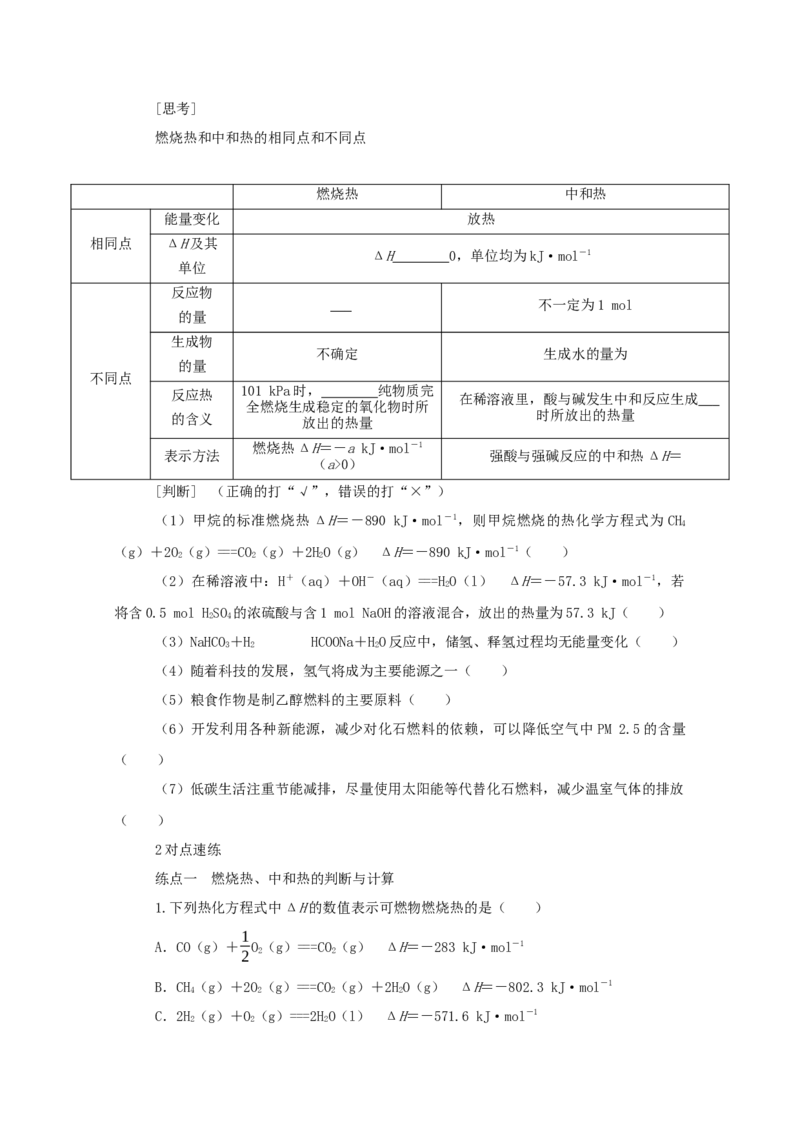
5.已知1 g H (g)完全转化成HO,其能量变化如图所示,则下列表示该反应的热化学
2 2
方程式正确的是( )
A.2H(g)+O(g)===2HO(g) ΔH=+285.8 kJ/mol
2 2 2
B.2H(g)+O(g)===2HO(l) ΔH=-285.8 kJ/mol
2 2 2
C.2H(g)+O(g)===2HO(g) ΔH=+571.6 kJ/mol
2 2 2
D.2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ/mol
2 2 2
6.根据能量变化示意图,下列热化学方程式书写正确的是( )
A.C(金刚石,s)+O(g)===CO(g) ΔH=(E-E) kJ/mol
2 2 4 1
B.2C(石墨,s)+O(g)===2CO(g) ΔH=(E-E) kJ/mol
2 2 3C.C(石墨,s)=C(金刚石,s) ΔH=(E-E) kJ/mol
3 4
D.2CO(g)===2CO(g)+O(g) ΔH=2(E-E) kJ/mol
2 2 2 1
练点四 信息型热化学方程式的书写
7.写出满足下列给定信息条件的热化学方程式:
(1)101 kPa时,1 mol CH 完全燃烧生成液态水和CO 气体,放出890.3 kJ的热量,反
4 2
应的热化学方程式:________________________________。
(2)0.3 mol乙硼烷(分子式BH)在氧气中燃烧,生成固态三氧化二硼和液态水,放出
2 6
649.5 kJ 的 热 量 , 则 其 热 化 学 方 程 式 为
________________________________________________________________________。
(3)已知1 mol Na的单质在足量O 中燃烧,恢复至室温,放出255.5 kJ热量,写出该
2
反 应 的 热 化 学 方 程 式 :
________________________________________________________________________
________________________________________________________________________。
(4)在25 ℃、101 kPa下,已知SiH 气体在氧气中完全燃烧后恢复至原状态,平均每
4
转 移 1 mol 电 子 放 出 190.0 kJ 的 热 量 , 该 反 应 的 热 化 学 方 程 式 为
________________________________________________________________________
________________________________________________________________________。
(5)化学反应N+3H 2NH 的能量变化如下图所示(假设该反应反应完全)。
2 2⇌ 3
写 出 N(g) 和 H(g) 反 应 生 成 NH(l) 的 热 化 学 方 程 式 :
2 2 3
________________________________________________________________________。
(6)下图是1 mol NO 和1 mol CO反应生成CO 和NO过程中能量变化示意图,写出NO
2 2 2
和 CO 反 应 的 热 化 学 方 程 式 :
________________________________________________________________________
________________________________________________________________________。方法总结
“五审”法突破热化学方程式的正误判断
考点二 燃烧热、中和热、能源
1知识梳理
1.燃烧热
(1)概念:在101 kPa时, 纯物质完全燃烧生成稳定的氧化物时所放出的热量,
叫做该物质的燃烧热。
其中的“完全燃烧”,是指物质中下列元素完全转变成对应的氧化物:C→ ,
H→ ,S→ 等。
(2)在书写热化学方程式时,应以燃烧1 mol物质为标准来配平其余物质的化学计量
数。例如:
25
CH (l)+ O(g)===8CO(g)+9HO(l)
8 18 2 2 2 2
ΔH=-5 518 kJ·mol-1。2.中和热
(1)概念:在稀溶液中,强酸跟强碱发生中和反应生成 时的反应热叫
中和热。
(2)用离子方程式可表示为 OH-(aq)+H+(aq)===HO(l) ΔH=-57.3
2
kJ·mol-1。
3.中和热的测定
(1)装置(请在横线上填写仪器名称)
(2)计算公式
(m +m )·c·(t −t )
ΔH=- 碱 酸 2 1 kJ·mol-1
n
t—起始温度,t—终止温度,n—生成水的物质的量。
1 2
(3)注意事项
① 泡 沫 塑 料 板 和 碎 泡 沫 塑 料 ( 或 纸 条 ) 的 作 用 是
。
②为保证酸完全中和,采取的措施是 。
4.能源
(1)能源分类
(2)解决能源问题的措施
①提高能源的利用效率。
②开发新能源。[思考]
燃烧热和中和热的相同点和不同点
燃烧热 中和热
能量变化 放热
相同点 ΔH及其
ΔH 0,单位均为kJ·mol-1
单位
反应物
不一定为1 mol
的量
生成物
不确定 生成水的量为
的量
不同点
反应热 101 kPa时, 纯物质完 在稀溶液里,酸与碱发生中和反应生成
全燃烧生成稳定的氧化物时所
的含义 放出的热量 时所放出的热量
燃烧热ΔH=-a kJ·mol-1
表示方法 强酸与强碱反应的中和热ΔH=
(a>0)
[判断] (正确的打“√”,错误的打“×”)
(1)甲烷的标准燃烧热ΔH=-890 kJ·mol-1,则甲烷燃烧的热化学方程式为CH
4
(g)+2O(g)===CO(g)+2HO(g) ΔH=-890 kJ·mol-1( )
2 2 2
(2)在稀溶液中:H+(aq)+OH-(aq)===HO(l) ΔH=-57.3 kJ·mol-1,若
2
将含0.5 mol HSO 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量为57.3 kJ( )
2 4
(3)NaHCO+HHCOONa+HO反应中,储氢、释氢过程均无能量变化( )
3 2 2
(4)随着科技的发展,氢气将成为主要能源之一( )
(5)粮食作物是制乙醇燃料的主要原料( )
(6)开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM 2.5的含量
( )
(7)低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放
( )
2对点速练
练点一 燃烧热、中和热的判断与计算
1.下列热化方程式中ΔH的数值表示可燃物燃烧热的是( )
1
A.CO(g)+ O(g)===CO(g) ΔH=-283 kJ·mol-1
2 2 2
B.CH(g)+2O(g)===CO(g)+2HO(g) ΔH=-802.3 kJ·mol-1
4 2 2 2
C.2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2D.H(g)+Cl(g)===2HCl(g) ΔH=-184.6 kJ·mol-1
2 2
2.已知反应:
①101 kPa时,2C(s)+O(g)===2CO(g)
2
ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)===HO(l)
2
ΔH=-57.3 kJ·mol-1
下列结论中正确的是( )
A.碳的燃烧热等于110.5 kJ·mol-1
B.①的反应热为221 kJ·mol-1
C.稀硫酸与稀NaOH溶液反应的中和热为114.6 kJ·mol-1
D.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.65 kJ的热量
练点二 中和热的测定
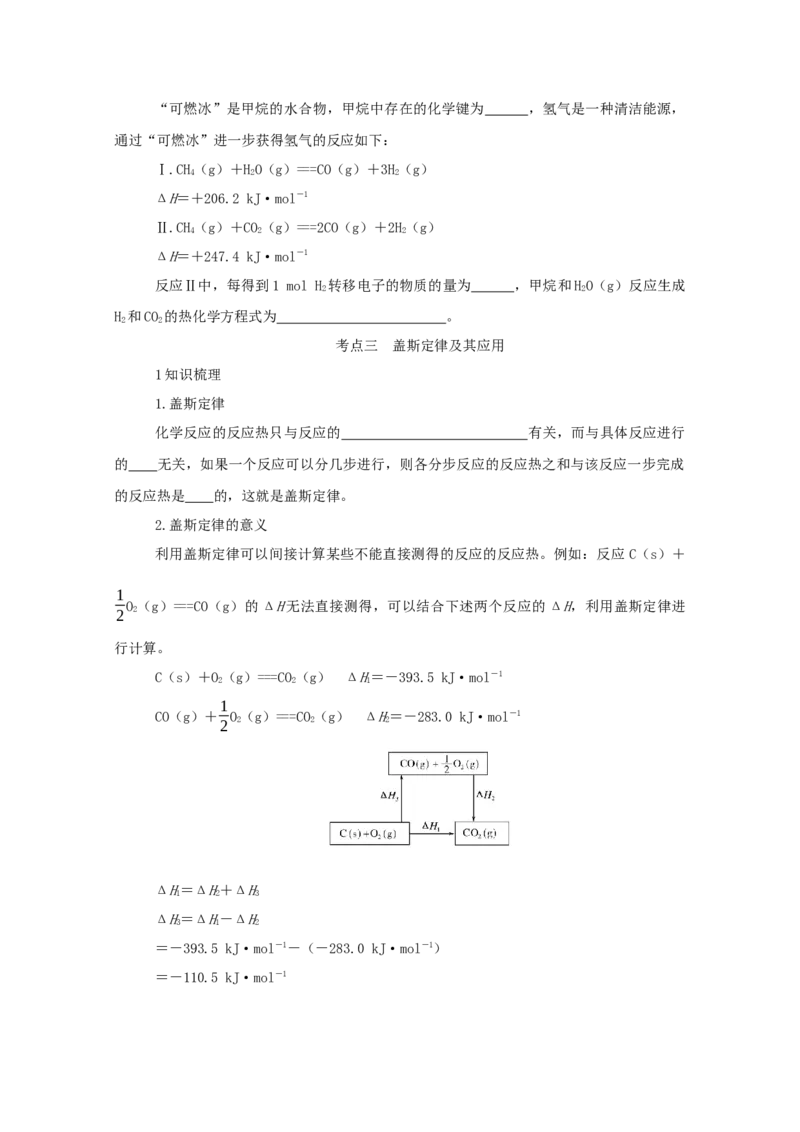
3.测定稀硫酸和氢氧化钠溶液反应的中和热(实验装置如图所示)。
(1)图中尚缺少的一种仪器是 。
(2)实验时环形玻璃搅拌棒的运动方向是 。
a.上下运动 b.左右运动
c.顺时针运动 d.逆时针运动
( 3 ) 写 出 反 应 的 热 化 学 方 程 式 为
________________________________________________________________________
________________________________________________________________________
(中和热为57.3 kJ·mol-1)。
(4)该同学每次分别取0.50 mol·L-1 50 mL NaOH溶液和0.50 mol·L-1 30 mL硫酸
进行实验,通过多次实验测定中和热ΔH=-53.5 kJ·mol-1,与57.3 kJ·mol-1有偏差,
产生偏差的原因不可能是 (填字母)。
a.实验装置保温、隔热效果差
b.用量筒量取NaOH溶液的体积时仰视读数c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
方法总结
中和热测定实验误差分析
50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液反应的误差分析:
引起误差的实验操作 t终-t |ΔH|
始
保温措施不好 偏小 偏小
搅拌不充分 偏小 偏小
所用酸、碱浓度过大 偏大 偏大
用同浓度的氨水代替NaOH溶液 偏小 偏小
用同浓度的醋酸代替盐酸 偏小 偏小
用50 mL 0.50 mol·L-1 NaOH溶液 偏小 偏小
练点三 能源问题
4.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可能再生。
下列属于未来新能源的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.③④⑤⑥⑦⑧
C.③⑤⑥⑦⑧ D.⑤⑥⑦⑧
5.为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用
太阳能制取氢能的构想。下列说法正确的是( )
A.HO的分解反应是放热反应
2
B.氢能源已被普遍使用
C.2 mol HO具有的总能量低于2 mol H 和1 mol O 的能量
2 2 2
D.氢气不易贮存和运输,无开发利用价值
6.我国在南海神狐海域天然气水合物(又称“可燃冰”)试采成功,海洋科学研究引
起全球关注。“可燃冰”是甲烷的水合物,甲烷中存在的化学键为 ,氢气是一种清洁能源,
通过“可燃冰”进一步获得氢气的反应如下:
Ⅰ.CH(g)+HO(g)===CO(g)+3H(g)
4 2 2
ΔH=+206.2 kJ·mol-1
Ⅱ.CH(g)+CO(g)===2CO(g)+2H(g)
4 2 2
ΔH=+247.4 kJ·mol-1
反应Ⅱ中,每得到1 mol H 转移电子的物质的量为 ,甲烷和HO(g)反应生成
2 2
H 和CO 的热化学方程式为 。
2 2
考点三 盖斯定律及其应用
1知识梳理
1.盖斯定律
化学反应的反应热只与反应的 有关,而与具体反应进行
的 无关,如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成
的反应热是 的,这就是盖斯定律。
2.盖斯定律的意义
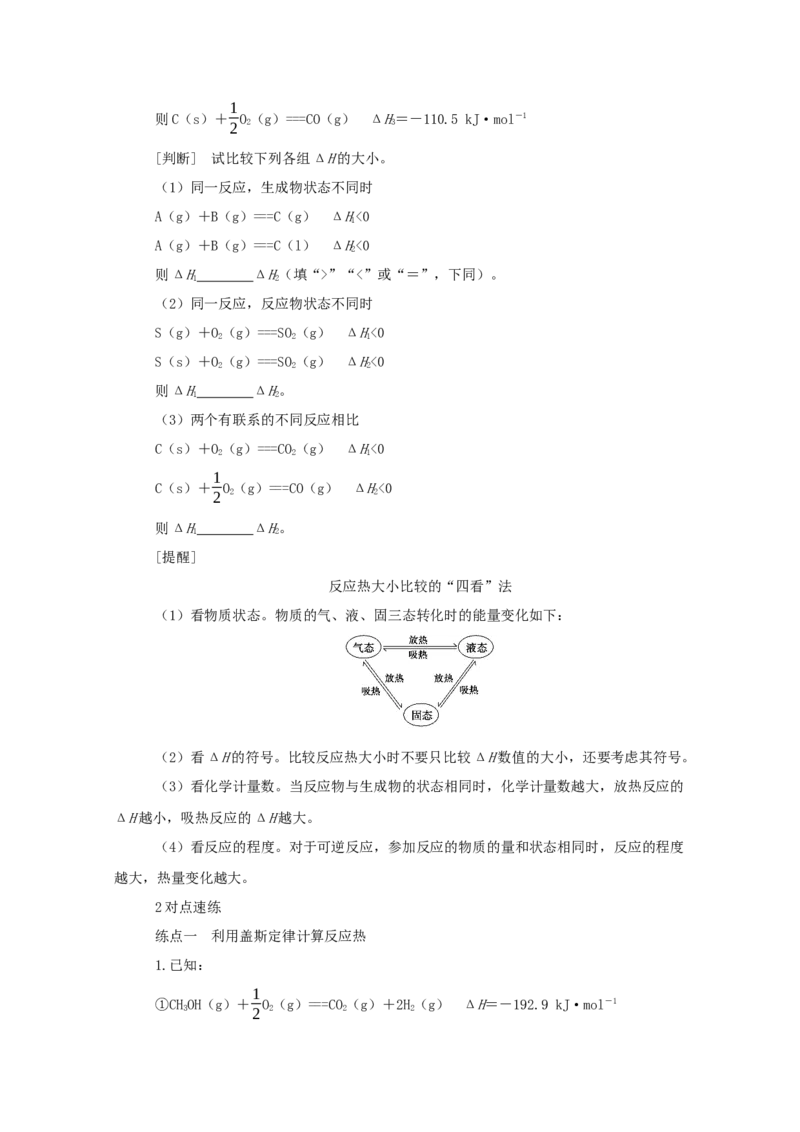
利用盖斯定律可以间接计算某些不能直接测得的反应的反应热。例如:反应 C(s)+
1
O (g)===CO(g)的ΔH无法直接测得,可以结合下述两个反应的ΔH,利用盖斯定律进
2 2
行计算。
C(s)+O(g)===CO(g) ΔH=-393.5 kJ·mol-1
2 2 1
1
CO(g)+ O(g)===CO(g) ΔH=-283.0 kJ·mol-1
2 2 2 2
ΔH=ΔH+ΔH
1 2 3
ΔH=ΔH-ΔH
3 1 2
=-393.5 kJ·mol-1-(-283.0 kJ·mol-1)
=-110.5 kJ·mol-11
则C(s)+ O(g)===CO(g) ΔH=-110.5 kJ·mol-1
2 2 3
[判断] 试比较下列各组ΔH的大小。
(1)同一反应,生成物状态不同时
A(g)+B(g)===C(g) ΔH<0
1
A(g)+B(g)===C(l) ΔH<0
2
则ΔH ΔH(填“>”“<”或“=”,下同)。
1 2
(2)同一反应,反应物状态不同时
S(g)+O(g)===SO(g) ΔH<0
2 2 1
S(s)+O(g)===SO(g) ΔH<0
2 2 2
则ΔH ΔH。
1 2
(3)两个有联系的不同反应相比
C(s)+O(g)===CO(g) ΔH<0
2 2 1
1
C(s)+ O(g)===CO(g) ΔH<0
2 2 2
则ΔH ΔH。
1 2
[提醒]
反应热大小比较的“四看”法
(1)看物质状态。物质的气、液、固三态转化时的能量变化如下:
(2)看ΔH的符号。比较反应热大小时不要只比较ΔH数值的大小,还要考虑其符号。
(3)看化学计量数。当反应物与生成物的状态相同时,化学计量数越大,放热反应的
ΔH越小,吸热反应的ΔH越大。
(4)看反应的程度。对于可逆反应,参加反应的物质的量和状态相同时,反应的程度
越大,热量变化越大。
2对点速练
练点一 利用盖斯定律计算反应热
1.已知:
1
①CHOH(g)+ O(g)===CO(g)+2H(g) ΔH=-192.9 kJ·mol-1
3 2 2 2 21
②H(g)+ O(g)===HO(l) ΔH=-285.8 kJ·mol-1
2 2 2 2
3
则CHOH(g)+ O(g)===CO(g)+2HO(l)的ΔH为( )
3 2 2 2 2
A.+478.7 kJ·mol-1 B.-764.5 kJ·mol-1
C.-478.7 kJ·mol-1 D.+764.5 kJ·mol-1
2.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO(s)+3C(s)===KS(s)+N(g)+3CO(g) ΔH=x kJ·mol-1
3 2 2 2
已知:碳的燃烧热ΔH=a kJ·mol-1
1
S(s)+2K(s)===KS(s) ΔH=b kJ·mol-1
2 2
2K(s)+N(g)+3O(g)===2KNO(s) ΔH=c kJ·mol-1,则x为( )
2 2 3 3
A.3a+b-c B.c-3a-b
C.a+b-c D.c-a-b
3.(1)已知C(s)+HO(g)===CO(g)+H(g) ΔH=a kJ·mol-1
2 2
2C(s)+O(g)===2CO(g) ΔH=-220 kJ·mol-1
2
H—H、O===O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-
1,则a为( )
A.-332 B.-118
C.+350 D.+130
(2)CH—CO 催化重整不仅可以得到合成气(CO和H ),还对温室气体的减排具有重
4 2 2
要意义。回答下列问题:
CH—CO 催化重整反应为:CH(g)+CO(g)===2CO(g)+2H(g)。
4 2 4 2 2
已知:C(s)+2H(g)===CH(g) ΔH=-75 kJ·mol-1
2 4
C(s)+O(g)===CO(g) ΔH=-394 kJ·mol-1
2 2
1
C(s)+ O(g)===CO(g) ΔH=-111 kJ·mol-1
2 2
该催化重整反应的ΔH= kJ·mol-1。
归纳总结
根据盖斯定律计算时的注意点
(1)参照目标热化学方程式,结合原热化学方程式(一般为2~3个)进行合理
“变形”,(如热化学方程式颠倒、乘或除以某一个数,然后将它们相加、减。)可得出目
标热化学方程式的ΔH与原热化学方程式ΔH之间的换算关系。(2)当热化学方程式乘、除以某一个数时,ΔH也应相应地乘、除以某一个数;方程
式进行加减运算时,ΔH也同样要进行加减运算,且要带“+”“-”符号。
(3)将一个热化学方程式颠倒书写时,ΔH的符号也随之改变,但数值不变。
(4)在涉及反应过程中,会遇到同一物质的三态(固、液、气)的相互转化,状态由
固→液→气变化时,会吸热;反之会放热。
练点二 利用盖斯定律比较ΔH大小
4.已知:
1
①H(g)+ O(g)===HO(g)ΔH=a kJ·mol-1
2 2 2 2 1
②2H(g)+O(g)===2HO(g)ΔH=b kJ·mol-1
2 2 2 2
1
③H(g)+ O(g)===HO(l)ΔH=c kJ·mol-1
2 2 2 2 3
④2H(g)+O(g)===2HO(l)ΔH=d kJ·mol-1
2 2 2 4
下列关系式中正确的是( )
A.ad>0
C.2a=b<0 D.2c=d>0
5.已知室温下,将CuSO·5HO(s)溶于水会使溶液温度降低,将CuSO (s)溶于水
4 2 4
会使溶液温度升高,则下列能量转化关系的判断不正确的是( )
A.ΔH>0 B.ΔH>ΔH
1 2 3
C.ΔH>ΔH D.ΔH=ΔH+ΔH
3 1 2 1 3
方法总结
反应热大小比较法——盖斯定律“矢量三角”
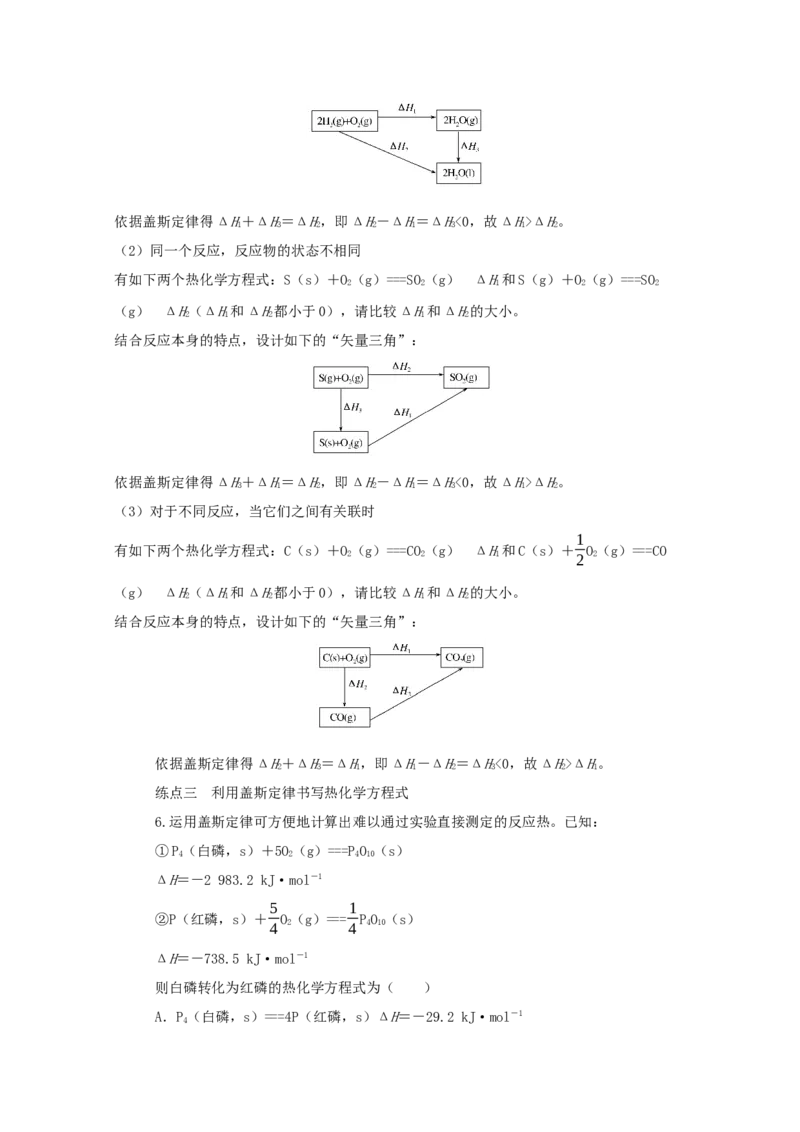
(1)同一个反应,生成物的状态不相同
有如下两个热化学方程式:2H(g)+O(g)===2HO(g) ΔH和2H(g)+O(g)
2 2 2 1 2 2
===2HO(l)
2
ΔH(ΔH和ΔH都小于0),请比较ΔH和ΔH的大小。
2 1 2 1 2
结合反应本身的特点,设计如下的“矢量三角”:依据盖斯定律得ΔH+ΔH=ΔH,即ΔH-ΔH=ΔH<0,故ΔH>ΔH。
1 3 2 2 1 3 1 2
(2)同一个反应,反应物的状态不相同
有如下两个热化学方程式:S(s)+O(g)===SO(g) ΔH和S(g)+O(g)===SO
2 2 1 2 2
(g) ΔH(ΔH和ΔH都小于0),请比较ΔH和ΔH的大小。
2 1 2 1 2
结合反应本身的特点,设计如下的“矢量三角”:
依据盖斯定律得ΔH+ΔH=ΔH,即ΔH-ΔH=ΔH<0,故ΔH>ΔH。
3 1 2 2 1 3 1 2
(3)对于不同反应,当它们之间有关联时
1
有如下两个热化学方程式:C(s)+O(g)===CO(g) ΔH和C(s)+ O(g)===CO
2 2 1 2 2
(g) ΔH(ΔH和ΔH都小于0),请比较ΔH和ΔH的大小。
2 1 2 1 2
结合反应本身的特点,设计如下的“矢量三角”:
依据盖斯定律得ΔH+ΔH=ΔH,即ΔH-ΔH=ΔH<0,故ΔH>ΔH。
2 3 1 1 2 3 2 1
练点三 利用盖斯定律书写热化学方程式
6.运用盖斯定律可方便地计算出难以通过实验直接测定的反应热。已知:
①P(白磷,s)+5O(g)===PO (s)
4 2 4 10
ΔH=-2 983.2 kJ·mol-1
5 1
②P(红磷,s)+ O(g)=== PO (s)
4 2 4 4 10
ΔH=-738.5 kJ·mol-1
则白磷转化为红磷的热化学方程式为( )
A.P(白磷,s)===4P(红磷,s)ΔH=-29.2 kJ·mol-1
4B.P(白磷,s)===4P(红磷,s)ΔH=+29.2 kJ·mol-1
4
C.P(白磷,s)===4P(红磷,s)
4
ΔH=-2 244.7 kJ·mol-1
D.P(白磷,s)===4P(红磷,s)ΔH=+2 244.7 kJ·mol-1
4
7.阅读信息,写出指定条件的热化学方程式。
(1)工业上制取硝酸铵的流程图如下所示:
已知:4NO(g)+4NH(g)+O(g) 4N(g)+6HO(g)
3 2 ⇌ 2 2
ΔH=-1 745.2 kJ·mol-1;
6NO(g)+4NH(g) 5N(g)+6HO(g)
3 ⇌ 2 2
ΔH=-1 925.2 kJ·mol-1。
则 反 应 Ⅰ 的 热 化 学 方 程 式 可 表 示 为
________________________________________________________________________
________________________________________________________________________。
(2)饮用水中的NO− 主要来自于NH+ 。已知在微生物的作用下,NH+
经过两步反应被
3 4 4
氧化成NO−
。两步反应的能量变化示意图如下:
3
1 mol
NHH+ 全部被氧化成NO−
的热化学方程式为
4 3
________________________________________________________________________
________________________________________________________________________。
(3)TiO 与Cl 难以直接反应,加碳生成CO和CO 可使反应得以进行。
2 2 2
已知:TiO(s)+2Cl(g)===TiCl(g)+O(g)
2 2 4 2
ΔH=+175.4 kJ·mol-1
1
2C(s)+O(g)===2CO(g) ΔH=-220.9 kJ·mol-1
2 2沸 腾 炉 中 加 碳 氯 化 生 成 TiCl ( g ) 和 CO ( g ) 的 热 化 学 方 程 式 :
4
________________________________________________________________________
________________________________________________________________________。
(4)标准摩尔生成焓是指在25 ℃和101 kPa时,最稳定的单质生成1 mol化合物的
焓变。已知25 ℃和101 kPa时下列反应:
①2CH(g)+7O(g)===4CO(g)+6HO(l)
2 6 2 2 2
ΔH=-3 116 kJ·mol-1
②C(石墨,s)+O(g)===CO(g) ΔH=-393.5 kJ·mol-1
2 2
③2H(g)+O(g)===2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2
写出表示乙烷标准摩尔生成焓的热化学方程式:________________________
。
本讲真题研练
1.[2020·全国卷Ⅱ,28(1)]天然气的主要成分为CH ,一般还含有CH 等烃类,是
4 2 6
重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:CH (g)===CH (g)+H (g) ΔH,相关
2 6 2 4 2 1
物质的燃烧热数据如表所示:
物质 CH(g) CH(g) H(g)
2 6 2 4 2
燃烧热ΔH/(kJ·mol-
-1 560 -1 411 -286
1)
①ΔH= kJ·mol-1。
1
2.[2019·全国卷Ⅲ,28(2)]Deacon直接氧化法可按下列催化过程进行:
1
CuCl(s)===CuCl(s)+ Cl(g)
2 2 2
ΔH=83 kJ·mol-1
11 1
CuCl(s)+ O(g)===CuO(s)+ Cl(g)
2 2 2 2
ΔH=-20 kJ·mol-1
2
CuO(s)+2HCl(g)===CuCl(s)+HO(g)
2 2
ΔH=-121 kJ·mol-1
3
则4HCl(g)+O(g)===2Cl(g)+2HO(g)的ΔH= kJ·mol-1。
2 2 2
3.[2018·全国卷Ⅱ,27(1)]CH -CO 催化重整不仅可以得到合成气(CO和H ),还
4 2 2
对温室气体的减排具有重要意义。回答下列问题:
CH-CO 催化重整反应为:CH(g)+CO(g)===2CO(g)+2H(g)。
4 2 4 2 2
已知:C(s)+2H(g)===CH(g) ΔH=-75 kJ·mol-1
2 4
C(s)+O(g)===CO(g) ΔH=-394 kJ·mol-1
2 2
1
C(s)+ O(g)===CO(g) ΔH=-111 kJ·mol-1
2 2
该催化重整反应的ΔH= kJ·mol-1。
4.[2020·天津卷,10]理论研究表明,在101 kPa和298 K下,HCN(g) HNC(g)
⇌
异构化反应过程的能量变化如图所示。下列说法错误的是( )
A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3 kJ·mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
5.[2020·浙江7月,22]关于下列ΔH的判断正确的是( )
CO2− (aq)+H+(aq)===HCO−
(aq) ΔH
3 3 1
CO2− (aq)+HO(l) HCO− (aq)+OH-(aq) ΔH
3 2 ⇌ 3 2
OH-(aq)+H+(aq)===HO(l) ΔH
2 3
OH-(aq)+CHCOOH(aq)===CHCOO-(aq)+HO(l) ΔH
3 3 2 4A.ΔH<0 ΔH<0 B.ΔH<ΔH
1 2 1 2
C.ΔH<0 ΔH >0 D.ΔH>ΔH
3 4 3 4
6.[2019·浙江4月,23]MgCO 和CaCO 的能量关系如图所示(M===Ca、Mg):
3 3
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是( )
A.ΔH(MgCO)>ΔH(CaCO)>0
1 3 1 3
B.ΔH(MgCO)=ΔH(CaCO)>0
2 3 2 3
C.ΔH(CaCO)-ΔH(MgCO)=ΔH(CaO)-ΔH(MgO)
1 3 1 3 3 3
D.对于MgCO 和CaCO,ΔH+ΔH>ΔH
3 3 1 2 3
第六章 化学反应与能量
第1讲 化学能与热能
考点一
1知识梳理
1.(1)物质 能量 (2)质量 能量 (3)热能 热量
2.(1)所释放或吸收的热量 (2)反应热 (3)ΔH (4)kJ·mol-1 kJ/mol
4.(1)物质的量 反应热 (2)物质 能量 1 mol固体碳和1 mol氧气反应 1 mol
二氧化碳 393.5 kJ的热量
判断 答案:(1)√ (2)× (3)× (4)√ (5)√ (6)√ (7)× (8)×
2对点速练
1.解析:A项,由能量—反应过程图像中状态Ⅰ和状态Ⅲ知,CO和O生成CO 是放热
2
反应,错误;B项,由状态Ⅱ知,在CO与O生成CO 的过程中CO没有断键形成C和O,错误;
2
C项,由状态Ⅲ及CO 的结构式O===C===O知,CO 分子中存在碳氧极性共价键,正确;D项,
2 2由能量—反应过程图像中状态Ⅰ(CO和O)和状态Ⅲ(CO)分析,状态Ⅰ→状态Ⅲ表示CO和O原
2
子反应生成CO 的过程,错误。
2
答案:C
2.解析:由图示可知CO 和CH 在Ni催化作用下,最终生成CO和H ,故A项正确;化
2 4 2
学反应的过程中存在构成反应物的键的断裂和生成物中键的形成,由图示可知①→②过程中
既有碳氧键的断裂,又有碳氧键的形成,故B项正确;①的能量总和大于②的能量总和,则
①→②的过程放出能量,故C项错误;由图示可知CO 和CH 催化重整生成CO和H 的过程中
2 4 2
Ni的质量和化学性质没有发生变化,则Ni为催化剂,故D项正确。
答案:C
3.解析:曲线Ⅰ(表示没有使用催化剂)和曲线Ⅱ(表示使用了催化剂)是同一个反应的
能量变化,A项错误;曲线Ⅱ可以表示使用了催化剂的放热反应的能量变化,但二氧化锰催
化氯酸钾分解的反应属于吸热反应,B项错误;放热反应不一定不需要加热,C项错误;反应
的ΔH等于生成物的总能量减去反应物的总能量,D项正确。
答案:D
4.解析:由图可知,正反应放热,ΔH为负值;逆反应吸热,ΔH为正值,D错误。
答案:D
5.解析:由图可知,1 g H (g)(即0.5 mol)和8 g O (g)(即0.25 mol)完全反应生成
2 2
HO(l)放出142.9 kJ能量,据此写出热化学方程式:2H(g)+O(g)===2HO(l) ΔH=-
2 2 2 2
571.6 kJ/mol。
答案:D
6.解析:A项由图可知,1 mol O (g)+1 mol C(金刚石,s)具有的能量为E kJ,1
2 4
mol CO (g)具有的能量为E kJ,且E>E,则反应C(金刚石,s)+O(g)===CO(g)为放热反
2 1 4 1 2 2
应,ΔH=(E-E) kJ/mol,错误。B项,1 mol CO(g)+0.5 mol O (g)具有的能量为E
1 4 2 2
1
kJ,则反应C(石墨,s)+ O(g)===CO(g)的ΔH=(E-E) kJ/mol,错误。C项,由图可知,
2 2 2 3
C(石墨,s)===C(金刚石,s)为吸热反应,则有ΔH=(E-E) kJ/mol,错误。D项,由图可
4 3
1
知 , CO(g)===CO(g) + O(g) 为 吸 热 反 应 , ΔH= (E - E) kJ/mol , 从 而 可 知
2 2 2 2 1
2CO(g)===2CO(g)+O(g)的ΔH=2(E-E) kJ/mol,正确。
2 2 2 1
答案:D
7.答案:(1)CH(g)+2O(g)===CO(g)+2HO(l)
4 2 2 2ΔH=-890.3 kJ·mol-1
(2)BH(g)+3O(g)===BO(s)+3HO(l)
2 6 2 2 3 2
ΔH=-2 165 kJ·mol-1
(3)2Na(s)+O(g)===NaO(s) ΔH=-511 kJ·mol-1
2 2 2
(4)SiH(g)+2O(g)===SiO(s)+2HO(l) ΔH=-1 520.0 kJ·mol-1
4 2 2 2
(5)N(g)+3H(g) 2NH(l) ΔH=-2(c+b-a) kJ·mol-1
2 2 ⇌ 3
(6)NO(g)+CO(g)===CO(g)+NO(g) ΔH=-234 kJ·mol-1
2 2
考点二
1知识梳理
1.(1)1 mol CO(g) HO(l) SO(g)
2 2 2
2.(1)1 mol液态HO
2
3.(1)环形玻璃搅拌棒 温度计 (3)保温隔热,减少实验过程中的热量损失 使碱稍
过量
思考 答案:< 1 mol 1 mol 1 mol 1 mol HO -57.3 kJ/mol
2
判断 答案:(1)× (2)× (3)× (4)√ (5)√ (6)√ (7)√
2对点速练
1.解析:A项,符合燃烧热的概念,正确;B项,生成物中的水是气体,属于不稳定
氧化物,错误;C项,热化学方程式中是2 mol可燃物氢气燃烧放热,不符合燃烧热的概念,
错误;D项,HCl不是氧化物,不符合燃烧热的概念要求,错误。
答案:A
2.解析:反应①没有生成稳定氧化物,因此碳的燃烧热大于 110.5 kJ·mol-1,故A
项错误;①的反应热为-221 kJ·mol-1,故B项错误;稀硫酸与稀NaOH溶液反应的中和热
为57.3 kJ·mol-1,故C项错误;20 g NaOH 的物质的量n(NaOH)=0.5 mol,则Q=0.5
mol×57.3 kJ·mol-1=28.65 kJ,D项正确。
答案:D
3.解析:实验测定中和热ΔH=-53.5 kJ·mol-1与57.3 kJ·mol-1有偏差,是因为
实验过程中热量有散失。此实验中硫酸过量,用量筒量取NaOH溶液的体积时仰视读数使
NaOH的量偏多,所测中和热数值偏大。
答案:(1)温度计 (2)a1 1
(3)NaOH(aq)+ HSO(aq)=== NaSO(aq)+HO(l) ΔH=-57.3 kJ·mol-1
2 2 4 2 2 4 2
或2NaOH(aq)+HSO(aq)===NaSO(aq)+2HO(l) ΔH=-114.6 kJ·mol-1
2 4 2 4 2
(4)b
4.解析:新能源要符合污染小,可再生性强等特点,选D。
答案:D
5.解析:水的分解是吸热反应,A错误;氢能源由于受贮存和运输等因素的限制,还
未普遍使用,但有巨大的开发利用的价值,B、D错误。
答案:C
6.答案:共价键 3 mol CH(g)+2HO(g)===CO(g)+4H(g) ΔH=+165 kJ·mol
4 2 2 2
-1
考点三
1知识梳理
1.始态(各反应物)和终态(各生成物) 途径 相同
判断 答案:(1)> (2)< (3)<
2对点速练
1.解析:分析题给热化学方程式可知,要得到目标热化学方程式,应将①和②中的
H(g)消去,而①和②中的H(g)分别在方程式的两边,因此通过②×2+①即可得到目标热化
2 2
3
学方程式,则CHOH(g)+ O(g)===CO(g)+2HO(l) ΔH=(-285.8 kJ·mol-1×2)+(-
3 2 2 2 2
192.9 kJ·mol-1)=-764.5 kJ·mol-1。
答案:B
2.解析:由题可得
C(s)+O(g)===CO(g) ΔH=a kJ·mol-1①
2 2 1
S(s)+2K(s)===KS(s) ΔH=b kJ·mol-1②
2 2
2K(s)+N(g)+3O(g)===2KNO(s) ΔH=c kJ·mol-1③
2 2 3 3
由盖斯定律得①×3+②-③为所给方程式,即x=3a+b-c,选A。
答案:A
3.解析:(1)已知①C(s)+HO(g)===CO(g)+H(g) ΔH=a kJ·mol-1,
2 2
②2C(s)+O(g)===2CO(g) ΔH=-220 kJ·mol-1
2
①×2-②得:2HO(g)===O(g)+2H(g) ΔH=(2a+220) kJ·mol-1,
2 2 24×462-496-2×436=2a+220,解得a=+130。
(2)将已知中3个反应依次记为①、②、③,根据盖斯定律③×2-①-②得该催化重
整反应的ΔH=(-111×2+75+394) kJ·mol-1=+247 kJ·mol-1。
答案:(1)D (2)247
4.解析:由于氢气的燃烧是放热反应,故四个反应的ΔH都小于0,即B、D错误;①、
②式反应物、生成物的状态相同,①×2=②,即2ΔH=ΔH,2a=b,又H 的燃烧反应为放
1 2 2
热反应,故2a=b<0,C正确;③-①得:HO(g)===HO(l),由于气态水转变为液态水要放热,
2 2
故其ΔH=ΔH-ΔH=c-a<0,c0,正确;
4 2 4 1
B项,ΔH>0,ΔH<0,则ΔH>ΔH,正确;C项,ΔH<0,ΔH>0,则ΔH<ΔH,错误;D
2 3 2 3 3 1 3 1
项,根据盖斯定律可知:ΔH=ΔH+ΔH,正确。
2 1 3
答案:C
6.解析:反应②×4可得③4P(红磷,s)+5O(g)===PO (s) ΔH=-2 954 kJ·mol
2 4 10
-1。可见等质量的白磷比红磷含有的能量高,物质含有的能量越高,物质的稳定性就越弱。
由①-③整理可得:P(白磷,s)===4P(红磷,s) ΔH=-29.2 kJ·mol-1,A正确。
4
答案:A
7.解析:(1)将已知的两个热化学方程式从上到下依次标记为①和②,根据盖斯定律
由①×5-②×4得:4NH(g)+5O(g) 4NO(g)+6HO(g) ΔH=-1 025.2 kJ·mol-1。
3 2 ⇌ 2
(4)根据标准摩尔生成焓的定义,乙烷的标准摩尔生成焓是指由单质 C和单质H 生成1
2
mol C H 的焓变。根据盖斯定律,(②×4-①+③×3)÷2 得:2C(石墨,s)+
2 6
3H(g)===CH(g) ΔH=-86.4 kJ·mol-1。
2 2 6
答案:(1)4NH(g)+5O(g) 4NO(g)+6HO(g)
3 2 ⇌ 2
ΔH=-1 025.2 kJ·mol-1
(2)NH+ (aq)+2O(g)===NO− (aq)+2H+(aq)+HO(l) ΔH=-346 kJ·mol-1
4 2 3 2
(3)TiO(s)+2Cl(g)+2C(s)===TiCl(g)+2CO(g) ΔH=-45.5 kJ·mol-1
2 2 4
(4)2C(石墨,s)+3H(g)===CH(g) ΔH=-86.4 kJ·mol-1
2 2 6
本讲真题研练
1.解析:(1)①根据题表中数据信息可写出热化学方程式7
(ⅰ)CH(g)+ O(g)===2CO(g)+3HO(l)
2 6 2 2 2 2
ΔH=-1 560 kJ·mol-1、
(ⅱ)CH(g)+3O(g)===2CO(g)+2HO(l)
2 4 2 2 2
ΔH=-1 411 kJ·mol-1、
1
(ⅲ)H(g)+ O(g)===HO(l) ΔH=-286 kJ·mol-1,根据盖斯定律,由(ⅰ)-(ⅱ)
2 2 2 2
-(ⅲ)得CH(g)===CH(g)+H(g) ΔH=+137 kJ·mol-1。
2 6 2 4 2 1
答案:(1)①+137
2.解析:将题给反应过程依次记为①、②、③,则根据盖斯定律,由③×2+②×2+
①×2 可得到 4HCl(g)+O(g)===2Cl(g)+2HO(g) ΔH=2ΔH+2ΔH+2ΔH=-116
2 2 2 3 2 1
kJ·mol-1。
答案:-116
3.解析:将已知中3个反应依次记为①、②、③,根据盖斯定律③×2-①-②得该
催化重整反应的ΔH=(-111×2+75+394)kJ·mol-1=+247 kJ·mol。
答案:+247
4.解析:本题考查反应过程的能量图分析,考查的化学学科核心素养是宏观辨识与微
观探析、证据推理与模型认知。HNC的能量比HCN高,则稳定性较好的是HCN,A项正确;该
异构化反应的ΔH= +59.3 kJ·mol-1,为吸热反应,则正反应的活化能大于逆反应的活化
能,B、C项正确;使用催化剂只能改变反应的历程,但是不影响反应的反应热,D项错误。
答案:D
5.解析:本题考查反应热知识,考查的化学学科核心素养是证据推理与模型认知。形
成化学键要放出热量,ΔH<0,第二个反应是盐类的水解反应,是吸热反应,ΔH>0,A项错
1 2
误;ΔH是负值,ΔH是正值,ΔH<ΔH,B项正确;酸碱中和反应是放热反应,ΔH<0,
1 2 1 2 3
ΔH<0,C项错误;第四个反应(醋酸是弱酸,电离吸热)放出的热量小于第三个反应,但ΔH
4 3
和ΔH都是负值,则ΔH<ΔH,D项错误。
4 3 4
答案:B
6.解析:根据已知信息,离子电荷相同时,半径越小,离子键越强。由于 r(Mg2
+)ΔH(CaCO)>0 , A 项 正 确 ; 由 于 ΔH 只 与 CO 相 关 , 故 ΔH(MgCO) =
1 3 1 3 2 2 3
ΔH(CaCO)>0,B 项正确;根据能量关系图可知 ΔH=ΔH+ΔH-ΔH,由于
2 3 1 2 3ΔH(MgCO)≠ΔH(CaCO) , 故 ΔH(MgCO) + ΔH(MgCO) - ΔH(MgO)≠ΔH(CaCO) +
3 3 1 3 2 3 3 1 3
ΔH(CaCO) - ΔH(CaO) 而 ΔH(MgCO) = ΔH(CaCO) , 故 ΔH(MgCO) -
2 3 3 2 3 2 3 1 3
ΔH(MgO)≠ΔH(CaCO)-ΔH(CaO),ΔH(CaCO)-ΔH(MgCO)≠ΔH(CaO)-ΔH(MgO),C
3 1 3 3 1 3 1 3 3 3
项错误;由于ΔH+ΔH=ΔH+ΔH,而ΔH>0,故ΔH+ΔH>ΔH,D项正确,故选C。
3 1 2 1 2 3
答案:C