文档内容
第2讲 水的电离和溶液的pH
[考纲要求]
1.了解水的电离、离子积常数。
2.了解溶液pH的定义。了解测定溶液pH的方法,能进行pH的简单计算。
3.能根据中和滴定实验试题要求,分析或处理实验数据,得出合理结论。
考点一 水的电离平衡
1知识梳理
1.水的电离
水 是 极 弱 的 电 解 质 , 水 的 电 离 方 程 式 为 ______________________ 或
________________________。
2.水的离子积常数
K=c(H+)·c(OH-)。
w
(1)室温下:K=__________。
w
(2)影响因素:只与____有关,升高温度,K____。
w
(3)适用范围:K不仅适用于纯水,也适用于稀的________水溶液。
w
(4)K揭示了在任何水溶液中均存在H+和OH-,只要温度不变,K不变。
w w
3.影响水电离平衡的因素
(1)升高温度,水的电离程度________,K________。
w
(2)加入酸或碱,水的电离程度________,K________。
w
(3)加入可水解的盐(如FeCl、NaCO),水的电离程度________,K________。
3 2 3 w
[思考]
外界条件对水电离平衡的具体影响
c(OH c(H
条件体系变化 平衡移动方向 K 水的电离程度
w -) +)
___
HCl ____ ____ ____ ____
_
___
NaOH ____ ____ ____ ____
_
NaCO ___
2 ____ ____ ____ ____
_
3
可水解的盐
___
NHCl ____ ____ ____ ____
4 ____
升温 ____ ____ ____ ____
_
温度
___
降温 ____ ____ ____ ____
_
___
其他:如加入Na ____ ____ ____ ____
_
[判断] (正确的打“√”,错误的打“×”)
(1)纯水中c(H+)随着温度的升高而降低( )
(2)25 ℃时,0.10 mol·L-1NaHCO 溶液加水稀释后,c(H+)与c(OH-)的乘积变大(
3
)
(3)在蒸馏水中滴加浓HSO,K不变( )
2 4 w
(4)向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,K不变( )
w
(5)向水中加入AlCl 溶液对水的电离不产生影响( )
3
(6)100 ℃的纯水中c(H+)=1×10-6 mol·L-1,此时水呈酸性( )
[提醒]
(1)水的离子积常数显示了在任何水溶液中均存在水的电离平衡,都有H+和OH-共存,
只是相对含量不同而已。
(2)任何情况下水电离产生的c(H+)和c(OH-)总是相等的。升高温度,水的电离程度增
大,c(H+)增大,pH减小,但仍呈中性。
(3)水的离子积常数K=c(H+)·c(OH-),其实质是水溶液中的H+和OH-浓度的乘积,
w
不一定是水电离出的H+和OH-浓度的乘积,所以与其说K是水的离子积常数,不如说是水溶
w
液中的H+和OH-的离子积常数。即K不仅适用于水,还适用于酸性或碱性的稀溶液。
w
2对点速练
练点一 水的电离平衡判断
1.一定温度下,水存在HO H++OH- ΔH>0的平衡,下列叙述一定正确的是( )
2 ⇌
A.向水中滴入少量稀盐酸,平衡逆向移动,K减小
w
B.将水加热,K增大,pH减小
w
C.向水中加入少量固体CHCOONa,平衡逆向移动,c(H+)降低
3
D.向水中加入少量固体硫酸钠,c(H+)=10-7 mol·L-1,K不变
w
2.下列有关水电离情况的说法正确的是( )
A.100 ℃时,K=10-12,此温度下pH=7的溶液一定呈中性
w
B.NHCl、CHCOONa、NaHCO、NaHSO 溶于水,对水的电离都有促进作用
4 3 3 4
C.25 ℃时,pH=12的烧碱溶液与纯碱溶液,水的电离程度相同D.如图为水的电离平衡曲线,若从A点到C点,可采用升高温度的方法
练后归纳
正确理解水的电离平衡曲线
(1)曲线上任意点的K 都相同,即c(H+)·c(OH-)相同,温度相同。
w
(2)曲线外在任意点与曲线上任意点的K 不同,温度不同。
w
(3)实现曲线上点之间的转化需保持温度不变,改变酸碱性;实现曲线上点与曲线外点
之间的转化一定得改变温度。
练点二 水电离程度大小比较
3.若往20 mL 0.01 mol·L-1 CH COOH溶液中逐滴加入一定浓度的烧碱溶液,测得混
3
合溶液的温度变化如图所示,下列有关说法正确的是( )
A.c点时,醋酸的电离程度和电离常数都最大,溶液呈中性
B.若b点混合溶液显酸性,则2c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
C.混合溶液中水的电离程度:b>c>d
D.由图可知,该反应的中和热先增大后减小
4.如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
A.两条曲线间任意点均有c(H+)·c(OH-)=K
w
B.M区域内任意点均有c(H+)<c(OH-)
C.图中T<T
1 2
D.XZ线上任意点均有pH=75.25 ℃时,将浓度均为0.1 mol·L-1、体积分别为V和V的HA溶液与BOH溶液按
a b
不同体积比混合,保持V+V=100 mL,V、V与混合液的pH的关系如图所示。下列说法正
a b a b
确的是( )
A.由图可知BOH一定是强碱
B.K(HA)=1×10-6
a
C.b点时,c(B-)=c(A-)=c(OH-)=c(H+)
D.a→b过程中水的电离程度始终增大
6.下表是不同温度下水的离子积数据:
温度/℃ 25 t t
1 2
水的离子积常数 1×10-14 K 1×10-12
w
试回答下列问题:
(1)若25<t<t,则K________(填“>”“<”或“=”)1×10-14,做出此判断的
1 2 w
理由是________。
(2)在t ℃时,测得纯水中的c(H+)=2.4×10-7 mol·L-1,则c(OH-)为________。
1
该温度下,测得某HSO 溶液中c(SO2− )=5×10-6 mol·L-1,该溶液中c(OH-)=________
2 4 4
mol·L-1。
考点二 溶液的酸碱性与pH
1知识梳理
1.溶液的酸碱性
溶液的酸碱性取决于溶液中c(H+)和c(OH-)的相对大小。
(1)酸性溶液:c(H+)____c(OH-),常温下,pH____7。
(2)中性溶液:c(H+)____c(OH-),常温下,pH____7。(3)碱性溶液:c(H+)____c(OH-),常温下,pH____7。
2.溶液的pH及其测量方法
(1)计算公式:pH=________。
(2)溶液的酸碱性与pH的关系
常温下:
(3)测量方法
①pH试纸法:用镊子夹取一小块试纸放在洁净的______或______上,用玻璃棒蘸取待
测液点在试纸的中央,变色后与标准比色卡对照,即可确定溶液的pH。
pH试纸的适用范围0~14,使用时不能用蒸馏水湿润且只能测整数值。
②pH计测量法。
3.溶液pH的计算
(1)单一溶液的pH计算
强酸溶液:如HA,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lg c(H+)=-
n
lg(nc)。
10-14
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=
n
nc
-lg c(H+)=14+lg(nc)。
(2)混合溶液pH的计算类型
① 两 种 强 酸 混 合 : 直 接 求 出 c(H + ) , 再 据 此 求 pH 。 c(H + ) =
混 混
c(H+)V +c(H+)V
1 1 2 2。
V +V
1 2
②两种强碱混合:先求出c(OH-) ,再据K求出c(H+) ,最后求pH。
混 w 混
c(OH−)V +c(OH−)V
c(OH-) = 1 1 2 2。
混
V +V
1 2
③强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最
后求pH。
c(H+) 或c(OH-)
混 混c(H+) V −c(OH−) V碱
= 酸 酸 碱 。
V +V
酸 碱
[判断] (正确的打“√”,错误的打“×”)
(1)任何温度下,利用H+和OH-浓度的相对大小均可判断溶液的酸碱性( )
(2)某溶液的c(H+)>10-7 mol·L-1,则该溶液呈酸性( )
(3)用蒸馏水润湿的pH试纸测溶液的pH,一定会使结果偏低( )
(4)一定温度下,pH=a的氨水,稀释10倍后,其pH=b,则a=b+1( )
(5)常温常压时,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合后,滴入石蕊溶
液呈红色( )
(6)根据溶液的pH判断该溶液的酸碱性( )
(7)把pH=2与pH=12的酸、碱溶液等体积混合后,所得溶液的pH为7( )
[提醒]
(1)溶液呈现酸、碱性的实质是c(H+)与c(OH-)的相对大小,不能只看pH,一定温
度下pH=6的溶液也可能显中性,也可能显酸性,应注意温度。
(2)酸碱的强弱和溶液酸碱性的强弱不是等同关系:前者看电离程度,后者看溶液中
c(H+)和c(OH-)的相对大小。强酸溶液的酸性不一定比弱酸溶液的酸性强。
2对点速练
练点一 溶液酸碱性的判断
1.已知温度T时水的离子积常数为K,该温度下,将浓度为a mol·L-1的一元酸HA
w
与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
①a=b ②混合溶液的pH=7 ③混合溶液中c(OH-)=10-7 mol·L-1 ④混合溶液中,
c(H+)=√K mol·L-1 ⑤混合溶液中,c(B+)=c(A-)
W
A.②③ B.④⑤
C.①④ D.②⑤
2.在常温下,某溶液中由水电离出的c(H+)=1×10-11 mol·L-1,下列说法中正确的
是( )
A.该溶液肯定显碱性
B.该溶液肯定显酸性
C.该溶液的pH可能是11,也可能是3
D.该溶液的pH肯定不是113.常温下,有a mol·L-1HX和b mol·L-1HY两种酸溶液,下列说法不正确的是(
)
A.若a=b且c(X-)>c(Y-),则酸性:HX>HY
B.若a>b且c(X-)=c(Y-),则酸性:HX>HY
C.若a<b且两者pH相同,则HY一定是弱酸
D.若向HX溶液中加入等浓度、等体积的NaOH溶液,所得溶液pH>7,则HX为弱酸
方法总结
溶液酸碱性的判断方法
(1)根据c(H+)和c(OH-)的相对大小
c(H+)>c(OH-),呈酸性;c(H+)=c(OH-),呈中性;c(H+)<c(OH-),呈碱性。
(2)根据pH、pOH、p√K 进行判断
W
pH<p√K <pOH,呈酸性;pH=pOH=p√K ,呈中性;pOH<p√K <pH,呈碱性。
W W W
其中:pOH=-lg c(OH-),p√K =-lg √K ,pH+pOH=2p√K 。
W W W
(3)室温下,已知酸和碱pH之和的溶液等体积混合酸碱性分析(两强混合)
a.若pH之和等于14,则混合后溶液显中性,pH=7。
b.若pH之和大于14,则混合后溶液显碱性,pH>7。
c.若pH之和小于14,则混合后溶液显酸性,pH<7。
练点二 溶液pH的计算
4.常温下,下列叙述正确的是( )
A.将pH=a的氨水稀释10倍后,其pH=b,则a=b+1
B.将pH=3.0的盐酸稀释105倍后,溶液的pH=8.0
C.将pH=9.0的NaOH溶液与pH=11.0的NaOH溶液等体积混合,所得溶液的pH=9.3
D.若将1 mL pH=1.0的盐酸与100 mL NaOH溶液混合后,溶液的pH=7.0,则NaOH
溶液的pH=11.0
5.下列说法不正确的是( )
A.室温下,0.01 mol·L-1的盐酸中由水电离出的c(H+)为1.0×10-12 mol·L-1
B.室温下,0.01 mol·L-1的NaOH溶液中由水电离出的c(OH-)为1.0×10-12 mol·L-1
C.室温下,在pH=11的某溶液中,由水电离出的c(OH-)为1.0×10-3 mol·L-1
D.室温下,若某溶液中由水电离出的c(H+)=1.0×10-13 mol·L-1,则该溶液的pH
可能是1或13
6.25 ℃时,将体积为V、pH=a的某一元强碱与体积为V、pH=b的某二元强酸混合。
a b
(1)若所得溶液的pH=11,且a=13,b=2,则V∶V=________。
a b
(2)若所得溶液的pH=7,且已知V>V,b=0.5a,b值是否可以等于4?________(填
a b
“是”或“否”)。
方法总结
溶液pH计算的一般思维模型
练点三 与稀释有关的图像分析
7.pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如
下图所示。分别滴加NaOH溶液(c=0.1 mol/L)至pH=7,消耗NaOH溶液的体积为V、V,则
x y
( )
A.x为弱酸,VV
x y
C.y为弱酸,VV
x y
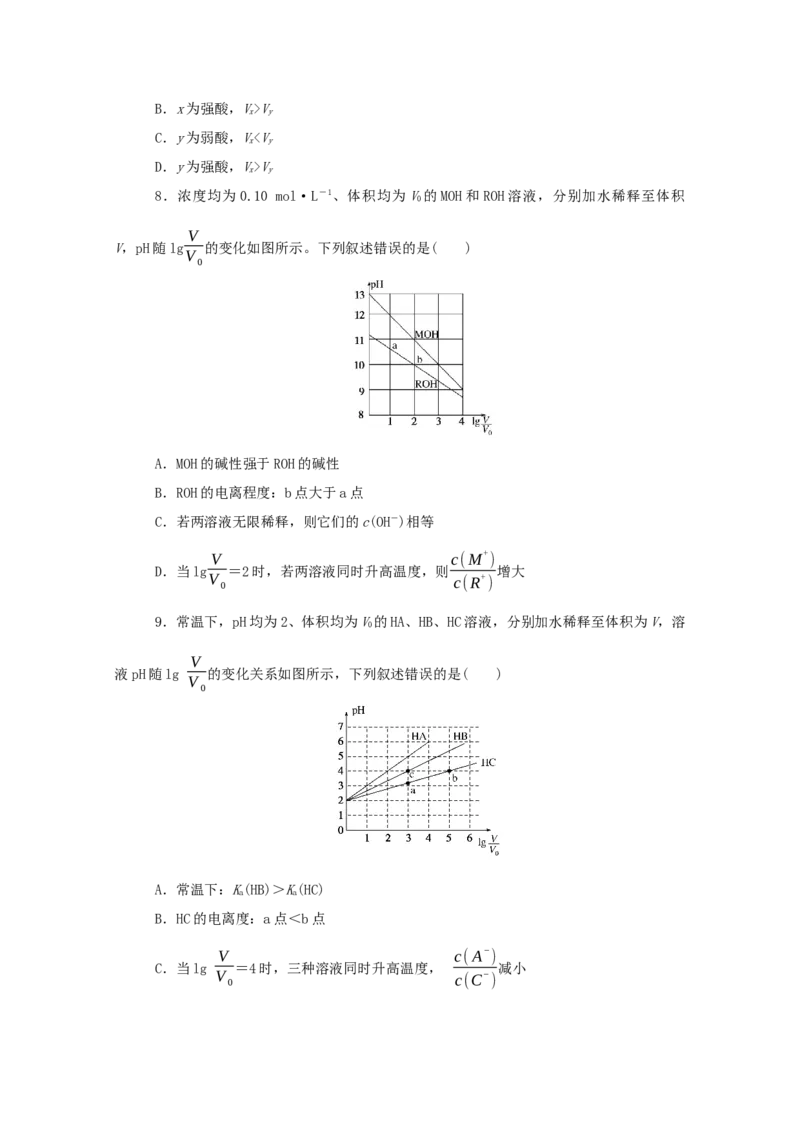
8.浓度均为0.10 mol·L-1、体积均为V的MOH和ROH溶液,分别加水稀释至体积
0
V
V,pH随lg 的变化如图所示。下列叙述错误的是( )
V
0
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
V c(M+ )
D.当lg =2时,若两溶液同时升高温度,则 增大
V c(R+
)
0
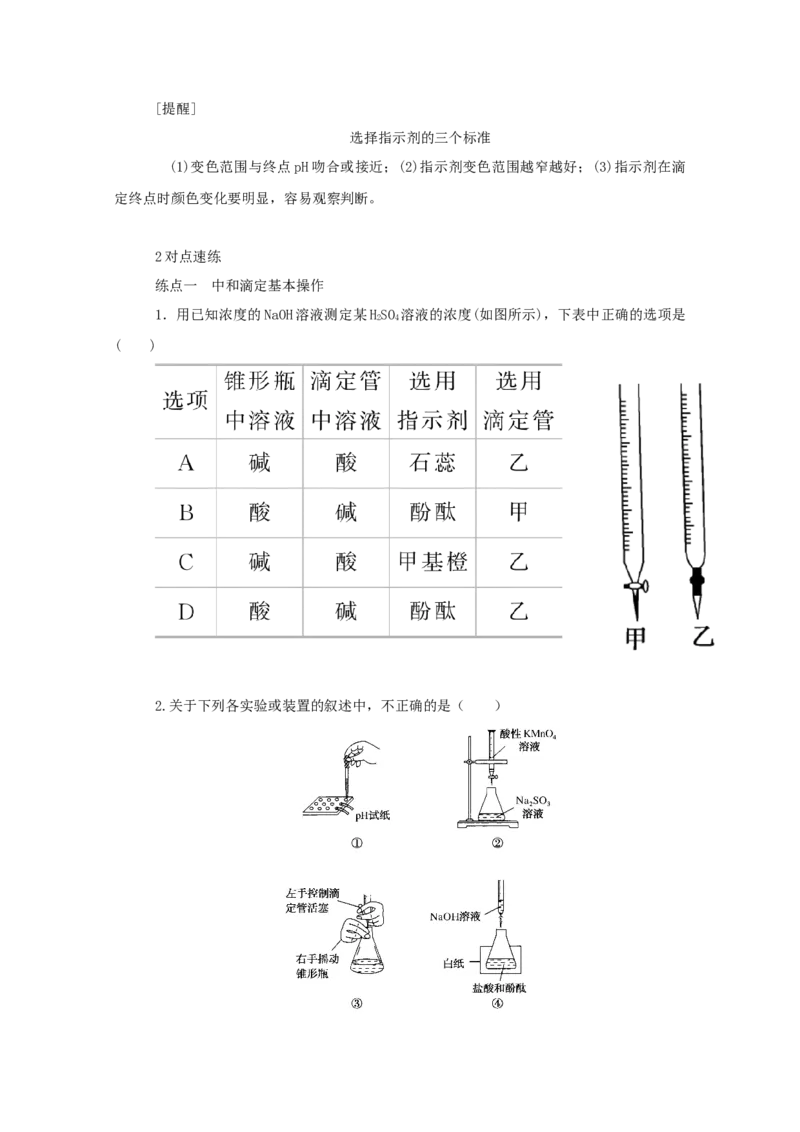
9.常温下,pH均为2、体积均为V的HA、HB、HC溶液,分别加水稀释至体积为V,溶
0
V
液pH随lg 的变化关系如图所示,下列叙述错误的是( )
V
0
A.常温下:K(HB)>K(HC)
a a
B.HC的电离度:a点<b点
V c(A− )
C.当lg =4时,三种溶液同时升高温度, 减小
V
0
c(C−
)V
D.当lg =5时,HA溶液的pH为7
V
0考点三 酸碱中和滴定
1知识梳理
1.实验原理
(1)概念:用已知物质的量浓度的________来测定未知物质的量浓度的________的方法。
c ×V
标 标
(2)计算公式:c = (以一元酸与一元碱的滴定为例)。
待 V
待
2.酸碱中和滴定的关键
(1)准确测定参加反应的酸、碱溶液的________。
(2)选取适当指示剂,准确判断________。
3.仪器与试剂
(1)主要仪器:__________、__________、铁架台(带滴定管夹)、______、大烧杯。
(2)试剂
标准液、待测液、指示剂、蒸馏水。
4.中和滴定实验操作
(1)滴定前的准备。
(2)滴定。(3)终点判断:等到滴入最后一滴反应液,指示剂变色,且在________内不能恢复原来
的颜色,视为滴定终点,并记录标准液的体积。
(4)数据处理:按上述操作重复2~3次,求出用去标准盐酸体积的平均值,根据原理
计算。
5.常用酸碱指示剂及变色范围
指示剂 变色范围的pH
石蕊 <5.0红色 5.0~8.0__色 >8.0蓝色
甲基橙 <3.1__色 3.1~4.4橙色 >4.4黄色
酚酞 <8.2无色 8.2~10.0____色 >10.0__色
[思考]
下列滴定中,写出指示剂和滴定终点颜色变化
已知:2KMnO+5KSO+3HSO===6KSO+2MnSO+3HO、I+NaS===2NaI+S↓
4 2 3 2 4 2 4 4 2 2 2
滴定终点颜色变
选项 滴定管中的溶液 锥形瓶中的溶液 指示剂
化
(1) NaOH溶液 CHCOOH溶液 ________ ________
3
(2) HCl溶液 氨水 ________ ________
(3) 酸性KMnO 溶液 KSO 溶液 无 ________
4 2 3
(4) 碘水 亚硫酸溶液 ________ ________
[判断] (正确的打“√”,错误的打“×”)
(1)滴定终点就是酸碱恰好中和的点( )
(2)滴定管盛标准液时,其液面一定要调在0刻度( )
(3)用碱式滴定管量取20.00 mL KMnO 溶液( )
4
(4)滴定管在加入反应液之前一定要用所要盛装的反应液润洗2~3遍( )
(5)若用标准盐酸滴定待测NaOH溶液,滴定前仰视,滴定后俯视则测定值偏大( )
(6)中和滴定操作中所需标准溶液越浓越好,指示剂一般加入2~3 mL( )
(7)中和滴定实验中,必须用待装标准液润洗滴定管,用待测液润洗锥形瓶( )
(8)中和滴定时,眼睛必须注视滴定管中的液面变化( )[提醒]
选择指示剂的三个标准
(1)变色范围与终点pH吻合或接近;(2)指示剂变色范围越窄越好;(3)指示剂在滴
定终点时颜色变化要明显,容易观察判断。
2对点速练
练点一 中和滴定基本操作
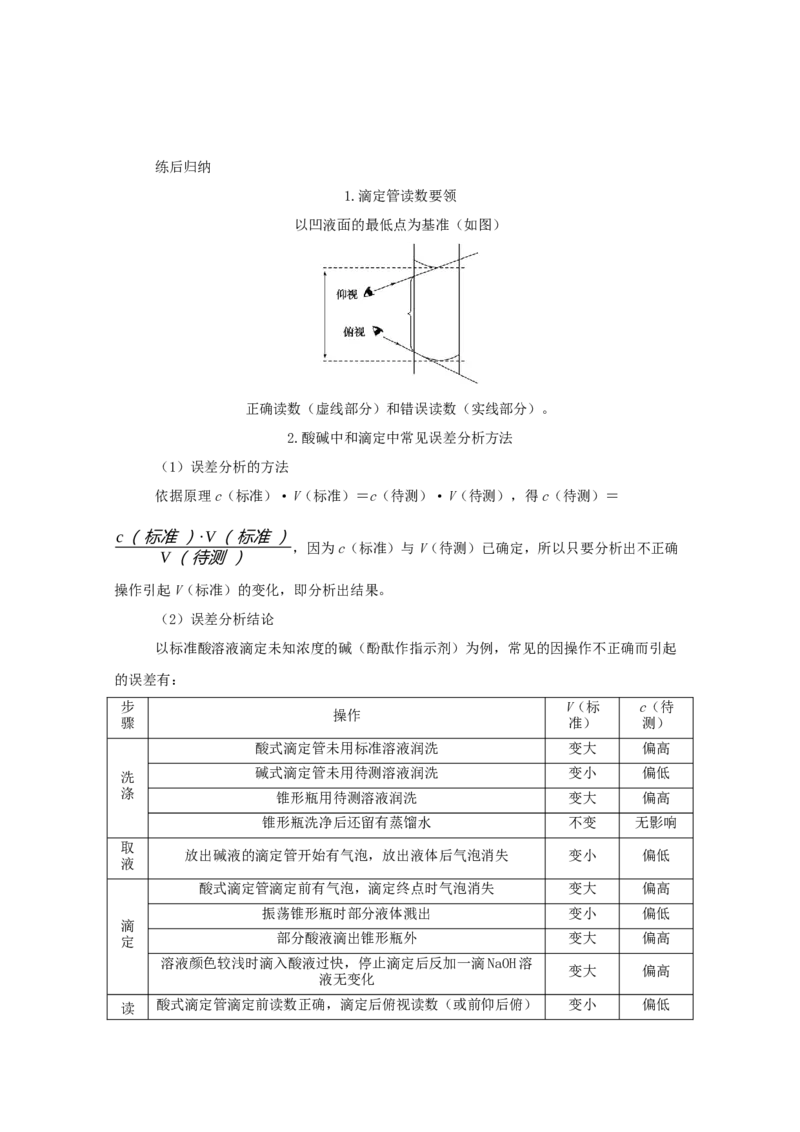
1.用已知浓度的NaOH溶液测定某HSO 溶液的浓度(如图所示),下表中正确的选项是
2 4
( )
2.关于下列各实验或装置的叙述中,不正确的是( )A.实验①可用于测溶液pH
B.实验②是用酸性KMnO 溶液滴定
4
C.装置③是滴定操作时手的操作
D.装置④中最后一滴NaOH标准液使溶液由无色变为红色,即达到滴定终点
3.某学生用0.150 0 mol·L-1NaOH溶液测定某未知浓度的盐酸,其操作可分解为如下
几步:( )
A.用蒸馏水洗净滴定管
B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸25.00mL,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作2~3次
E.检查滴定管是否漏水
F.取下碱式滴定管用标准NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上
2~3 cm处,再把碱式滴定管固定好,调节液面到“0”刻度或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记
下滴定管液面所在刻度
完成以下填空:
(1)滴定时正确操作的顺序是(用字母填写): → →F→
→ → →D
(2)操作F中应该选择如图中滴定管 (填“甲”或“乙”)。
(3)滴定时边滴边摇动锥形瓶,眼睛应注意观察 。
滴 定 终 点 溶 液 颜 色 的 变 化 是
________________________________________________________________________
________________________________________________________________________。
(4)滴定结果如表所示:
滴定次数 待测液体积/mL 标准溶液的体积/ mL滴定前刻度 滴定后刻度
1 25.00 1.02 21.03
2 25.00 0.60 20.60
3 25.00 0.20 20.19
计算该盐酸的物质的量浓度为 (精确至0.000 1)。
练点二 数据处理与误差分析
4.实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可
能使测定结果偏低的是( )
A.用量筒量取NaOH溶液时仰视读数
B.滴定结束后,滴定管尖嘴处有一悬挂液滴
C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
5.欲测定某NaOH溶液的物质的量浓度,可用0.100 0 mol·L-1的盐酸标准溶液进行
中和滴定(用甲基橙作指示剂)。
请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为 。
(2)盛装标准盐酸的仪器名称为 。
(3)滴定至终点的颜色变化为 。
(4)若甲学生在实验过程中,记录滴定前滴定管内液面读数为 0.50 mL,滴定后液面
如图,则此时消耗标准溶液的体积为 。
(5)乙学生做了三组平行实验,数据记录如下:
0.1000mol·L-1HCl溶液的体积/
mL
实验序号 待测NaOH溶液的体积/mL
滴定前刻度 滴定后刻度
1 25.00 0.00 26.29
2 25.00 1.00 31.00
3 25.00 1.00 27.31
选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为 。(保留四位有效数字)
(6)下列哪些操作会使测定结果偏高 (填字母)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数练后归纳
1.滴定管读数要领
以凹液面的最低点为基准(如图)
正确读数(虚线部分)和错误读数(实线部分)。
2.酸碱中和滴定中常见误差分析方法
(1)误差分析的方法
依据原理c(标准)·V(标准)=c(待测)·V(待测),得c(待测)=
c(标准)·V(标准)
,因为c(标准)与V(待测)已确定,所以只要分析出不正确
V(待测)
操作引起V(标准)的变化,即分析出结果。
(2)误差分析结论
以标准酸溶液滴定未知浓度的碱(酚酞作指示剂)为例,常见的因操作不正确而引起
的误差有:
步 V(标 c(待
操作
骤 准) 测)
酸式滴定管未用标准溶液润洗 变大 偏高
碱式滴定管未用待测溶液润洗 变小 偏低
洗
涤
锥形瓶用待测溶液润洗 变大 偏高
锥形瓶洗净后还留有蒸馏水 不变 无影响
取
放出碱液的滴定管开始有气泡,放出液体后气泡消失 变小 偏低
液
酸式滴定管滴定前有气泡,滴定终点时气泡消失 变大 偏高
振荡锥形瓶时部分液体溅出 变小 偏低
滴
定 部分酸液滴出锥形瓶外 变大 偏高
溶液颜色较浅时滴入酸液过快,停止滴定后反加一滴NaOH溶
变大 偏高
液无变化
读 酸式滴定管滴定前读数正确,滴定后俯视读数(或前仰后俯) 变小 偏低数 酸式滴定管滴定前读数正确,滴定后仰视读数(或前俯后仰) 变大 偏高
练点三 滴定曲线分析
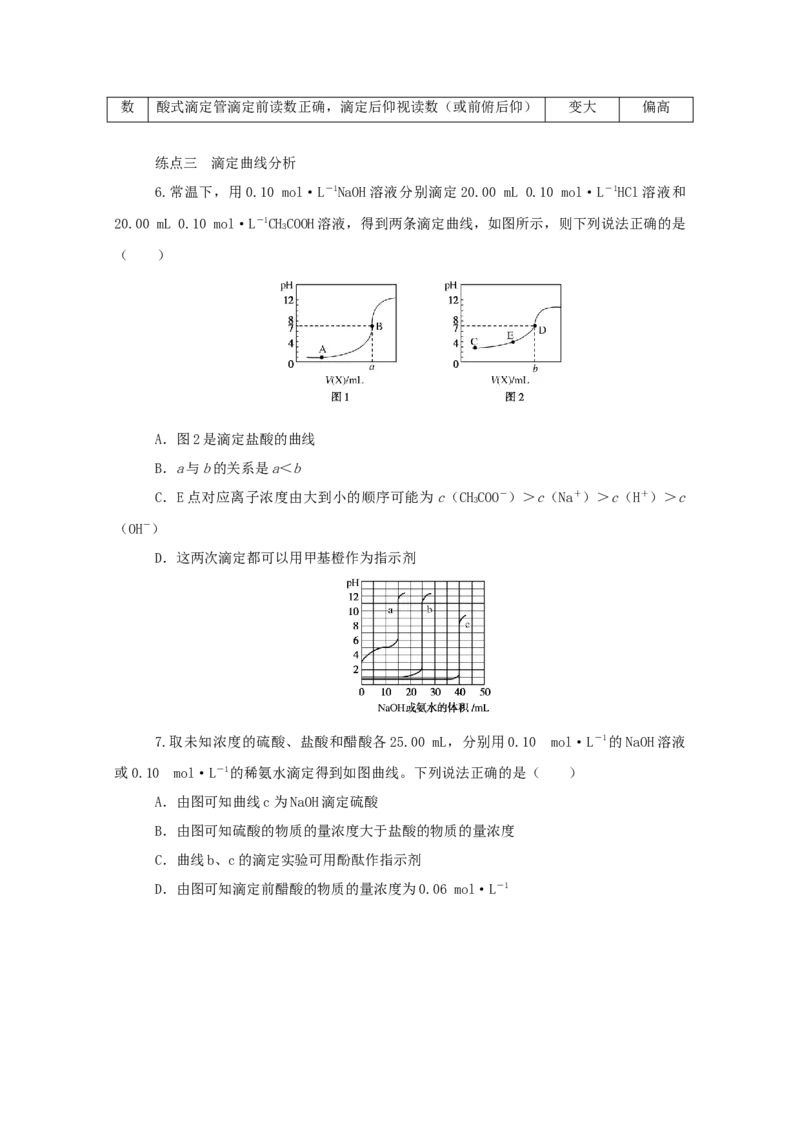
6.常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00 mL 0.10 mol·L-1HCl溶液和
20.00 mL 0.10 mol·L-1CHCOOH溶液,得到两条滴定曲线,如图所示,则下列说法正确的是
3
( )
A.图2是滴定盐酸的曲线
B.a与b的关系是a<b
C.E点对应离子浓度由大到小的顺序可能为c(CHCOO-)>c(Na+)>c(H+)>c
3
(OH-)
D.这两次滴定都可以用甲基橙作为指示剂
7.取未知浓度的硫酸、盐酸和醋酸各25.00 mL,分别用0.10 mol·L-1的NaOH溶液
或0.10 mol·L-1的稀氨水滴定得到如图曲线。下列说法正确的是( )
A.由图可知曲线c为NaOH滴定硫酸
B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度
C.曲线b、c的滴定实验可用酚酞作指示剂
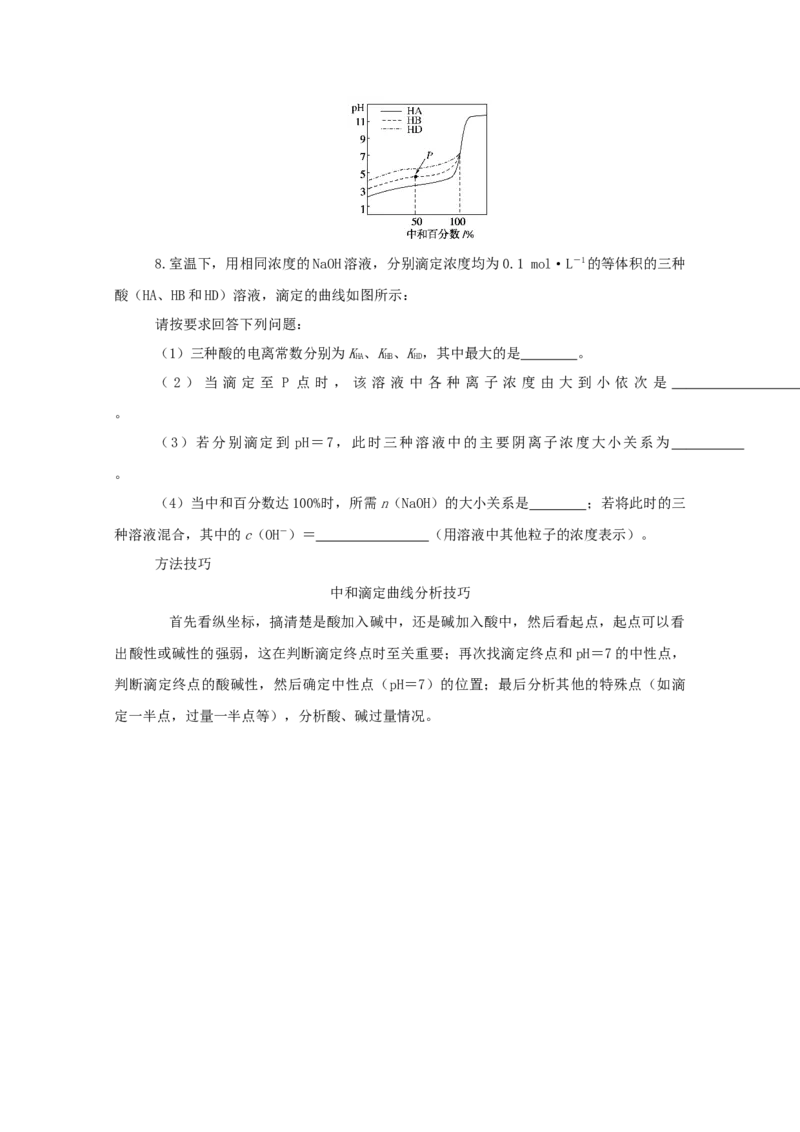
D.由图可知滴定前醋酸的物质的量浓度为0.06 mol·L-18.室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1 mol·L-1的等体积的三种
酸(HA、HB和HD)溶液,滴定的曲线如图所示:
请按要求回答下列问题:
(1)三种酸的电离常数分别为K、K、K,其中最大的是 。
HA HB HD
( 2 ) 当 滴 定 至 P 点 时 , 该 溶 液 中 各 种 离 子 浓 度 由 大 到 小 依 次 是
。
(3)若分别滴定到 pH=7,此时三种溶液中的主要阴离子浓度大小关系为
。
(4)当中和百分数达100%时,所需n(NaOH)的大小关系是 ;若将此时的三
种溶液混合,其中的c(OH-)= (用溶液中其他粒子的浓度表示)。
方法技巧
中和滴定曲线分析技巧
首先看纵坐标,搞清楚是酸加入碱中,还是碱加入酸中,然后看起点,起点可以看
出酸性或碱性的强弱,这在判断滴定终点时至关重要;再次找滴定终点和pH=7的中性点,
判断滴定终点的酸碱性,然后确定中性点(pH=7)的位置;最后分析其他的特殊点(如滴
定一半点,过量一半点等),分析酸、碱过量情况。本讲真题研练
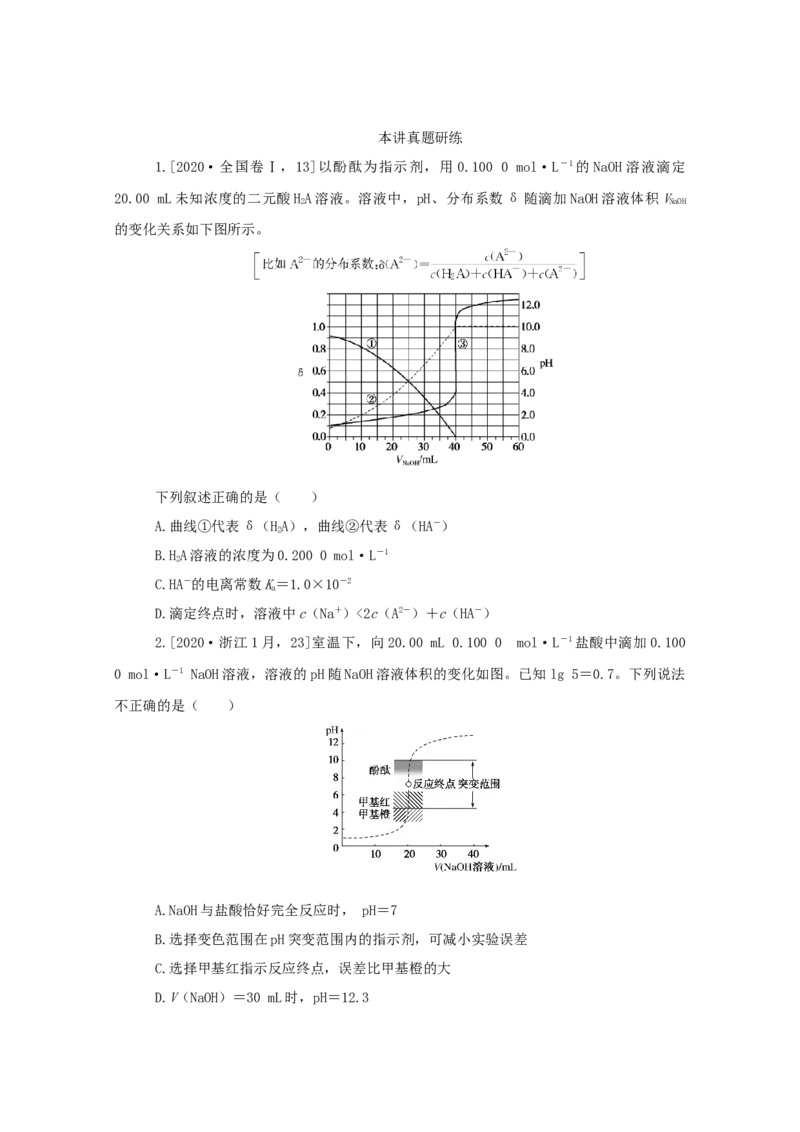
1.[2020·全国卷Ⅰ,13]以酚酞为指示剂,用 0.100 0 mol·L-1的NaOH溶液滴定
20.00 mL未知浓度的二元酸HA溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V
2 NaOH
的变化关系如下图所示。
下列叙述正确的是( )
A.曲线①代表δ(HA),曲线②代表δ(HA-)
2
B.HA溶液的浓度为0.200 0 mol·L-1
2
C.HA-的电离常数K=1.0×10-2
a
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
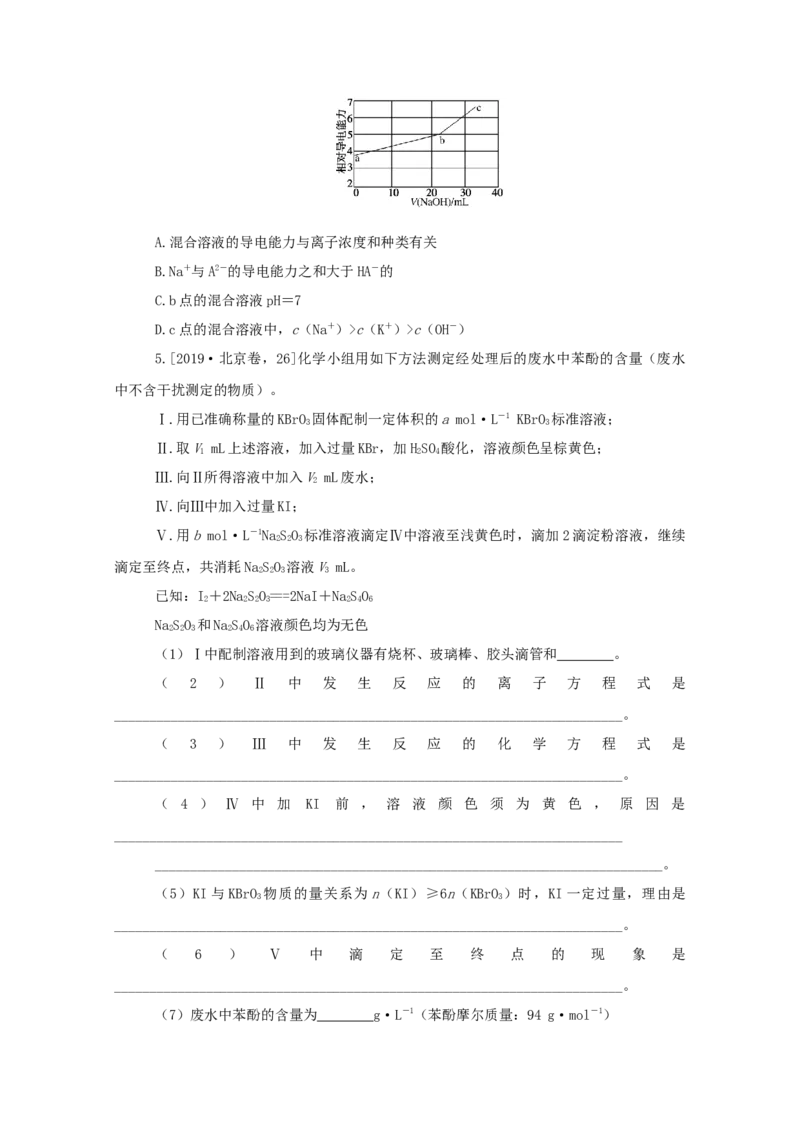
2.[2020·浙江1月,23]室温下,向20.00 mL 0.100 0 mol·L-1盐酸中滴加0.100
0 mol·L-1 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图。已知lg 5=0.7。下列说法
不正确的是( )
A.NaOH与盐酸恰好完全反应时, pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30 mL时,pH=12.33.[2020·江苏卷,18]次氯酸钠溶液和二氯异氰尿酸钠(CNOClNa)都是常用的杀
3 3 3 2
菌消毒剂。NaClO可用于制备二氯异氰尿酸钠。
(1)NaClO溶液可由低温下将Cl 缓慢通入NaOH溶液中而制得。制备NaClO的离子方
2
程式为 ;用于环境杀菌消毒的NaClO溶液须稀释并及时
使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是
________________________________________________________________________
________________________________________________________________________。
(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠
样品是否达到优质品标准。实验检测原理为
CNOCl− +H++2HO===CHNO+2HClO
3 3 3 2 2 3 3 3 3
HClO+2I-+H+===I+Cl-+HO
2 2
I+2SO2− ===SO2− +2I-
2 2 3 4 6
准确称取1.120 0 g样品,用容量瓶配成250.0 mL溶液;取25.00 mL上述溶液于碘
量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5 min;用0.100 0 mol·L-1
NaSO 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗NaSO 溶液
2 2 3 2 2 3
20.00 mL。
①通过计算判断该样品是否为优质品。
(写出计算过程,该样品的有效氯=
测定中转化为HClO的氯元素×质2 量
×100%)
样品质量
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值 (填“偏
高”或“偏低”)。
4.[2019·全国卷Ⅰ,11]NaOH 溶液滴定邻苯二甲酸氢钾(邻苯二甲酸 HA 的K =
2 a1
1.1×10-3 ,K =3.9×10-6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中 b点
a2
为反应终点。下列叙述错误的是( )A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2-的导电能力之和大于HA-的
C.b点的混合溶液pH=7
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH-)
5.[2019·北京卷,26]化学小组用如下方法测定经处理后的废水中苯酚的含量(废水
中不含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO 固体配制一定体积的a mol·L-1 KBrO 标准溶液;
3 3
Ⅱ.取V mL上述溶液,加入过量KBr,加HSO 酸化,溶液颜色呈棕黄色;
1 2 4
Ⅲ.向Ⅱ所得溶液中加入V mL废水;
2
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L-1NaSO 标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续
2 2 3
滴定至终点,共消耗NaSO 溶液V mL。
2 2 3 3
已知:I+2NaSO===2NaI+NaSO
2 2 2 3 2 4 6
NaSO 和NaSO 溶液颜色均为无色
2 2 3 2 4 6
(1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和 。
( 2 ) Ⅱ 中 发 生 反 应 的 离 子 方 程 式 是
________________________________________________________________________。
( 3 ) Ⅲ 中 发 生 反 应 的 化 学 方 程 式 是
________________________________________________________________________。
( 4 ) Ⅳ 中 加 KI 前 , 溶 液 颜 色 须 为 黄 色 , 原 因 是
________________________________________________________________________
________________________________________________________________________。
(5)KI与KBrO 物质的量关系为n(KI)≥6n(KBrO )时,KI一定过量,理由是
3 3
________________________________________________________________________。
( 6 ) Ⅴ 中 滴 定 至 终 点 的 现 象 是
________________________________________________________________________。
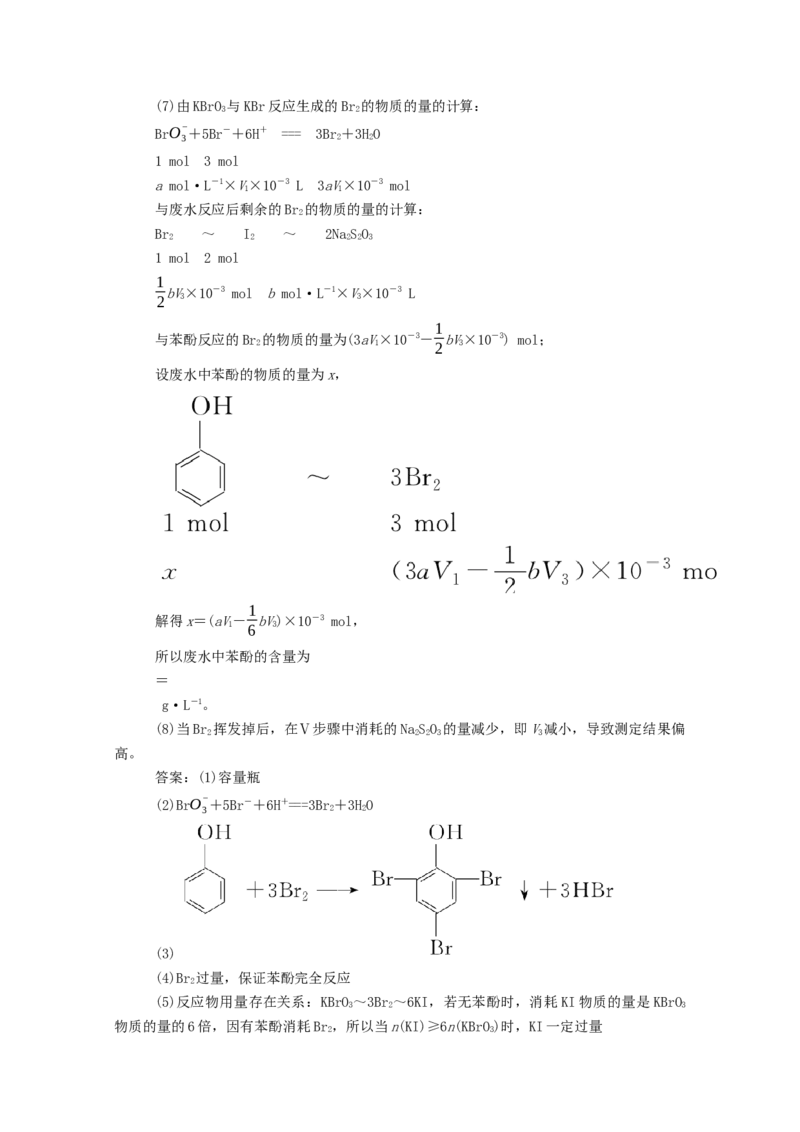
(7)废水中苯酚的含量为 g·L-1(苯酚摩尔质量:94 g·mol-1)(8)由于Br 具有 性质,Ⅱ~Ⅳ中反应须在密闭容器中进行,否则会造成测
2
定结果偏高。
第2讲 水的电离和溶液的pH
考点一
1知识梳理
1.H
2
O+H
2
OH
3
O++OH- H
2
OH++OH-
2.(1)1×10-14 (2)温度 增大 (3)电解质
3.(1)增大 增大 (2)减小 不变 (3)增大 不变
思考 答案:
逆 不变 减小 减小 增大
逆 不变 减小 增大 减小
正 不变 增大 增大 减小
正 不变 增大 减小 增大
正 增大 增大 增大 增大
逆 减小 减小 减小 减小
正 不变 增大 增大 减小
判断 答案:(1)× (2)× (3)× (4)× (5)× (6)×
2对点速练
1.解析:A项,K应不变;C项,平衡应正向移动;D项,由于没有指明温度,c(H+)
w
不一定等于10-7 mol·L-1。
答案:B
2.解析:100 ℃时,K=c(H+)·c(OH-)=10-12,中性溶液中c(H+)=c(OH-)=√K
w w
=10-6 mol·L-1,即pH=6,此温度下pH=7的溶液呈碱性,A项错误;NHCl、CHCOONa、
4 3
NaHCO 促进水的电离,NaHSO 抑制水的电离,B项错误;烧碱是NaOH,抑制水的电离,纯碱
3 4
是NaCO ,促进水的电离,C项错误;图中A点到C点,c(H+)与c(OH-)同等程度增大,说明
2 3
是温度升高的结果,D项正确。
答案:D
3.解析:c点时,CHCOOH和NaOH恰好完全反应,得到CHCOONa溶液,由于CHCOO-
3 3 3
水解,溶液呈碱性,A项错误;b点时,反应得到等物质的量浓度的CHCOOH、CHCOONa的混
3 3
合溶液,根据物料守恒得2c(Na+)=c(CHCOOH)+c(CHCOO-),B项正确;b点为等物质的量
3 3
浓度的 CHCOOH、CHCOONa的混合溶液,c点为 CHCOONa溶液,d点为等物质的量浓度的
3 3 3
NaOH、CHCOONa的混合溶液,故c点水的电离程度最大,C项错误;中和热与酸碱的用量无
3关 ,中和热保持不变,D项错误。
答案:B
4.解析:由水的离子积的定义知两条曲线间任意点均有c(H+)·c(OH-)=K,A项正
w
确;由图中纵横轴的大小可知M区域内任意点均有c(H+)<c(OH-),B项正确;温度越高,水
的电离程度越大,电离出的c(H+)与c(OH-)越大,所以T>T,C项正确;XZ线上任意点都
2 1
有c(H+)=c(OH-),只有当c(H+)=10-7mol·L-1时,才有pH=7,D项错误。
答案:D
5.解析:根据图知,0.1 mol·L-1HA溶液的pH=3,则c(H+)<0.1 mol·L-1,说明
HA是弱酸;0.1 mol·L-1BOH溶液的pH=11,c(OH-)<0.1 mol·L-1,则BOH是弱碱,A项
c(H+ )·c(A−
)
10-3×10-3
错误;K(HA)= = ≈1×10-5,B项错误;b点是两者等体积混合
a c(HA) 0.1−10-3
溶液呈中性,c(B-)=c(A-),c(OH-)=c(H+),盐电离产生离子的浓度远大于水电离产生的
离子浓度,故c(B-)=c(A-)>c(OH-)=c(H+),C项错误;HA是弱酸,酸电离产生的H+对水
的电离平衡起抑制作用,在a→b过程中,酸被碱中和,溶液中酸电离产生的c(H+)减小,其
对水的电离的抑制作用减弱,同时生成弱酸弱碱盐(BA)对水的电离起促进作用,故a→b过程
中水的电离程度始终增大,D项正确。
答案:D
6.解析:(1)水是弱电解质,存在电离平衡,电离吸热,所以温度升高,水的电离程
度增大 ,离子积增大。
(2)水电离出的氢离子浓度和氢氧根离子浓度相同,某温度下纯水中的 c(H+)=
2.4×10-7 mol·L-1,则此时纯水中的 c(OH-)=2.4×10-7 mol·L-1,K=2.4×10-
w
7×2.4×10-7=5.76×10-14。该温度下,某HSO 溶液中c(SO2− )=5×10-6 mol·L-1,则溶
2 4 4
5.76×10-14
液中氢离子浓度是1×10-5 mol·L-1,c(OH-)= mol·L-1=5.76×10-9 mol·L
1×10-5
-1。
答案:(1)> 水的电离是吸热过程,升高温度,平衡向正反应方向移动,c(H+)增大,
c(OH-)增大,K=c(H+)·c(OH-),K增大
w w
(2)2.4×10-7 mol·L-1 5.76×10-9
考点二
1知识梳理
1.(1)> < (2)= = (3)< >
2.(1)-lgc(H+) (2)酸性 碱性 (3)玻璃片 表面皿
判断 答案:(1)√ (2)× (3)× (4)× (5)√ (6)× (7)×
2对点速练
1.解析:因为酸、碱的强弱未知,不能依据a=b判断,①错误;温度不能确定为25
℃,溶液的pH=7,c(OH-)=10-7 mol·L-1不能判断溶液呈中性,②、③错误;K=c(H
w+)·c(OH-),当c(H+)=c(OH-)=√K mol·L-1时,溶液一定呈中性,④正确;根据电荷
w
守恒c(H+)+c(B+)=c(A-)+c(OH-),当c(B+)=c(A-)时,c(H+)=c(OH-),溶液一定呈中
性,B项正确。
答案:B
2.解析:首先要掌握本题中,由水电离出的c(H+) =1×10-11 mol·L-1,则由水电
水
离出的c(OH-) =1×10-11 mol·L-1。如在酸溶液中,c(OH-) =c(OH-) =1×10-11
水 溶液 水
mol·L-1,此时c(H+)=1×10-3 mol·L-1,pH=3,溶液显酸性;又如在碱溶液中c(H+)
溶液
=c(H+) =1×10-11 mol·L-1,此时溶液的pH=11,溶液显碱性。
水
答案:C
3.解析:若a=b且c(X-)>c(Y-),这说明电离程度HX>HY,则酸性:HX>HY,A正
确;若a>b且c(X-)=c(Y-),这说明电离程度:HX<HY,则酸性:HX<HY,B错误;若a<
b且两者pH 相同,这说明电离出的氢离子浓度相等,则HY一定是弱酸,C正确;若向HX溶
液中加入等浓度、等体积的NaOH溶液,所得溶液pH>7,这说明X-水解,则HX为弱酸,D正
确。
答案:B
4.解析:一水合氨为弱电解质,加水稀释,促进其电离,溶液pH变化比强碱的小,
故将pH=a的氨水稀释10倍后,其pH=b,则aK>K 。(2)滴定至P点时,溶液中未反应的
HA HB HD
HB与生成的NaB的浓度相等,且溶液呈酸性,说明HB的电离程度大于B-的水解程度,故c(B
-)>c(Na+)>c(HB)>c(H+)>c(OH-)。(3)pH=7时,根据电荷守恒,三种离子的浓度分别等于
c(Na+),然而三种溶液中阴离子水解程度不同,pH=7时加入的NaOH的体积不同,即酸性越
强,加入氢氧化钠越多,钠离子浓度越大,所以c(A-)>c(B-)>c(D-)。(4)中和百分数100%
指的是三种酸恰好完全反应,根据酸的物质的量相同,所以需要氢氧化钠的量完全相同;根
据质子守恒即可得出,完全中和后的三种溶液混合后溶液的质子守恒关系:c(HA)+c(HB)+
c(HD)+c(H+)=c(OH-)。
答案:(1)K
HA
(2)c(B-)>c(Na+)>c(H+)>c(OH-)
(3)c(A-)>c(B-)>c(D-)
(4)相等 c(HA)+c(HB)+c(HD)+c(H+)
本讲真题研练
1.解析:由题图可知加入NaOH溶液的体积为40 mL时,溶液pH发生突跃,达到滴定
1 1
终点,溶质为NaA,故有n(HA)=20.00 mL×c(HA)= n(NaOH)= ×0.100 0 mol/L×40
2 2 2 2 2
mL,则c(HA)=0.100 0 mol/L,而起点时pH约为1,故HA的电离过程应为HA===HA-+H
2 2 2
+,HA-A2-+H+,故曲线①表示δ(HA-),曲线②表示δ(A2-),A、B项错误;由K=
a
c(A2- )·c(H+
)
,V 等于25 mL时,pH=2.0,且c(A2-)=c(HA-),可知K=1.0×10-2,
c(H A- ) NaOH a
C项正确;以酚酞作指示剂,滴定终点时的溶质为 NaA,溶液呈碱性,根据电荷守恒c(Na+)
2
+c(H+)=c(OH-)+c(HA-)+2c(A2-),结合c(H+)c(HA-)+2c(A2
-),D项错误。
答案:C2.解析:本题考查酸碱中和滴定过程中溶液pH随NaOH溶液体积变化的关系。由题图
可知,甲基橙变色范围在突变范围之外,甲基红变色范围在突变范围内,接近反应终点,甲
基橙误差会更大,C错误;因为是一元强酸与一元强碱之间的反应,恰好完全反应时pH=7,
A正确;指示剂的变色范围应该在中和滴定pH突变范围内,这样的误差较小,B正确;当消
耗NaOH溶液体积为30 mL时,反应后溶液中c(OH-)=0.02 mol·L-1,pH约为12.3,D正
确。
答案:C
3.解析:本题考查离子方程式书写、次氯酸的性质、滴定计算等。(1)Cl 与NaOH反
2
应生成NaCl、NaClO和HO。HClO的酸性弱于HCO ,则NaClO溶液露置于空气中,与空气中
2 2 3
CO 反应产生HClO,HClO见光易分解,故会导致消毒作用减弱。(2)①依据三个反应得出关
2
系式:CNOCI−
~2HClO~2I
~4SO2−
,根据NaSO 的消耗量,可以计算出测定中转化为
3 3 3 2 2 2 3 2 2 3
HClO 的 氯 的 物 质 的 量 , 进 而 得 出 氯 元 素 的 质 量 , 再 由 有 效 氯 的 计 算 公 式
测定中转化为HClO的氯元素×质2 量
×100%,可计算出有效氯。②加入的稀硫酸的量
样品质量
过少,则生成的I 少,消耗NaSO 的量减少,则计算出的HClO的量偏少,导致样品的有效
2 2 2 3
氯测定值偏低。
答案:(1)Cl +2OH-===ClO-+Cl-+HO NaClO溶液吸收空气中的CO 后产生HClO,
2 2 2
HClO见光分解
(2)①n(SO2− )=0.100 0 mol·L-1×0.020 00 L=2.000×10-3 mol
2 3
根据物质转换和得失电子守恒关系:CNOCl−
~2HClO~2I
~4SO2−
得n(Cl)=0.5n(S
3 3 3 2 2 2 3 2
O2− )=1.000×10-3 mol
3
氯元素的质量:
m(Cl)=1.000×10-3 mol×35.5 g·mol-1=0.035 50 g
0.035 50 g
该样品的有效氯为: 25.00mL ×2×100%=63.39%
1.120 0 g×
250.00mL
该样品的有效氯大于60%,故该样品为优质品
②偏低
4.解析:KHA与NaOH反应的过程中引入了Na+,HA-转化为A2-,由图像可知a到b过
程中导电能力逐渐增强,A、B项正确;b点时,KHA与NaOH恰好完全反应生成正盐,A2-水解
使溶液呈碱性,C项错误;b点时,Na+、K+浓度相等,继续滴加NaOH溶液至c点,c(Na+)增
大,由图可知c(OH-)小于c(K+),D项正确。
答案:C
5.解析:(1)配制标准溶液用到的玻璃仪器除了给出的三种仪器外,还有容量瓶。
(4)溶液为黄色说明仍有Br 存在,此时废水中的苯酚已完全反应。
2
(5)假设废水中没有苯酚,KBrO 和KBr反应生成的Br 完全和KI反应时,消耗KI的物
3 2
质的量刚好是KBrO 的6倍。实际上苯酚一定会消耗一定量的Br ,所以当n(KI):n(KBrO)=
3 2 3
6:1时,KI就已经过量了。(7)由KBrO 与KBr反应生成的Br 的物质的量的计算:
3 2
BrO− +5Br-+6H+ === 3Br+3HO
3 2 2
1 mol 3 mol
a mol·L-1×V×10-3 L 3aV×10-3 mol
1 1
与废水反应后剩余的Br 的物质的量的计算:
2
Br ~ I ~ 2NaSO
2 2 2 2 3
1 mol 2 mol
1
bV×10-3 mol b mol·L-1×V×10-3 L
2 3 3
1
与苯酚反应的Br 的物质的量为(3aV×10-3- bV×10-3) mol;
2 1 2 3
设废水中苯酚的物质的量为x,
1
解得x=(aV- bV)×10-3 mol,
1 6 3
所以废水中苯酚的含量为
=
g·L-1。
(8)当Br 挥发掉后,在Ⅴ步骤中消耗的NaSO 的量减少,即V减小,导致测定结果偏
2 2 2 3 3
高。
答案:(1)容量瓶
(2)BrO− +5Br-+6H+===3Br+3HO
3 2 2
(3)
(4)Br 过量,保证苯酚完全反应
2
(5)反应物用量存在关系:KBrO ~3Br ~6KI,若无苯酚时,消耗KI物质的量是KBrO
3 2 3
物质的量的6倍,因有苯酚消耗Br,所以当n(KI)≥6n(KBrO)时,KI一定过量
2 3(6)溶液蓝色恰好消失
(7)
(8)易挥发