文档内容
专项提能特训 11 电解原理在工农业生产中的应用
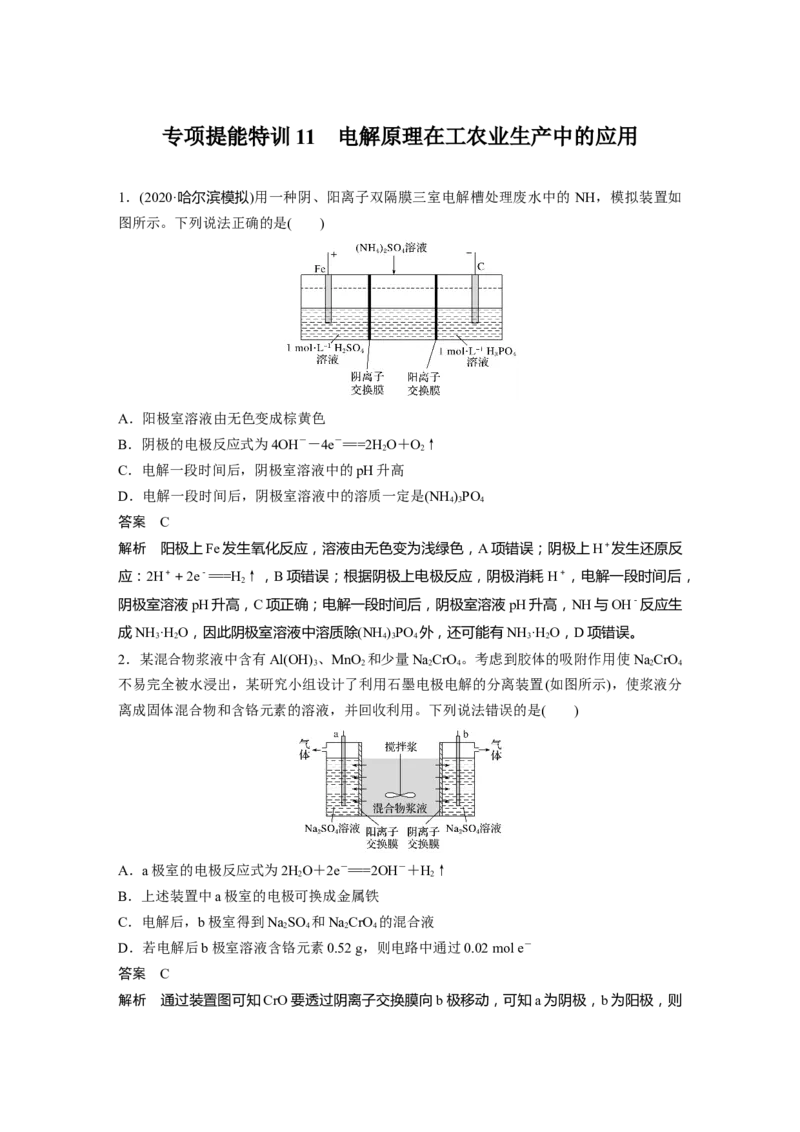
1.(2020·哈尔滨模拟)用一种阴、阳离子双隔膜三室电解槽处理废水中的 NH,模拟装置如
图所示。下列说法正确的是( )
A.阳极室溶液由无色变成棕黄色
B.阴极的电极反应式为4OH--4e-===2HO+O↑
2 2
C.电解一段时间后,阴极室溶液中的pH升高
D.电解一段时间后,阴极室溶液中的溶质一定是(NH )PO
4 3 4
答案 C
解析 阳极上Fe发生氧化反应,溶液由无色变为浅绿色,A项错误;阴极上H+发生还原反
应:2H++2e-===H↑,B项错误;根据阴极上电极反应,阴极消耗 H+,电解一段时间后,
2
阴极室溶液pH升高,C项正确;电解一段时间后,阴极室溶液pH升高,NH与OH-反应生
成NH ·H O,因此阴极室溶液中溶质除(NH )PO 外,还可能有NH ·H O,D项错误。
3 2 4 3 4 3 2
2.某混合物浆液中含有Al(OH) 、MnO 和少量NaCrO。考虑到胶体的吸附作用使NaCrO
3 2 2 4 2 4
不易完全被水浸出,某研究小组设计了利用石墨电极电解的分离装置(如图所示),使浆液分
离成固体混合物和含铬元素的溶液,并回收利用。下列说法错误的是( )
A.a极室的电极反应式为2HO+2e-===2OH-+H↑
2 2
B.上述装置中a极室的电极可换成金属铁
C.电解后,b极室得到NaSO 和NaCrO 的混合液
2 4 2 4
D.若电解后b极室溶液含铬元素0.52 g,则电路中通过0.02 mol e-
答案 C
解析 通过装置图可知CrO要透过阴离子交换膜向b极移动,可知a为阴极,b为阳极,则a极室的电极反应式为2HO+2e-===2OH-+H↑,A说法正确;a极上发生还原反应,故
2 2
将电极换成铁电极,Fe 不会被消耗,B 说法正确;电解时 b 极发生反应:2HO-4e-
2
===O↑+4H+,b极产生H+,发生反应2CrO+2H+Cr O+HO,因此b极室还有Cr O
2 2 2 2
存在,C说法错误;0.52 g铬元素的物质的量为0.01 mol,说明有0.01 mol CrO透过阴离子
交换膜,则电路中通过0.02 mol电子,D说法正确。
3.NaFeO 是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常
2 4
利用如图装置生产NaFeO,下列有关说法不正确的是( )
2 4
A.右侧电极反应式:
Fe+8OH--6e-===FeO+4HO
2
B.左侧为阳离子交换膜,当Cu电极生成1 mol气体时,有2 mol Na+通过阳离子交换膜
C.可以将左侧流出的氢氧化钠补充到该装置中部,以保证装置连续工作
D.NaFeO 具有强氧化性且产物为Fe3+,因此可以利用NaFeO 除去水中的细菌、固体颗
2 4 2 4
粒以及Ca2+等
答案 D
解析 根据图示,Cu电极为阴极,Fe电极为阳极。右侧电极为Fe电极,Fe失去电子发生
氧化反应生成FeO,结合原子守恒和电荷守恒可得电极反应式为Fe-6e-+8OH-===FeO+
4HO,A项正确;左侧为阴极室,Cu电极上的电极反应式为2HO+2e-===H↑+2OH-,
2 2 2
当Cu电极上生成1 mol气体时,同时产生2 mol OH-,此时中部有2 mol Na+通过阳离子交
换膜进入阴极室平衡电荷,B项正确;根据B项分析,阴极室生成 NaOH,左侧流出的
NaOH溶液的浓度大于加入的NaOH溶液的浓度,即b%>a%,可将左侧流出的NaOH补充
到该装置中部,以保证装置连续工作,C项正确;NaFeO 具有强氧化性,可利用NaFeO
2 4 2 4
除去水中的细菌,NaFeO 的还原产物为Fe3+,Fe3+水解生成Fe(OH) 胶体,Fe(OH) 胶体可
2 4 3 3
吸附固体颗粒,但二者均不能除去水中的Ca2+,D项错误。
4.某些无公害免农药果园利用如图所示电解装置,进行果品的安全生产,解决了农药残留
所造成的生态及健康危害问题。下列说法正确的是( )A.a为直流电源的负极,与之相连的电极为阴极
B.离子交换膜为阴离子交换膜
C.“酸性水”具有强氧化性,能够杀菌
D.阴极反应式为HO+2e-===H↑+O2-
2 2
答案 C
解析 由“碱性水”可推知b为直流电源的负极,a为直流电源的正极,A项错误;右侧生
成OH-,K+穿过离子交换膜移到右侧,即该离子交换膜为阳离子交换膜,B项错误;阳极
反应为2Cl--2e-===Cl↑,Cl +HOHCl+HClO,故“酸性水”中含HClO,具有强氧
2 2 2
化性,能杀菌,C项正确;水溶液中不可能存在O2-,D项错误。
5.城市地下潮湿的土壤中常埋有纵横交错的管道和输电线路,当有电流泄漏并与金属管道
形成回路时,就会引起金属管道的腐蚀。原理如图所示,但若电压等条件适宜,钢铁管道也
可能减缓腐蚀,此现象被称为“阳极保护”。下列有关说法不正确的是( )
A.该装置能够将电能转化为化学能
B.管道右端腐蚀比左端快,右端电极反应式为Fe-2e-===Fe2+
C.如果没有外加电源,潮湿的土壤中的钢铁管道比较容易发生吸氧腐蚀
D.钢铁“阳极保护”的实质是在阳极金属表面形成一层耐腐蚀的钝化膜
答案 B
解析 该装置相当于电解池,能将电能转化为化学能,A正确;左端是阳极,腐蚀得更快,
B错误;如果没有外加电源,潮湿的土壤(接近中性)中的钢铁管道发生原电池反应,所以发
生的是吸氧腐蚀,C正确;根据题意可知“阳极保护”实际上是在金属表面形成了一层致密
的保护膜,D正确。
6.(2020·广西南宁三中月考)FFC电解法可由金属氧化物直接电解制备金属单质,西北稀有
金属材料研究院利用此法成功电解制备钽粉(Ta),其原理如图所示。下列说法正确的是(
)A.该装置将化学能转化为电能
B.a极为电源的正极
C.TaO 极发生的电极反应式为TaO+10e-===2Ta+5O2—
2 5 2 5
D.常温常压下,石墨电极上生成22.4 L O ,则电路中转移的电子数为4N
2 A
答案 C
解析 该装置是电解池,将电能转化为化学能,A错误;电解池工作时,O2-向阳极移动,
则石墨电极为阳极,b极为电源的正极,a极为电源的负极,B错误;TaO 极为阴极,发生
2 5
还原反应,电极反应式为TaO +10e-===2Ta+5O2-,C正确;常温常压下,22.4 L O 的物
2 5 2
质的量小于1 mol,阳极还有CO和CO 生成,转移电子数无法计算,D错误。
2
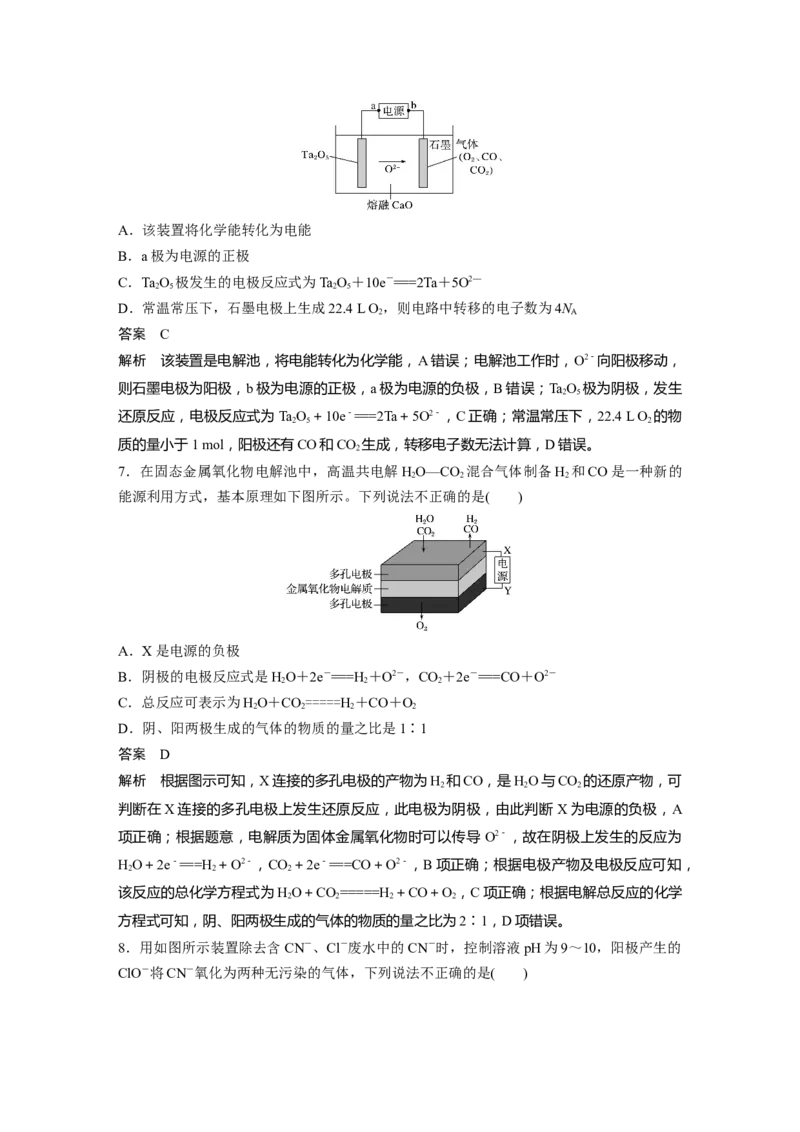
7.在固态金属氧化物电解池中,高温共电解HO—CO 混合气体制备H 和CO是一种新的
2 2 2
能源利用方式,基本原理如下图所示。下列说法不正确的是( )
A.X是电源的负极
B.阴极的电极反应式是HO+2e-===H+O2-,CO+2e-===CO+O2-
2 2 2
C.总反应可表示为HO+CO=====H+CO+O
2 2 2 2
D.阴、阳两极生成的气体的物质的量之比是1∶1
答案 D
解析 根据图示可知,X连接的多孔电极的产物为H 和CO,是HO与CO 的还原产物,可
2 2 2
判断在X连接的多孔电极上发生还原反应,此电极为阴极,由此判断 X为电源的负极,A
项正确;根据题意,电解质为固体金属氧化物时可以传导 O2-,故在阴极上发生的反应为
HO+2e-===H +O2-,CO +2e-===CO+O2-,B项正确;根据电极产物及电极反应可知,
2 2 2
该反应的总化学方程式为HO+CO=====H +CO+O ,C项正确;根据电解总反应的化学
2 2 2 2
方程式可知,阴、阳两极生成的气体的物质的量之比为2∶1,D项错误。
8.用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的
ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )A.阴极的电极反应式为2HO+2e-===H↑+2OH-
2 2
B.阳极的电极反应式为Cl-+2OH--2e-===ClO-+HO
2
C.电解时使用锂钒氧化物二次电池(V O +x Li LiVO)作电源,电池充电时a电极的
2 5 x 2 5
电极反应式为LiVO-xe-===VO+xLi+
x 2 5 2 5
D.除去CN-的反应:2CN-+5ClO-+2H+===N↑+2CO↑+5Cl-+HO
2 2 2
答案 D
解析 阳极产生的ClO-将CN-氧化为两种无污染的气体,两种气体为CO 和N ,该反应在
2 2
碱性环境中发生,反应的离子方程式不应出现H+,D项错误。
9.(2020·浙江7月选考,21)电解高浓度RCOONa(羧酸钠)的NaOH溶液,在阳极RCOO-放
电可得到R—R(烷烃)。下列说法不正确的是( )
A.电解总反应方程式:2RCOONa+2HO=====R—R+2CO↑+H↑+2NaOH
2 2 2
B.RCOO-在阳极放电,发生氧化反应
C.阴极的电极反应:2HO+2e-===2OH-+H↑
2 2
D.电解CHCOONa、CHCHCOONa和NaOH混合溶液可得到乙烷、丙烷和丁烷
3 3 2
答案 A
解析 由于电解液呈强碱性,电解反应不能释放出 CO 气体,A 错误;电解高浓度
2
RCOONa的NaOH溶液,阳极上RCOO-发生氧化反应,得到R—R(烷烃),B正确;阴极上
HO得电子放出H ,电极反应式为2HO+2e-===2OH-+H↑,C正确;根据题中电解原
2 2 2 2
理,电解 RCOONa 和NaOH 混合液可得到 R—R(烷烃),类比推理,电解 CHCOONa、
3
CHCHCOONa 和 NaOH 混合溶液,可得到 CHCH(乙烷)、CHCHCH(丙烷)和
3 2 3 3 3 2 3
CHCHCHCH(丁烷),D正确。
3 2 2 3
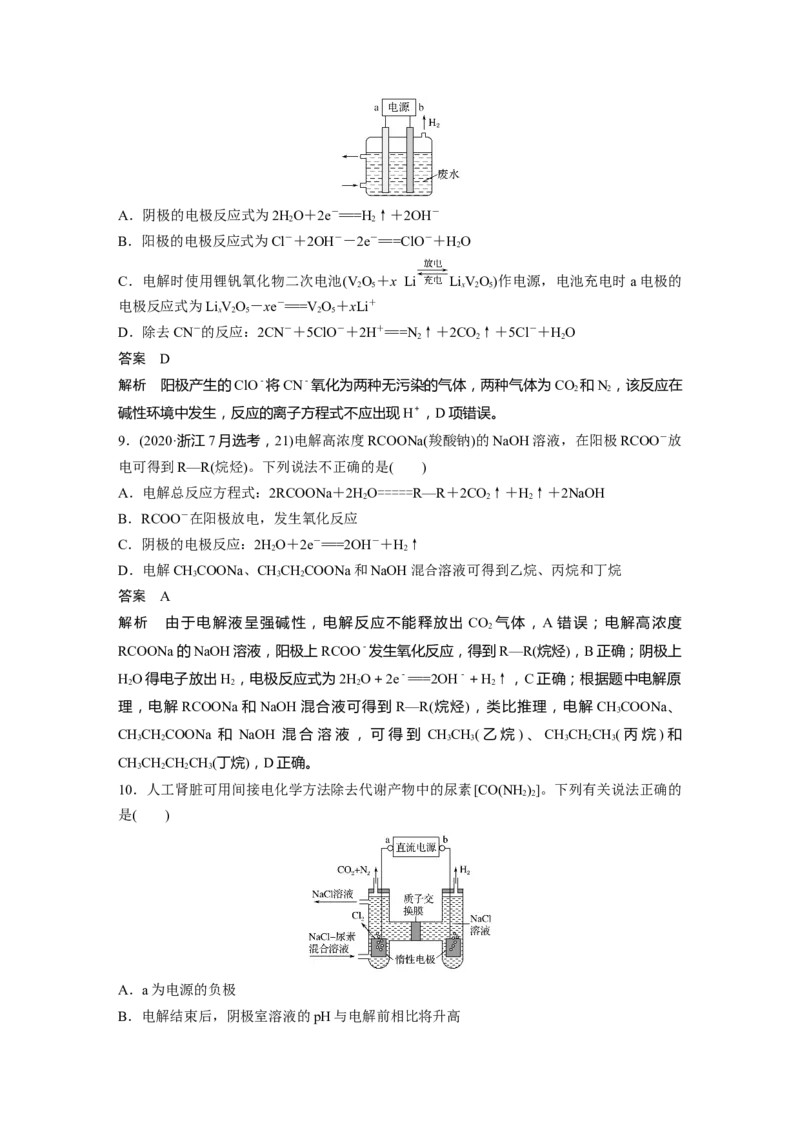
10.人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH)]。下列有关说法正确的
2 2
是( )
A.a为电源的负极
B.电解结束后,阴极室溶液的pH与电解前相比将升高C.除去尿素的反应为CO(NH)+2Cl+HO===N+CO+4HCl
2 2 2 2 2 2
D.若两极共收集到气体0.6 mol,则除去的尿素为0.12 mol(忽略气体溶解,假设氯气全部
参与反应)
答案 D
解析 由图可知,左室电极产物为CO 和N,发生氧化反应,则左室电极为阳极,a为电源
2 2
的正极,阳极反应式为6Cl--6e-===3Cl↑,CO(NH) +3Cl +HO===N +CO +6HCl,
2 2 2 2 2 2 2
右室电解产物为 H ,发生还原反应,则右室电极为阴极,b为电源负极,阴极反应式为
2
6HO+6e-===6OH-+3H↑。由上述分析可知,a为电源的正极,A项错误;根据上述反应
2 2
式可以看出在阴、阳极上产生的OH-、H+的数目相等,阳极室中反应产生的H+通过质子
交换膜进入阴极室与OH-恰好反应生成水,所以阴极室中电解前后溶液的pH不变,B项错
误;由上述分析可知,C项错误;若两极共收集到气体0.6 mol,则n(N )=n(CO)=0.6×
2 2
mol=
0.12 mol,由反应CO(NH) +3Cl +HO===N +CO +6HCl可知,所消耗的CO(NH) 的物
2 2 2 2 2 2 2 2
质的量也为0.12 mol,D项正确。
11.按要求回答下列问题
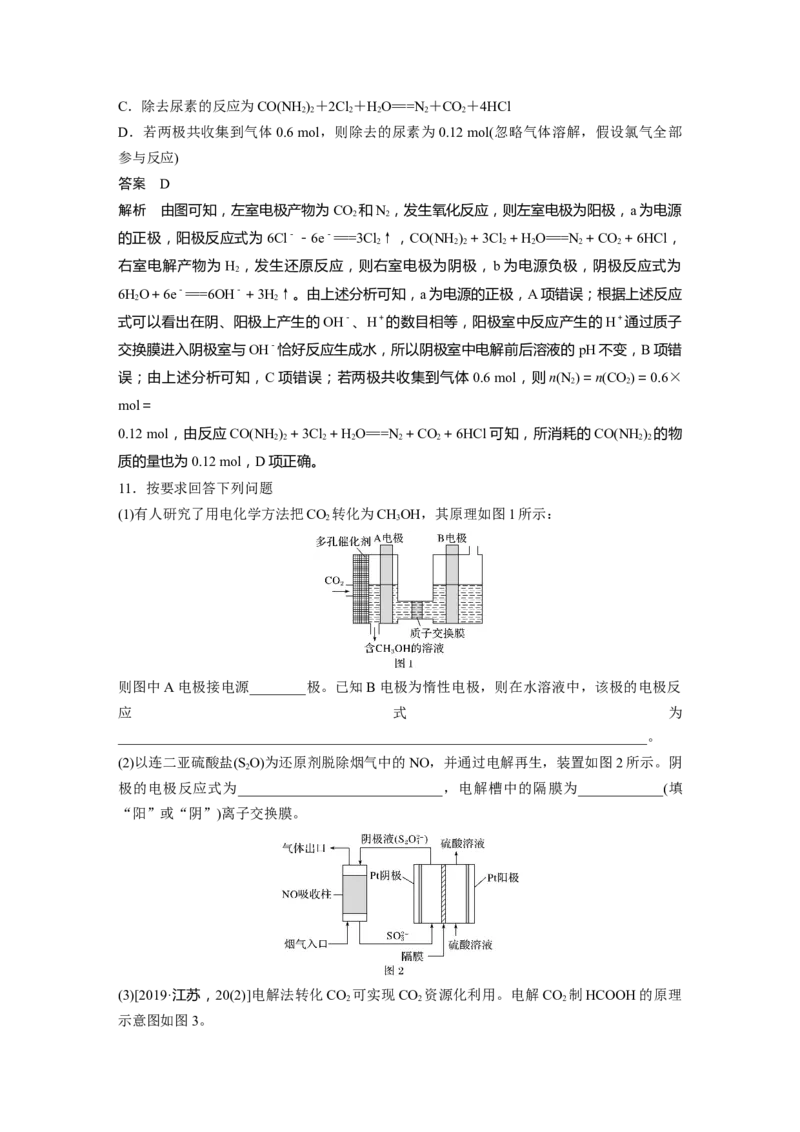
(1)有人研究了用电化学方法把CO 转化为CHOH,其原理如图1所示:
2 3
则图中A电极接电源________极。已知B电极为惰性电极,则在水溶液中,该极的电极反
应 式 为
___________________________________________________________________________。
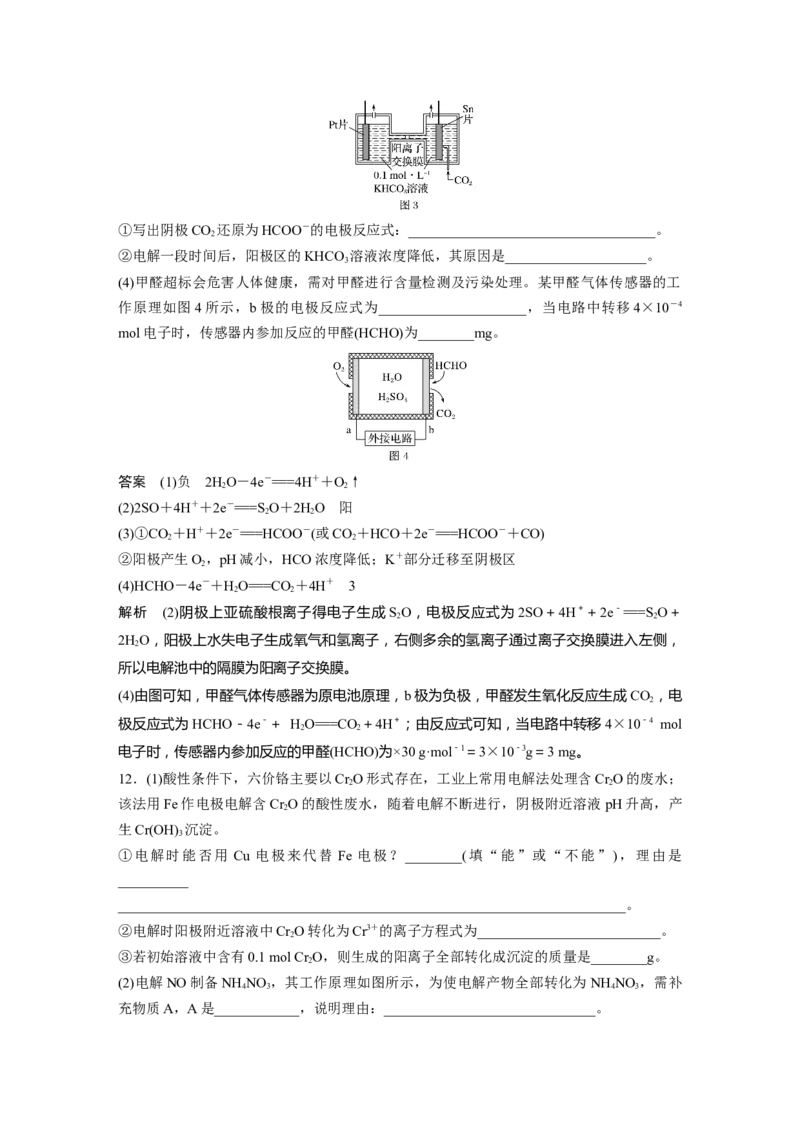
(2)以连二亚硫酸盐(S O)为还原剂脱除烟气中的NO,并通过电解再生,装置如图2所示。阴
2
极的电极反应式为_____________________________,电解槽中的隔膜为____________(填
“阳”或“阴”)离子交换膜。
(3)[2019·江苏,20(2)]电解法转化CO 可实现CO 资源化利用。电解CO 制HCOOH的原理
2 2 2
示意图如图3。①写出阴极CO 还原为HCOO-的电极反应式:___________________________________。
2
②电解一段时间后,阳极区的KHCO 溶液浓度降低,其原因是____________________。
3
(4)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。某甲醛气体传感器的工
作原理如图4所示,b极的电极反应式为_____________________,当电路中转移4×10-4
mol电子时,传感器内参加反应的甲醛(HCHO)为________mg。
答案 (1)负 2HO-4e-===4H++O↑
2 2
(2)2SO+4H++2e-===SO+2HO 阳
2 2
(3)①CO+H++2e-===HCOO-(或CO+HCO+2e-===HCOO-+CO)
2 2
②阳极产生O,pH减小,HCO浓度降低;K+部分迁移至阴极区
2
(4)HCHO-4e-+HO===CO+4H+ 3
2 2
解析 (2)阴极上亚硫酸根离子得电子生成SO,电极反应式为2SO+4H++2e-===SO+
2 2
2HO,阳极上水失电子生成氧气和氢离子,右侧多余的氢离子通过离子交换膜进入左侧,
2
所以电解池中的隔膜为阳离子交换膜。
(4)由图可知,甲醛气体传感器为原电池原理,b极为负极,甲醛发生氧化反应生成CO ,电
2
极反应式为HCHO-4e-+ HO===CO +4H+;由反应式可知,当电路中转移4×10-4 mol
2 2
电子时,传感器内参加反应的甲醛(HCHO)为×30 g·mol-1=3×10-3g=3 mg。
12.(1)酸性条件下,六价铬主要以Cr O形式存在,工业上常用电解法处理含Cr O的废水;
2 2
该法用Fe作电极电解含Cr O的酸性废水,随着电解不断进行,阴极附近溶液pH升高,产
2
生Cr(OH) 沉淀。
3
①电解时能否用 Cu 电极来代替 Fe 电极?________(填“能”或“不能”),理由是
__________
________________________________________________________________________。
②电解时阳极附近溶液中Cr O转化为Cr3+的离子方程式为__________________________。
2
③若初始溶液中含有0.1 mol Cr O,则生成的阳离子全部转化成沉淀的质量是________g。
2
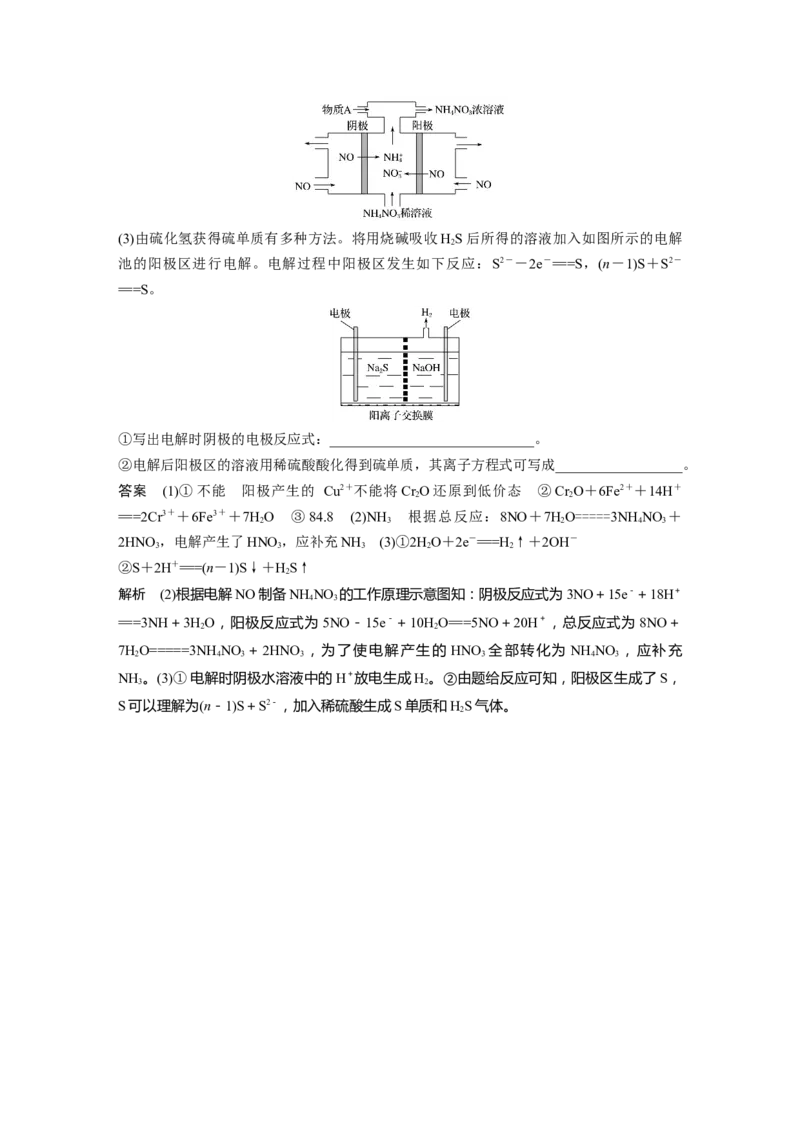
(2)电解NO制备NH NO ,其工作原理如图所示,为使电解产物全部转化为NH NO ,需补
4 3 4 3
充物质A,A是____________,说明理由:______________________________。(3)由硫化氢获得硫单质有多种方法。将用烧碱吸收HS后所得的溶液加入如图所示的电解
2
池的阳极区进行电解。电解过程中阳极区发生如下反应:S2--2e-===S,(n-1)S+S2-
===S。
①写出电解时阴极的电极反应式:_____________________________。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成__________________。
答案 (1)①不能 阳极产生的 Cu2+不能将Cr O还原到低价态 ②Cr O+6Fe2++14H+
2 2
===2Cr3++6Fe3++7HO ③84.8 (2)NH 根据总反应:8NO+7HO=====3NH NO +
2 3 2 4 3
2HNO,电解产生了HNO,应补充NH (3)①2HO+2e-===H↑+2OH-
3 3 3 2 2
②S+2H+===(n-1)S↓+HS↑
2
解析 (2)根据电解NO制备NH NO 的工作原理示意图知:阴极反应式为3NO+15e-+18H+
4 3
===3NH+3HO,阳极反应式为5NO-15e-+10HO===5NO+20H+,总反应式为8NO+
2 2
7HO=====3NH NO +2HNO ,为了使电解产生的 HNO 全部转化为 NH NO ,应补充
2 4 3 3 3 4 3
NH 。(3)①电解时阴极水溶液中的H+放电生成H 。②由题给反应可知,阳极区生成了S,
3 2
S可以理解为(n-1)S+S2-,加入稀硫酸生成S单质和HS气体。
2