文档内容
2023届高考化学一轮备考专题强化训练:有机推断题
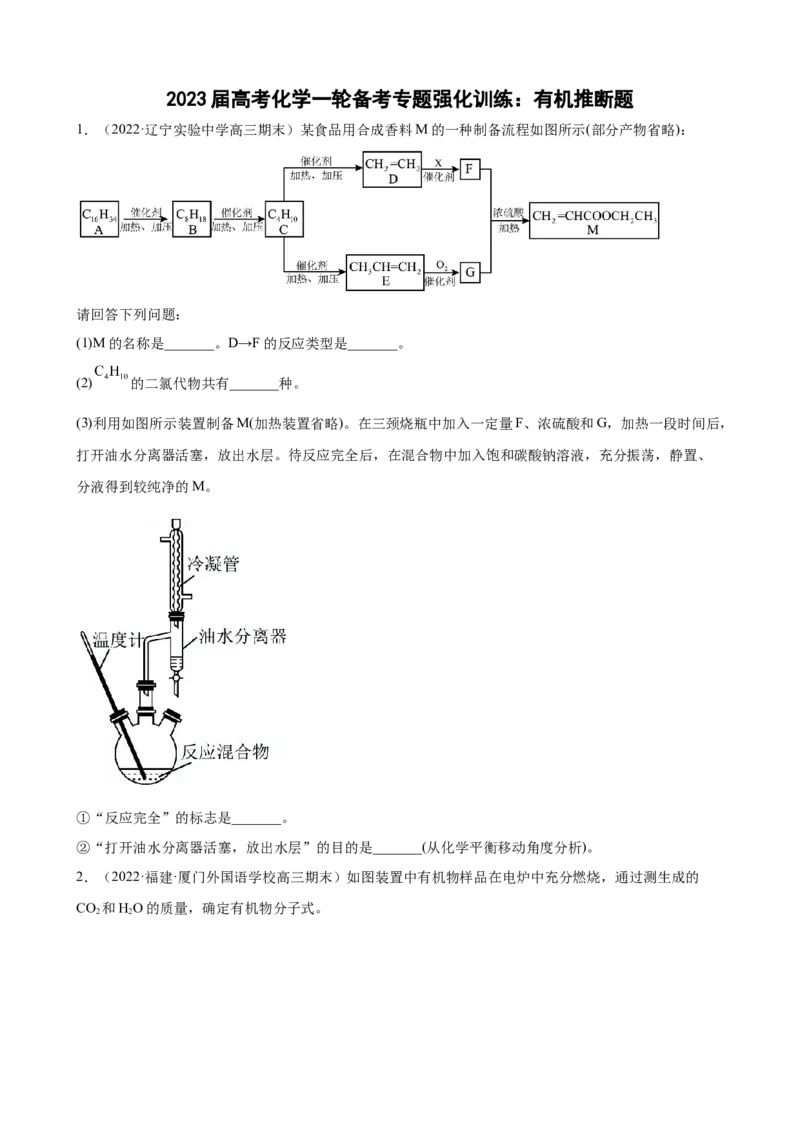
1.(2022·辽宁实验中学高三期末)某食品用合成香料M的一种制备流程如图所示(部分产物省略):
请回答下列问题:
(1)M的名称是_______。D→F的反应类型是_______。
(2) 的二氯代物共有_______种。
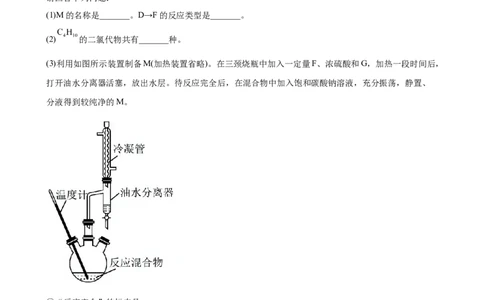
(3)利用如图所示装置制备M(加热装置省略)。在三颈烧瓶中加入一定量F、浓硫酸和G,加热一段时间后,
打开油水分离器活塞,放出水层。待反应完全后,在混合物中加入饱和碳酸钠溶液,充分振荡,静置、
分液得到较纯净的M。
①“反应完全”的标志是_______。
②“打开油水分离器活塞,放出水层”的目的是_______(从化学平衡移动角度分析)。
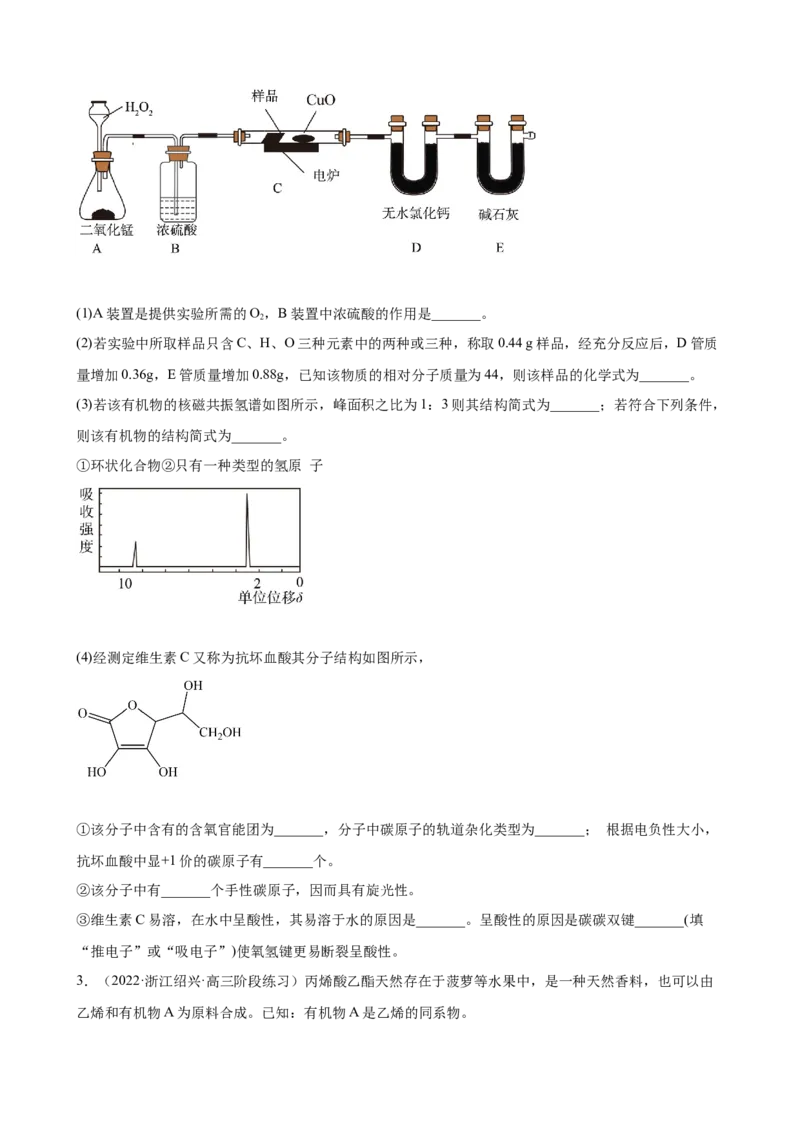
2.(2022·福建·厦门外国语学校高三期末)如图装置中有机物样品在电炉中充分燃烧,通过测生成的
CO 和HO的质量,确定有机物分子式。
2 2(1)A装置是提供实验所需的O,B装置中浓硫酸的作用是_______。
2
(2)若实验中所取样品只含C、H、O三种元素中的两种或三种,称取0.44 g样品,经充分反应后,D管质
量增加0.36g,E管质量增加0.88g,已知该物质的相对分子质量为44,则该样品的化学式为_______。
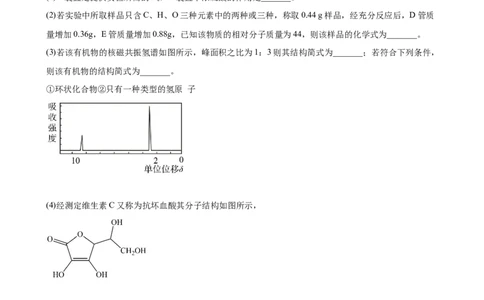
(3)若该有机物的核磁共振氢谱如图所示,峰面积之比为1:3则其结构简式为_______;若符合下列条件,
则该有机物的结构简式为_______。
①环状化合物②只有一种类型的氢原 子
(4)经测定维生素C又称为抗坏血酸其分子结构如图所示,
①该分子中含有的含氧官能团为_______,分子中碳原子的轨道杂化类型为_______; 根据电负性大小,
抗坏血酸中显+1价的碳原子有_______个。
②该分子中有_______个手性碳原子,因而具有旋光性。
③维生素C易溶,在水中呈酸性,其易溶于水的原因是_______。呈酸性的原因是碳碳双键_______(填
“推电子”或“吸电子”)使氧氢键更易断裂呈酸性。
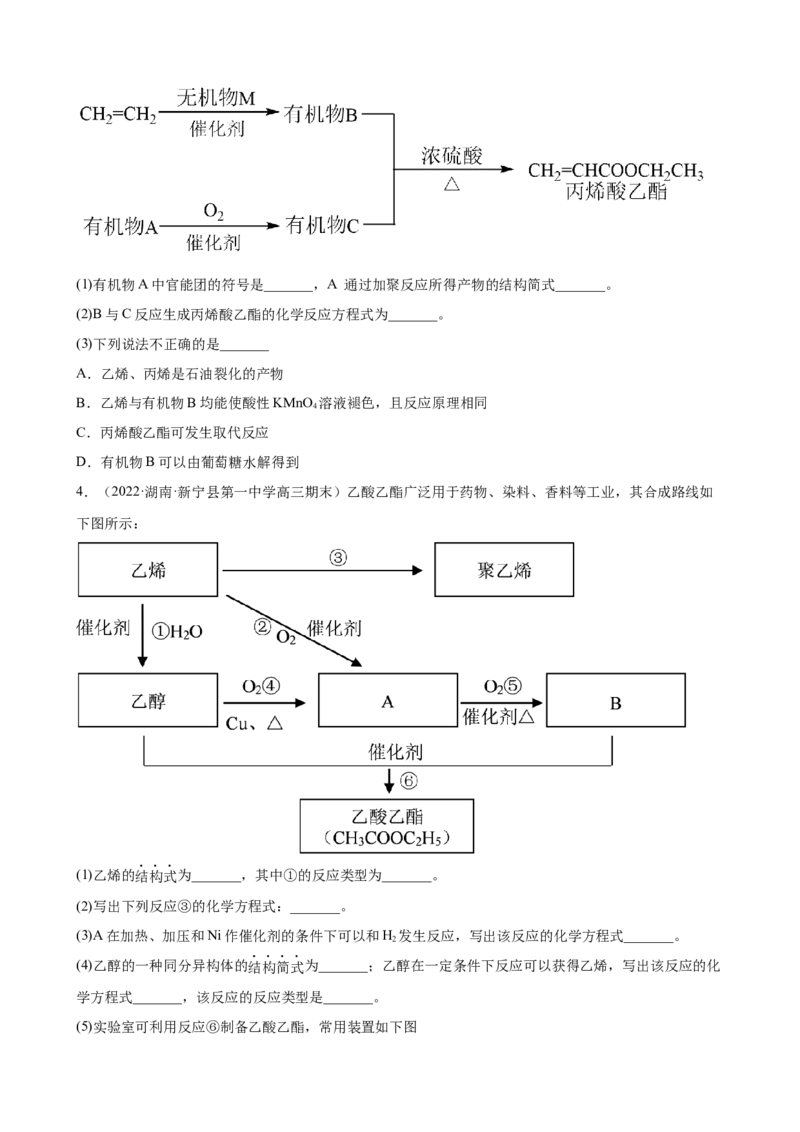
3.(2022·浙江绍兴·高三阶段练习)丙烯酸乙酯天然存在于菠萝等水果中,是一种天然香料,也可以由
乙烯和有机物A为原料合成。已知:有机物A是乙烯的同系物。(1)有机物A中官能团的符号是_______,A 通过加聚反应所得产物的结构简式_______。
(2)B与C反应生成丙烯酸乙酯的化学反应方程式为_______。
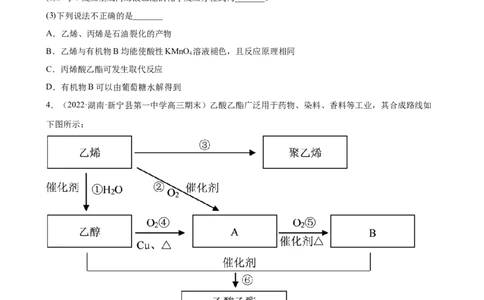
(3)下列说法不正确的是_______
A.乙烯、丙烯是石油裂化的产物
B.乙烯与有机物B均能使酸性KMnO 溶液褪色,且反应原理相同
4
C.丙烯酸乙酯可发生取代反应
D.有机物B可以由葡萄糖水解得到
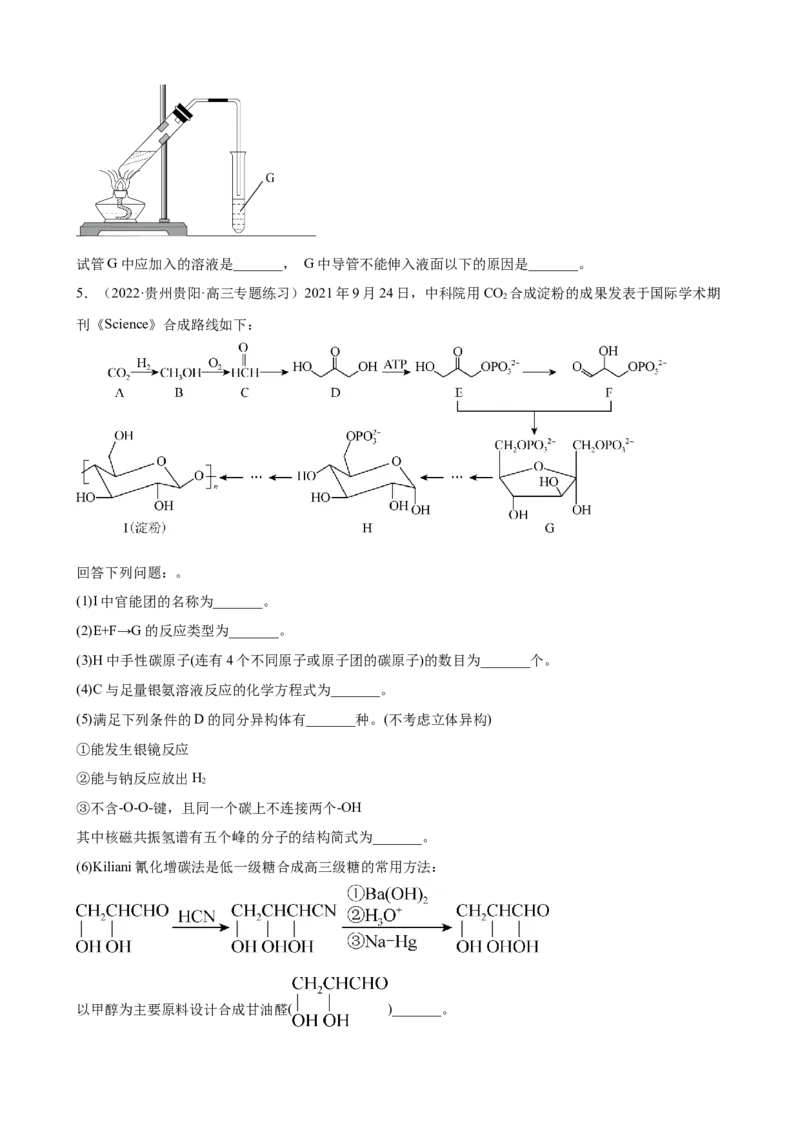
4.(2022·湖南·新宁县第一中学高三期末)乙酸乙酯广泛用于药物、染料、香料等工业,其合成路线如
下图所示:
(1)乙烯的结构式为_______,其中①的反应类型为_______。
(2)写出下列反应③的化学方程式:_______。
(3)A在加热、加压和Ni作催化剂的条件下可以和H 发生反应,写出该反应的化学方程式_______。
2
(4)乙醇的一种同分异构体的结构简式为_______;乙醇在一定条件下反应可以获得乙烯,写出该反应的化
学方程式_______,该反应的反应类型是_______。
(5)实验室可利用反应⑥制备乙酸乙酯,常用装置如下图试管G中应加入的溶液是_______, G中导管不能伸入液面以下的原因是_______。
5.(2022·贵州贵阳·高三专题练习)2021年9月24日,中科院用CO 合成淀粉的成果发表于国际学术期
2
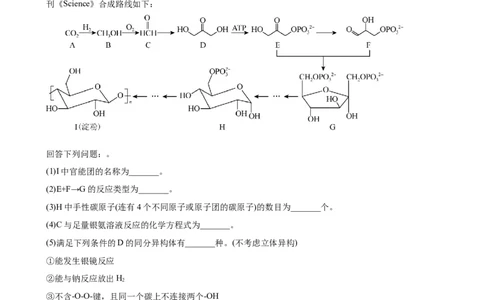
刊《Science》合成路线如下:
回答下列问题:。
(1)I中官能团的名称为_______。
(2)E+F→G的反应类型为_______。
(3)H中手性碳原子(连有4个不同原子或原子团的碳原子)的数目为_______个。
(4)C与足量银氨溶液反应的化学方程式为_______。
(5)满足下列条件的D的同分异构体有_______种。(不考虑立体异构)
①能发生银镜反应
②能与钠反应放出H
2
③不含-O-O-键,且同一个碳上不连接两个-OH
其中核磁共振氢谱有五个峰的分子的结构简式为_______。
(6)Kiliani氰化增碳法是低一级糖合成高三级糖的常用方法:
以甲醇为主要原料设计合成甘油醛( )_______。6.(2022·湖南省茶陵县第一中学高三期末)食品添加剂必须严格按照国家食品安全标准的规定使用。防
腐剂G的一种合成路线如图所示(部分反应条件略)。
(1)D中含氧官能团的名称是_______、_______。
(2)流程中A→B步骤的作用是_______。
(3)D→E发生的反应类型是_______。
(4)B的同分异构体有多种,写出符合下列条件的同分异构体_______。
①属于芳香族化合物
②遇FeCl 溶液显紫色
3
③分子中有4种不同化学环境的氢
(5)鉴别E、G用的试剂是_______(填写下面的选项字母,下同),将E转化为 需要的试剂可以是
_______。
A.Na B.NaOH C.NaHCO D.NaNO
3 3
7.(2022·黑龙江·海伦市第一中学高三期末)A~F为芳香族化合物,它们的转化关系如图所示:
已知B分子中含有一个甲基。
回答下列问题:
(1)D中所含官能团名称为_______;B→D的反应条件为_______。
(2)B→C的反应方程式为_______。
(3)C→D、D→E的反应类型分别为_______、_______。
(4)F存在于栀子香油中,其结构简式为_______。
8.(2022·黑龙江·海伦市第一中学高三期末)一种合成有机物F的路线如下:回答下列问题:
(1)A中官能团的名称为_______。
(2)A→B的反应类型为_______。
(3)已知-OH为取代基,E的化学名称为_______。
(4)合成路线中设计B→C的目的是_______。
(5)E→F的反应条件为_______。
(6)G是D的一种同分异构体,1molG与足量的银氨溶液反应,可生成432g单质银。任写出一种G的结构
简式:_______。
9.(2022·山东省淄博第一中学高三期末)W是一种高分子功能材料,在生产、生活中有广泛应用。一
种合成W的路线如图。
请回答下列问题:
(1)A中含官能团的名称是_______,B的名称是_______。写出A与新制氢氧化铜溶液反应的化学方程式
_______
(2)A→C的反应类型为_______。
(3)已知E的分子式为 ,F的结构简式为_______。(4)G→W的化学方程式为_______。
(5)设计以2,3-二氯丁烷、丙烯醛为原料合成苯甲醛的合成路线(无机试剂任选)_______。
10.(2022·湖南怀化·一模)立方烷( )具有高度对称性、高致密性、高张力能及高稳定性等特点,
因此合成立方烷及其衍生物成为化学界关注的热点。下面是立方烷衍生物Ⅰ的一种合成路线:
回答下列问题:
(1)A的名称是_______;写出I中官能团的名称_______。
(2)反应②的化学方程式为_______;③的反应类型为_______。
(3)E的结构简式为_______。
(4)J为I的同分异构体,符合下列条件的J有_______种。
①含有苯环;②能使 的 溶液褪色;③1molJ能与 恰好完全反应。其中核磁共振氢谱
有5组峰,且峰面积之比为 的结构简式为_______(写出其中一种)。
(5)参照上述合成路线,以 和乙烯为原料,设计合成 的路线_______(其他试剂任选)。
11.(2022·贵州贵阳·高三专题练习)有机物K是合成酪氨酸血症药物尼替西农的中间体,其合成路线如
下:
(1)A中官能团的名称为_______。D→E的反应类型_______。
(2)B→C的反应方程式为_______。
(3)H的结构简式为_______。(4)关于物质G,下列说法正确的是 。
A.能使酸性高锰酸钾褪色
B.能与液溴在FeBr 存在下发生取代反应
3
C.能发生加聚反应
D.1molG在空气中完全燃烧消耗氧气6mol
(5)M(C H O)是D的同系物,其核磁共振氢谱峰面积之比为6:2:1:1,则M的结构简式为_______(写出所
9 10 2
有可能的结构)。
(6)以 为原料合成 试写出合成路线_______(无机试剂任选)。
12.(2022·湖南·益阳市第一中学高三期末)A是一种重要的化工原料,已知A是一氯代烃,相对分子质
量为92.5,其核磁共振氢谱中只有一个峰,C是一种高分子化合物,M是一种六元环状酯,转化关系如
图所示,回答下列问题:
(1)A的分子式为_______;B→D的反应类型_______;A→B的反应条件是_______。
(2)有机物C的结构简式为_______。
(3)写出下列反应的化学方程式:D→E:_______;F→G:_______。
(4)满足下列条件的H的同分异构体共有_______种(不考虑立体异构)。
①属于酯类;②能发生银镜反应;③能与金属钠反应放出气体。
13.(2022·天津市第二南开中学高三期末)回答下列问题:
(1)某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化学工业发展水平,A在一
定条件下可发生如图所示的转化,请回答下列问题:
①写出A的电子式____,C的结构简式为____。
②写出反应③的化学方程式____,该反应类型为____。③写出反应④的化学方程式____,该反应类型为____。
④除去B中混有的少量杂质A,所用的试剂为____。
⑤写出D催化氧化的化学方程式____。
(2)牛奶放置时间长了会变酸,这是因为牛奶中含有的乳糖在微生物的作用下分解变成了乳酸。乳酸最初
就是从酸牛奶中得到并由此而得名的。乳酸的结构简式为 。完成下列问题:
①写出乳酸与足量金属钠反应的化学方程式:____。
②乳酸发生下列变化: ,
所用的试剂是a____,b____(写化学式)。
③写出乳酸与乙醇反应的化学方程式____,并注明反应类型____。
14.(2022·辽宁·沈阳二中高三期末)化合物H(硝苯地平)是一种治疗高血压的药物,其一种合成如下:
已知:
回答下列问题:
(1)②的反应类型_______,D分子中官能团名称_______。
(2)G的结构简式为_______
(3)反应①的化学方程式_______
(4)M与D互为同分构体,写出三种同时满足下列条件的M的结构简式_______
a.能发生银镜反应,遇 显紫色;
b.结构中存在 ;不存在碳碳双键c.核磁共振氢谱显示有4组峰,峰面积之比为1∶2∶2∶2。
(5)设计由 和乙醇为起始原料制备 的合成路线(其他无机试剂任
选)_______。
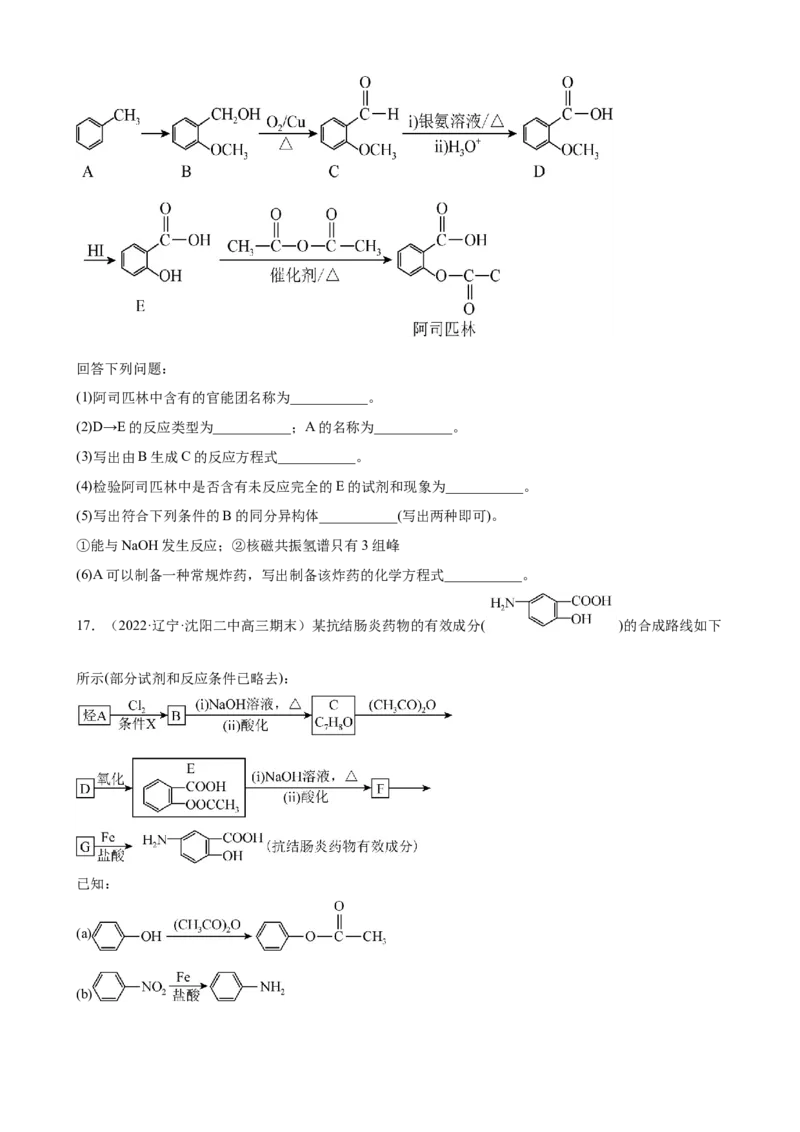
15.(2022·河北省唐县第一中学高三阶段练习)乙酸苯乙酯是一种具有玫瑰花香,并带有可可香韵的有
机物,常用于调配玫瑰、紫罗兰、晚香玉、野蔷薇等香精。天然乙酸苯乙酯存在于白兰花油和玫瑰花油
中,也可通过化学方法合成。下图是一种合成路线(部分反应物和条件省略)。
已知A是一种不饱和烃,B、C、D都是含碳原子数相同的常见有机物。请回答下列问题:
(1)乙酸苯乙酯(H)的分子式为___________,A的结构简式为___________。
(2)A→B属于___________反应,
(3)下列对图中有关化合物的叙述中正确的是___________。(填序号)
①化合物E所有原子可能在同一平面上 ②化合物B、E都属于烃
③化合物G属于醇类 ④化合物D所含官能团为羟基
(4)写出B→C的化学方程式:___________。
(5)写出D+G→H的化学方程式:___________。
16.(2022·山东济南·高三期末)阿司匹林是常用的解热镇痛药。其中一种制备路线如下:回答下列问题:
(1)阿司匹林中含有的官能团名称为___________。
(2)D→E的反应类型为___________;A的名称为___________。
(3)写出由B生成C的反应方程式___________。
(4)检验阿司匹林中是否含有未反应完全的E的试剂和现象为___________。
(5)写出符合下列条件的B的同分异构体___________(写出两种即可)。
①能与NaOH发生反应;②核磁共振氢谱只有3组峰
(6)A可以制备一种常规炸药,写出制备该炸药的化学方程式___________。
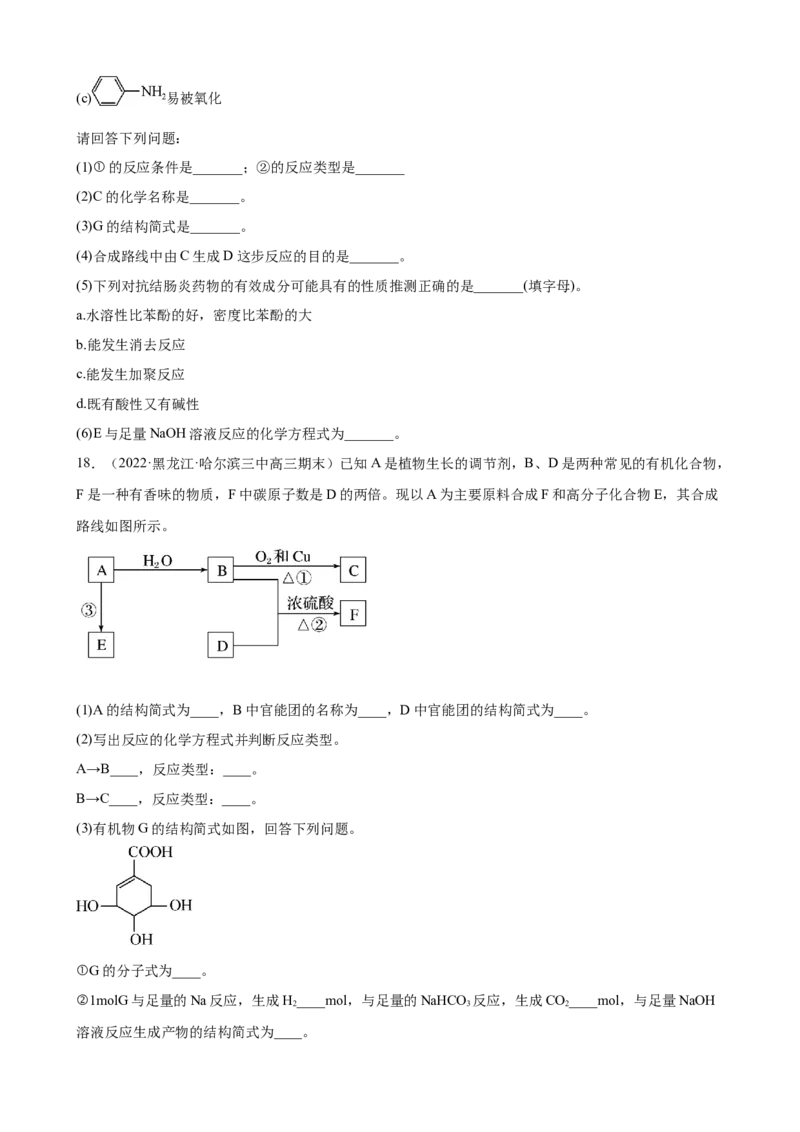
17.(2022·辽宁·沈阳二中高三期末)某抗结肠炎药物的有效成分( )的合成路线如下
所示(部分试剂和反应条件已略去):
已知:
(a)
(b)(c) 易被氧化
请回答下列问题:
(1)①的反应条件是_______;②的反应类型是_______
(2)C的化学名称是_______。
(3)G的结构简式是_______。
(4)合成路线中由C生成D这步反应的目的是_______。
(5)下列对抗结肠炎药物的有效成分可能具有的性质推测正确的是_______(填字母)。
a.水溶性比苯酚的好,密度比苯酚的大
b.能发生消去反应
c.能发生加聚反应
d.既有酸性又有碱性
(6)E与足量NaOH溶液反应的化学方程式为_______。
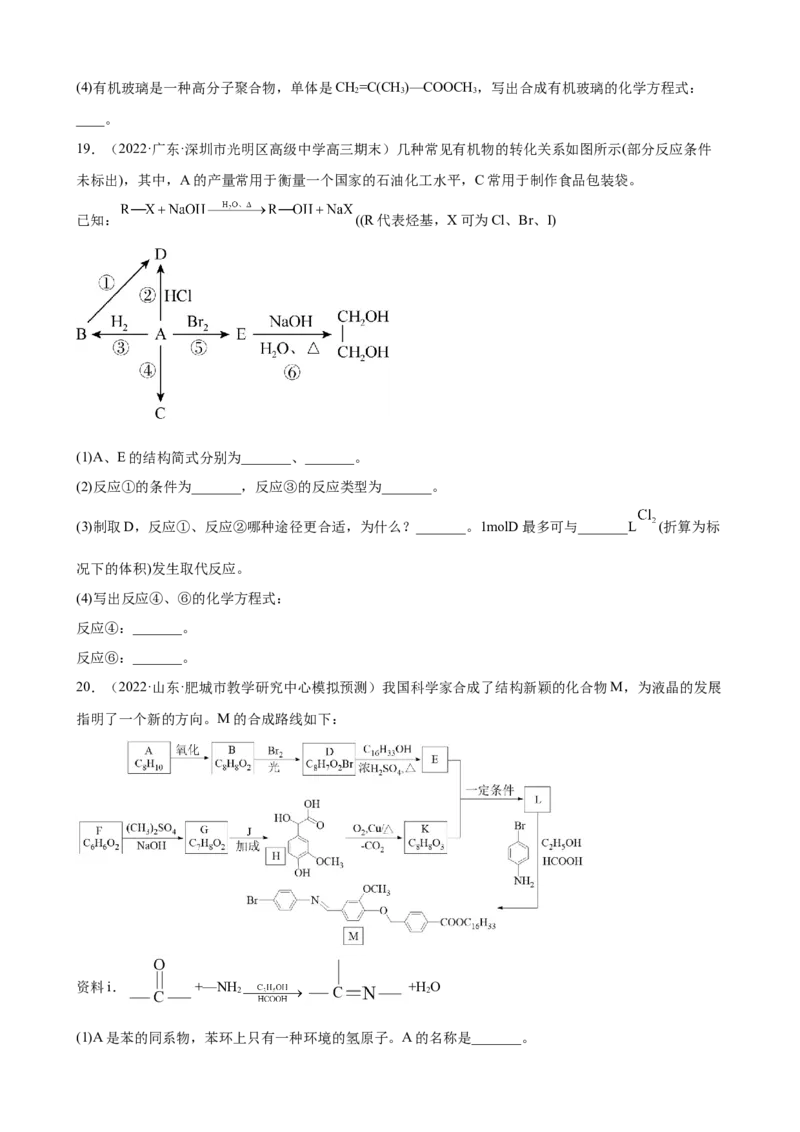
18.(2022·黑龙江·哈尔滨三中高三期末)已知A是植物生长的调节剂,B、D是两种常见的有机化合物,
F是一种有香味的物质,F中碳原子数是D的两倍。现以A为主要原料合成F和高分子化合物E,其合成
路线如图所示。
(1)A的结构简式为____,B中官能团的名称为____,D中官能团的结构简式为____。
(2)写出反应的化学方程式并判断反应类型。
A→B____,反应类型:____。
B→C____,反应类型:____。
(3)有机物G的结构简式如图,回答下列问题。
①G的分子式为____。
②1molG与足量的Na反应,生成H____mol,与足量的NaHCO 反应,生成CO____mol,与足量NaOH
2 3 2
溶液反应生成产物的结构简式为____。(4)有机玻璃是一种高分子聚合物,单体是CH=C(CH )—COOCH ,写出合成有机玻璃的化学方程式:
2 3 3
____。
19.(2022·广东·深圳市光明区高级中学高三期末)几种常见有机物的转化关系如图所示(部分反应条件
未标出),其中,A的产量常用于衡量一个国家的石油化工水平,C常用于制作食品包装袋。
已知: ((R代表烃基,X可为Cl、Br、I)
(1)A、E的结构简式分别为_______、_______。
(2)反应①的条件为_______,反应③的反应类型为_______。
(3)制取D,反应①、反应②哪种途径更合适,为什么?_______。1molD最多可与_______L (折算为标
况下的体积)发生取代反应。
(4)写出反应④、⑥的化学方程式:
反应④:_______。
反应⑥:_______。
20.(2022·山东·肥城市教学研究中心模拟预测)我国科学家合成了结构新颖的化合物M,为液晶的发展
指明了一个新的方向。M的合成路线如下:
资料i. +—NH +H O
2 2
(1)A是苯的同系物,苯环上只有一种环境的氢原子。A的名称是_______。(2)D的官能团的名称是_______。
(3)B→D的反应类型是_______。
(4)J的结构简式为_______。
(5)下列有关K的说法正确的是_______(填序号)。
a.与FeCl 溶液作用显紫色
3
b.含有醛基、羟基和醚键
c.存在含有苯环和碳碳双键的酯类同分异构体
(6)K的同分异构体中,能与FeCl 溶液发生显色反应且在碱性条件下可发生水解反应的有19种(不考虑立
3
体异构):其中核磁共振氢谱峰面积之比为2:2:2:1:1的同分异构体的结构简式为_______。
(7)E与K生成L的化学方程式是_______。
(8)依据资料i和资料ii,某小组完成了尼龙6的合成设计。
资料ii.
P、Q的分子式都是C H ON,生成尼龙6的化学方程式是_______。
6 11
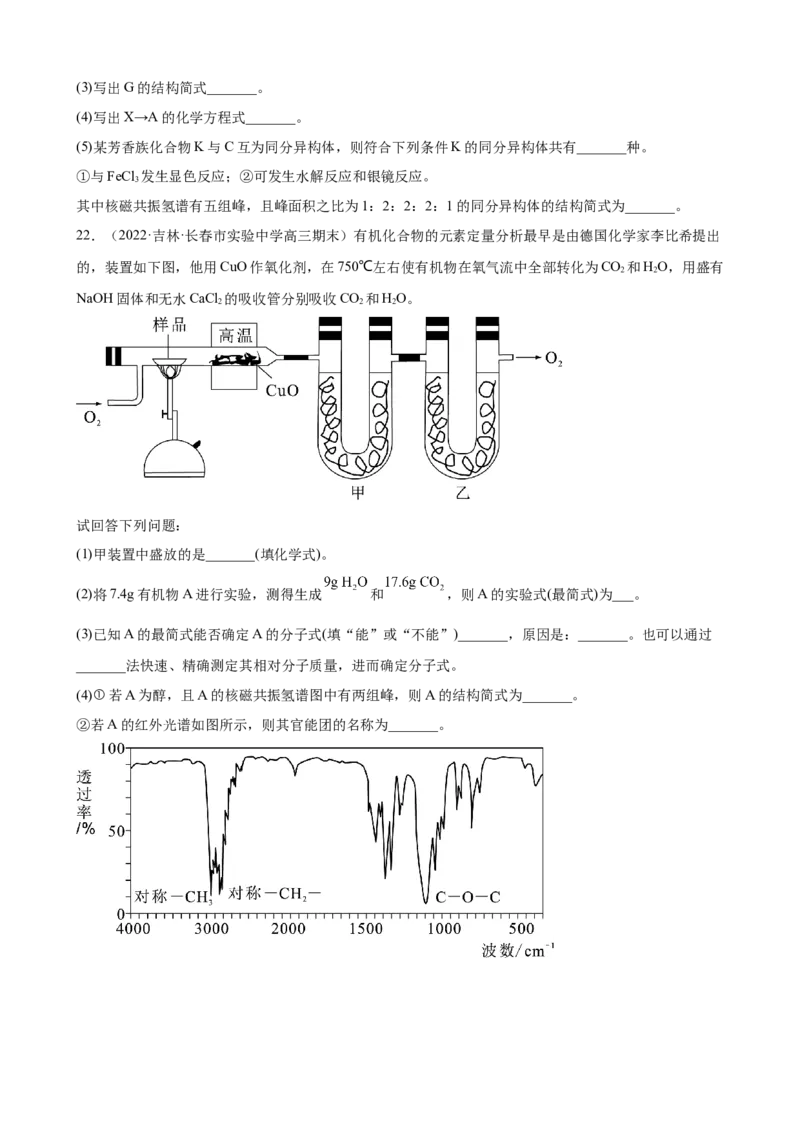
21.(2022·安徽·淮南第一中学模拟预测)有机物F是我国最早批准的可用于抗新冠肺炎临床试验的药物
之一,而最新文献研究也证实了其对新型冠状肺炎有治疗作用。F的合成路线如下图所示,已知:分子
中-Ar表示-C H。
6 5
已知:RCOCH +R′COCl RCOCH COR′+HCl
3 2
ROH+(CH CO) O→ROCOCH +CH COOH
3 2 3 3
(1)写出F的分子式_______。
(2)A→B的反应类型是_______,B中含氧官能团的名称为_______。(3)写出G的结构简式_______。
(4)写出X→A的化学方程式_______。
(5)某芳香族化合物K与C互为同分异构体,则符合下列条件K的同分异构体共有_______种。
①与FeCl 发生显色反应;②可发生水解反应和银镜反应。
3
其中核磁共振氢谱有五组峰,且峰面积之比为1:2:2:2:1的同分异构体的结构简式为_______。
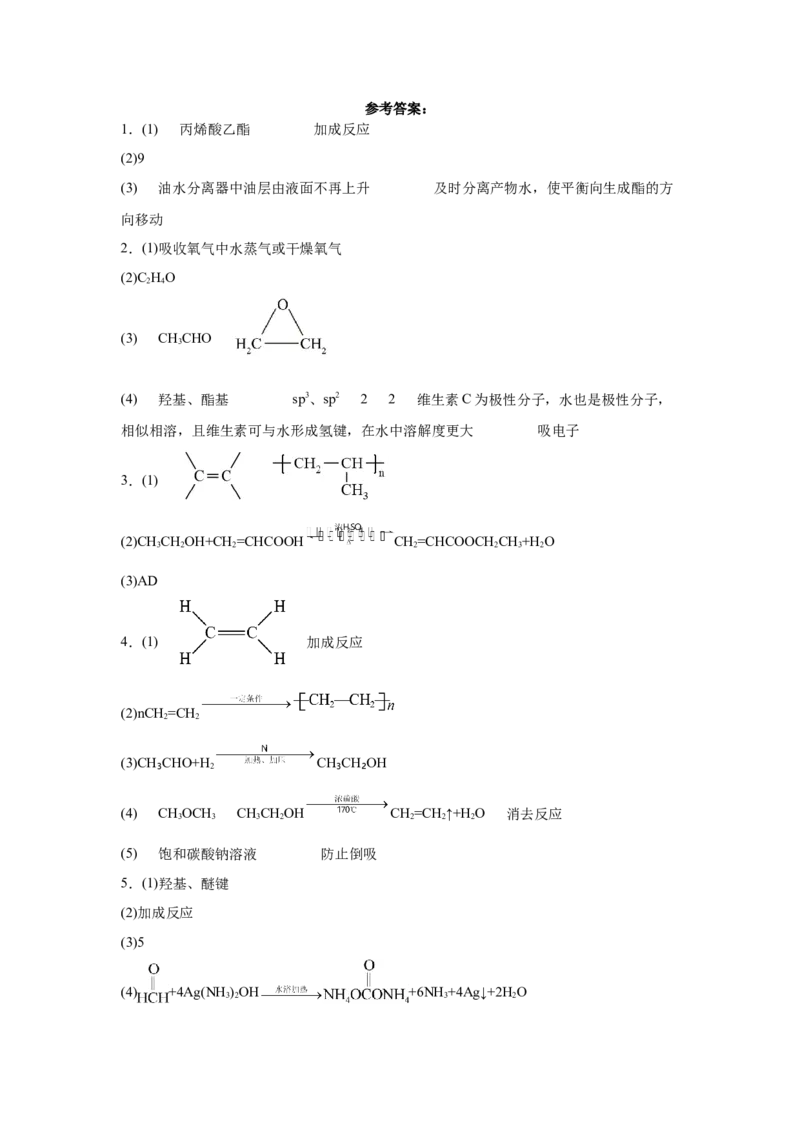
22.(2022·吉林·长春市实验中学高三期末)有机化合物的元素定量分析最早是由德国化学家李比希提出
的,装置如下图,他用CuO作氧化剂,在750℃左右使有机物在氧气流中全部转化为CO 和HO,用盛有
2 2
NaOH固体和无水CaCl 的吸收管分别吸收CO 和HO。
2 2 2
试回答下列问题:
(1)甲装置中盛放的是_______(填化学式)。
(2)将7.4g有机物A进行实验,测得生成 和 ,则A的实验式(最简式)为___。
(3)已知A的最简式能否确定A的分子式(填“能”或“不能”)_______,原因是:_______。也可以通过
_______法快速、精确测定其相对分子质量,进而确定分子式。
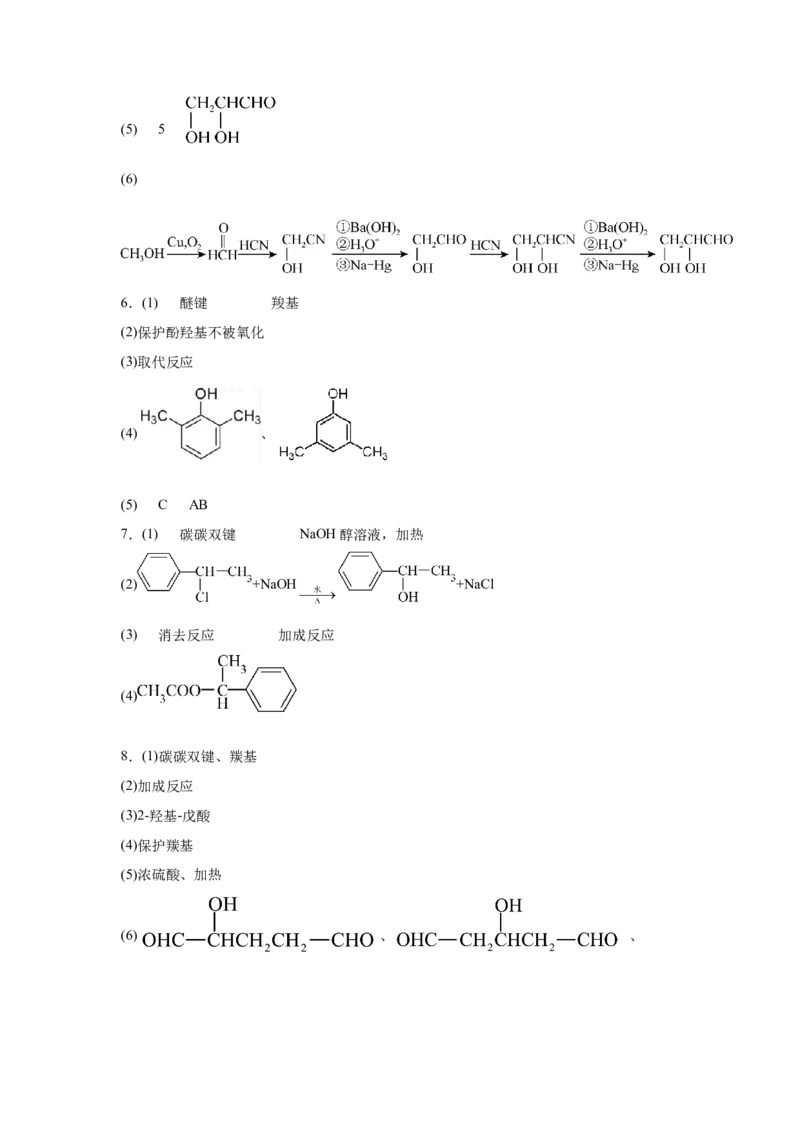
(4)①若A为醇,且A的核磁共振氢谱图中有两组峰,则A的结构简式为_______。
②若A的红外光谱如图所示,则其官能团的名称为_______。参考答案:
1.(1) 丙烯酸乙酯 加成反应
(2)9
(3) 油水分离器中油层由液面不再上升 及时分离产物水,使平衡向生成酯的方
向移动
2.(1)吸收氧气中水蒸气或干燥氧气
(2)C HO
2 4
(3) CHCHO
3
(4) 羟基、酯基 sp3、sp2 2 2 维生素C为极性分子,水也是极性分子,
相似相溶,且维生素可与水形成氢键,在水中溶解度更大 吸电子
3.(1)
(2)CH CHOH+CH =CHCOOH CH=CHCOOCH CH+H O
3 2 2 2 2 3 2
(3)AD
4.(1) 加成反应
(2)nCH =CH
2 2
(3)CH₃CHO+H CH₃CH₂OH
2
(4) CHOCH CHCHOH CH=CH ↑+H O 消去反应
3 3 3 2 2 2 2
(5) 饱和碳酸钠溶液 防止倒吸
5.(1)羟基、醚键
(2)加成反应
(3)5
(4) +4Ag(NH )OH +6NH+4Ag↓+2H O
3 2 3 2(5) 5
(6)
6.(1) 醚键 羧基
(2)保护酚羟基不被氧化
(3)取代反应
(4) 、
(5) C AB
7.(1) 碳碳双键 NaOH醇溶液,加热
(2) +NaOH +NaCl
(3) 消去反应 加成反应
(4)
8.(1)碳碳双键、羰基
(2)加成反应
(3)2-羟基-戊酸
(4)保护羰基
(5)浓硫酸、加热
(6) 、 、、 、
、 、
、 、
、 、
,任写一种即可。
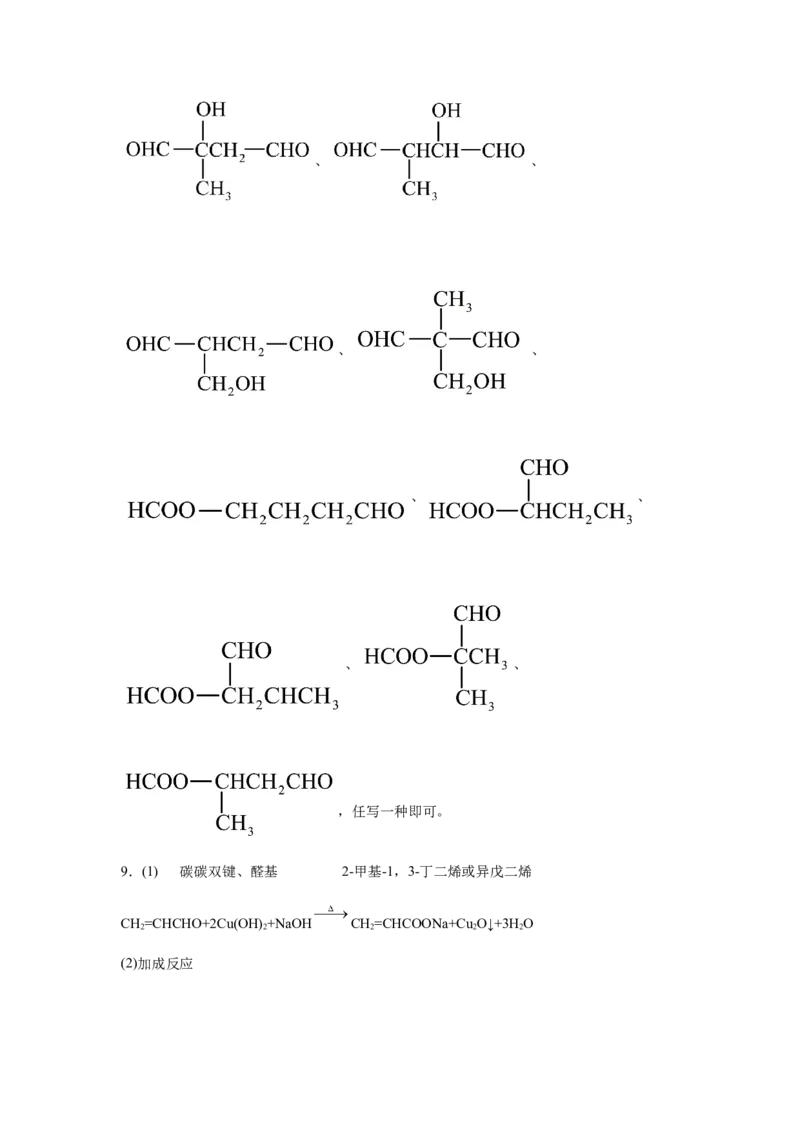
9.(1) 碳碳双键、醛基 2-甲基-1,3-丁二烯或异戊二烯
CH=CHCHO+2Cu(OH) +NaOH CH=CHCOONa+Cu O↓+3HO
2 2 2 2 2
(2)加成反应(3)
(4)n +
(n-1)H O
2
(5)
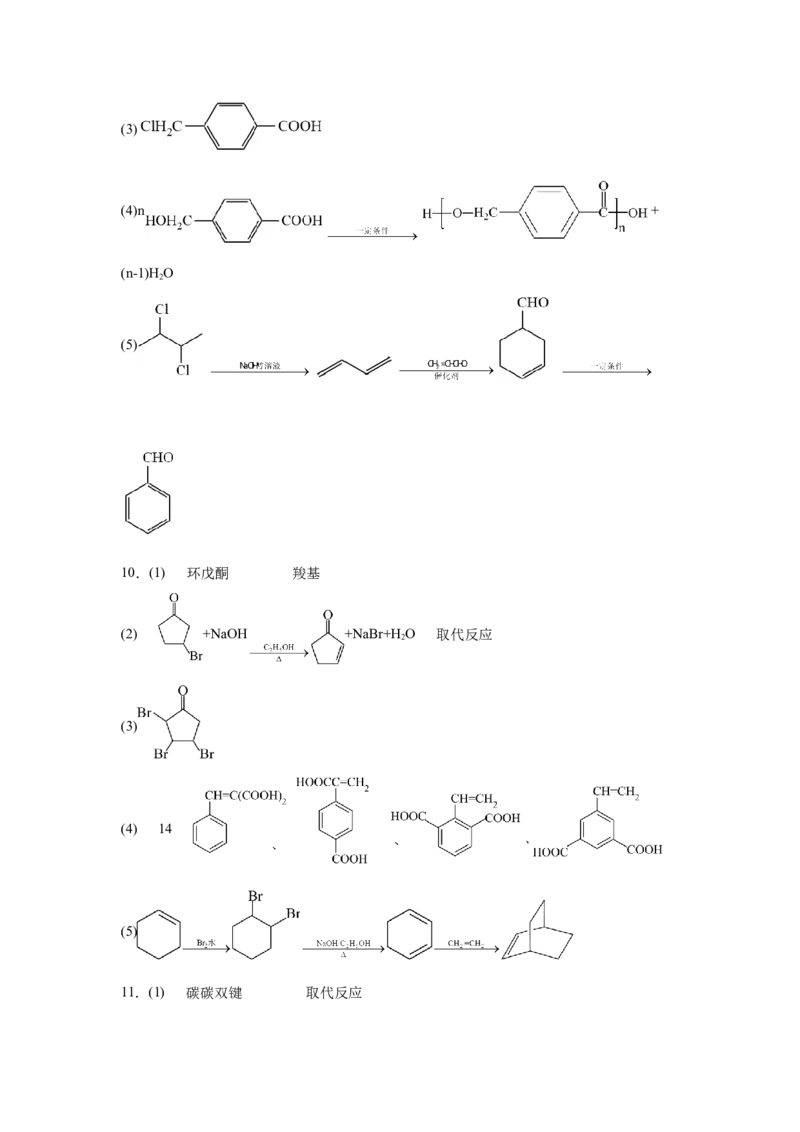
10.(1) 环戊酮 羧基
(2) +NaOH +NaBr+H O 取代反应
2
(3)
(4) 14
(5)
11.(1) 碳碳双键 取代反应(2)2 +O 2 +2H O
2 2
(3)
(4)A
(5) 或者
(6)
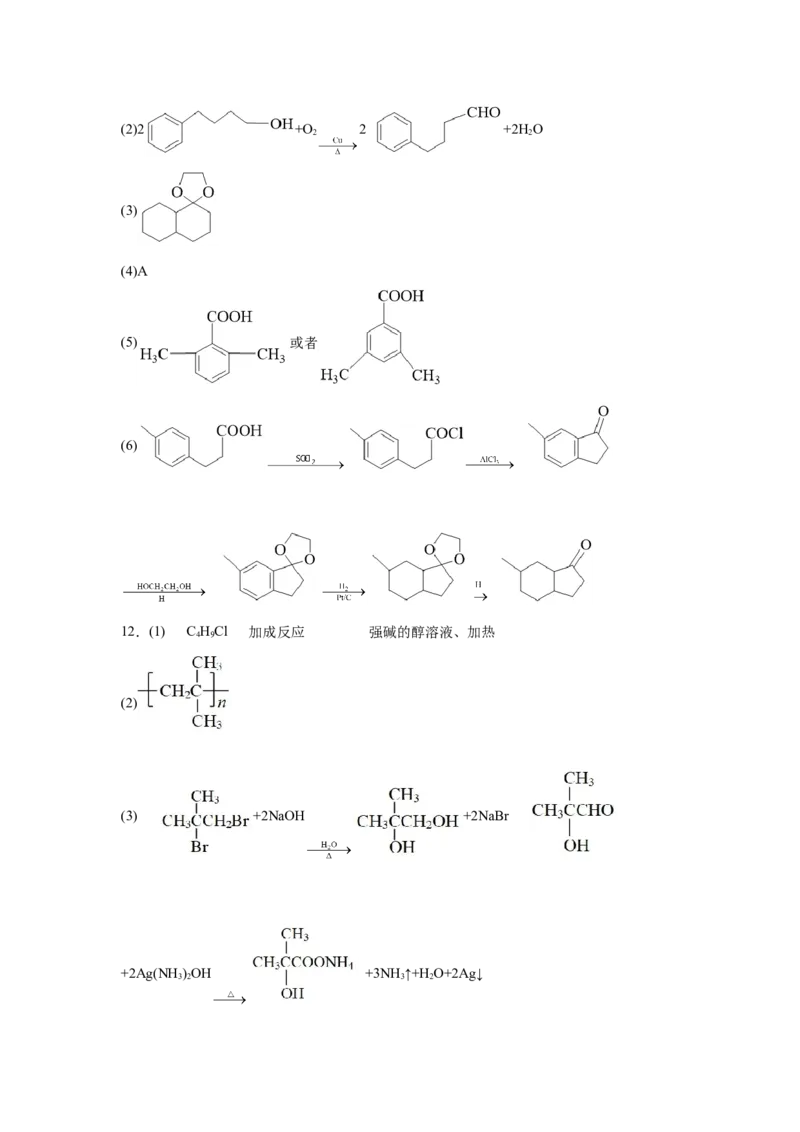
12.(1) C HCl 加成反应 强碱的醇溶液、加热
4 9
(2)
(3) +2NaOH +2NaBr
+2Ag(NH )OH +3NH↑+H O+2Ag↓
3 2 3 2(4)5
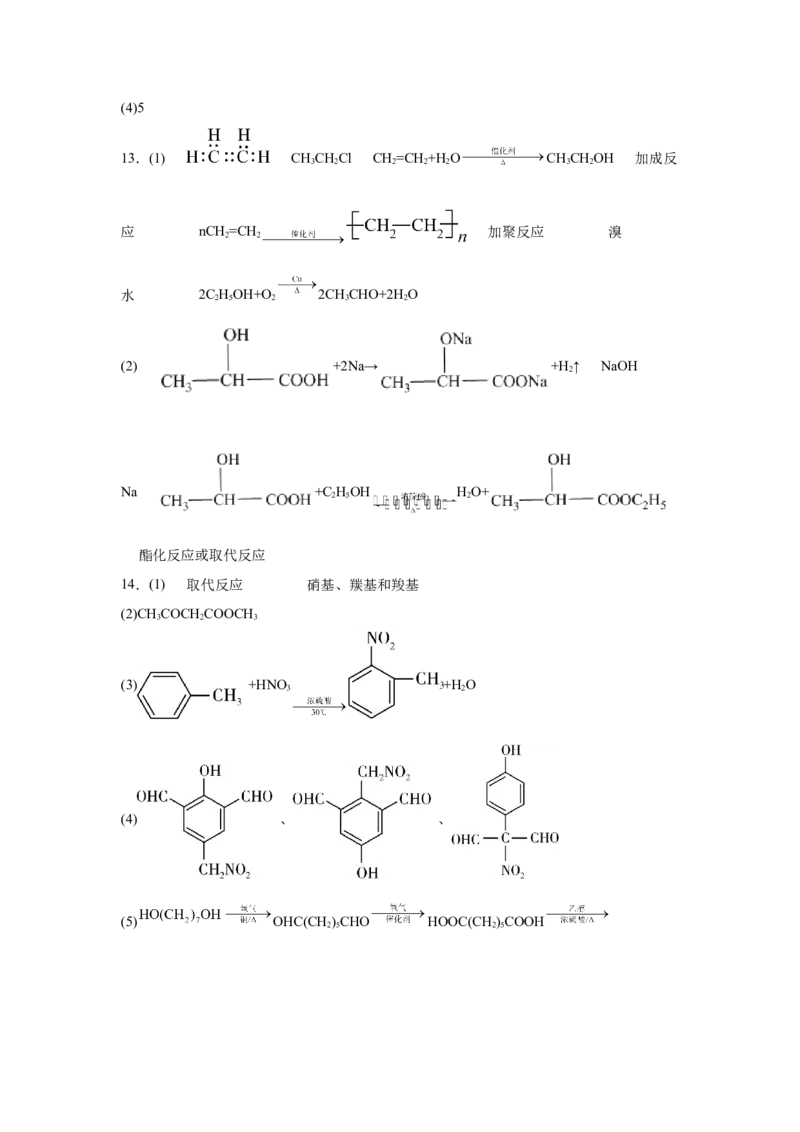
13.(1) CHCHCl CH=CH +H O CHCHOH 加成反
3 2 2 2 2 3 2
应 nCH=CH 加聚反应 溴
2 2
水 2C HOH+O 2CHCHO+2H O
2 5 2 3 2
(2) +2Na→ +H ↑ NaOH
2
Na +C HOH HO+
2 5 2
酯化反应或取代反应
14.(1) 取代反应 硝基、羰基和羧基
(2)CH COCH COOCH
3 2 3
(3) +HNO +H O
3 2
(4) 、 、
(5) OHC(CH )CHO HOOC(CH )COOH
2 5 2 5C HOOC(CH )COOC H
2 5 2 5 2 5
15.(1) C H O CH=CH
10 12 2 2 2
(2)加成
(3)①③
(4)2CH HOH +O 2CHCHO+2H O
3 2 2 3 2
(5) +CH COOH
3
+H O
2
16.(1)羧基、酯基
(2) 取代反应 甲苯
(3)2 +O 2 +2H O
2 2
(4)FeCl 溶液,若有E溶液显紫色
3
(5) 、 、
(6) +3HNO +3H O
3 2
17.(1) 铁粉 取代反应
(2)邻甲基苯酚(3)
(4)防止酚羟基被氧化
(5)ad
(6) +3NaOH→ +CH COONa+2H O
3 2
18.(1) CH=CH 羟基 -COOH
2 2
(2) 加成反应
氧化反应
(3) C H O 2 1
7 10 5
(4)
19.(1) CH=CH BrCHCHBr
2 2 2 2
(2) 氯气、光照 加成反应(或还原反应)
(3) 反应②,反应②只得氯乙烷一种产物,而反应①会得到多种有机产物和HCl 112
(4) +2NaOH
+2NaBr
20.(1)对二甲苯或1,4-二甲苯
(2)羧基、溴原子
(3)取代反应(4)HOOCCHO
(5)ab
(6)
(7) +
+HBr
(8)n
21.(1)
(2) 取代反应 酯基、羰基
(3)ArCOCl
(4) +2(CH CO) O +2CH COOH
3 2 3
(5) 13
22.(1)CaCl
2
(2)C H O
4 10
(3) 能 H原子已经饱和C原子的四价结构,最简式即为分子式 质谱
法(4) (CH)C-OH 醚键
3 3