文档内容
单元检测八 化学反应与能量
一、选择题(本题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.下列叙述正确的是( )
A.升高温度可降低活化能
B.废电池需回收,主要是要利用电池外壳的金属材料
C.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
D.推广使用太阳能、风能、地热能、氢能,有利于缓解温室效应
2.中国化学家研究的一种新型复合催化剂[碳纳米点(CQDs)/氮化碳(C N)纳米复合物]可以
3 4
利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是( )
A.C N 中C的化合价为-4
3 4
B.反应的两个阶段均为吸热过程
C.阶段Ⅱ中,HO 既是氧化剂,又是还原剂
2 2
D.通过该反应,实现了化学能向太阳能的转化
3.18O 标记的乙酸甲酯在足量 NaOH 溶液中发生水解,部分反应历程可表示为:
+OH- +CHO-能量变化如图所
3
示。已知 为快速平衡,下列说法正确的是( )
.
A.反应Ⅱ、Ⅲ为决速步B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CHOH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
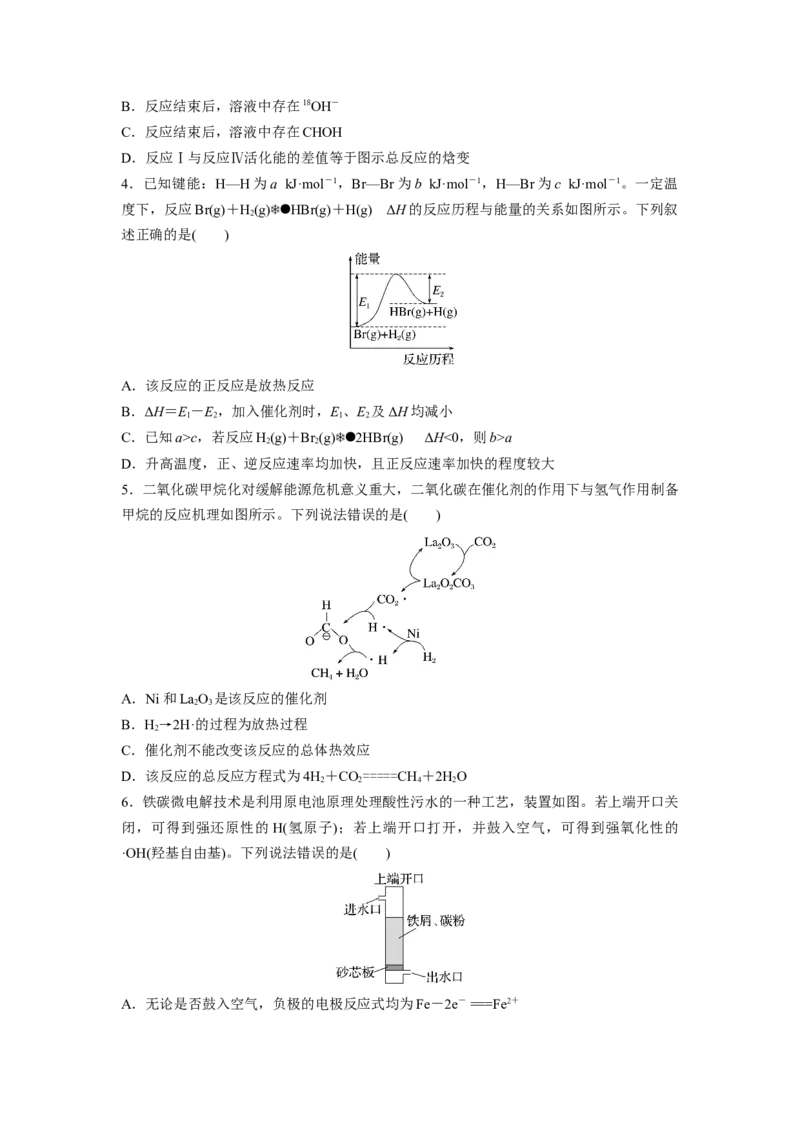
4.已知键能:H—H为a kJ·mol-1,Br—Br为b kJ·mol-1,H—Br为c kJ·mol-1。一定温
度下,反应Br(g)+H(g)HBr(g)+H(g) ΔH的反应历程与能量的关系如图所示。下列叙
2
述正确的是( )
A.该反应的正反应是放热反应
B.ΔH=E-E,加入催化剂时,E、E 及ΔH均减小
1 2 1 2
C.已知a>c,若反应H(g)+Br (g)2HBr(g) ΔH<0,则b>a
2 2
D.升高温度,正、逆反应速率均加快,且正反应速率加快的程度较大
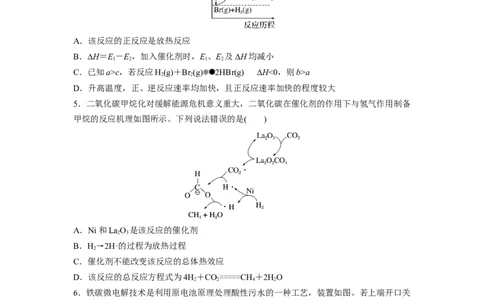
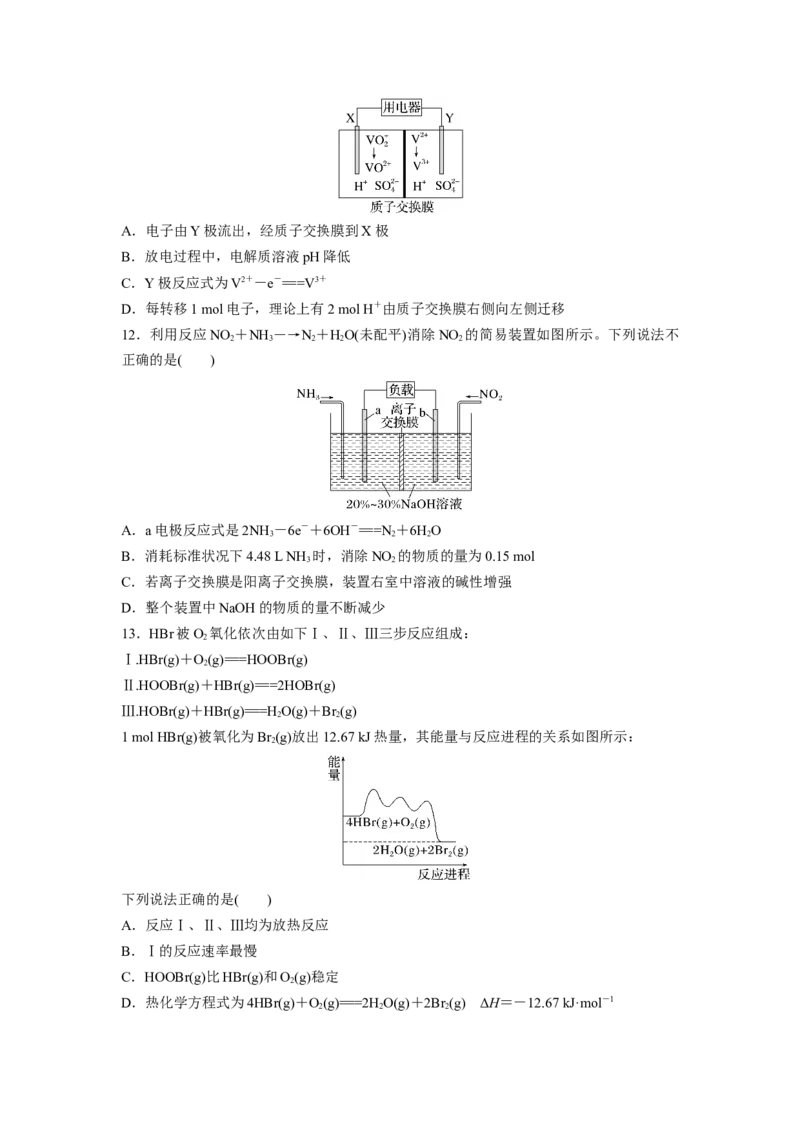
5.二氧化碳甲烷化对缓解能源危机意义重大,二氧化碳在催化剂的作用下与氢气作用制备
甲烷的反应机理如图所示。下列说法错误的是( )
A.Ni和LaO 是该反应的催化剂
2 3
B.H→2H·的过程为放热过程
2
C.催化剂不能改变该反应的总体热效应
D.该反应的总反应方程式为4H+CO=====CH+2HO
2 2 4 2
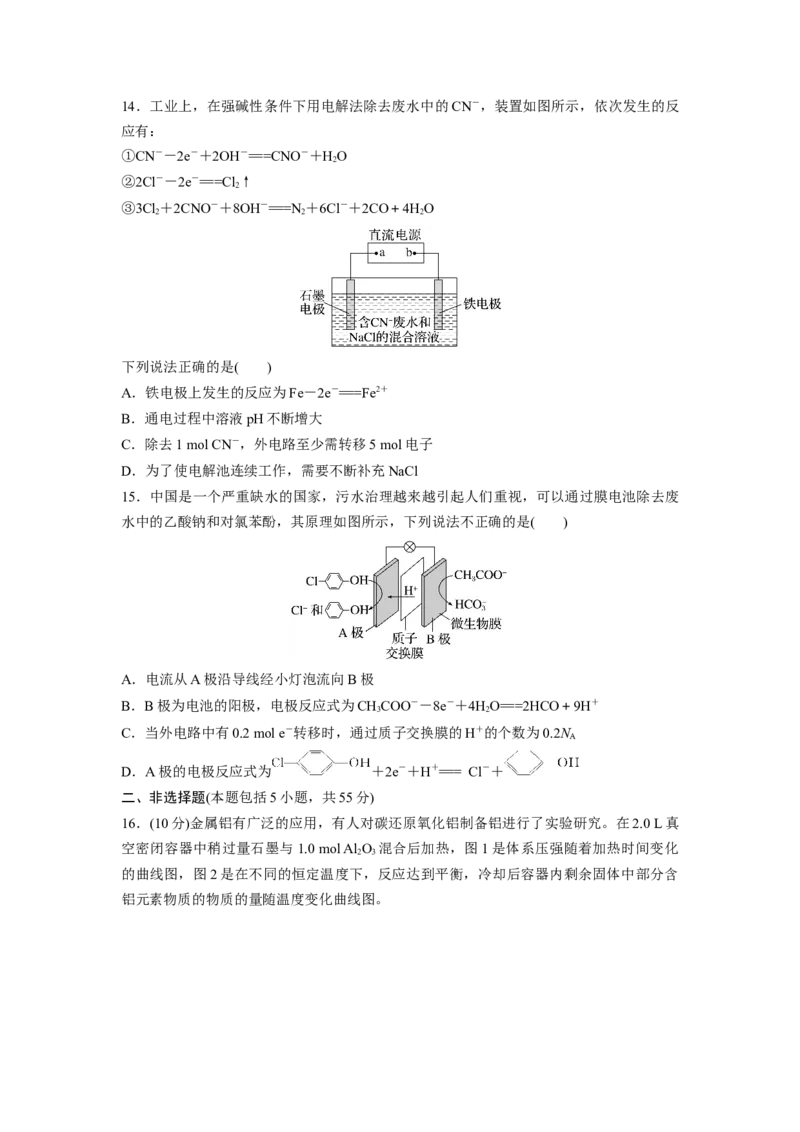
6.铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如图。若上端开口关
闭,可得到强还原性的H(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的
·OH(羟基自由基)。下列说法错误的是( )
A.无论是否鼓入空气,负极的电极反应式均为Fe-2e- ===Fe2+B.不鼓入空气时,正极的电极反应式为H+ + e- === H
C.鼓入空气时,每生成1 mol·OH有2 mol电子发生转移
D.处理含有草酸(H C O)的污水时,上端开口应打开并鼓入空气
2 2 4
7.原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法正确的是
( )
A.由Fe、Cu、FeCl 溶液组成的原电池中,负极反应式为Cu-2e-===Cu2+
3
B.由Al、Cu、稀硫酸组成的原电池中,负极反应式为Cu-2e-===Cu2+
C.由Al、Mg、NaOH溶液组成的原电池中,负极反应式为 Al+4OH--3e-===AlO+
2HO
2
D.由Al、Cu、浓硝酸组成的原电池中,负极反应式为Al-3e-===Al3+
8.化学与生产、生活有着密切的关系,下列叙述正确的是( )
A.钢铁发生析氢腐蚀时,H+得电子释放出H,钢铁被腐蚀
2
B.钢铁发生吸氧腐蚀时,OH-失电子释放出O,钢铁被腐蚀
2
C.船底镶嵌锌块,锌发生还原反应而被消耗,以保护船体
D.外加电源的正极连接在海水中的钢铁闸门上,可保护闸门
9.1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:
①CH==CH—CH==CH(g)+2H(g)―→CHCHCHCH(g) ΔH=-236.6 kJ·mol-1
2 2 2 3 2 2 3
②CH—C≡C—CH(g)+2H(g)―→CHCHCHCH(g) ΔH=-272.7 kJ·mol-1
3 3 2 3 2 2 3
由此不能判断( )
A.1,3-丁二烯和2-丁炔稳定性的相对大小
B.1,3-丁二烯和2-丁炔分子储存能量的相对高低
C.1,3-丁二烯和2-丁炔相互转化的热效应
D.一个碳碳三键的键能与两个碳碳双键的键能之和的大小
10 . 常 温 下 , 0.01 mol·L - 1 MOH 溶 液 的 pH 为 10 。 已 知 : 2MOH(aq) +
HSO (aq)===MSO (aq)+2HO(l) ΔH =-24.2 kJ·mol-1;H+(aq)+OH-(aq)===HO(l)
2 4 2 4 2 1 2
ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
2
A.+33.1 kJ·mol-1
B.+45.2 kJ·mol-1
C.-81.5 kJ·mol-1
D.-33.1 kJ·mol-1
11.全钒氧化还原液流电池是一种新型绿色的二次电池,其工作原理如图所示。下列叙述
正确的是( )A.电子由Y极流出,经质子交换膜到X极
B.放电过程中,电解质溶液pH降低
C.Y极反应式为V2+-e-===V3+
D.每转移1 mol电子,理论上有2 mol H+由质子交换膜右侧向左侧迁移
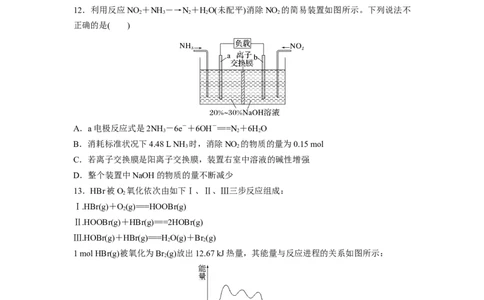
12.利用反应NO +NH ―→N +HO(未配平)消除NO 的简易装置如图所示。下列说法不
2 3 2 2 2
正确的是( )
A.a电极反应式是2NH -6e-+6OH-===N+6HO
3 2 2
B.消耗标准状况下4.48 L NH 时,消除NO 的物质的量为0.15 mol
3 2
C.若离子交换膜是阳离子交换膜,装置右室中溶液的碱性增强
D.整个装置中NaOH的物质的量不断减少
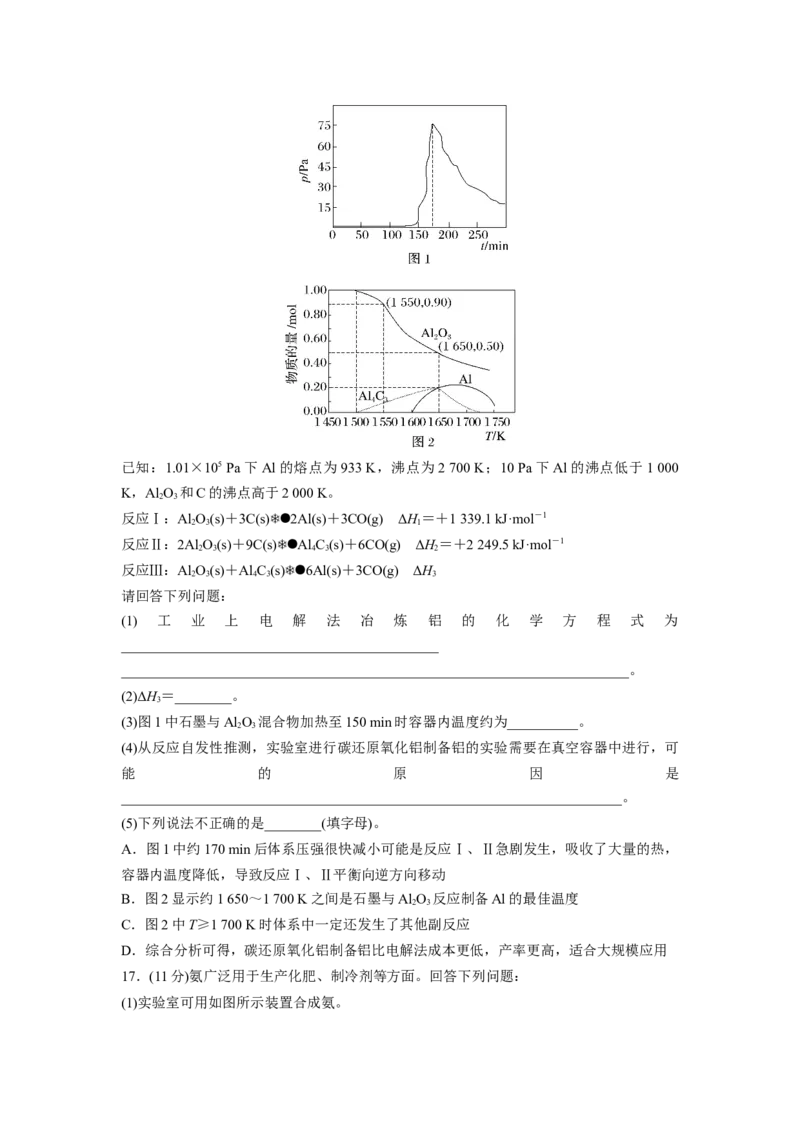
13.HBr被O 氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成:
2
Ⅰ.HBr(g)+O(g)===HOOBr(g)
2
Ⅱ.HOOBr(g)+HBr(g)===2HOBr(g)
Ⅲ.HOBr(g)+HBr(g)===HO(g)+Br (g)
2 2
1 mol HBr(g)被氧化为Br (g)放出12.67 kJ热量,其能量与反应进程的关系如图所示:
2
下列说法正确的是( )
A.反应Ⅰ、Ⅱ、Ⅲ均为放热反应
B.Ⅰ的反应速率最慢
C.HOOBr(g)比HBr(g)和O(g)稳定
2
D.热化学方程式为4HBr(g)+O(g)===2HO(g)+2Br (g) ΔH=-12.67 kJ·mol-1
2 2 214.工业上,在强碱性条件下用电解法除去废水中的CN-,装置如图所示,依次发生的反
应有:
①CN--2e-+2OH-===CNO-+HO
2
②2Cl--2e-===Cl↑
2
③3Cl+2CNO-+8OH-===N+6Cl-+2CO+4HO
2 2 2
下列说法正确的是( )
A.铁电极上发生的反应为Fe-2e-===Fe2+
B.通电过程中溶液pH不断增大
C.除去1 mol CN-,外电路至少需转移5 mol电子
D.为了使电解池连续工作,需要不断补充NaCl
15.中国是一个严重缺水的国家,污水治理越来越引起人们重视,可以通过膜电池除去废
水中的乙酸钠和对氯苯酚,其原理如图所示,下列说法不正确的是( )
A.电流从A极沿导线经小灯泡流向B极
B.B极为电池的阳极,电极反应式为CHCOO--8e-+4HO===2HCO+9H+
3 2
C.当外电路中有0.2 mol e-转移时,通过质子交换膜的H+的个数为0.2N
A
D.A极的电极反应式为 +2e-+H+=== Cl-+
二、非选择题(本题包括5小题,共55分)
16.(10分)金属铝有广泛的应用,有人对碳还原氧化铝制备铝进行了实验研究。在2.0 L真
空密闭容器中稍过量石墨与1.0 mol Al O 混合后加热,图1是体系压强随着加热时间变化
2 3
的曲线图,图2是在不同的恒定温度下,反应达到平衡,冷却后容器内剩余固体中部分含
铝元素物质的物质的量随温度变化曲线图。已知:1.01×105 Pa下Al的熔点为933 K,沸点为2 700 K;10 Pa下Al的沸点低于1 000
K,Al O 和C的沸点高于2 000 K。
2 3
反应Ⅰ:Al O(s)+3C(s)2Al(s)+3CO(g) ΔH=+1 339.1 kJ·mol-1
2 3 1
反应Ⅱ:2Al O(s)+9C(s)Al C (s)+6CO(g) ΔH=+2 249.5 kJ·mol-1
2 3 4 3 2
反应Ⅲ:Al O(s)+Al C (s)6Al(s)+3CO(g) ΔH
2 3 4 3 3
请回答下列问题:
(1) 工 业 上 电 解 法 冶 炼 铝 的 化 学 方 程 式 为
_____________________________________________
________________________________________________________________________。
(2)ΔH=________。
3
(3)图1中石墨与Al O 混合物加热至150 min时容器内温度约为__________。
2 3
(4)从反应自发性推测,实验室进行碳还原氧化铝制备铝的实验需要在真空容器中进行,可
能 的 原 因 是
_______________________________________________________________________。
(5)下列说法不正确的是________(填字母)。
A.图1中约170 min后体系压强很快减小可能是反应Ⅰ、Ⅱ急剧发生,吸收了大量的热,
容器内温度降低,导致反应Ⅰ、Ⅱ平衡向逆方向移动
B.图2显示约1 650~1 700 K之间是石墨与Al O 反应制备Al的最佳温度
2 3
C.图2中T≥1 700 K时体系中一定还发生了其他副反应
D.综合分析可得,碳还原氧化铝制备铝比电解法成本更低,产率更高,适合大规模应用
17.(11分)氨广泛用于生产化肥、制冷剂等方面。回答下列问题:
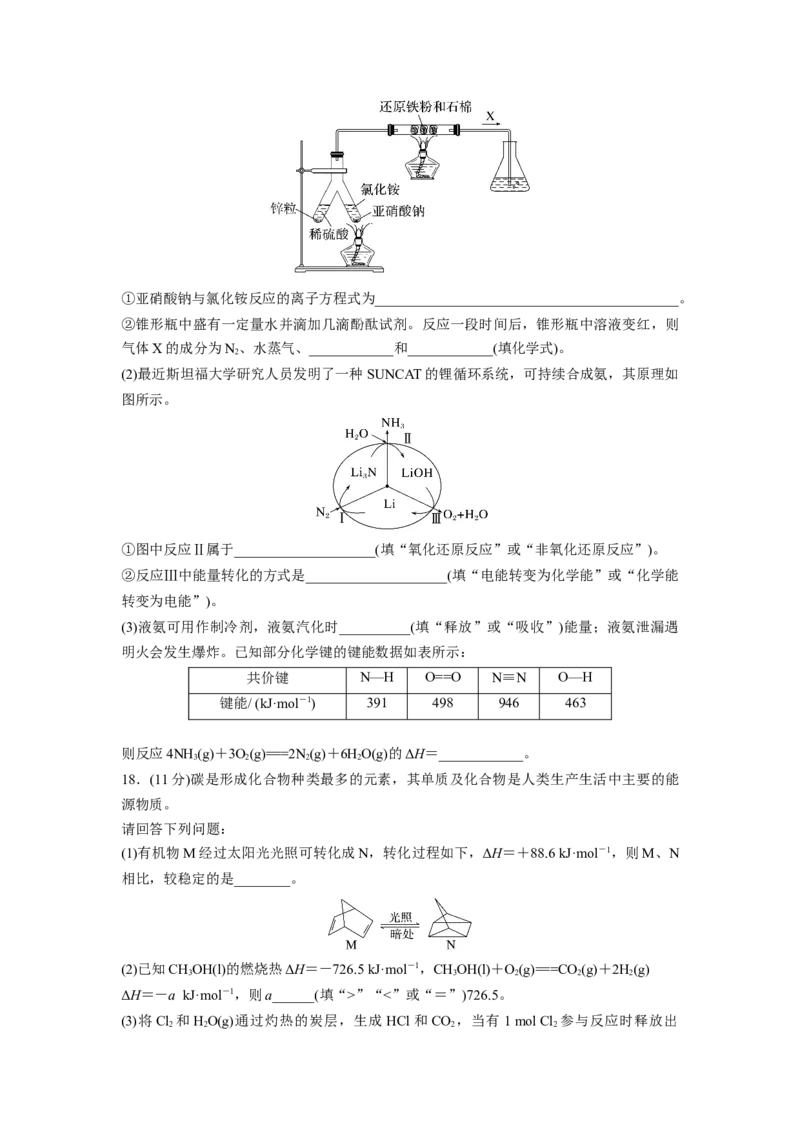
(1)实验室可用如图所示装置合成氨。①亚硝酸钠与氯化铵反应的离子方程式为___________________________________________。
②锥形瓶中盛有一定量水并滴加几滴酚酞试剂。反应一段时间后,锥形瓶中溶液变红,则
气体X的成分为N、水蒸气、____________和____________(填化学式)。
2
(2)最近斯坦福大学研究人员发明了一种SUNCAT的锂循环系统,可持续合成氨,其原理如
图所示。
①图中反应Ⅱ属于____________________(填“氧化还原反应”或“非氧化还原反应”)。
②反应Ⅲ中能量转化的方式是____________________(填“电能转变为化学能”或“化学能
转变为电能”)。
(3)液氨可用作制冷剂,液氨汽化时__________(填“释放”或“吸收”)能量;液氨泄漏遇
明火会发生爆炸。已知部分化学键的键能数据如表所示:
共价键 N—H O==O N≡N O—H
键能/ (kJ·mol-1) 391 498 946 463
则反应4NH (g)+3O(g)===2N(g)+6HO(g)的ΔH=____________。
3 2 2 2
18.(11分)碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活中主要的能
源物质。
请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下,ΔH=+88.6 kJ·mol-1,则M、N
相比,较稳定的是________。
(2)已知CHOH(l)的燃烧热ΔH=-726.5 kJ·mol-1,CHOH(l)+O(g)===CO(g)+2H(g)
3 3 2 2 2
ΔH=-a kJ·mol-1,则a______(填“>”“<”或“=”)726.5。
(3)将Cl 和HO(g)通过灼热的炭层,生成 HCl和CO ,当有1 mol Cl 参与反应时释放出
2 2 2 2145.0 kJ 热 量 , 写 出 该 反 应 的 热 化 学 方 程 式 :
_____________________________________________。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温
下煅烧,所得物质可作耐高温材料:4Al(s)+3TiO(s)+3C(s)===2Al O(s)+3TiC(s) ΔH=
2 2 3
-1 176.0 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为__________。
(5)已知:①C(s)+O(g)===CO(g) ΔH=-393.5 kJ·mol-1
2 2 1
②2CO(g)+O(g)===2CO(g)
2 2
ΔH=-566 kJ·mol-1
2
③TiO(s)+2Cl(g)===TiCl (s)+O(g)
2 2 4 2
ΔH=+141 kJ·mol-1
3
则TiO(s)+2Cl(g)+2C(s)===TiCl (s)+2CO(g)的ΔH=__________。
2 2 4
(6)已知拆开1 mol H—H,1 mol N—H,1 mol N≡N分别需要的能量是436 kJ、391 kJ、946
kJ , 则 N(g) 与 H(g) 反 应 生 成 NH (g) 的 热 化 学 方 程 式 为
2 2 3
___________________________________。
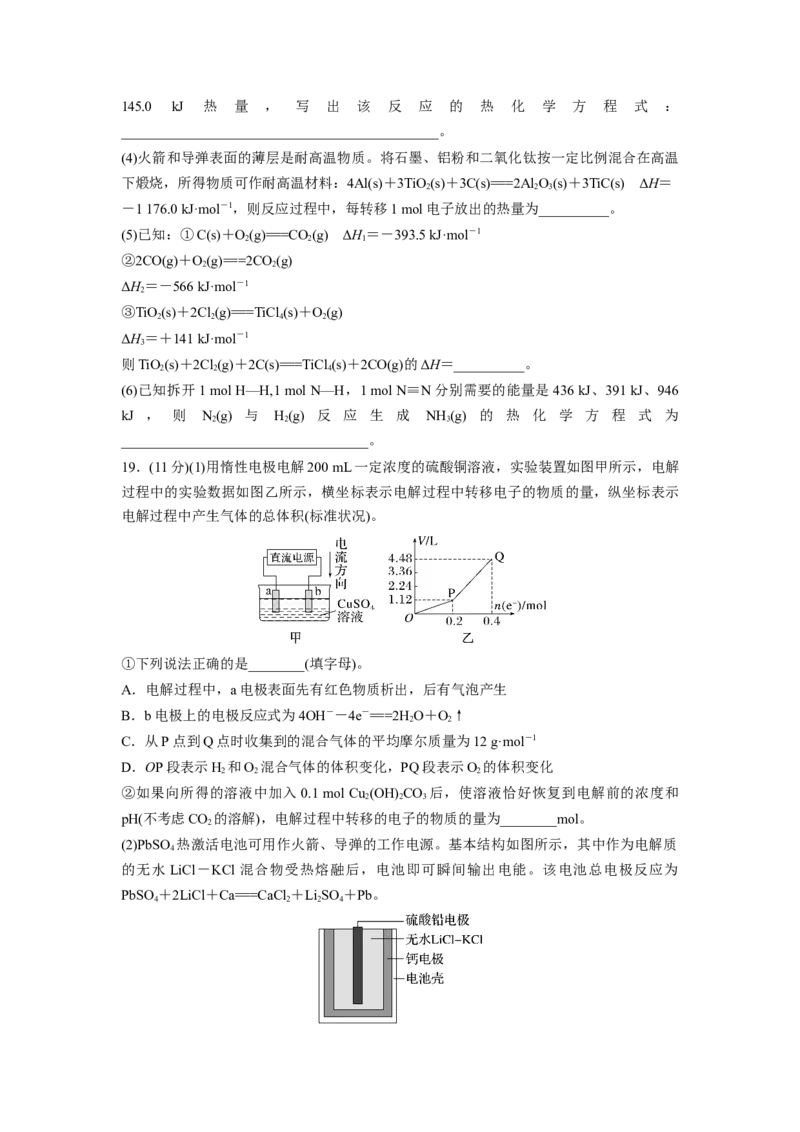
19.(11分)(1)用惰性电极电解200 mL一定浓度的硫酸铜溶液,实验装置如图甲所示,电解
过程中的实验数据如图乙所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示
电解过程中产生气体的总体积(标准状况)。
①下列说法正确的是________(填字母)。
A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上的电极反应式为4OH--4e-===2HO+O↑
2 2
C.从P点到Q点时收集到的混合气体的平均摩尔质量为12 g·mol-1
D.OP段表示H 和O 混合气体的体积变化,PQ段表示O 的体积变化
2 2 2
②如果向所得的溶液中加入0.1 mol Cu (OH) CO 后,使溶液恰好恢复到电解前的浓度和
2 2 3
pH(不考虑CO 的溶解),电解过程中转移的电子的物质的量为________mol。
2
(2)PbSO 热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质
4
的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总电极反应为
PbSO +2LiCl+Ca===CaCl +LiSO +Pb。
4 2 2 4①放电过程中,Li+向________(填“负极”或“正极”)移动。
②负极反应式为__________________________________________________________。
③电路中每转移0.2 mol电子,理论上生成________g Pb。
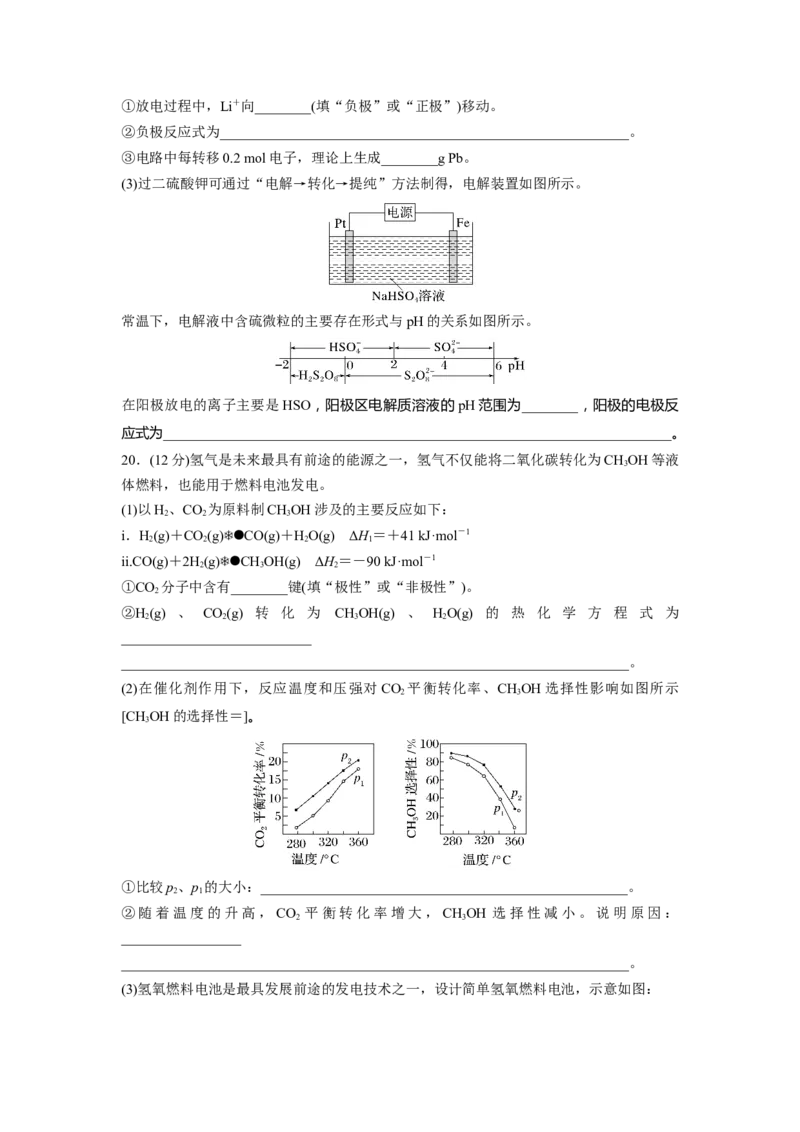
(3)过二硫酸钾可通过“电解→转化→提纯”方法制得,电解装置如图所示。
常温下,电解液中含硫微粒的主要存在形式与pH的关系如图所示。
在阳极放电的离子主要是HSO,阳极区电解质溶液的pH范围为________,阳极的电极反
应式为________________________________________________________________________。
20.(12分)氢气是未来最具有前途的能源之一,氢气不仅能将二氧化碳转化为CHOH等液
3
体燃料,也能用于燃料电池发电。
(1)以H、CO 为原料制CHOH涉及的主要反应如下:
2 2 3
i.H(g)+CO(g)CO(g)+HO(g) ΔH=+41 kJ·mol-1
2 2 2 1
ii.CO(g)+2H(g)CHOH(g) ΔH=-90 kJ·mol-1
2 3 2
①CO 分子中含有________键(填“极性”或“非极性”)。
2
②H(g) 、 CO(g) 转 化 为 CHOH(g) 、 HO(g) 的 热 化 学 方 程 式 为
2 2 3 2
___________________________
________________________________________________________________________。
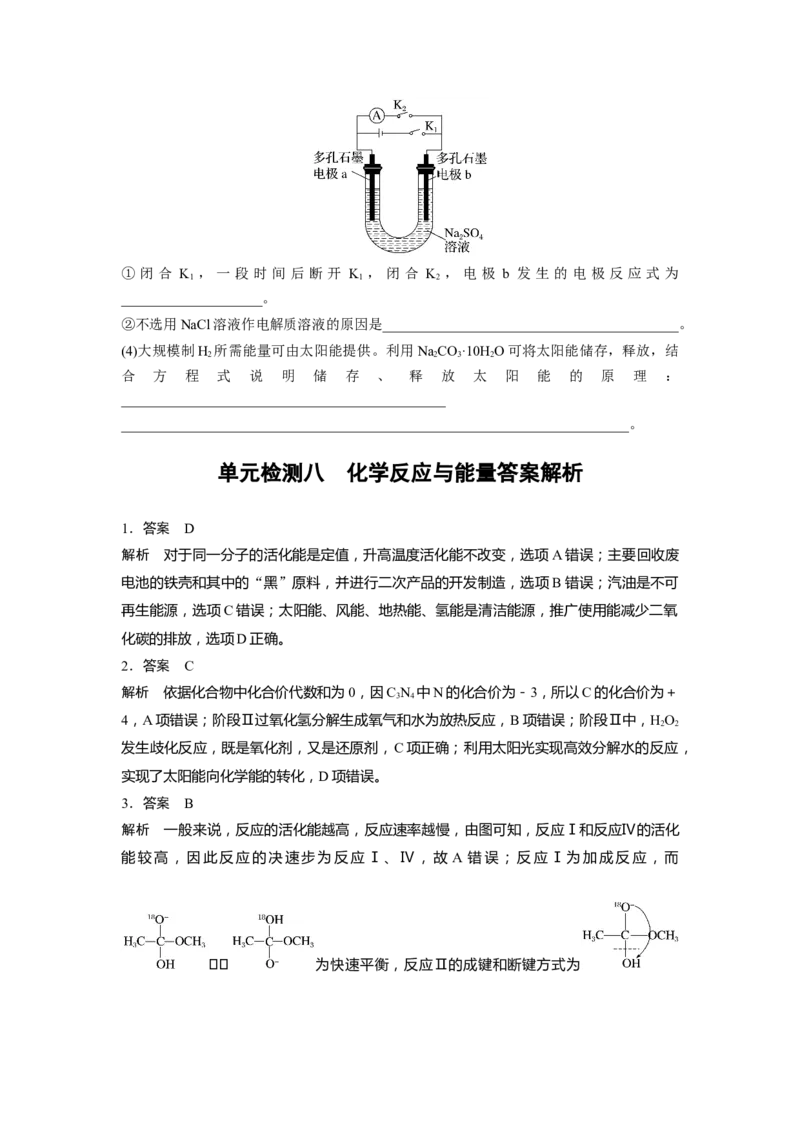
(2)在催化剂作用下,反应温度和压强对 CO 平衡转化率、CHOH选择性影响如图所示
2 3
[CHOH的选择性=]。
3
①比较p、p 的大小:____________________________________________________。
2 1
②随着温度的升高,CO 平衡转化率增大,CHOH 选择性减小。说明原因:
2 3
_________________
________________________________________________________________________。
(3)氢氧燃料电池是最具发展前途的发电技术之一,设计简单氢氧燃料电池,示意如图:① 闭 合 K , 一 段 时 间 后 断 开 K , 闭 合 K , 电 极 b 发 生 的 电 极 反 应 式 为
1 1 2
____________________。
②不选用NaCl溶液作电解质溶液的原因是__________________________________________。
(4)大规模制H 所需能量可由太阳能提供。利用NaCO·10H O可将太阳能储存,释放,结
2 2 3 2
合 方 程 式 说 明 储 存 、 释 放 太 阳 能 的 原 理 :
______________________________________________
________________________________________________________________________。
单元检测八 化学反应与能量答案解析
1.答案 D
解析 对于同一分子的活化能是定值,升高温度活化能不改变,选项A错误;主要回收废
电池的铁壳和其中的“黑”原料,并进行二次产品的开发制造,选项B错误;汽油是不可
再生能源,选项C错误;太阳能、风能、地热能、氢能是清洁能源,推广使用能减少二氧
化碳的排放,选项D正确。
2.答案 C
解析 依据化合物中化合价代数和为0,因C N 中N的化合价为-3,所以C的化合价为+
3 4
4,A项错误;阶段Ⅱ过氧化氢分解生成氧气和水为放热反应,B项错误;阶段Ⅱ中,HO
2 2
发生歧化反应,既是氧化剂,又是还原剂,C项正确;利用太阳光实现高效分解水的反应,
实现了太阳能向化学能的转化,D项错误。
3.答案 B
解析 一般来说,反应的活化能越高,反应速率越慢,由图可知,反应Ⅰ和反应Ⅳ的活化
能较高,因此反应的决速步为反应Ⅰ、Ⅳ,故 A 错误;反应Ⅰ为加成反应,而
为快速平衡,反应Ⅱ的成键和断键方式为或 ,后者能生成18OH-,因此反应结束后,溶液中存在18OH-,故B正确;
反应Ⅲ的成键和断键方式为 或 ,因此反应结束后溶液中不
会存在CHOH,故C错误;该总反应对应反应物的总能量高于生成物的总能量,总反应为
放热反应,因此 和CHO-的总能量与 和OH-的总能量之差
3
等于图示总反应的焓变,故D错误。
4.答案 D
解析 由图可知,E 为正反应活化能,E 为逆反应活化能,E>E ,ΔH=E -E>0,为吸
1 2 1 2 1 2
热反应,A错误;加入催化剂时,E 、E 减小,但ΔH不变,B错误;由于H—H的键能大
1 2
于H—Br的键能,若反应H(g)+Br (g)2HBr(g) ΔH<0,则Br—Br的键能应小于H—Br
2 2
的键能,即c>b,又a>c,则a>b,C错误;该反应为吸热反应,升高温度,正、逆反应速
率均加快,正反应速率加快的程度大于逆反应速率加快的程度,使平衡向正反应方向移动,
D正确。
5.答案 B
解析 由图可知该循环中Ni和LaO 是该反应的催化剂,故A正确;H→2H·为断键的过
2 3 2
程,该过程为吸热过程,故B错误;催化剂可以降低反应的活化能,但不能改变该反应的
总体热效应,故C正确;根据图中信息得到该反应的总反应方程式为4H +CO=====CH
2 2 4
+2HO,故D正确。
2
6.答案 C
解析 在原电池中,铁作负极,电极反应式是 Fe-2e-===Fe2+,故A正确;不鼓入空气
时,正极发生还原反应为H++ e- === H,故B正确;鼓入空气时,氧气在正极发生的电
极反应为O+4e-+2HO===4·OH,每生成1 mol·OH有1 mol电子发生转移,故C错误。
2 2
7.答案 C
解析 该原电池中,Fe失电子作负极,Cu作正极,负极反应式为Fe-2e-===Fe2+,故A
错误;该原电池中,Al失电子作负极、Cu作正极,负极反应式为Al-3e-===Al3+,故B
错误;该原电池中,Al失电子作负极、Mg作正极,负极反应式为Al+4OH--3e-===AlO
+2HO,故C正确;该原电池中,铜失电子作负极、Al作正极,负极反应式为Cu-2e-
2
===Cu2+,故D错误。
8.答案 A
解析 B项发生吸氧腐蚀时,正极反应式为O +2HO+4e-===4OH-,整个过程是吸收O
2 2 2而不是释放O ,错误;C项为牺牲阳极的阴极保护法,金属锌发生氧化反应,错误;D项
2
为外加电流的阴极保护法,钢铁闸门应与外加电源的负极相连,错误。
9.答案 D
解析 根据盖斯定律可知,①-②即得到 CH==CH—CH==CH(g)―→CH—C≡C—
2 2 3
CH(g) ΔH=+36.1 kJ·mol-1,这说明1,3-丁二烯转化为2-丁炔是吸热反应,因此在物质
3
的量相等的条件下,1,3-丁二烯的总能量低于2-丁炔的总能量,则1,3-丁二烯比2-丁炔的稳
定性强,因此A、B、C三项均正确;反应热等于断开化学键吸收的能量与形成化学键所放
出的能量的差值,但由于不能确定碳碳单键的键能,因此根据热化学方程式不能确定一个
碳碳三键的键能与两个碳碳双键的键能之和的大小,D项错误。
10.答案 B
解析 根据常温下,0.01 mol·L-1 MOH溶液的pH=10知,MOH为弱碱,MOH溶液与硫
酸的中和反应可以看作两个过程:MOH(aq)M+(aq)+OH-(aq) ΔH、H+(aq)+OH-
(aq)===
HO(l) ΔH ,根据盖斯定律知ΔH =2(ΔH+ΔH),则ΔH=ΔH -ΔH =×(-24.2 kJ·mol-1)
2 2 1 2 1 2
-(-57.3 kJ·mol-1)=+45.2 kJ·mol-1,B项正确。
11.答案 C
解析 观察装置图,由物质转化可以确定右边发生氧化反应,Y极为负极,左边发生还原
反应,X极为正极。电子由Y极经导线流向X极,故A错误;放电过程中,电池反应式为
V2++VO+2H+===V3++VO2++HO,消耗H+,pH升高,故B错误;Y极为负极,发生
2
氧化反应,由离子转化关系知反应式为V2+-e-===V3+,故C正确;X极反应式为VO+
2H++e-===VO2++HO,得失电子数决定氢离子迁移数目,转移1 mol电子,只有1 mol
2
H+迁移,故D错误。
12.答案 D
解析 a电极通入的是NH ,发生氧化反应,电极反应式是2NH -6e-+6OH-===N +
3 3 2
6HO,A项正确;标准状况下4.48 L NH 的物质的量为0.2 mol,根据得失电子守恒可得
2 3
4NH ~3NO ,列式得=,解得n(NO )=0.15 mol,B项正确;右室中发生的电极反应为
3 2 2
2NO +8e-+4HO===N +8OH-,钠离子透过阳离子交换膜进入右极室,因反应生成 OH
2 2 2
-,使右室溶液的碱性增强,C项正确;因电池总反应为6NO +8NH ===7N +12HO,所
2 3 2 2
以整个装置中NaOH的物质的量不变,D项错误。
13.答案 B
解析 第一步反应的反应物总能量低于生成物总能量,所以为吸热反应,故A错误;第一
步反应需要的活化能最大,即反应Ⅰ的反应速率最慢,故 B正确;HOOBr(g)的能量比
HBr(g)和 O(g)的总能量高,能量越高,物质越不稳定,故 C 错误;根据题意,1 mol
2
HBr(g)被氧化为Br (g)放出12.67 kJ热量,则热化学方程式为4HBr(g)+O(g)===2HO(g)+
2 2 22Br (g) ΔH=-50.68 kJ·mol-1,故D错误。
2
14.答案 C
解析 铁电极为电解池的阴极,则只能是水提供的氢离子得电子,A错误;根据电极反应
式,阴极为2HO+2e-===H↑+2OH-,阳极为①CN--2e-+2OH-===CNO-+HO,
2 2 2
②2Cl--2e-===Cl↑,③3Cl +2CNO-+8OH-===N +6Cl-+2CO+4HO,得失电子数
2 2 2 2
相等时,消耗氢氧根离子,pH减小,B错误;根据反应:3Cl +2CNO-+8OH-===N +
2 2
6Cl-+2CO+4HO,除去1 mol CN-,消耗1.5 mol氯气,转移3 mol电子,根据CN--2e-
2
+2OH-===CNO-+HO,转移2 mol电子,所以外电路至少需转移5 mol电子,C正确;
2
根据电极反应,为了使电解池连续工作,需要补充氢氧化钠,D错误。
15.答案 B
解析 原电池工作时,电流从正极经导线流向负极,即电流从A极沿导线经小灯泡流向B
极,故 A 正确;B 极为电池的负极,失去电子,电极反应式为 CHCOO--8e-+
3
4HO===2HCO+9H+,故B错误;根据得失电子守恒可知,当外电路中有 0.2 mol e-转移
2
时,通过质子交换膜的H+的个数为0.2N ,故C正确;A为正极,得到电子,正极有氢离
A
子参与反应,电极反应式为 +2e-+H+===Cl-+ ,故D正确。
16.答案 (1)2AlO(熔融)=====4Al+3O↑
2 3 2
(2)+1 767.8 kJ·mol-1 (3)1 500 K (4)减小体系压强可以使铝的沸点降低,实验时铝呈气
态使反应Ⅰ熵变(或生成物熵)增大,有利于反应自发进行 (5)D
解析 (2)根据盖斯定律,将(Ⅰ)×3-(Ⅱ),整理可得Al O(s)+Al C (s)6Al(s)+3CO(g)
2 3 4 3
ΔH=+1 767.8 kJ·mol-1。
3
(3)图1中石墨与Al O 混合物加热至150 min时,反应还未开始,物质的量为 1.0 mol;结
2 3
合图2中物质的量与温度关系可知:反应温度约为1 500 K。
(5)图1中约170 min后体系压强很快减小可能是反应Ⅰ、Ⅱ急剧发生,吸收了大量的热,
导致容器内温度降低,化学平衡向放热的逆方向移动,A正确;由图2显示约1 650~1 700
K之间Al生成量增加,因此是石墨与Al O 反应制备Al的最佳温度,B正确;图2中T≥1
2 3
700 K时,体系中Al的物质的量逐渐减小,一定是体系中发生了其他副反应,如发生反应
产生Al C ,C正确;综合分析可知:碳还原氧化铝所需温度太高,难以实现,制备铝比电
4 3
解法成本更高,产率更低,不适合大规模应用,D错误。
17.答案 (1)①NO+NH=====N↑+2HO
2 2
②H NH (2)①非氧化还原反应
2 3
②电能转变为化学能 (3)吸收 -1 262 kJ·mol-1
解析 (1)①亚硝酸钠具有强氧化性与氯化铵发生氧化还原反应生成氮气,反应的离子方程
式为NO+NH=====N↑+2HO。②锌与稀硫酸反应生成的氢气与亚硝酸钠和氯化铵反应
2 2
生成的氮气在催化剂作用下反应生成了氨气,因此锥形瓶中酚酞溶液变红,则气体X的成分为N、水蒸气、H、NH 。(2)①反应Ⅱ是LiN与HO反应生成NH 和LiOH的过程,反
2 2 3 3 2 3
应中没有元素化合价的变化,属于非氧化还原反应。②反应Ⅲ中氢氧化锂转变为锂、氧气
和水,发生了非自发的氧化还原反应,属于电解池反应,能量转化的方式是电能转变为化
学能。
(3)液氨可用作制冷剂,是因为液氨汽化时吸收能量,导致周围温度降低;反应 4NH (g)+
3
3O(g)===2N(g)+6HO(g) ΔH=反应物的键能之和-生成物的键能之和=391 kJ·mol-
2 2 2
1×3
×4+498 kJ·mol-1×3-946 kJ·mol-1×2-463 kJ·mol-1×2×6=-1 262 kJ·mol-1。
18.答案 (1)M (2)<
(3)2Cl (g)+2HO(g)+C(s)===4HCl(g)+CO(g) ΔH=-290.0 kJ·mol-1
2 2 2
(4)98.0 kJ (5)-80 kJ·mol-1
(6)N (g)+3H(g)2NH (g) ΔH=-92.0 kJ·mol-1
2 2 3
解析 (1)有机物M经过太阳光光照转化为N的过程吸收能量,则N能量高,比M活泼,
较稳定的化合物为M。
(2)甲醇燃烧生成CO(g)和H(g)属于不完全燃烧,放出的热量少,所以a<726.5。
2 2
(3)有1 mol Cl 参与反应时释放出145.0 kJ热量,2 mol 氯气反应放热290.0 kJ,反应的热化
2
学方程式:2Cl(g)+2HO(g)+C(s)===4HCl(g)+CO(g) ΔH=-290.0 kJ·mol-1。
2 2 2
(4)4Al(s)+3TiO(s)+3C(s)===2Al O(s)+3TiC(s) ΔH=-1 176.0 kJ·mol-1,转移12 mol电
2 2 3
子放热1 176.0 kJ,则反应过程中,每转移1 mol电子放出的热量为 kJ=98.0 kJ。
(5)根据盖斯定律,由①×2-②+③得:TiO(s)+2Cl(g)+2C(s)===TiCl (s)+2CO(g),其焓
2 2 4
变ΔH=ΔH×2-ΔH+ΔH=-80 kJ·mol-1。
1 2 3
(6)在反应N +3H2NH 中,断裂3 mol H—H、1 mol N≡N共吸收的能量:3×436 kJ+
2 2 3
946 kJ=2 254 kJ,生成2 mol NH ,共形成6 mol N—H,放出的能量为6×391 kJ=2 346
3
kJ,吸收的热量少,放出的热量多,该反应为放热反应,放出的热量为 2 346 kJ-2 254 kJ
=92 kJ,则N(g)与H(g)反应生成NH (g)的热化学方程式为N(g)+3H(g)2NH (g) ΔH
2 2 3 2 2 3
=-92.0 kJ·
mol-1。
19.答案 (1)①ABC ②0.6 (2)①正极 ②Ca+2Cl--2e-===CaCl ③20.7 (3)0~2
2
2HSO-2e-===SO+2H+
2
解析 (1)①根据电流方向分析,判断b为阳极,a为阴极,用惰性电极电解一定浓度的硫
酸铜溶液,电池总反应:2CuSO +2HO=====2Cu+O↑+2HSO ;结合图乙可知,通过
4 2 2 2 4
0.2 mol 电子时是电解的硫酸铜溶液,然后是电解硫酸溶液,发生的电池总反应为
2HO=====2H↑+O↑。a电极为阴极,先发生的电极反应为Cu2++2e-===Cu,后发生的
2 2 2
电极反应为2H++2e-===H↑,A对;b电极上发生的电极反应为4OH--4e-===2HO+
2 2O↑,B对;从P点到Q点时收集到H 和O 的混合气体,由电解水反应可知通过0.2 mol
2 2 2
电子时生成0.1 mol H、0.05 mol O,则混合气体的平均摩尔质量为=12 g·
2 2
mol-1,C正确;OP段表示O 的体积变化,PQ段表示H 和O 混合气体的体积变化,D错
2 2 2
误。②0.1 mol Cu (OH) CO 可以看作0.2 mol CuO、0.1 mol H O和0.1 mol CO ,相当于有
2 2 3 2 2
0.2 mol硫酸铜和0.1 mol水被电解,则转移电子的物质的量为0.6 mol。(3)在阳极放电的离
子主要是HSO,根据阳极区含硫微粒的主要存在形式与pH的关系,电解质溶液的pH范围
为0~2,故HSO失电子生成SO,故其电极反应式为2HSO-2e-===SO+2H+。
2 2
20.答案 (1)①极性 ②3H(g)+CO(g)===CHOH(g)+HO(g) ΔH=-49 kJ·mol-1
2 2 3 2
(2)①p>p ②温度升高,反应ⅰ正向进行,CO 转化率增大;反应ⅱ为放热反应,温度升
2 1 2
高,不利于CHOH的生成
3
(3)①H -2e-===2H+ ②闭合K ,a极发生反应的电极方程式:2Cl--2e-===Cl↑;闭合
2 1 2
K,a极发生反应的电极方程式:Cl+2e-===2Cl-,不能形成氢氧燃料电池
2 2
(4)Na CO·10H O===NaCO +10HO,该过程需要吸收能量,将太阳能储存;NaCO +
2 3 2 2 3 2 2 3
10HO===NaCO·10H O,该过程放出能量,将储存的太阳能释放
2 2 3 2
解析 (1)①CO 的结构简式为O==C==O,含有极性共价键。②根据盖斯定律,将ⅰ+ⅱ得
2
热化学方程式:3H(g)+CO(g)===CHOH(g)+HO(g) ΔH=-49 kJ·mol-1。(2)①根据温
2 2 3 2
度与CO 平衡转化率的关系,作等温线,增大压强,平衡向正反应方向移动,CO 的平衡
2 2
转化率增大,即p>p。②反应i为吸热反应,反应ii为放热反应,升高温度,反应ⅰ正向
2 1
进行,CO 转化率增大,反应ⅱ向逆反应方向进行,不利于CHOH的生成,因此升高温度,
2 3
CO 平衡转化率增大,CHOH选择性降低。(3)①闭合K ,该装置为电解池,电极b为阴
2 3 1
极,电极反应式为2HO+2e-===H↑+2OH-,电极a为阳极,电极反应式为2HO-4e-
2 2 2
===O↑+4H+,断开K,闭合K,构成氢氧燃料电池,电极b为负极,电极反应式为H-
2 1 2 2
2e-===2H+。②若选用NaCl溶液,阳极上发生反应的电极方程式为2Cl--2e-===Cl↑,
2
不能构成氢氧燃料电池。