文档内容
第 16 讲 金属及其化合物知识落实与拓展
复习目标 1.进一步巩固Na、Fe及其化合物的转化关系。2.了解热点金属元素及其化合物
的转化。3.能用热重分析法计算、判断金属化合物的组成。
考点一 金属及其化合物知识再落实
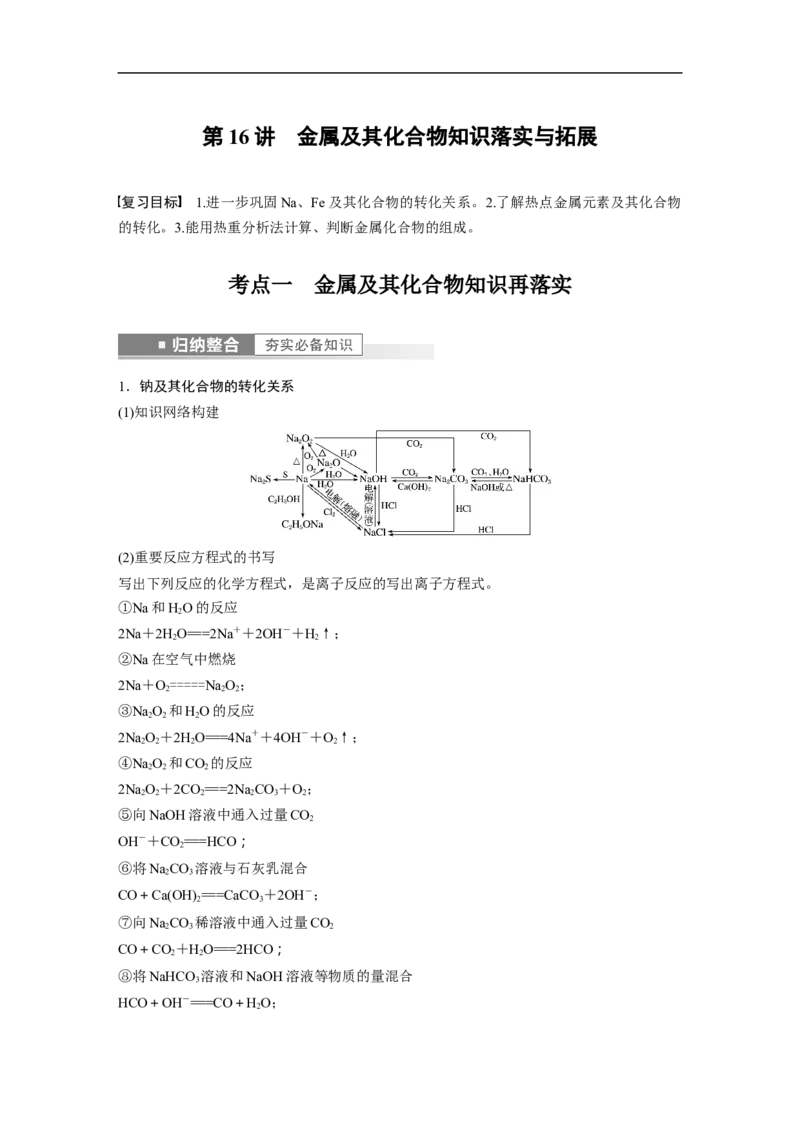
1.钠及其化合物的转化关系
(1)知识网络构建
(2)重要反应方程式的书写
写出下列反应的化学方程式,是离子反应的写出离子方程式。
①Na和HO的反应
2
2Na+2HO===2Na++2OH-+H↑;
2 2
②Na在空气中燃烧
2Na+O=====NaO;
2 2 2
③NaO 和HO的反应
2 2 2
2NaO+2HO===4Na++4OH-+O↑;
2 2 2 2
④NaO 和CO 的反应
2 2 2
2NaO+2CO===2NaCO+O;
2 2 2 2 3 2
⑤向NaOH溶液中通入过量CO
2
OH-+CO===HCO;
2
⑥将NaCO 溶液与石灰乳混合
2 3
CO+Ca(OH) ===CaCO +2OH-;
2 3
⑦向NaCO 稀溶液中通入过量CO
2 3 2
CO+CO+HO===2HCO;
2 2
⑧将NaHCO 溶液和NaOH溶液等物质的量混合
3
HCO+OH-===CO+HO;
2⑨将NaHCO 溶液与澄清石灰水等物质的量混合
3
HCO+Ca2++OH-===CaCO ↓+HO;
3 2
⑩将NaHCO 溶液与少量澄清石灰水混合
3
2HCO+Ca2++2OH-===CaCO ↓+CO+2HO。
3 2
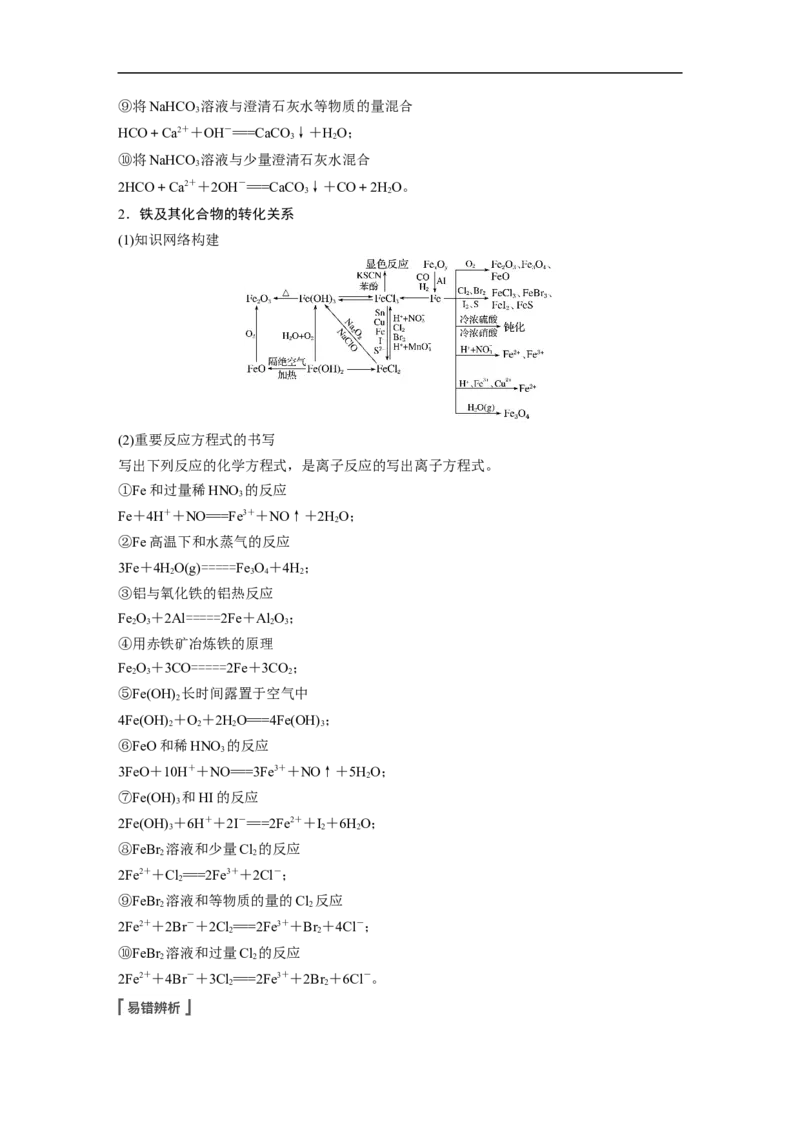
2.铁及其化合物的转化关系
(1)知识网络构建
(2)重要反应方程式的书写
写出下列反应的化学方程式,是离子反应的写出离子方程式。
①Fe和过量稀HNO 的反应
3
Fe+4H++NO===Fe3++NO↑+2HO;
2
②Fe高温下和水蒸气的反应
3Fe+4HO(g)=====Fe O+4H;
2 3 4 2
③铝与氧化铁的铝热反应
Fe O+2Al=====2Fe+Al O;
2 3 2 3
④用赤铁矿冶炼铁的原理
Fe O+3CO=====2Fe+3CO;
2 3 2
⑤Fe(OH) 长时间露置于空气中
2
4Fe(OH) +O+2HO===4Fe(OH) ;
2 2 2 3
⑥FeO和稀HNO 的反应
3
3FeO+10H++NO===3Fe3++NO↑+5HO;
2
⑦Fe(OH) 和HI的反应
3
2Fe(OH) +6H++2I-===2Fe2++I+6HO;
3 2 2
⑧FeBr 溶液和少量Cl 的反应
2 2
2Fe2++Cl===2Fe3++2Cl-;
2
⑨FeBr 溶液和等物质的量的Cl 反应
2 2
2Fe2++2Br-+2Cl===2Fe3++Br +4Cl-;
2 2
⑩FeBr 溶液和过量Cl 的反应
2 2
2Fe2++4Br-+3Cl===2Fe3++2Br +6Cl-。
2 21.Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应( )
2.Al、Cl 均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同( )
2
3.在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO 固体,铜粉会溶解( )
3
4.金属单质Na、Mg、Fe在一定条件下与水反应都生成H 和相应的碱( )
2
5.铝和氢氧化钠溶液反应生成Al(OH) 和Na( )
3
6.钠在空气中燃烧生成淡黄色的NaO( )
2
7.铁在高温下与水蒸气反应生成Fe O 和H( )
3 4 2
8.用碳酸钠和氢氧化钙反应制NaHCO ( )
3
答案 1.√ 2.√ 3.√ 4.× 5.× 6.× 7.√ 8.×
一、沉淀法除去铁元素的流程
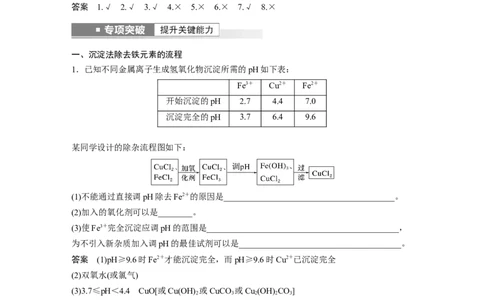
1.已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
Fe3+ Cu2+ Fe2+
开始沉淀的pH 2.7 4.4 7.0
沉淀完全的pH 3.7 6.4 9.6
某同学设计的除杂流程图如下:
(1)不能通过直接调pH除去Fe2+的原因是________________________________________。
(2)加入的氧化剂可以是________。
(3)使Fe3+完全沉淀应调pH的范围是_____________________________________________,
为不引入新杂质加入调pH的最佳试剂可以是______________________________________。
答案 (1)pH≥9.6时Fe2+才能沉淀完全,而pH≥9.6时Cu2+已沉淀完全
(2)双氧水(或氯气)
(3)3.7≤pH<4.4 CuO[或Cu(OH) 或CuCO 或Cu (OH) CO]
2 3 2 2 3
二、价态多变、形式多样的铁盐
2.硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]在空气中比一般亚铁盐稳定,是定量分析化学中常
4 2 4 2 2
用的还原剂,其实验室制备流程如图所示:下列说法不正确的是( )
A.“除油污”过程中使用热的NaCO 溶液效果更好
2 3
B.制备硫酸亚铁时铁屑与硫酸反应完全时的现象是不再有气泡产生
C.“趁热过滤”后的滤液略显黄色的原因是4Fe2++O+4H+===4Fe3++2HO
2 2
D.理论上加入(NH )SO 固体的质量为6.0 g
4 2 4
答案 D
解析 NaCO 溶液中CO水解使溶液呈碱性,油污在碱性环境中能够水解,升高温度,CO
2 3
水解平衡正向移动,溶液碱性增强,故用热的 NaCO 溶液除油污效果更好,A项正确;为
2 3
防止Fe2+氧化,加入的铁屑过量,铁屑与硫酸反应完全就是硫酸反应完全,反应完全时不
再有气泡产生,B项正确;“趁热过滤”后的滤液略显黄色是因为Fe2+在空气中被氧气氧化
为Fe3+,反应的离子方程式为4Fe2++O +4H+===4Fe3++2HO,C项正确;由工艺流程图
2 2
可知,反应的铁的质量为5.0 g-2.2 g=2.8 g,物质的量为=0.05 mol,理论上可制备
0.05 mol硫酸亚铁铵晶体,则需要加入0.05 mol (NH )SO ,所以加入(NH )SO 固体的质量
4 2 4 4 2 4
为0.05 mol×132 g·mol-1=6.6 g,D项错误。
3.[2019·江苏,18(1)]聚合硫酸铁[Fe (OH) (SO )] 广泛用于水的净化。以FeSO ·7H O为
2 6-2n 4 n m 4 2
原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
将一定量的FeSO ·7H O溶于稀硫酸,在约70 ℃下边搅拌边缓慢加入一定量的HO 溶液,
4 2 2 2
继续反应一段时间,得到红棕色黏稠液体。HO 氧化Fe2+的离子方程式为_______________;
2 2
水解聚合反应会导致溶液的pH______。
答案 2Fe2++HO+2H+===2Fe3++2HO 减小
2 2 2
解析 HO 氧化Fe2+生成Fe3+,自身被还原为HO,根据得失电子守恒、电荷守恒、元素
2 2 2
守恒配平离子方程式。Fe3+发生水解聚合反应使溶液pH减小。
4.高铁酸钾(K FeO)是一种比KMnO 、O 和Cl 的氧化能力强的强氧化剂。
2 4 4 3 2
(1)有科学家曾提出在氧气流下,温度控制在350~370 ℃,煅烧氧化铁和过氧化钾(K O)固
2 2
体混合物可直接制备高铁酸钾,该反应只有两种产物,另一种产物为氧化钾,则该反应的化
学 方 程 式 :
________________________________________________________________________。
(2)“熔融法”是最早发现+6价高铁酸盐的方法,以该法制备高铁酸盐的原理:
①FeSO +NaO――→NaFeO+NaO+NaSO +O↑
4 2 2 2 4 2 2 4 2
②NaFeO+2KOH===KFeO↓+2NaOH
2 4 2 4
反应①中被氧化的NaO 与被FeSO 还原的NaO 的物质的量比为1∶4,请写出反应①配平
2 2 4 2 2
后的化学方程式:_______________________________________________________________;
若反应①产生16.8 L(标准状况)O ,则转移电子的物质的量为________ mol;反应②能发生
2
的 原 因 是
_________________________________________________________________________。
(3)水是万物之源,为探究高铁酸钾在水质处理中发挥的作用,查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反
应 的 化 学 方 程 式 :
__________________________________________________________________。
答案 (1)Fe O +3KO=====2KFeO +KO (2)2FeSO +6NaO=====2NaFeO +2NaO+
2 3 2 2 2 4 2 4 2 2 2 4 2
2NaSO +O↑ 7.5 碱性条件下,KFeO 的溶解度小于NaFeO 的溶解度 (3)4K FeO +
2 4 2 2 4 2 4 2 4
10HO===8KOH+4Fe(OH) (胶体)+3O↑
2 3 2
解析 (2)反应中氧化剂是NaO ,还原剂是NaO 和FeSO ,4 mol Na O 氧化2 mol FeSO ,
2 2 2 2 4 2 2 4
1 mol Na O 氧化1 mol Na O,NaO 与FeSO 物质的量之比为3∶1,然后配平。由方程式可
2 2 2 2 2 2 4
知每生成1 mol O 转移10 mol电子,生成0.75 mol O 转移电子7.5 mol。反应②中KFeO 以
2 2 2 4
沉淀形式析出,说明该条件下KFeO 的溶解度小于NaFeO 的溶解度。
2 4 2 4
KFeO 的应用
2 4
(1)K FeO 中Fe呈+6价,KFeO 具有强氧化性,可用于水体的杀菌消毒。
2 4 2 4
(2)K FeO 与水反应生成Fe(OH) 胶体,吸附水体中的悬浮物,起到净水的作用。
2 4 3
考点二 化工流程题中的过渡金属
过渡金属元素常具有多种可变化合价,形成化合物种类较多,近年高考题常以Cr、Mn、
V、Zn等元素化合物的制备流程为载体,考查不同价态物质转化规律,条件控制、物质的
分离提纯等关键能力。
例1 利用钒钛磁铁矿冶炼后产生的钒渣(主要含FeO·V O 、Al O 、SiO 及少量可溶性磷酸
2 3 2 3 2
盐)生产VO 的工艺流程如下,回答下列问题:
2 5
已知:①VO 、Al O 、SiO 可与NaCO 、NaCl组成的混合钠盐在高温下反应,并转化为
2 5 2 3 2 2 3
NaVO 、NaAlO 、NaSiO 等可溶性钠盐。
3 2 2 3
②AlO+4H+===Al3++2HO。
2
(1)焙烧Ⅰ包括氧化和钠化成盐两个过程,氧化的目的是获得 VO ,写出氧化过程中
2 5
FeO·V O 发 生 反 应 的 化 学 方 程 式 :
2 3
_________________________________________________________;废渣Ⅰ的主要成分是_____________________________________________________________;
精制Ⅰ中加盐酸调pH的主要作用是________________________________,加入NH ·H O后
3 2
发生反应的离子方程式为_________________________________________________________。
(2)精制Ⅱ中加入CaCl 溶液除去磷酸盐,pH过小时影响除磷效果的原因是_______________;
2
pH过大时,沉淀量增大的原因是________________________________。
(3)沉钒所得NH VO 沉淀需进行洗涤,洗涤时除去的阴离子主要是____________。NH VO
4 3 4 3
在500 ℃时焙烧脱氨制得产品VO ,反应的化学方程式为2NH VO =====VO +HO↑+
2 5 4 3 2 5 2
2NH ↑。但脱氨过程中,部分VO 会转化成VO ,反应中氧化剂与还原剂物质的量之比为
3 2 5 2 4
3∶2,该反应的化学方程式为_____________________________________________________。
答案 (1)4FeO·V O + 5O=====2Fe O + 4VO Fe O 除Si并将AlO转化为Al3+ Al3
2 3 2 2 3 2 5 2 3
+ +3NH ·H O===Al(OH) ↓+3NH、H++NH ·H O===HO+NH
3 2 3 3 2 2
(2)形成溶解度较大的酸式盐(或形成溶解度较大的磷酸氢钙或磷酸二氢钙) 产生了Ca(OH)
2
沉淀
(3)Cl- 3VO+2NH =====3VO+N+3HO
2 5 3 2 4 2 2
解析 (1)氧化过程 FeO·V O 生成对应的金属氧化物 Fe O 和 VO ,化学方程式为
2 3 2 3 2 5
4FeO·V O + 5O=====2Fe O +4VO ;经过氧化和钠化后,VO 、Al O 、SiO 均转化为
2 3 2 2 3 2 5 2 5 2 3 2
可溶性盐,Fe O 成为滤渣;精制Ⅰ中加盐酸调pH是为了和SiO反应生成硅酸沉淀,并将
2 3
AlO转化为Al3+;加入NH ·H O后与Al3+发生反应生成Al(OH) 沉淀,还可以中和酸,反应
3 2 3
的化学方程式为Al3++3NH ·H O===Al(OH) ↓+3NH、H++NH ·H O===HO+NH。
3 2 3 3 2 2
(2)精制Ⅱ中加入CaCl 溶液生成磷酸钙沉淀,除去磷酸盐,pH过小时易形成溶解度较大的
2
酸式盐;pH过大时易形成Ca(OH) 沉淀。
2
(3)沉钒时加入试剂NH Cl,因此所得NH VO 沉淀含有的阴离子主要为Cl-;脱氨过程中,
4 4 3
部分VO 会转化成VO ,且反应中氧化剂与还原剂物质的量之比为3∶2,则VO 为氧化
2 5 2 4 2 5
剂,NH 为还原剂,还原产物为 VO ,氧化产物为 N ,则氧化还原方程式为 3VO +
3 2 4 2 2 5
2NH =====3VO+N+3HO。
3 2 4 2 2
例2 铬是一种具有战略意义的金属,它具有多种价态,单质铬熔点为1 857 ℃。
(1)工业上以铬铁矿[主要成分是Fe(CrO )]为原料冶炼铬的流程如图所示:
2 2
①Fe(CrO ) 中各元素化合价均为整数,则铬为________价。
2 2
②高温氧化时反应的化学方程式为_______________________________________。
③操作a由两种均发生了化学反应的过程构成,其内容分别是________、铝热反应。
(2)Cr(OH) 是两性氢氧化物,请写出其分别与NaOH、稀硫酸反应时生成的两种盐的化学式:
3
__________________、______________。(3)水中的铬元素对水质及环境均有严重的损害作用,必须进行无害化处理。转化为重要产
品磁性铁铬氧体(CrFeO):先向含CrO的污水中加入适量的硫酸及硫酸亚铁,待充分反应
x y z
后再通入适量空气(氧化部分Fe2+)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬
氧体。
①写出CrO在酸性条件下被Fe2+还原为Cr3+的离子方程式:_________________。
②若处理含1 mol CrO(不考虑其他含铬微粒)的污水时恰好消耗10 mol FeSO ,则当铁铬氧体
4
中n(Fe2+)∶n(Fe3+)=3∶2时,铁铬氧体的化学式为________________________________。
答案 (1)①+3 ②4Fe(CrO ) +7O +8NaCO=====2Fe O +8NaCrO +8CO ③灼烧使
2 2 2 2 3 2 3 2 4 2
Cr(OH) 分解
3
(2)NaCrO Cr (SO )
2 2 4 3
(3)①3Fe2++CrO+8H+===3Fe3++Cr3++4HO ②Cr Fe O
2 2 20 27
解析 (3)②根据Fe守恒,铁铬氧体中n(Fe2+)=10 mol×=6 mol,n(Fe3+)=10 mol×=
4 mol,根据Cr守恒,铁铬氧体中n(Cr3+)=n(CrO)=1 mol,根据电荷守恒,铁铬氧体中
n(O2-)==13.5 mol,铁铬氧体中n(Cr)∶n(Fe)∶n(O)=
1 mol∶10 mol∶13.5 mol=2∶20∶27,铁铬氧体的化学式为Cr Fe O 。
2 20 27
考点三 热重分析判断金属及其化合物的组成
热重分析的一般方法和规律
(1)设晶体为1 mol,其质量为m。
(2)失重一般是先失水,再失非金属氧化物。
(3)计算每步固体剩余的质量(m )
余
×100%=固体残留率。
(4)晶体中金属质量不再减少,仍在m 中。
余
(5)失重最后一般为金属氧化物,由质量守恒得m ,由n ∶n ,即可求出失重后物质的
氧 金属 氧
化学式。
1.8.34 g FeSO ·7H O(M=278 g·mol-1)样品受热脱水过程的热重曲线(样品质量随温度变化
4 2
的曲线)如图所示,下列说法正确的是( )A.温度为78 ℃时,固体M的化学式为FeSO ·5H O
4 2
B.温度为159 ℃时,固体N的化学式为FeSO ·2H O
4 2
C.在隔绝空气条件下,由N得到P的化学方程式为FeSO ·H O=====FeSO +HO
4 2 4 2
D.取适量380 ℃时所得的样品P,隔绝空气加热至650 ℃,得到一种固体Q,同时有两种
无色气体生成,Q的化学式为Fe O
3 4
答案 C
解析 8.34 g FeSO·7H O样品的物质的量为0.03 mol,其中m(H O)=0.03 mol×7×18 g·
4 2 2
mol-1=3.78 g,如晶体全部失去结晶水,固体的质量应为8.34 g-3.78 g=4.56 g,可知在加
热到373 ℃之前,晶体失去部分结晶水,加热至635 ℃时,固体的质量为2.40 g,应为铁
的氧化物,其中n(Fe)=n(FeSO ·7H O)=0.03 mol,m(Fe)=0.03 mol×56 g·mol-1=1.68 g,
4 2
则固体中 m(O)=2.40 g-1.68 g=0.72 g,n(O)=0.045 mol ,则 n(Fe)∶n(O)=0.03
mol∶0.045 mol =2∶3,则固体Q的化学式为Fe O 。温度为78 ℃时,固体质量为 6.72
2 3
g,其中 m(FeSO )=0.03 mol ×152 g·mol-1=4.56 g,m(H O)=6.72 g-4.56 g=2.16 g,
4 2
n(H O)=0.12 mol,则 n(H O)∶n(FeSO )=0.12 mol ∶0.03 mol =4∶1,则化学式为
2 2 4
FeSO ·4H O,故A错误;温度为159 ℃时,固体质量为5.10 g,其中m(H O)=5.10 g-4.56
4 2 2
g=0.54 g,n(H O)=0.03 mol,则n(H O)∶n(FeSO )=0.03 mol∶0.03 mol=1∶1,则化学式
2 2 4
为FeSO ·H O,故B错误;N的化学式为FeSO ·H O,P的化学式为FeSO ,在隔绝空气条
4 2 4 2 4
件下由N得到P的化学方程式为FeSO ·H O=====FeSO +HO,故C正确;P的化学式为
4 2 4 2
FeSO ,Q的化学式为Fe O,铁的化合价升高,必有硫的化合价降低,即有二氧化硫生成,
4 2 3
根据原子守恒,必有SO 生成,故D错误。
3
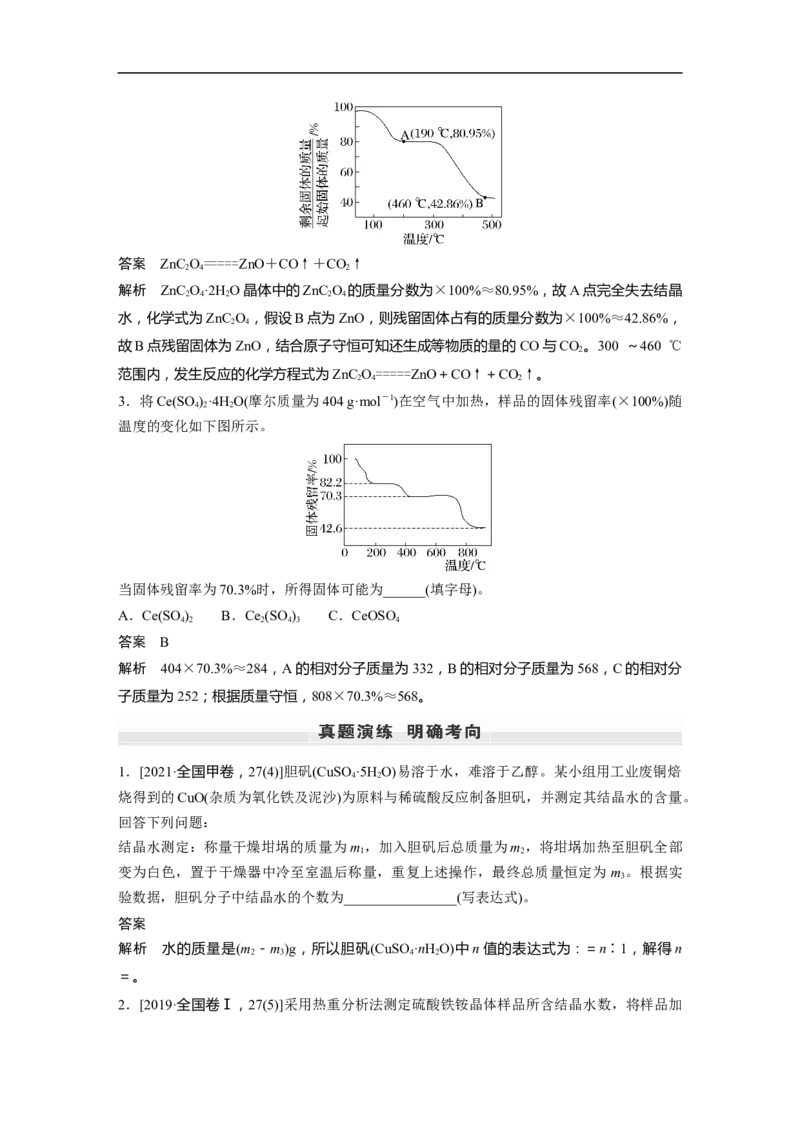
2.将草酸锌晶体(ZnC O·2H O)加热分解可得到一种纳米材料。加热过程中固体残留率随温
2 4 2
度 的 变 化 如 图 所 示 , 300 ~ 460 ℃ 范 围 内 , 发 生 反 应 的 化 学 方 程 式 为
______________________。答案 ZnC O=====ZnO+CO↑+CO↑
2 4 2
解析 ZnC O·2H O晶体中的ZnC O 的质量分数为×100%≈80.95%,故A点完全失去结晶
2 4 2 2 4
水,化学式为ZnC O ,假设B点为ZnO,则残留固体占有的质量分数为×100%≈42.86%,
2 4
故B点残留固体为ZnO,结合原子守恒可知还生成等物质的量的CO与CO 。300 ~460 ℃
2
范围内,发生反应的化学方程式为ZnC O=====ZnO+CO↑+CO↑。
2 4 2
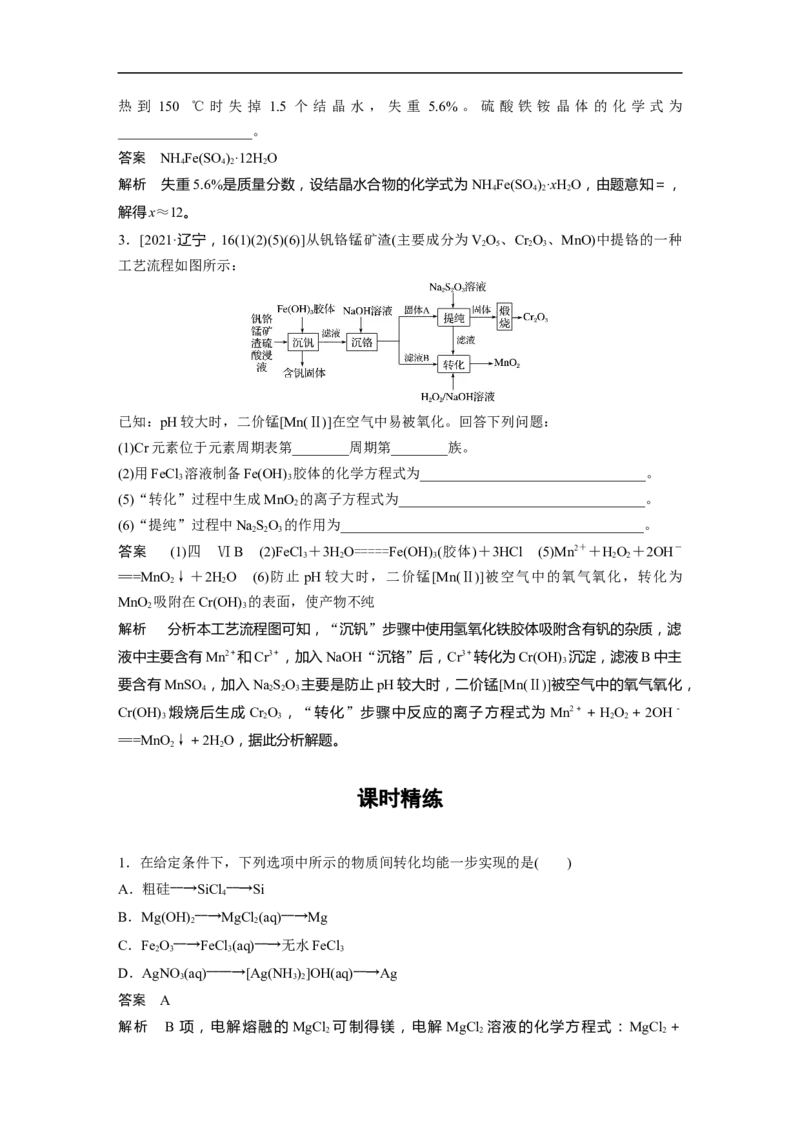
3.将Ce(SO)·4H O(摩尔质量为404 g·mol-1)在空气中加热,样品的固体残留率(×100%)随
4 2 2
温度的变化如下图所示。
当固体残留率为70.3%时,所得固体可能为______(填字母)。
A.Ce(SO) B.Ce (SO ) C.CeOSO
4 2 2 4 3 4
答案 B
解析 404×70.3%≈284,A的相对分子质量为332,B的相对分子质量为568,C的相对分
子质量为252;根据质量守恒,808×70.3%≈568。
1.[2021·全国甲卷,27(4)]胆矾(CuSO ·5H O)易溶于水,难溶于乙醇。某小组用工业废铜焙
4 2
烧得到的CuO(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。
回答下列问题:
结晶水测定:称量干燥坩埚的质量为m ,加入胆矾后总质量为m ,将坩埚加热至胆矾全部
1 2
变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为 m 。根据实
3
验数据,胆矾分子中结晶水的个数为________________(写表达式)。
答案
解析 水的质量是(m -m)g,所以胆矾(CuSO ·nHO)中n值的表达式为∶=n∶1,解得n
2 3 4 2
=。
2.[2019·全国卷Ⅰ,27(5)]采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热 到 150 ℃ 时 失 掉 1.5 个 结 晶 水 , 失 重 5.6% 。 硫 酸 铁 铵 晶 体 的 化 学 式 为
___________________。
答案 NH Fe(SO )·12H O
4 4 2 2
解析 失重5.6%是质量分数,设结晶水合物的化学式为NH Fe(SO )·xHO,由题意知=,
4 4 2 2
解得x≈12。
3.[2021·辽宁,16(1)(2)(5)(6)]从钒铬锰矿渣(主要成分为VO 、Cr O 、MnO)中提铬的一种
2 5 2 3
工艺流程如图所示:
已知:pH较大时,二价锰[Mn(Ⅱ)]在空气中易被氧化。回答下列问题:
(1)Cr元素位于元素周期表第________周期第________族。
(2)用FeCl 溶液制备Fe(OH) 胶体的化学方程式为________________________________。
3 3
(5)“转化”过程中生成MnO 的离子方程式为___________________________________。
2
(6)“提纯”过程中NaSO 的作用为___________________________________________。
2 2 3
答案 (1)四 ⅥB (2)FeCl +3HO=====Fe(OH) (胶体)+3HCl (5)Mn2++HO +2OH-
3 2 3 2 2
===MnO ↓+2HO (6)防止pH较大时,二价锰[Mn(Ⅱ)]被空气中的氧气氧化,转化为
2 2
MnO 吸附在Cr(OH) 的表面,使产物不纯
2 3
解析 分析本工艺流程图可知,“沉钒”步骤中使用氢氧化铁胶体吸附含有钒的杂质,滤
液中主要含有Mn2+和Cr3+,加入NaOH“沉铬”后,Cr3+转化为Cr(OH) 沉淀,滤液B中主
3
要含有MnSO ,加入NaSO 主要是防止pH较大时,二价锰[Mn(Ⅱ)]被空气中的氧气氧化,
4 2 2 3
Cr(OH) 煅烧后生成 Cr O ,“转化”步骤中反应的离子方程式为 Mn2++HO +2OH-
3 2 3 2 2
===MnO ↓+2HO,据此分析解题。
2 2
课时精练
1.在给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
A.粗硅――→SiCl ――→Si
4
B.Mg(OH) ――→MgCl (aq)――→Mg
2 2
C.Fe O――→FeCl (aq)――→无水FeCl
2 3 3 3
D.AgNO(aq)――――→[Ag(NH)]OH(aq)――→Ag
3 3 2
答案 A
解析 B 项,电解熔融的 MgCl 可制得镁,电解 MgCl 溶液的化学方程式:MgCl +
2 2 22HO=====Mg(OH) ↓+H↑+Cl↑,错误;C项,FeCl 溶液蒸干过程中发生反应:FeCl
2 2 2 2 3 3
+3HO=====Fe(OH) ↓+3HCl↑,错误。
2 3
2.下图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①②均为置
换反应,满足条件的物质组是( )
序号 U W Y X
① Na HO NaO NaOH
2 2 2
② Fe HO C H
2 2
③ HBr Cl CH HCl
2 4
④ CuCl (aq) Al HCl(aq) AlCl (aq)
2 3
A.②④ B.②③
C.①②④ D.①②③④
答案 A
3.对某溶液中部分离子的定性检测流程如下。相关分析正确的是( )
A.步骤①所加试剂可以是浓NaOH溶液
B.可以用湿润的蓝色石蕊试纸检验生成的无色气体
C.红褐色沉淀与HI反应的离子方程式为Fe(OH) +3H+===Fe3++3HO
3 2
D.步骤②的反应为Al3++3HCO===Al(OH) ↓+CO↑
3 2
答案 A
解析 无色气体为氨气,红褐色沉淀为氢氧化铁,X溶液为偏铝酸钠溶液,所以步骤①所加
试剂可以是浓NaOH溶液,故A正确;应该用湿润的红色石蕊试纸检验氨气,故 B错误;
Fe3+可以氧化I-生成I,故C错误;步骤②的反应为AlO+HCO+HO===CO+Al(OH) ↓,
2 2 3
故D错误。
4.某废催化剂含SiO 、ZnS、CuS及少量的Fe O 。某实验小组以废催化剂为原料,进行回
2 3 4
收利用。设计实验流程如图:已知:CuS既不溶于稀硫酸,也不与稀硫酸反应。下列说法正确的是( )
A.步骤①操作中,生成的气体可用碱液吸收
B.滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水检验
C.滤渣1成分是SiO 和CuS,滤渣2成分一定是SiO
2 2
D.步骤④要滴加稀硫酸防止CuSO 水解
4
答案 A
解析 由题给流程可知,向废催化剂中加入稀硫酸,硫化锌和四氧化三铁与稀硫酸反应得到
硫酸锌、硫酸铁和硫酸亚铁的混合溶液,二氧化硅和硫化铜不与稀硫酸反应,过滤得到含有
硫酸锌、硫酸铁和硫酸亚铁的滤液1和含有二氧化硅和硫化铜的滤渣1;滤液1经蒸发浓缩、
冷却结晶、过滤得到含有杂质的粗皓矾;向滤渣1中加入稀硫酸和过氧化氢的混合溶液,酸
性条件下,硫化铜与过氧化氢反应生成硫酸铜、硫沉淀和水,过滤得到含有硫酸铜的滤液 2
和含有硫和二氧化硅的滤渣2;滤液2经蒸发浓缩、冷却结晶、过滤得到粗蓝矾。
5.碱式碳酸铝镁[Mg Al (OH)(CO)·xHO]常用作塑料阻燃剂。为确定碱式碳酸铝镁的组成,
a b c 3 d 2
进行如下实验:
①准确称取3.390 g样品与足量稀盐酸充分反应,生成0.560 L CO(已换算成标准状况下)。
2
②另取一定量样品在空气中加热,样品的固体残留率(×100%)随温度的变化如图所示(样品
在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO)=________。
答案 3∶5
解析 碱式碳酸铝镁的化学式不确定,题中只表示为MgAl (OH)(CO)·xHO,无法求得摩
a b c 3 d 2
尔质量。试题中以3.390 g样品为研究对象,不妨暂定3.390 g样品为1 mol。3.390 g样品与
足 量 的 稀 盐 酸 充 分 反 应 , 生 成 CO 体 积 为 0.560 L( 标 准 状 况 ) 。 n(CO) = =
2 2
0.025 mol,根据C元素守恒,即可确定d为0.025。270 ℃时已完全失去结晶水,失去结晶水的质量为3.390 g×(1-73.45%)≈0.9 g,600 ℃以上残留固体为金属氧化物的混合物,说明
又失去了除结晶水外的氢元素。失去的氢元素只能再结合样品中的氧元素生成水。600 ℃时
失重的质量为 3.390 g×(1-37.02%)≈2.135 g,失去氢元素再生成水的质量为 2.135 g-
(0.025 mol
×44 g·mol-1)-0.9 g=0.135 g。n(H)=×2=0.015 mol,根据氢元素守恒,c=0.015。故碱式
碳酸铝镁样品中的n(OH-)∶n(CO)=0.015∶0.025=3∶5。
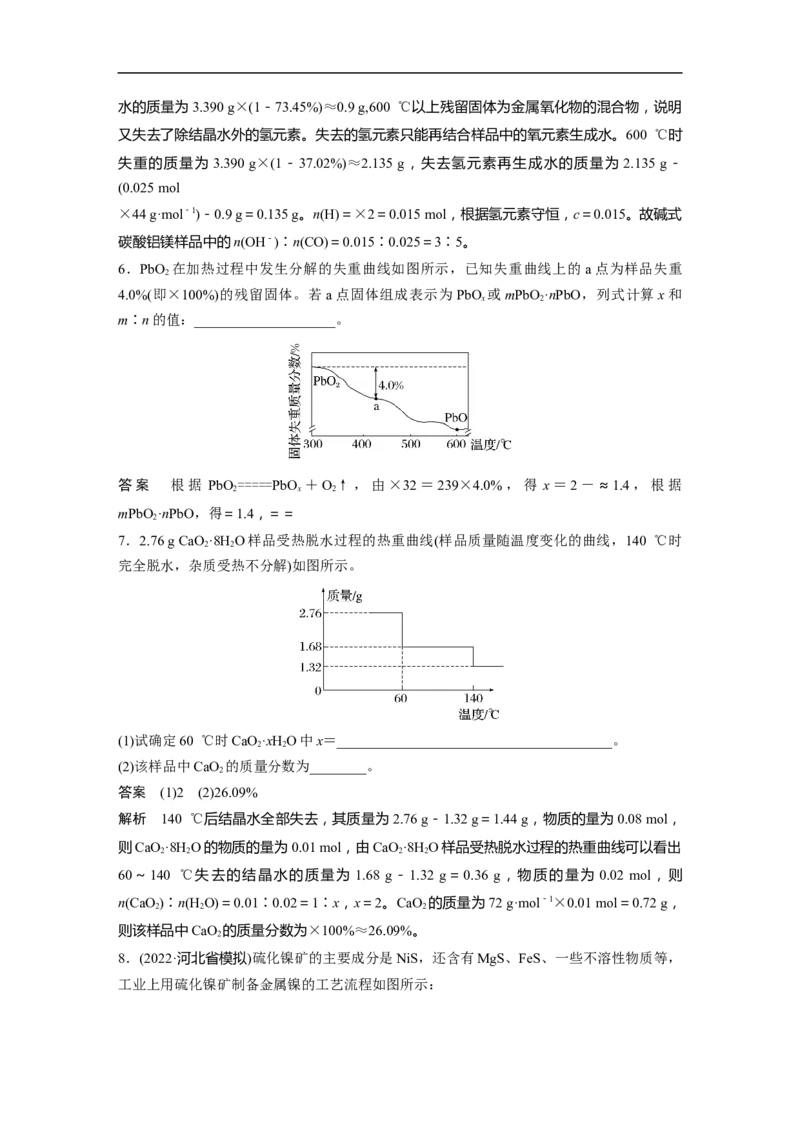
6.PbO 在加热过程中发生分解的失重曲线如图所示,已知失重曲线上的 a点为样品失重
2
4.0%(即×100%)的残留固体。若a点固体组成表示为PbO 或mPbO ·nPbO,列式计算x和
x 2
m∶n的值:____________________。
答案 根据 PbO =====PbO +O↑,由×32=239×4.0%,得 x=2-≈1.4,根据
2 x 2
mPbO ·nPbO,得=1.4,==
2
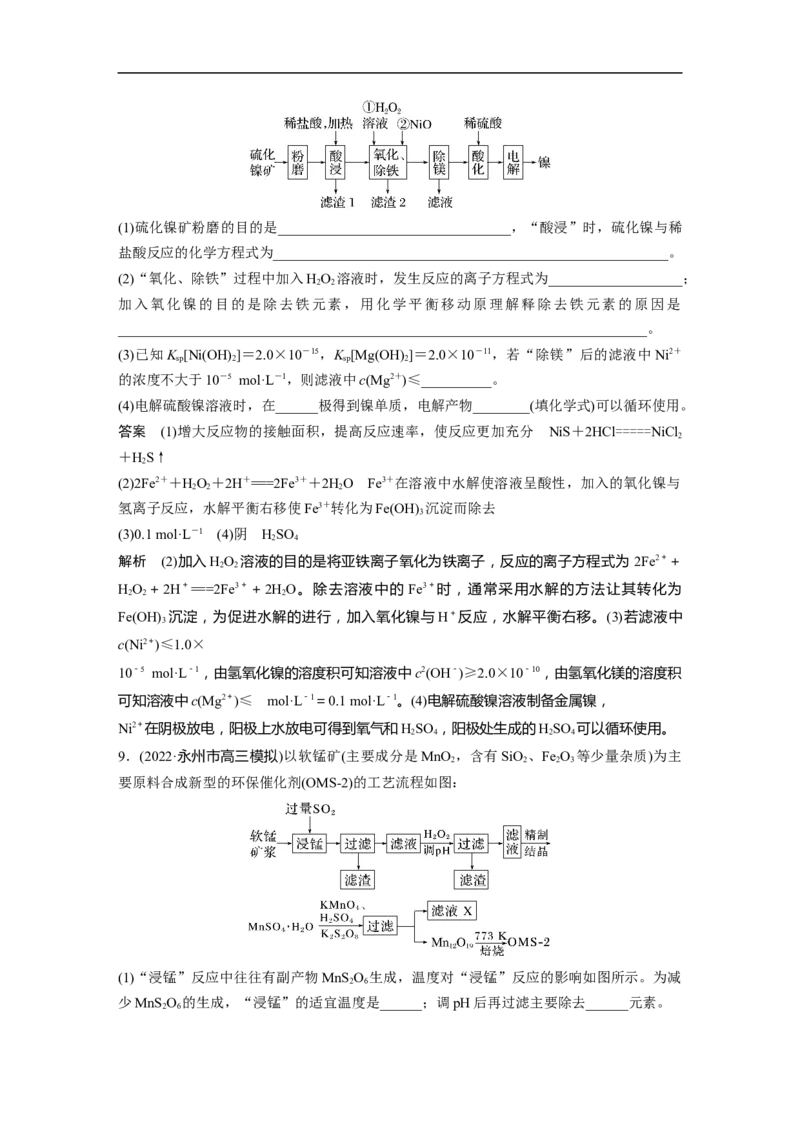
7.2.76 g CaO ·8H O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140 ℃时
2 2
完全脱水,杂质受热不分解)如图所示。
(1)试确定60 ℃时CaO·xHO中x=_______________________________________。
2 2
(2)该样品中CaO 的质量分数为________。
2
答案 (1)2 (2)26.09%
解析 140 ℃后结晶水全部失去,其质量为2.76 g-1.32 g=1.44 g,物质的量为0.08 mol,
则CaO·8H O的物质的量为0.01 mol,由CaO·8H O样品受热脱水过程的热重曲线可以看出
2 2 2 2
60~140 ℃失去的结晶水的质量为 1.68 g-1.32 g=0.36 g,物质的量为 0.02 mol,则
n(CaO)∶n(H O)=0.01∶0.02=1∶x,x=2。CaO 的质量为72 g·mol-1×0.01 mol=0.72 g,
2 2 2
则该样品中CaO 的质量分数为×100%≈26.09%。
2
8.(2022·河北省模拟)硫化镍矿的主要成分是NiS,还含有MgS、FeS、一些不溶性物质等,
工业上用硫化镍矿制备金属镍的工艺流程如图所示:(1)硫化镍矿粉磨的目的是_________________________________,“酸浸”时,硫化镍与稀
盐酸反应的化学方程式为________________________________________________________。
(2)“氧化、除铁”过程中加入HO 溶液时,发生反应的离子方程式为___________________;
2 2
加入氧化镍的目的是除去铁元素,用化学平衡移动原理解释除去铁元素的原因是
___________________________________________________________________________。
(3)已知K [Ni(OH) ]=2.0×10-15,K [Mg(OH) ]=2.0×10-11,若“除镁”后的滤液中Ni2+
sp 2 sp 2
的浓度不大于10-5 mol·L-1,则滤液中c(Mg2+)≤__________。
(4)电解硫酸镍溶液时,在______极得到镍单质,电解产物________(填化学式)可以循环使用。
答案 (1)增大反应物的接触面积,提高反应速率,使反应更加充分 NiS+2HCl=====NiCl
2
+HS↑
2
(2)2Fe2++HO +2H+===2Fe3++2HO Fe3+在溶液中水解使溶液呈酸性,加入的氧化镍与
2 2 2
氢离子反应,水解平衡右移使Fe3+转化为Fe(OH) 沉淀而除去
3
(3)0.1 mol·L-1 (4)阴 HSO
2 4
解析 (2)加入HO 溶液的目的是将亚铁离子氧化为铁离子,反应的离子方程式为 2Fe2++
2 2
HO +2H+===2Fe3++2HO。除去溶液中的 Fe3+时,通常采用水解的方法让其转化为
2 2 2
Fe(OH) 沉淀,为促进水解的进行,加入氧化镍与H+反应,水解平衡右移。(3)若滤液中
3
c(Ni2+)≤1.0×
10-5 mol·L-1,由氢氧化镍的溶度积可知溶液中c2(OH-)≥2.0×10-10,由氢氧化镁的溶度积
可知溶液中c(Mg2+)≤ mol·L-1=0.1 mol·L-1。(4)电解硫酸镍溶液制备金属镍,
Ni2+在阴极放电,阳极上水放电可得到氧气和HSO ,阳极处生成的HSO 可以循环使用。
2 4 2 4
9.(2022·永州市高三模拟)以软锰矿(主要成分是MnO ,含有SiO 、Fe O 等少量杂质)为主
2 2 2 3
要原料合成新型的环保催化剂(OMS-2)的工艺流程如图:
(1)“浸锰”反应中往往有副产物MnS O 生成,温度对“浸锰”反应的影响如图所示。为减
2 6
少MnS O 的生成,“浸锰”的适宜温度是______;调pH后再过滤主要除去______元素。
2 6(2)Mn O 中氧元素化合价均为-2价,锰元素的化合价有两种,则Mn(Ⅲ)、Mn(Ⅳ)物质的
12 19
量之比为______。生产过程中KMnO 、MnSO ·HO按物质的量之比1∶5与KSO 反应,
4 4 2 2 2 8
产物中硫元素全部以SO的形式存在,该反应的离子方程式为___________________。
(3)滤液X可进一步分离出多种化合物,其一为盐类,该盐在农业生产中可用作______。
(4)甲醛(HCHO)在OMS-2催化氧化作用下生成CO 和HO,现利用OMS-2对某密闭空间的
2 2
甲醛进行催化氧化实验。实验开始时,该空间内甲醛含量为 1.22 mg·L-1,CO 含量为0.59
2
mg·
L-1,一段时间后测得 CO 含量升高至 1.47 mg·L-1,该实验中甲醛的转化率为
2
__________(保留三位有效数字)。
答案 (1)90 ℃ Fe (2)5∶1 2MnO+2SO+10Mn2++11HO===Mn O ↓+4SO+22H+
2 2 12 19
(3)钾肥 (4)49.2%
解析 (2)Mn O 中氧元素化合价均为-2价,设Mn (Ⅲ)为x个,则Mn (Ⅳ)为12-x个,根
12 19
据化合物中元素化合价代数和为0,即得3x+4(12-x)=2×19,x=10,Mn (Ⅳ)为2个,Mn
(Ⅲ)、Mn (Ⅳ) 物质的量之比为5∶1;根据题意生产过程中的原料KMnO 、MnSO ·H O按
4 4 2
物质的量比1∶5反应,产物中硫元素全部以SO的形式存在,该反应的离子方程式为2MnO
+2SO+10Mn2++11HO===Mn O ↓+4SO+22H+。
2 2 12 19
(4)设体积为V L,CO 含量由0.59 mg·L-1升高至1.47 mg·L-1,CO 含量增多0.88 mg·L-1,
2 2
反应生成的CO 的物质的量为×V L×10-3 g·mg-1=2V×10-5 mol,根据原子个数守恒,
2
参与反应的甲醛的物质的量为 2V×10-5 mol,故该实验中甲醛的转化率为
×100%≈49.2%。
10.(2022·河北模拟)钴酸锂电池的正极材料含有钴酸锂(LiCoO )、导电剂乙炔黑、铝箔及少
2
量铁,通过如图工艺流程可回收铝、钴、锂。
回答下列问题:(1)钴酸锂电池放电时负极反应式为LiC -xe-===C +xLi+,拆解废旧电池前进行放电处理,
x 6 6
既可保证安全又有利于回收锂。有利于回收锂的原因是_______________________。
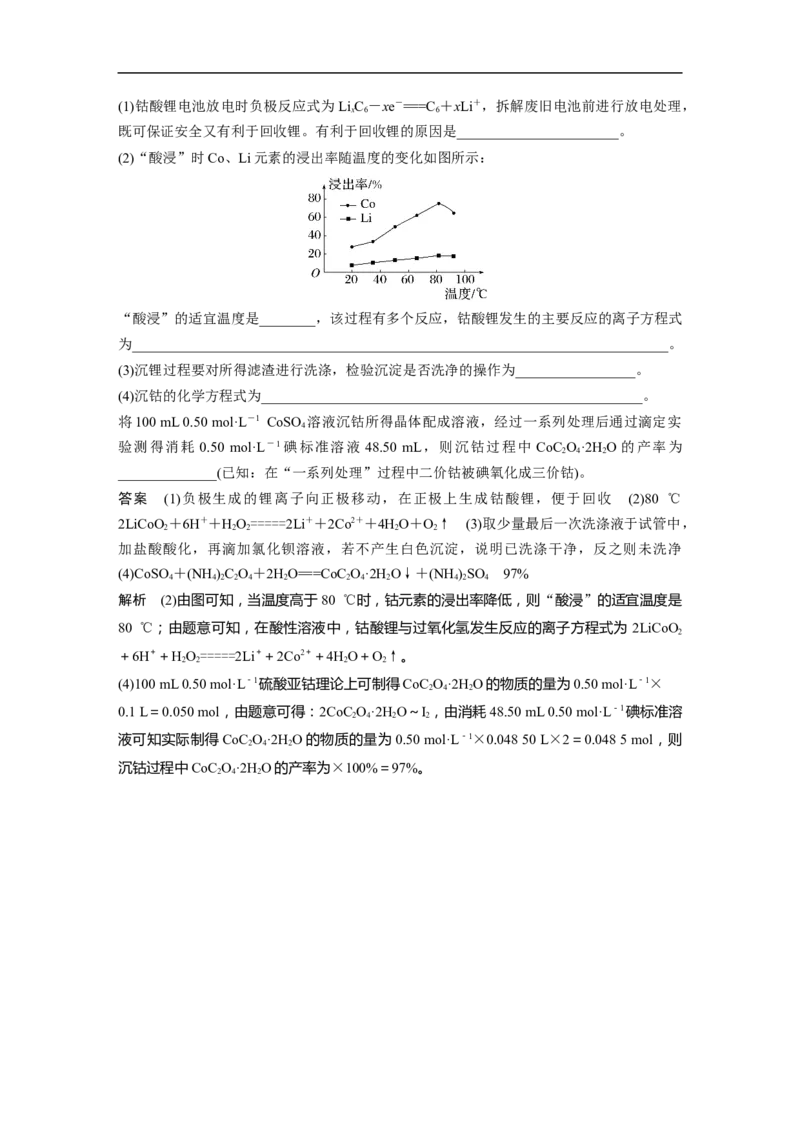
(2)“酸浸”时Co、Li元素的浸出率随温度的变化如图所示:
“酸浸”的适宜温度是________,该过程有多个反应,钴酸锂发生的主要反应的离子方程式
为____________________________________________________________________________。
(3)沉锂过程要对所得滤渣进行洗涤,检验沉淀是否洗净的操作为_________________。
(4)沉钴的化学方程式为______________________________________________________。
将100 mL 0.50 mol·L-1 CoSO 溶液沉钴所得晶体配成溶液,经过一系列处理后通过滴定实
4
验测得消耗 0.50 mol·L-1碘标准溶液 48.50 mL,则沉钴过程中 CoC O·2H O 的产率为
2 4 2
______________(已知:在“一系列处理”过程中二价钴被碘氧化成三价钴)。
答案 (1)负极生成的锂离子向正极移动,在正极上生成钴酸锂,便于回收 (2)80 ℃
2LiCoO +6H++HO=====2Li++2Co2++4HO+O↑ (3)取少量最后一次洗涤液于试管中,
2 2 2 2 2
加盐酸酸化,再滴加氯化钡溶液,若不产生白色沉淀,说明已洗涤干净,反之则未洗净
(4)CoSO +(NH )C O+2HO===CoC O·2H O↓+(NH )SO 97%
4 4 2 2 4 2 2 4 2 4 2 4
解析 (2)由图可知,当温度高于80 ℃时,钴元素的浸出率降低,则“酸浸”的适宜温度是
80 ℃;由题意可知,在酸性溶液中,钴酸锂与过氧化氢发生反应的离子方程式为 2LiCoO
2
+6H++HO=====2Li++2Co2++4HO+O↑。
2 2 2 2
(4)100 mL 0.50 mol·L-1硫酸亚钴理论上可制得CoC O·2H O的物质的量为0.50 mol·L-1×
2 4 2
0.1 L=0.050 mol,由题意可得:2CoC O·2H O~I ,由消耗48.50 mL 0.50 mol·L-1碘标准溶
2 4 2 2
液可知实际制得CoC O·2H O的物质的量为0.50 mol·L-1×0.048 50 L×2=0.048 5 mol,则
2 4 2
沉钴过程中CoC O·2H O的产率为×100%=97%。
2 4 2