文档内容
专项特训 2 非金属及其化合物对环境的影响
1.我国计划在2030年实现“碳达峰”,体现了对解决全球环境问题的大国担当。下列说法
正确的是( )
A.利用火力发电,减少CO 的排放
2
B.燃煤中加入CaO减少CO 气体的排放
2
C.采取节能低碳生活方式,禁止使用化石燃料
D.用CO 合成聚碳酸酯可降解塑料,实现CO 的资源化利用
2 2
答案 D
解析 利用火力发电,会增加煤炭的燃烧,不利于减少 CO 的排放,故A错误;CaO和
2
CO 高温下几乎不反应,因此燃煤中加入CaO不能减少CO 气体的排放,故B错误;采取
2 2
节能低碳生活方式,不能禁止使用化石燃料,只能尽量使用新能源代替化石燃料,故C错
误。
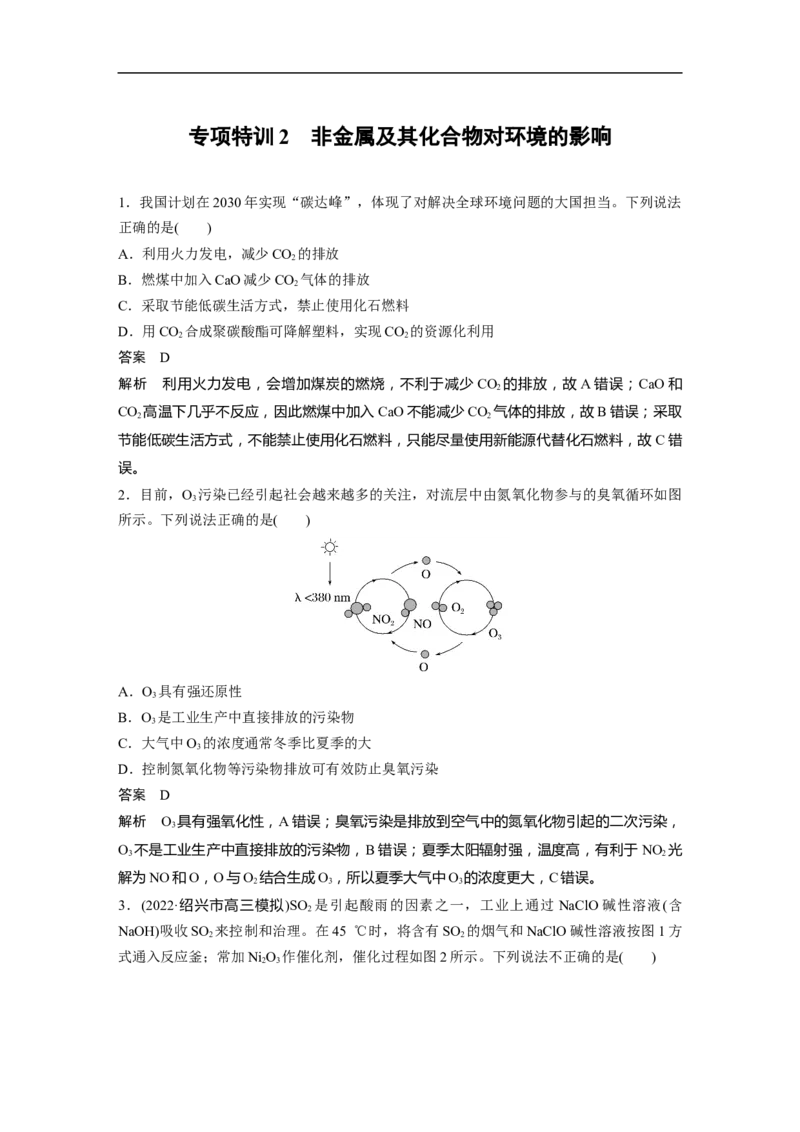
2.目前,O 污染已经引起社会越来越多的关注,对流层中由氮氧化物参与的臭氧循环如图
3
所示。下列说法正确的是( )
A.O 具有强还原性
3
B.O 是工业生产中直接排放的污染物
3
C.大气中O 的浓度通常冬季比夏季的大
3
D.控制氮氧化物等污染物排放可有效防止臭氧污染
答案 D
解析 O 具有强氧化性,A错误;臭氧污染是排放到空气中的氮氧化物引起的二次污染,
3
O 不是工业生产中直接排放的污染物,B错误;夏季太阳辐射强,温度高,有利于NO 光
3 2
解为NO和O,O与O 结合生成O,所以夏季大气中O 的浓度更大,C错误。
2 3 3
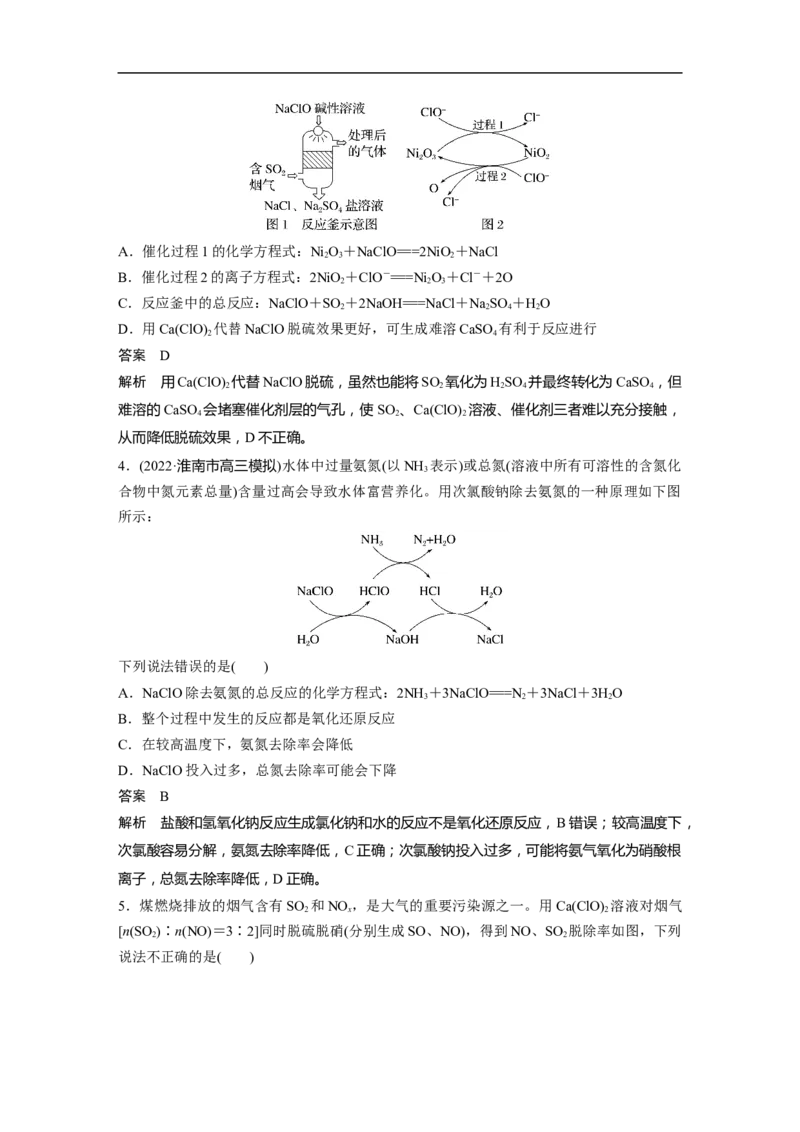
3.(2022·绍兴市高三模拟)SO 是引起酸雨的因素之一,工业上通过 NaClO碱性溶液(含
2
NaOH)吸收SO 来控制和治理。在45 ℃时,将含有SO 的烟气和NaClO碱性溶液按图1方
2 2
式通入反应釜;常加Ni O 作催化剂,催化过程如图2所示。下列说法不正确的是( )
2 3A.催化过程1的化学方程式:Ni O+NaClO===2NiO+NaCl
2 3 2
B.催化过程2的离子方程式:2NiO+ClO-===Ni O+Cl-+2O
2 2 3
C.反应釜中的总反应:NaClO+SO +2NaOH===NaCl+NaSO +HO
2 2 4 2
D.用Ca(ClO) 代替NaClO脱硫效果更好,可生成难溶CaSO 有利于反应进行
2 4
答案 D
解析 用Ca(ClO) 代替NaClO脱硫,虽然也能将SO 氧化为HSO 并最终转化为CaSO,但
2 2 2 4 4
难溶的CaSO 会堵塞催化剂层的气孔,使SO 、Ca(ClO) 溶液、催化剂三者难以充分接触,
4 2 2
从而降低脱硫效果,D不正确。
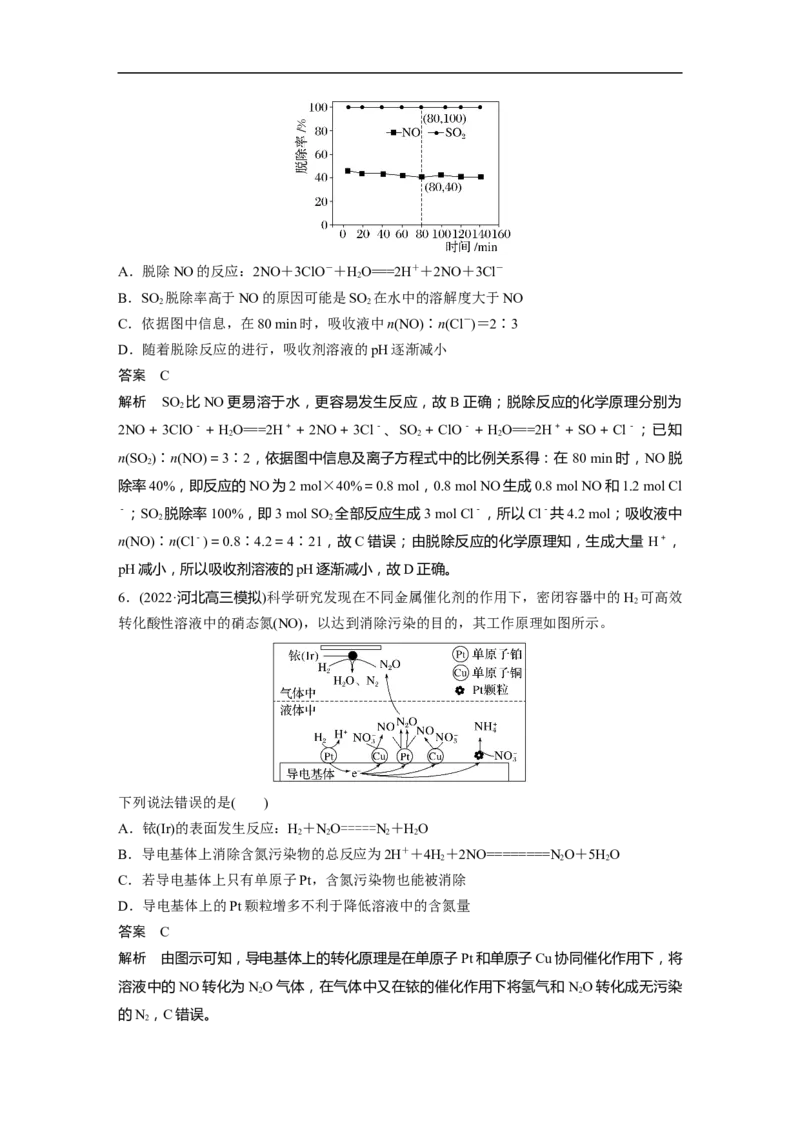
4.(2022·淮南市高三模拟)水体中过量氨氮(以NH 表示)或总氮(溶液中所有可溶性的含氮化
3
合物中氮元素总量)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如下图
所示:
下列说法错误的是( )
A.NaClO除去氨氮的总反应的化学方程式:2NH +3NaClO===N+3NaCl+3HO
3 2 2
B.整个过程中发生的反应都是氧化还原反应
C.在较高温度下,氨氮去除率会降低
D.NaClO投入过多,总氮去除率可能会下降
答案 B
解析 盐酸和氢氧化钠反应生成氯化钠和水的反应不是氧化还原反应,B错误;较高温度下,
次氯酸容易分解,氨氮去除率降低,C正确;次氯酸钠投入过多,可能将氨气氧化为硝酸根
离子,总氮去除率降低,D正确。
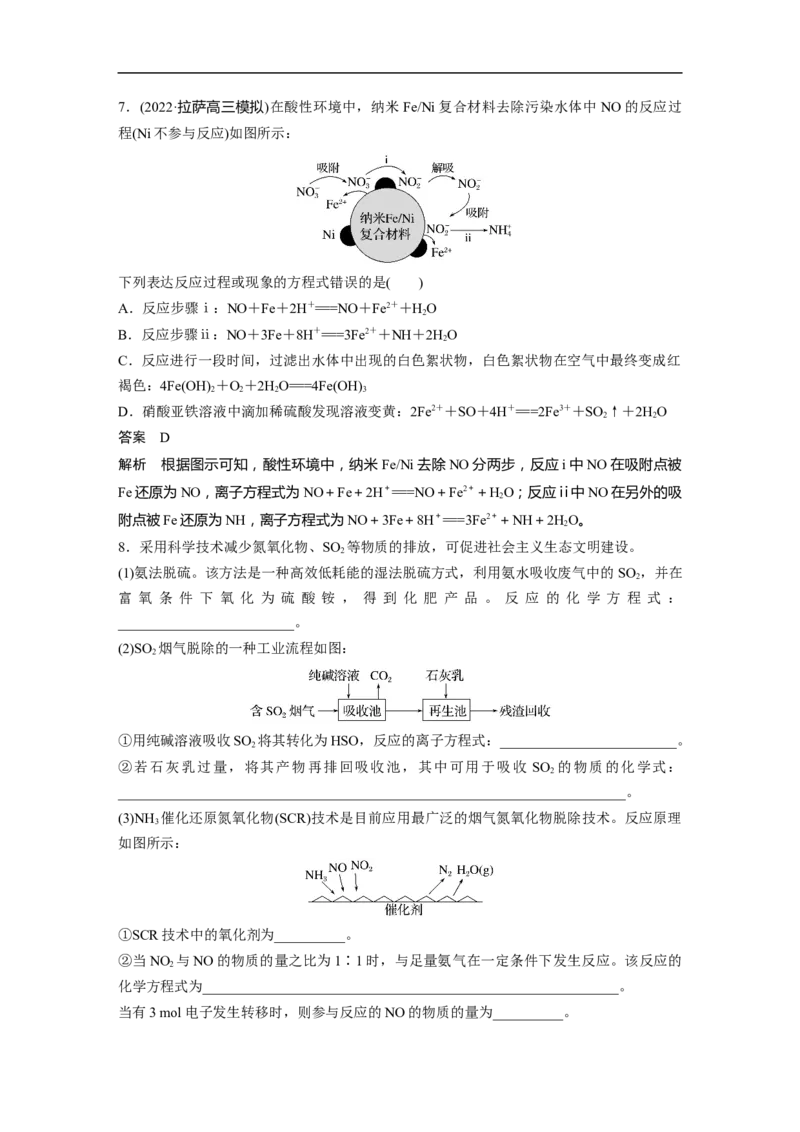
5.煤燃烧排放的烟气含有SO 和NO,是大气的重要污染源之一。用Ca(ClO) 溶液对烟气
2 x 2
[n(SO )∶n(NO)=3∶2]同时脱硫脱硝(分别生成SO、NO),得到NO、SO 脱除率如图,下列
2 2
说法不正确的是( )A.脱除NO的反应:2NO+3ClO-+HO===2H++2NO+3Cl-
2
B.SO 脱除率高于NO的原因可能是SO 在水中的溶解度大于NO
2 2
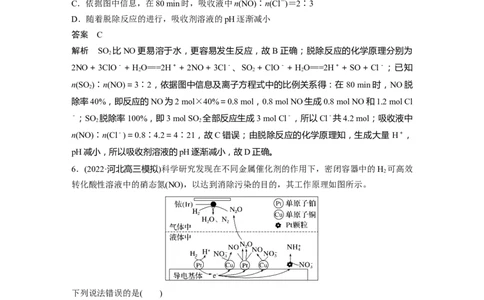
C.依据图中信息,在80 min时,吸收液中n(NO)∶n(Cl-)=2∶3
D.随着脱除反应的进行,吸收剂溶液的pH逐渐减小
答案 C
解析 SO 比NO更易溶于水,更容易发生反应,故B正确;脱除反应的化学原理分别为
2
2NO+3ClO-+HO===2H++2NO+3Cl-、SO +ClO-+HO===2H++SO+Cl-;已知
2 2 2
n(SO )∶n(NO)=3∶2,依据图中信息及离子方程式中的比例关系得:在 80 min时,NO脱
2
除率40%,即反应的NO为2 mol×40%=0.8 mol,0.8 mol NO生成0.8 mol NO和1.2 mol Cl
-;SO 脱除率100%,即3 mol SO 全部反应生成3 mol Cl-,所以Cl-共4.2 mol;吸收液中
2 2
n(NO)∶n(Cl-)=0.8∶4.2=4∶21,故C错误;由脱除反应的化学原理知,生成大量 H+,
pH减小,所以吸收剂溶液的pH逐渐减小,故D正确。
6.(2022·河北高三模拟)科学研究发现在不同金属催化剂的作用下,密闭容器中的H 可高效
2
转化酸性溶液中的硝态氮(NO),以达到消除污染的目的,其工作原理如图所示。
下列说法错误的是( )
A.铱(Ir)的表面发生反应:H+NO=====N+HO
2 2 2 2
B.导电基体上消除含氮污染物的总反应为2H++4H+2NO========NO+5HO
2 2 2
C.若导电基体上只有单原子Pt,含氮污染物也能被消除
D.导电基体上的Pt颗粒增多不利于降低溶液中的含氮量
答案 C
解析 由图示可知,导电基体上的转化原理是在单原子Pt和单原子Cu协同催化作用下,将
溶液中的NO转化为NO气体,在气体中又在铱的催化作用下将氢气和NO转化成无污染
2 2
的N,C错误。
27.(2022·拉萨高三模拟)在酸性环境中,纳米Fe/Ni复合材料去除污染水体中NO的反应过
程(Ni不参与反应)如图所示:
下列表达反应过程或现象的方程式错误的是( )
A.反应步骤ⅰ:NO+Fe+2H+===NO+Fe2++HO
2
B.反应步骤ⅱ:NO+3Fe+8H+===3Fe2++NH+2HO
2
C.反应进行一段时间,过滤出水体中出现的白色絮状物,白色絮状物在空气中最终变成红
褐色:4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
D.硝酸亚铁溶液中滴加稀硫酸发现溶液变黄:2Fe2++SO+4H+===2Fe3++SO ↑+2HO
2 2
答案 D
解析 根据图示可知,酸性环境中,纳米 Fe/Ni去除NO分两步,反应i中NO在吸附点被
Fe还原为NO,离子方程式为NO+Fe+2H+===NO+Fe2++HO;反应ⅱ中NO在另外的吸
2
附点被Fe还原为NH,离子方程式为NO+3Fe+8H+===3Fe2++NH+2HO。
2
8.采用科学技术减少氮氧化物、SO 等物质的排放,可促进社会主义生态文明建设。
2
(1)氨法脱硫。该方法是一种高效低耗能的湿法脱硫方式,利用氨水吸收废气中的SO ,并在
2
富 氧 条 件 下 氧 化 为 硫 酸 铵 , 得 到 化 肥 产 品 。 反 应 的 化 学 方 程 式 :
_________________________。
(2)SO 烟气脱除的一种工业流程如图:
2
①用纯碱溶液吸收SO 将其转化为HSO,反应的离子方程式:_________________________。
2
②若石灰乳过量,将其产物再排回吸收池,其中可用于吸收 SO 的物质的化学式:
2
________________________________________________________________________。
(3)NH 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理
3
如图所示:
①SCR技术中的氧化剂为__________。
②当NO 与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应。该反应的
2
化学方程式为___________________________________________________________。
当有3 mol电子发生转移时,则参与反应的NO的物质的量为__________。答案 (1)4NH ·H O+2SO +O===2(NH )SO +2HO (2)①HO+2SO +CO===2HSO+
3 2 2 2 4 2 4 2 2 2
CO ②Ca(OH) (3)①NO、NO
2 2 2
②2NH +NO+NO ===2N+3HO(g) 0.5 mol
3 2 2 2
解析 (3)②当NO 与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生反应生
2
成氮气和水蒸气,该反应的化学方程式为2NH +NO+NO ===2N +3HO(g)。根据方程式
3 2 2 2
可知消耗1 mol NO,转移6 mol电子,则当有3 mol电子发生转移时,则参与反应的NO的
物质的量为0.5 mol。