文档内容
(三)化学反应原理
1.环己烷和苯均是重要的化工原料,对环己烷—苯系统的研究既有生产实际价值,也具有
理论意义。回答下列问题。
(1)环己烷脱氢生苯的热效应研究
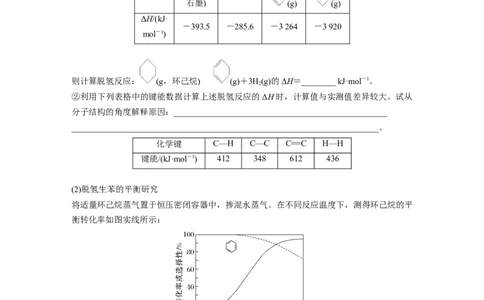
①已知下列物质的燃烧热数据如下:
C(s,
物质 H(g)
2
石墨) (g) (g)
ΔH/(kJ·
-393.5 -285.6 -3 264 -3 920
mol-1)
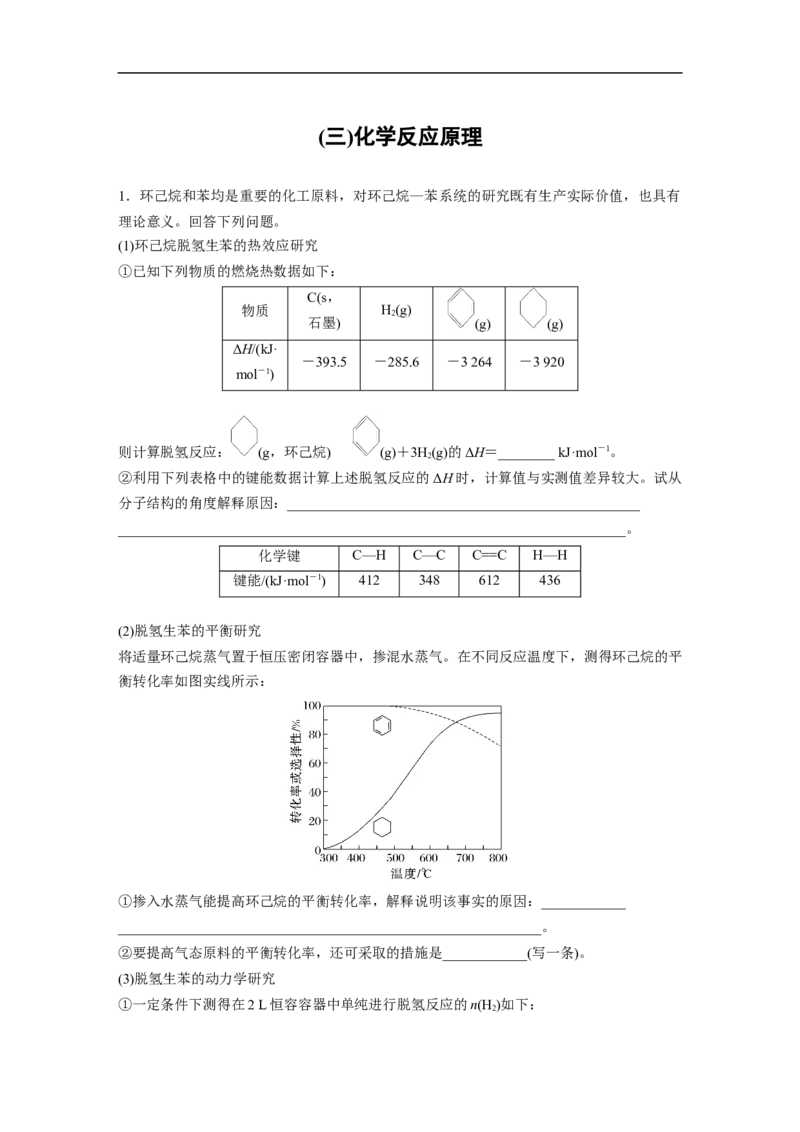
则计算脱氢反应: (g,环己烷) (g)+3H(g)的ΔH=________ kJ·mol-1。
2
②利用下列表格中的键能数据计算上述脱氢反应的ΔH时,计算值与实测值差异较大。试从
分子结构的角度解释原因:__________________________________________________
________________________________________________________________________。
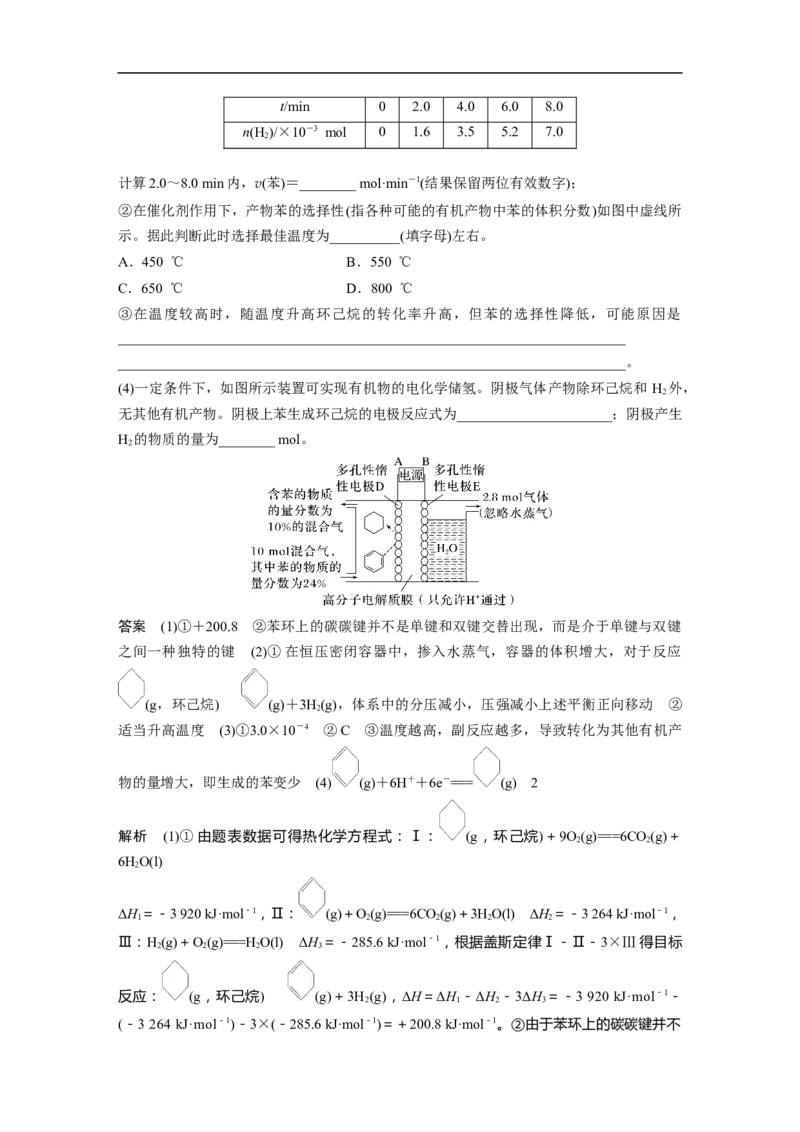
化学键 C—H C—C C==C H—H
键能/(kJ·mol-1) 412 348 612 436
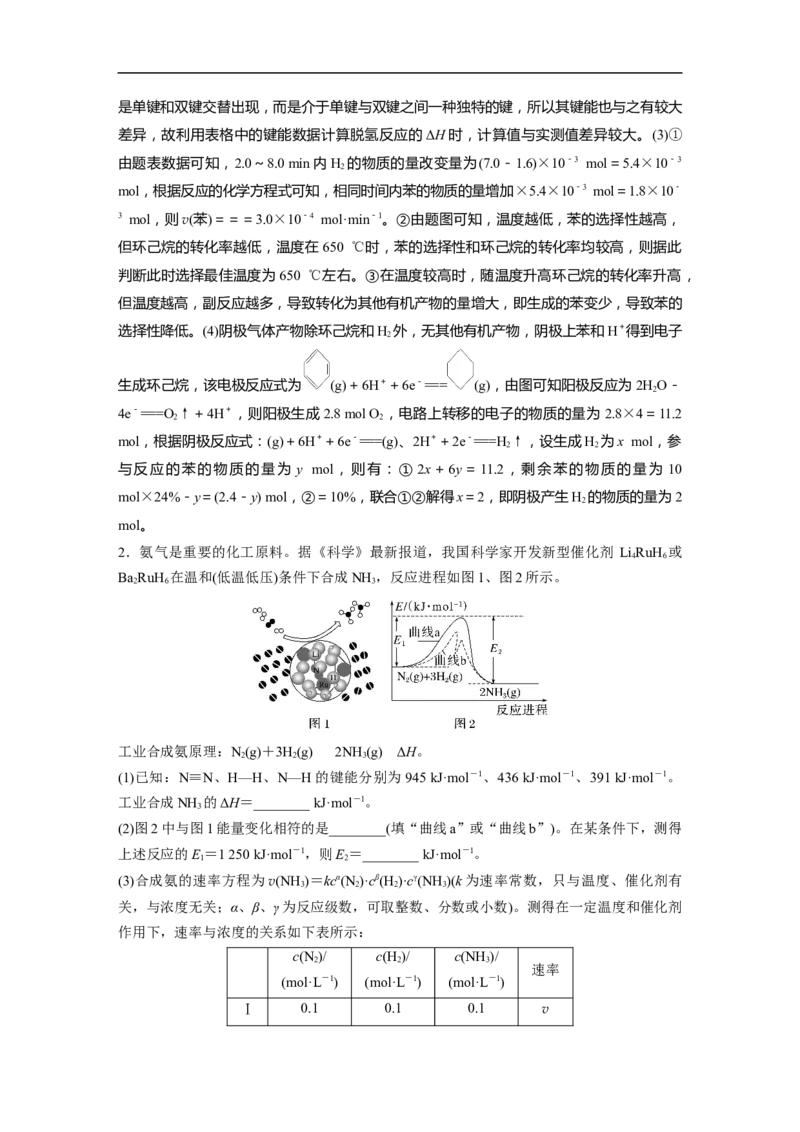
(2)脱氢生苯的平衡研究
将适量环己烷蒸气置于恒压密闭容器中,掺混水蒸气。在不同反应温度下,测得环己烷的平
衡转化率如图实线所示:
①掺入水蒸气能提高环己烷的平衡转化率,解释说明该事实的原因:____________
____________________________________________________________。
②要提高气态原料的平衡转化率,还可采取的措施是____________(写一条)。
(3)脱氢生苯的动力学研究
①一定条件下测得在2 L恒容容器中单纯进行脱氢反应的n(H )如下:
2t/min 0 2.0 4.0 6.0 8.0
n(H )/×10-3 mol 0 1.6 3.5 5.2 7.0
2
计算2.0~8.0 min内,v(苯)=________ mol·min-1(结果保留两位有效数字);
②在催化剂作用下,产物苯的选择性(指各种可能的有机产物中苯的体积分数)如图中虚线所
示。据此判断此时选择最佳温度为__________(填字母)左右。
A.450 ℃ B.550 ℃
C.650 ℃ D.800 ℃
③在温度较高时,随温度升高环己烷的转化率升高,但苯的选择性降低,可能原因是
________________________________________________________________________
________________________________________________________________________。
(4)一定条件下,如图所示装置可实现有机物的电化学储氢。阴极气体产物除环己烷和 H 外,
2
无其他有机产物。阴极上苯生成环己烷的电极反应式为______________________;阴极产生
H 的物质的量为________ mol。
2
答案 (1)①+200.8 ②苯环上的碳碳键并不是单键和双键交替出现,而是介于单键与双键
之间一种独特的键 (2)①在恒压密闭容器中,掺入水蒸气,容器的体积增大,对于反应
(g,环己烷) (g)+3H(g),体系中的分压减小,压强减小上述平衡正向移动 ②
2
适当升高温度 (3)①3.0×10-4 ②C ③温度越高,副反应越多,导致转化为其他有机产
物的量增大,即生成的苯变少 (4) (g)+6H++6e-=== (g) 2
解析 (1)①由题表数据可得热化学方程式:Ⅰ: (g,环己烷)+9O(g)===6CO(g)+
2 2
6HO(l)
2
ΔH=-3 920 kJ·mol-1,Ⅱ: (g)+O(g)===6CO(g)+3HO(l) ΔH=-3 264 kJ·mol-1,
1 2 2 2 2
Ⅲ:H(g)+O(g)===HO(l) ΔH =-285.6 kJ·mol-1,根据盖斯定律Ⅰ-Ⅱ-3×Ⅲ得目标
2 2 2 3
反应: (g,环己烷) (g)+3H (g),ΔH=ΔH -ΔH -3ΔH =-3 920 kJ·mol-1-
2 1 2 3
(-3 264 kJ·mol-1)-3×(-285.6 kJ·mol-1)=+200.8 kJ·mol-1。②由于苯环上的碳碳键并不是单键和双键交替出现,而是介于单键与双键之间一种独特的键,所以其键能也与之有较大
差异,故利用表格中的键能数据计算脱氢反应的ΔH时,计算值与实测值差异较大。(3)①
由题表数据可知,2.0~8.0 min内H 的物质的量改变量为(7.0-1.6)×10-3 mol=5.4×10-3
2
mol,根据反应的化学方程式可知,相同时间内苯的物质的量增加×5.4×10-3 mol=1.8×10-
3 mol,则v(苯)===3.0×10-4 mol·min-1。②由题图可知,温度越低,苯的选择性越高,
但环己烷的转化率越低,温度在650 ℃时,苯的选择性和环己烷的转化率均较高,则据此
判断此时选择最佳温度为650 ℃左右。③在温度较高时,随温度升高环己烷的转化率升高,
但温度越高,副反应越多,导致转化为其他有机产物的量增大,即生成的苯变少,导致苯的
选择性降低。(4)阴极气体产物除环己烷和H 外,无其他有机产物,阴极上苯和H+得到电子
2
生成环己烷,该电极反应式为 (g)+6H++6e-=== (g),由图可知阳极反应为2HO-
2
4e-===O↑+4H+,则阳极生成2.8 mol O ,电路上转移的电子的物质的量为 2.8×4=11.2
2 2
mol,根据阴极反应式:(g)+6H++6e-===(g)、2H++2e-===H↑,设生成H 为x mol,参
2 2
与反应的苯的物质的量为 y mol,则有:① 2x+6y=11.2,剩余苯的物质的量为 10
mol×24%-y=(2.4-y) mol,②=10%,联合①②解得x=2,即阴极产生H 的物质的量为2
2
mol。
2.氨气是重要的化工原料。据《科学》最新报道,我国科学家开发新型催化剂 LiRuH 或
4 6
Ba RuH 在温和(低温低压)条件下合成NH ,反应进程如图1、图2所示。
2 6 3
工业合成氨原理:N(g)+3H(g)2NH (g) ΔH。
2 2 3
(1)已知:N≡N、H—H、N—H的键能分别为945 kJ·mol-1、436 kJ·mol-1、391 kJ·mol-1。
工业合成NH 的ΔH=________ kJ·mol-1。
3
(2)图2中与图1能量变化相符的是________(填“曲线a”或“曲线b”)。在某条件下,测得
上述反应的E=1 250 kJ·mol-1,则E=________ kJ·mol-1。
1 2
(3)合成氨的速率方程为v(NH )=kcα(N )·cβ(H )·cγ(NH )(k为速率常数,只与温度、催化剂有
3 2 2 3
关,与浓度无关;α、β、γ为反应级数,可取整数、分数或小数)。测得在一定温度和催化剂
作用下,速率与浓度的关系如下表所示:
c(N )/ c(H )/ c(NH )/
2 2 3
速率
(mol·L-1) (mol·L-1) (mol·L-1)
Ⅰ 0.1 0.1 0.1 vⅡ 0.2 0.1 0.1 2v
Ⅲ 0.2 0.4 0.1 16v
Ⅳ 0.4 0.9 0.2 54v
Ⅴ 0.4 m 0.4 64v
则α=________;β=__________;γ=__________;m=________。
(4)向密闭容器中充入1 mol N 和2.6 mol H ,在一定条件下合成NH ,相同时间内测得体系
2 2 3
中N 的物质的量(mol)与温度、压强的关系如图3所示。
2
①p________(填“>”“<”或“=”)1.8 MPa。
②投料比一定时,随着温度升高,不同压强下 N 的物质的量趋向相等,其主要原因是
2
________________________________________________________________________
________________________________________________________________________。
③在1.8 MPa、373 K时,平衡常数K =________ MPa-2(提示:用分压计算的平衡常数为
p
K ,分压=总压×物质的量分数)。
p
答案 (1)-93 (2)曲线b 1 343 (3)1 1.5 -1 1.6 (4)①> ②温度升高,温度对平衡
的影响大于压强对平衡的影响 ③12.5
解析 (1)由ΔH=反应物的键能之和-生成物的键能之和可得:ΔH=(945 kJ·mol-1+
436 kJ·mol-1×3)-(391 kJ·mol-1×2×3)=-93 kJ·mol-1。(2)图1为有催化剂参与合成氨反
应的反应进程,图2中曲线b表示有催化剂参与合成氨反应的反应进程与能量变化,则曲线
b与图1能量变化相符;由ΔH=-(E -E)可得:-93 kJ·mol-1=-(E -1 250 kJ·mol-1),
2 1 2
解得E =1 343 kJ·mol-1。(3)依据题给数据,由Ⅰ和Ⅱ的速率相比可得:=,解得α=1;由
2
Ⅱ和Ⅲ的速率相比可得:=,解得β=1.5;由Ⅰ和Ⅳ的速率相比可得:=,解得γ=-1;
由Ⅰ和Ⅴ的速率相比可得:=,解得m=1.6。(4)①合成氨反应为气体体积减小的反应,增
大压强,平衡向正反应方向移动,氮气的物质的量减小,由图可知,温度一定时,压强为 p
时氮气的物质的量小于压强为1.8 MPa时氮气的物质的量,则p大于1.8 MPa。②投料比一
定时,随着温度升高,不同压强下氮气的物质的量趋向相等说明温度升高,温度对平衡的影
响大于压强对平衡的影响。③由图可知,在1.8 MPa、373 K条件下,反应达到平衡时,氮
气的物质的量为0.4 mol,由化学方程式可知,平衡时氢气、氨气的物质的量分别为 2.6 mol
-(1 mol-0.4 mol)×3=0.8 mol、(1 mol-0.4 mol)×2=1.2 mol,则氮气、氢气、氨气的平衡分压分别为×1.8 MPa=0.3 MPa、×1.8 MPa=0.6 MPa、×1.8 MPa=0.9 MPa,平衡常数K
p
==12.5 MPa-2。
3.近年来,我国大力加强温室气体CO 氢化合成甲醇技术的工业化量产研究,实现可持续
2
发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。
(1)已知:①CO(g)+H(g)HO(g)+CO(g)
2 2 2
ΔH=+41.4 kJ·mol-1
1
②CO(g)+2H(g)CHOH(g)
2 3
ΔH=-90.5 kJ·mol-1
2
则反应③CO(g)+3H(g)CHOH(g)+HO(g) ΔH=________ kJ·mol-1。
2 2 3 2 3
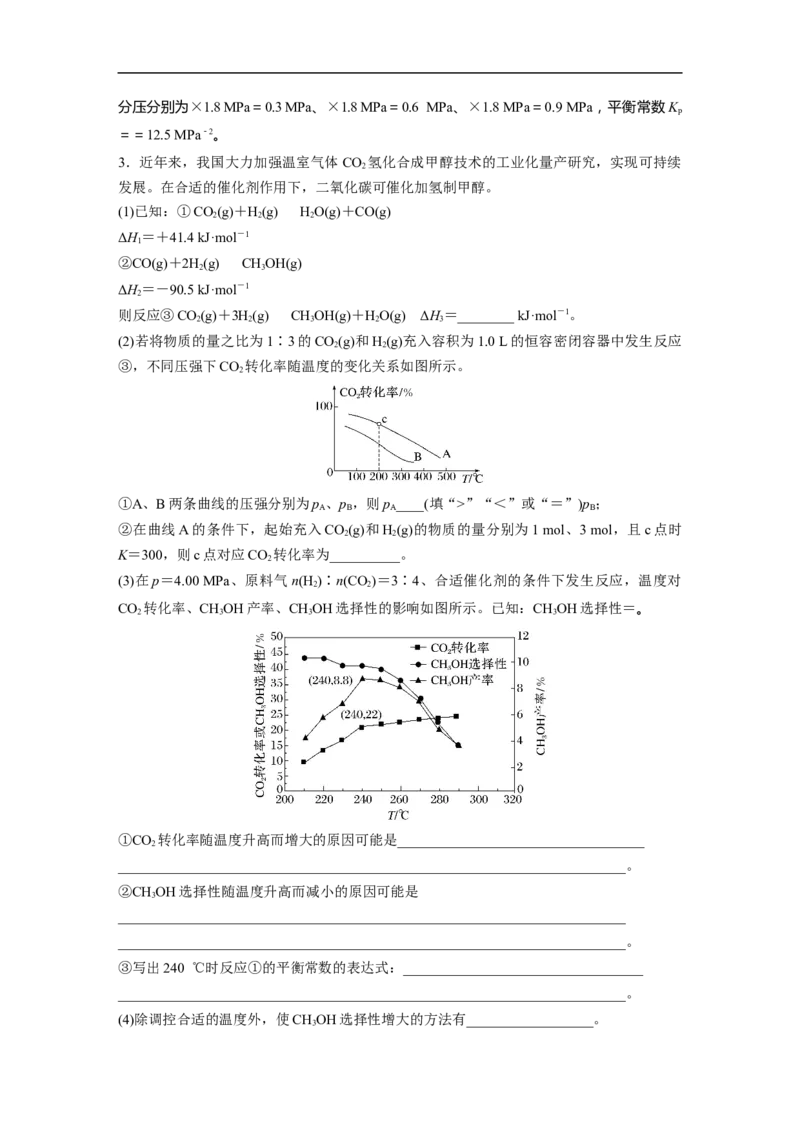
(2)若将物质的量之比为1∶3的CO(g)和H(g)充入容积为1.0 L的恒容密闭容器中发生反应
2 2
③,不同压强下CO 转化率随温度的变化关系如图所示。
2
①A、B两条曲线的压强分别为p 、p ,则p ____(填“>”“<”或“=”)p ;
A B A B
②在曲线A的条件下,起始充入CO(g)和H(g)的物质的量分别为1 mol、3 mol,且c点时
2 2
K=300,则c点对应CO 转化率为__________。
2
(3)在p=4.00 MPa、原料气n(H )∶n(CO)=3∶4、合适催化剂的条件下发生反应,温度对
2 2
CO 转化率、CHOH产率、CHOH选择性的影响如图所示。已知:CHOH选择性=。
2 3 3 3
①CO 转化率随温度升高而增大的原因可能是___________________________________
2
________________________________________________________________________。
②CHOH选择性随温度升高而减小的原因可能是
3
________________________________________________________________________
________________________________________________________________________。
③写出240 ℃时反应①的平衡常数的表达式:__________________________________
________________________________________________________________________。
(4)除调控合适的温度外,使CHOH选择性增大的方法有__________________。
3答案 (1)-49.1 (2)①> ②90% (3)①反应①为吸热反应,温度升高不但能加快反应速
率,而且有利于该反应正向进行 ②反应②(或反应③)为放热反应,而反应①为吸热反应,
所以温度升高不利于CHOH的合成,但有利于CO的生成,所以CHOH产率降低 ③K=
3 3
(4)增大压强或使用更高效的催化剂
解析 (1)反应③=反应①+反应②,则ΔH =ΔH +ΔH =+41.4 kJ·mol-1+(-90.5 kJ·mol-1)
3 1 2
=-49.1 kJ·mol-1。(2)①反应③是气体体积减小的反应,同一温度下,增大压强,平衡正向
移动,CO 转化率升高,则p >p 。②在曲线A的条件下,起始充入CO(g)和H(g)的物质
2 A B 2 2
的量分别为1 mol、3 mol,则CO(g)和H(g)的起始浓度分别为1 mol·L-1、3 mol·L-1,设c
2 2
点时,CO 的转化浓度为x mol·L-1,则H、CHOH、HO的转化浓度分别为3x mol·L-1、x
2 2 3 2
mol·
L-1、x mol·L-1,则c点时CO 、H 、CHOH、HO的浓度分别为(1-x) mol·L-1、(3-3x)
2 2 3 2
mol·
L-1、x mol·L-1、x mol·L-1,K==300,则=300,解得x=0.9,则c点对应CO 转化率为
2
×100%=90%。(3)①反应①为吸热反应,温度升高不但能加快反应速率,而且有利于该反
应正向进行,故CO 转化率随温度升高而增大。②反应②(或反应③)为放热反应,而反应①
2
为吸热反应,所以温度升高不利于CHOH的合成,但有利于CO的生成,所以CHOH产率
3 3
降低,CHOH选择性减小。③反应①的平衡常数的表达式为K=。(4)反应②(或反应③)是气
3
体体积减小的反应,反应①是气体体积不变的反应,增大压强,反应①的平衡不移动,反应
②(或反应③)的平衡正向移动,CHOH产率增大,CHOH选择性增大;使用更高效的催化
3 3
剂,加快反应②(或反应③)的速率,使CHOH产率增大,从而使CHOH选择性增大。
3 3
4.氮氧化物治理是环境学家研究的热点之一。回答下列问题:
(1)NH 还原法
3
研究发现NH 还原NO的反应历程如图1。下列说法正确的是________(填字母)。
3
A.Fe3+能降低总反应的活化能,提高反应速率
B.总反应为6NO+4NH ===5N+6HO
3 2 2
C.该反应历程中形成了非极性键和极性键
(2)已知有关反应如下:
①C(s)+O(g)===CO(g)
2 2
ΔH=-393.5 kJ·mol-1
1
②CO(g)+C(s)===2CO(g)
2ΔH=+172.5 kJ·mol-1
2
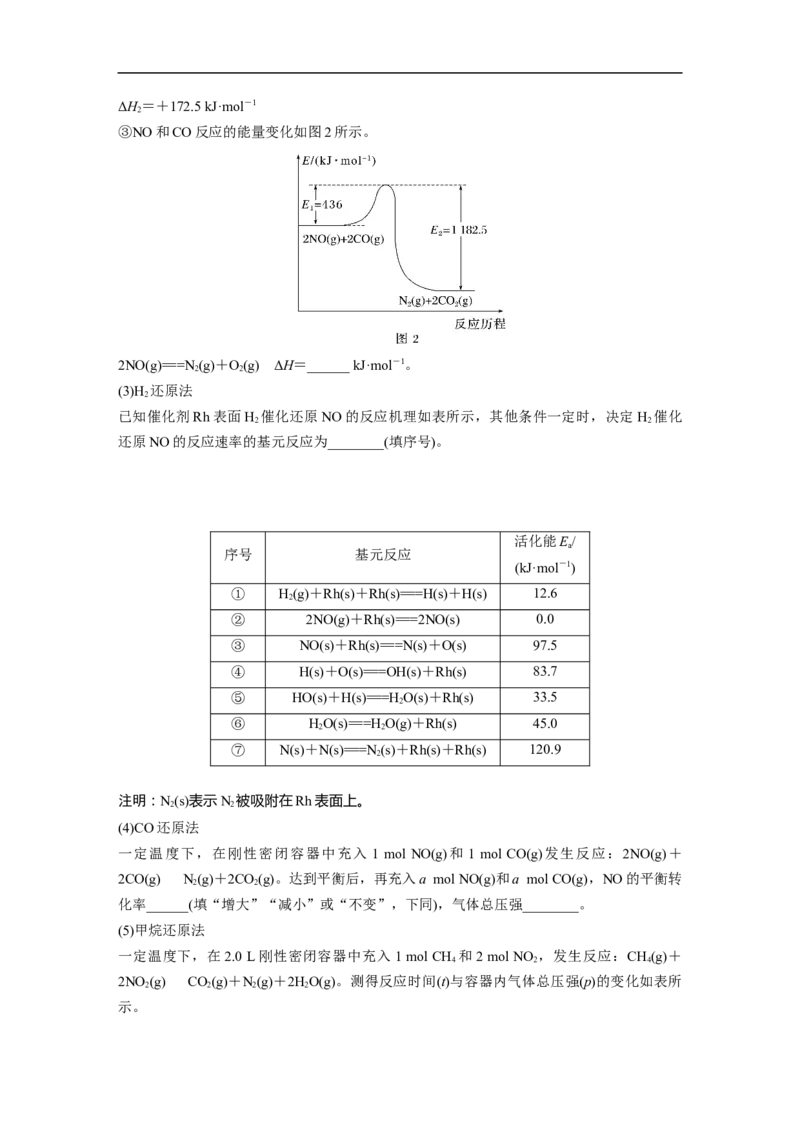
③NO和CO反应的能量变化如图2所示。
2NO(g)===N(g)+O(g) ΔH=______ kJ·mol-1。
2 2
(3)H 还原法
2
已知催化剂Rh表面H 催化还原NO的反应机理如表所示,其他条件一定时,决定H 催化
2 2
还原NO的反应速率的基元反应为________(填序号)。
活化能E/
a
序号 基元反应
(kJ·mol-1)
① H(g)+Rh(s)+Rh(s)===H(s)+H(s) 12.6
2
② 2NO(g)+Rh(s)===2NO(s) 0.0
③ NO(s)+Rh(s)===N(s)+O(s) 97.5
④ H(s)+O(s)===OH(s)+Rh(s) 83.7
⑤ HO(s)+H(s)===HO(s)+Rh(s) 33.5
2
⑥ HO(s)===HO(g)+Rh(s) 45.0
2 2
⑦ N(s)+N(s)===N(s)+Rh(s)+Rh(s) 120.9
2
注明:N(s)表示N 被吸附在Rh表面上。
2 2
(4)CO还原法
一定温度下,在刚性密闭容器中充入 1 mol NO(g)和 1 mol CO(g)发生反应:2NO(g)+
2CO(g)N(g)+2CO(g)。达到平衡后,再充入a mol NO(g)和a mol CO(g),NO的平衡转
2 2
化率______(填“增大”“减小”或“不变”,下同),气体总压强________。
(5)甲烷还原法
一定温度下,在2.0 L刚性密闭容器中充入1 mol CH 和2 mol NO ,发生反应:CH(g)+
4 2 4
2NO (g)CO(g)+N(g)+2HO(g)。测得反应时间(t)与容器内气体总压强(p)的变化如表所
2 2 2 2
示。反应时间
0 2 4 6 8 10
(t)/min
p/(100 kPa) 4.80 5.44 5.76 5.92 6.00 6.00
达到平衡时,NO 的转化率为____________。若起始时加入3 mol CH 和2 mol NO ,则在该
2 4 2
温度下的压强平衡常数K =__________ kPa(以分压表示的平衡常数为K ,分压=总压×物
p p
质的量分数)。
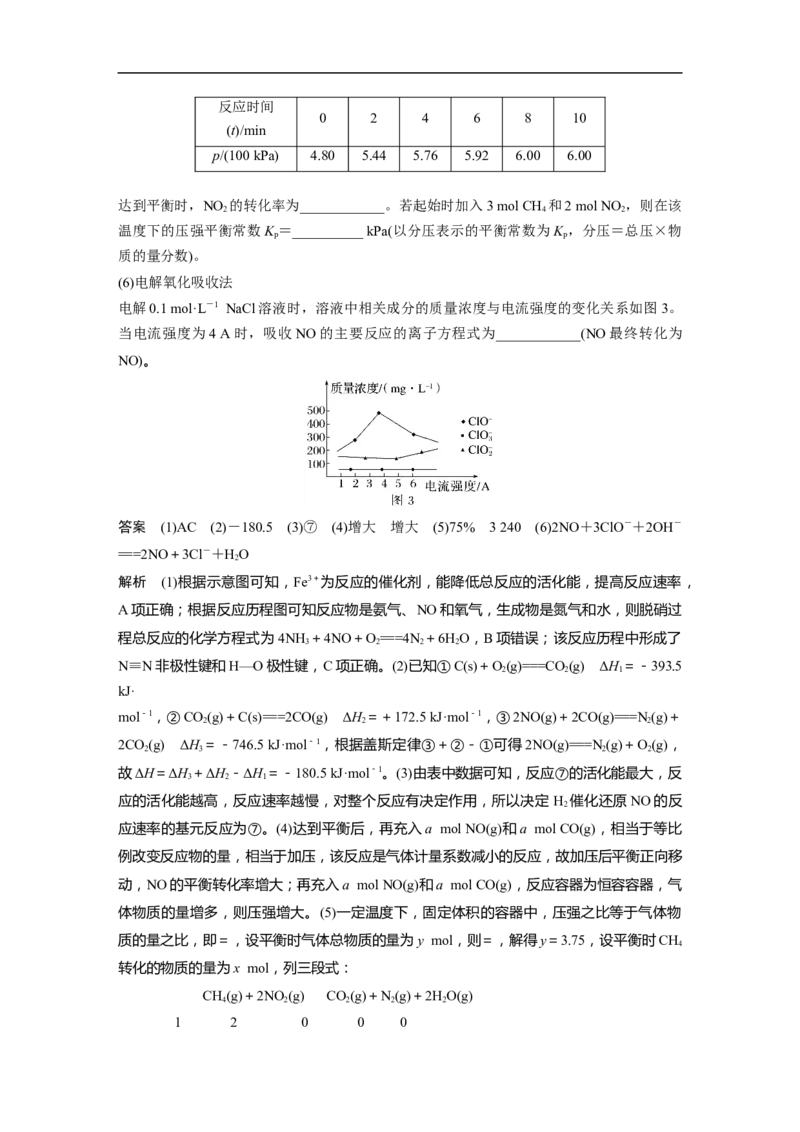
(6)电解氧化吸收法
电解0.1 mol·L-1 NaCl溶液时,溶液中相关成分的质量浓度与电流强度的变化关系如图3。
当电流强度为4 A时,吸收NO的主要反应的离子方程式为____________(NO最终转化为
NO)。
答案 (1)AC (2)-180.5 (3)⑦ (4)增大 增大 (5)75% 3 240 (6)2NO+3ClO-+2OH-
===2NO+3Cl-+HO
2
解析 (1)根据示意图可知,Fe3+为反应的催化剂,能降低总反应的活化能,提高反应速率,
A项正确;根据反应历程图可知反应物是氨气、NO和氧气,生成物是氮气和水,则脱硝过
程总反应的化学方程式为4NH +4NO+O===4N +6HO,B项错误;该反应历程中形成了
3 2 2 2
N≡N非极性键和H—O极性键,C项正确。(2)已知①C(s)+O(g)===CO(g) ΔH =-393.5
2 2 1
kJ·
mol-1,②CO(g)+C(s)===2CO(g) ΔH =+172.5 kJ·mol-1,③2NO(g)+2CO(g)===N(g)+
2 2 2
2CO(g) ΔH =-746.5 kJ·mol-1,根据盖斯定律③+②-①可得2NO(g)===N(g)+O(g),
2 3 2 2
故ΔH=ΔH +ΔH -ΔH =-180.5 kJ·mol-1。(3)由表中数据可知,反应⑦的活化能最大,反
3 2 1
应的活化能越高,反应速率越慢,对整个反应有决定作用,所以决定 H 催化还原NO的反
2
应速率的基元反应为⑦。(4)达到平衡后,再充入a mol NO(g)和a mol CO(g),相当于等比
例改变反应物的量,相当于加压,该反应是气体计量系数减小的反应,故加压后平衡正向移
动,NO的平衡转化率增大;再充入a mol NO(g)和a mol CO(g),反应容器为恒容容器,气
体物质的量增多,则压强增大。(5)一定温度下,固定体积的容器中,压强之比等于气体物
质的量之比,即=,设平衡时气体总物质的量为y mol,则=,解得y=3.75,设平衡时CH
4
转化的物质的量为x mol,列三段式:
CH(g)+2NO (g)CO(g)+N(g)+2HO(g)
4 2 2 2 2
1 2 0 0 0x 2x x x 2x
1-x 2-2x x x 2x
可得1-x+2-2x+x+x+2x=3.75,解得x=0.75,NO 的转化率为×100%=75%;K ==
2 p
kPa=3 240 kPa;温度不变,平衡常数不变,故若起始时加入 3 mol CH 和2 mol NO ,则在
4 2
该温度下的压强平衡常数还是 3 240 kPa。(6)由图3可知当电流强度为4 A时,氯的主要存
在形式为ClO-,故此时是ClO-和一氧化氮反应生成氯离子和硝酸根离子,反应的离子方程
式为2NO+3ClO-+2OH-===2NO+3Cl-+HO。
2