文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷 第 18套 ① ②
组编人:于洪强
做题时间:2022 年__月___日,__:__—__:__ 校对人: 汪志新
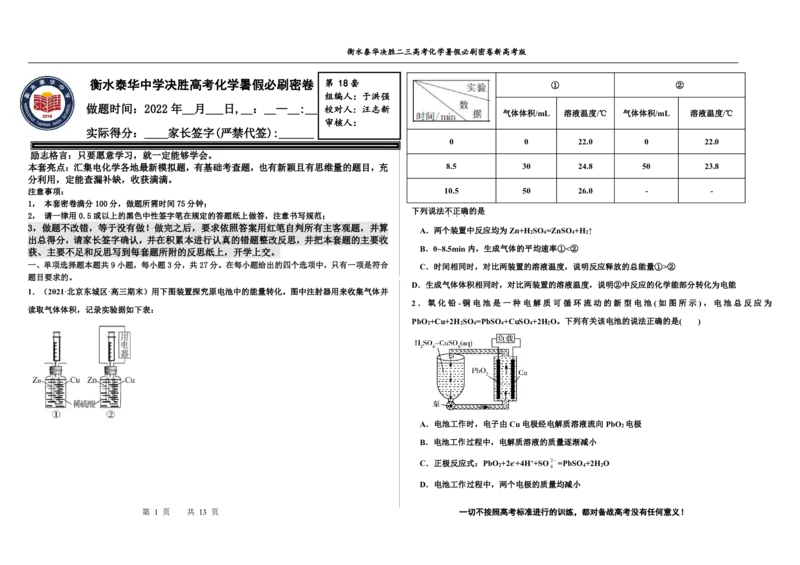
气体体积/mL 溶液温度/℃ 气体体积/mL 溶液温度/℃
审核人:
实际得分:____家长签字(严禁代签):______
0 0 22.0 0 22.0
励志格言:只要愿意学习,就一定能够学会。
本套亮点:汇集电化学各地最新模拟题,有基础考查题,也有新颖且有思维量的题目,充 8.5 30 24.8 50 23.8
分利用,定能查漏补缺,收获满满。
注意事项: 10.5 50 26.0 - -
1, 本套密卷满分100分,做题所需时间75分钟;
下列说法不正确的是
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范; ...
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并算
A.两个装置中反应均为Zn+H SO =ZnSO +H ↑
2 4 4 2
出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的主要收
获、主要不足和反思写到每套题所附的反思纸上,开学上交。
B.0~8.5min内,生成气体的平均速率①<②
一、单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合 C.时间相同时,对比两装置的溶液温度,说明反应释放的总能量①>②
题目要求的。
D.生成气体体积相同时,对比两装置的溶液温度,说明②中反应的化学能部分转化为电能
1.(2021·北京东城区·高三期末)用下图装置探究原电池中的能量转化。图中注射器用来收集气体并
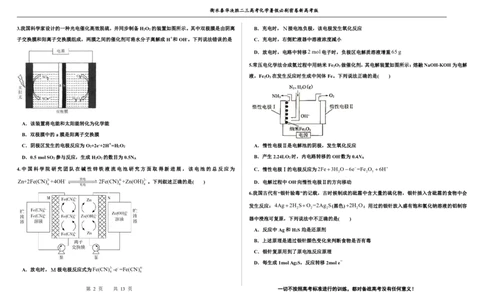
2.氧化铅-铜电池是一种电解质可循环流动的新型电池(如图所示),电池总反应为
读取气体体积,记录实验据如下表:
PbO +Cu+2H SO =PbSO +CuSO +2H O。下列有关该电池的说法正确的是( )
2 2 4 4 4 2
A.电池工作时,电子由Cu电极经电解质溶液流向PbO 电极
2
B.电池工作过程中,电解质溶液的质量逐渐减小
C.正极反应式:PbO +2e-+4H++SO 2 =PbSO +2H O
2 4 4 2
D.电池工作过程中,两个电极的质量均减小
第 1 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
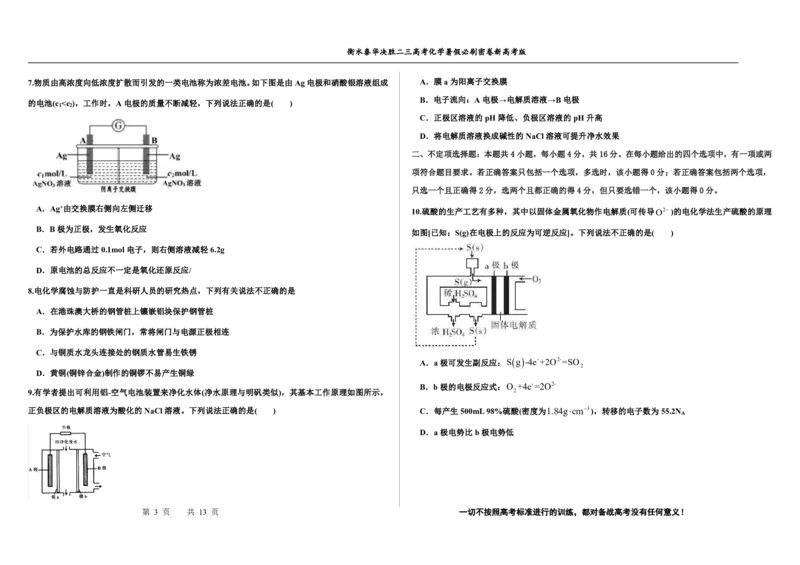
3.我国科学家设计的一种光电催化高效脱硫,并同步制备H O 的装置如图所示。其中双极膜是由阴离 B.充电时,N接电池负极,该电极发生氧化反应
2 2
子交换膜和阳离子交换膜组成,两膜之间的催化剂可将水分子离解成H+和OH-。下列说法错误的是 C.充电时,右侧贮液器中溶液浓度减小
D.放电时,电路中转移2mol电子时,负极区电解质溶液增重65g
5.常压电化学法合成氨过程中用纳米Fe O 做催化剂,其电解装置如图所示:熔融NaOH-KOH为电解
2 3
液,Fe O 在发生反应时生成中间体Fe。下列说法正确的是( )
2 3
A.该装置将电能和太阳能转化为化学能
B.双极膜中的a膜是阳离子交换膜
C.阴极区发生的电极反应为O +2e-+2H+=H O A.惰性电极Ⅱ是电解池的阴极,发生氧化反应
2 2 2
D.0.5molSO 2 参与反应,生成H 2 O 2 的数目为0.5N A B.产生2.24LO 2 时,内电路转移的OH-数为0.4N A
4.中国科学院研究团队在碱性锌铁液流电池研究方面取得新进展,该电池的总反应为 C.惰性电极Ⅰ的电极反应为2Fe3H O6e=Fe O 6H
2 2 3
Zn+2Fe(CN)3-+4OH- 放 电 2Fe(CN)4-+Zn(OH)2-。下列叙述正确的是( ) D.电解过程中OH-向惰性电极Ⅱ的方向移动
6 充电 6 4
6.我国古代有“银针验毒”的记载,古时候制成的砒霜中含大量的硫化物,银针插入含砒霜的食物中会
发生反应:4Ag2H SO =2Ag S(黑色) 2H O;用过的银针放入盛有饱和氯化钠溶液的铝制容
2 2 2 2
器中浸泡可复原,下列说法中不正确的是( )
A.反应中Ag和H S均是还原剂
2
B.上述原理是通过银针颜色变化来判断食物是否有毒
C.银针复原用到了原电池反应原理
D.每生成1molAg S,反应转移2mole-
2
A.放电时,M极电极反应式为Fe(CN)3--e-=Fe(CN)4-
6 6
第 2 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
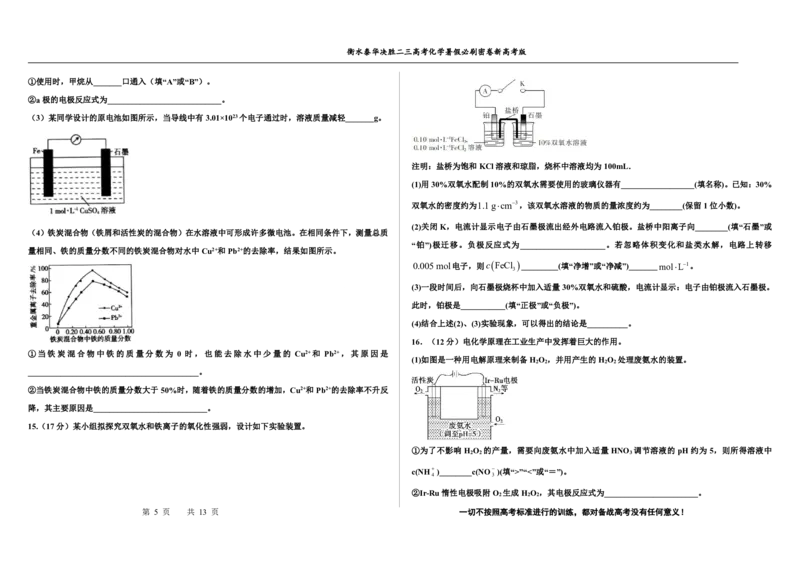
7.物质由高浓度向低浓度扩散而引发的一类电池称为浓差电池。如下图是由Ag电极和硝酸银溶液组成 A.膜a为阳离子交换膜
的电池(c ”“<”或“=”)。
4 3
②Ir-Ru惰性电极吸附O 生成H O ,其电极反应式为_______________________。
2 2 2
第 5 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
③理论上电路中每转移3mol电子,最多可以处理废氨水中溶质(以NH 计)的质量是___________g。
3
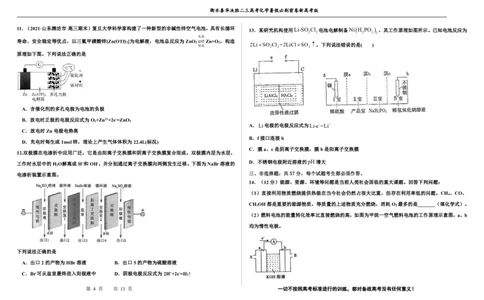
(2)利用铜基配合物1,10-phenanthroline-Cu催化剂电催化CO
2
还原制备碳基燃料(包括CO、烷烃和 (3)在稀H
2
SO
4
中利用电催化可将CO
2
同时转化为多种燃料,其原理如图所示。
酸等)是减少CO 在大气中累计和实现可再生能源有效利用的关键手段之一,其装置原理如图所示。
2
① 一段时间后,Cu极区溶液质量___________(填“增加”“减少”或“不变”)。
② 铜极上产生乙烯的电极反应式为___________。
①电池工作过程中,图中Pt电极附近溶液的pH值_____________(填“增大”、“减小”或“不变”)。
③ 若阴极只生成0.17molCO和0.33molHCOOH,则电路中转移电子的物质的量为___________mol。
②阴极的电极反应式为______________。
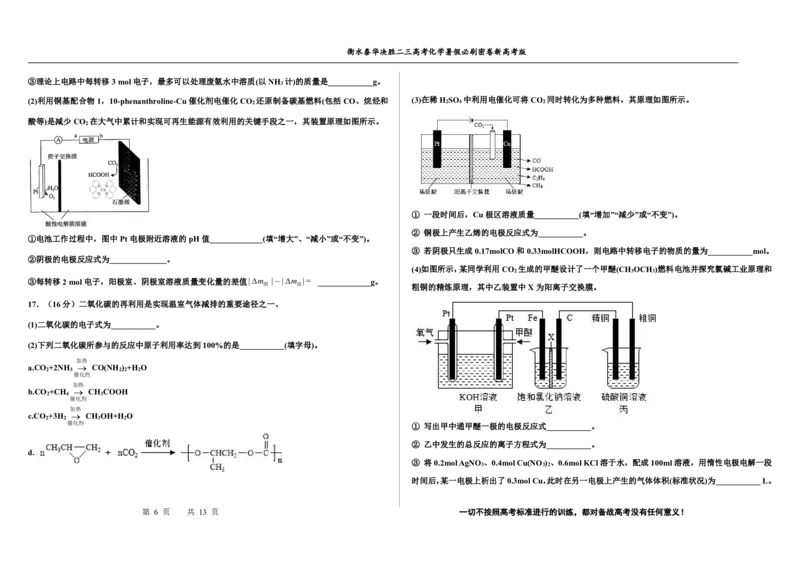
(4)如图所示,某同学利用CO 生成的甲醚设计了一个甲醚(CH OCH )燃料电池并探究氯碱工业原理和
2 3 3
③每转移2mol电子,阳极室、阴极室溶液质量变化量的差值|m ||m |= _____________g。
阴 阳 粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
17.(16分)二氧化碳的再利用是实现温室气体减排的重要途径之一、
(1)二氧化碳的电子式为___________。
(2)下列二氧化碳所参与的反应中原子利用率达到100%的是___________(填字母)。
加热
a.CO +2NH CO(NH ) +H O
2 3 2 2 2
催化剂
加热
b.CO +CH CH COOH
2 4 3
催化剂
加热
c.CO +3H CH OH+H O
2 2 3 2
催化剂 ① 写出甲中通甲醚一极的电极反应式___________。
② 乙中发生的总反应的离子方程式为___________。
d.
③ 将0.2molAgNO 、0.4molCu(NO ) 、0.6molKCl溶于水,配成100ml溶液,用惰性电极电解一段
3 3 2
时间后,某一电极上析出了0.3molCu,此时在另一电极上产生的气体体积(标准状况)为___________L。
第 6 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
化学假期作业(十八)答题纸 ②
(总分 57 分,除标注外,其余每空 2 分) ③
姓名 学号 得分 (2)①
14、(12分) ②
(1) ③
(2)① 17、(16分)
② (1)
(3) (2)
(4)① (3)①
② ②
15、(17分) ③
(1) (4)①
(2) ②
③
(3)
(4) (3分)
16、(12分)
(1)①
第 7 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第十八套化学参考答案 A.该装置有电源,为电解池,装置中还有太阳光,所以是将电能和太阳能转化为化学能的装置,A
正确,不符合题意;
1、【答案】C
A.装置①和②发生反应的实质都是锌与稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为 B.左边上实现的是二氧化硫变成硫酸根离子,失去电子,电极反应为SO 2 +4OH--2e-= SO2 4 - +2H 2 O,
Zn+H SO =ZnSO +H ↑,故A正确; 为阳极,所以水电离出的氢氧根离子通过阴离子交换膜进入左侧,故a为阴离子交换膜,B错误,不
2 4 4 2
B.由表格数据可知,相同时间内,装置②中生成的氢气的体积比装置①中大,生成气体的平均速率 符合题意;
①<②,故B正确; C.右边为阴极,是氧气变成过氧化氢,电极反应为O +2e-+2H+=H O ,C正确,不符合题意;
2 2 2
C.由能量转化形式可知,装置①中化学能转化为热能,装置②中化学能转化为电能和热能,由两装置 D.0.5molSO 参与反应,转移1mol电子,对应生成H O 的数目为0.5N ,D正确,不符合题意;
2 2 2 A
的溶液温度可知,装置①中化学能转化为热能的能量大于装置②中化学能转化为热能的能量,但相同 故选B。
时间内,装置②中生成的氢气的体积比装置①中大,反应释放的总能量①<②,故C错误; 4、【答案】C
D.生成气体体积相同时,两装置反应释放的总能量相等,由两装置的溶液温度可知,装置①中化学能 【分析】
转化为热能的能量大于装置②中化学能转化为热能的能量,说明②中反应的化学能部分转化为电能, 根据图示及总反应可知,放电时,N为负极,Zn失去电子,发生氧化反应,M为正极,Fe(CN)3-得
6
故D正确;
电子,发生还原反应;充电时,N为阴极,Zn(OH)2-得电子,发生还原反应,M为阳极,Fe(CN)4-
4 6
故选C。
失去电子,发生氧化反应。
2、【答案】C
【详解】
【详解】
A.电池工作时,电子不能流经电解质溶液,只能在外电路中流动,故A项镨误;
A.根据分析,放电时,M 为电池正极, Fe(CN)3
6
- 得电子,发生还原反应,电极反应式为
B.由电池总反应可知,若反应的PbO 2 为1mol,则电解质溶液中增加了2molO,1molCu,减少了 Fe(CN)3-+e-=Fe(CN)4-,故A项错误;
6 6
1molSO
2,则增加和减少的质量相等,反应前后电解质溶液的质量不变,故B项错误;
4 B.充电时,N为阴极,接电池负极,Zn(OH)2-得电子,发生还原反应,故B项错误;
4
C.由总反应可知,PbO 得电子,正极反应式为PbO +2e-+4H++SO 2 =PbSO +2H O,故C项正确;
2 2 4 4 2 C.充电时,右侧贮液器中Zn(OH)2-得到电子生成Zn,离子减少,溶液浓度减小,故C项正确;
4
D.正极反应生成的硫酸铅附着在PbO 电极上,其质量增加,故D项错误;
2
D.放电时,Zn 失电子后与氢氧根生成Zn(OH)2-,当电路中转移2mol电子时,溶液增加的质量为
4
故选C。
1molZn和2molOH-的质量之和,大于65g,故D项错误。
3、【答案】B
故答案选:C。
【详解】
第 8 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
5、【答案】D AgNO ~ e
3
【详解】 所以由 170g 1mol 可知,若外电路通过0.1mol电子,则右侧溶液减轻17.0g,故C错;
17.0g 0.1mol
A.根据分析可知电极Ⅱ为阳极,失电子发生氧化反应,A错误;
B.温度和压强未知,无法确定2.24LO 的物质的量,则无法确定转移电子数,B错误;
D.负极的电极反应式为:Age=Ag,正极的电极反应式为:Ag e=Ag,总反应为:Ag=Ag
2
C.根据分析可知惰性电极Ⅰ上Fe O 被还原生成Fe,电极反应为Fe O +3H O+6e-=2Fe+6OH-,C错 属于非氧化还原反应,故选D。
2 3 2 3 2
误; 答案选D。
D.电解池中阴离子向阳极移动,即向惰性电极Ⅱ的方向移动,D正确; 8、【答案】B
综上所述答案为D。 【详解】
6、【答案】A A.在港珠澳大桥的钢管桩上镶嵌铝块,铁、铝构成原电池,铝是负极,属于牺牲阳极的阴极保护法,
【详解】 故A正确;
A.反应中Ag化合价升高,是还原剂,H S中化合价未变,既不是还原剂也不是氧化剂,故A错误; B.为保护水库的钢铁闸门,常将闸门与电源负极相连,故B错误;
2
B.砒霜中含大量的硫化物,银针插入变为黑色,因此可以通过银针颜色变化来判断食物是否有毒, C.铁、铜构成原电池,铁为负极,所以与铜质水龙头连接处的钢质水管易生铁锈,故C正确;
故B正确; D.铜、锌构成原电池,锌是负极,黄铜(铜锌合金)制作的铜锣不易产生铜绿,故D正确;
C.银针复原是Al—Ag S—饱和食盐水的原电池反应原理,Al做负极,Ag S做正极,故C正确; 选B。
2 2
D.该反应方程式是2molAg失去2mol电子变为1molAg S,因此每生成1molAg S,反应转移2mole 9、【答案】A
2 2
-,故D正确。 【详解】
综上所述,答案为A。 该装置的净水原理与明矾类似,则会产生氢氧化铝胶体(Al3+水解),
7、【答案】D
A. 电解质溶液显酸性,A极为铝电极,为负极,电极反应式为Al-3e-=Al3+,B极为正极,电极反
【详解】
应式为O +4H++4e-=2H O,为达到净水的目的,负极生成的Al3+需要通过膜a进入待净化废水中,
2 2
A.由图示分析可知,工作时,A电极的质量不断减轻,则A为负极、B为正极;由于装置中所用的
Al3+水解生成氢氧化铝胶体,则膜a为阳离子交换膜,故A正确;
隔膜为阴离子交换膜,则只能阴离子通过,所以NO由交换膜右侧向左侧迁移,故A错;
3
B. 原电池中电子从负极经导线流向正极,则该原电池中电子流向:A电极→导线→B电极,故B错
B.由A分析可知,A为负极发生氧化反应,B为正极发生还原反应,故B错;
误;
C.若外电路通过0.1mol电子,则右侧溶液中有0.1molNO
3
向左侧迁移,0.1molAg+得到电子生成Ag,
C. 根据A项分析知,正极区溶液的氢离子浓度减小,pH增大,负极区溶液的pH不变,故C错误;
第 9 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
D.将电解质溶液换成碱性的NaCl溶液,则负极生成AlO- ,达不到净水的效果,故D错误; D.根据总反应可知,充电时每生成1mol锌,会生成1mol的氧气,1mol氧气的体积为22.4L(标况),
2
D项正确;
故选A。
答案选BD。
10、【答案】C
12、【答案】D
【分析】
【详解】
因为固体电解质能传导O2-,则通O 的电极发生的电极反应为:O +4e-=2O2-,从而得出b极为正极,
2 2
A. 电解时, 溶液中的阳离子向阴极移动,阴离子向阳极移动,溶液中的Na+向阴极移动,与双极膜
a极为负极。
提供的氢氧根离子结合,出口2的产物为NaOH溶液,A错误;
【详解】
B. 电解时, 溶液中的阳离子向阴极移动,阴离子向阳极移动,溶液中的Br-向阳极移动,与双极膜
A.由以上分析可知,a极为负极,主反应为S(g)失电子产物与电解质中的O2-等反应,最终生成硫酸,
提供的氢离子结合,故出口4的产物为HBr溶液,钠离子不能通过双极膜,故出口5不是硫酸,B错
可能发生副反应为:S g -4e-+2O2-=SO ,A正确;
2
误;
B.由分析可知,b极为正极,O
2
得电子生成O2-,电极反应式:O
2
+4e-=2O2-,B正确;
C. 结合选项B,Br-不会从盐室最终进入阳极液中,C错误;
C.在负极,S(g)—H SO —6e-,每产生 500mL 98%硫酸(密度为1.84gcm3),转移的电子数为 D. 电解池阴极处,发生的反应是物质得到电子被还原,发生还原反应,水解离成H+和OH−,则在
2 4
阴极处发生的反应为2H++2e-=H ↑,D正确;
2
500mL1.84g/mL98%
98g/mol 6N A =55.2N A ,但还有副反应发生,所以转移电子总数大于55.2N A ,C不 答案选D。
13、【答案】BC
正确;
【分析】
D.a极为负极,b极为正极,正极电势比负极高,则a极电势比b极电势低,D正确;
故选C。
由电极反应式2LiSO
2
Cl
2
=2LiClSO
2
可知,Li转化为Li+,则Li电极为负极,C电极为正极;
11、【答案】BD
因为要电解制备Ni
H PO
,则镍电极应失电子,所以镍电极为阳极,g与f相连;h与e相连;
2 2 2
【详解】
Ni失电子生成Ni2+通过膜a进入产品室(Ⅱ室),则膜a为阳膜;H PO 通过膜b进入产品室(Ⅱ室),
2 2
A.多孔电极通空气,得电子,发生还原反应,为电池的正极,A项错误;
则膜b为阴膜;在阴极(不锈钢),H O得电子生成H 和OH-,所以Ⅲ室中的Na+通过膜c进入Ⅳ室,
充电 2 2
B.由电池总反应:ZnO 2 放 电 Zn+O 2 可知,放电时,正极得电子,电极反应式为O 2 +Zn2++2e-=ZnO 2 ,
膜c为阳膜。
B项正确;
【详解】
C.放电时,Zn电极为负极,其电势低,C项错误;
第 10 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
A.由电极反应式2LiSO Cl =2LiClSO 可知,Li 转化为 Li+,则Li电极的电极反应式为
(3)由图可知,Fe为负极,石墨为正极,电解质为CuSO
4
,正极上Cu2+得电子生成Cu,电极反应为
2 2 2
Cu2++2e-=Cu,导线中有3.01×1023个电子流过,即转移0.5mol电子时,溶液中Cu2+转化为Cu的质
Li-e-=Li+,A正确;
量为64g/mol×0.25mol=16g,负极上Fe-2e-=Fe2+,进入溶液的Fe2+的质量为56g/mol×0.25mol=14g,
B.由上面的分析可知,f(正极)接口连接g(阳极),B错误;
所以溶液质量减少16g-14g=2g;
C.由上面分析可知,膜a、c是阳离子交换膜,膜b是阴离子交换膜,C错误;
(4)①当铁炭混合物中铁的质量分数为0时,则只有碳粉,由于活性炭粉具有吸附性,也可起到净水的
D.在不锈钢电极(阴极)附近,溶液中的水得电子,电极反应式为2H
2
O+2e-=H
2
↑+2OH-,溶液的pH增
作用,因此可去除水中少量的Cu2+和Pb2+;
大,D正确; ②随着铁的质量分数的增加,碳铁混合物在水溶液中形成的微电池数目减少,反应速率减小,则Cu2+
故选BC。 和Pb2+的去除率不升反降。
14.【答案】(1)CH 15【答案】
4
(2)①A ②CH -8e-+10OH-=CO 2 +7H O (1)烧杯,量筒、玻璃棒 9.7 molL1
4 3 2
(3) 2 (2) 铂
(4) ①活性炭具有吸附性,可以吸附少量的Cu2+和Pb2+ H O 2e=2H O 净减 0.05
2 2 2
② 碳铁混合物在水溶液中形成的微电池数目减少
(3)负极 较弱酸性条件,Fe3氧化性比H O 强;较强酸性条件下,H O 氧化性比Fe3 强
2 2 2 2
【详解】
【详解】
(1)CH 、CO、CH OH燃烧的方程式分别是:CH +2O 点燃CO +2H O、2CO+O 点燃2CO 、
4 3 4 2 2 2 2 2
(1)稀释一定质量分数的溶液只需要量筒、烧杯和玻璃棒;根据物质的量浓度与质量分数之间的转换关
2CH OH+3O 点燃 2CO +4H O,根据方程式可知,1g 燃料完全燃烧消耗 O 的质量分别是 1000ρω 10001.10.3
3 2 2 2 2 系式,c molL19.7molL1,故答案为:烧杯,量筒、玻璃棒;
M 34
1g 1g 1 4g 1g 3
2324g、 32 、 321.5g ,所以等质量的上述气体充分燃烧,消耗
16 28 2 7 32 2 9.7molL1;
O 最多的是CH ;
2 4 (2)在原电池中,电子由负极流向正极,依题意,石墨极为负极,铂极为正极,盐桥中钾离子向正极迁
(2)①根据图中电子流向可判断a为负极,b为正极,燃料电池中正极需通入O ,所以空气从B口通入,
2
移,维持电荷守恒;双氧水在负极上发生氧化反应生成O ,溶液酸性增强,负极反应式为
2
甲烷从A口通入;
0.005mol
H O 2e=2H O ;正极反应式为Fe3 e=Fe2,净减浓度为 0.05molL1,
②CH 在负极发生氧化反应,碱性环境中生成 CO 2 ,负极电极反应为:CH -8e-+10OH-= 2 2 2 0.1L
4 3 4
故答案为:铂;H O 2e=2H O ;净减;0.05;
CO 2 +7H O; 2 2 2
3 2
第 11 页 共 13 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(3)由电子流向可知,铂极为负极,故答案为:负极; |m m |=46g-18g=28g。
阴 阳
(4)分析(2)(3)步骤中溶液酸碱性可知,开始双氧水接近中性,双氧水还原铁离子,发生总反应为
17.【答案】
2Fe3 H O =2Fe2 O 2H,氧化性:Fe3 H O ;加入双氧水和硫酸后,双氧水氧化亚
2 2 2 2 2 (1) (2)bd
铁离子,发生总反应为2Fe2 H O 2H=2Fe3 2H O,氧化性:H O Fe3,故答案为:较 (3)①增加 ②2CO +12H++12e-=C H +4H O ③1
2 2 2 2 2 2 2 4 2
(4)①CH OCH -12e-+16OH-=2CO 2 +11H O
弱酸性条件,Fe3氧化性比H O 强;较强酸性条件下,H O 氧化性比Fe3强。 3 3 3 2
2 2 2 2
通电
16、【答案】 ②2Cl-+2H 2 O Cl 2 ↑+H 2 ↑+2OH- ③5.6
(1)①< ②O +2e-+2H+=H O ③17 【详解】
2 2 2
(2)①减小 ②CO 2 +2e-+2H+=HCOOH ③28g (1)二氧化碳分子中碳原子与两个氧原子分别共用两对电子,电子式为 ;
【详解】
(2)a.有副产品水生成,原子利用率没有达到100%,故a错误;
(1)①溶液中存在电荷守恒 c(NO )+ c(OH-)= c(NH )+ c(H+),溶液显酸性,所以 c(H+)> c(OH-),则 b.反应为化合反应,反应物全部转化为生成物,没有其它物质生成,则原子利用率达100%,故b正
3 4
确;
c(NH )