文档内容
衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷 第 19 套 B.放电时NaCl溶液的pH减小
组编人:张晓燕
C.放电时NaCl溶液的浓度增大
做题时间:2022 年__月___日,__:__—__:__ 校对人: 贾美菁
审核人:王立明 D.每生成1mol Cl ,电极a质量理论上增加23g
2
实际得分:____家长签字(严禁代签):______
2.(2022·浙江·高考真题)下列说法正确的是
励志格言:幸福不会从天而降,梦想不会自动成真。实现我们的奋斗目标,开创我们
A.工业上通过电解六水合氯化镁制取金属镁
的美好未来,必须紧紧依靠人民、始终为了人民
B.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
本套亮点:汇集电化学各地最新模拟题,有基础考查题,也有新颖且有思维量的题目,充
分利用,定能查漏补缺,收获满满。 C.浓硝酸与铁在常温下不能反应,所以可用铁质容器贮运浓硝酸
注意事项:
D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用
1, 本套密卷满分100分,做题所需时间75分钟;
2, 请一律用0.5或以上的黑色中性签字笔在规定的答题纸上做答,注意书写规范; 3.(2022·全国·高考真题)Li-O 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科
2
3,做题不改错,等于没有做!做完之后,要求依照答案用红笔自判所有主客观题,并算
出总得分,请家长签字确认,并在积累本进行认真的错题整改反思,并把本套题的主要收 学家研究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子
e
和空穴
h
,驱动
2
获、主要不足和反思写到每套题所附的反思纸上,开学上交。
一、单项选择题本题共9小题,每小题3分,共27分。在每小题给出的四个选项中,只有一项是符合 阴极反应 Li e Li 和阳极反应(Li 2 O 2 +2h+=2Li++O 2 )对电池进行充电。下列叙述错误的是
题目要求的。
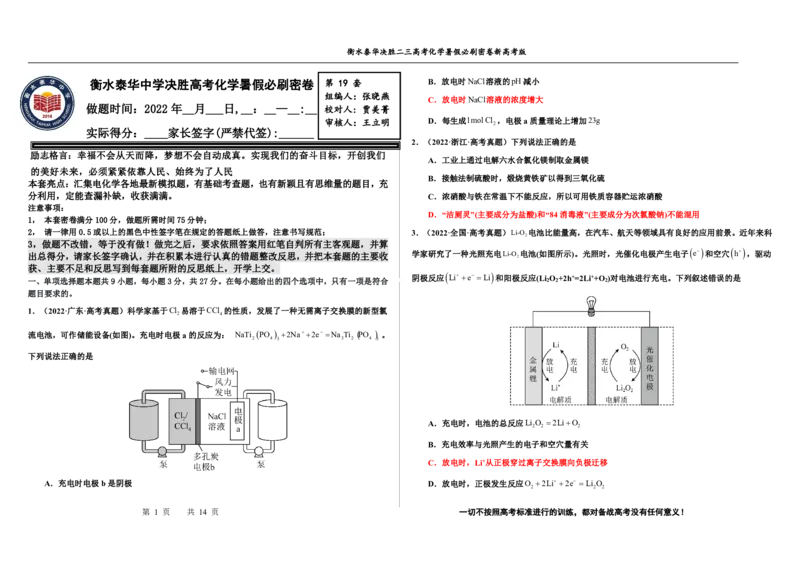
1.(2022·广东·高考真题)科学家基于Cl 易溶于CCl 的性质,发展了一种无需离子交换膜的新型氯
2 4
流电池,可作储能设备(如图)。充电时电极a的反应为: NaTi PO 2Na2e Na Ti PO 。
2 4 3 3 2 4 3
下列说法正确的是
A.充电时,电池的总反应Li O 2LiO
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
A.充电时电极b是阴极 D.放电时,正极发生反应O 2Li 2e Li O
2 2 2
第 1 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
4. (2021·山东·高考真题)以KOH溶液为离子导体,分别组成CH OH—O 、N H —O 、
3 2 2 4 2
(CH ) NNH —O 清洁燃料电池,下列说法正确的是
3 2 2 2
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH ) NNH —O 燃料电池的理论放电量最大
3 2 2 2
D.消耗1molO 时,理论上N H —O 燃料电池气体产物的体积在标准状况下为11.2L
2 2 4 2
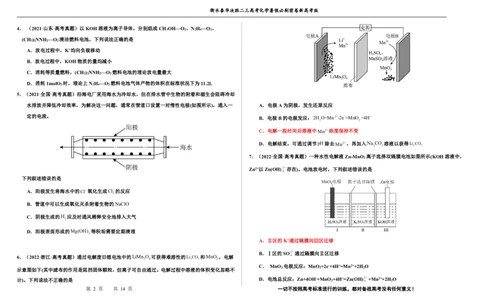
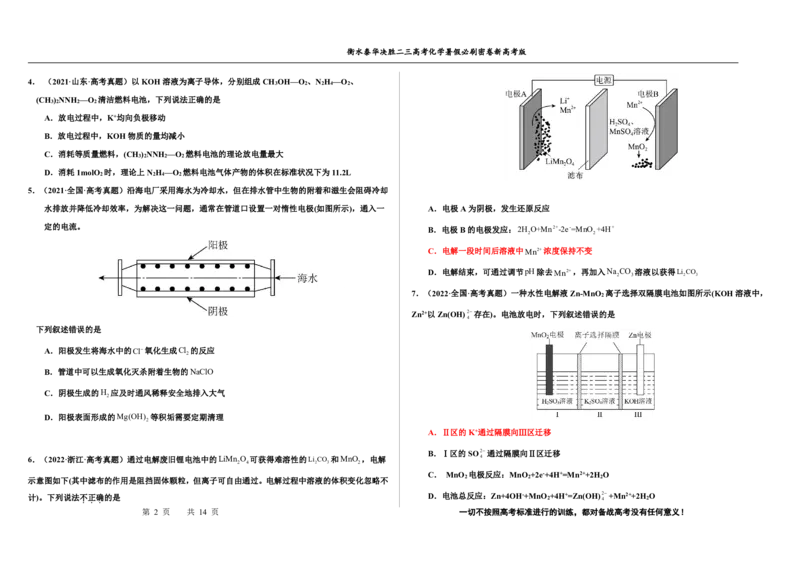
5.(2021·全国·高考真题)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却
水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一 A.电极A为阴极,发生还原反应
定的电流。
B.电极B的电极发应:2H O+Mn2+-2e-=MnO +4H+
2 2
C.电解一段时间后溶液中Mn2+浓度保持不变
D.电解结束,可通过调节pH除去Mn2+,再加入Na CO 溶液以获得Li CO
2 3 2 3
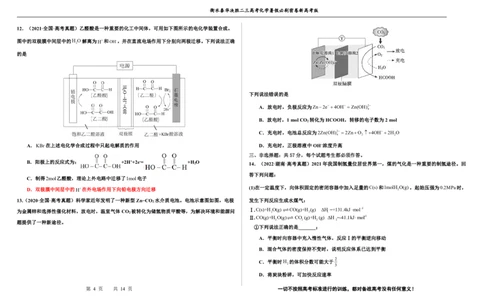
7.(2022·全国·高考真题)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,
2
Zn2+以Zn(OH)2存在)。电池放电时,下列叙述错误的是
4
下列叙述错误的是
A.阳极发生将海水中的Cl氧化生成Cl 的反应
2
B.管道中可以生成氧化灭杀附着生物的NaClO
C.阴极生成的H 应及时通风稀释安全地排入大气
2
D.阳极表面形成的Mg(OH) 等积垢需要定期清理
2
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO2通过隔膜向Ⅱ区迁移
6.(2022·浙江·高考真题)通过电解废旧锂电池中的LiMn O 可获得难溶性的Li CO 和MnO ,电解 4
2 4 2 3 2
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不 2 2 2
计)。下列说法不 . 正 . 确 . 的是 D.电池总反应:Zn+4OH-+MnO 2 +4H+=Zn(OH)2 4 +Mn2++2H 2 O
第 2 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
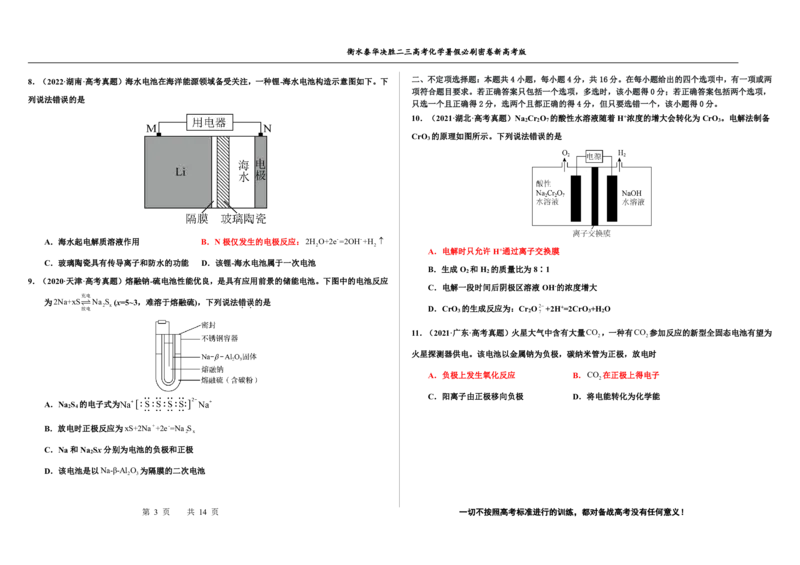
8.(2022·湖南·高考真题)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下 二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有一项或两
项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,
列说法错误的是
只选一个且正确得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
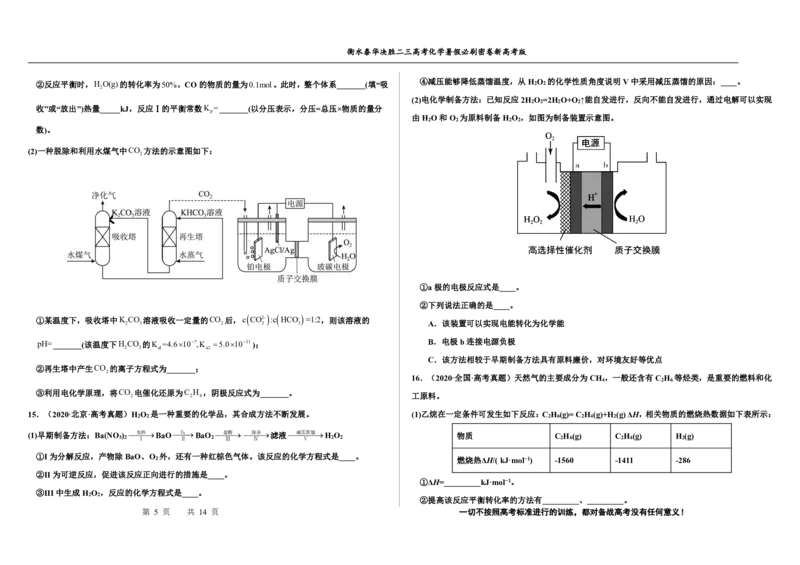
10.(2021·湖北·高考真题)Na Cr O 的酸性水溶液随着H+浓度的增大会转化为CrO 。电解法制备
2 2 7 3
CrO 的原理如图所示。下列说法错误的是
3
A.海水起电解质溶液作用 B.N极仅发生的电极反应:2H O+2e-=2OH-+H
2 2
A.电解时只允许H+通过离子交换膜
C.玻璃陶瓷具有传导离子和防水的功能 D.该锂-海水电池属于一次电池
B.生成O 和H 的质量比为8∶1
2 2
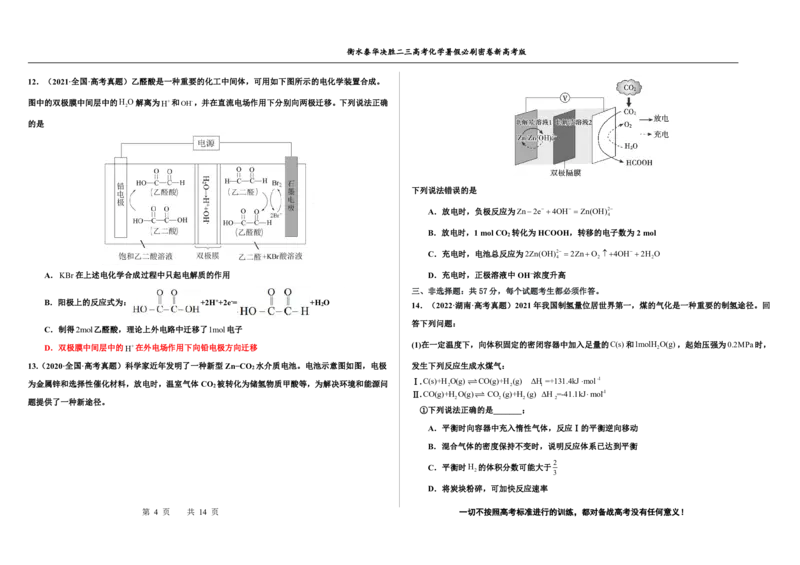
9.(2020·天津·高考真题)熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应
C.电解一段时间后阴极区溶液OH-的浓度增大
充电
为2Na+xS 放电 Na 2 S x (x=5~3,难溶于熔融硫),下列说法错 . 误 . 的是 D.CrO 3 的生成反应为:Cr 2 O 7 2+2H+=2CrO 3 +H 2 O
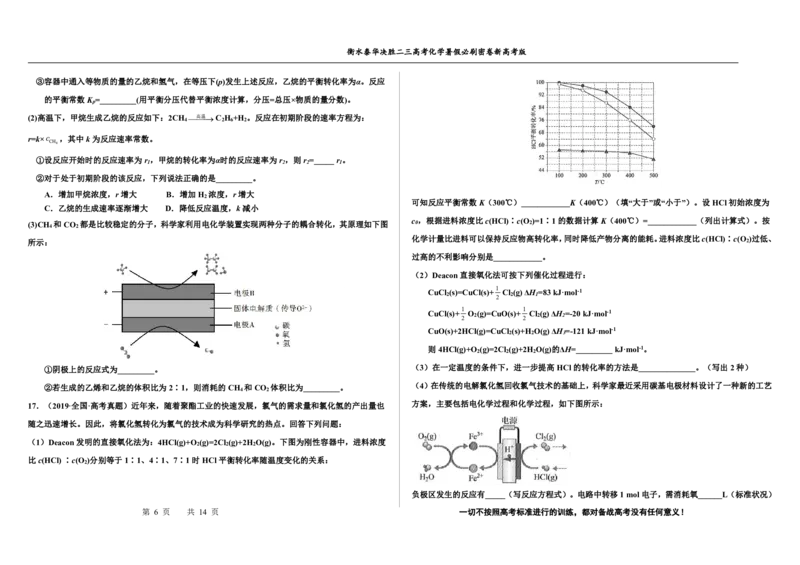
11.(2021·广东·高考真题)火星大气中含有大量CO ,一种有CO 参加反应的新型全固态电池有望为
2 2
火星探测器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生氧化反应 B.CO 在正极上得电子
2
C.阳离子由正极移向负极 D.将电能转化为化学能
A.Na S 的电子式为
2 4
B.放电时正极反应为xS+2Na++2e-=Na S
2 x
C.Na和Na Sx分别为电池的负极和正极
2
D.该电池是以Na-β-Al O 为隔膜的二次电池
2 3
第 3 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
12.(2021·全国·高考真题)乙醛酸是一种重要的化工中间体,可用如下图所示的电化学装置合成。
图中的双极膜中间层中的H O解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法正确
2
的是
下列说法错误的是
A.放电时,负极反应为Zn2e4OH Zn(OH)2
4
B.放电时,1molCO 转化为HCOOH,转移的电子数为2mol
2
C.充电时,电池总反应为2Zn(OH)2 2ZnO 4OH2H O
4 2 2
A.KBr在上述电化学合成过程中只起电解质的作用 D.充电时,正极溶液中OH−浓度升高
三、非选择题:共57分,每个试题考生都必须作答。
B.阳极上的反应式为: +2H++2e-= +H 2 O 14.(2022·湖南·高考真题)2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回
答下列问题:
C.制得2mol乙醛酸,理论上外电路中迁移了1mol电子
D.双极膜中间层中的H+在外电场作用下向铅电极方向迁移
(1)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1molH
2
O(g),起始压强为0.2MPa时,
13.(2020·全国·高考真题)科学家近年发明了一种新型Zn−CO 水介质电池。电池示意图如图,电极 发生下列反应生成水煤气:
2
为金属锌和选择性催化材料,放电时,温室气体CO
2
被转化为储氢物质甲酸等,为解决环境和能源问 Ⅰ.C(s)+H
2
O(g) CO(g)+H
2
(g) ΔH
1
=+131.4kJmol-1
Ⅱ.CO(g)+H O(g) CO (g)+H (g) ΔH =-41.1kJmol-1
2 2 2 2
题提供了一种新途径。
①下列说法正确的是_______;
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
2
C.平衡时H 的体积分数可能大于
2 3
D.将炭块粉碎,可加快反应速率
第 4 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
②反应平衡时,H O(g)的转化率为50%,CO的物质的量为0.1mol。此时,整个体系_______(填“吸 ④减压能够降低蒸馏温度,从H 2 O 2 的化学性质角度说明V中采用减压蒸馏的原因:____。
2
(2)电化学制备方法:已知反应2H O =2H O+O ↑能自发进行,反向不能自发进行,通过电解可以实现
2 2 2 2
收”或“放出”)热量_____kJ,反应Ⅰ的平衡常数K =_______(以分压表示,分压=总压×物质的量分
p
由H O和O 为原料制备H O ,如图为制备装置示意图。
2 2 2 2
数)。
(2)一种脱除和利用水煤气中CO 方法的示意图如下:
2
①a极的电极反应式是____。
②下列说法正确的是____。
①某温度下,吸收塔中K CO 溶液吸收一定量的CO 后,c
CO2-
:c
HCO-
=1:2,则该溶液的
2 3 2 3 3 A.该装置可以实现电能转化为化学能
pH=_______(该温度下H CO 的K =4.6107,K 5.01011); B.电极b连接电源负极
2 3 al a2
C.该方法相较于早期制备方法具有原料廉价,对环境友好等优点
②再生塔中产生CO 的离子方程式为_______;
2
16.(2020·全国·高考真题)天然气的主要成分为CH ,一般还含有C H 等烃类,是重要的燃料和化
4 2 6
③利用电化学原理,将CO
2
电催化还原为C
2
H
4
,阴极反应式为_______。
工原料。
15.(2020·北京·高考真题)H O 是一种重要的化学品,其合成方法不断发展。 (1)乙烷在一定条件可发生如下反应:C H (g)=C H (g)+H (g)ΔH,相关物质的燃烧热数据如下表所示:
2 2 2 6 2 4 2
(1)早期制备方法:Ba(NO 3 ) 2 加 Ⅰ 热BaO Ⅱ O2BaO 2 盐 Ⅲ 酸 除 Ⅳ 杂滤液减压 Ⅴ 蒸馏H 2 O 2 物质 C 2 H 6 (g) C 2 H 4 (g) H 2 (g)
①I为分解反应,产物除BaO、O 外,还有一种红棕色气体。该反应的化学方程式是____。
2 燃烧热ΔH/(kJ·mol−1) -1560 -1411 -286
②II为可逆反应,促进该反应正向进行的措施是____。
①ΔH=_________kJ·mol−1。
③III中生成H O ,反应的化学方程式是____。
2 2
②提高该反应平衡转化率的方法有_________、_________。
第 5 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应
的平衡常数K =_________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
p
(2)高温下,甲烷生成乙烷的反应如下:2CH 高温C H +H 。反应在初期阶段的速率方程为:
4 2 6 2
r=k×c ,其中k为反应速率常数。
CH4
①设反应开始时的反应速率为r ,甲烷的转化率为α时的反应速率为r ,则r =_____r 。
1 2 2 1
②对于处于初期阶段的该反应,下列说法正确的是_________。
A.增加甲烷浓度,r增大 B.增加H 浓度,r增大
2
可知反应平衡常数K(300℃)____________K(400℃)(填“大于”或“小于”)。设HCl初始浓度为
C.乙烷的生成速率逐渐增大 D.降低反应温度,k减小
(3)CH 和CO 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图 c 0 ,根据进料浓度比c(HCl)∶c(O 2 )=1∶1的数据计算K(400℃)=____________(列出计算式)。按
4 2
所示:
化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O
2
)过低、
过高的不利影响分别是____________。
(2)Deacon直接氧化法可按下列催化过程进行:
1
CuCl (s)=CuCl(s)+ Cl (g)ΔH =83kJ·mol-1
2 2 1
2
1 1
CuCl(s)+ O (g)=CuO(s)+ Cl (g)ΔH =-20kJ·mol-1
2 2 2
2 2
CuO(s)+2HCl(g)=CuCl (s)+H O(g)ΔH =-121kJ·mol-1
2 2 3
则4HCl(g)+O (g)=2Cl (g)+2H O(g)的ΔH=_________kJ·mol-1。
2 2 2
①阴极上的反应式为_________。 (3)在一定温度的条件下,进一步提高HCl的转化率的方法是______________。(写出2种)
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH 和CO 体积比为_________。 (4)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺
4 2
17.(2019·全国·高考真题)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也 方案,主要包括电化学过程和化学过程,如下图所示:
随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(1)Deacon发明的直接氧化法为:4HCl(g)+O (g)=2Cl (g)+2H O(g)。下图为刚性容器中,进料浓度
2 2 2
比c(HCl)∶c(O )分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
2
负极区发生的反应有_____(写反应方程式)。电路中转移1mol电子,需消耗氧______L(标准状况)
第 6 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
化学假期作业(十九)答题纸 16.(16分,每空2分)
14.(14分,每空2分)
(1)①_________。
(1)①_______;
②____________________________、___________________________。
②_______ _______, _______。
③___________________________________。
(2)①________________________;
(2)①_____________________ 。
②________________________;
②_________。
③_________________________________________。
(3)①____________________________________。
15.(12分,每空2分)
②_________。
(1)①_________________________________________。
17.(15分,除标注外每空2分)
②_________________________________________。
(1)____________。____________________________。_______________________________________。
③_________________________________________。
(2)_________ 。
④_________________________________________。
(3)_________________________________________。
(2)①_________________________________________。
(4)_______________________________________________。__________(3分)
②_________________________________________。
第 7 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
衡水泰华中学决胜高考化学暑假必刷密卷第十九套化学参考答案 综上所述,本题选D。
3.C
1.C
【分析】
【详解】
充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应(Li O +2h+=2Li++O ),
A.由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电极b是阳极, 2 2 2
则充电时总反应为Li O =2Li+O ,结合图示,充电时金属Li电极为阴极,光催化电极为阳极;则放
故A错误; 2 2 2
电时金属Li电极为负极,光催化电极为正极;据此作答。
B.放电时电极反应和充电时相反,则由放电时电极a的反应为
【详解】
NaTi PO 2e NaTi PO 2Na可知,NaCl溶液的pH不变,故B错误;
3 2 4 3 2 4 3
A.光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应
C.放电时负极反应为Na
3
Ti
2
PO
4
3
2e NaTi
2
PO
4
3
2Na,正极反应为Cl
2
2e 2Cl,反应后
和阳极反应,充电时电池的总反应为Li 2 O 2 =2Li+O 2 ,A正确;
Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,故C正确; B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电
D.充电时阳极反应为2Cl2e Cl ,阴极反应为NaTi PO 2Na2e NaTi PO ,由得 效率与光照产生的电子和空穴量有关,B正确;
2 2 4 3 3 2 4 3
C.放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
失电子守恒可知,每生成1molCl ,电极a质量理论上增加23g/mol2mol=46g,故D错误;
2
D.放电时总反应为2Li+O =Li O ,正极反应为O +2Li++2e-=Li O ,D正确;
答案选C。 2 2 2 2 2 2
答案选C。
2.D
4.C
【详解】
【分析】
A.六水合氯化镁没有自由移动的离子,不能导电,工业上通过电解熔融的无水氯化镁制取金属镁,A
碱性环境下,甲醇燃料电池总反应为:2CH OH+3O +4KOH=2K CO +6H O;N H -O 清洁燃料电池
不正确; 3 2 2 3 2 2 4 2
总反应为:N H +O =N +2H O;偏二甲肼[(CH ) NNH ]中C和N的化合价均为-2价,H元素化合价
B.接触法制硫酸时,煅烧黄铁矿只能得到二氧化硫,二氧化硫在接触室经催化氧化才能转化为三氧 2 4 2 2 2 3 2 2
为+1价,所以根据氧化还原反应原理可推知其燃料电池的总反应为:
化硫,B不正确;
(CH ) NNH +4O +4KOH=2K CO +N +6H O,据此结合原电池的工作原理分析解答。
C.在常温下铁与浓硝酸发生钝化反应,在铁表面生成一层致密的氧化物薄膜并阻止反应继续发生, 3 2 2 2 2 3 2 2
【详解】
所以可用铁质容器贮运浓硝酸,C不正确;
A.放电过程为原电池工作原理,所以钾离子均向正极移动,A错误;
D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用,若两者混用会发生归中
B.根据上述分析可知,N H -O 清洁燃料电池的产物为氮气和水,其总反应中未消耗KOH,所以KOH
反应生成氯气,不仅达不到各自预期的作用效果,还会污染环境,D正确; 2 4 2
的物质的量不变,其他两种燃料电池根据总反应可知,KOH的物质的量减小,B错误;
第 8 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
C.理论放电量与燃料的物质的量和转移电子数有关,设消耗燃料的质量均为mg,则甲醇、N H 和 极,电极A为阴极,得电子,发生还原反应,A正确;
2 4
(CH ) NNH 放电量(物质的量表达式)分别是: mg 6、 mg 4、 mg 16,通过比较 B.由电解示意图可知,电极B上Mn2+失电子转化为了MnO 2 ,电极反应式为:
3 2 2
32g/mol 32g/mol 60g/mol
2H O+Mn2+-2e-=MnO +4H+,B正确;
可知(CH ) NNH 理论放电量最大,C正确; 2 2
3 2 2
C.电极A为阴极, LiMn O 得电子,电极反应式为:2LiMn O +6e-+16H+=2Li++4Mn2++8H O,依
D.根据转移电子数守恒和总反应式可知,消耗1molO 生成的氮气的物质的量为1mol,在标准状况 2 4 2 4 2
2
据得失电子守恒,电解池总反应为:2LiMn O +4H+=2Li++Mn2++3MnO +2H O,反应生成了Mn2+,
下为22.4L,D错误; 2 4 2 2
Mn2+浓度增大,C错误;
故选C。
D.电解池总反应为:2LiMn O +4H+=2Li++Mn2++3MnO +2H O,电解结束后,可通过调节溶液pH
5.D 2 4 2 2
将锰离子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;
【分析】
答案选C。
海水中除了水,还含有大量的Na+、Cl-、Mg2+等,根据题干信息可知,装置的原理是利用惰性电极电
7.A
解海水,阳极区溶液中的Cl-会优先失电子生成Cl ,阴极区H O优先得电子生成H 和OH-,结合海
2 2 2
【分析】
水成分及电解产物分析解答。
根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为
【详解】
A.根据分析可知,阳极区海水中的Cl-会优先失去电子生成Cl 2 ,发生氧化反应,A正确;
Zn-2e-+4OH-=Zn(OH)2
4
,Ⅰ区MnO
2
为电池的正极,电极反应为MnO
2
+2e-+4H+=Mn2++2H
2
O;电池
B.设置的装置为电解池原理,根据分析知,阳极区生成的Cl 与阴极区生成的OH-在管道中会发生反 在工作过程中,由于两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可
2
应生成NaCl、NaClO和H 2 O,其中NaClO具有强氧化性,可氧化灭杀附着的生物,B正确; 以通过阴、阳离子,因此可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO2向
4
C.因为H 是易燃性气体,所以阴极区生成的H 需及时通风稀释,安全地排入大气,以排除安全隐
2 2
Ⅱ区移动,Ⅲ区消耗OH-,生成Zn(OH)2,Ⅱ区的SO2向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此
4 4
患,C正确;
分析答题。
D.阴极的电极反应式为:2H O+2e-=H ↑+2OH-,会使海水中的Mg2+沉淀积垢,所以阴极表面会形成
2 2
【详解】
Mg(OH) 等积垢需定期清理,D错误。
2
A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
故选D。
6.C
B.根据分析,Ⅰ区的SO2
4
向Ⅱ区移动,B正确;
【详解】 C.MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
A.由电解示意图可知,电极B上Mn2+转化为了MnO 2 ,锰元素化合价升高,失电子,则电极B为阳 D.电池的总反应为Zn+4OH-+MnO +4H+=Zn(OH)2+Mn2++2H O,D正确;
2 4 2
第 9 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
故答案选A。
D.放电时,该电池是以钠作负极,硫作正极的原电池,充电时,是电解池,Na-β-Al O 为隔膜,起
2 3
8.B
到电解质溶液的作用,该电池为二次电池,故D正确;
【分析】
答案选C。
锂海水电池的总反应为2Li+2H O═2LiOH+H ↑, M极上Li失去电子发生氧化反应,则M电极为负
2 2 10.A
极,电极反应为Li-e-=Li+,N极为正极,电极反应为2H O+2e-=2OH-+H ↑,同时氧气也可以在N极得
2 2 【分析】
电子,电极反应为O +4e-+2H O=4OH-。
2 2
根据左侧电极上生成O ,右侧电极上生成H ,知左侧电极为阳极,发生反应:2H O4e═4HO ,
2 2 2 2
【详解】
A.海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶液,故A正确;
右侧电极为阴极,发生反应:2H
2
O2e═2OHH
2
;由题意知,左室中Na
2
Cr
2
O
7
随着H浓度增
B.由上述分析可知,N为正极,电极反应为2H 2 O+2e-=2OH-+H 2 ↑,和反应O 2 +4e-+2H 2 O=4OH-,故B 大转化为CrO :CrO22H═2CrO H O,因此阳极生成的H不能通过离子交换膜。
3 2 7 3 2
错误;
【详解】
C.Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传导离子,故C正确;
A.由以上分析知,电解时通过离子交换膜的是Na,A项错误;
D.该电池不可充电,属于一次电池,故D正确;
B.根据各电极上转移电子数相同,由阳极反应和阴极反应,知生成O 和H 的物质的量之比为1∶2,
2 2
答案选B。
其质量比为8∶1,B项正确;
9.C
C.根据阴极反应知,电解一段时间后阴极区溶液OH的浓度增大,C项正确:
【分析】
充电 D.电解过程中阳极区H的浓度增大,Na CrO 转化为CrO :CrO22H═2CrO H O,D项正确。
根据电池反应:2Na+xSNa S 可知,放电时,钠作负极,发生氧化反应,电极反应为:Na-e-=Na+, 2 2 2 3 2 7 3 2
2 x
放电
故选A。
硫作正极,发生还原反应,电极反应为xS+2Na++2e-=Na S ,据此分析。
2 x
11.AB
【详解】
【详解】
A.Na 2 S 4 属于离子化合物,4个硫原子间形成三对共用电子对,电子式为 , 根据题干信息可知,放电时总反应为4Na+3CO =2Na CO +C。
2 2 3
故A正确; A.放电时负极上Na发生氧化反应失去电子生成Na+,故A正确;
B.放电时发生的是原电池反应,正极发生还原反应,电极反应为:xS+2Na++2e-=Na S ,故B正确;
B.放电时正极为CO
2
得到电子生成C,故B正确;
2 x
C.放电时阳离子移向还原电极,即阳离子由负极移向正极,故C错误;
C.放电时,Na为电池的负极,正极为硫单质,故C错误;
D.放电时装置为原电池,能量转化关系为化学能转化为电能和化学能等,故D错误;
第 10 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
综上所述,符合题意的为B项,故答案为B。 数为2mol,故B正确,不选;
12.D
C.充电时,阳极上H O转化为O ,负极上Zn(OH)2-转化为Zn,电池总反应为:
2 2 4
【分析】
2Zn(OH)2-=2Zn+O +4OH-+2H O ,故C正确,不选;
4 2 2
该装置通电时,乙二酸被还原为乙醛酸,因此铅电极为电解池阴极,石墨电极为电解池阳极,阳极上
Br-被氧化为Br 2 ,Br 2 将乙二醛氧化为乙醛酸,双极膜中间层的H+在直流电场作用下移向阴极,OH-
D.充电时,正极即为阳极,电极反应式为:2H
2
O-4e-=4H++O
2
,溶液中H+浓度增大,溶液中
移向阳极。 c(H+)•c(OH-)=K ,温度不变时,K 不变,因此溶液中OH-浓度降低,故D错误,符合题意;
W W
【详解】 答案选D。
A.KBr在上述电化学合成过程中除作电解质外,同时还是电解过程中阳极的反应物,生成的Br 为
2
14【答案】(1) BD 吸收 31.2 0.02MPa
乙二醛制备乙醛酸的中间产物,故A错误;
Δ
B.阳极上为Br-失去电子生成Br 2 ,Br 2 将乙二醛氧化为乙醛酸,故B错误; (2) 10 2HCO 3 - CO 2 ↑+CO 3 2-+H 2 O 2CO 2 +12e-+12H+=C 2 H 4 +4H 2 O
C.电解过程中阴阳极均生成乙醛酸,1mol乙二酸生成1mol乙醛酸转移电子为2mol,1mol乙二醛生 【解析】
成1mol乙醛酸转移电子为2mol,根据转移电子守恒可知每生成1mol乙醛酸转移电子为1mol,因此 (1)
制得2mol乙醛酸时,理论上外电路中迁移了2mol电子,故C错误; ①A.在恒温恒容条件下,平衡时向容器中充入情性气体不能改变反应混合物的浓度,因此反应Ⅰ的
D.由上述分析可知,双极膜中间层的H+在外电场作用下移向阴极,即H+移向铅电极,故D正确; 平衡不移动,A说法不正确;
综上所述,说法正确的是D项,故答案为D。 B.在反应中有固体C转化为气体,气体的质量增加,而容器的体积不变,因此气体的密度在反应过
13.D 程中不断增大,当混合气体的密度保持不变时,说明反应体系已达到平衡,B说法正确;
【分析】 C.若C(s)和H O(g)完全反应全部转化为CO (g)和H (g),由C(s)+2H O(g)=CO (g)+2H (g)可知,
2 2 2 2 2 2
由题可知,放电时,CO
2
转化为HCOOH,即CO
2
发生还原反应,故放电时右侧电极为正极,左侧电
H 的体积分数的极值为
2
,由于可逆反应只有一定的限度,反应物不可能全部转化为生成物,因此,
2
3
极为负极,Zn发生氧化反应生成Zn(OH)2
4
-;充电时,右侧为阳极,H
2
O发生氧化反应生成O
2
,左侧
平衡时H 的体积分数不可能大于 2 ,C说法不正确;
2
3
为阴极,Zn(OH)2
4
-发生还原反应生成Zn,以此分析解答。
D.将炭块粉碎可以增大其与H 2 O(g)的接触面积,因此可加快反应速率,D说法正确;
【详解】 综上所述,相关说法正确的是BD。
A.放电时,负极上Zn发生氧化反应,电极反应式为:Zn-2e-+4OH-=Zn(OH)2- ,故A正确,不选;
②反应平衡时,H
2
O(g)的转化率为50%,则水的变化量为0.5mol,水的平衡量也是0.5mol,由于CO
4
的物质的量为0.1mol,则根据O原子守恒可知CO 的物质的量为0.2mol,生成0.2molCO 时消耗了
B.放电时,CO 转化为HCOOH,C元素化合价降低2,则1molCO 转化为HCOOH时,转移电子 2 2
2 2
第 11 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
0.2molCO,故在反应Ⅰ实际生成了0.3molCO。根据相关反应的热化学方程式可知,生成0.3molCO (1)根据流程图示,硝酸钡受热分解,生成氧化钡、氧气和二氧化氮,氧化钡与氧气反应生成过氧化钡,
要吸收热量39.42kJ ,生成0.2molCO 要放出热量8.22kJ此时,因此整个体系吸收热量 过氧化钡与盐酸反应生成氯化钡和双氧水,向反应后的溶液中加入试剂除去钡离子,过滤后对滤液进
2
39.42kJ-8.22kJ=31.2kJ;由H原子守恒可知,平衡时H 的物质的量为0.5mol,CO的物质的量为0.1mol, 行减压蒸馏,得到双氧水,据此分析解答;
2
CO 的物质的量为0.2mol,水的物质的量为0.5mol,则平衡时气体的总物质的量为 (2)根据图示,左端电极上氧气转化为双氧水,氧元素的化合价由0价变为-1价,得电子发生还原反应,
2
0.5mol+0.1mol+0.2mol+0.5mol=1.3mol,在同温同体积条件下,气体的总压之比等于气体的总物质的量 则a电极为阴极,电极反应为O +2H++2e-=H O ,b电极为阳极,失电子发生氧化反应,电极反应为
2 2 2
之比,则平衡体系的总压为0.2MPa1.3=0.26MPa,反应I(C(s)+H
2
O(g) CO(g)+H
2
(g))的平衡 2H
2
O-4e-=4H++O
2
↑,据此分析解答。
0.1 0.5 【详解】
1.3 1.3 0.1
常数K p = 0.5 P 总 1.3 0.26MPa 0.02MPa 。 (1)①I为分解反应,产物除BaO、O 2 外,还有一种红棕色气体,该气体为NO 2 。根据氧化还原反应电
1.3
加热
子得失守恒配平该反应的化学方程式为:2Ba(NO ) 2BaO+O ↑+4NO ↑;
3 2 2 2
(2)
②II为BaO与氧气反应生成BaO ,是可逆反应,反应方程式为:2BaO(s)+O (g)2BaO (s),正反应
2 2 2
c(CO2)c(H)
①某温度下,吸收塔中K 2 CO 3 溶液吸收一定量的CO 2 后,c(CO 3 2):c(HCO 3 )=1:2,由K a2 c(H 3 CO) 为气体体积减小的放热反应,促进该反应正向进行的措施是增大压强或增大氧气的浓度或降低温度;
3
③III中过氧化钡与盐酸反应生成氯化钡和双氧水,反应的化学方程式是BaO +2HCl=BaCl +H O ;
2 2 2 2
c(HCO-)
可知,c(H)=
c(CO2-
3
)
K
a2
25.010-11molL-1 1.010-10molL-1,则该溶液的pH=10;
④H 2 O 2 受热易分解,采用减压能够降低蒸馏温度,防止双氧水分解导致产率降低;
3
(2)①根据分析,a极的电极反应式是O +2H++2e-=H O ;
②再生塔中KHCO 受热分解生成K CO 、H O和CO ,该反应的离子方程式为 2 2 2
3 2 3 2 2
Δ ②A.2H 2 O 2 =2H 2 O+O 2 ↑能自发进行,反向不能自发进行,根据图示,该装置有电源,属于电解池,电
2HCO- CO ↑+CO2-+H O;
3 2 3 2
解池是将电能转化为化学能的装置,故A正确;
③利用电化学原理,将CO 电催化还原为C H ,阴极上发生还原反应,阳极上水放电生成氧气和H+,
2 2 4 B.根据分析,电极b为阳极,电解池阳极与电源正极连接,故B错误;
H+通过质子交换膜迁移到阴极区参与反应生成乙烯,铂电极和Ag/AgCl电极均为阴极,在电解过程中
C.根据分析,该装置的总反应为2H O+O 电解 2H O ,根据反应可知,制取双氧水的原料为氧气和水,
2 2 2 2
AgCl可以转化为Ag,则阴极的电极反应式为2CO +12e-+12H+=C H +4H O
2 2 4 2
来源广泛,原料廉价,对环境友好等优点,故C正确;
加热
15【答案】 2Ba(NO ) 2BaO+O ↑+4NO ↑ 增大压强或增大氧气的浓度或降低温
3 2 2 2
答案选AC。
度 BaO +2HCl=BaCl +H O H O 受热易分解 O +2H++2e-=H O AC
2 2 2 2 2 2 2 2 2 【点睛】
【解析】
易错点为(1)中的④,H O 受热易分解,减压能够降低蒸馏温度,减小双氧水的分解,提高双氧水的产
2 2
【分析】
率。
第 12 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
16【答案】 +137 升高温度 减小压强(增大体积) ③设起始时加入的乙烷和氢气各为1mol,列出三段式,
α(1+α)
p (1-α) AD CO +2e−=CO+O2− 6∶5 C 2 H 6 (g) C 2 H 4 (g)+H 2 (g)
(2+α)(1-α) 2
【解析】 起始(mol) 1 0 1
【分析】
转化(mol) α
(1)①先写出三种气体的燃烧热的热化学方程式,然后根据盖斯定律进行计算,得到目标反应的∆H;
α α
平衡(mol) 1-α α 1+α
②反应C H (g) C H (g)+H (g)为气体体积增大的吸热反应,升高温度、减小压强平衡等都向正反
2 6 2 4 2
1α α 1α
应方向移动; 平衡时,C 2 H 6 、C 2 H 4 和H 2 平衡分压分别为 p、 p和 p,则反应的平衡常数为
2α 2α 2α
③根据已知乙烷的转化率,设起始时加入的乙烷和氢气各为1mol,列出三段式,求出平衡时各物质的
K =
(1α)
;
p(2α)(1α)
分压,带入平衡常数的计算公式进行计算;
(2)①根据r=k×c ,若r =kc,甲烷转化率为α时,甲烷的浓度为c(1-α),则r =kc(1-α),所以r =(1-α)r ;
CH4 1 2 2 1
(2)①根据r=k×c ,若r =kc,甲烷转化率为α时,甲烷的浓度为c(1-α),则r =kc(1-α);
CH4 1 2
②A.增大反应物浓度反应速率增大,故A说法正确;
②根据反应初期的速率方程为:r=k×c
CH4
,其中k为反应速率常数,据此分析速率变化的影响因素;
B.由速率方程可知,初期阶段的反应速率与氢气浓度无关,故B说法错误;
(3)①由图可知,CO 在阴极得电子发生还原反应,电解质传到O2-,据此写出电极反应; C.反应物甲烷的浓度逐渐减小,结合速率方程可知,乙烷的生成速率逐渐减小,故C说法错误;
2
②令生成乙烯和乙烷分别为2体积和1体积,根据阿伏加德罗定律,同温同压下,气体体积比等于物 D.化学反应速率与温度有关,温度降低,反应速率常数减小,故D正确。
质的量之比,再根据得失电子守恒,得到发生的总反应,进而计算出为消耗CH 和CO 的体积比。 答案选AD。
4 2
【详解】 (3)①由图可知,CO 在阴极得电子发生还原反应,电极反应为CO +2e-=CO+O2-;
2 2
(1)①由表中燃烧热数值可知: ②令生成乙烯和乙烷分别为2体积和1体积,根据阿伏加德罗定律,同温同压下,气体体积比等于物
①C H (g)+ 7 O (g) O (g)+3H O(l)∆H =-1560kJ∙mol-1;②C H (g)+3O (g) O (g)+2H O(l)∆H = 质的量之比,再根据得失电子守恒,得到发生的总反应为:6CH 4 +5CO 2 =2C 2 H 4 +C 2 H 6 +5H 2 O+5CO,
2 6 2 2 2 1 2 4 2 2 2 2
2
=2C =2C
即消耗CH
4
和CO
2
的体积比为6:5。故答案为:6:5。
1
-1411kJ∙mol-1;③H (g)+ O (g) H O(l)∆H =-286kJ∙mol-1;根据盖斯定律可知,①-②-③得C H (g)
2 2 2 3 2 6
2 (0.42)2(0.42)2
17【答案】 大于 O 和Cl 分离能耗较高、HCl转化率较低 ﹣116 增
= (10.84)4(10.21)c 2 2
C H (g)+H (g),则∆H=∆H -∆H -∆H =(-1560kJ∙mol-1)-(-1411kJ∙mol-1)-(-286kJ∙mol-1)=137kJ∙mol-1, 0
2 4 2 1 2 3
加反应体系压强、及时除去产物 Fe3++e−=Fe2+,4Fe2++O +4H+=4Fe3++2H O 5.6
=故答案为137; 2 2
【解析】
②反应C H (g) C H (g)+H (g)为气体体积增大的吸热反应,升高温度、减小压强平衡都向正反应
2 6 2 4 2
【详解】
方向移动,故提高该反应平衡转化率的方法有升高温度、减小压强(增大体积);
第 13 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!衡水泰华决胜二三高考化学暑假必刷密卷新高考版
(1)根据反应方程式知,HCl平衡转化率越大,平衡常数K越大,结合图像知升高温度平衡转化率
降低,说明升高温度平衡向逆反应方向进行,则K(300℃)>K(400℃);
第( )套化学暑假必刷密卷专用反思表
由图像知,400℃时,HCl平衡转化率为84%,用三段式法对数据进行处理得:
填表时间:2022 年__月___日,__:__;反思人:___________家长签字:_____________
4HCl(g)O (g)2Cl (g)2H O(g) 本套暴露的主要问题
2 2 2
板块 该板块失分 对每一分失分的原因反思
起始(浓度) c c 0 0
0 0
单项选 总分27 分
变化(浓度) 0.84c 0.21c 0.42c 0.42c 择题 丢了( )分
0 0 0 0
双选题 总分16 分
平衡(浓度)(1-0.84)c (1-0.21)c 0.42c 0.42c 丢了( )分
0 0 0 0
主观题 总分57 分
(0.42)2(0.42)2
则K= ;根据题干信息知,进料浓度比过低,氧气大量剩余,导致分离产物氯气和 丢了( )分
(10.84)4(10.21)c
0
本套题的主要收获
氧气的能耗较高;进料浓度比过高,HCl不能充分反应,导致HCl转化率较低;
知识上
的收获
(2)根据盖斯定律知,(反应I+反应II+反应III)×2得4HCl(g)O (g)2Cl (g)2H O(g) ∆H=
2 2 2
(∆H +∆H +∆H )×2=-116kJ·mol-1; 技巧上
1 2 3
的收获
(3)若想提高HCl的转化率,应该促使平衡正向移动,该反应为气体体积减小的反应,根据勒夏特
本套题的综合反思
列原理,可以增大压强,使平衡正向移动;也可以及时除去产物,减小产物浓度,使平衡正向移动; 做题状
态
(4)电解过程中,负极区即阴极上发生的是得电子反应,元素化合价降低,属于还原反应,则图中左
做题结
侧为负极反应,根据图示信息知电极反应为:Fe3++e-=Fe2+和4Fe2++O +4H+=4Fe3++2H O;电路中转 果
2 2
自我提
移1mol电子,根据电子得失守恒可知需消耗氧气的物质的量是1mol÷4=0.25mol,在标准状况下的体
醒
积为0.25mol×22.4L/mol=5.6L。
第 14 页 共 14 页 一切不按照高考标准进行的训练,都对备战高考没有任何意义!