文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题13
1.溶液中存在Na+、SO Cl-、NH、SO,加入某物质后既产生了白色沉淀,又产生了无色刺激
、
性气体,该物质可以是
A. FeCl B. KHSO C. CaO D. Ba(NO )
3 4 3 2
答案:C
解析:A.FeCl 加入,铁离子和亚硫酸根反应生成亚铁离子和硫酸根,没有沉淀,也没有气体
3
生成,故A不符合题意;
B.KHSO 加入,氢离子与亚硫酸根反应生成二氧化硫气体和水,没有白色沉淀生成,故B不
4
符合题意;
C.CaO加入,可以理解氧化钙和水反应生成氢氧化钙,氢氧化钙和硫酸根生成硫酸钙白色沉
淀,和铵根反应生成氨气,故C符合题意;
D.Ba(NO ) 加入生成硫酸钡、亚硫酸钡白色沉淀,没有气体放出,故D不符合题意。
3 2
2. 25℃时,下列各组离子在指定溶液中一定能大量共存的是
A. pH=1的溶液中:Na+、NH、[Ag(NH)]+、NO
3 2
B. 麦芽糖溶液中:MnO Na+、SO、H+
、
C. 澄清透明的溶液中:Cu2+、Al3+、SO、NO
D. 能使甲基橙变为红色的溶液中:Fe2+、K+、Cl-、NO
答案:C
解析:A.酸性溶液中银氨离子[Ag(NH)]+不能存在,A错误;
3 2
B.麦芽糖具有还原性,与MnO H+发生氧化还原反应,不能存在,B错误;
、
C.澄清透明溶液中几种离子可以共存,C正确;
D.能使甲基橙变为红色的溶液为酸性溶液,亚铁离子和硝酸根在酸性环境下发生氧化还原反
应,不能共存,D错误;
3.下列各组粒子在水溶液中能大量共存的是。
A. NH、CHCOO-、HCO NO B. Fe3+、ClO-、Na+、SO
3 、
C. Fe2+、Al3+、[Fe(CN) ]3-、Cl- D. Ag+、K+、NH 、NO
6 3
答案:A
解析:A.铵根离子和碳酸氢根离子发生双水解反应的程度很小,可以共存,A符合题意;
B.Fe3+和ClO-在碱性条件下可以发生反应生成Cl-和高铁酸根,不能共存,B不符合题意;
C.亚铁离子和[Fe(CN) ]3-反应生成蓝色沉淀,不能共存,C不符合题意;
6
D.氨气的水溶液显碱性,能和银离子反应,不能共存,D不符合题意;
4. 能正确表示下列反应的离子方程式的是
A. 小苏打溶液与过量盐酸混合:CO +=CO↑+H O
+2H 2 2
B. 用铁电极电解饱和食盐水:2C1-+2H O=====Cl↑+H ↑+2OH-
2 2 2
C. Fe(NO ) 溶液中通入足量SO :Fe3++3NO +4H O=Fe2++3NO↑+5SO +8H+
3 3 2 +5SO2 2 3D. 硫酸铜溶液中加入过量氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
3 2 2
答案:C
解析:A.小苏打为碳酸氢钠,离子方程式为:HCO +=CO ↑+H O,故A错误;
+H 2 2
B.铁作阳极时铁失电子,则电解反应为:Fe+2H O=====H↑+Fe(OH) ,故B错误;
2 2 2
C.Fe(NO ) 溶液中通入二氧化硫,溶液显酸性,NO
3 3 表现强氧化性,能将二氧化硫氧化成硫酸根离子,同时二氧化硫也能将
C正确;
铁离子还原为亚铁离子,离子方程式正确,故
D.硫酸铜溶液中加入过量氨水,形成配合物:Cu2++4NH·H O=[Cu(NH )]2++4 H O,故D错
3 2 3 4 2
误;
5.下列离子方程式中,正确的是
A.金属钠投入水中:Na+HO=Na++OH-+H ↑
2 2
B.铁氰化钾溶液检验亚铁离子时生成了蓝色沉淀:3Fe2++2[Fe(CN)]3-=Fe [Fe(CN) ]↓
6 3 6 2
C.等体积等物质的量浓度的NH HSO 溶液与NaOH溶液混合:NH+OH-=NH ·H O
4 4 3 2
D.KClO碱性溶液与Fe(OH) 反应制备高铁酸钾:3ClO-+2Fe(OH) =2FeO+3Cl-+4H++H O
3 3 2
答案:B
解析:A.金属钠投入水中:2Na+2HO=2Na++2OH-+H ↑,故A错误;
2 2
B.铁氰化钾溶液检验亚铁离子时生成了蓝色沉淀:3Fe2++2[Fe(CN)]3-=Fe [Fe(CN) ]↓,故B
6 3 6 2
正确;
C.等体积等物质的量浓度的NH HSO 溶液与NaOH溶液混合,NaOH先与氢离子反应:H+
4 4
+OH-=H O,故C错误;
2
D.KClO碱性溶液与Fe(OH) 反应制备高铁酸钾:3ClO-+2Fe(OH) +4OH-=2 FeO+3Cl-
3 3
+5H O,故D错误;
2
6.下列离子反应方程式书写正确的是
A.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++HO
2
B.漂白粉溶液中通入少量SO :Ca2++2ClO-+SO +HO=CaSO↓+2HClO
2 2 2 3
C.电解饱和食盐水:2Cl-+2H+=====Cl↑+H↑
2 2
D.Al溶于NaOH溶液:2Al+2OH-+2HO=2AlO+3H↑
2 2
答案:D
解析:A项硝酸具有强氧化性,FeO会被氧化成Fe3+,A项错误;B项CaSO 和HClO会继续
3
反应生成CaSO,B项错误;C项水不可拆,C项错误;D项Al和NaOH反应,D项正确;答案选
4
D。
7.现有下列实验探究摩尔盐[(NH )Fe(SO )∙6HO]的化学性质。
4 2 4 2 2
实
装置 试剂a 现象
验
① 紫色石蕊溶液 溶液变红色
② BaCl 溶液 产生白色沉淀
2③ 稀硝酸溶液 溶液变黄色
④ 浓NaOH溶液 产生具有刺激性气味的气体
下列离子方程式不能准确解释相应实验现象的是
A.①中溶液变红:NH+HO NH ∙HO+H+、Fe2++2HO Fe(OH) +2H+
2 3 2 2 2
B.②中产生白色沉淀:Ba2++SO=BaSO↓
4
C.③中溶液变黄:Fe2++NO +=Fe3++NO ↑+HO
+2H 2 2
D.④中产生有刺激性气体:NH+OH-=NH ↑+HO
3 2
答案:C
解析:A.铵根离子、亚铁离子水解使得溶液显酸性,酸性溶液使紫色石蕊试液变红色,能准
确解释相应实验现象,A不符合题意;
B.硫酸根离子和钡离子生成硫酸钡白色沉淀,能准确解释相应实验现象,B不符合题意;
C.亚铁离子和硝酸根离子生成铁离子和一氧化氮气体,3Fe2++NO +=3Fe3++NO↑+2HO,
+4H 2
不能准确解释相应实验现象,C符合题意;
D.铵根离子和氢氧根离子生成刺激性气体氨气,能准确解释相应实验现象,D不符合题意;
8.下列指定反应的离子方程式书写正确的是
A.NO 通入NaOH浓溶液中:2NO +2OH-=NO+NO HO
2 2 + 2
B.(CHCOO) Pb溶液中滴入稀硫酸:Pb2++SO=PbSO ↓
3 2 4
C.NaAlO 溶液中加入少量盐酸:AlO+4H+=Al3++2HO
2 2
D.NH HSO 溶液中加入少量Ba(OH) 溶液:HSO Ba2++OH-=BaSO↓+HO
4 3 2 + 3 2
答案:A
解析:A.NO 通入NaOH浓溶液中,发生歧化反应,生成NaNO 、NaNO 和水,反应的离子
2 2 3
方程式为:2NO +2OH-=NO+NO HO,A正确;
2 + 2
B.(CHCOO) Pb溶液中滴入稀硫酸,醋酸铅和醋酸都是弱电解质,不能拆开,反应的离子方
3 2
程式为:Pb(CH COO) +2H++SO=PbSO ↓+2CH COOH,B不正确;
3 2 4 3
C.NaAlO 溶液中加入少量盐酸,生成Al(OH) 等,离子方程式为:AlO+H++H O=Al(OH) ↓
2 3 2 3
,C不正确;
D.NH HSO 溶液中加入少量Ba(OH) 溶液:2HSO Ba2++2OH-=BaSO↓+2HO+SO
4 3 2 + 3 2 ,D不正确;
9.高铁酸钾(K FeO)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶
2 4
于浓KOH溶液,且能与水反应放出氧气,并生成Fe(OH) 胶体,常用作水处理剂。高铁酸钾有强
3
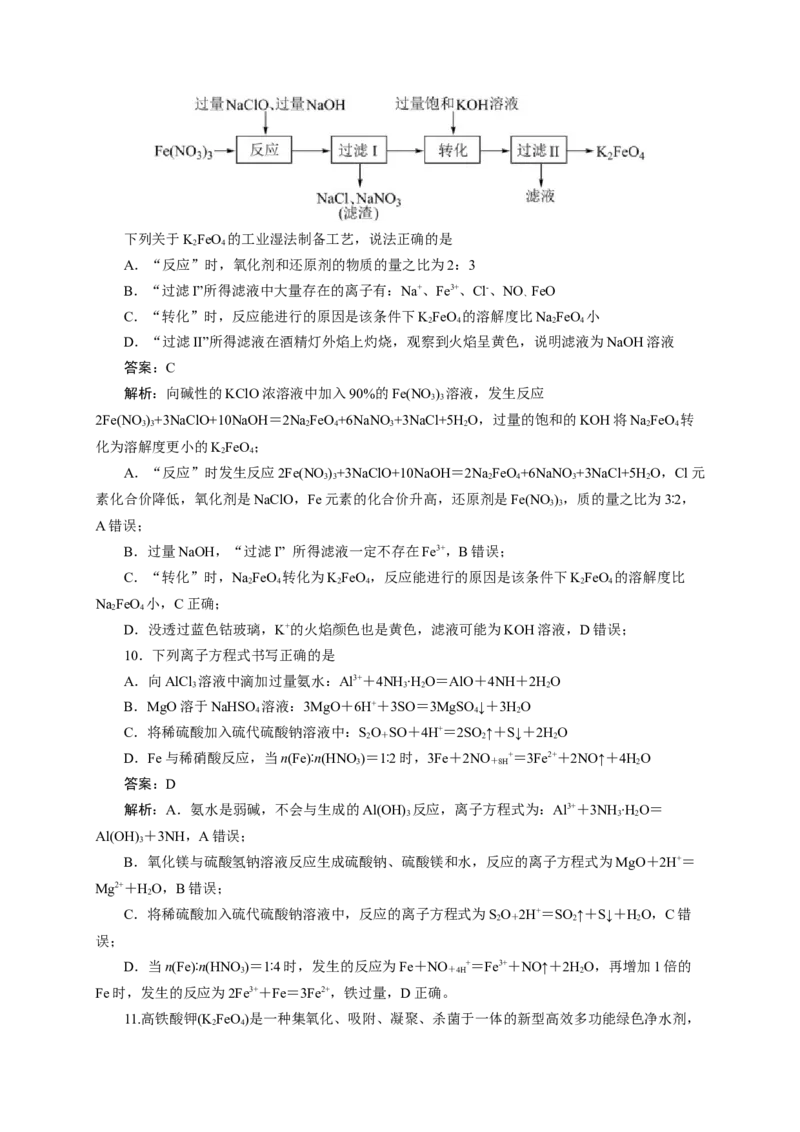
氧化性,酸性条件下,其氧化性强于Cl、KMnO 等。工业上湿法制备KFeO 的流程如下:
2 4 2 4下列关于KFeO 的工业湿法制备工艺,说法正确的是
2 4
A.“反应”时,氧化剂和还原剂的物质的量之比为2:3
B.“过滤I”所得滤液中大量存在的离子有:Na+、Fe3+、Cl-、NO FeO
、
C.“转化”时,反应能进行的原因是该条件下KFeO 的溶解度比NaFeO 小
2 4 2 4
D.“过滤II”所得滤液在酒精灯外焰上灼烧,观察到火焰呈黄色,说明滤液为NaOH溶液
答案:C
解析:向碱性的KClO浓溶液中加入90%的Fe(NO ) 溶液,发生反应
3 3
2Fe(NO )+3NaClO+10NaOH=2NaFeO+6NaNO +3NaCl+5HO,过量的饱和的KOH将NaFeO 转
3 3 2 4 3 2 2 4
化为溶解度更小的KFeO;
2 4
A.“反应”时发生反应2Fe(NO )+3NaClO+10NaOH=2NaFeO+6NaNO +3NaCl+5HO,Cl元
3 3 2 4 3 2
素化合价降低,氧化剂是NaClO,Fe元素的化合价升高,还原剂是Fe(NO ),质的量之比为3∶2,
3 3
A错误;
B.过量NaOH,“过滤I” 所得滤液一定不存在Fe3+,B错误;
C.“转化”时,NaFeO 转化为KFeO,反应能进行的原因是该条件下KFeO 的溶解度比
2 4 2 4 2 4
NaFeO 小,C正确;
2 4
D.没透过蓝色钴玻璃,K+的火焰颜色也是黄色,滤液可能为KOH溶液,D错误;
10.下列离子方程式书写正确的是
A.向AlCl 溶液中滴加过量氨水:Al3++4NH ∙HO=AlO+4NH+2HO
3 3 2 2
B.MgO溶于NaHSO 溶液:3MgO+6H++3SO=3MgSO ↓+3HO
4 4 2
C.将稀硫酸加入硫代硫酸钠溶液中:SO SO+4H+=2SO ↑+S↓+2HO
2 + 2 2
D.Fe与稀硝酸反应,当n(Fe)∶n(HNO)=1∶2时,3Fe+2NO +=3Fe2++2NO↑+4HO
3 +8H 2
答案:D
解析:A.氨水是弱碱,不会与生成的Al(OH) 反应,离子方程式为:Al3++3NH ∙HO=
3 3 2
Al(OH) +3NH,A错误;
3
B.氧化镁与硫酸氢钠溶液反应生成硫酸钠、硫酸镁和水,反应的离子方程式为MgO+2H+=
Mg2++HO,B错误;
2
C.将稀硫酸加入硫代硫酸钠溶液中,反应的离子方程式为SO 2H+=SO ↑+S↓+HO,C错
2 + 2 2
误;
D.当n(Fe)∶n(HNO)=1∶4时,发生的反应为Fe+NO +=Fe3++NO↑+2HO,再增加1倍的
3 +4H 2
Fe时,发生的反应为2Fe3++Fe=3Fe2+,铁过量,D正确。
11.高铁酸钾(K FeO)是一种集氧化、吸附、凝聚、杀菌于一体的新型高效多功能绿色净水剂,
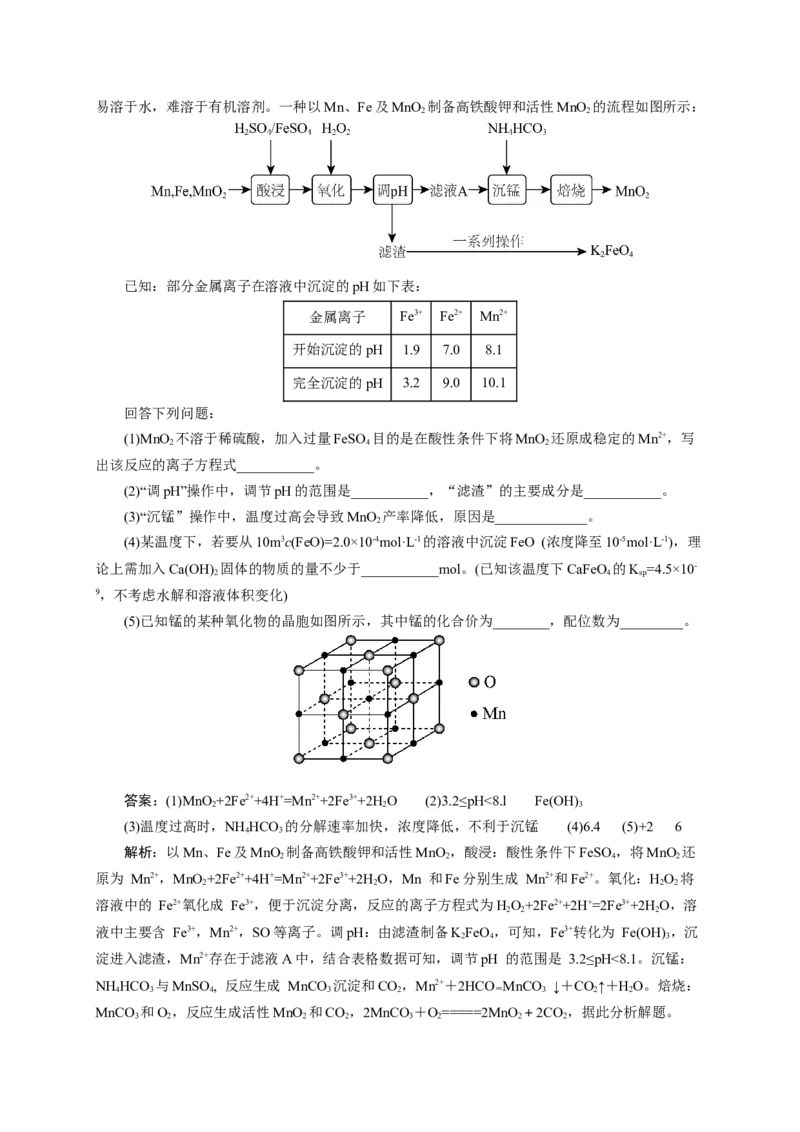
2 4易溶于水,难溶于有机溶剂。一种以Mn、Fe及MnO 制备高铁酸钾和活性MnO 的流程如图所示:
2 2
已知:部分金属离子在溶液中沉淀的pH如下表:
金属离子 Fe3+ Fe2+ Mn2+
开始沉淀的pH 1.9 7.0 8.1
完全沉淀的pH 3.2 9.0 10.1
回答下列问题:
(1)MnO 不溶于稀硫酸,加入过量FeSO 目的是在酸性条件下将MnO 还原成稳定的Mn2+,写
2 4 2
出该反应的离子方程式___________。
(2)“调pH”操作中,调节pH的范围是___________,“滤渣”的主要成分是___________。
(3)“沉锰”操作中,温度过高会导致MnO 产率降低,原因是_____________。
2
(4)某温度下,若要从10m3c(FeO)=2.0×10-4mol·L-1的溶液中沉淀FeO (浓度降至10-5mol·L-1),理
论上需加入Ca(OH) 固体的物质的量不少于___________mol。(已知该温度下CaFeO 的K =4.5×10-
2 4 sp
9,不考虑水解和溶液体积变化)
(5)已知锰的某种氧化物的晶胞如图所示,其中锰的化合价为________,配位数为_________。
答案:(1)MnO +2Fe2++4H+=Mn2++2Fe3++2H O (2)3.2≤pH<8.l Fe(OH)
2 2 3
(3)温度过高时,NH HCO 的分解速率加快,浓度降低,不利于沉锰 (4)6.4 (5)+2 6
4 3
解析:以Mn、Fe及MnO 制备高铁酸钾和活性MnO ,酸浸:酸性条件下FeSO ,将MnO 还
2 2 4 2
原为 Mn2+,MnO +2Fe2++4H+=Mn2++2Fe3++2H O,Mn 和Fe分别生成 Mn2+和Fe2+。氧化:HO 将
2 2 2 2
溶液中的 Fe2+氧化成 Fe3+,便于沉淀分离,反应的离子方程式为HO+2Fe2++2H+=2Fe3++2H O,溶
2 2 2
液中主要含 Fe3+,Mn2+,SO等离子。调pH:由滤渣制备KFeO,可知,Fe3+转化为 Fe(OH) ,沉
2 4 3
淀进入滤渣,Mn2+存在于滤液A中,结合表格数据可知,调节pH 的范围是 3.2≤pH<8.1。沉锰:
NH HCO 与MnSO , 反应生成 MnCO 沉淀和CO,Mn2++2HCO MnCO ↓+CO↑+HO。焙烧:
4 3 4 3 2 = 3 2 2
MnCO 和O,反应生成活性MnO 和CO,2MnCO +O=====2MnO +2CO,据此分析解题。
3 2 2 2 3 2 2 2(1)酸性条件下FeSO ,将MnO 还原为 Mn2+,离子方程式为MnO +2Fe2++4H+=Mn2++2Fe3++
4 2 2
2HO,故答案为MnO +2Fe2++4H+=Mn2++2Fe3++2H O。
2 2 2
(2)由滤渣制备KFeO,可知,Fe3+转化为 Fe(OH) ,沉淀进入滤渣,Mn2+存在于滤液A中,结
2 4 3
合表格数据可知,调节pH 的范围是 3.2≤pH<8.1,故答案为3.2≤pH<8.1;Fe(OH) 。
3
(3)NH HCO 受热易分解,当温度高于 60℃,会加速NH HCO 的分解,导致MnO 产率降低,
4 3 4 3 2
故答案为温度过高时,NH HCO 的分解速率加快,浓度降低,不利于沉锰。
4 3
(4)若要将溶液中FeO的浓度从2.0×10-4mol·L-1降至10-5mol·L-1,需要加入n[Ca(OH) ]=(2.0×10-
2
4mol·L-1-10-5mol·L-1)×1×104L=1.9mol,当溶液中FeO浓度降至10-5mol·L-1,溶液中c(Ca2+)===
4.5×10-4mol·L-1,n(Ca2+)=4.5×10-4mol·L-1×1×104L=4.5mol,共需要加入Ca(OH) 固体的物质的量不
2
少于为1.9+4.5=6.4mol,故答案为6.4。
(5)根据晶胞结构示意图,一个晶胞中含有Mn原子个数为1+12×=4,含有O原子个数为×8+
×6=4,所以该锰的氧化物化学式为MnO,所以锰的化合价为+2,位于中心的Mn的配位数为6;
故答案为+2;6。
12.锰酸锂(LiMn O)是一种锂电池的正极材料。工业上以方锰矿(主要成分为MnO,还含有少量
2 4
的Fe O、Al O、CaO、SiO))为原料制备锰酸锂的流程如下:
3 4 2 3 2
已知:i.25℃时,相关物质的K 或K 如下表:
sp b
物质 Mn(OH) Fe(OH) Fe(OH) Al(OH) Ca(OH) NH ·H O
2 2 3 3 2 3 2
K 或K 2×10-13 5×10-17 1×10-39 1×10-32 6×10-6 2×10-5
sp b
ii.离子浓度低于1x10-5mol·L-1时即为该离子沉淀完全。回答下列问题:
(1)能加快步骤①反应速率和提高锰元素浸取率的措施有___________(任写一种)。
(2)滤液1中主要含有的金属离子是___________,步骤②中加入MnO 的作用是___________
2
(3)为了使A13+沉淀完全,步骤③中pH至少调至___________;反应Al3+(aq)+3NH·H O(aq)
3 2
Al(OH) (s)+3NH(aq)的平衡常数K=___________。
3
(4)步骤④反应未见气体生成,则反应的离子方程式为______________________________。步骤
⑤发生的反应中氧化剂与还原剂的物质的量之比为___________。
(5)某铁氮化合物晶体的晶胞如图所示,则该晶体的化学式为___________;若晶胞中距离最近
的两个铁原子距离为apm,阿伏伽德罗常数的值为N ,则晶体的密度为___________g/cm3(列出计
A
算式即可)。答案:(1)粉碎方锰矿(或升温、适当提高硫酸浓度等)
(2)Fe2+、Fe3+、Al3+、Mn2+ 将Fe2+氧化成Fe3+ (3)5 8×1017
(4)2Mn2++3CO O=MnCO ·Mn(OH) ↓+2HCO ∶4 (5) Fe N
+2H2 3 2 3 4
解析:由题给流程可知,方锰矿用稀硫酸酸溶时,金属氧化物与稀硫酸反应转化为硫酸盐,二
氧化硅不与稀硫酸反应,过滤得到含有硫酸钙、二氧化硅的滤渣1和含有可溶性硫酸盐的滤液1;
向滤液1中加入二氧化锰将溶液中亚铁离子氧化为铁离子后,加入氨水调节溶液的pH,将溶液中
铁离子、铝离子转化为氢氧化铁、氢氧化铝沉淀,过滤得到含有氢氧化铁、氢氧化铝的滤渣2和含
有硫酸锰的滤液2,滤液2经离子交换、淋洗涤液洗脱后,加入碳酸铵溶液将溶液中的锰离子转化
为碱式碳酸锰沉淀,过滤得到碱式碳酸锰和滤液3,碱式碳酸锰和碳酸锂在高温条件下在空气中煅
烧制得锰酸锂,据此分析解答。
(1)能加快步骤①反应速率和提高锰元素浸取率的措施有:粉碎方锰矿(或升温、适当提高硫酸
浓度等);
(2)由以上分析可知滤液1中含相应金属的硫酸盐,主要含有的金属离子Fe2+、Fe3+、Al3+、
Mn2+,步骤②中加入MnO 将溶液中亚铁离子氧化为铁离子;
2
(3)由分析可知,加入氨水调节溶液pH的目的是将溶液中铁离子、铝离子转化为氢氧化铁、氢
氧化铝沉淀,而锰离子不转化为氢氧化锰沉淀,由氢氧化铝的溶度积可知,溶液中氢氧根离子不小
于=1×10-9mol/L,由氢氧化锰的溶度积可知溶液中氢氧根离子浓度不大于=1×10-6mol/L,则溶液的
nH范围为5~8,pH至少调至5;由方程式可知,反应的平衡常数K=== 8×1017;
=
(4)步骤④中加入碳酸铵溶液将溶液中的锰离子转化为碱式碳酸锰沉淀,反应未见气体生成,可
知生成碳酸氢根离子,反应离子方程式为:2Mn2++3CO O=MnCO ·Mn(OH) ↓+2HCO ⑤发生
+2H2 3 2 ;步骤
的反应2LiCO+4MnCO ∙Mn(OH) +3O=====4LiMn O+6CO↑+4HO,反应中氧化剂为氧气,
2 3 3 2 2 2 4 2 2
还原剂为MnCO ·Mn(OH) ,两者物质的量之比为3∶4;
3 2
(5)由晶胞结构可知Fe位于顶点和面心,个数为:×8+×6=4;N位于体心个数为1,则Fe:
N=4:1,化学式为:Fe N;晶胞中距离最近的两个铁原子距离为面对角线的一半,为a pm,则晶
4
胞边长apm,晶胞的质量==g,晶胞体积=(a×10-10)3cm3,则晶胞密度=。