文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题13
1.溶液中存在Na+、SO Cl-、NH、SO,加入某物质后既产生了白色沉淀,又产生了无色刺激
、
性气体,该物质可以是
A. FeCl B. KHSO C. CaO D. Ba(NO )
3 4 3 2
2. 25℃时,下列各组离子在指定溶液中一定能大量共存的是
A. pH=1的溶液中:Na+、NH、[Ag(NH)]+、NO
3 2
B. 麦芽糖溶液中:MnO Na+、SO、H+
、
C. 澄清透明的溶液中:Cu2+、Al3+、SO、NO
D. 能使甲基橙变为红色的溶液中:Fe2+、K+、Cl-、NO
3.下列各组粒子在水溶液中能大量共存的是。
A. NH、CHCOO-、HCO NO B. Fe3+、ClO-、Na+、SO
3 、
C. Fe2+、Al3+、[Fe(CN) ]3-、Cl- D. Ag+、K+、NH 、NO
6 3
4. 能正确表示下列反应的离子方程式的是
A. 小苏打溶液与过量盐酸混合:CO +=CO↑+H O
+2H 2 2
B. 用铁电极电解饱和食盐水:2C1-+2H O=====Cl↑+H ↑+2OH-
2 2 2
C. Fe(NO ) 溶液中通入足量SO :Fe3++3NO +4H O=Fe2++3NO↑+5SO +8H+
3 3 2 +5SO2 2 3
D. 硫酸铜溶液中加入过量氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
3 2 2
5.下列离子方程式中,正确的是
A.金属钠投入水中:Na+HO=Na++OH-+H ↑
2 2
B.铁氰化钾溶液检验亚铁离子时生成了蓝色沉淀:3Fe2++2[Fe(CN)]3-=Fe [Fe(CN) ]↓
6 3 6 2
C.等体积等物质的量浓度的NH HSO 溶液与NaOH溶液混合:NH+OH-=NH ·H O
4 4 3 2
D.KClO碱性溶液与Fe(OH) 反应制备高铁酸钾:3ClO-+2Fe(OH) =2FeO+3Cl-+4H++H O
3 3 2
6.下列离子反应方程式书写正确的是
A.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++HO
2
B.漂白粉溶液中通入少量SO :Ca2++2ClO-+SO +HO=CaSO↓+2HClO
2 2 2 3
C.电解饱和食盐水:2Cl-+2H+=====Cl↑+H↑
2 2
D.Al溶于NaOH溶液:2Al+2OH-+2HO=2AlO+3H↑
2 2
7.现有下列实验探究摩尔盐[(NH )Fe(SO )∙6HO]的化学性质。
4 2 4 2 2
实
装置 试剂a 现象
验
① 紫色石蕊溶液 溶液变红色
② BaCl 溶液 产生白色沉淀
2
③ 稀硝酸溶液 溶液变黄色
④ 浓NaOH溶液 产生具有刺激性气味的气体下列离子方程式不能准确解释相应实验现象的是
A.①中溶液变红:NH+HO NH ∙HO+H+、Fe2++2HO Fe(OH) +2H+
2 3 2 2 2
B.②中产生白色沉淀:Ba2++SO=BaSO↓
4
C.③中溶液变黄:Fe2++NO 2H+=Fe3++NO ↑+HO
+ 2 2
D.④中产生有刺激性气体:NH+OH-=NH ↑+HO
3 2
8.下列指定反应的离子方程式书写正确的是
A.NO 通入NaOH浓溶液中:2NO +2OH-=NO+NO HO
2 2 + 2
B.(CHCOO) Pb溶液中滴入稀硫酸:Pb2++SO=PbSO ↓
3 2 4
C.NaAlO 溶液中加入少量盐酸:AlO+4H+=Al3++2HO
2 2
D.NH HSO 溶液中加入少量Ba(OH) 溶液:HSO Ba2++OH-=BaSO↓+HO
4 3 2 + 3 2
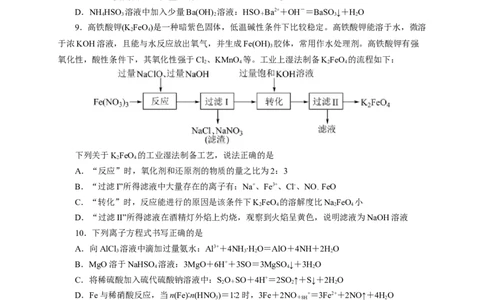
9.高铁酸钾(K FeO)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶
2 4
于浓KOH溶液,且能与水反应放出氧气,并生成Fe(OH) 胶体,常用作水处理剂。高铁酸钾有强
3
氧化性,酸性条件下,其氧化性强于Cl、KMnO 等。工业上湿法制备KFeO 的流程如下:
2 4 2 4
下列关于KFeO 的工业湿法制备工艺,说法正确的是
2 4
A.“反应”时,氧化剂和还原剂的物质的量之比为2:3
B.“过滤I”所得滤液中大量存在的离子有:Na+、Fe3+、Cl-、NO FeO
、
C.“转化”时,反应能进行的原因是该条件下KFeO 的溶解度比NaFeO 小
2 4 2 4
D.“过滤II”所得滤液在酒精灯外焰上灼烧,观察到火焰呈黄色,说明滤液为NaOH溶液
10.下列离子方程式书写正确的是
A.向AlCl 溶液中滴加过量氨水:Al3++4NH ∙HO=AlO+4NH+2HO
3 3 2 2
B.MgO溶于NaHSO 溶液:3MgO+6H++3SO=3MgSO ↓+3HO
4 4 2
C.将稀硫酸加入硫代硫酸钠溶液中:SO SO+4H+=2SO ↑+S↓+2HO
2 + 2 2
D.Fe与稀硝酸反应,当n(Fe)∶n(HNO)=1∶2时,3Fe+2NO +=3Fe2++2NO↑+4HO
3 +8H 2
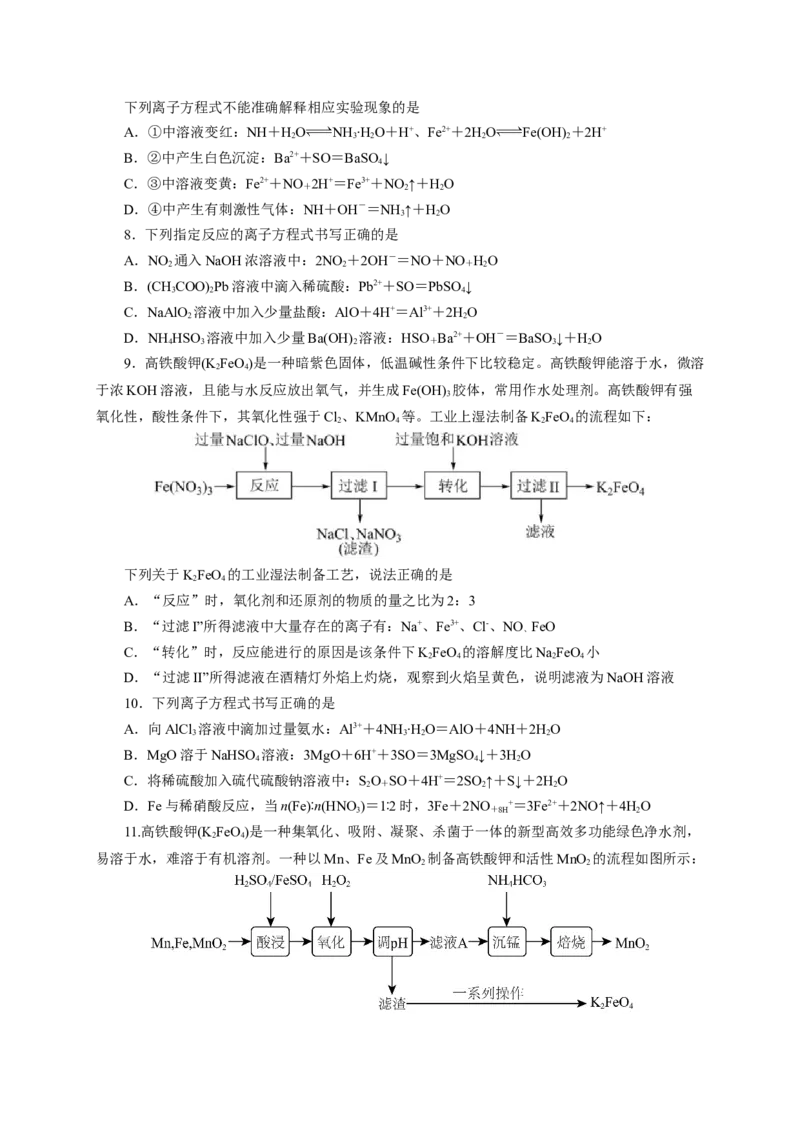
11.高铁酸钾(K FeO)是一种集氧化、吸附、凝聚、杀菌于一体的新型高效多功能绿色净水剂,
2 4
易溶于水,难溶于有机溶剂。一种以Mn、Fe及MnO 制备高铁酸钾和活性MnO 的流程如图所示:
2 2已知:部分金属离子在溶液中沉淀的pH如下表:
金属离子 Fe3+ Fe2+ Mn2+
开始沉淀的pH 1.9 7.0 8.1
完全沉淀的pH 3.2 9.0 10.1
回答下列问题:
(1)MnO 不溶于稀硫酸,加入过量FeSO 目的是在酸性条件下将MnO 还原成稳定的Mn2+,写
2 4 2
出该反应的离子方程式___________。
(2)“调pH”操作中,调节pH的范围是___________,“滤渣”的主要成分是___________。
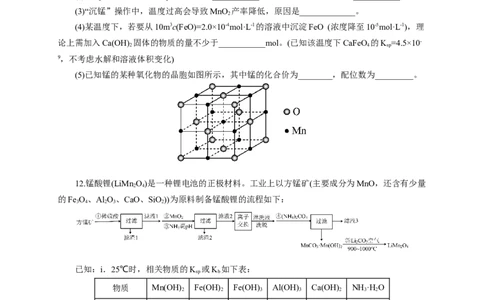
(3)“沉锰”操作中,温度过高会导致MnO 产率降低,原因是_____________。
2
(4)某温度下,若要从10m3c(FeO)=2.0×10-4mol·L-1的溶液中沉淀FeO (浓度降至10-5mol·L-1),理
论上需加入Ca(OH) 固体的物质的量不少于___________mol。(已知该温度下CaFeO 的K =4.5×10-
2 4 sp
9,不考虑水解和溶液体积变化)
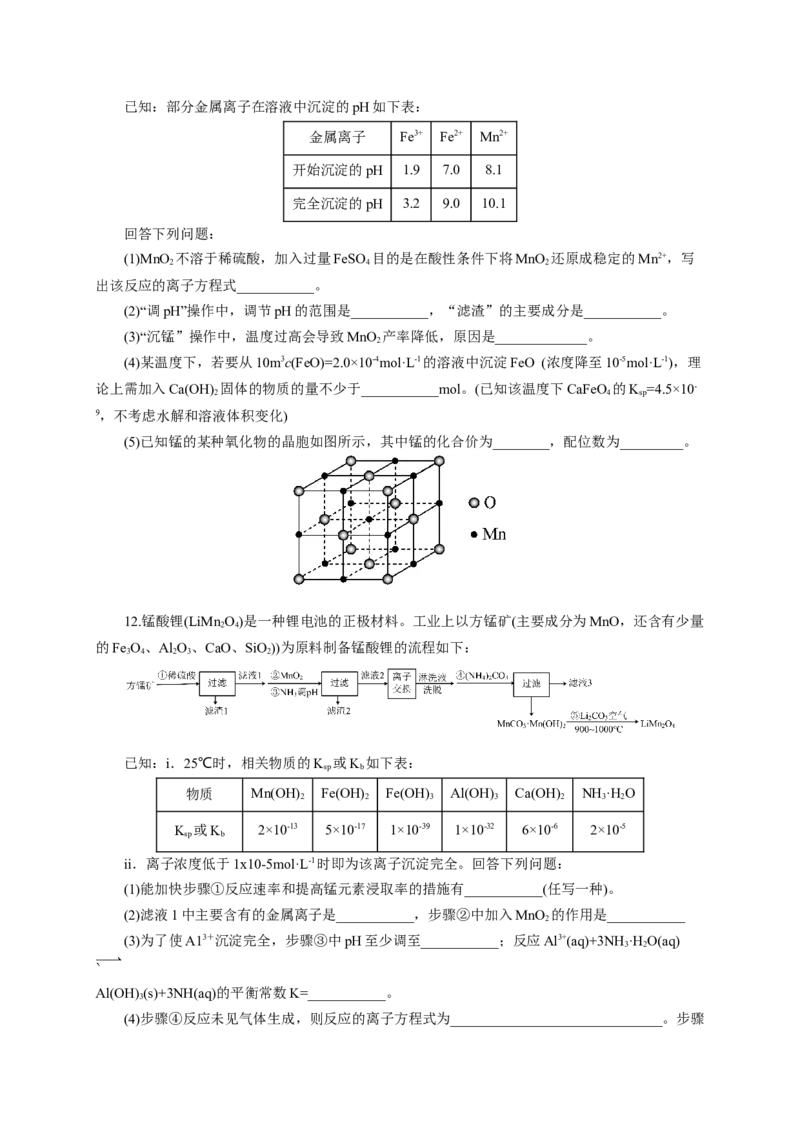
(5)已知锰的某种氧化物的晶胞如图所示,其中锰的化合价为________,配位数为_________。
12.锰酸锂(LiMn O)是一种锂电池的正极材料。工业上以方锰矿(主要成分为MnO,还含有少量
2 4
的Fe O、Al O、CaO、SiO))为原料制备锰酸锂的流程如下:
3 4 2 3 2
已知:i.25℃时,相关物质的K 或K 如下表:
sp b
物质 Mn(OH) Fe(OH) Fe(OH) Al(OH) Ca(OH) NH ·H O
2 2 3 3 2 3 2
K 或K 2×10-13 5×10-17 1×10-39 1×10-32 6×10-6 2×10-5
sp b
ii.离子浓度低于1x10-5mol·L-1时即为该离子沉淀完全。回答下列问题:
(1)能加快步骤①反应速率和提高锰元素浸取率的措施有___________(任写一种)。
(2)滤液1中主要含有的金属离子是___________,步骤②中加入MnO 的作用是___________
2
(3)为了使A13+沉淀完全,步骤③中pH至少调至___________;反应Al3+(aq)+3NH·H O(aq)
3 2
Al(OH) (s)+3NH(aq)的平衡常数K=___________。
3
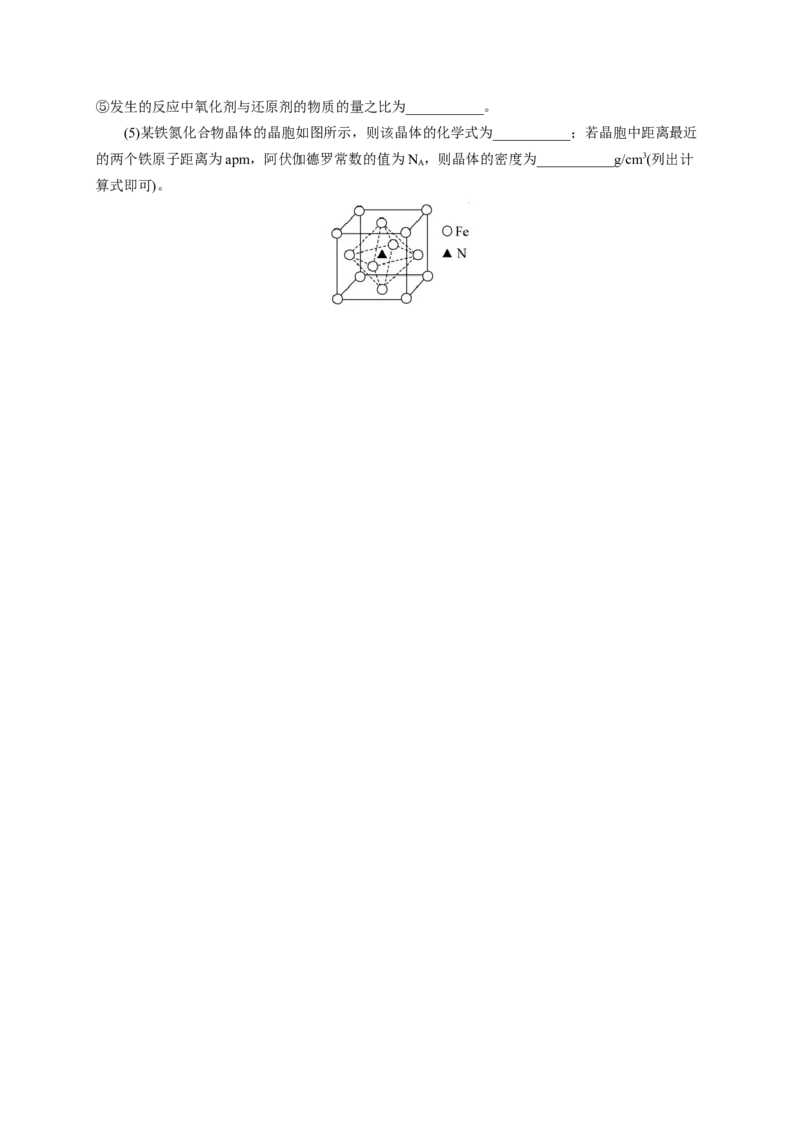
(4)步骤④反应未见气体生成,则反应的离子方程式为______________________________。步骤⑤发生的反应中氧化剂与还原剂的物质的量之比为___________。
(5)某铁氮化合物晶体的晶胞如图所示,则该晶体的化学式为___________;若晶胞中距离最近
的两个铁原子距离为apm,阿伏伽德罗常数的值为N ,则晶体的密度为___________g/cm3(列出计
A
算式即可)。