文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题12
1.常温下,下列各组离子在指定环境中能大量共存的是
A. 能使石蕊试液变红的溶液:NH、K+、I-、CrO
B. 在FeCl 溶液中:Na+、Mg2+、SCN-、SO
3
C. 水电离出的c(H+)=1×10-10的溶液中:Na+、K+、NO SO
、
D. c(OH-)<mol·L-1的溶液中:Ca2+、NH、AlO、Cl-
答案:C
解析:A.使石蕊试液变红的溶液呈酸性,在酸性条件下,I-与CrO要反应,而且H+与CrO反
应生成Cr O,不能大量共存,A不符合;
2
B.Fe3+与SCN-要反应,不能大量共存,B不符合;
C.水电离出的c(H+)=1×10-10的溶液,可能是酸溶液,也可能是碱溶液,Na+、K+、NO SO
、
无论是在酸溶液,还是在碱溶液中都能共存,C符合;
D.c(OH-)<说明是酸溶液,在酸溶液中,AlO要与H+反应,不能大量共存,D不符合。
2. 25℃,下列指定条件下离子能够大量共存的是
A.酸性条件下,Fe3+可以大量存在的体系:NO SO NH、Br-
、 2 、
B.pOH=12的溶液[pOH=lgc(OH-)]:Fe2+、NH、Br-、Cl-
C.等浓度醋酸溶液和醋酸钠溶液等体积混合时:Cl-、HCO NH、ClO-
、
D.惰性电极电解时,一开始就能产生氧气的溶液:SO HCO Na+、OH-
、 、
答案:B
解析:A.酸性条件下,硝酸根离子具有强的氧化性,可以将硫代硫酸根离子氧化,A错误;
B.pOH=12的溶液显酸性, Fe2+、NH、Br-、Cl-可以大量共存,B正确;
C.等浓度醋酸溶液和醋酸钠溶液等体积混合溶液显酸性,氢离子与碳酸氢根离子、次氯酸根
离子不能大量共存,且酸性环境下氯离子和次氯酸跟离子能发生氧化还原反应而不能大量共存,C
错误;
D.碳酸氢根离子与氢氧根离子不能大量共存,D错误;
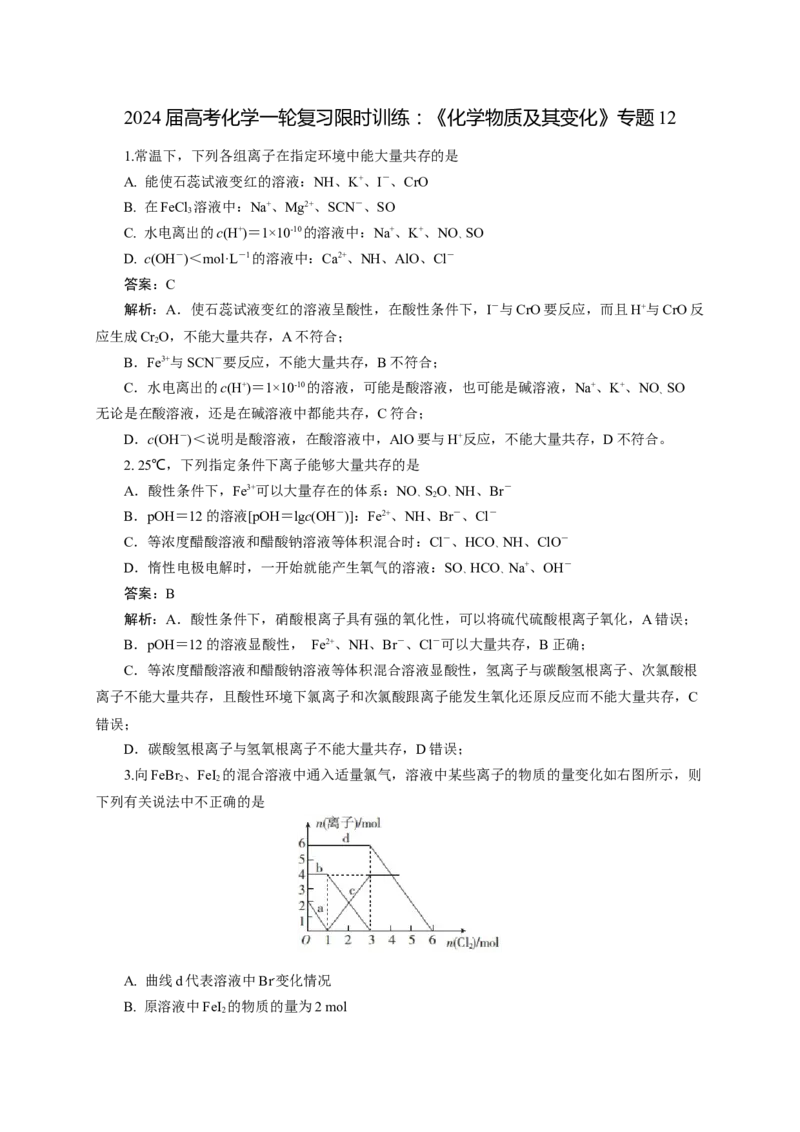
3.向FeBr 、FeI 的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如右图所示,则
2 2
下列有关说法中不正确的是
A. 曲线d代表溶液中Br-变化情况
B. 原溶液中FeI 的物质的量为2 mol
2C. 原溶液中n(Fe2+)∶n(Br-) = 2∶3
D. 当通入2molCl 时,溶液中离子反应为2I-+ 2Fe2++ 2Cl =I+2Fe3++ 4C1-
2 2 2
答案:B
解析:还原性强弱:I->Fe2+ >Br-,则:
A. 根据氧化还原反应的先后顺序,d代表Br-变化情况,故A正确;
B. a代表的是I-的变化情况,2I-+Cl=I+2Cl-,n(I-)=2mol,则n(FeI )=1mol,故B错误;
2 2 2
C. b点代表Fe2+ 变化情况,2Fe2++Cl = 2Fe3++2Cl-,n(Fe2+ ) = 4mol,d发生反应2Br-+Cl
2 2
=Br +2Cl-,n(Br-)=6mol,两者比值为4∶6=2∶3,故C正确;
2
D. 加入2molCl ,I-全部参加反应,部分Fe2+ 参加反应,因此离子反应2I-+2Fe2++2Cl=I
2 2 2
+2Fe3++4Cl-,故D正确。
4.下列物质属于盐类且水溶液呈碱性的是
A.KCl B. Na CO C. BaO D. (NH )SO
2 3 4 2 4
答案:B
解析:A.KCl是强酸强碱盐,水溶液显中性,A错误;
B.NaCO 是弱酸强碱盐,水溶液显碱性,B正确;
2 3
C.BaO不属于盐类,C错误;
D.(NH )SO 是强酸弱碱盐,水溶液显酸性,D错误;
4 2 4
5. 已知反应3IF+6OH-=2I-+IO -+3HO,下列说法不正确的是
+6F 2
A.IO 既是氧化剂又是还原剂
是氧化产物 B.IF
C.3mol IF反应时转移5mol电子 D.IF可能会与HSO 反应
2 3
答案:C
解析:在3IF+6OH-=2I-+IO -+3HO中IF中I为+1价,该反应为歧化反应,经过反应后I
+6F 2
变为-1和+5价,3mol IF反应时转移4mol电子,据此分析解答。
解析:A.IO
中I化合价升高是氧化产物,A正确;
B.IF既是氧化剂又是还原剂,B正确;
C.3mol IF反应时转移4mol电子,C错误;
D.IF中中I为+1价有氧化性,HSO 具有还原性,二者可能发生反应,D正确;
2 3
6.下列反应的离子方程式不正确的是
A.NO 通入水中:3NO +HO=2H++2NO
2 2 2 +NO
B.Al(OH) 溶于氢氧化钠溶液中:Al(OH) +OH-=[Al(OH) ]-
3 3 4
C.少量CO 通入次氯酸钙溶液中:CO+ClO-+HO=HClO+HCO
2 2 2
D.水中的溶解氧氧化氢氧化亚铁:4Fe(OH) +O+2HO=4Fe(OH)
2 2 2 3
答案:C
解析:A.NO 通入水中生成硝酸和NO,反应的离子方程式为3NO +HO=2H++2NO
2 2 2 +NO,故A
正确;
B.Al(OH) 溶于氢氧化钠溶液中生成四羟基合铝酸钠,反应的离子方程式是Al(OH) +OH-=
3 3[Al(OH) ]-,故B正确;
4
C.少量CO 通入次氯酸钙溶液中生成碳酸钙沉淀和次氯酸,反应的离子方程式是Ca2++CO
2 2
+2ClO-+HO=2HClO+CaCO ↓,故C错误;
2 3
D.水中的溶解氧氧化氢氧化亚铁生成氢氧化铁沉淀,反应的离子方程式为4Fe(OH) +O+
2 2
2HO=4Fe(OH) ,故D正确;
2 3
7.下列物质中属于盐且水溶液呈碱性的是
A. NaHCO B. NH Cl C. KNO D. CaO
3 4 3
答案:A
解析:A.NaHCO 属于盐因碳酸氢根离子水解溶液呈碱性,A符合题意;
3
B.NH Cl属于盐因铵根离子水解水溶液呈酸性,B不符合题意;
4
C.KNO 属于盐水溶液呈中性,C不符合题意;
3
D.CaO属于氧化物,溶于水溶液呈碱性,D不符合题意;
8.KNO 和NH Cl混合加热可发生反应2KNO+2NH Cl===2N↑+O↑+2KCl+4HO,下列说
3 4 3 4 2 2 2
法正确的是
A. 还原产物是N 和O
2 2
B. 实验室加热可用氯化铵制备NH
3
C. KNO 既是氧化剂又是还原剂
3
D. 每生成1 mol N ,反应总共转移6 mol电子
2
答案:C
解析:A.在该反应中N元素化合价由反应前KNO 中的+5价变为反应后N 中的0价,化合价
3 2
降低,得到电子被还原,故N 是还原产物;O元素化合价由反应前KNO 中的-2价变为反应后O
2 3 2
的0价,化合价升高,失去电子被氧化,故O 是氧化产物,A错误;
2
B.在实验室中一般是加热氯化铵和Ca(OH) 混合物的方法制备NH ,B错误;
2 3
C.在该反应中N元素化合价由反应前KNO 中的+5价变为反应后N 中的0价,化合价降低,
3 2
得到电子被还原,KNO 作氧化剂;O元素化合价由反应前KNO 中的-2价变为反应后O 的0价,
3 3 2
化合价升高,失去电子被氧化,KNO 作还原剂,故KNO 既是氧化剂又是还原剂,C正确;
3 3
D.根据在氧化还原反应中元素化合价升降总数等于反应过程中电子转移总数,根据方程式可
知:每反应产生2 mol N ,反应过程中转移10 mol电子,则每生成1 mol N ,反应总共转移5 mol
2 2
电子,D错误;
9.下列反应的方程式不正确的是
A. 将碳酸氢钙溶液与过量的澄清石灰水混合:HCO Ca2++OH-=CaCO ↓+HO
+ 3 2
B. 将稀硫酸加入硫代硫酸钠溶液:SO SO+4H+=2SO ↑+S↓+2HO
2 + 2 2
C. CuSO 溶液与闪锌矿(ZnS)反应生成铜蓝(CuS):Cu2+(aq)+ZnS(s)=Zn+(aq)+CuS(s)
4
D. 向银氨溶液中滴加乙醛,水浴加热,析出光亮银镜:CHCHO+
3
2Ag(NH)OH===CHCOONH+2Ag↓+3NH +HO
3 2 3 4 3 2
答案:B解析:A.碳酸氢钙溶液与过量的澄清石灰水混合反应生成碳酸钙沉淀和水,离子方程式正确,
故A正确;
B.稀硫酸加入硫代硫酸钠溶液,硫代硫酸根离子在酸性条件下会发生歧化反应,其离子方程
式为:SO 2H+=SO ↑+S↓+HO,故B错误;
2 + 2 2
C.CuSO 溶液与ZnS反应生成CuS和硫酸锌,其中ZnS和CuS难溶于水,离子方程式正确,
4
故C正确;
D.银氨溶液中滴加乙醛,水浴加热,反应生成乙酸铵、Ag和水,离子方程式正确,故D正
确;
10. 含有下列各组离子的溶液中,通入(或加入)过量的某种物质后仍能太量共存的是
A. 通入SO 气体,H+、Ba2+、Fe3+、NO
2
B. 通入NH 气体,Mg2+、K+、Cl-、NH
3
C. 通入CO 气体,H+、NH、Ba2+、Cl-
2
D. 加入AlCl 溶液,K+、Na+、I-、S2-
3
答案:C
解析:A.H++NO 气体发生氧化还原反应,A不符合题意;
组合具有强氧化性,能和SO2
B.NH 通入溶液中生成NH ∙HO,Mg2+与NH ∙HO反应生成Mg(OH) 沉淀,B不符合题意;
3 3 2 3 2 2
C.溶液中有大量H+,故CO 不与Ba2+反应,C符合题意;
2
D.Al3+与S2-发生双水解反应生成氢氧化铝沉淀和HS,D不符合题意;
2
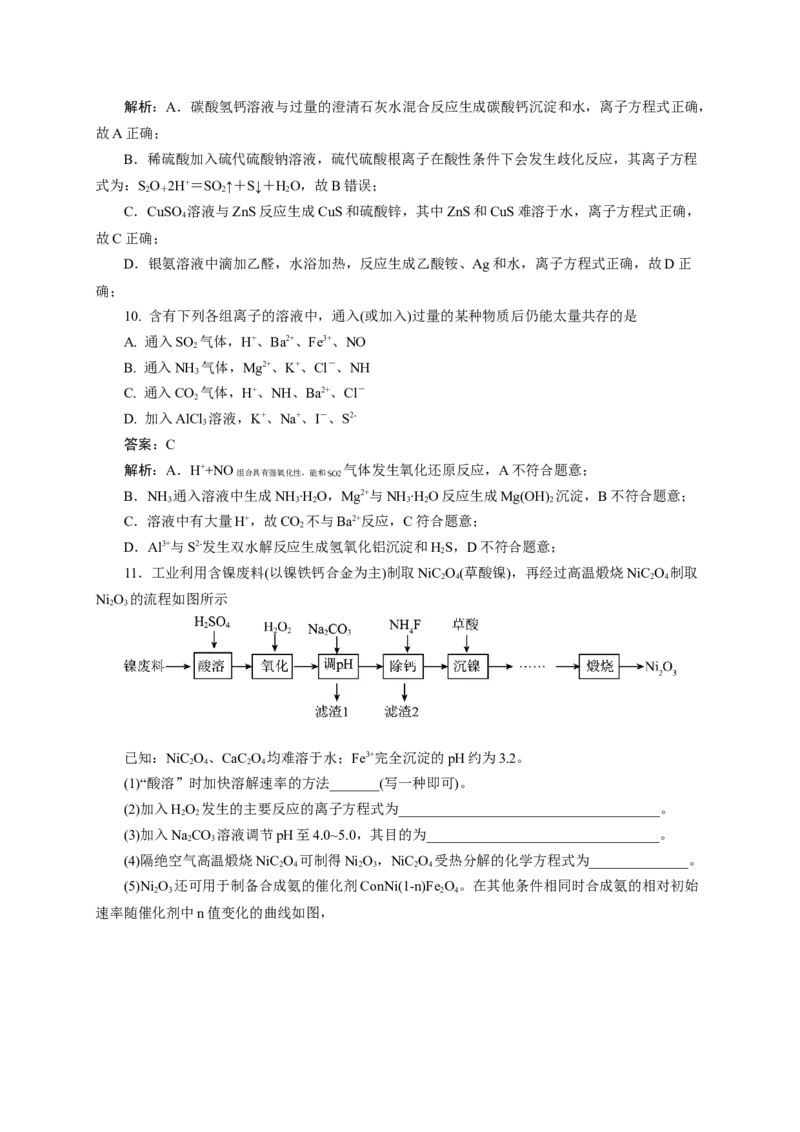
11.工业利用含镍废料(以镍铁钙合金为主)制取NiC O(草酸镍),再经过高温煅烧NiC O 制取
2 4 2 4
Ni O 的流程如图所示
2 3
已知:NiC O、CaC O 均难溶于水;Fe3+完全沉淀的pH约为3.2。
2 4 2 4
(1)“酸溶”时加快溶解速率的方法_______(写一种即可)。
(2)加入HO 发生的主要反应的离子方程式为_____________________________________。
2 2
(3)加入NaCO 溶液调节pH至4.0~5.0,其目的为_________________________________。
2 3
(4)隔绝空气高温煅烧NiC O 可制得Ni O,NiC O 受热分解的化学方程式为______________。
2 4 2 3 2 4
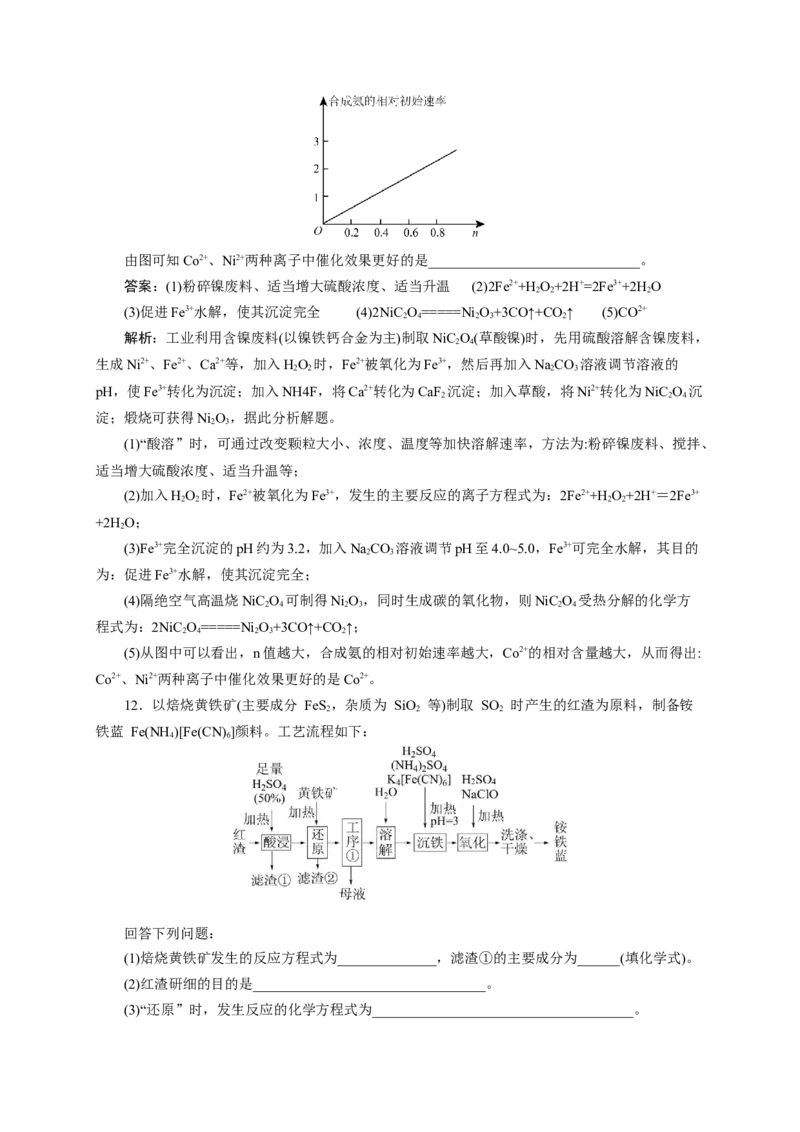
(5)NiO 还可用于制备合成氨的催化剂ConNi(1-n)Fe O。在其他条件相同时合成氨的相对初始
2 3 2 4
速率随催化剂中n值变化的曲线如图,由图可知Co2+、Ni2+两种离子中催化效果更好的是______________________________。
答案:(1)粉碎镍废料、适当增大硫酸浓度、适当升温 (2)2Fe2++H O+2H+=2Fe3++2H O
2 2 2
(3)促进Fe3+水解,使其沉淀完全 (4)2NiC O=====Ni O+3CO↑+CO ↑ (5)CO2+
2 4 2 3 2
解析:工业利用含镍废料(以镍铁钙合金为主)制取NiC O(草酸镍)时,先用硫酸溶解含镍废料,
2 4
生成Ni2+、Fe2+、Ca2+等,加入HO 时,Fe2+被氧化为Fe3+,然后再加入NaCO 溶液调节溶液的
2 2 2 3
pH,使Fe3+转化为沉淀;加入NH4F,将Ca2+转化为CaF 沉淀;加入草酸,将Ni2+转化为NiC O 沉
2 2 4
淀;煅烧可获得Ni O,据此分析解题。
2 3
(1)“酸溶”时,可通过改变颗粒大小、浓度、温度等加快溶解速率,方法为:粉碎镍废料、搅拌、
适当增大硫酸浓度、适当升温等;
(2)加入HO 时,Fe2+被氧化为Fe3+,发生的主要反应的离子方程式为:2Fe2++H O+2H+=2Fe3+
2 2 2 2
+2H O;
2
(3)Fe3+完全沉淀的pH约为3.2,加入NaCO 溶液调节pH至4.0~5.0,Fe3+可完全水解,其目的
2 3
为:促进Fe3+水解,使其沉淀完全;
(4)隔绝空气高温烧NiC O 可制得Ni O,同时生成碳的氧化物,则NiC O 受热分解的化学方
2 4 2 3 2 4
程式为:2NiC O=====Ni O+3CO↑+CO ↑;
2 4 2 3 2
(5)从图中可以看出,n值越大,合成氨的相对初始速率越大,Co2+的相对含量越大,从而得出:
Co2+、Ni2+两种离子中催化效果更好的是Co2+。
12.以焙烧黄铁矿(主要成分 FeS,杂质为 SiO 等)制取 SO 时产生的红渣为原料,制备铵
2 2 2
铁蓝 Fe(NH )[Fe(CN) ]颜料。工艺流程如下:
4 6
回答下列问题:
(1)焙烧黄铁矿发生的反应方程式为______________,滤渣①的主要成分为______(填化学式)。
(2)红渣研细的目的是_________________________________。
(3)“还原”时,发生反应的化学方程式为_____________________________________。(4)工序①得到绿矾(FeSO
4
·7H
2
O)和母液,则工序①的操作名称为 __________。
(5)用K
3
[Fe(CN)
6
]可检验工序①所得母液中的金属阳离子,检验时发生的离子方程式为_____
____________________________________,所得母液循环使用。
(6)沉铁工序产生的白色沉淀 Fe(NH ) [Fe(CN) ]中 Fe 的化合价为 ,氧化工序发生反应的离
4 2 6
子方程式为________________________________________。
答案:(1)4FeS +11O=====2Fe O+8SO SiO
2 2 2 3 2 2
(2)增大固液接触面积,加快反应速率,提高红渣的利用率
(3)Fe (SO )+FeS=3FeSO +2S
2 4 3 2 4
(4)蒸发浓缩、冷却结晶、过滤(洗涤)
(5)K++Fe2++[Fe(CN) ]3-=KFeFe(CN) ↓
6 6
(6)+2 2Fe(NH )[Fe(CN) ]+ClO-+2H+=2Fe(NH )[Fe(CN) ]+Cl-+2NH+HO
4 2 6 4 6 2
解析:已知黄铁矿高温煅烧生成Fe O,反应原理为:4FeS+11O =====2Fe O+8SO,故产生
2 3 2 2 2 3 2
的红渣主要成分为Fe O 和SiO,将红渣粉碎后加入足量的50%的HSO 溶液加热充酸浸,反应原
2 3 2 2 4
理为:Fe O+3H SO =Fe (SO )+3H O,过滤出滤渣①,主要成分为SiO,向滤液中加入黄铁矿进行
2 3 2 4 2 4 3 2 2
还原,将Fe3+还原为Fe2+,由”过滤“知有生成S沉淀,则反应原理为:
Fe (SO )+FeS =3FeSO+2S↓,然后进行工序①为蒸发浓缩、冷却结晶,得到FeSO 晶体和母液主要
2 4 3 2 4 4
含有FeSO 溶液,加水溶解FeSO 晶体,向所得溶液中加入(NH )SO 、K[Fe(CN) ]并用HSO 调节
4 4 4 2 4 4 6 2 4
溶液的pH为3,进行沉铁过程,反应原理为:Fe2++2NH+[Fe(CN)]4-=Fe(NH )Fe(CN) ↓,然后过滤
6 4 2 6
出沉淀,洗涤后加入HSO 和NaClO进行氧化步骤,反应原理为2Fe(NH )[Fe(CN) ]+ClO- +2H+=
2 4 4 2 6
2Fe(NH )[Fe(CN) ]+H O+Cl- +2NH Fe(NH )[Fe(CN) ],据此分析解题。
4 6 2 ,过滤、洗涤干燥即制得 4 6