文档内容
第 13 讲 碳酸钠和碳酸氢钠 碱金属
[复习目标] 1.掌握NaCO 、NaHCO 的基本性质及相互转化。2.掌握NaCO 、NaHCO 的
2 3 3 2 3 3
鉴别及除杂。3.了解碱金属的通性与特性及焰色试验。
考点一 碳酸钠和碳酸氢钠
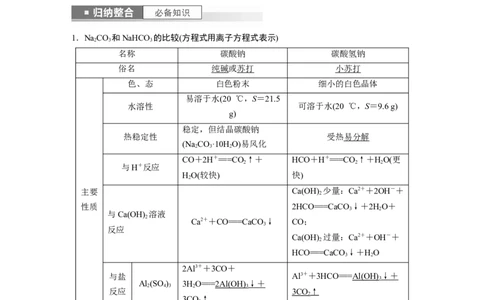
1.NaCO 和NaHCO 的比较(方程式用离子方程式表示)
2 3 3
名称 碳酸钠 碳酸氢钠
俗名 纯碱或苏打 小苏打
色、态 白色粉末 细小的白色晶体
易溶于水(20 ℃,S=21.5
水溶性 可溶于水(20 ℃,S=9.6 g)
g)
稳定,但结晶碳酸钠
热稳定性 受热易分解
(Na CO·10H O)易风化
2 3 2
CO+2H+===CO↑+ HCO+H+===CO↑+HO(更
2 2 2
与H+反应
HO(较快) 快)
2
主要 Ca(OH) 少量:Ca2++2OH-+
2
性质 2HCO===CaCO ↓+2HO+
3 2
与Ca(OH) 溶液
2
Ca2++CO===CaCO ↓ CO;
3
反应
Ca(OH) 过量:Ca2++OH-+
2
HCO===CaCO ↓+HO
3 2
2Al3++3CO+
与盐 Al3++3HCO===Al(OH) ↓ +
3
Al (SO ) 3HO===2Al(OH) ↓ +
2 4 3 2 3
反应 3CO↑
2
3CO↑
2
与水作用 水解,碱性较强 水解,碱性较弱
用于制玻璃、制肥皂、合
灭火器、治疗胃酸过多、发酵
主要用途 成洗涤剂、造纸、纺织、
粉的主要成分之一
石油、冶金等工业中
2.NaCO 和NaHCO 的相互转化
2 3 3
NaCONaHCO
2 3 3
应用举例选择适当的试剂或方法除去杂质,并完成转化的化学方程式,“[ ]”内为杂质。
(1)Na CO(s)[NaHCO ]_____________________________________________________,
2 3 3
________________________________________________________________________。
(2)NaHCO (aq)[Na CO]____________________________________________________,
3 2 3
________________________________________________________________________。
(3)Na CO(aq)[NaHCO ]____________________________________________________,
2 3 3
________________________________________________________________________。
答案 (1)充分灼烧至恒重 2NaHCO =====NaCO+HO+CO↑
3 2 3 2 2
(2)通入足量CO NaCO+HO+CO===2NaHCO
2 2 3 2 2 3
(3)滴加适量NaOH 溶液 NaHCO +NaOH===NaCO+HO
3 2 3 2
3.NaCO、NaHCO 的鉴别方法
2 3 3
(1)利用热稳定性不同
(2)相同条件下,利用和酸反应生成气体的速率不同
(3)利用溶液的碱性不同
4.NaCO、NaHCO 与酸反应的图像分析
2 3 3
实验操作和反应 n(CO)—n(HCl)图像
2
向NaCO 溶液中逐滴加入盐酸,离子方程式:
2 3
Oa段:CO+H+===HCO
ab段:HCO+H+===HO+CO↑
2 2
图像特点:Oa=ab
向NaHCO 溶液中逐滴加入盐酸,离子方程式:HCO
3
+H+===HO+CO↑
2 2
向等物质的量的NaOH、NaCO 的混合溶液中逐滴加
2 3
入盐酸,离子方程式:
Oa段:H++OH-===HO、CO+H+===HCO
2
ab段:HCO+H+===HO+CO↑
2 2图像特点:Oa=2ab
1.碳酸钠、碳酸氢钠都能与盐酸、氢氧化钠溶液反应( )
2.用热碱水清除炊具上残留的油污,没有发生化学反应( )
3.Al (SO ) 和小苏打反应可用作泡沫灭火器灭火( )
2 4 3
4.向饱和NaCO 溶液中通入CO,有NaHCO 晶体析出( )
2 3 2 3
5.将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡( )
6.用酚酞溶液可鉴别饱和食盐水和饱和碳酸钠溶液( )
7.苏打是面包发酵粉的主要成分之一( )
8.相同温度下,溶解度:小苏打<苏打,热稳定性:NaCO>NaHCO( )
2 3 3
答案 1.× 2.× 3.√ 4.√ 5.× 6.√ 7.× 8.√
一、NaCO、NaHCO 性质比较与鉴别
2 3 3
1.(2023·佛山调研)NaCO 和NaHCO 混合溶液具有控制酸碱平衡的作用。室温下,通过下
2 3 3
列实验探究一定浓度的NaCO 和NaHCO 混合溶液的性质。
2 3 3
实验1:向混合溶液中滴几滴酚酞,溶液显红色;
实验2:向实验1所得溶液中滴加几滴稀盐酸,溶液红色变浅;
实验3:向混合溶液中通入过量的CO,无明显现象;
2
实验4:向实验3所得溶液中滴加少量Ba(OH) 溶液,产生白色沉淀。
2
下列有关说法正确的是( )
A.实验1中溶液显红色的主要原因是CO+2HOHCO+2OH-
2 2 3
B.实验2中溶液红色变浅的原因是HCO+H+HO+CO↑
2 2
C.实验3中无明显现象说明没有发生化学反应
D.实验4中产生白色沉淀的原因是2HCO+Ba2++2OH-===2HO+CO+BaCO ↓
2 3
答案 D
解析 CO的水解能力比HCO强,实验1中溶液显红色的主要原因是CO的水解,CO分步
水解,以第一步水解为主:CO+HOHCO+OH-,A项错误;实验2中滴加几滴稀盐酸,
2
溶液红色变浅,碳酸钠更容易与酸反应,故主要原因是CO+H+===HCO,B项错误;实验
3中无明显现象,但发生了化学反应:CO +NaCO +HO===2NaHCO ,C项错误;实验4
2 2 3 2 3
中产生白色沉淀,是少量氢氧化钡与碳酸氢钠反应生成了碳酸钡,离子方程式为 2HCO+
Ba2++2OH-===2HO+CO+BaCO ↓,D项正确。
2 32.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实
验,如图Ⅰ~Ⅳ所示。
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是________(填装置序号)。
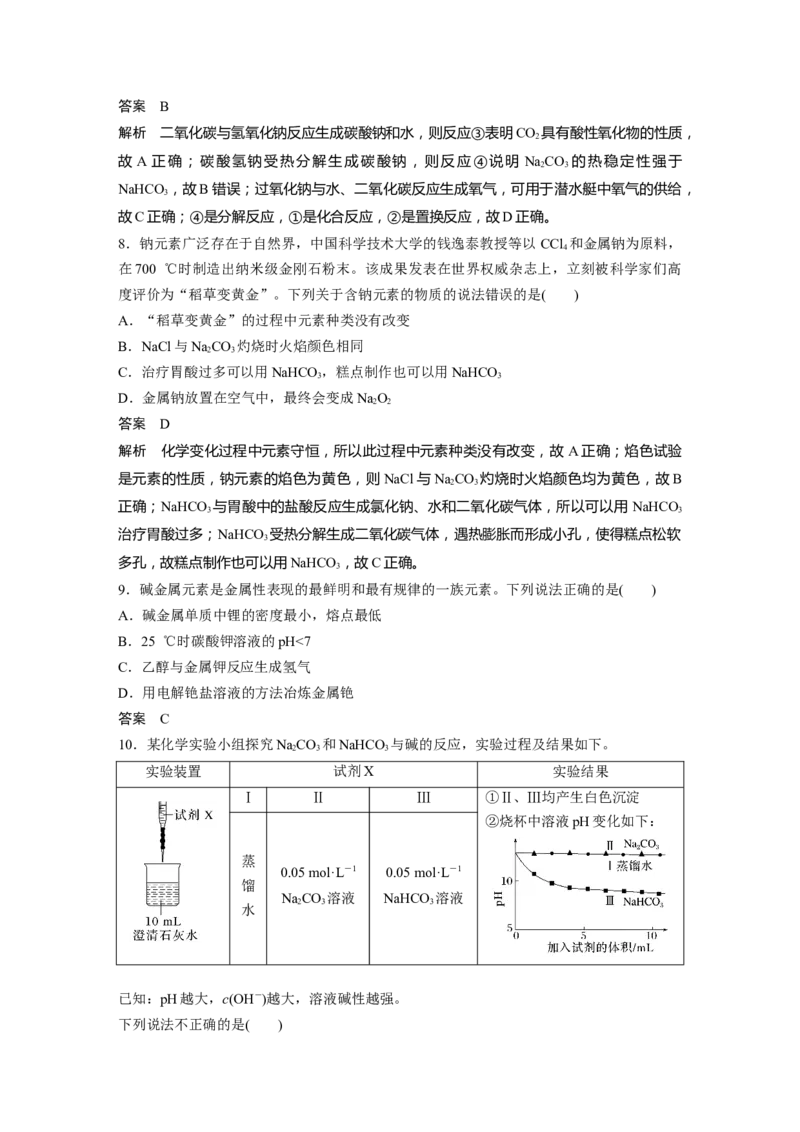
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为______________
________________________________________________________________________;
与实验Ⅲ相比,实验Ⅳ的优点是________(填字母)。
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管 B 中装入的固体最好是
___________________________________________________________________(填化学式)。
答案 (1)Ⅱ (2)2NaHCO =====NaCO +HO+CO↑,CO +Ca(OH) ===CaCO ↓+HO
3 2 3 2 2 2 2 3 2
D
(3)NaHCO
3
解析 (1)图Ⅰ不能达到实验目的,因为碳酸钠和碳酸氢钠均可以与盐酸反应产生二氧化碳,
二氧化碳气体使澄清石灰水变浑浊;图Ⅱ可以鉴别,因为等质量的碳酸钠和碳酸氢钠与足量
的稀盐酸反应,生成的二氧化碳气体的量不同,可根据气球膨胀程度来判断。(3)试管B装
入碳酸氢钠,试管A装入碳酸钠,这样直接加热的碳酸钠,温度高,不分解,澄清石灰水
不变浑浊,而间接加热的碳酸氢钠分解,澄清石灰水变浑浊,表明了碳酸氢钠不稳定。
二、NaCO、NaHCO 与H+反应定量关系应用
2 3 3
3.将一定物质的量的NaCO 、NaHCO 组成的混合物溶于水,配成1 L溶液,取出50 mL
2 3 3
溶液,然后滴加一定物质的量浓度的盐酸,得到的图像如图所示。按要求回答问题:
(1)写出依次发生反应的化学方程式:________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)①代表________的变化曲线;②代表________的变化曲线;③代表________的变化曲线。
(3)盐酸的物质的量浓度为__________________________________________________。
(4)加入盐酸为150 mL时,放出的CO 在标准状况下的体积为________。
2
答案 (1)Na CO+HCl===NaCl+NaHCO 、NaHCO +HCl===NaCl+HO+CO↑
2 3 3 3 2 2
(2)NaHCO NaCl NaCO
3 2 3
(3)0.05 mol·L-1 (4)0.112 L
解析 (3)当加入 150 mL 盐酸时正好生成 NaCl 溶液,n(HCl)=n(NaCl)=2n(Na CO)+
2 3
n(NaHCO )=2.5×10-3×2 mol+2.5×10-3 mol=7.5×10-3 mol,c(HCl)==0.05 mol·L-
3
1。(4)n(CO)=n(Na CO)+n(NaHCO )=(2.5+2.5)×10-3 mol=5×10-3 mol,标况下V(CO)
2 2 3 3 2
=5×10-3 mol×22.4 L·mol-1=0.112 L。
4.向浓度相等、体积均为100 mL的A、B两份NaOH溶液中,分别通入一定量的CO 后,
2
逐滴加入0.1 mol·L-1盐酸,产生CO 的体积(标准状况)与所加盐酸的体积关系如图所示。
2
(1)A曲线表明,原溶液通入CO________mL(标准状况)。
2
(2)B曲线表明,原溶液通入CO 后,所得溶液中溶质的物质的量之比为________。
2
(3)原NaOH溶液的物质的量浓度为________。
答案 (1)134.4 (2)1∶1 (3)0.09 mol·L-1
解析 (1)分析图中A曲线,有60 mL盐酸与NaHCO 反应生成CO ,根据元素质量守恒,A
3 2
曲线对应的最终生成的CO 的体积等于之前通入NaOH溶液的CO 的体积,根据第二步反应
2 2
物质的量关系,n(CO)=n(NaHCO )=n(HCl)=0.1 mol·L-1×0.06 L=0.006 mol,V(CO)=
2 3 2
V ·n(CO)=22.4 L·mol-1×0.006 mol=0.134 4 L=134.4 mL。
m 2
(2)分析图中B曲线,只有30 mL盐酸与NaHCO 反应生成CO ,而未生成气体时耗用盐酸
3 2
60 mL,说明该混合溶液中有 NaOH、NaCO ,无 NaHCO ,NaOH 消耗 30 mL 盐酸,
2 3 3NaCO 生成NaHCO 消耗30 mL盐酸,生成的NaHCO 又消耗30 mL盐酸生成CO ,根据
2 3 3 3 2
NaOH+HCl===NaCl+HO,NaCO 生成NaHCO 消耗盐酸的量与NaOH消耗盐酸的量相等,
2 2 3 3
则有 n(NaOH)∶n(Na CO)=1∶1。(3)根据元素质量守恒,最终 NaCl 中Na+的来源就是
2 3
NaOH,所以最终 n(NaCl)等于最初 n(NaOH),而 NaCl 中 Cl-的来源是 90 mL 盐酸中的
HCl,故 n(NaCl)=n(HCl),那么 n(NaOH)=n(HCl)=0.1 mol·L-1×0.09 L=0.009 mol,
c(NaOH)===0.09 mol·L-1。
考点二 碱金属 焰色试验
(一)碱金属的通性
1.碱金属的相似性和递变性
相似性 递变性(由Li→Cs)
电子层数逐渐增多;核电荷数逐
原子结构 最外层均为 1 个 电子
渐增大;原子半径逐渐增大
都具有较强的金属性,最
元素性质 金属性逐渐增强
高正价均为 + 1 价
(除Cs外)都呈银白色,密 密度逐渐增大(钾反常),熔、沸
物理性质
单质 度较小,熔、沸点较低 点逐渐降低
性质 还原性逐渐增强;与O 反应越来
2
化学性质 都具有较强的还原性
越剧烈,产物越来越复杂
2.碱金属的特性
(1)碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠的小。
(2)碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度而将锂保存在石蜡中。
(3)试剂瓶中的药品取出后,一般不能放回原瓶,但Na、K等需放回原试剂瓶。
(4)锂与O 反应与钠不同,只生成LiO。
2 2
(二)焰色试验
1.焰色试验的概念
某些金属或它们的化合物在灼烧时都会使火焰呈现出特征颜色,属于物理变化,是元素的性
质。
2.焰色试验的操作
(1)清洗铂丝:将铂丝用盐酸洗净,在外焰上灼烧至与原来的火焰颜色相同。
(2)灼烧试样:蘸取试样在外焰上灼烧,观察火焰的颜色。
(3)清洗铂丝:将铂丝再用盐酸洗净后,在外焰上灼烧至与原来的火焰颜色相同。提醒 做钾的焰色试验时,需透过蓝色钴玻璃观察火焰的颜色。
3.熟记常见金属的焰色
钠元素:黄色;钾元素:紫色(透过蓝色钴玻璃观察);铜元素:绿色;钡元素:黄绿色;钙
元素:砖红色。
(三)碱金属氢化物的性质及应用
碱金属跟氢气反应生成的碱金属氢化物都是离子化合物,其中氢以H-形式存在,显-1价,
碱金属氢化物是强还原剂。
1.在酒精灯加热的条件下,NaCO、NaHCO 固体都会分解( )
2 3 3
2.KOH的碱性比NaOH的弱( )
3.常温下,Rb、Cs露置在空气中不易变质( )
4.焰色试验是金属化合物的性质( )
5.碱金属元素由Li到Cs,随着核电荷数的递增,单质密度逐渐增大,熔、沸点逐渐降低(
)
答案 1.× 2.× 3.× 4.× 5.×
一、焰色试验
1.下列有关焰色试验操作注意事项的说法正确的是( )
①钾的火焰颜色要透过蓝色钴玻璃观察 ②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取
被检验的物质 ③每次实验后,要将铂丝用盐酸洗净 ④实验时最好选择本身颜色较浅的火
焰 ⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确
C.仅有⑤不正确 D.全对
答案 D
解析 由于焰色试验是通过观察火焰颜色来检验金属元素是否存在的方法,所以实验时所用
火焰和所用金属丝在灼烧时都不应该有很明显的颜色,否则将无法观察到被检验金属元素的
真实焰色;观察钾的火焰颜色时要透过蓝色钴玻璃,目的是滤去黄光,避免钠的干扰。
二、碱金属元素性质规律的应用
2.碱金属单质及其化合物有广泛应用。回答下列问题:
(1)锂是最轻的活泼金属,常用于制造高效锂电池。电解池中的电解液不能用水作溶剂,原
因是________________________________________________________________________。
(2)金属钾是一种活泼的金属,下列有关其性质的说法正确的是________(填字母)。
A.钾在空气中燃烧时,只生成KO
2
B.钾与水反应,由于反应剧烈可能会发生爆炸
C.1 mol·L-1KOH溶液比1 mol·L-1NaOH溶液碱性强(3)KH是一种野外供氢剂,其电子式为________,与水反应放出氢气,化学方程式为
________________________________________________________________________
________________________________________________________________________。
生成1 mol氢气时,反应中转移的电子数为__________________________________。
(4)NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe O),脱锈过程中
2 3
生成两种产物,其反应的化学方程式:______________________________________
________________________________________________________________________。
答案 (1)锂可以与水反应 (2)B
(3)K+[H ]- KH+HO===KOH+H↑
2 2
N (或6.02×1023)
A
(4)3NaH+Fe O===2Fe+3NaOH
2 3
1.正误判断,正确的打“√”,错误的打“×”。
(1)碳酸氢钠可做食品膨松剂(2022·全国乙卷,7B)( )
(2)焰火中红色来源于钠盐灼烧(2022·全国乙卷,7D)( )
(3)面包师用小苏打作发泡剂烘焙面包,是因为NaCO 可与酸反应(2022·广东,6A)( )
2 3
(4)NaHCO 的热稳定性比NaCO 强(2020·浙江7月选考,8B)( )
3 2 3
(5)盐碱地(含较多NaCO 等)不利于作物生长,可施加熟石灰进行改良(2019·天津,3C)(
2 3
)
(6)碳酸钠可用于去除餐具的油污(2018·全国卷Ⅱ,7A)( )
(7)溶解度:NaCOpH(NaHCO ),故A正确;实验后,
2 3 3 2 3 3
碳酸钠溶液和氯化钙溶液恰好反应生成碳酸钙沉淀和氯化钠,溶液中的离子主要有 Na+、Cl
-,而碳酸氢钠溶液和氯化钙溶液反应生成碳酸钙沉淀和氯化钠、碳酸,碳酸大部分分解为
二氧化碳气体和水,氯化钙有剩余,溶液中的离子主要有Na+、Cl-、Ca2+,故两者的离子
种类不完全相同,故B错误;加入氯化钙后,左侧试管中只有白色沉淀生成,则反应的化
学方程式为NaCO +CaCl ===CaCO ↓+2NaCl,右侧试管中有白色沉淀和无色气体产生,
2 3 2 3
则反应的化学方程式为2NaHCO +CaCl ===CaCO ↓+2NaCl+CO↑+HO,由化学方程式
3 2 3 2 2
可知起始CO、HCO的物质的量相同时,NaCO 溶液中生成的沉淀比NaHCO 溶液中生成
2 3 3
的沉淀多,故C正确;两试管中发生的反应均为复分解反应,故D正确。
6.下列各组中两种物质作用时,反应条件或反应物用量改变,对生成物没有影响的是(
)
A.NaOH溶液与CO
2
B.NaHCO 和盐酸
3
C.Na与O
2
D.NaHSO 溶液与Ba(OH) 溶液
4 2
答案 B
解析 NaOH溶液与CO 反应,少量的二氧化碳生成碳酸钠,过量的二氧化碳生成碳酸氢钠,
2
A不符合题意;无论NaHCO 和盐酸的量多少,无论条件如何,反应均生成氯化钠、水和二
3
氧化碳,B符合题意;Na与O 不加热生成NaO,加热生成NaO,C不符合题意;NaHSO
2 2 2 2 4
溶液与Ba(OH) 溶液反应,NaHSO 少量,产物为硫酸钡、氢氧化钠、水,NaHSO 过量,产
2 4 4
物为硫酸钡、硫酸钠、水,D不符合题意。
7.(2023·厦门模拟)以不同类别物质间的转化为线索,认识钠及其化合物。
下列分析不正确的是( )
A.反应③表明CO 具有酸性氧化物的性质
2
B.反应④说明NaHCO 的热稳定性强于NaCO
3 2 3
C.反应⑤⑥可用于潜水艇中氧气的供给
D.上述转化中发生的反应有分解反应、化合反应、置换反应答案 B
解析 二氧化碳与氢氧化钠反应生成碳酸钠和水,则反应③表明CO 具有酸性氧化物的性质,
2
故 A 正确;碳酸氢钠受热分解生成碳酸钠,则反应④说明 NaCO 的热稳定性强于
2 3
NaHCO ,故B错误;过氧化钠与水、二氧化碳反应生成氧气,可用于潜水艇中氧气的供给,
3
故C正确;④是分解反应,①是化合反应,②是置换反应,故D正确。
8.钠元素广泛存在于自然界,中国科学技术大学的钱逸泰教授等以 CCl 和金属钠为原料,
4
在700 ℃时制造出纳米级金刚石粉末。该成果发表在世界权威杂志上,立刻被科学家们高
度评价为“稻草变黄金”。下列关于含钠元素的物质的说法错误的是( )
A.“稻草变黄金”的过程中元素种类没有改变
B.NaCl与NaCO 灼烧时火焰颜色相同
2 3
C.治疗胃酸过多可以用NaHCO ,糕点制作也可以用NaHCO
3 3
D.金属钠放置在空气中,最终会变成NaO
2 2
答案 D
解析 化学变化过程中元素守恒,所以此过程中元素种类没有改变,故 A正确;焰色试验
是元素的性质,钠元素的焰色为黄色,则NaCl与NaCO 灼烧时火焰颜色均为黄色,故B
2 3
正确;NaHCO 与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,所以可以用 NaHCO
3 3
治疗胃酸过多;NaHCO 受热分解生成二氧化碳气体,遇热膨胀而形成小孔,使得糕点松软
3
多孔,故糕点制作也可以用NaHCO ,故C正确。
3
9.碱金属元素是金属性表现的最鲜明和最有规律的一族元素。下列说法正确的是( )
A.碱金属单质中锂的密度最小,熔点最低
B.25 ℃时碳酸钾溶液的pH<7
C.乙醇与金属钾反应生成氢气
D.用电解铯盐溶液的方法冶炼金属铯
答案 C
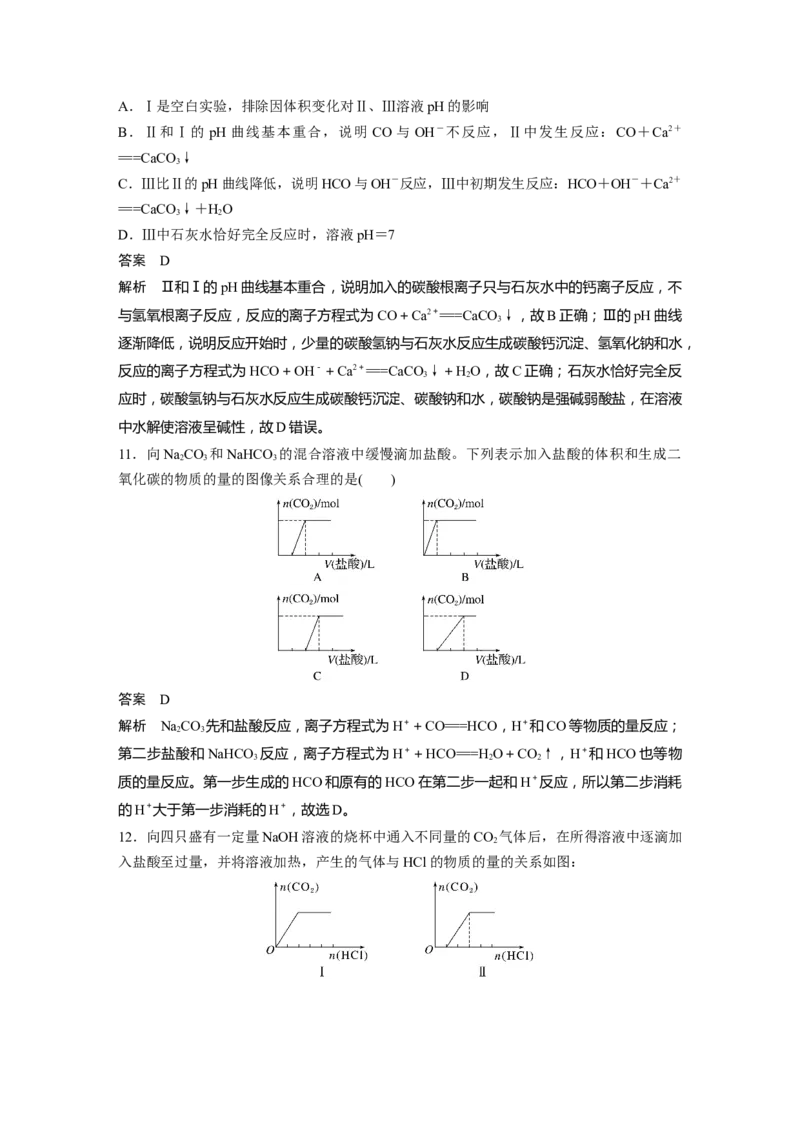
10.某化学实验小组探究NaCO 和NaHCO 与碱的反应,实验过程及结果如下。
2 3 3
实验装置 试剂X 实验结果
Ⅰ Ⅱ Ⅲ ①Ⅱ、Ⅲ均产生白色沉淀
②烧杯中溶液pH变化如下:
蒸
0.05 mol·L-1 0.05 mol·L-1
馏
NaCO 溶液 NaHCO 溶液
2 3 3
水
已知:pH越大,c(OH-)越大,溶液碱性越强。
下列说法不正确的是( )A.Ⅰ是空白实验,排除因体积变化对Ⅱ、Ⅲ溶液pH的影响
B.Ⅱ和Ⅰ的 pH 曲线基本重合,说明 CO 与 OH-不反应,Ⅱ中发生反应:CO+Ca2+
===CaCO ↓
3
C.Ⅲ比Ⅱ的pH曲线降低,说明HCO与OH-反应,Ⅲ中初期发生反应:HCO+OH-+Ca2+
===CaCO ↓+HO
3 2
D.Ⅲ中石灰水恰好完全反应时,溶液pH=7
答案 D
解析 Ⅱ和Ⅰ的pH曲线基本重合,说明加入的碳酸根离子只与石灰水中的钙离子反应,不
与氢氧根离子反应,反应的离子方程式为CO+Ca2+===CaCO ↓,故B正确;Ⅲ的pH曲线
3
逐渐降低,说明反应开始时,少量的碳酸氢钠与石灰水反应生成碳酸钙沉淀、氢氧化钠和水,
反应的离子方程式为HCO+OH-+Ca2+===CaCO ↓+HO,故C正确;石灰水恰好完全反
3 2
应时,碳酸氢钠与石灰水反应生成碳酸钙沉淀、碳酸钠和水,碳酸钠是强碱弱酸盐,在溶液
中水解使溶液呈碱性,故D错误。
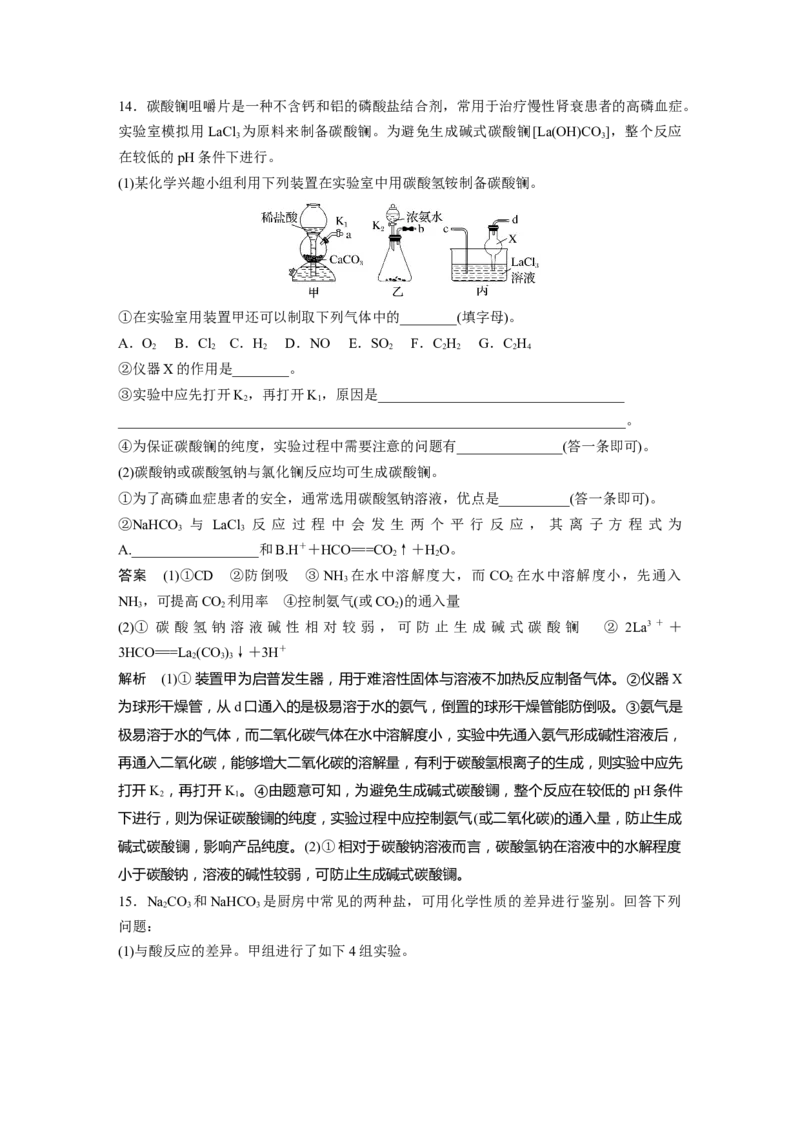
11.向NaCO 和NaHCO 的混合溶液中缓慢滴加盐酸。下列表示加入盐酸的体积和生成二
2 3 3
氧化碳的物质的量的图像关系合理的是( )
答案 D
解析 NaCO 先和盐酸反应,离子方程式为H++CO===HCO,H+和CO等物质的量反应;
2 3
第二步盐酸和NaHCO 反应,离子方程式为H++HCO===HO+CO↑,H+和HCO也等物
3 2 2
质的量反应。第一步生成的HCO和原有的HCO在第二步一起和H+反应,所以第二步消耗
的H+大于第一步消耗的H+,故选D。
12.向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO 气体后,在所得溶液中逐滴加
2
入盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图:则下列分析都正确的是( )
选项 溶质的成分 对应图像 溶液中离子浓度关系
A NaHCO 、NaCO Ⅱ c(CO)c(CO)
2 3
C NaCO Ⅳ c(Na+)=c(CO)+c(HCO)+c(H CO)
2 3 2 3
D NaHCO Ⅰ c(Na+)=c(HCO)
3
答案 A
13.实验室使用pH传感器来测定NaCO 和NaHCO 混合物中NaHCO 的含量。称取1.59 g
2 3 3 3
样品,溶于水配成250.00 mL溶液,取出该溶液25.00 mL用 0.1 mol·L-1盐酸进行滴定,得
到如下曲线。以下说法或操作正确的是( )
A.计量点①前发生反应的离子方程式为HCO+H+===HO+CO↑
2 2
B.计量点②溶液中大量存在的阴离子是Cl-、HCO
C.此样品n(NaHCO )=(28.1-2×11.9)×10-3 mol
3
D.使用该方法测定NaCO 和NaOH混合溶液中氢氧化钠的含量,只会得到1个计量点
2 3
答案 C
解析 根据图示知,计量点①前发生反应的离子方程式:CO+H+===HCO,故A错误;计
量点②溶液pH=4,呈酸性,HCO不能存在,故B错误;NaCO 和NaHCO 混合溶液中加
2 3 3
盐酸,首先是碳酸钠转化为碳酸氢钠:CO+H+===HCO,此时消耗盐酸的体积为11.9 mL,
随后是碳酸氢钠转化为CO 的过程:HCO+H+===HO+CO↑,由于CO+H+===HCO过
2 2 2
程和 HCO+H+===H O+CO ↑过程消耗盐酸的体积相同,所以碳酸钠消耗的盐酸为
2 2
2×11.9 mL,则碳酸氢钠消耗的盐酸n(HCl)=(28.1-2×11.9)×10-3 L×0.1 mol·L-1=(28.1
-2×11.9)×10-4 mol,所以此样品中n(NaHCO )=(28.1-2×11.9)×10-4 mol×10=(28.1-
3
2×11.9)×10-3 mol,故C正确;NaCO 和NaOH混合溶液中加入盐酸,盐酸先是和氢氧化
2 3
钠中和,随后是和碳酸钠发生反应,生成碳酸氢钠,最后生成氯化钠,会得到 3个计量点,
故D错误。14.碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,常用于治疗慢性肾衰患者的高磷血症。
实验室模拟用LaCl 为原料来制备碳酸镧。为避免生成碱式碳酸镧[La(OH)CO ],整个反应
3 3
在较低的pH条件下进行。
(1)某化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
①在实验室用装置甲还可以制取下列气体中的________(填字母)。
A.O B.Cl C.H D.NO E.SO F.C H G.C H
2 2 2 2 2 2 2 4
②仪器X的作用是________。
③实验中应先打开K,再打开K,原因是___________________________________
2 1
________________________________________________________________________。
④为保证碳酸镧的纯度,实验过程中需要注意的问题有_______________(答一条即可)。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,优点是__________(答一条即可)。
②NaHCO 与 LaCl 反 应 过 程 中 会 发 生 两 个 平 行 反 应 , 其 离 子 方 程 式 为
3 3
A.__________________和B.H++HCO===CO↑+HO。
2 2
答案 (1)①CD ②防倒吸 ③NH 在水中溶解度大,而 CO 在水中溶解度小,先通入
3 2
NH ,可提高CO 利用率 ④控制氨气(或CO)的通入量
3 2 2
(2)① 碳 酸 氢 钠 溶 液 碱 性 相 对 较 弱 , 可 防 止 生 成 碱 式 碳 酸 镧 ② 2La3 + +
3HCO===La(CO)↓+3H+
2 3 3
解析 (1)①装置甲为启普发生器,用于难溶性固体与溶液不加热反应制备气体。②仪器X
为球形干燥管,从d口通入的是极易溶于水的氨气,倒置的球形干燥管能防倒吸。③氨气是
极易溶于水的气体,而二氧化碳气体在水中溶解度小,实验中先通入氨气形成碱性溶液后,
再通入二氧化碳,能够增大二氧化碳的溶解量,有利于碳酸氢根离子的生成,则实验中应先
打开K ,再打开K 。④由题意可知,为避免生成碱式碳酸镧,整个反应在较低的pH条件
2 1
下进行,则为保证碳酸镧的纯度,实验过程中应控制氨气(或二氧化碳)的通入量,防止生成
碱式碳酸镧,影响产品纯度。(2)①相对于碳酸钠溶液而言,碳酸氢钠在溶液中的水解程度
小于碳酸钠,溶液的碱性较弱,可防止生成碱式碳酸镧。
15.NaCO 和NaHCO 是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列
2 3 3
问题:
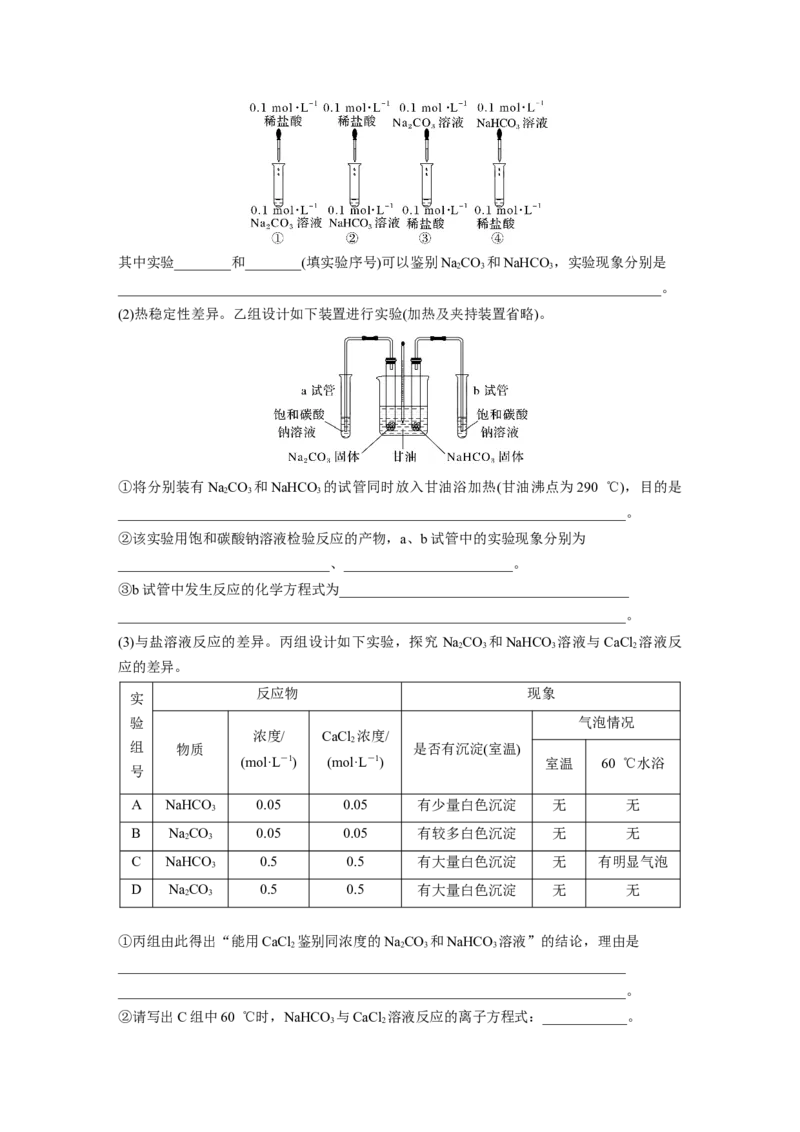
(1)与酸反应的差异。甲组进行了如下4组实验。其中实验________和________(填实验序号)可以鉴别NaCO 和NaHCO ,实验现象分别是
2 3 3
_____________________________________________________________________________。
(2)热稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。
①将分别装有NaCO 和NaHCO 的试管同时放入甘油浴加热(甘油沸点为290 ℃),目的是
2 3 3
________________________________________________________________________。
②该实验用饱和碳酸钠溶液检验反应的产物,a、b试管中的实验现象分别为
______________________________、________________________。
③b试管中发生反应的化学方程式为_________________________________________
________________________________________________________________________。
(3)与盐溶液反应的差异。丙组设计如下实验,探究 NaCO 和NaHCO 溶液与CaCl 溶液反
2 3 3 2
应的差异。
反应物 现象
实
验 气泡情况
浓度/ CaCl 浓度/
2
组 物质 是否有沉淀(室温)
(mol·L-1) (mol·L-1) 室温 60 ℃水浴
号
A NaHCO 0.05 0.05 有少量白色沉淀 无 无
3
B NaCO 0.05 0.05 有较多白色沉淀 无 无
2 3
C NaHCO 0.5 0.5 有大量白色沉淀 无 有明显气泡
3
D NaCO 0.5 0.5 有大量白色沉淀 无 无
2 3
①丙组由此得出“能用CaCl 鉴别同浓度的NaCO 和NaHCO 溶液”的结论,理由是
2 2 3 3
________________________________________________________________________
________________________________________________________________________。
②请写出C组中60 ℃时,NaHCO 与CaCl 溶液反应的离子方程式:____________。
3 2答案 (1)① ② 碳酸钠溶液中逐滴加入盐酸,开始无现象,后来产生气泡;碳酸氢钠溶
液中逐滴加入盐酸,开始就有气泡产生
(2)①提供较高温度,便于盐分解实验 ②a试管中开始有少量气泡,后来无现象 b试管中
有气泡,后有晶体析出 ③CO+HO+NaCO===2NaHCO ↓
2 2 2 3 3
(3)①在浓度较稀时,与CaCl 反应产生较多沉淀的是NaCO ,产生少量沉淀的是NaHCO
2 2 3 3
②2HCO+Ca2+===CaCO ↓+CO↑+HO
3 2 2
解析 (1)碳酸钠溶液中逐滴加入盐酸,开始无现象,后来产生气泡,碳酸氢钠溶液中逐滴
加入盐酸,开始就有气泡,因此实验①和②可以鉴别NaCO 和NaHCO 。(2)②该实验用饱
2 3 3
和碳酸钠溶液检验反应的产物,碳酸钠受热不分解,碳酸氢钠受热分解生成二氧化碳气体、
水和碳酸钠,二氧化碳气体与饱和碳酸钠溶液反应生成碳酸氢钠晶体。(3)②C组中60 ℃时,
NaHCO 与CaCl 溶液反应能产生气泡,根据质量守恒说明气泡是二氧化碳气体,其离子方
3 2
程式为2HCO+Ca2+===CaCO ↓+CO↑+HO。
3 2 2