文档内容
第 36 讲 晶胞结构分析与计算
[复习目标] 1.掌握均摊法计算的一般方法,能根据晶胞中微粒的位置计算晶胞的化学式。
2.掌握晶体密度与晶胞参数计算的一般步骤。
考点一 晶胞模型与均摊法计算
1.晶胞中微粒数的计算方法——均摊法
(1)长方体(包括立方体)晶胞中不同位置的粒子数的计算
如某个粒子为N个晶胞所共有,则该粒子有属于这个晶胞。中学中常见的晶胞为立方晶胞,
立方晶胞中微粒数的计算方法如图1。
(2)非长方体晶胞
在六棱柱(如图2)中,顶角上的原子有属于此晶胞,面上的原子有属于此晶胞,因此六棱柱
中镁原子个数为12×+2×=3,硼原子个数为6。
2.三种典型立方晶胞结构
3.晶胞中微粒配位数的计算
一个粒子周围最邻近的粒子数称为配位数,它反映了晶体中粒子排列的紧密程度。
(1)晶体中原子(或分子)的配位数
若晶体中的微粒为同种原子或同种分子,则某原子(或分子)的配位数指的是该原子(或分子)
最接近且等距离的原子(或分子)的数目,常见晶胞的配位数如下:
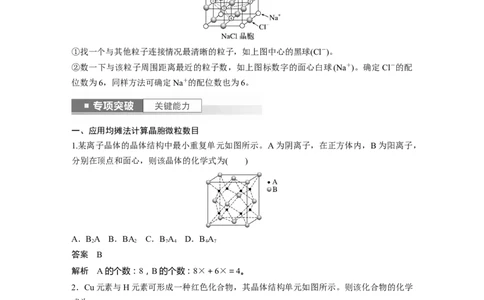
简单立方:配位数为6 面心立方:配位数为12 体心立方:配位数为8(2)离子晶体的配位数
指一个离子周围最接近且等距离的异种电性离子的数目。
以NaCl晶体为例
①找一个与其他粒子连接情况最清晰的粒子,如上图中心的黑球(Cl-)。
②数一下与该粒子周围距离最近的粒子数,如上图标数字的面心白球(Na+)。确定Cl-的配
位数为6,同样方法可确定Na+的配位数也为6。
一、应用均摊法计算晶胞微粒数目
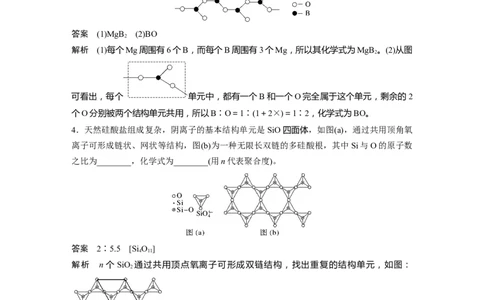
1.某离子晶体的晶体结构中最小重复单元如图所示。A为阴离子,在正方体内,B为阳离子,
分别在顶点和面心,则该晶体的化学式为( )
A.B A B.BA C.B A D.B A
2 2 7 4 4 7
答案 B
解析 A的个数:8,B的个数:8×+6×=4。
2.Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学
式为________。
答案 CuH
解析 根据晶胞结构可以判断:Cu:2×+12×+3=6;H:6×+1+3=6,所以化学式为
CuH。3.(1)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,
下图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化
学式为________。
(2)在硼酸盐中,阴离子有链状、环状等多种结构形式。如图是一种链状结构的多硼酸根,
则多硼酸根离子符号为________。
答案 (1)MgB (2)BO
2
解析 (1)每个Mg周围有6个B,而每个B周围有3个Mg,所以其化学式为MgB 。(2)从图
2
可看出,每个 单元中,都有一个B和一个O完全属于这个单元,剩余的2
个O分别被两个结构单元共用,所以B∶O=1∶(1+2×)=1∶2,化学式为BO。
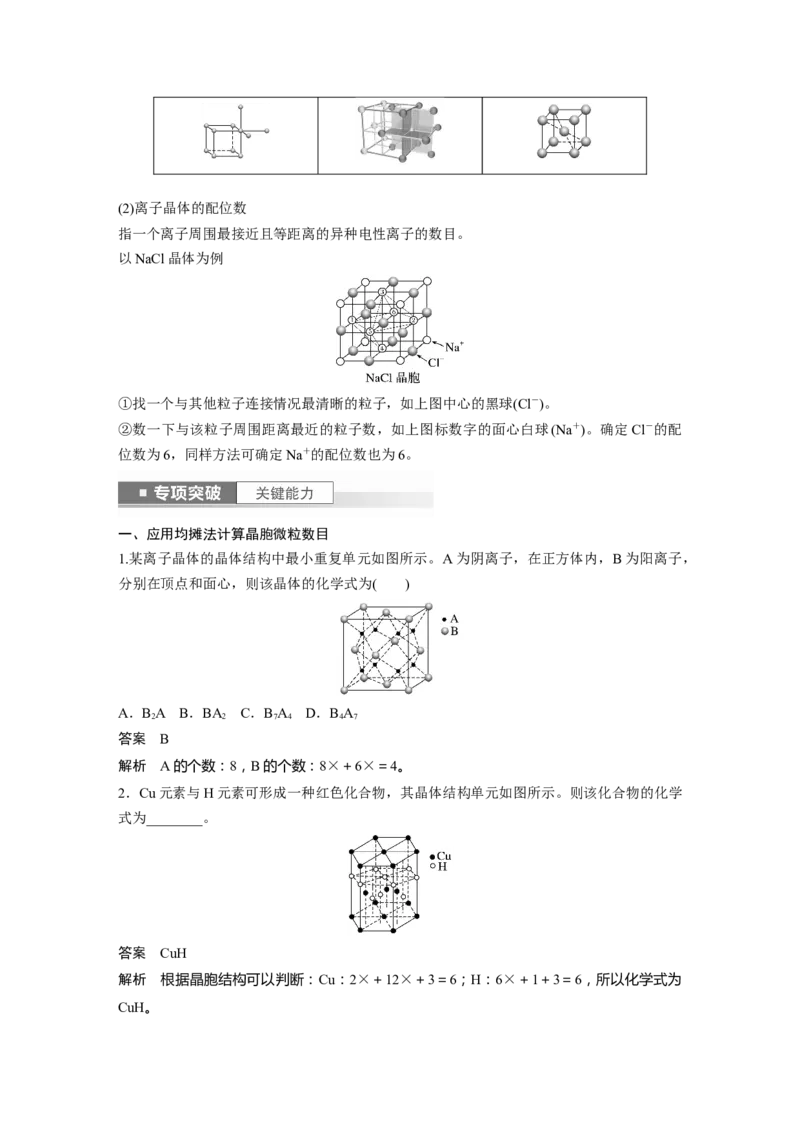
4.天然硅酸盐组成复杂,阴离子的基本结构单元是SiO四面体,如图(a),通过共用顶角氧
离子可形成链状、网状等结构,图(b)为一种无限长双链的多硅酸根,其中Si与O的原子数
之比为________,化学式为________(用n代表聚合度)。
答案 2∶5.5 [Si O ]
4 11
解析 n个SiO 通过共用顶点氧离子可形成双链结构,找出重复的结构单元,如图:
2
,由于是双链,其中顶点氧占,Si原子数为4,O原子数为4×+
6×+4+2=11,其中Si与O的原子数之比为2∶5.5,化学式为[Si O ]。
4 11
二、晶胞中粒子配位数计算
5.硅化镁是一种窄带隙n型半导体材料,在光电子器件、能源器件、激光、半导体制造等领
域具有重要应用前景。硅化镁的晶胞参数a=0.639 1 nm,属于面心立方晶胞,结构如图所
示。Si原子的配位数为________。答案 8
解析 根据晶胞结构,以面心Si原子为基准,同一晶胞内等距离且最近的Mg原子有4个,
紧邻晶胞还有4个Mg原子,共8个,故Si原子的配位数为8。
6.如图是一种由Y(与Sc同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球
代表Y,四方锥中心和八面体中心的球代表Fe,其余小球代表O。
(1)该晶体的化学式为________。
(2)其中Y的配位数为________。
答案 (1)YBa Fe O (2)8
2 3 8
解析 (1)由晶胞结构可知,Y位于顶点,原子数为×8=1;Ba位于棱上,原子数为×8=2;
O原子有12个位于面上,2个位于晶胞内,原子数为×12+2=8;3个Fe原子位于晶胞内,
该晶体的化学式为YBa Fe O 。(2)从晶胞结构知Y位于晶胞顶点,距离Y最近的原子共有8
2 3 8
个,即Y的配位数为8。
考点二 晶胞参数计算
1.晶胞参数
晶胞的形状和大小可以用6个参数来表示,包括晶胞的3组棱长a、b、c和3组棱相互间的
夹角α、β、γ,即晶格特征参数,简称晶胞参数。
2.晶体结构的相关计算
(1)空间利用率=×100%。
(2)金属晶体中体心立方堆积、面心立方堆积中的几组计算公式(设棱长为a)
①面对角线长=a。
②体对角线长=a。
③体心立方堆积4r=a(r为原子半径)。④面心立方堆积4r=a(r为原子半径)。
3.宏观晶体密度与微观晶胞参数的关系
例 钒的某种氧化物的立方晶胞结构如图所示,晶胞参数为 a pm。下列说法错误的是(
)
A.该钒的氧化物的化学式为VO
2
B.V原子在该晶体中的堆积方式为体心立方
C.V原子的配位数与O原子的配位数之比为1∶2
D.该晶胞的密度为 g·cm-3
答案 C
解析 晶胞中V原子位于顶角和体心,数目为1+8×=2;O原子位于上下面上和体内,数
目为2+4×=4,二者原子数目之比为1∶2,故氧化物的化学式为VO ,故A正确;晶胞V
2
原子位于顶角和体心,符合体心立方的堆积方式,故B正确;体心V原子的配位数为6,O
原子的配位数为3,所以V原子的配位数与O原子的配位数之比为2∶1,故C错误;m=
g,V=a3 pm3=(a×10-10)3cm3,ρ== g·cm-3,故D正确。
1.Zn与S所形成化合物晶体的晶胞如图所示。Zn2+的配位数是________,S2-填充在Zn2+形
成的正四面体空隙中。若该晶体的密度为d g·cm-3,阿伏加德罗常数的值为N ,则该晶胞
A
参数a= ________ nm。
答案 4 ×107
解析 根据晶胞结构可知晶胞中含有Zn2+个数为8×+6×=4,S2-全部在晶胞内,共4个,
其化学式是ZnS。根据晶胞结构可知S2-位于4个Zn2+形成的正四面体空隙中,S2-的配位数
是4,根据化学式可判断Zn2+的配位数也是4。若该晶体的密度为d g·cm-3,阿伏加德罗常数的值为N ,则d=,因此该晶胞参数a= cm=×107 nm。
A
2.如图是Fe单质的晶胞模型。已知晶体密度为d g·cm-3,铁原子的半径为________ nm(用
含有d、N 的代数式表示)。
A
答案 ××107
解析 由Fe单质的晶胞图可知,晶胞中含铁原子个数为 2,晶胞的质量为 g,晶胞体积为
cm3,则晶胞边长为 cm,设Fe原子的半径为r,则4r=× cm,r=××107 nm。
3.立方氮化硼的硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立
方氮化硼属于________晶体,其中硼原子的配位数为________。已知:立方氮化硼的密度为
d g·cm-3,B原子半径为x pm,N原子半径为y pm,阿伏加德罗常数的值为N ,则该晶胞
A
中原子的空间利用率为______________(列出化简后的计算式)。
答案 共价 4 ×100%
解析 立方氮化硼的硬度仅次于金刚石,晶体类型类似于金刚石,是共价晶体;晶胞中每个
N原子连接4个B原子,氮化硼的化学式为BN,所以晶胞中每个B原子也连接4个N原子,
即硼原子的配位数为4;晶胞中N原子数为4,B原子数为8×+6×=4,晶胞的质量m=
g,晶胞的体积 V== cm3= cm3,B、N原子总体积 V′=4×[+]=×(x3+y3)×10-30
cm3,晶胞中原子的空间利用率为×100%=×100%=×100%。
4.氮化硼是一种性能优异的新型材料,主要结构有六方氮化硼(图1)和立方氮化硼(图2)。
前者与石墨结构类似。
(1)50.0 g六方氮化硼晶体中含有六元环的数目为______。
(2)立方氮化硼中N的配位数为________。已知立方氮化硼密度为d g·cm-3,N 代表阿伏加
A
德罗常数的值,立方氮化硼晶胞中面心上6个N原子相连构成正八面体,该正八面体的边
长为________ pm(列式即可)。
答案 (1)2N (2)4 ××1010
A
解析 (1)根据均摊法,一个六方氮化硼晶体的六元环含有一个N、一个B,50.0 g六方氮化硼晶体中含有六元环的数目为×N =2N 。
A A
(2)由图2可知,立方氮化硼中N的配位数为4;面心上6个N原子构成正八面体,该正八面
体的边长等于面对角线的一半,设BN晶胞边长为a cm,1个晶胞中含有4个B原子,含有
N原子数为8×+6×=4,则1个晶胞中含有4个BN,所以d=,解得a=,故正八面体的
边长为××1010 pm。
1.[2022·江苏,14(2)]FeS 具有良好半导体性能。FeS 的一种晶体与NaCl晶体的结构相似,
2 2
该FeS 晶体的一个晶胞中S的数目为__________,在FeS 晶体中,每个S原子与三个Fe2+
2 2
紧邻,且Fe—S间距相等,如图给出了FeS 晶胞中的Fe2+和位于晶胞体心的S(S中的S—S
2
键位于晶胞体对角线上,晶胞中的其他S已省略)。如图中用“-”将其中一个S原子与紧
邻的Fe2+连接起来。
答案 4
解析 因为FeS 的晶体与NaCl晶体的结构相似,由NaCl晶体结构可知,一个NaCl晶胞含
2
有4个Na和4个Cl,则该FeS 晶体的一个晶胞中S的数目也为4;FeS 晶体中,每个S原
2 2
子与三个Fe2+紧邻,且Fe—S间距相等,根据FeS 晶胞中的Fe2+和S的位置(S中的S—S键
2
位于晶胞体对角线上)可知,每个S原子与S—S键所在体对角线上距离最近的顶点相邻的三
个面的三个面心位置的 Fe2+紧邻且间距相等,其中一个 S原子与紧邻的 Fe2+连接图为
。
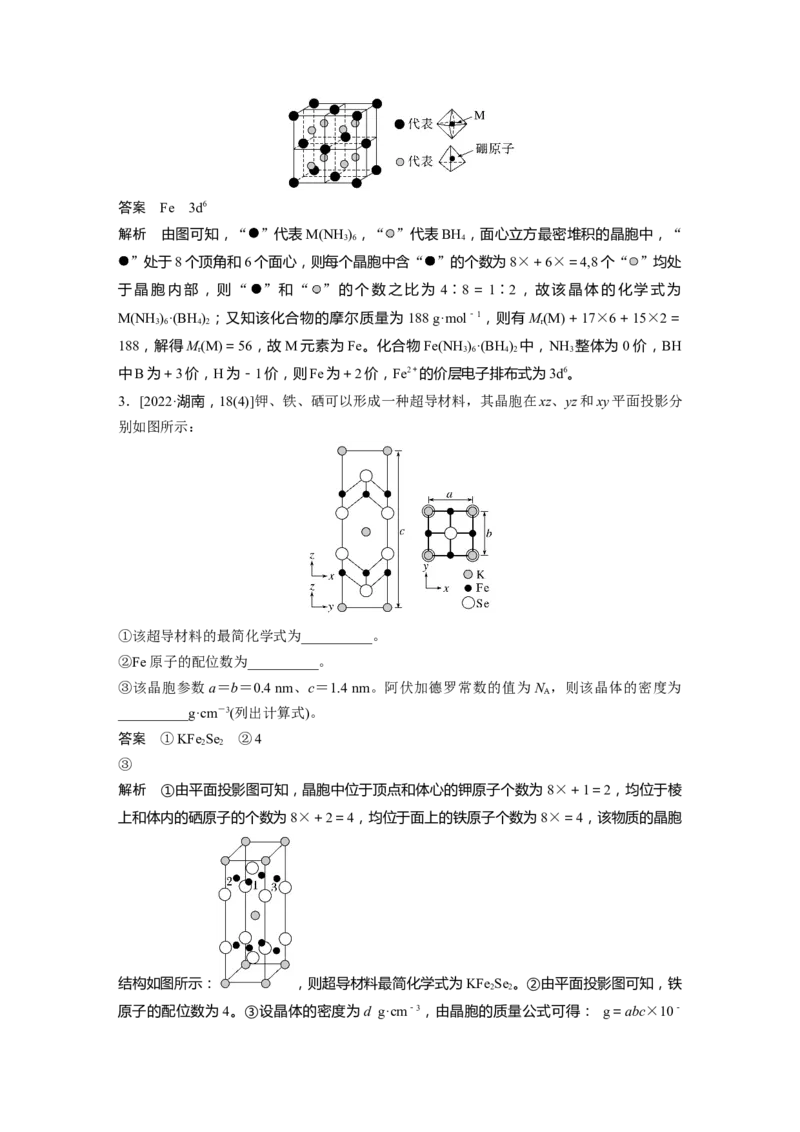
2.[2022·辽宁,18(6)]某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为
NH 配体;四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为 188 g·mol-1,则M元
3
素为__________(填元素符号);在该化合物中,M离子的价层电子排布式为______________。答案 Fe 3d6
解析 由图可知,“ ”代表M(NH) ,“ ”代表BH ,面心立方最密堆积的晶胞中,“
3 6 4
”处于8个顶角和6个面心,则每个晶胞中含“ ”的个数为8×+6×=4,8个“ ”均处
于晶胞内部,则“ ”和“ ”的个数之比为 4∶8=1∶2,故该晶体的化学式为
M(NH)·(BH ) ;又知该化合物的摩尔质量为188 g·mol-1,则有M(M)+17×6+15×2=
3 6 4 2 r
188,解得M(M)=56,故M元素为Fe。化合物Fe(NH )·(BH ) 中,NH 整体为0价,BH
r 3 6 4 2 3
中B为+3价,H为-1价,则Fe为+2价,Fe2+的价层电子排布式为3d6。
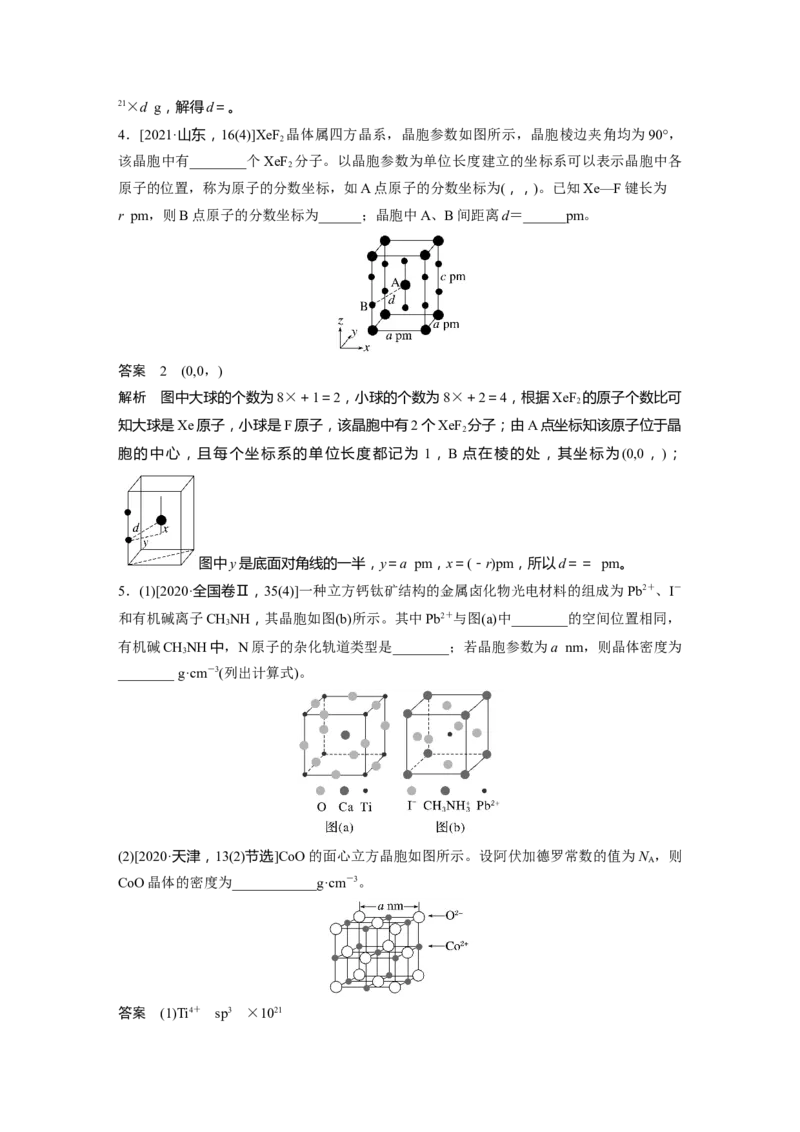
3.[2022·湖南,18(4)]钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分
别如图所示:
①该超导材料的最简化学式为__________。
②Fe原子的配位数为__________。
③该晶胞参数a=b=0.4 nm、c=1.4 nm。阿伏加德罗常数的值为N ,则该晶体的密度为
A
__________g·cm-3(列出计算式)。
答案 ①KFe Se ②4
2 2
③
解析 ①由平面投影图可知,晶胞中位于顶点和体心的钾原子个数为 8×+1=2,均位于棱
上和体内的硒原子的个数为8×+2=4,均位于面上的铁原子个数为8×=4,该物质的晶胞
结构如图所示: ,则超导材料最简化学式为KFe Se 。②由平面投影图可知,铁
2 2
原子的配位数为4。③设晶体的密度为d g·cm-3,由晶胞的质量公式可得: g=abc×10-21×d g,解得d=。
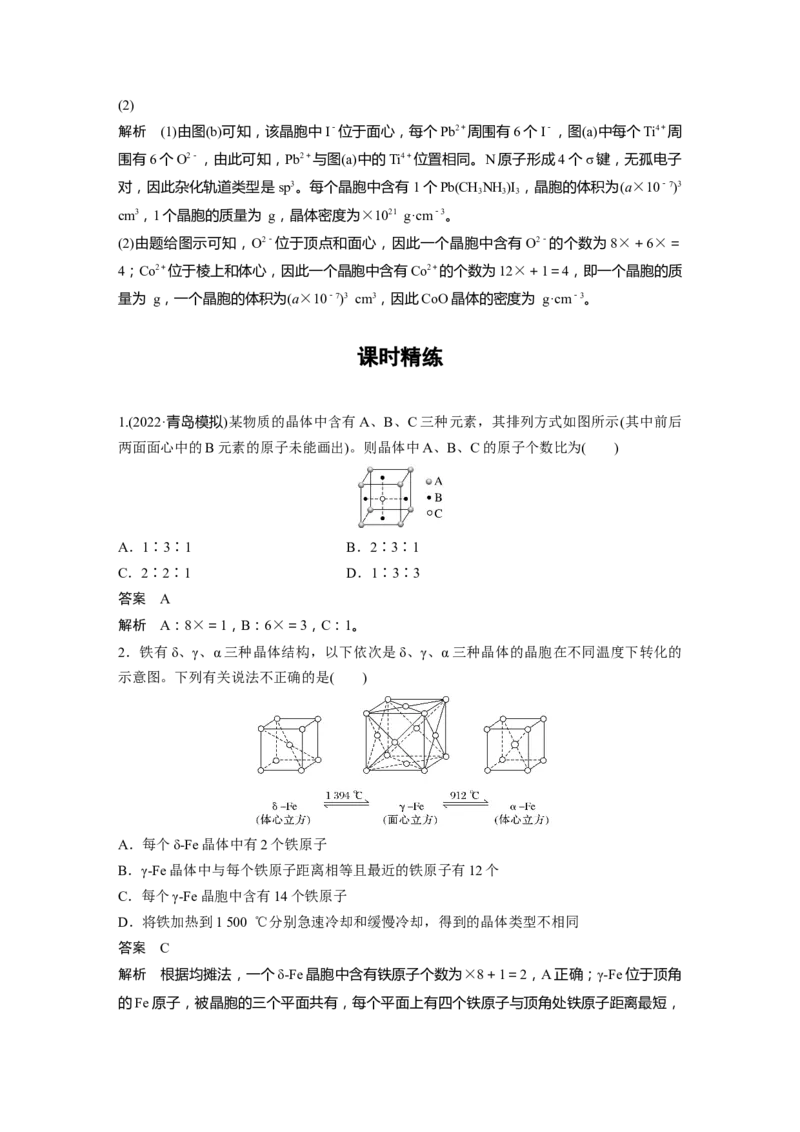
4.[2021·山东,16(4)]XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,
2
该晶胞中有________个XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各
2
原子的位置,称为原子的分数坐标,如A点原子的分数坐标为(,,)。已知Xe—F键长为
r pm,则B点原子的分数坐标为______;晶胞中A、B间距离d=______pm。
答案 2 (0,0,)
解析 图中大球的个数为8×+1=2,小球的个数为8×+2=4,根据XeF 的原子个数比可
2
知大球是Xe原子,小球是F原子,该晶胞中有2个XeF 分子;由A点坐标知该原子位于晶
2
胞的中心,且每个坐标系的单位长度都记为 1,B 点在棱的处,其坐标为(0,0,);
图中y是底面对角线的一半,y=a pm,x=(-r)pm,所以d== pm。
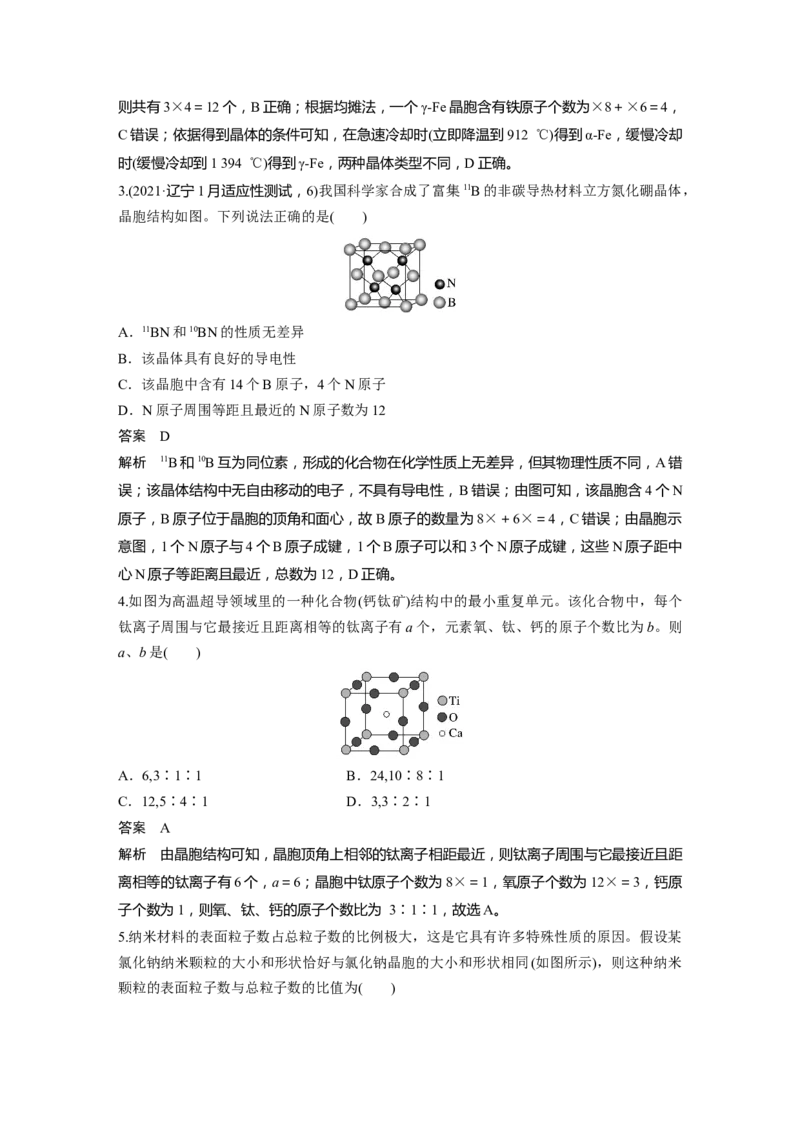
5.(1)[2020·全国卷Ⅱ,35(4)]一种立方钙钛矿结构的金属卤化物光电材料的组成为 Pb2+、I-
和有机碱离子CHNH,其晶胞如图(b)所示。其中Pb2+与图(a)中________的空间位置相同,
3
有机碱CHNH中,N原子的杂化轨道类型是________;若晶胞参数为a nm,则晶体密度为
3
________ g·cm-3(列出计算式)。
(2)[2020·天津,13(2)节选]CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为N ,则
A
CoO晶体的密度为____________g·cm-3。
答案 (1)Ti4+ sp3 ×1021(2)
解析 (1)由图(b)可知,该晶胞中I-位于面心,每个Pb2+周围有6个I-,图(a)中每个Ti4+周
围有6个O2-,由此可知,Pb2+与图(a)中的Ti4+位置相同。N原子形成4个σ键,无孤电子
对,因此杂化轨道类型是 sp3。每个晶胞中含有1个Pb(CH NH )I ,晶胞的体积为(a×10-7)3
3 3 3
cm3,1个晶胞的质量为 g,晶体密度为×1021 g·cm-3。
(2)由题给图示可知,O2-位于顶点和面心,因此一个晶胞中含有O2-的个数为8×+6×=
4;Co2+位于棱上和体心,因此一个晶胞中含有Co2+的个数为12×+1=4,即一个晶胞的质
量为 g,一个晶胞的体积为(a×10-7)3 cm3,因此CoO晶体的密度为 g·cm-3。
课时精练
1.(2022·青岛模拟)某物质的晶体中含有A、B、C三种元素,其排列方式如图所示(其中前后
两面面心中的B元素的原子未能画出)。则晶体中A、B、C的原子个数比为( )
A.1∶3∶1 B.2∶3∶1
C.2∶2∶1 D.1∶3∶3
答案 A
解析 A:8×=1,B:6×=3,C:1。
2.铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体的晶胞在不同温度下转化的
示意图。下列有关说法不正确的是( )
A.每个δ-Fe晶体中有2个铁原子
B.γ-Fe晶体中与每个铁原子距离相等且最近的铁原子有12个
C.每个γ-Fe晶胞中含有14个铁原子
D.将铁加热到1 500 ℃分别急速冷却和缓慢冷却,得到的晶体类型不相同
答案 C
解析 根据均摊法,一个δ-Fe晶胞中含有铁原子个数为×8+1=2,A正确;γ-Fe位于顶角
的Fe原子,被晶胞的三个平面共有,每个平面上有四个铁原子与顶角处铁原子距离最短,则共有3×4=12个,B正确;根据均摊法,一个γ-Fe晶胞含有铁原子个数为×8+×6=4,
C错误;依据得到晶体的条件可知,在急速冷却时(立即降温到912 ℃)得到α-Fe,缓慢冷却
时(缓慢冷却到1 394 ℃)得到γ-Fe,两种晶体类型不同,D正确。
3.(2021·辽宁1月适应性测试,6)我国科学家合成了富集11B的非碳导热材料立方氮化硼晶体,
晶胞结构如图。下列说法正确的是( )
A.11BN和10BN的性质无差异
B.该晶体具有良好的导电性
C.该晶胞中含有14个B原子,4个N原子
D.N原子周围等距且最近的N原子数为12
答案 D
解析 11B和10B互为同位素,形成的化合物在化学性质上无差异,但其物理性质不同,A错
误;该晶体结构中无自由移动的电子,不具有导电性,B错误;由图可知,该晶胞含4个N
原子,B原子位于晶胞的顶角和面心,故B原子的数量为8×+6×=4,C错误;由晶胞示
意图,1个N原子与4个B原子成键,1个B原子可以和3个N原子成键,这些N原子距中
心N原子等距离且最近,总数为12,D正确。
4.如图为高温超导领域里的一种化合物(钙钛矿)结构中的最小重复单元。该化合物中,每个
钛离子周围与它最接近且距离相等的钛离子有a个,元素氧、钛、钙的原子个数比为b。则
a、b是( )
A.6,3∶1∶1 B.24,10∶8∶1
C.12,5∶4∶1 D.3,3∶2∶1
答案 A
解析 由晶胞结构可知,晶胞顶角上相邻的钛离子相距最近,则钛离子周围与它最接近且距
离相等的钛离子有6个,a=6;晶胞中钛原子个数为8×=1,氧原子个数为12×=3,钙原
子个数为1,则氧、钛、钙的原子个数比为 3∶1∶1,故选A。
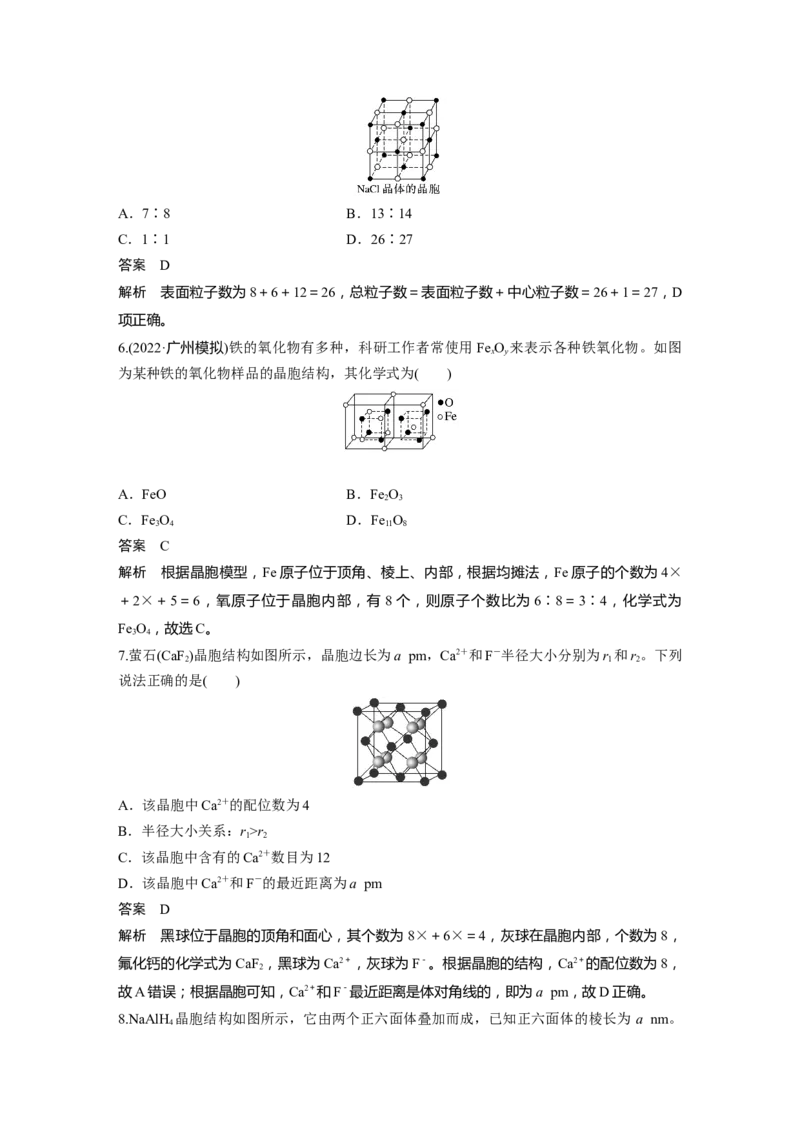
5.纳米材料的表面粒子数占总粒子数的比例极大,这是它具有许多特殊性质的原因。假设某
氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米
颗粒的表面粒子数与总粒子数的比值为( )A.7∶8 B.13∶14
C.1∶1 D.26∶27
答案 D
解析 表面粒子数为8+6+12=26,总粒子数=表面粒子数+中心粒子数=26+1=27,D
项正确。
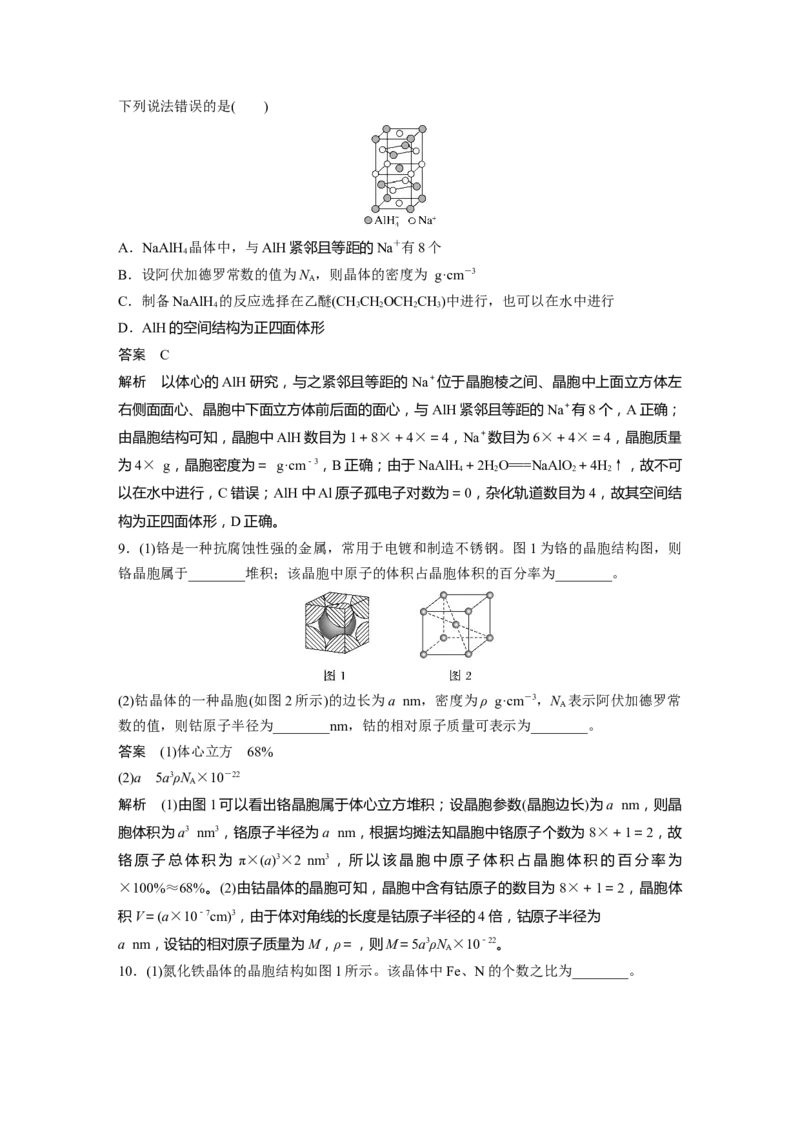
6.(2022·广州模拟)铁的氧化物有多种,科研工作者常使用FeO 来表示各种铁氧化物。如图
x y
为某种铁的氧化物样品的晶胞结构,其化学式为( )
A.FeO B.Fe O
2 3
C.Fe O D.Fe O
3 4 11 8
答案 C
解析 根据晶胞模型,Fe原子位于顶角、棱上、内部,根据均摊法,Fe原子的个数为4×
+2×+5=6,氧原子位于晶胞内部,有 8个,则原子个数比为 6∶8=3∶4,化学式为
Fe O,故选C。
3 4
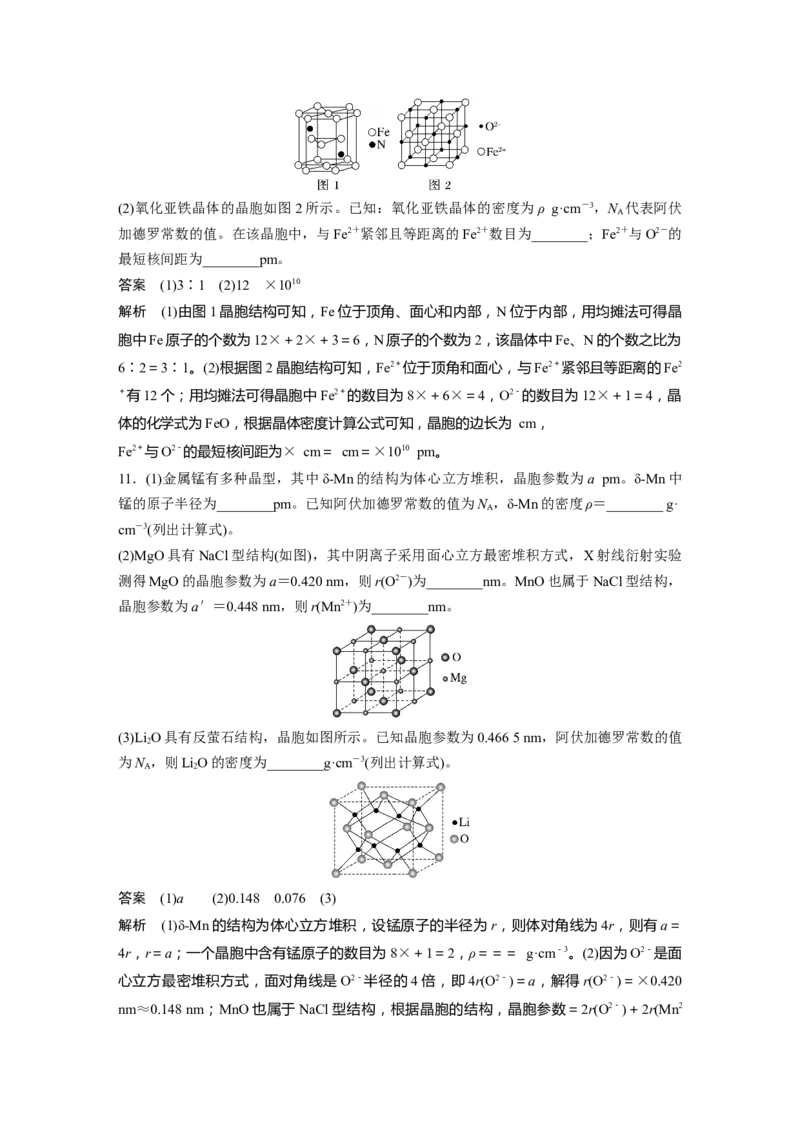
7.萤石(CaF )晶胞结构如图所示,晶胞边长为a pm,Ca2+和F-半径大小分别为r 和r。下列
2 1 2
说法正确的是( )
A.该晶胞中Ca2+的配位数为4
B.半径大小关系:r>r
1 2
C.该晶胞中含有的Ca2+数目为12
D.该晶胞中Ca2+和F-的最近距离为a pm
答案 D
解析 黑球位于晶胞的顶角和面心,其个数为8×+6×=4,灰球在晶胞内部,个数为8,
氟化钙的化学式为CaF ,黑球为Ca2+,灰球为F-。根据晶胞的结构,Ca2+的配位数为8,
2
故A错误;根据晶胞可知,Ca2+和F-最近距离是体对角线的,即为a pm,故D正确。
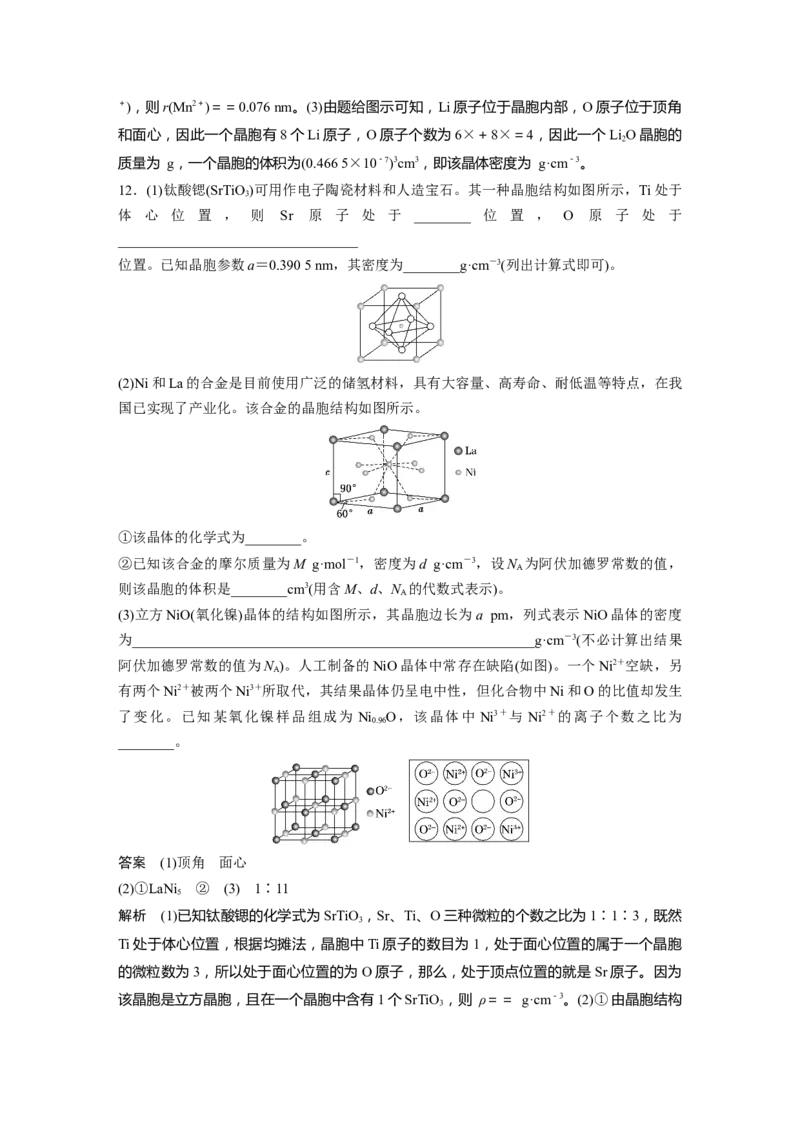
8.NaAlH 晶胞结构如图所示,它由两个正六面体叠加而成,已知正六面体的棱长为 a nm。
4下列说法错误的是( )
A.NaAlH 晶体中,与AlH紧邻且等距的Na+有8个
4
B.设阿伏加德罗常数的值为N ,则晶体的密度为 g·cm-3
A
C.制备NaAlH 的反应选择在乙醚(CHCHOCH CH)中进行,也可以在水中进行
4 3 2 2 3
D.AlH的空间结构为正四面体形
答案 C
解析 以体心的AlH研究,与之紧邻且等距的Na+位于晶胞棱之间、晶胞中上面立方体左
右侧面面心、晶胞中下面立方体前后面的面心,与AlH紧邻且等距的Na+有8个,A正确;
由晶胞结构可知,晶胞中AlH数目为1+8×+4×=4,Na+数目为6×+4×=4,晶胞质量
为4× g,晶胞密度为= g·cm-3,B正确;由于NaAlH +2HO===NaAlO +4H↑,故不可
4 2 2 2
以在水中进行,C错误;AlH中Al原子孤电子对数为=0,杂化轨道数目为4,故其空间结
构为正四面体形,D正确。
9.(1)铬是一种抗腐蚀性强的金属,常用于电镀和制造不锈钢。图1为铬的晶胞结构图,则
铬晶胞属于________堆积;该晶胞中原子的体积占晶胞体积的百分率为________。
(2)钴晶体的一种晶胞(如图2所示)的边长为a nm,密度为ρ g·cm-3,N 表示阿伏加德罗常
A
数的值,则钴原子半径为________nm,钴的相对原子质量可表示为________。
答案 (1)体心立方 68%
(2)a 5a3ρN ×10-22
A
解析 (1)由图1可以看出铬晶胞属于体心立方堆积;设晶胞参数(晶胞边长)为a nm,则晶
胞体积为a3 nm3,铬原子半径为a nm,根据均摊法知晶胞中铬原子个数为8×+1=2,故
铬原子总体积为 π×(a)3×2 nm3,所以该晶胞中原子体积占晶胞体积的百分率为
×100%≈68%。(2)由钴晶体的晶胞可知,晶胞中含有钴原子的数目为8×+1=2,晶胞体
积V=(a×10-7cm)3,由于体对角线的长度是钴原子半径的4倍,钴原子半径为
a nm,设钴的相对原子质量为M,ρ=,则M=5a3ρN ×10-22。
A
10.(1)氮化铁晶体的晶胞结构如图1所示。该晶体中Fe、N的个数之比为________。(2)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρ g·cm-3,N 代表阿伏
A
加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为________;Fe2+与O2-的
最短核间距为________pm。
答案 (1)3∶1 (2)12 ×1010
解析 (1)由图1晶胞结构可知,Fe位于顶角、面心和内部,N位于内部,用均摊法可得晶
胞中Fe原子的个数为12×+2×+3=6,N原子的个数为2,该晶体中Fe、N的个数之比为
6∶2=3∶1。(2)根据图2晶胞结构可知,Fe2+位于顶角和面心,与Fe2+紧邻且等距离的Fe2
+有12个;用均摊法可得晶胞中Fe2+的数目为8×+6×=4,O2-的数目为12×+1=4,晶
体的化学式为FeO,根据晶体密度计算公式可知,晶胞的边长为 cm,
Fe2+与O2-的最短核间距为× cm= cm=×1010 pm。
11.(1)金属锰有多种晶型,其中δ-Mn的结构为体心立方堆积,晶胞参数为a pm。δ-Mn中
锰的原子半径为________pm。已知阿伏加德罗常数的值为N ,δ-Mn的密度ρ=________ g·
A
cm-3(列出计算式)。
(2)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验
测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,
晶胞参数为a′=0.448 nm,则r(Mn2+)为________nm。
(3)Li O具有反萤石结构,晶胞如图所示。已知晶胞参数为0.466 5 nm,阿伏加德罗常数的值
2
为N ,则LiO的密度为________g·cm-3(列出计算式)。
A 2
答案 (1)a (2)0.148 0.076 (3)
解析 (1)δ-Mn的结构为体心立方堆积,设锰原子的半径为r,则体对角线为4r,则有a=
4r,r=a;一个晶胞中含有锰原子的数目为8×+1=2,ρ=== g·cm-3。(2)因为O2-是面
心立方最密堆积方式,面对角线是O2-半径的4倍,即4r(O2-)=a,解得r(O2-)=×0.420
nm≈0.148 nm;MnO也属于NaCl型结构,根据晶胞的结构,晶胞参数=2r(O2-)+2r(Mn2+),则r(Mn2+)==0.076 nm。(3)由题给图示可知,Li原子位于晶胞内部,O原子位于顶角
和面心,因此一个晶胞有8个Li原子,O原子个数为6×+8×=4,因此一个LiO晶胞的
2
质量为 g,一个晶胞的体积为(0.466 5×10-7)3cm3,即该晶体密度为 g·cm-3。
12.(1)钛酸锶(SrTiO )可用作电子陶瓷材料和人造宝石。其一种晶胞结构如图所示,Ti处于
3
体 心 位 置 , 则 Sr 原 子 处 于 ________ 位 置 , O 原 子 处 于
__________________________________
位置。已知晶胞参数a=0.390 5 nm,其密度为________g·cm-3(列出计算式即可)。
(2)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在我
国已实现了产业化。该合金的晶胞结构如图所示。
①该晶体的化学式为________。
②已知该合金的摩尔质量为M g·mol-1,密度为d g·cm-3,设N 为阿伏加德罗常数的值,
A
则该晶胞的体积是________cm3(用含M、d、N 的代数式表示)。
A
(3)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为a pm,列式表示NiO晶体的密度
为_________________________________________________________g·cm-3(不必计算出结果
阿伏加德罗常数的值为N )。人工制备的NiO晶体中常存在缺陷(如图)。一个Ni2+空缺,另
A
有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生
了变化。已知某氧化镍样品组成为 Ni O,该晶体中 Ni3+与 Ni2+的离子个数之比为
0.96
________。
答案 (1)顶角 面心
(2)①LaNi ② (3) 1∶11
5
解析 (1)已知钛酸锶的化学式为SrTiO ,Sr、Ti、O三种微粒的个数之比为1∶1∶3,既然
3
Ti处于体心位置,根据均摊法,晶胞中Ti原子的数目为1,处于面心位置的属于一个晶胞
的微粒数为3,所以处于面心位置的为O原子,那么,处于顶点位置的就是Sr原子。因为
该晶胞是立方晶胞,且在一个晶胞中含有1个SrTiO ,则 ρ== g·cm-3。(2)①由晶胞结构
3图可知,1个晶胞中La原子的个数为8×=1,Ni原子的个数为8×+1=5,则该晶体的化
学式为LaNi 。②1个晶胞的质量m=,由V=可知,1个晶胞的体积V= cm3。(3)晶胞中
5
Ni原子数目为1+12×=4,O原子数目为8×+6×=4,晶胞质量为 g,晶胞边长为 a
pm,晶胞体积为(a×10-10 cm)3,NiO晶体的密度为= g·cm-3;设1 mol Ni O中含Ni3+的
0.96
物质的量为x mol,
Ni2+的物质的量为(0.96-x)mol,根据晶体仍呈电中性可知,3x+2×(0.96-x)=2×1,x=
0.08,Ni2+的物质的量为(0.96-x) mol=0.88 mol,即离子数之比为 N(Ni3+)∶N(Ni2+)=
0.08∶0.88=1∶11。