文档内容
2024 年高考化学临考押题卷 02
(考试时间:75分钟 试卷满分:100分)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.科技强国。下列说法不正确的是
A.“北斗三号”导航卫星搭载铷原子钟,铷是碱金属元素
B.“弹性陶瓷塑料”具有很好的硬度和弹性,其中塑料的主要成分为有机物
C.量子计算机“悟空”即将面世,其传输信号的光纤主要成分为二氧化硅
D. 的发现开启了碳纳米材料应用的新时代, 属于混合型晶体
【答案】D
【解析】A.铷是ⅠA族元素,是碱金属元素,A项正确;
B.塑料是有机合成高分子材料,主要成分为有机物,B项正确;
C.二氧化硅是光纤的主要成分,C项正确;
D. 属于分子晶体,D项错误;
答案选D。
2.化学处处呈现美。下列说法正确的是
A.环己烷呈现对称美,是正六边形平面结构
B. 分子呈现“皇冠”结构, 属于共价晶体
C.霓虹灯发出五颜六色的光,该过程属于化学变化
D.锌片在 溶液中生成“银树”,反应中锌被氧化
【答案】D
【解析】A.环己烷中碳原子为饱和碳原子,为四面体结构,6个碳原子不可能在同一平面,A错误;
B. 属于分子晶体,B错误;
C.霓虹灯中充入惰性气体,在高压电场下电子被激发,然后在回到基态的过程中释放出能量,其中一部
分能量被荧光粉吸收发出可见光,没有生成新物质,没有发生化学反应,C错误;
D.锌片加入AgNO 溶液中,可以产生美丽的“银树”,该过程发生了氧化还原反应,锌置换出银
3
Zn+2AgNO=Zn(NO)+2Ag,反应中锌被氧化,D正确;
3 3 2
故选:D。
3.用下列实验装置进行的实验中,说法正确的是A.实验①:检验溴乙烷中的溴原子
B.实验②:铁片最终完全溶解,且高锰酸钾溶液褪色
C.实验③:所示实验无法比较硫、碳、硅三种元素的非金属性强弱
D.实验④:烧杯中液体变为红褐色后,继续加热煮沸,会出现浑浊
【答案】D
【解析】A.溴乙烷在NaOH溶液中加热发生水解反应,没有加硝酸中和NaOH,不能检验溴离子,故A
错误;
B.常温下Fe与浓硫酸发生钝化,生成致密的氧化膜阻止反应的进一步发生,不能生成二氧化硫,则高锰
酸钾溶液不褪色,故B错误;
C.发生强酸制取弱酸的反应,可知酸性为硫酸>碳酸>硅酸,则非金属性S>C>Si,故C错误;
D.向沸水在滴加饱和氯化铁溶液,液体变为红褐色可生成氢氧化铁胶体,继续加热煮沸,发生聚沉,则
会出现浑浊,故D正确;
故选:D。
4.SCl 常用于制作橡胶的粘结剂,SCl 与水反应的化学方程式为2 S Cl+2HO=SO ↑+3S↓+4HCl。设N
2 2 2 2 2 2 2 2 A
表示阿伏加德罗常数的值。下列说法错误的是
A.32gS 与32gS 均含有N 个硫原子
2 8 A
B.0.1molSCl 含有6.6N 个质子
2 2 A
C.标准状况下,2.24LSO 中S原子的孤电子对数为0.1N
2 A
D.若有4molHCl生成,则该反应中转移的电子数为6N
A
【答案】D
【解析】A.32gS 物质的量为 ,32gS 的物质的量为
2 8
,所含的硫原子数为1N ,故A正确;
A
B.质子数=原子序数,0.1molSCl 含有0.1mol×66×N mol-1=6.6N 个质子,故B正确;
2 2 A A
C.标准状况下,2.24LSO 物质的量为 ,SO 中S原子的孤电子对数为
2 2
,则孤电子对数为0.1N ,故C正确;
A
D .SCl 中S的化合价为+1价,生成1mol SO 转移3mol电子,若有4molHCl生成,则该反应中转移的电
2 2 2
子数为3N ,故D错误;
A故选D。
5.一种在室温下可循环充放电的新型纤维 电池有望应用于可穿戴设备的储能,其工作原理为:
,放电时
A. 发生还原反应 B. 在正极失电子
C.阳离子由正极移向负极 D.每消耗 ,转移 电子
【答案】D
【解析】A. 中Ca元素化合价上升, 发生氧化反应,故A错误;
B. 中O元素化合价下降, 在正极得电子,故B错误;
C.原电池中阳离子由负极移向正极,故C错误;
D. 中O元素由0价下降到-1价,每消耗 ,转移 电子,故D正确;
故选D。
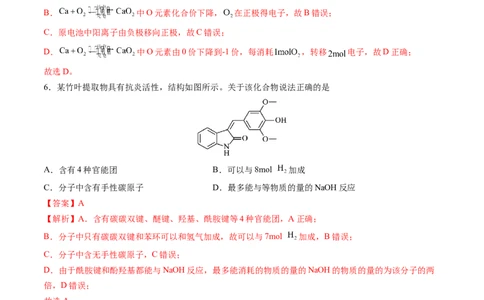
6.某竹叶提取物具有抗炎活性,结构如图所示。关于该化合物说法正确的是
A.含有4种官能团 B.可以与8mol 加成
C.分子中含有手性碳原子 D.最多能与等物质的量的NaOH反应
【答案】A
【解析】A.含有碳碳双键、醚键、羟基、酰胺键等4种官能团,A正确;
B.分子中只有碳碳双键和苯环可以和氢气加成,故可以与7mol 加成,B错误;
C.分子中含无手性碳原子,C错误;
D.由于酰胺键和酚羟基都能与NaOH反应,最多能消耗的物质的量的NaOH的物质的量的为该分子的两
倍,D错误;
故选A。
7.下列对应离子方程式书写正确的是
A.酚酞滴入碳酸钠溶液中变红:
B. 投入水中:
C.等体积、等物质的量浓度的 和 混合:
D.漂白粉溶液中通入过量 :【答案】A
【解析】A.碳酸钠在水中会水解,水解方程式: ,A正确;
B.NaO 与HO反应生成NaOH和O,其反应的离子方程式为 :,
2 2 2 2
B错误;
C.等体积、等物质的量浓度的 和 混合:
,C错误;
D.Ca2++2ClO- + 2SO + 2H O =2 Cl- + CaSO↓ +SO + 4H+,D错误;
2 2 4
故选A。
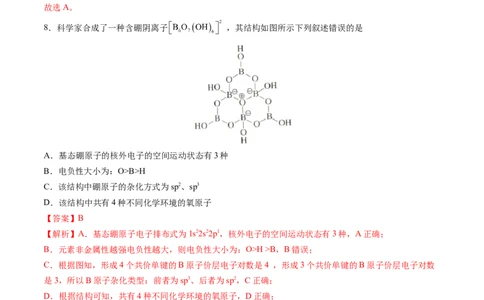
8.科学家合成了一种含硼阴离子 ,其结构如图所示下列叙述错误的是
A.基态硼原子的核外电子的空间运动状态有3种
B.电负性大小为:O>B>H
C.该结构中硼原子的杂化方式为sp2、sp3
D.该结构中共有4种不同化学环境的氧原子
【答案】B
【解析】A.基态硼原子电子排布式为1s22s22p1,核外电子的空间运动状态有3种,A正确;
B.元素非金属性越强电负性越大,则电负性大小为:O>H >B,B错误;
C.根据图知,形成4个共价单键的B原子价层电子对数是4 ,形成3个共价单键的B原子价层电子对数
是3,所以B原子杂化类型:前者为sp3、后者为sp2,C正确;
D.根据结构可知,共有4种不同化学环境的氧原子,D正确;
答案选B。
9.催化剂(XYZ ME )的组成元素均为主族元素且在每个短周期均有分布,X的基态原子p轨道电子总数比
6 5
s轨道电子总数多1个;仅Y、M、E处于同一周期,原子序数依次增大且相邻;E在地壳中含量最多。下
列说法不正确的是
A.第一电离能:M>E>X B.简单氢化物的稳定性:E>M
C.氧化物的熔点:X>Y>Z D. 和 的空间结构相同
【答案】C
【分析】催化剂(XYZ ME )的组成元素均为主族元素且在每个短周期均有分布,X的基态原子p轨道电子
6 5总数比s轨道电子总数多1个,则X原子核外电子排布可能是1s22s22p5,也可能是1s22s22p63s23p1,则X可
能是F元素,也可能是Al元素;E在地壳中含量最多,则E是O元素,仅Y、M、E处于同一周期,原子
序数依次增大且相邻,所以M是N元素,Y是C元素,则可推知X是Al元素;由于这几种元素在每个短
周期均有分布,可知Z是H元素,然后根据问题分析解答。
【解析】根据上述分析可知:X是Al,Y是C,Z是H,M是N,E是O元素。
A.X是Al,M是N,E是O元素,非金属元素在反应中容易获得电子,金属元素的原子在反应中容易失
去电子,因此非金属元素的第一电离能大于金属元素;则Al元素的第一电离能在三种元素中最小;同一周
期相邻元素,一般是原子序数越大,元素的第一电离能就越大,但N、O是同一周期相邻元素,由于N原
子核外电子排布处于轨道的半充满的稳定状态,其第一电离能大于同一周期相邻元素,所以第一电离能:
N>O,故三种元素的第一电离能大小关系为:M(N)>E(O)>X(Al),A正确;
B.M是N,E是O元素,元素的非金属性:O>N,元素的非金属性越强,其形成的简单氢化物的稳定性
就越强,所以简单氢化物的稳定性:E(HO)>M(NH),B正确;
2 3
C.X是Al,Y是C,Z是H,Al的氧化物为Al O,该物质是离子化合物,熔点很高;C的氧化物可能是
2 3
CO,也可能是CO,它们都是气体,熔点很低;H元素的氧化物可能是HO、HO,在室温下二者都是呈
2 2 2 2
液态,熔点比C元素的氧化物的高,故相应的氧化物的熔点由高到低的顺序:X>Z>Y,C错误;
D.Y是C,M是N,E是O元素, 为 ,中心C原子价层电子对数是:3+ =3,无孤对存
在,空间构型是平面三角形; 是 ,中心N原子价层电子对数是:3+ =3,空间构型也是
平面三角形,因此二者的空间构型相同,D正确;
故合理选项是C。
10.下列猜想对应的实验方案以及验证猜想成立的现象均正确的是
选项 猜想 实验方案 验证猜想成立的现象
苯酚能与 溶液反
A 向苯酚浊液中加入适量 固体 苯酚浊液变澄清
应
取少量该溶液,先滴加少量 溶液,再 产生白色沉淀且沉淀不
B 某溶液中一定含有
滴加足量稀盐酸 溶于稀盐酸
加热条件下 能与
C 将灼热的铜丝插入无水乙醇中 铜丝由红色变成黑色
反应
D 浓 具有漂白性 向滴有酚酞的NaOH溶液中加入浓 溶液红色褪去
【答案】A
【解析】A.向苯酚浊液中加入适量碳酸钠固体,苯酚与碳酸钠反应生成苯酚钠和碳酸氢钠,溶液变澄
清,说明苯酚能与NaCO 溶液反应,A正确;
2 3
B.取少量溶液,先滴加少量BaCl 溶液,再滴加足量稀盐酸,产生白色沉淀且沉淀不溶于稀盐酸,有可能
2是原溶液含Ag+,产生AgCl沉淀,B错误;
C.将灼热的、表面含有CuO的铜丝插入无水乙醇中,铜丝表面由黑色变为红色,才说明加热条件下
C HOH能与CuO反应,C错误;
2 5
D.向滴有酚酞的NaOH溶液中加入浓HNO,溶液红色褪去有可能是因为氢氧化钠被硝酸中和导致的,无
3
法说明浓HNO 具有漂白性,D错误;
3
本题选A。
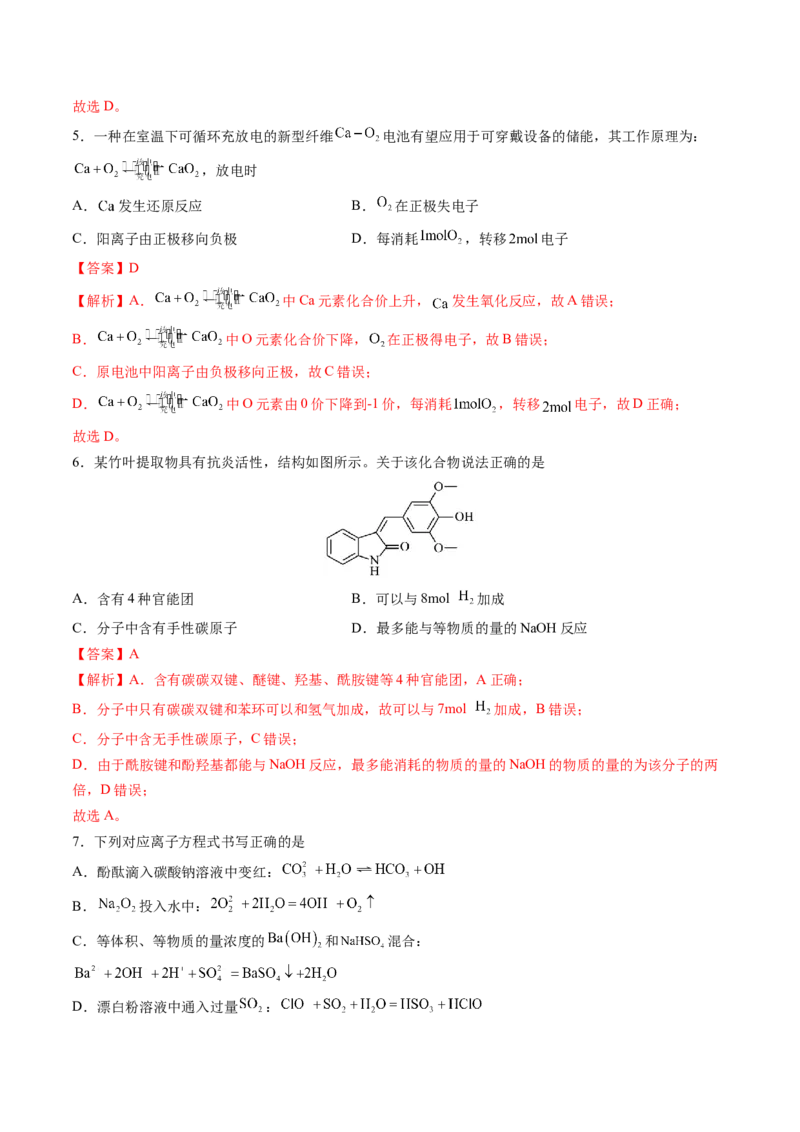
11.一种多功能金属性 催化剂,实现了空气中 的直接捕获和光−热协同催化转化,其机
理如图所示,下列说法正确的是
A. 纳米颗粒表面 活化为氢原子 B.该过程涉及碳氧双键的断裂与形成
C.该过程中的还原产物只有 D.步骤③中 在 表面与 作用
【答案】D
【分析】催化剂吸附二氧化碳和氢气分子,在光的作用下氢氢键断裂生成氢原子,和二氧化碳加成生成了
, 和氢原子反应生成CO、 和水, 和氢原子反应生成甲烷和水。
【解析】A.Pt纳米颗粒表面 活化为氢原子,故A错误;
B.该过程在第三步和第四步涉及碳氧双键的断裂,整个过程没有碳氧双键的形成,故B错误;
C.该过程中的还原产物有 和CO,故C错误;
D.步骤③中 在 表面与 作用生成 ,故D正确;
故选:D。
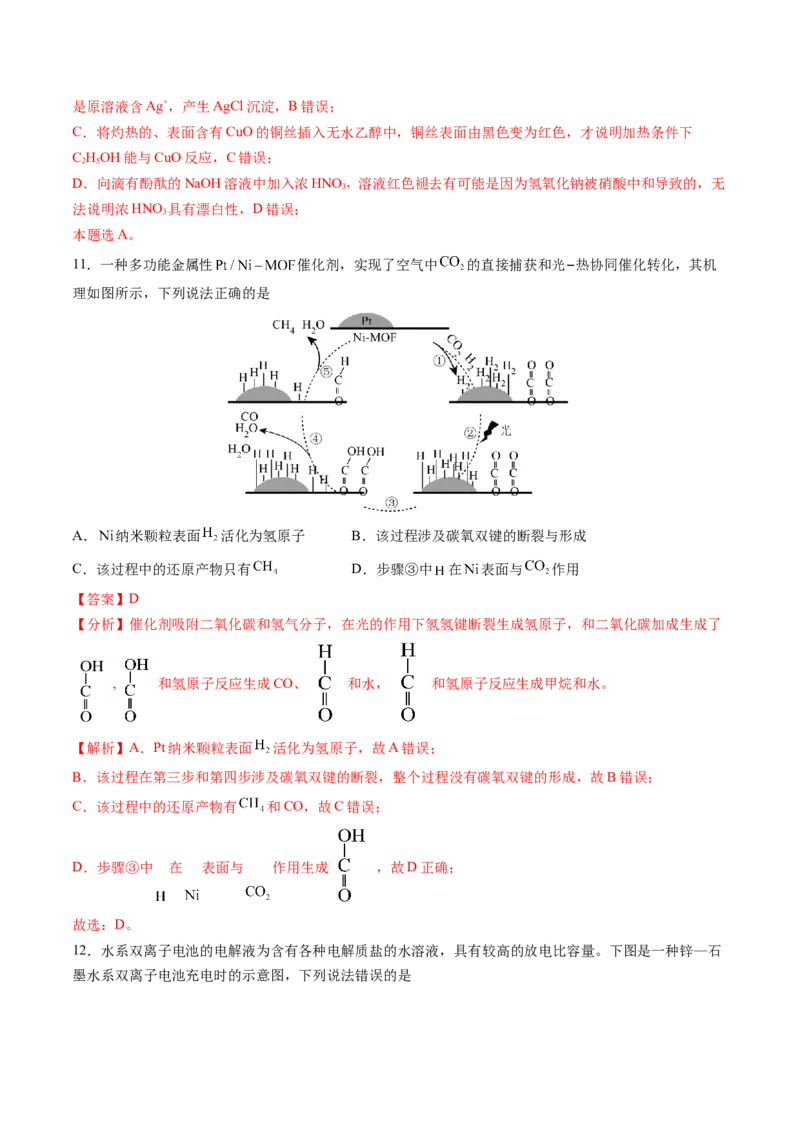
12.水系双离子电池的电解液为含有各种电解质盐的水溶液,具有较高的放电比容量。下图是一种锌—石
墨水系双离子电池充电时的示意图,下列说法错误的是A.放电时,电解液中的 从石墨层间脱离
B.充电时,右侧可能发生电极反应
C.a和b为离子交换膜,且均只允许阴离子通过
D.水系双离子电池的电解液,不仅是离子传输介质,也是电池的活性材料
【答案】C
【分析】充电时,石墨连接电源的正极,是阳极,锌连接电源的负极,是阴极,所以放电时,石墨是正
极,锌是负极。由图可知,充电时, 嵌入石墨中,Zn2+嵌入金属锌中,所以放电时, 从石墨中脱
离,Zn2+从金属锌中脱离。
【解析】A.根据分析知,放电时,电解液中的 从石墨层间脱离,A正确;
B.充电时,右侧是阴极,可能是水中的H+放电,即 ,B正确;
C.根据充电时的示意图知,a是阴离子交换膜,只允许阴离子通过,b为阳离子交换膜,只允许阳离子通
过,C错误;
D.根据分析可知,水系双离子电池的电解液,不仅是离子传输介质,也是电池的活性材料,D正确;
故选C。
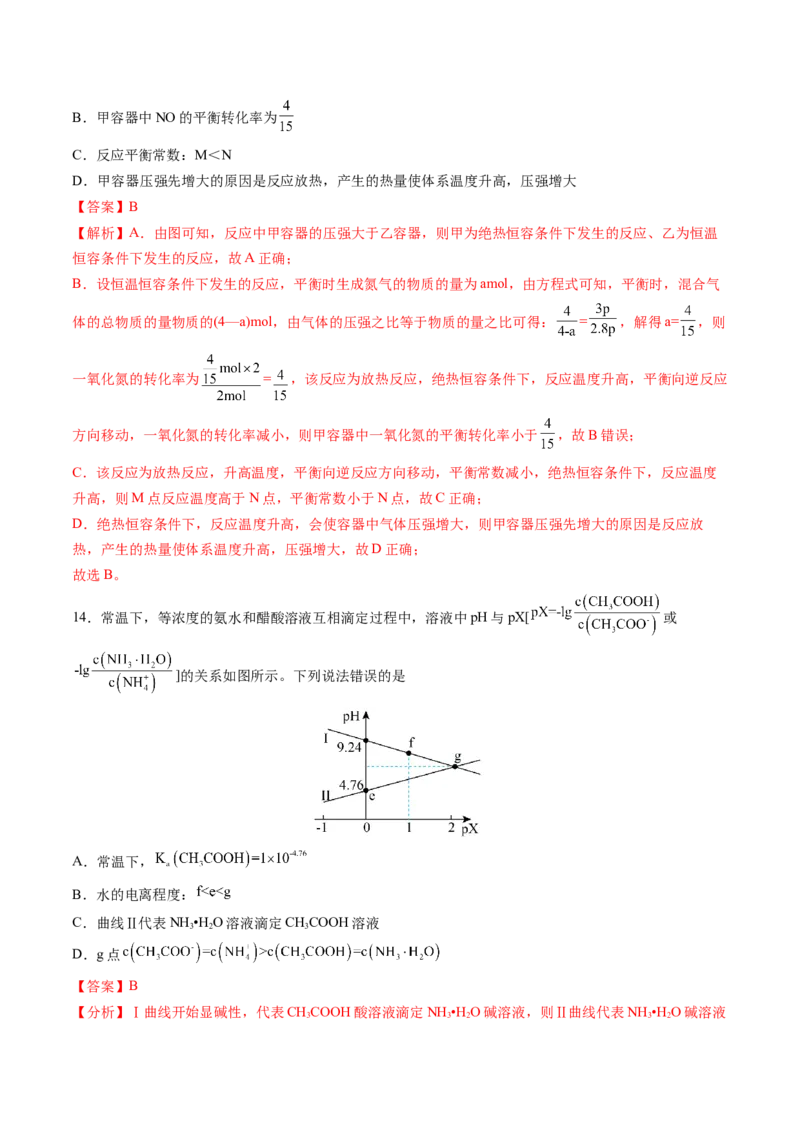
13.氮氧化物的排放是导致酸雨的原因。某研究小组利用反应探究NO的转化:
,向体积均为IL的两个密闭容器中分别加入2molCO(g)和
2molNO(g),探究绝热恒容和恒温恒容条件下压强随时间的变化曲线,如图所示,下列有关说法错误的
是
A.乙为恒温恒容条件下发生的反应B.甲容器中NO的平衡转化率为
C.反应平衡常数:M<N
D.甲容器压强先增大的原因是反应放热,产生的热量使体系温度升高,压强增大
【答案】B
【解析】A.由图可知,反应中甲容器的压强大于乙容器,则甲为绝热恒容条件下发生的反应、乙为恒温
恒容条件下发生的反应,故A正确;
B.设恒温恒容条件下发生的反应,平衡时生成氮气的物质的量为amol,由方程式可知,平衡时,混合气
体的总物质的量物质的(4—a)mol,由气体的压强之比等于物质的量之比可得: = ,解得a= ,则
一氧化氮的转化率为 = ,该反应为放热反应,绝热恒容条件下,反应温度升高,平衡向逆反应
方向移动,一氧化氮的转化率减小,则甲容器中一氧化氮的平衡转化率小于 ,故B错误;
C.该反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,绝热恒容条件下,反应温度
升高,则M点反应温度高于N点,平衡常数小于N点,故C正确;
D.绝热恒容条件下,反应温度升高,会使容器中气体压强增大,则甲容器压强先增大的原因是反应放
热,产生的热量使体系温度升高,压强增大,故D正确;
故选B。
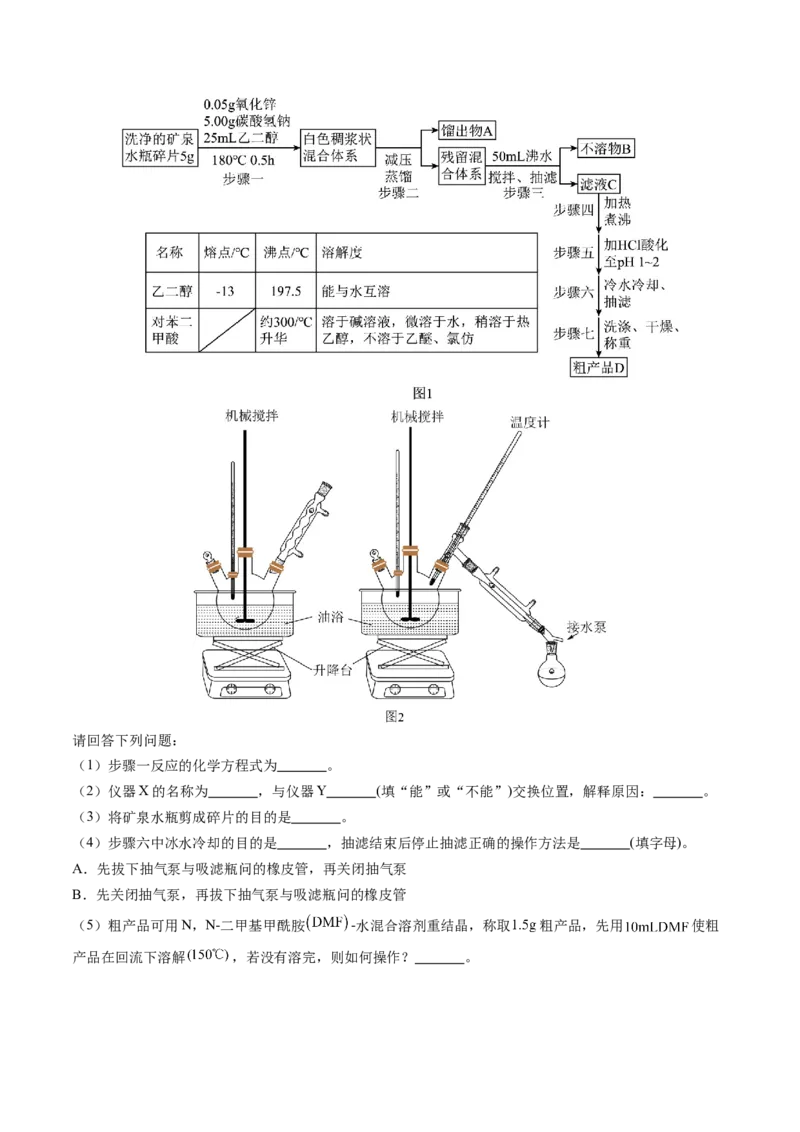
14.常温下,等浓度的氨水和醋酸溶液互相滴定过程中,溶液中pH与pX[ 或
]的关系如图所示。下列说法错误的是
A.常温下,
B.水的电离程度:
C.曲线Ⅱ代表NH •H O溶液滴定CHCOOH溶液
3 2 3
D.g点
【答案】B
【分析】Ⅰ曲线开始显碱性,代表CHCOOH酸溶液滴定NH •H O碱溶液,则Ⅱ曲线代表NH •H O碱溶液
3 3 2 3 2滴定CHCOOH酸溶液;因为为等浓度NH •H O碱溶液和CHCOOH酸溶液互相滴定,则g点代表两者恰
3 3 2 3
好完全反应,此时溶质为CHCOONH,据此分析作答。
3 4
【解析】A.当pH=4.76,呈酸性,-lg =lg =0,即 =1,
K(CHCOOH)= =10-4.76,A正确;
a 3
B.由于CHCOONH 是盐溶液,促进水的电离,所以水的电离程度最大,当碱溶液中c(OH-)与酸溶液中
3 4
c(H+)相等时,都会水的电离抑制程度相同,水的电离程度也相同,所以水的电离程度:e=f<g,B错误;
C.由分析可知,曲线Ⅱ代表NH •H O溶液滴定CHCOOH溶液,C正确;
3 2 3
D.由图可知,g点的溶质是弱酸弱碱盐CHCOONH,pH=7,则g点c(CHCOO- )=c( B+)>
3 4 3
c(CHCOOH)=c(NH •H O),D正确;
3 3 2
故答案为:B。
二、非选择题:本题共4小题,共58分。
15.(14分)锡酸钠 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡
的复合渣(主要成分为 及 等)为原料制备锡酸钠晶体 的工艺流程如
下:
已知:①相关物质的沸点如下:
物质
沸点 1800 2260 1550 1740
②锡酸钠晶体易溶于水,难溶于乙醇。
回答下列问题:
(1) 元素在周期表中的位置为 。
(2)“高温真空蒸发”控制温度在 左右,目的是 。
(3)“高温碱熔”时,单质 与 和 反应生成 的化学方程式为 。
(4)已知“溶浸”后溶液中的阴离子主要为 和少量 ,“沉铅”时发生反应的离子方程式为
。
(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、 (填试剂名称)洗涤、
(填“低温”或“高温”)干燥。
(6)利用焦炭在 高温下还原 可制得单质 。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
。
【答案】(1)第五周期、第IVA族
(2)将 气化分离
(3)
(4)
(5)乙醇 低温
(6)
【分析】将复合渣送入高温真空蒸发装置中,可以就爱那个复合渣中的某些物质汽化除去,随后将剩余固
体与NaOH、NaNO 共熔,可以将含Sn元素的物质转化为NaSnO ,后续利用溶浸、NaS沉铅等方法进一
3 2 3 2
步纯化锡酸钠溶液,最后将含有锡酸钠的溶液通过蒸发浓缩、冷却结晶、过滤、醇洗等方法进行结晶,得
到锡酸钠晶体。
【解析】(1)Sn元素在周期表中的位置为第五周期ⅣA族
(2)Sb O 的沸点为1550℃,为了分离除去Sb O,“高温真空蒸发”应控制温度在1600℃左右;
2 3 2 3
(3)“高温碱熔”时,单质Sn参与的反应为:5Sn+6NaOH+4NaNO =5Na SnO +2N ↑+3H O;
3 2 3 2 2
(4)沉铅”时发生反应的离子方程式为:S2-+PbO +2H O=PbS↓+4OH-;
2
(5)锡酸钠易溶于水,难溶于乙醇,为了防止锡酸钠损失,过滤后用乙醇进行洗涤,并低温干燥,防止
锡酸钠脱水;
(6)灰锡的晶体结构与金刚石相似,最近的两个锡原子间的距离为体对角线的四分之一,即 。
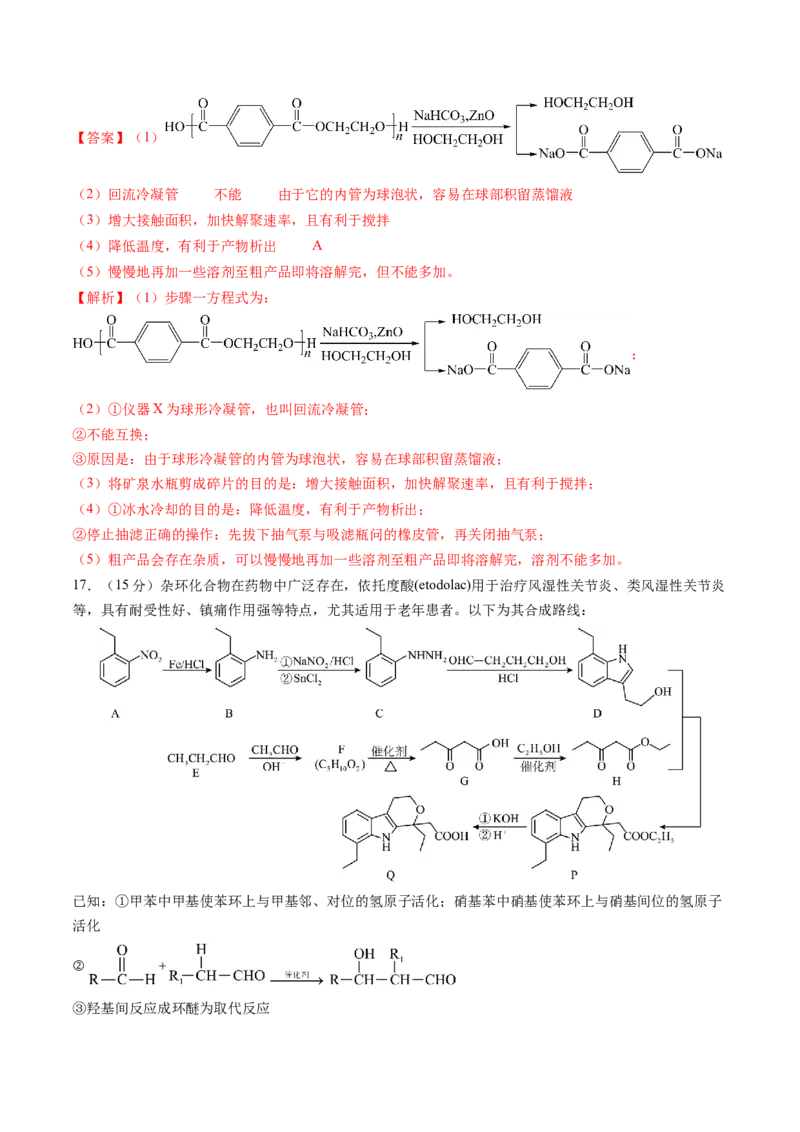
16.(15分)实验室用氧化锌作催化剂、以乙二醇和碳酸氢钠为复合解聚剂常压下快速、彻底解聚聚对苯
二甲酸乙二醇酯( ),同时回收对苯二甲酸和乙二醇。其实
验流程与有关数据如图1所示,实验部分装置如图2所示。请回答下列问题:
(1)步骤一反应的化学方程式为 。
(2)仪器X的名称为 ,与仪器Y (填“能”或“不能”)交换位置,解释原因: 。
(3)将矿泉水瓶剪成碎片的目的是 。
(4)步骤六中冰水冷却的目的是 ,抽滤结束后停止抽滤正确的操作方法是 (填字母)。
A.先拔下抽气泵与吸滤瓶问的橡皮管,再关闭抽气泵
B.先关闭抽气泵,再拔下抽气泵与吸滤瓶问的橡皮管
(5)粗产品可用N,N-二甲基甲酰胺 -水混合溶剂重结晶,称取 粗产品,先用 使粗
产品在回流下溶解 ,若没有溶完,则如何操作? 。【答案】(1)
(2)回流冷凝管 不能 由于它的内管为球泡状,容易在球部积留蒸馏液
(3)增大接触面积,加快解聚速率,且有利于搅拌
(4)降低温度,有利于产物析出 A
(5)慢慢地再加一些溶剂至粗产品即将溶解完,但不能多加。
【解析】(1)步骤一方程式为:
;
(2)①仪器X为球形冷凝管,也叫回流冷凝管;
②不能互换;
③原因是:由于球形冷凝管的内管为球泡状,容易在球部积留蒸馏液;
(3)将矿泉水瓶剪成碎片的目的是:增大接触面积,加快解聚速率,且有利于搅拌;
(4)①冰水冷却的目的是:降低温度,有利于产物析出;
②停止抽滤正确的操作:先拔下抽气泵与吸滤瓶问的橡皮管,再关闭抽气泵;
(5)粗产品会存在杂质,可以慢慢地再加一些溶剂至粗产品即将溶解完,溶剂不能多加。
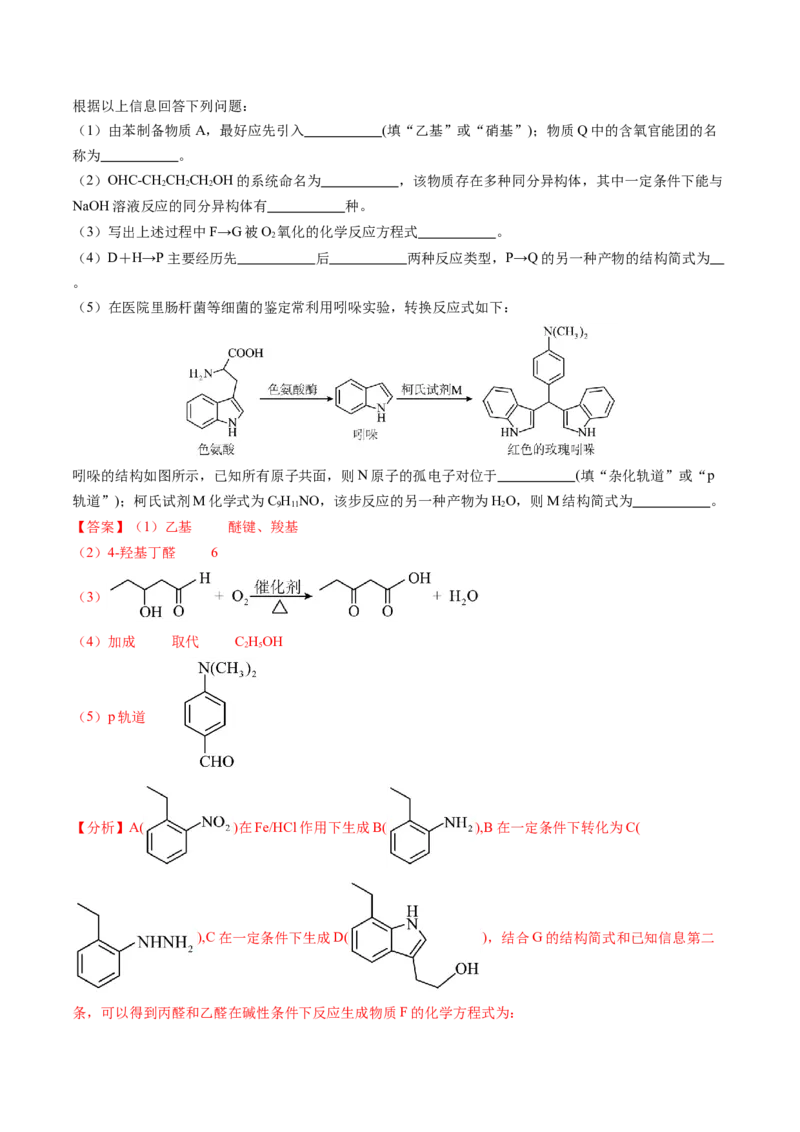
17.(15分)杂环化合物在药物中广泛存在,依托度酸(etodolac)用于治疗风湿性关节炎、类风湿性关节炎
等,具有耐受性好、镇痛作用强等特点,尤其适用于老年患者。以下为其合成路线:
已知:①甲苯中甲基使苯环上与甲基邻、对位的氢原子活化;硝基苯中硝基使苯环上与硝基间位的氢原子
活化
② +
③羟基间反应成环醚为取代反应根据以上信息回答下列问题:
(1)由苯制备物质A,最好应先引入 (填“乙基”或“硝基”);物质Q中的含氧官能团的名
称为 。
(2)OHC-CH CHCHOH的系统命名为 ,该物质存在多种同分异构体,其中一定条件下能与
2 2 2
NaOH溶液反应的同分异构体有 种。
(3)写出上述过程中F→G被O 氧化的化学反应方程式 。
2
(4)D+H→P主要经历先 后 两种反应类型,P→Q的另一种产物的结构简式为
。
(5)在医院里肠杆菌等细菌的鉴定常利用吲哚实验,转换反应式如下:
吲哚的结构如图所示,已知所有原子共面,则N原子的孤电子对位于 (填“杂化轨道”或“p
轨道”);柯氏试剂M化学式为C H NO,该步反应的另一种产物为HO,则M结构简式为 。
9 11 2
【答案】(1)乙基 醚键、羧基
(2)4-羟基丁醛 6
(3)
(4)加成 取代 C HOH
2 5
(5)p轨道
【分析】A( )在Fe/HCl作用下生成B( ),B在一定条件下转化为C(
),C在一定条件下生成D( ),结合G的结构简式和已知信息第二
条,可以得到丙醛和乙醛在碱性条件下反应生成物质F的化学方程式为:,F在催化剂和加热条件下反应,
转化为G( ),G和乙醇发生酯化反应生成H( ),对比D、H、P的结
构简式可知,D先与H中羰基之间发生加成反应,得到 ,然后两个羟基之
间脱水形成环醚得到P( ),形成环醚的反应属于取代反应,P在碱性条件下
彻底发生水解反应,在酸性条件下又发生强酸制弱酸,生成Q( ),据此回答
下列问题;
【解析】(1)①根据已知信息第一条:甲苯中甲基使苯环上与甲基邻、对位的氢原子活化;硝基苯中硝
基使苯环上与硝基间位的氢原子活化,结合A的结构简式,可知最好先引入乙基;
②根据结构分析,可知Q中的含氧官能团为醚键和羧基;
(2)①根据系统命名法可知,OHC—CH CHCHOH的系统命名为:4—羟基丁醛;
2 2 2
②符合要求的化合物分为羧酸和酯
属于羧酸的有
属于酯的有
HCOOCH CHCH、CHCOOCH CH、CHCHCOOCH
2 2 3 3 2 3 3 2 3
共有6种(3)根据分析可知,F( )被氧化为G( )的化学方程式为:
(4)①根据已知信息第三条:羟基间形成环醚属于取代反应可知,H( )的羰基先发
生加成反应生成醇,再和D( )在一定条件下发生取代反应生成环醚P(
);
②根据分析可知:P( )在碱性条件下彻底发生水解反应,在酸性条件下
又发生强酸制弱酸,生成Q( ),另一产物为乙醇(CHCHOH);
3 2
(5)①根据分子中所有原子共平面,可知氮原子采取sp 2杂化,氮原子上的孤电子未参与杂化,形成的是p
轨道;
②柯氏试剂M的化学式为:C H NO,该步反应的另一种产物是水,对比吲哚、红色的玫瑰吲哚结构可推知
9 11
M的结构简式为: 。
18.(14分)减少NO 、CO 的排放,实现资源化利用是化学工作者研究的重要课题。
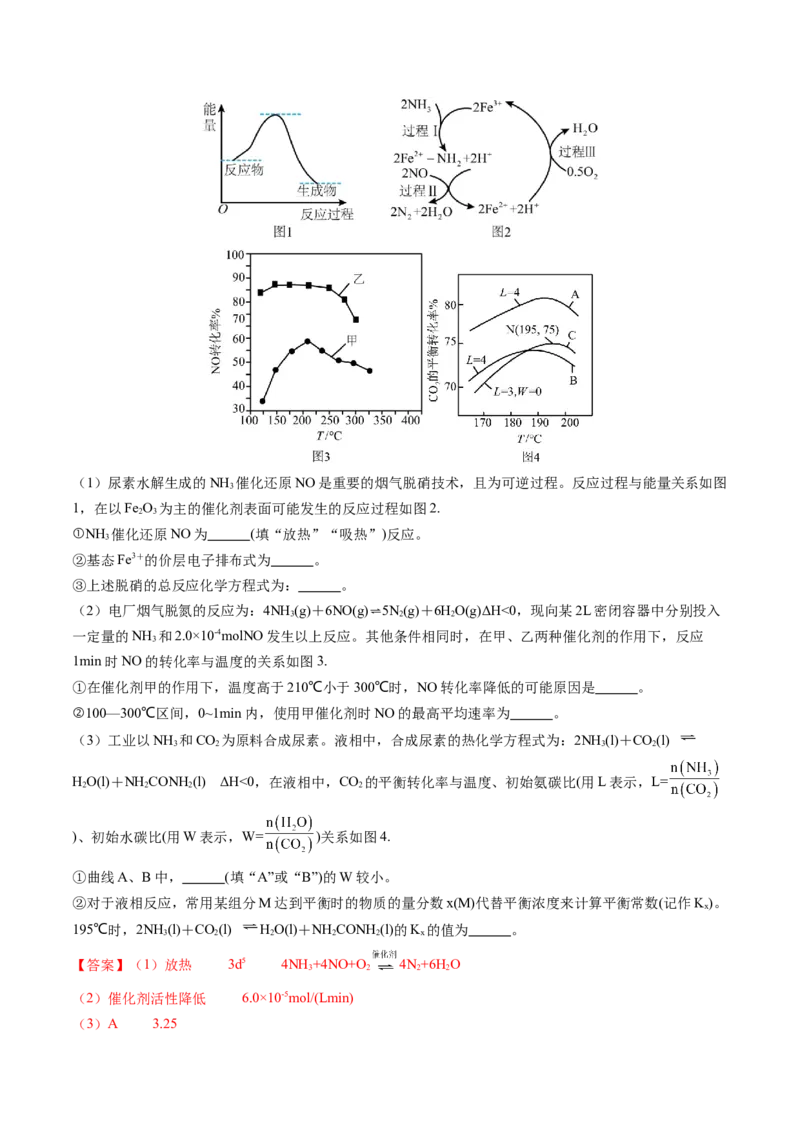
x 2(1)尿素水解生成的NH 催化还原NO是重要的烟气脱硝技术,且为可逆过程。反应过程与能量关系如图
3
1,在以Fe O 为主的催化剂表面可能发生的反应过程如图2.
2 3
①NH 催化还原NO为 (填“放热”“吸热”)反应。
3
②基态Fe3+的价层电子排布式为 。
③上述脱硝的总反应化学方程式为: 。
(2)电厂烟气脱氮的反应为:4NH
3
(g)+6NO(g)⇌5N
2
(g)+6H
2
O(g)ΔH<0,现向某2L密闭容器中分别投入
一定量的NH 和2.0×10-4molNO发生以上反应。其他条件相同时,在甲、乙两种催化剂的作用下,反应
3
1min时NO的转化率与温度的关系如图3.
①在催化剂甲的作用下,温度高于210℃小于300℃时,NO转化率降低的可能原因是 。
②100—300℃区间,0~1min内,使用甲催化剂时NO的最高平均速率为 。
(3)工业以NH 和CO 为原料合成尿素。液相中,合成尿素的热化学方程式为:2NH (l)+CO(l)
3 2 3 2
HO(l)+NH CONH (l) ΔH<0,在液相中,CO 的平衡转化率与温度、初始氨碳比(用L表示,L=
2 2 2 2
)、初始水碳比(用W表示,W= )关系如图4.
①曲线A、B中, (填“A”或“B”)的W较小。
②对于液相反应,常用某组分M达到平衡时的物质的量分数x(M)代替平衡浓度来计算平衡常数(记作K)。
x
195℃时,2NH (l)+CO(l) HO(l)+NH CONH (l)的K 的值为 。
3 2 2 2 2 x
【答案】(1)放热 3d5 4NH +4NO+O 4N+6H O
3 2 2 2
(2)催化剂活性降低 6.0×10-5mol/(Lmin)
(3)A 3.25【分析】(1)①由图可知反应物的总能量高于生成物的总能量,为放热反应;
②Fe的价电子排布式为3d64s2,而Fe3+失去3个电子,因此为3d5
③由图可知,反应物为氨气、一氧化氮、氧气、生成物为氮气和水,则脱硝的总反应为
;
(2)①催化剂的活性受温度的影响,温度升高催化剂的活性可能降低,因此转化率减小;
②由图可知100℃-300℃之间,NO的最高转化率为60%,故NO的变化量为2.0 10-4 60%=1.2 10-4mol,由
公式可知为 ;
(3)①当初始氨碳比相同,水碳比越大,二氧化碳的转化率越小,根据图中信息可知,曲线A二氧化碳
转化率大于B曲线,则W较小的曲线A。
②N点氨碳比为3,初始水碳比为0,二氧化碳的转化率为75%,设初始氨气物质的量为3a mol,
平衡时总物质的量为3.25a mol,则