文档内容
2024 年高考化学临考押题卷 02
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 Al 27 Cl 35.5 Fe 56
评卷人 得分
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小
题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.我国科研人员不断研发出新材料提升国家创新力,下列使用材料为有机高分子材料的是
A.高铁动车使用的大丝
B.天问一号使用的
C.天和核心舱太阳翼 D.C919上使用的芳砜
束碳纤维 电池的砷化镓器件 纶纤维
气溶胶
【答案】D
【解析】碳纤维、SiO2 气溶胶和砷化镓均属于无机非金属材料,芳砜纶纤维属于合成有机高分子材料,D
选项符合题意,故选D。
2.广东人爱“饮茶”,毛泽东有“饮茶粤海未能忘”诗句。下列说法错误的是
A.茶饼浸泡前要掰成小块,可使之更快浸出茶香
B.使用沸水泡茶,可加速茶叶中物质的溶解
C.茶叶封装时常附带一包铁粉,可减慢茶叶的氧化
D.某温度下测得茶水的 ,则该茶水一定呈酸性
【答案】D
【解析】A.茶饼浸泡前要掰成小块,增大其与水的接触面积,可使之更快浸出茶香,A正确;
B.使用沸水泡茶,温度升高,可加速茶叶中物质的溶解,B正确;
C.茶叶封装时常附带一包铁粉,铁粉吸收包装袋内的氧气,可减慢茶叶的氧化,C正确;
D.溶液呈酸性指氢离子浓度大于氢氧根离子浓度,某温度下水的离子积未知,pH=6.6不能判断溶液的酸
碱性,D错误;
故选D。
3.化学推动科技进步。下列说法正确的是
A.我国科学家首次合成了新核素 , 和 互为同位素
B.中国空间站机械臂采用铝合金材料,Al是第ⅢA族元素
C.鹊桥号中继卫星的天线由镀金钼丝织成,镀金钼丝是无机非金属材料
D.中国天眼主镜面的防腐膜中含有聚苯乙烯,聚苯乙烯是天然高分子材料
【答案】B
【解析】A.同位素是指质子数相同,中子数不同的同一元素的不同原子,W与Os不是同种元素,它们
不互为同位素,故A错误;B.Al的原子序数为13,位于第三周期ⅢA族,故B正确;
C.镀金钼丝属于金属材料,故C错误;
D.聚苯乙烯属于合成高分子化合物,不属于天然高分子材料,故D错误;
答案为B。
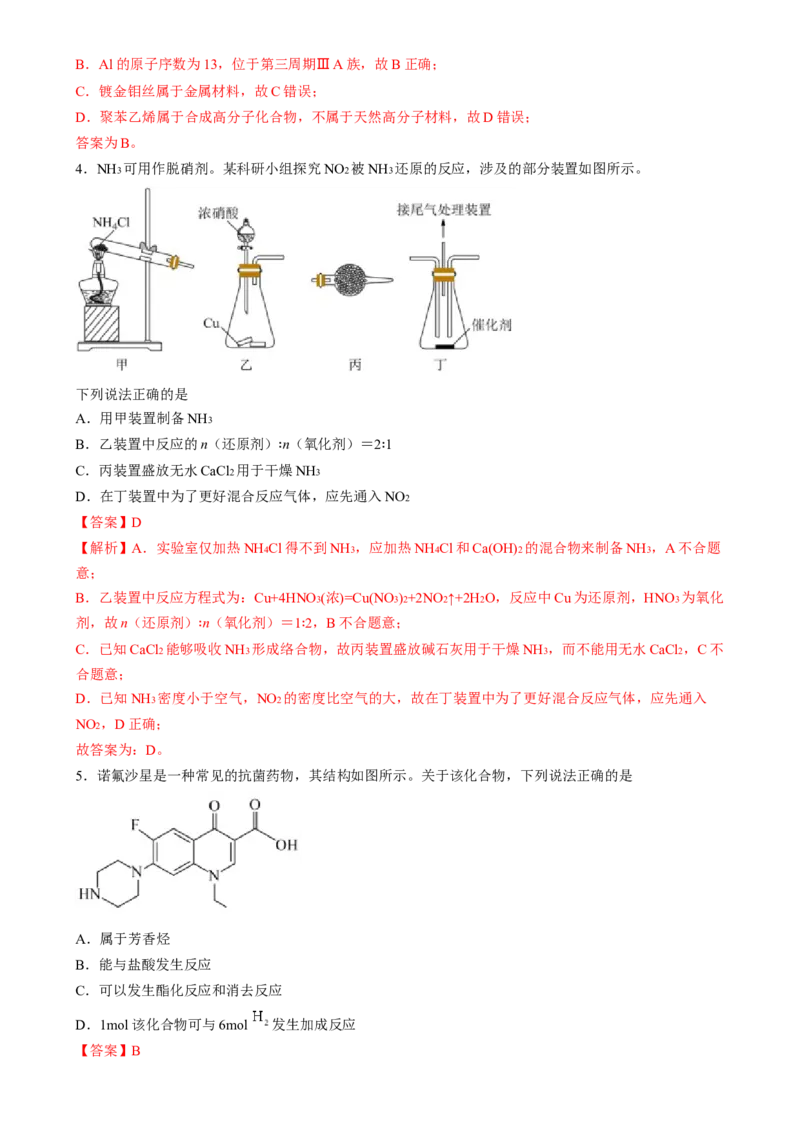
4.NH3 可用作脱硝剂。某科研小组探究NO2 被NH3 还原的反应,涉及的部分装置如图所示。
下列说法正确的是
A.用甲装置制备NH3
B.乙装置中反应的n(还原剂) n(氧化剂)=2 1
C.丙装置盛放无水CaCl2 用于干
∶
燥NH3
∶
D.在丁装置中为了更好混合反应气体,应先通入NO2
【答案】D
【解析】A.实验室仅加热NH4Cl得不到NH3 ,应加热NH4Cl和Ca(OH)2 的混合物来制备NH3 ,A不合题
意;
B.乙装置中反应方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,反应中Cu为还原剂,HNO3 为氧化
剂,故n(还原剂) n(氧化剂)=1 2,B不合题意;
C.已知CaCl2 能够吸
∶
收NH3 形成络合
∶
物,故丙装置盛放碱石灰用于干燥NH3 ,而不能用无水CaCl2 ,C不
合题意;
D.已知NH3 密度小于空气,NO2 的密度比空气的大,故在丁装置中为了更好混合反应气体,应先通入
NO2 ,D正确;
故答案为:D。
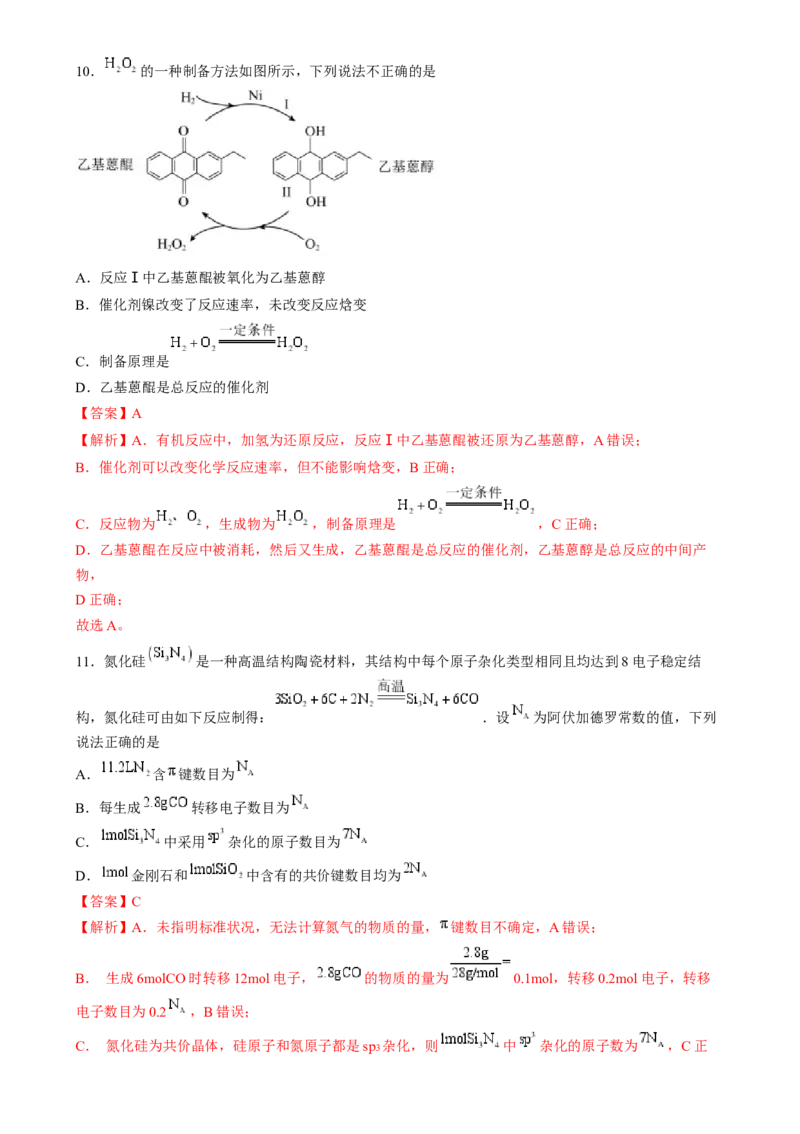
5.诺氟沙星是一种常见的抗菌药物,其结构如图所示。关于该化合物,下列说法正确的是
A.属于芳香烃
B.能与盐酸发生反应
C.可以发生酯化反应和消去反应
D.1mol该化合物可与6mol 发生加成反应
【答案】B【解析】A.该物质中含除C、H外的元素,不是烃类有机物,A错误;
B.该有机物中含氨基结构,具有碱性,可以盐酸反应,B正确;
C.该物质中含羧基,可发生取代反应,但不能发生消去反应,C错误;
D.苯环和碳碳双键、羰基均能与H2 发生加成反应,所以1mol氧氟沙星最多可与5mol H2 加成,D错
误;
答案选B。
6.“一勤天下无难事”。下列劳动项目所用的化学知识正确的是
选项 劳动项目 化学知识
A 医疗消毒:用苯酚水溶液进行环境消毒 苯酚有强氧化性
B 家务劳动:用醋酸去除热水壶中的水垢 醋酸能溶解硫酸钙
C
工业劳作:用 溶液处理钢材的锈迹 是强酸,与铁锈反应
D 家庭卫生:用管道通(含烧碱和铝粒)清通管道 使用过程中产生大量气体
【答案】D
【解析】A.苯酚可用于消毒是因为其可使蛋白质变性,与强氧化性无关,A错误;
B.用醋酸去除热水壶中的水垢是因为醋酸能溶解碳酸钙,B错误;
C. 为强酸弱碱盐,其水溶液呈酸性,可用于除锈迹,C错误;
D.烧碱和铝粒反应产生大量氢气,且大量放热均有利于清理管道中杂物,D正确;
答案选D。
7.化学助力体育事业的发展。下列说法错误的是
选
用途 物质 原因
项
A “球场大夫” 氯乙烷 易分解且吸收热量
B 泳池消毒剂 漂粉精 在空气中易生成强氧化性物质
C 羽毛球拍网线 尼龙66 强度高且弹性好
运动场人造草
D 聚乙烯 无毒、耐腐蚀、耐磨性好
坪
【答案】A
【解析】A.“球场大夫”的主要成分是沸点低的氯乙烷,氯乙烷挥发时会吸收热量,故A错误;
B.泳池消毒剂漂粉精的有效成分为次氯酸钙,次氯酸钙易与空气中的二氧化碳和水蒸气反应生成具有强
氧化性的次氯酸,而起到杀菌消毒的作用,故B正确;
C.羽毛球拍网线是由尼龙66制成,尼龙66具有强度高且弹性好的优良性能,故C正确;
D.运动场人造草坪的主要成分是聚乙烯,聚乙烯具有无毒、耐腐蚀、耐磨性好的优良性能,故D正确;
故选A。
8.部分含氮物质的分类与相应化合物关系如图所示。下列说法错误的是A.b具有碱性和还原性
B.反应Ⅰ中氧化产物和还原产物的物质的量之比为1 1
C.反应Ⅱ过程中生成0.1mol 时,转移1mol电子 ∶
D.反应Ⅲ能有效降低水体中的氮元素含量
【答案】D
【分析】部分含氮物质的分类与相应化合物关系图,则a为NH3 、b为N2H4 、c为铵盐、d为+3价氮的
盐、e为硝酸盐;
【解析】A.b为肼,结构简式为H2N-NH2 ,氨基具有碱性,N呈-2价化合价可升高具有还原性,A正
确;
B.反应Ⅰ中-3价氮化合价变为0价,得到氧化产物氮气,+3价氮化合价变为0价,得到还原产物氮气,
结合电子守恒可知,氧化产物和还原产物的物质的量之比为1 1,B正确;
C.反应Ⅱ为硝酸根离子被亚铁离子还原为氮气,氮化合价由+∶5变为0,则生成0.1mol 时,转移
0.1mol×2×5=1mol电子,C正确;
D.反应Ⅲ为d转化为c,+3价氮转化为-3价,亚硝酸盐转变未铵盐,不能有效降低水体中的氮元素含
量,D错误;
故选D。
9.锌-空气电池因工作电压高、制造成本低等特点备受关注。该电池以特定晶型的 为催化剂,KOH
溶液为电解质,放电时,下列叙述正确的是
A. 移向锌电极 B. 在正极发生氧化反应
C.负极发生反应: D.用盐酸作电解质能减少锌电极的损耗
【答案】A
【分析】由题意可知,放电时,锌为空气电池的负极,碱性条件下锌在负极失去电子发生氧化反应生成四
羟基合锌离子,通入空气的电极为正极,水分子作用下氧气在正极得到电子发生还原反应生成氢氧根离
子。
【解析】A.由分析可知,放电时,锌为空气电池的负极,通入空气的电极为正极,则氢氧根离子移向锌
电极,故A正确;
B.由分析可知,通入空气的电极为正极,水分子作用下氧气在正极得到电子发生还原反应生成氢氧根离
子,故B错误;
C.由分析可知,放电时,锌为空气电池的负极,碱性条件下锌在负极失去电子发生氧化反应生成四羟基
合锌离子,电极反应式为 ,故C错误;
D.锌能与盐酸反应,所以用盐酸作电解质会增加锌电极的损耗,故D错误;
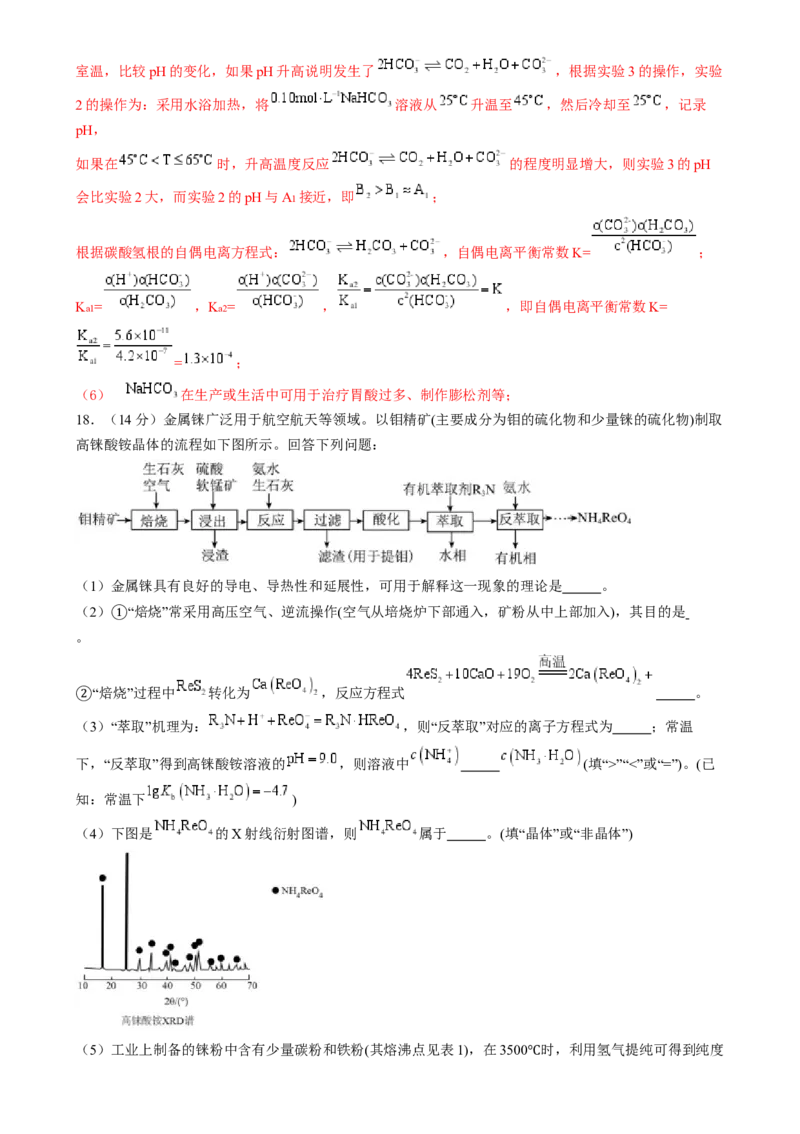
故选A。10. 的一种制备方法如图所示,下列说法不正确的是
A.反应Ⅰ中乙基蒽醌被氧化为乙基蒽醇
B.催化剂镍改变了反应速率,未改变反应焓变
C.制备原理是
D.乙基蒽醌是总反应的催化剂
【答案】A
【解析】A.有机反应中,加氢为还原反应,反应Ⅰ中乙基蒽醌被还原为乙基蒽醇,A错误;
B.催化剂可以改变化学反应速率,但不能影响焓变,B正确;
C.反应物为 ,生成物为 ,制备原理是 ,C正确;
D.乙基蒽醌在反应中被消耗,然后又生成,乙基蒽醌是总反应的催化剂,乙基蒽醇是总反应的中间产
物,
D正确;
故选A。
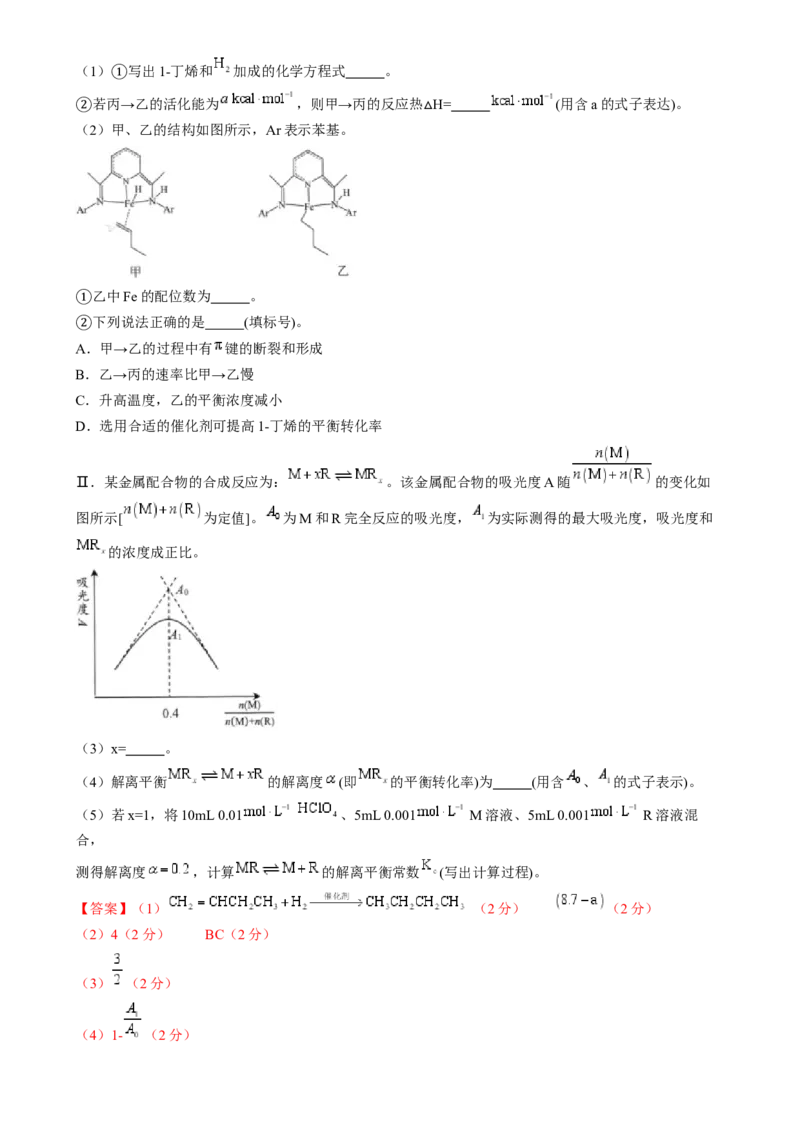
11.氮化硅 是一种高温结构陶瓷材料,其结构中每个原子杂化类型相同且均达到8电子稳定结
构,氮化硅可由如下反应制得: .设 为阿伏加德罗常数的值,下列
说法正确的是
A. 含 键数目为
B.每生成 转移电子数目为
C. 中采用 杂化的原子数目为
D. 金刚石和 中含有的共价键数目均为
【答案】C
【解析】A.未指明标准状况,无法计算氮气的物质的量, 键数目不确定,A错误;
B. 生成6molCO时转移12mol电子, 的物质的量为 0.1mol,转移0.2mol电子,转移
电子数目为0.2 ,B错误;
C. 氮化硅为共价晶体,硅原子和氮原子都是sp3 杂化,则 中 杂化的原子数为 ,C正确;
D. 中含有4molSi-O键,共价键数目为 ,D错误;
答案选C。
12.W、X、Z、Y、N为原子序数依次增大的短周期主族元素,W与Y原子的最外层电子数之和等于X
原子的最外层电子数,五种元素能组成如图所示的物质。下列说法错误的是
A.最高价氧化物对应水化物的酸性:N>Y B.简单氢化物的沸点:X>N>Y
C.元素的第一电离能:N>Y>Z D.简单离子半径:N>Y>X>Z
【答案】D
【分析】W、X、Z、Y、N为原子序数依次增大的短周期主族元素,由题中所给结构可知,Z形成带一个
单位正电荷的阳离子,则Z为IA族元素;X形成两个价键,X为VIA族元素,原子序数X小于Z ,所以
X为O、Z 为Na,W形成一个价键,W为IA族元素,则W为H;W与Y原子的最外层电子数之和等于
X原子的最外层电子数,即Y的最外层电子数为5,所以Y为P;N形成一个单键,且原子序数大于P,
所以N 为Cl。
【解析】A.N 为Cl、Y为P,Cl、P位于同一周期,同一周期从左到右元素非金属性递增、最高价氧化
物
对应水化物的酸性增强,所以最高价氧化物对应水化物的酸性:N>Y,故A正确;
B.X为O、N 为Cl、Y为P,简单氢化物分为H2O、HCl、PH3 ,H2O分子间存在氢键,H2O的沸点最
高,HCl的相对分子质量大于PH3 ,沸点HCl高于PH3 ,所以简单氢化物的沸点:X>N>Y,故B正确;
C.N 为Cl、Y为P、Z 为Na,三种元素位于同一周期,同一周期从左至右元素的第一电离能有增大的趋
势,所以第一电离能:N>Y>Z,故C正确;
D.N、Y、X、Z分别为Cl、P、O、Na,其简单离子分别为Cl- 、P3- 、O2- 、Na+ ,O2- 和Na+ 核外有两个电
子层、Cl- 和P3- 核外有三个电子层,所以Cl- 和P3- 的半径大于O2- 和Na+ ,O2- 和Na+ 具有相同的电子层结
构,核电荷数越大、半径越小,即半径大小O2- >Na+ ,Cl- 和P3- 具有相同的电子层结构,核电荷数越大、
半径越小,即半径大小Cl- <P3- ,所以简单离子半径: P3- >Cl- >O2- >Na+ ,故D错误;
故答案为:D。
13.下列除杂试剂、分离方法选用正确且除杂过程不涉及氧化还原反应的是
选项 物质(括号内为杂质) 除杂试剂 分离方法
A NO( ) 洗气
B NaCl溶液( ) NaOH溶液、 溶液、稀HCl 过滤
C 乙酸乙酯(乙酸) 饱和 溶液 分液
D 溴苯( ) NaOH溶液 分液
【答案】C【解析】A.NO(NO2 )通过水时,NO2 与水发生反应NO2+H2O=NO+HNO3 ,可以除去NO中的NO2 杂
质,但是反应是氧化还原反应,A不符合题意;
B.MgSO4 与NaOH反应生成的氢氧化镁会被稀盐酸溶解,镁又转化为离子,无法除去,B不符合题意;
C.饱和碳酸钠溶液可与乙酸反应从而除去乙酸,还可减小乙酸乙酯的溶解度,除去乙酸后,乙酸乙酯与
水相互不相溶,用分液法即可分离,所有反应不涉及氧化还原反应,C符合题意;
D.Br2 与NaOH反应生成可溶于水的NaBr和NaBrO,故可除去苯中溶解的溴,苯不溶于水,可用分液法
与水层分离,但Br2 与NaOH反应属于氧化还原反应,D不符合题意;
本题选C。
14.宏观辨识与微观探析是高中化学核心素养的重要组成部分。下列解释相应实验现象的离子方程式错误
的是
A.往AgCl沉淀中加入KI溶液,沉淀由白色变为黄色:
B.向 溶液中滴入过量 溶液:
C.南方水果运往北方时,用浸泡了酸性高锰酸钾溶液的硅藻土除去乙烯,防止水果腐烂:
D.苯甲醛与新制的 共热:
【答案】B
【解析】A.往AgCl沉淀中加入KI溶液,沉淀由白色变为黄色即AgCl沉淀转化为AgI沉淀,转化的离
子方程式为: ,A正确;
B.已知HNO3 的氧化性强于Fe3+ ,故向NaHSO3 溶液中滴入过量Fe(NO3)3 溶液的离子方程式为:
,B错误;
C.南方水果运往北方时,用浸泡了酸性高锰酸钾溶液的硅藻土除去乙烯,防止水果腐烂,即乙烯与酸性
高锰酸钾溶液反应生成CO2 ,反应的离子方程式为 ,C
正确;
D.根据乙醛与新制的Cu(OH)2 悬浊液反应原理可知,苯甲醛与新制的Cu(OH)2 共热的离子方程式为:
,D正确;
故答案为:B。
15.在一定条件下,将 和 通入恒容密闭容器中进行反应,容器中发生两个反应
和 。在不同温度下,测得平衡时体
系中 的物质的量与温度的关系如图所示。下列说法正确的是A.曲线c代表 的物质的量与温度的关系
B. 的平衡常数 (x点) (y点)
C. 时,随着温度升高, 的体积分数不断增大
D.一定温度下,当恒容密闭容器中混合气体的压强不再改变时,反应体系达到平衡状态
【答案】D
【解析】A.根据题意, 为放热反应,升高温度,平衡逆向移动,则平衡时
和 的物质的量增大,由于 和 的投料比等于化学计量数之比,则平衡时 和 的物质的量
之比为 ,故曲线、b、c分别代表 的物质的量与温度的关系,A错误;
B.该反应为放热反应,温度越高,K越小,则 的平衡常数 (x点) (y
点),B错误;
C. 时,随着温度升高,平衡 逆向移动, 的体积分数不断减小,
C错误;
D.一定温度下,在反应达到平衡前,恒容密闭容器中混合气体的物质的量一直在减小,则压强也一直在
减小,当压强不再改变时,反应体系达到平衡状态,D正确;
本题选D。
16.用热再生氨电池处理含Cu2+ 电镀废液的装置如图。该装置由电池部分和热再生部分组成:电池部分
中,a极室为(NH4)2SO4-NH3 混合液,b极室为(NH4)2SO4 溶液;热再生部分加热a极室流出液,使
[Cu(NH3)4]2+ 分解。下列说法不正确的是
A.装置中的离子交换膜为阳离子交换膜
B.a极的电极反应为:Cu-2e-+4NH3=[Cu(NH3)4]2+
C.电池部分的总反应为:Cu2++4NH3=[Cu(NH3)4]2+
D.该方法可以富集Cu2+ 并产生电能,同时循环利用NH3
【答案】A
【分析】甲、乙两室均预加相同的Cu2+ 电镀废液,a室铜失去电子发生氧化反应生成[Cu(NH3)4]2+ 为负极:
Cu-2e-+4NH3=[Cu(NH3)4]2+ ,b端为原电池正极,铜离子得到电子发生还原反应生成铜,电极反应Cu2++2e-
=Cu;中间为阴离子交换膜,硫酸根离子由正极迁移到负极。【解析】A.在原电池内电路中阳离子向正极移动,如隔膜为阳离子交换膜,电极溶解生成的铜离子要向
右侧移动,通入NH3 要消耗Cu2+ ,显然左侧阳离子不断减小,明显不利于电池反应正常进行,故离子交
换膜为阴离子交换膜,A错误;
B.由分析可知,a极的电极反应为:Cu-2e-+4NH3=[Cu(NH3)4]2+ ,B正确;
C.由分析可知,a:Cu-2e-+4NH3=[Cu(NH3)4]2+ ,b:Cu2++2e-=Cu;则总反应为:Cu2+
+4NH3=[Cu(NH3)4]2+ ,C正确;
D.该装置为原电池装置,可以富集Cu2+ 并产生电能,同时回收液受热分解释放出氨气,能循环利用
NH3 ,
D正确;
故选A。
评卷人 得分
二、非选择题:本题共4小题,共56分。
17.(14分) 用途广泛。某实验小组同学围绕 开展如下实验活动。
.配制溶液
(1)配制 的 溶液,需要称量 固体的质量为 。
(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有 (填标号)。
.实验探究
探究温度对 溶液 的影响,进行如下实验(不考虑水的挥发)。
实验序号 操作
测试温度
采用水浴加热,将 溶液从 持续升温至
1
,每隔 测量并记录溶液
(3) 溶液显碱性的原因是 (用离子方程式表示)。
(4)实验1中测得 ,可知当 时, 溶液的 随温度升高
而减小,这主要是 改变与水解平衡移动共同作用的结果,其中 发挥主导作用。实验1中测得
,且当 时,实验过程中观察到有气泡产生。(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料: 溶液中存在平衡: 。
提出猜想:对于 溶液,当 时,该反应进行程度很小;当
时,该反应进行程度明显增大。
实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
实验序号 操作 测试温度
2 采用水浴加热, ,然后冷却至 ,并记录溶液
①
采用水浴加热,将 溶液从 升温至 ,然
3
后冷却至 ,并记录溶液
实验结论: 根据实验1~3的结果,小组同学认为猜想成立,其判断依据是 。
拓展总结:② 溶液中存在 的自偶电离平衡: 时, 自偶
电离的平衡③常数为 [保留两位有效数字;已知: 时,
]。当温度升高时, 更易分解, 从体系逸出,
促进了 在溶液中的分解。
(6)写出 在生产或生活中的一种应用 。
【答案】(1) (1分)
(2) (2分)
(3) (2分)
(4) 改变(2分)
(5)将 溶液从 升温至 (2分) (或 ;或
) (2分) (2分)
(6)治疗胃酸过多、用于制作膨松剂等(1分)
【解析】(1)配制 的 溶液,需要称量 固体的质量为
=4.2g;
(2)配制一定物质的量浓度溶液的一般步骤为:计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶
等,用到的仪器:烧杯、玻璃棒、量筒、胶头滴管、500mL容量瓶,缺少的玻璃仪器为:500mL容量瓶
和烧杯,答案为BD;
(3)碳酸氢根水解导致碳酸氢钠溶液显碱性,离子方程式为: ;
(4)当 时, 溶液的 随温度升高而减小;而升高温度,Kw增大,
使c(H+)增大,pH减小;温度升高,水解平衡向右移动,使c(OH-)增大,pH增大,而溶液的 随温度升
高而减小,说明Kw的改变发挥了主要作用;
(5)实验2和实验3要验证提出的猜想,需要将 溶液升高到 及以上,再降低到室温,比较pH的变化,如果pH升高说明发生了 ,根据实验3的操作,实验
2的操作为:采用水浴加热,将 溶液从 升温至 ,然后冷却至 ,记录
pH,
如果在 时,升高温度反应 的程度明显增大,则实验3的pH
会比实验2大,而实验2的pH与A1 接近,即 ;
根据碳酸氢根的自偶电离方程式: ,自偶电离平衡常数K= ;
Ka1= ,Ka2= , ,即自偶电离平衡常数K=
= ;
(6) 在生产或生活中可用于治疗胃酸过多、制作膨松剂等;
18.(14分)金属铼广泛用于航空航天等领域。以钼精矿(主要成分为钼的硫化物和少量铼的硫化物)制取
高铼酸铵晶体的流程如下图所示。回答下列问题:
(1)金属铼具有良好的导电、导热性和延展性,可用于解释这一现象的理论是 。
(2) “焙烧”常采用高压空气、逆流操作(空气从培烧炉下部通入,矿粉从中上部加入),其目的是
。
①
“焙烧”过程中 转化为 ,反应方程式 。
②(3)“萃取”机理为: ,则“反萃取”对应的离子方程式为 ;常温
下,“反萃取”得到高铼酸铵溶液的 ,则溶液中 (填“>”“<”或“=”)。(已
知:常温下 )
(4)下图是 的X射线衍射图谱,则 属于 。(填“晶体”或“非晶体”)
(5)工业上制备的铼粉中含有少量碳粉和铁粉(其熔沸点见表1),在3500 时,利用氢气提纯可得到纯度
℃达99.995%的铼粉(下图为碳在高温氢气环境中气-固占比计算结果),请分析原因 。
表1
物质 熔点( ) 沸点( )
℃ ℃
3180 5900
C 3652 4827
1535 2750
(6)三氧化铼是简单立方晶胞,晶胞结构如下图所示,摩尔质量为Mg/mol,晶胞密度为 。铼原
子填在氧原子围成的 (填“四面体”“立方体”或“八面体”)空隙中,该晶胞中两个相距最近的O原子间
的距离为 cm。(列出计算式)
【答案】(1)电子气理论(1分)
(2)增大接触面积,提高反应速率,使焙烧充分,提高原料的利用率(2分) 8CaSO4 (2分)
(3) 或 (2分)
>(1分)
(4)晶体(1分)
(5)3500 时,Fe已气化去除,固态碳与H2 完全反应,形成了气态物质(2分)
℃
(6) 八面体 (1分) (2分)
【分析】钼精矿(主要成分为钼的硫化物和少量铼的硫化物)在空气中焙烧,硫元素转化成二氧化硫,二氧
化硫与生石灰、氧气反应生成硫酸钙,铼元素转化成Ca(ReO4)2 ,钼元素转化成CaMoO4 ,加入硫酸、软
锰矿,
硫酸钙属于微溶物,过滤,得到浸渣CaSO4 ,加入氨水和生石灰,得到NH4ReO4 ,然后过滤,通过酸
化、萃取和反萃取、蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到产品。【解析】(1)金属铼属于金属晶体,在金属晶体中,金属原子的价电子从金属原子上“脱落”下来形成“电
子气”,外力作用金属原子移位滑动,电子在其中起到“润滑”的作用,因此金属具有延展性;电子气在外电
场作用下定向移动,因此金属有良好的导电性;金属受热,加速自由电子与金属离子之间的能量交换,将热
能从一端传递到另一端而使金属有良好的导热性,因此可以用电子气理论解释金属Re具有良好的导电、
导热性和延展性;
(2) “焙烧”常采用高压空气、逆流操作可增大接触面积,提高反应速率,使焙烧充分,提高原料的利
用率;
①
ReS2 在反应中转化成Ca(ReO4)2 和CaSO4 ,ReS2 作还原剂,氧气作氧化剂,因此有CaO+ReS2+O2
②
Ca(ReO4)2+CaSO4 ,根据原子守恒配平即可,氧气最后配平,所得化学反应方程式为4ReS2+10CaO+19O2
2Ca(ReO4)2+8CaSO4 ;
(3)反萃取时R3N·HReO4 与氨气反应生成NH4ReO4 、R3N,反应离子方程式为:
或 ;
lgKb(NH3∙H2O)=-4.7,Kb(NH3∙H2O) =10-4.7 ,“反萃取”得到高铼酸铵溶液的pH=9.0,则溶液
中c(OH-)=10-5mol/L,则 =100.3 >1,c( )>c(NH3∙H2O);
(4)由NH4ReO4 的X射线衍射图谱可知,NH4ReO4 具有衍射峰,说明NH4ReO4 属于晶体;
(5)根据表中数据可知,在3500 时,铁转化成铁蒸气,根据图象可知,在3500 时,C和氢气生成气
态物质,得到高纯度的Re;
℃ ℃
(6)由图可知,顶角的Re原子周围有6个距离相等且最近的O原子,这6个O原子构成正八面体,因
此Re原子填在O原子围成的八面体空隙中;根据均摊法可计算出一个晶胞中Re和O的个数分别为1个
和3个,也就是1个晶胞含有1个ReO3 ,设晶胞的棱长为acm,则a3=V= = ,a=
,根据晶胞棱中心的是O原子,距离最近的O原子是两条相交棱上的O原子,两者的距离=
a= cm。
19.(14分)金属有机配合物广泛应用于各类催化反应。
Ⅰ.某铁的配合物催化1-丁烯和 加成的部分历程如图。(1) 写出1-丁烯和 加成的化学方程式 。
若丙①→乙的活化能为 ,则甲→丙的反应热 H= (用含a的式子表达)。
(2)甲、乙的结构如图所示,Ar表示苯基。
② △
乙中Fe的配位数为 。
下列说法正确的是 (填标号)。
①
A.甲→乙的过程中有 键的断裂和形成
②
B.乙→丙的速率比甲→乙慢
C.升高温度,乙的平衡浓度减小
D.选用合适的催化剂可提高1-丁烯的平衡转化率
Ⅱ.某金属配合物的合成反应为: 。该金属配合物的吸光度A随 的变化如
图所示[ 为定值]。 为M和R完全反应的吸光度, 为实际测得的最大吸光度,吸光度和
的浓度成正比。
(3)x= 。
(4)解离平衡 的解离度 (即 的平衡转化率)为 (用含 、 的式子表示)。
(5)若x=1,将10mL 0.01 、5mL 0.001 M溶液、5mL 0.001 R溶液混
合,
测得解离度 ,计算 的解离平衡常数 (写出计算过程)。
【答案】(1) (2分) (2分)
(2)4(2分) BC(2分)
(3) (2分)
(4)1- (2分)(5)1.25×10-5 (2分)
【解析】(1) 1-丁烯和 加成的化学方程式: ;
根据图示,甲①→乙的 ,乙→丙的活化能为23.8kcal/mol、丙→乙的活化能为
② ,则乙→丙的 ,根据盖斯定律:甲→丙的反应热
;
(2) 由乙的结构可知,乙中Fe的配位数为4;
A.对比甲、乙两物质结构可知,甲→乙的过程中有 键的断裂,但无 键的形成,A错误;
①
B.乙→丙的活化能大于甲→乙活化能,所以乙→丙速率比甲→乙速率慢,B正确;
②
C.甲→乙为放热过程,乙→丙为吸热过程,升高温度,乙的平衡浓度减小,C正确;
D.催化剂不影响化学平衡移动,不能提高1-丁烯的平衡转化率,D错误;
答案选BC。
(3)A0 为M和R完全反应的吸光度,由图示知 =0.4,解得 = ,则x= 。
(4)由图示知 =0.4时,M和R完全反应的吸光度为A0 ,A1 为实际测得的最大吸光度,即反
应达到平衡状态的吸光度,吸光度与MRx 的浓度成正比,说明反应达到平衡时M的平衡转化率为 ;
则解离平衡 的解离度α=1- 。
(5)若x=1,将10mL 0.01 、5mL 0.001 M溶液、5mL 0.001 R溶液混
合,若完全反应生成MR的浓度为 =2.5×10-4mol/L,解离度为0.2,则平衡时MR的浓度
为2.5×10-4mol/L×(1-0.2)=2×10-4mol/L,M、R的浓度都为5×10-5mol/L, 的解离平衡常数
Kc= =1.25×10-5 。
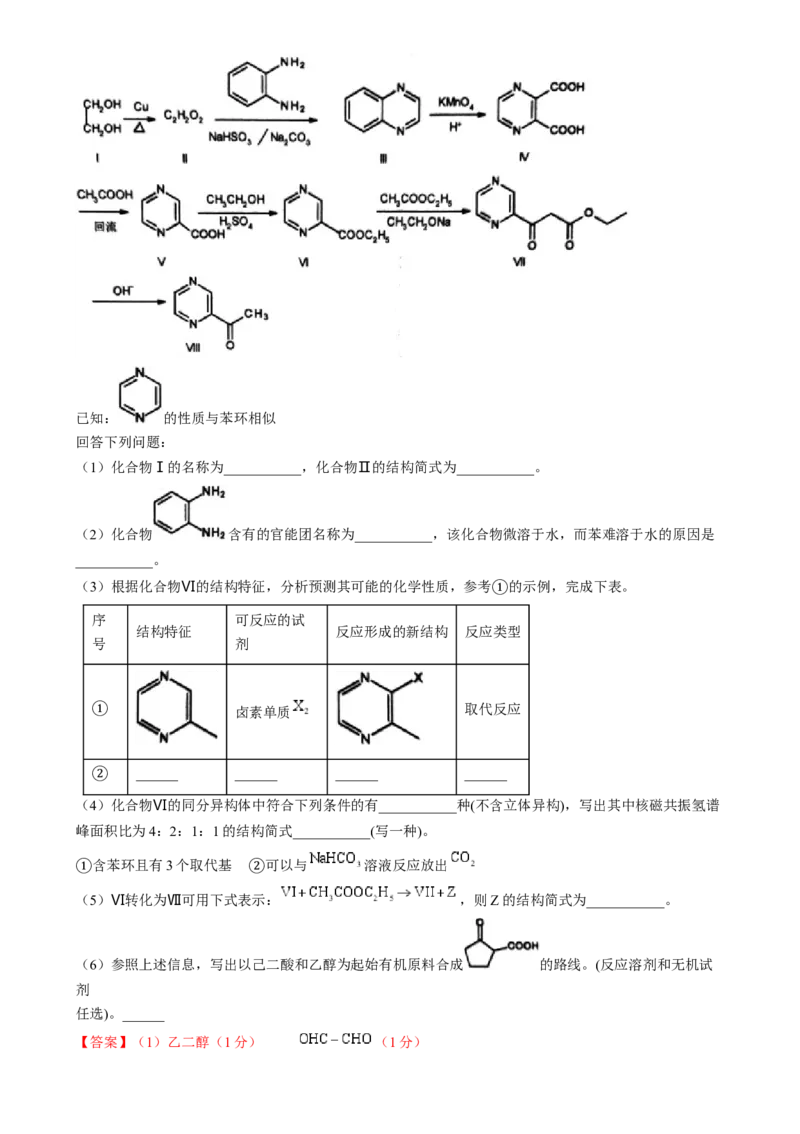
20.(14分)乙酰基吡嗪Ⅷ是一种香料,也是药物合成的重要有机原料,其合成路线如下:已知: 的性质与苯环相似
回答下列问题:
(1)化合物Ⅰ的名称为___________,化合物Ⅱ的结构简式为___________。
(2)化合物 含有的官能团名称为___________,该化合物微溶于水,而苯难溶于水的原因是
___________。
(3)根据化合物Ⅵ的结构特征,分析预测其可能的化学性质,参考 的示例,完成下表。
序 可反应的试 ①
结构特征 反应形成的新结构 反应类型
号 剂
卤素单质 取代反应
①
______ ______ ______ ______
(4②)化合物Ⅵ的同分异构体中符合下列条件的有___________种(不含立体异构),写出其中核磁共振氢谱
峰面积比为4:2:1:1的结构简式___________(写一种)。
含苯环且有3个取代基 可以与 溶液反应放出
①(5)Ⅵ转化为Ⅶ可用下式表②示: ,则Z的结构简式为___________。
(6)参照上述信息,写出以己二酸和乙醇为起始有机原料合成 的路线。(反应溶剂和无机试
剂
任选)。______
【答案】(1)乙二醇(1分) (1分)(2)氨基(1分) 能与水形成氢键,而苯环中没有能与水形成氢键的原子团(2分)
(3) (0.5分) 稀硫酸(0.5分) (0.5分)
水解反应(或取代反应)(0.5分)
(4) 6 (2分) 或者 (1分)
(5) (1分)
(6)
(3分)
【分析】根据流程,Ⅰ为乙二醇,被催化氧化生成乙二醛,Ⅱ为 , 与
反应,生成 , 被 氧化生成 ,
再与 反应生成 ,与 发生酯化反应,生成
,与 和 反应生成 ,最后
在碱性条件下得到产品:
。
【解析】(1)化合物Ⅰ的名称为乙二醇,化合物Ⅱ的结构简式为 ;
(2)化合物 含有的官能团名称为氨基,因为 能与水形成氢键,而苯环中没有能与水形
成氢键的原子团,所以该化合物微溶于水,而苯难溶于水;(3)化合物Ⅵ的结构为: ,可以反应的试剂为:稀硫酸,生成产物为:
,反应类型为:水解反应(或取代反应);
(4)化合物Ⅵ的同分异构体中, 含苯环,有3个取代基 可以与 溶液反应放出 ,含有
① ②
,基本结构为: 、 、 、
、 、 共6种,核磁共振氢谱峰面积比为
4:2:1:1的结构简式为: 和 ;
(5) ,与 反应生成 和 ,
所以Z为 ;
(6)根据以上合成信息, 和 反应生成 ,在
的作用下,生成 和 , 在稀硫酸再
发生水解反应生成产物: ,合成路线为:
。