文档内容
课时检测(十三) 钠及其化合物的基本知能评价
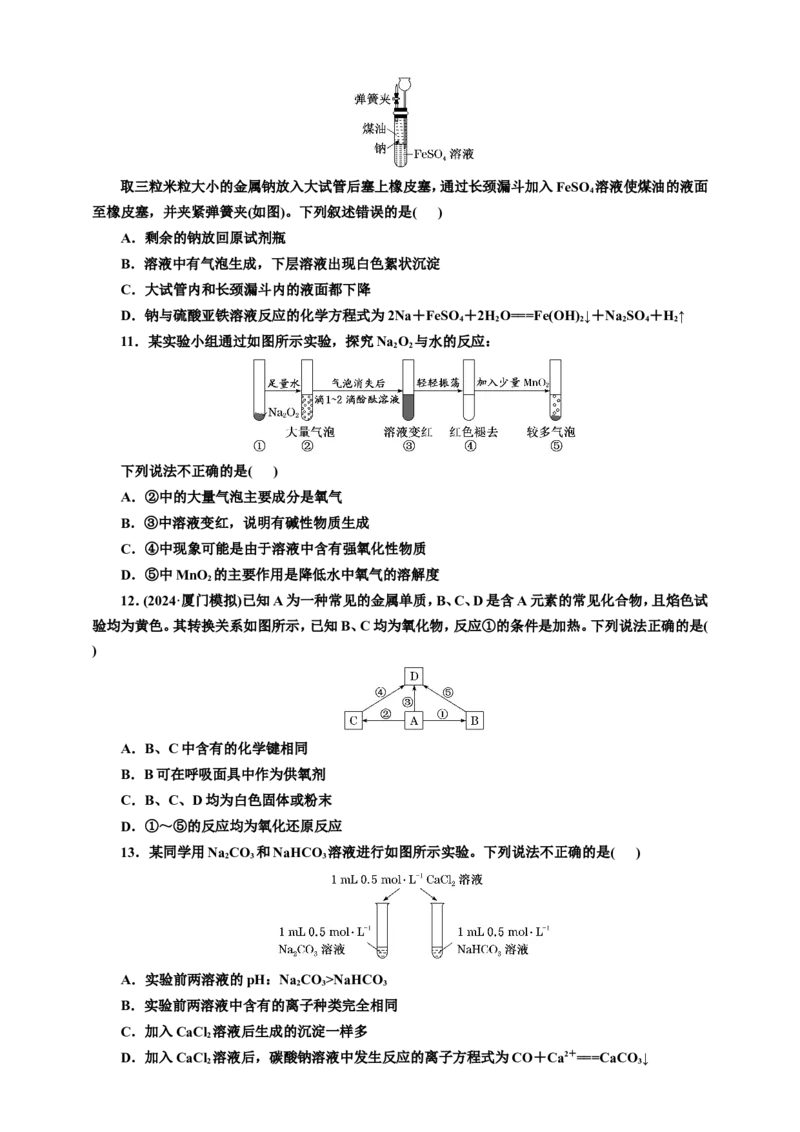
1.烟花绽放时能释放五彩缤纷的光芒。下列关于烟花燃放的化学原理说法错误的是( )
A.燃放时发生了氧化还原反应
B.发出黄色光芒,可见烟花中含有钠元素
C.未能观察到紫色光芒,可见烟花中不含钾元素
D.很多金属在灼烧时都会使火焰呈现出特征颜色
2.把一小块金属钠放入下列溶液中,说法正确的是( )
A.放入饱和NaOH溶液中:有氢气放出,恢复至原温度后溶液的pH增大
B.放入稀CuSO 溶液中:有氢气放出,有紫红色铜析出
4
C.放入MgCl 溶液中:有氢气放出,有白色沉淀生成
2
D.放入NH NO 溶液中:有无色无味气体放出
4 3
3.用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察到火焰呈黄色。下列判断正确的是(
)
A.只含有Na+
B.一定含有Na+,可能含有K+
C.既含有Na+,又含有K+
D.可能含有Na+,可能还含有K+
4.(2024·河南南阳模拟)钠及其化合物在工业生产中有重要作用,如图是钠的“价—类”二维图,
下列说法正确的是( )
A.Na在空气中燃烧生成Na O
2
B.Na O和Na O 都属于碱性氧化物
2 2 2
C.NaOH固体在空气中易变质,需密封保存
D.相同条件下,等物质的量的Na CO 和NaHCO 分别与足量盐酸反应,生成气体的体积不同
2 3 3
5.(2024·四川成都检测)如图,两圆圈相交的部分表示物质相互发生反应。已知钠及其氧化物的物
质的量均为0.1 mol,水的质量为100 g。下列说法正确的是( )
A.Na O 中阴、阳离子数目之比为1∶1
2 2
B.反应①的离子方程式为
Na+2HO===Na++2OH-+H↑
2 2
C.反应③转移的电子数为0.1N (N 表示阿伏加德罗常数的值)
A AD.①②③充分反应后所得溶液中NaOH的质量分数从小到大的顺序:①<③<②
6.下列有关铯及其化合物的说法不正确的是( )
A.CsOH的碱性比KOH的强
B.铯与水或稀盐酸反应剧烈,都生成H
2
C.Cs的还原性比Na的强,故Na+的氧化性强于Cs+
D.Li的金属性比Cs的强
7.(2024·台州模拟)某化学小组用如图中的实验装置证明过氧化钠可用作供氧剂,有关说法错误
的是( )
A.利用A装置可以制备H、O、CO 气体
2 2 2
B.B装置中应加入饱和Na CO 溶液,加入该试剂的目的是除去HCl气体
2 3
C.C装置中应加入Na O 固体,相关反应为
2 2
2Na O+2CO ===2Na CO +O
2 2 2 2 3 2
D.D装置中应加入浓NaOH溶液,加入该试剂的目的是除去多余的CO 气体
2
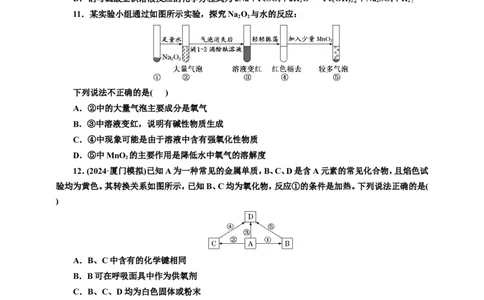
8.(2024·浙江嘉兴高三统考)探究钠及其化合物的性质,下列方案设计、现象和结论都正确的是(
)
实验方案 现象 结论
分别测定NaHCO 和 两者都大于7,且Na CO
3 2 3
A CO的水解能力强于HCO
Na CO 溶液的pH 溶液的pH大
2 3
对某未知溶液进行焰色试
B 火焰呈黄色 该溶液中含有钠盐
验
用形状和质量相同的钠,分
钠与乙醇反应比与苯酚反 乙醇中羟基的活性强于苯
C 别和等物质的量的苯酚和
应剧烈 酚中羟基的活性
乙醇反应
发生的反应:Ba2++
向饱和NaHCO 溶液中滴
3
D 溶液变浑浊同时产生气泡 2HCO=== BaCO ↓+CO ↑
3 2
加一定量的浓BaCl 溶液
2
+HO
2
9.将W g某气体与一定量的O 混合后通入装有足量 Na O 固体的密闭容器中,用间断电火花不
2 2 2
断地引燃气体,经过足够长的时间后,发现固体质量增加W g,则气体可能是( )
①H ②CO ③H 和CO的混合气体 ④甲醛(HCHO) ⑤乙二醇(CHOH—CH OH)蒸气
2 2 2 2
A.只有① B.只有①②
C.只有①②③ D.①②③④⑤
10.(2024·湖北黄冈联考)在隔绝空气的条件下让钠与FeSO 溶液反应,实验时,往100 mL 大试管
4
中先加40 mL煤油,取三粒米粒大小的金属钠放入大试管后塞上橡皮塞,通过长颈漏斗加入FeSO 溶液使煤油的液面
4
至橡皮塞,并夹紧弹簧夹(如图)。下列叙述错误的是( )
A.剩余的钠放回原试剂瓶
B.溶液中有气泡生成,下层溶液出现白色絮状沉淀
C.大试管内和长颈漏斗内的液面都下降
D.钠与硫酸亚铁溶液反应的化学方程式为2Na+FeSO+2HO===Fe(OH) ↓+Na SO +H↑
4 2 2 2 4 2
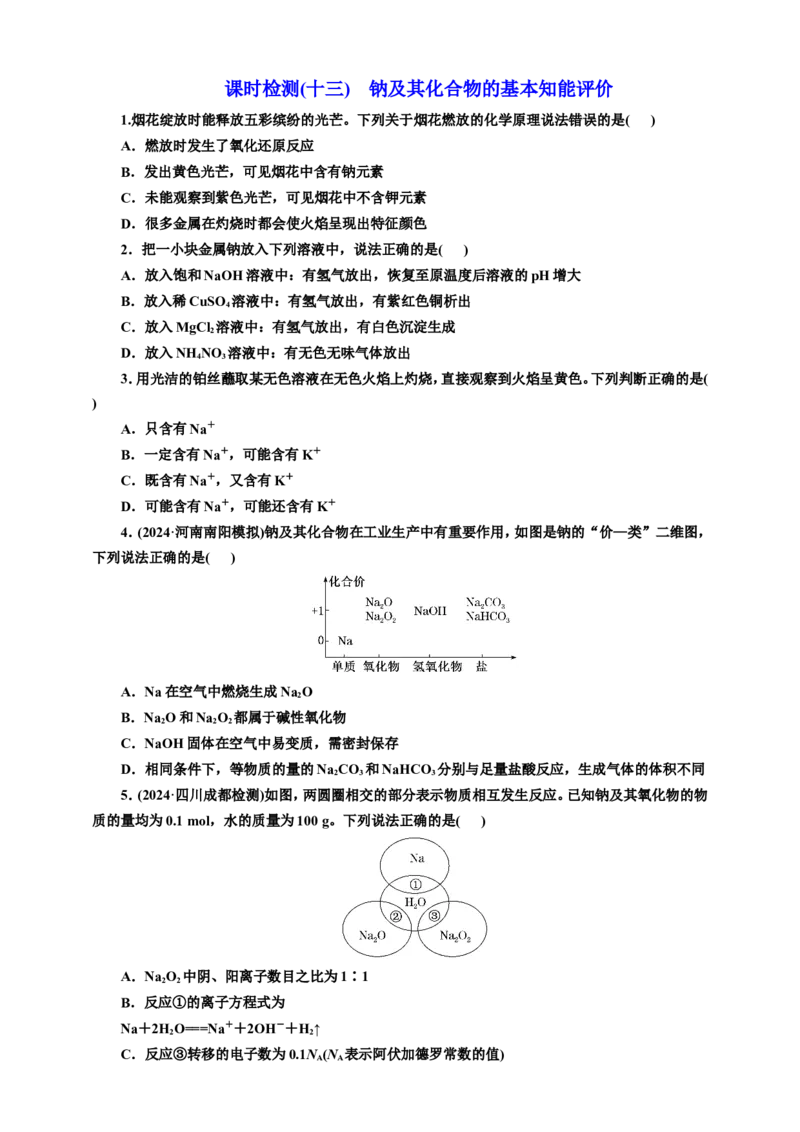
11.某实验小组通过如图所示实验,探究Na O 与水的反应:
2 2
下列说法不正确的是( )
A.②中的大量气泡主要成分是氧气
B.③中溶液变红,说明有碱性物质生成
C.④中现象可能是由于溶液中含有强氧化性物质
D.⑤中MnO 的主要作用是降低水中氧气的溶解度
2
12.(2024·厦门模拟)已知A为一种常见的金属单质,B、C、D是含A元素的常见化合物,且焰色试
验均为黄色。其转换关系如图所示,已知B、C均为氧化物,反应①的条件是加热。下列说法正确的是(
)
A.B、C中含有的化学键相同
B.B可在呼吸面具中作为供氧剂
C.B、C、D均为白色固体或粉末
D.①~⑤的反应均为氧化还原反应
13.某同学用Na CO 和NaHCO 溶液进行如图所示实验。下列说法不正确的是( )
2 3 3
A.实验前两溶液的pH:Na CO >NaHCO
2 3 3
B.实验前两溶液中含有的离子种类完全相同
C.加入CaCl 溶液后生成的沉淀一样多
2
D.加入CaCl 溶液后,碳酸钠溶液中发生反应的离子方程式为CO+Ca2+===CaCO ↓
2 314.某班级化学兴趣小组做如下实验,请回答相关问题:
(1) 甲 组 做 金 属 钠 在 空 气 中 燃 烧 的 实 验 。 实 验 室 取 用 金 属 钠 的 方 法 是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)金属钠燃烧时会生成 黑色固体, 黑色固体的可能 来源 是 ________________、
________________________________________________________________________。
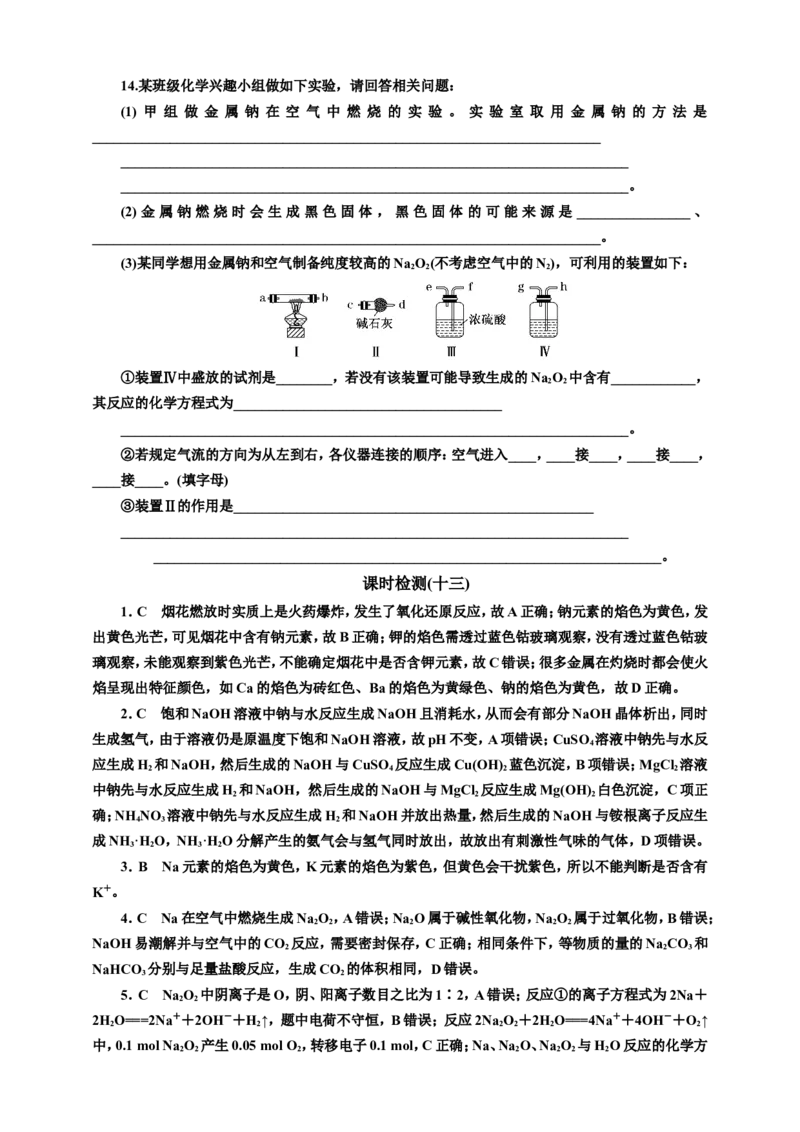
(3)某同学想用金属钠和空气制备纯度较高的Na O(不考虑空气中的N),可利用的装置如下:
2 2 2
①装置Ⅳ中盛放的试剂是________,若没有该装置可能导致生成的Na O 中含有____________,
2 2
其反应的化学方程式为______________________________________
________________________________________________________________________。
②若规定气流的方向为从左到右,各仪器连接的顺序:空气进入____,____接____,____接____,
____接____。(填字母)
③装置Ⅱ的作用是___________________________________________________
________________________________________________________________________
________________________________________________________________________。
课时检测(十三)
1.C 烟花燃放时实质上是火药爆炸,发生了氧化还原反应,故A正确;钠元素的焰色为黄色,发
出黄色光芒,可见烟花中含有钠元素,故B正确;钾的焰色需透过蓝色钴玻璃观察,没有透过蓝色钴玻
璃观察,未能观察到紫色光芒,不能确定烟花中是否含钾元素,故C错误;很多金属在灼烧时都会使火
焰呈现出特征颜色,如Ca的焰色为砖红色、Ba的焰色为黄绿色、钠的焰色为黄色,故D正确。
2.C 饱和NaOH溶液中钠与水反应生成NaOH且消耗水,从而会有部分NaOH晶体析出,同时
生成氢气,由于溶液仍是原温度下饱和NaOH溶液,故pH不变,A项错误;CuSO 溶液中钠先与水反
4
应生成H 和NaOH,然后生成的NaOH与CuSO 反应生成Cu(OH) 蓝色沉淀,B项错误;MgCl 溶液
2 4 2 2
中钠先与水反应生成H 和NaOH,然后生成的NaOH与MgCl 反应生成Mg(OH) 白色沉淀,C项正
2 2 2
确;NH NO 溶液中钠先与水反应生成H 和NaOH并放出热量,然后生成的NaOH与铵根离子反应生
4 3 2
成NH ·HO,NH ·HO分解产生的氨气会与氢气同时放出,故放出有刺激性气味的气体,D项错误。
3 2 3 2
3.B Na元素的焰色为黄色,K元素的焰色为紫色,但黄色会干扰紫色,所以不能判断是否含有
K+。
4.C Na在空气中燃烧生成Na O,A错误;Na O属于碱性氧化物,Na O 属于过氧化物,B错误;
2 2 2 2 2
NaOH易潮解并与空气中的CO 反应,需要密封保存,C正确;相同条件下,等物质的量的Na CO 和
2 2 3
NaHCO 分别与足量盐酸反应,生成CO 的体积相同,D错误。
3 2
5.C Na O 中阴离子是O,阴、阳离子数目之比为1∶2,A错误;反应①的离子方程式为2Na+
2 2
2HO===2Na++2OH-+H↑,题中电荷不守恒,B错误;反应2Na O+2HO===4Na++4OH-+O↑
2 2 2 2 2 2
中,0.1 mol Na O 产生0.05 mol O ,转移电子0.1 mol,C正确;Na、Na O、Na O 与HO反应的化学方
2 2 2 2 2 2 2程式分别为2Na+2HO===2NaOH+H↑,Na O+HO===2NaOH,2Na O+2HO===4NaOH+O↑,
2 2 2 2 2 2 2 2
0.1 mol Na、Na O、Na O 分别与水反应生成NaOH的物质的量为0.1 mol、0.2 mol、0.2 mol,溶液的质
2 2 2
量分别增加2.2 g、6.2 g、6.2 g,则质量分数分别为×100%、×100%、×100%,因此溶液中NaOH的质量
分数从小到大的顺序:①<②=③,D错误。
6.D 根据元素周期律,Cs的金属性比K强,故CsOH的碱性比KOH强;Cs的性质与钠相似,
Cs也能与水或稀盐酸反应生成H,反应更剧烈;Cs的还原性强于Na,则Na+得电子能力比Cs+强,即
2
氧化性:Na+>Cs+;A、B、C项正确。Li、Cs均为碱金属元素,Cs的电子层数多,更容易失去最外层电
子,故金属性:Cs>Li,D项错误。
7.B 饱和Na CO 溶液也吸收CO ,无法最后收集到O,B错误。
2 3 2 2
8.D 两溶液的浓度未知,不能根据溶液的pH值判断水解程度的大小,故A错误;焰色呈黄色说
明溶液中存在钠离子,不一定是钠盐,故B错误;钠与苯酚反应比钠与乙醇反应剧烈,苯酚中的羟基活
性强于乙醇中羟基,故C错误;通过现象可知反应生成碳酸钡和二氧化碳气体,则反应离子方程式为
Ba2++2HCO=== BaCO ↓+CO ↑+HO,故D正确。
3 2 2
9.D H 燃烧方程式为2H+O=====2HO,水与过氧化钠发生反应:2HO+2Na O===4NaOH
2 2 2 2 2 2 2
+O↑,方程式相加可得H+Na O===2NaOH,固体增加的质量相当于H 的质量;CO燃烧方程式为
2 2 2 2 2
2CO+O=====2CO ,二氧化碳与过氧化钠发生反应:2CO +2Na O===2Na CO +O,方程式相加
2 2 2 2 2 2 3 2
可得CO+Na O===Na CO ,固体增加的质量相当于CO的质量;由上述分析可知,CO、H 混合气体
2 2 2 3 2
的燃烧产物再通过过氧化钠,过氧化钠固体质量的增加量就是原混合气体中CO、H 的质量和;有机物
2
组成可以改写为(CO) ·yH 形式,相当于CO、H 的混合气体,燃烧产物再通过过氧化钠,固体质量的增
x 2 2
加量就是有机物蒸气的质量;故①②③④⑤均符合题意。
10.C 钠的密度大于煤油,故钠在煤油底部,与硫酸亚铁溶液接触并发生反应,生成氢氧化亚铁、
硫酸钠和氢气,反应的现象为溶液中有气泡生成,下层溶液出现白色絮状沉淀,据此分析。钠性质活泼
易与水、空气反应而引起火灾,故剩余的钠不能随意丢弃,应放回原试剂瓶,A正确;钠与水反应生成
NaOH和H,NaOH与FeSO 溶液反应生成白色絮状沉淀,B正确;由于生成H,反应一段时间后,大
2 4 2
试管内液面下降,长颈漏斗中液面上升,C错误;钠与水反应生成氢氧化钠,氢氧化钠与硫酸亚铁反应,
生成氢氧化亚铁沉淀,反应的化学方程式为2Na+FeSO+2HO===Fe(OH) ↓+Na SO +H↑,D正确。
4 2 2 2 4 2
11.D 过氧化钠和水反应生成氢氧化钠和氧气,②中的大量气泡主要成分是氧气,A正确;氢氧
化钠是碱,使酚酞溶液变红,B正确;④中溶液红色褪去,可能原因是过氧化钠和水反应生成的中间物
质过氧化氢具有强氧化性,能氧化有色物质,使溶液褪色,C正确;过氧化氢在二氧化锰作催化剂的条
件下分解生成水和氧气,即加入MnO 的目的是验证过氧化钠和水反应生成过氧化氢,而不是降低水
2
中氧气的溶解度,D错误。
12.B 已知A为一种常见的金属单质,B、C、D是含A元素的常见化合物,且焰色试验均为黄色,
则A为Na。已知B、C均为氧化物,反应①的条件是加热,则B为过氧化钠,C为氧化钠,D为氢氧化
钠。B(过氧化钠)含有离子键和非极性键,C(氧化钠)含有离子键,两者含有的化学键不相同,故A错误;
过氧化钠和二氧化碳、水反应生成氧气,因此B可在呼吸面具中作为供氧剂,故B正确;B为淡黄色固
体,故C错误;氧化钠和水反应生成氢氧化钠,则④反应为非氧化还原反应,故D错误。
13.C 等浓度的Na CO 和NaHCO 溶液中,碳酸钠溶液中碳酸根离子的水解程度大于碳酸氢根
2 3 3
离子的水解程度,碳酸钠溶液的pH大于碳酸氢钠溶液的pH,故A正确;实验前两溶液中含有的离子
种类完全相同,均为碳酸根离子、碳酸氢根离子、氢氧根离子、钠离子和氢离子,故B正确;碳酸氢钠和氯化钙溶液不反应,碳酸钠和氯化钙以1∶1反应生成碳酸钙沉淀,故C错误;加入CaCl 溶液后,碳
2
酸钠溶液中发生反应的离子方程式为CO+Ca2+===CaCO ↓,故D正确。
3
14.解析:(3)要制备高纯度的Na O,需要除去空气中的CO 和水蒸气。装置Ⅲ的作用是除去水蒸
2 2 2
气,装置Ⅳ的作用是除去CO ,如果不除去CO ,则CO 会与Na O 反应生成Na CO ;装置Ⅱ连接在
2 2 2 2 2 2 3
硬质玻璃管末端,作用是防止空气中的水蒸气和 CO 进入装置Ⅰ,所以连接顺序为空气
2
→h→g→f→e→a→b→c。
答案:(1)打开盛放金属钠的试剂瓶,用镊子取出一块钠,放在滤纸上吸干表面的煤油,再用小刀切
下所需大小的钠块,余下的放回原试剂瓶,盖好即可
(2)表面的煤油 空气中的二氧化碳 酒精灯挥发的酒精 金属钠中存在的杂质铁(答任意两点即
可)
(3)①氢氧化钠溶液 Na CO 2Na O+2CO ===2Na CO +O
2 3 2 2 2 2 3 2
②h g f e a(或b) b(或a) c
③防止空气中的水和二氧化碳进入装置Ⅰ