文档内容
难溶电解质的沉淀溶解平衡作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 1-7 题为三星,8-13 题为四星,14-16 题为五星。
1.下列说法正确的是( ) ☆☆☆
A.溶度积就是溶解平衡时难溶电解质在溶液中的各离子浓度的乘积
B.溶度积常数是不受任何条件影响的常数,简称溶度积
C.可用离子积 Qc 与溶度积 K 的比较来判断沉淀溶解平衡进行的方向
sp
D.所有物质的溶度积都是随温度的升高而增大的
【解答】
A、溶度积就是溶解平衡时难溶电解质在溶液中的各离子浓度幂次方乘积,
故 A 错误;
B、溶度积常数是受温度影响的常数,简称溶度积,故 B 错误;
C、可用离子积 Q 判断沉淀溶解平衡进行的方向,Qc>Ksp,平衡向沉淀方向进
c
行,Qc<Ksp,向物质溶解方向进行,Qc=Ksp,沉淀溶解达到平衡状态,故 C 正
确;
D、物质溶解度有的随温度升高增大,有的随温度升高减小,所以溶度积常数随
温度升高可逆增大或减小,如氢氧化钙沉淀溶解平衡状态,升温平衡沉淀方向进
行,故 D 错误。
故选 C.
2.下列有关沉淀溶解平衡的说法正确的是( ) ☆☆☆
A.K (AB)小于 K (CD),则物质 AB 的溶解度一定小于物质 CD 的溶解度
SP 2 SP 2
B.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的 K 增大
SP
第 1页(共 12页)C.在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘
化银沉淀
D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动
【解答】
A、因比较不同类型的难溶物的溶解度大小,必须通过计算溶解度比较,不能通
过溶度积直接比较,故 A 错误;
B、因难溶盐电解质的 Ksp 与温度有关,不受其他因素的影响,所以加入蒸馏水,
氯化银的 K 不变,故 B 错误;
SP
C、因氯化银的溶度积大于碘化银的溶度积,所以氯化银沉淀可转化为碘化银沉
淀,故 C 正确;
D、碳酸根离子与酸反应生成二氧化碳和水,生成物的浓度减小,碳酸钙的沉淀
溶解平衡正向移动,故 D 错误。
故选:C.
3.当氢氧化镁固体在水中达到溶解平衡 Mg(OH)
2
(s)
⇌
Mg2+(aq)+2OH﹣(aq),
为使固体的量减少,可加入少量的( ) ☆☆☆
A.NH•HO B.NaOH C.MgSO D.NaHSO
3 2 4
4
【解答】
A.NH
3
•H
2
O 电离出 OH﹣,生成物浓度增大,使 Mg(OH)
2
(s)
⇌
Mg2+(aq)+2OH
﹣
(aq)平衡逆向移动,固体增多,故 A 不选;
B.NaOH 电离出 OH﹣,生成物浓度增大,使 Mg(OH)
2
(s)
⇌
Mg2+(aq)+2OH﹣(aq)
平衡逆向移动,固体增多,故 B 不选;
C.MgSO (aq)+2OH﹣(aq)
2+
4
电离出 Mg2+,生成物浓度增大,使 Mg(OH)
2
(s)
⇌
Mg
平衡逆向移动,固体增多,故 C 不选;
D.NaHSO
4
电离出 H
+
,与 OH﹣反应,生成物浓度减小,则 Mg(OH)
2
(s)
⇌
Mg2+(aq)
+2OH﹣(aq)平衡正向移动,固体减少,故 D 选。
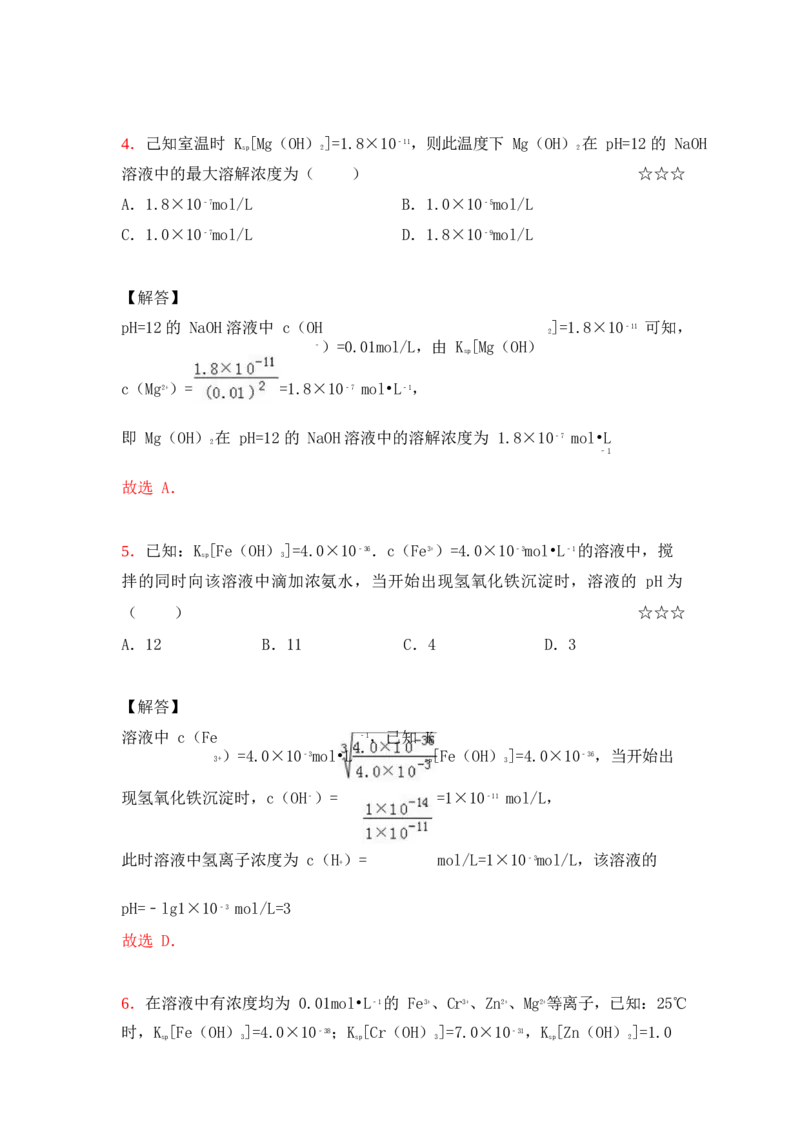
故选 D.第 2页(共 12页)4.己知室温时 K [Mg(OH)]=1.8×10﹣11,则此温度下 Mg(OH) 在 pH=12 的 NaOH
sp 2 2
溶液中的最大溶解浓度为( ) ☆☆☆
A.1.8×10﹣7mol/L B.1.0×10﹣5mol/L
C.1.0×10﹣7mol/L D.1.8×10﹣9mol/L
【解答】
pH=12 的 NaOH 溶液中 c(OH ]=1.8×10﹣11 可知,
2
﹣)=0.01mol/L,由 K [Mg(OH)
sp
c(Mg2+)= =1.8×10﹣7 mol•L﹣1,
即 Mg(OH) 在 pH=12 的 NaOH 溶液中的溶解浓度为 1.8×10﹣7 mol•L
2
﹣1
故选 A.
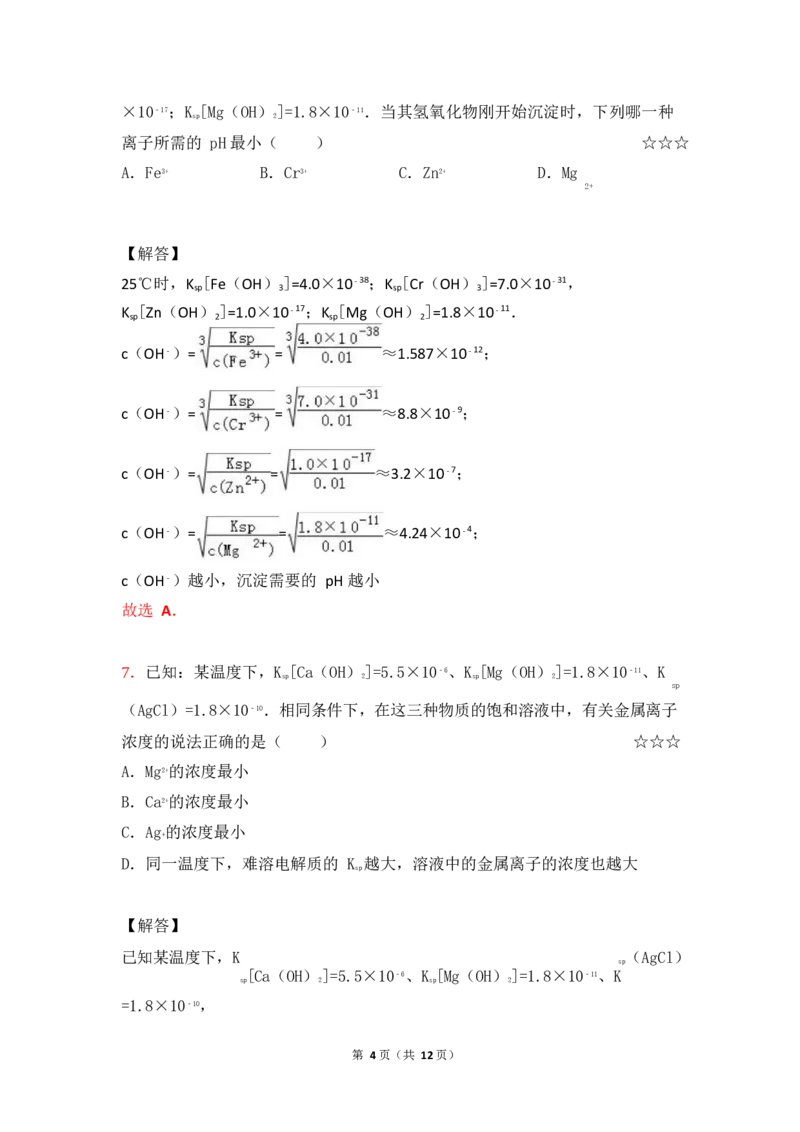
5.已知:K [Fe(OH)]=4.0×10﹣36.c(Fe3+)=4.0×10﹣3mol•L﹣1 的溶液中,搅
sp 3
拌的同时向该溶液中滴加浓氨水,当开始出现氢氧化铁沉淀时,溶液的 pH 为
( ) ☆☆☆
A.12 B.11 C.4 D.3
【解答】
溶液中 c(Fe ﹣1,已知 K
)=4.0×10﹣3mol•L [Fe(OH)]=4.0×10﹣36,当开始出
3+ sp 3
现氢氧化铁沉淀时,c(OH﹣)= =1×10﹣11 mol/L,
此时溶液中氢离子浓度为 c(H)= mol/L=1×10﹣3mol/L,该溶液的
+
pH=﹣lg1×10﹣3 mol/L=3
故选 D.
6.在溶液中有浓度均为 0.01mol•L﹣1 的 Fe3+、Cr3+、Zn2+、Mg2+等离子,已知:25℃
时,K [Fe(OH)]=4.0×10﹣38;K [Cr(OH)]=7.0×10﹣31,K [Zn(OH)]=1.0
sp 3 sp 3 sp 2第 3页(共 12页)×10﹣17;K [Mg(OH)]=1.8×10﹣11.当其氢氧化物刚开始沉淀时,下列哪一种
sp 2
离子所需的 pH 最小( ) ☆☆☆
A.Fe3+ B.Cr3+ C.Zn2+ D.Mg
2+
【解答】
25℃时,K [Fe(OH) ]=4.0×10﹣38;K [Cr(OH) ]=7.0×10﹣31,
sp 3 sp 3
K [Zn(OH) ]=1.0×10﹣17;K [Mg(OH) ]=1.8×10﹣11.
sp 2 sp 2
c(OH﹣)= = ≈1.587×10﹣12;
c(OH﹣)= = ≈8.8×10﹣9;
c(OH﹣)= = ≈3.2×10﹣7;
c(OH﹣)= = ≈4.24×10﹣4;
c(OH﹣)越小,沉淀需要的 pH 越小
故选 A.
7.已知:某温度下,K [Ca(OH)]=5.5×10﹣6、K [Mg(OH)]=1.8×10﹣11、K
sp 2 sp 2
sp
(AgCl)=1.8×10﹣10.相同条件下,在这三种物质的饱和溶液中,有关金属离子
浓度的说法正确的是( ) ☆☆☆
A.Mg2+的浓度最小
B.Ca2+的浓度最小
C.Ag的浓度最小
+
D.同一温度下,难溶电解质的 K 越大,溶液中的金属离子的浓度也越大
sp
【解答】
已知某温度下,K (AgCl)
sp
[Ca(OH)]=5.5×10﹣6、K [Mg(OH)]=1.8×10﹣11、K
sp 2 sp 2
=1.8×10﹣10,
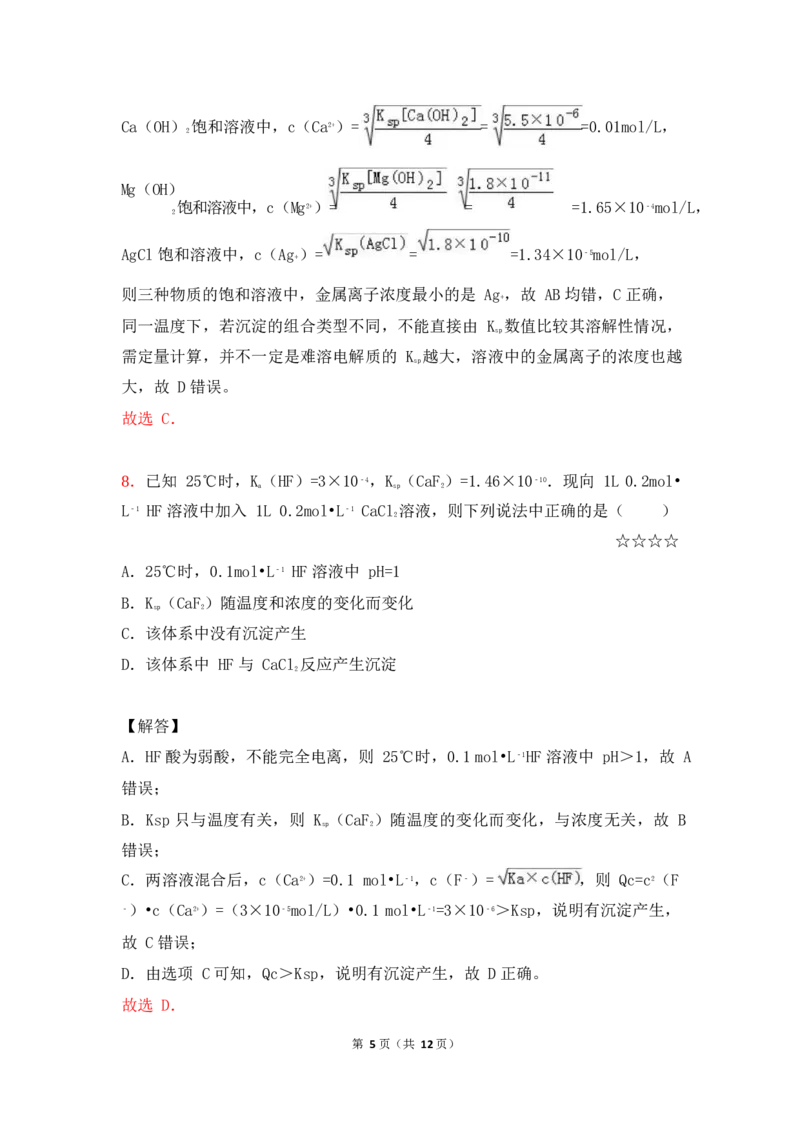
第 4页(共 12页)Ca(OH) 饱和溶液中,c(Ca2+)= = =0.01mol/L,
2
Mg(OH)
饱和溶液中,c(Mg2+)= = =1.65×10﹣4mol/L,
2
AgCl 饱和溶液中,c(Ag)= = =1.34×10﹣5mol/L,
+
则三种物质的饱和溶液中,金属离子浓度最小的是 Ag,故 AB 均错,C 正确,
+
同一温度下,若沉淀的组合类型不同,不能直接由 K 数值比较其溶解性情况,
sp
需定量计算,并不一定是难溶电解质的 K 越大,溶液中的金属离子的浓度也越
sp
大,故 D 错误。
故选 C.
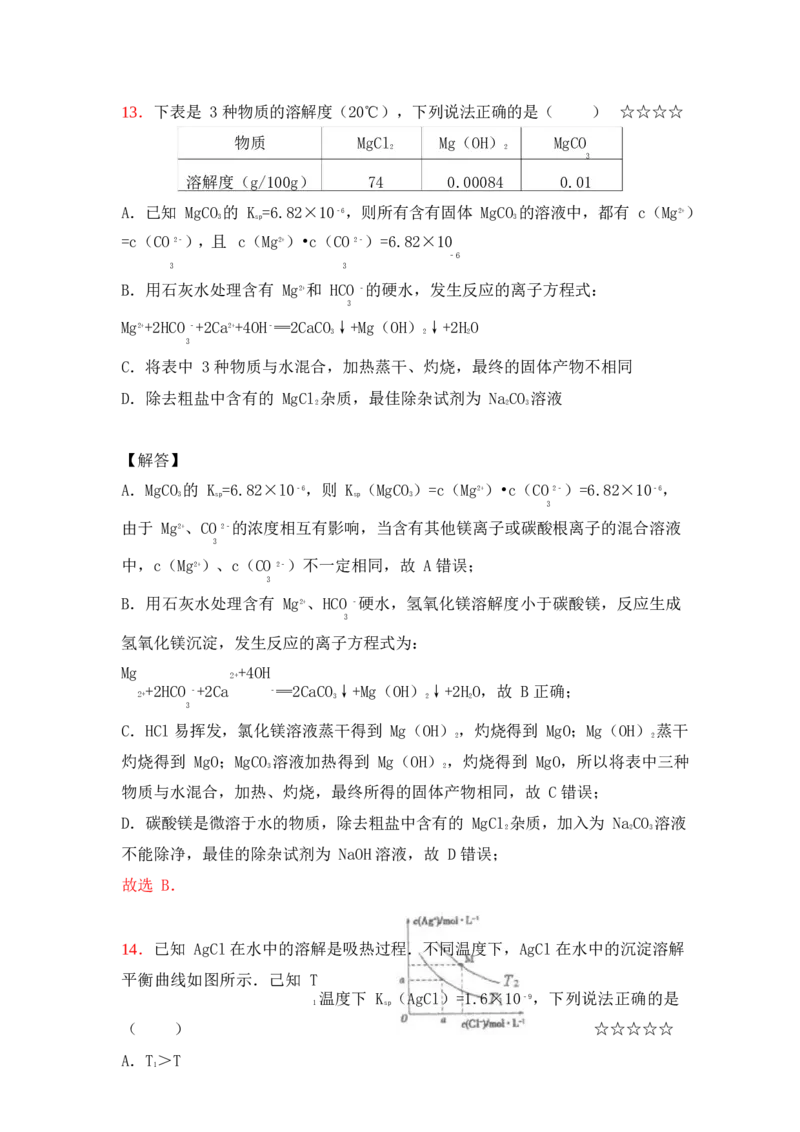
8.已知 25℃时,K(HF)=3×10﹣4,K (CaF)=1.46×10﹣10.现向 1L 0.2mol•
a sp 2
L﹣1 HF 溶液中加入 1L 0.2mol•L﹣1 CaCl 溶液,则下列说法中正确的是( )
2
☆☆☆☆
A.25℃时,0.1mol•L﹣1 HF 溶液中 pH=1
B.K (CaF)随温度和浓度的变化而变化
sp 2
C.该体系中没有沉淀产生
D.该体系中 HF 与 CaCl 反应产生沉淀
2
【解答】
A.HF 酸为弱酸,不能完全电离,则 25℃时,0.1 mol•L﹣1HF 溶液中 pH>1,故 A
错误;
B.Ksp 只与温度有关,则 K (CaF)随温度的变化而变化,与浓度无关,故 B
sp 2
错误;
C.两溶液混合后,c(Ca2+)=0.1 mol•L﹣1,c(F﹣)= ,则 Qc=c2(F
﹣)•c(Ca2+)=(3×10﹣5mol/L)•0.1 mol•L﹣1=3×10﹣6>Ksp,说明有沉淀产生,
故 C 错误;
D.由选项 C 可知,Qc>Ksp,说明有沉淀产生,故 D 正确。
故选 D.
第 5页(共 12页)9.已知:25℃时,K [Mg(OH)]=5.61×10﹣12,K [MgF]=7.42×10﹣11.下列说
sp 2 sp 2
法正确的是( ) ☆☆☆☆
A.25℃时,饱和 Mg(OH)
溶液与饱和 MgF 溶液相比,前者的 c(Mg2+)大
2 2
B.25℃时,在 Mg(OH)
的悬浊液加入少量的 NHCl 固体,c(Mg2+)增大
2 4
C.25℃时,Mg(OH)
固体在 20 mL 0.01 mol•L﹣1 氨水中的 K 比在 20 mL 0.01
2 sp
mol•L﹣1 NHCl 溶液中的 K 小
4 sp
D.25℃时,在 MgF 的悬浊液加入 NaOH 溶液后,MgF 不可能转化成为 Mg(OH)
2 2
2
【解答】
A、因氢氧化镁溶度积小,由 K
可知,则其 Mg2+浓度小,故 A 错误;
sp
B、NH 结合 OH﹣使氢氧化镁溶解平衡正向移动,Mg2+增大,故 B 正确;
+
4
C、Ksp 不随浓度变化,只与温度有关,故 C 错误;
D、氢氧化镁的溶度积小,只要加入 NaOH 溶液,就可以使氟化镁转化为氢氧化镁
沉淀,故 D 错误。
故选 B.
10.一定温度下,在 Ba(OH) 的悬浊液中,存在 Ba(OH) 固体与其电离的离
2 2
子间的溶解平衡关系:Ba(OH)
2
(s)
⇌
Ba2+(aq)+2OH﹣(aq) 向此体系中再
加入少量的 BaO 粉末,如果保持温度不变,则下列说法正确的是( )☆☆☆
☆
A.c(Ba2+)浓度增大 B.溶液中 Ba2+数目减少
C.溶液 pH 减小 D.溶液 pH 增大
【解答】
向悬浊液中加少量 BaO,发生:BaO+HO=Ba(OH),消耗水,因为 Ba(OH) 的
2 2 2
悬浊液,则溶液中浓度不变,因水减少,则析出 Ba(OH),溶液中 Ba2+数目减
2
少,pH 不变,只有 B 正确。故选 B.
第 6页(共 12页)11.常温下,K [Mg(OH)]=1.1×10﹣11,K (AgCl)=1.8×10﹣10,K (AgCrO)
sp 2 sp sp 2 4
=1.9×10﹣12,下列叙述不正确的是( ) ☆☆☆☆
A.浓度均为 2×10
﹣5mol•L﹣1 的 AgNO 溶液和 NaCl 溶液等体积混合,有白色沉淀
3
产生
B.将 0.001mol•L
﹣1 的 AgNO 溶液滴入 0.001mol•L﹣1 的 KCl 和 KCrO 的混合溶液
3 2 4
中,先产生 AgCl 沉淀
C.c(Mg2+)为 0.11mol•L﹣1 的溶液中要产生 Mg(OH) 沉淀,溶液的 pH 要控制
2
在 9 以上
D.其他条件不变,向饱和 AgCrO 水溶液中加入少量 KCrO 溶液,溶液中 c(Ag )
2 4 2 4 +
减小
【解答】
A.浓度均为 2×10
﹣5mol/L 的 AgNO 溶液和 NaCl 溶液等体积混合,混合后,c(Ag )
3 +
=1×10﹣5mol/L,c(Cl﹣)=1×10﹣5mol/L,
则浓度积 Qc=c(Ag)c(Cl﹣)=1×10﹣10<K (AgCl),沉淀溶解平衡向沉淀溶解
+ sp
的方向进行,没有 AgCl 白色沉淀生成,故 A 错误;
B.将 0.001mol/L 的 AgNO 溶液滴入 0.001mol/L 的 KCl 和 KCrO 的混合溶液中,
3 2 4
产生 AgCl 沉淀需要 Ag的浓度为 c(Ag)= =
+ +
=1.8 × 10 ﹣ 7mol/L , 产 生 Ag
2
CrO
4
需 要 Ag
+
的 浓 度 为 c ( Ag
+
)
= = =4.36×10﹣5mol/L,因此达到 AgCl 沉淀所需的
Ag浓度相对较小,优先产生 AgCl 沉淀,故 B 正确;
+
C.c(Mg
)为 0.11mol/L 溶液,要产生 Mg(OH) 沉淀,当恰好产生 Mg(OH)
2+ 2
2
沉淀时,溶液中 c(OH﹣)= = =1×10﹣5mol/L,则溶
液的 pH=14﹣pOH=9,即溶液的 pH 值控制在 9 以上,故 C 正确;
D.饱和 Ag2
CrO
4
水溶液存在沉淀溶解平衡:Ag
2
CrO
4
(s)
⇌
2Ag
+
(aq)+CrO 2﹣(aq),
4
第 7页(共 12页)加入少量的 KCrO
2
溶液,溶液中 c(CrO 2﹣)增大,平衡向左移动,溶液中 c(Ag )
4 +
4
减小,故 D 正确。
故选 A.
12.已知 25℃时,几种难溶电解质的溶度积常数 Ksp 如表所示:
难容电解质 AgCl AgBr Agl AgSO AgCrO
2 4 2
4
Ksp 1.8×10﹣10 5.4×10﹣13 8.5×10
﹣17
1.4×10﹣5 1.12×10﹣12
下列叙述正确的是( ) ☆☆☆☆
A.由溶度积常数可以判断相应物质的溶解性大小
B.将等体积的 4×10﹣3 mol/L 的 AgNO 溶液和 4×10﹣3 mol/L KCrO 溶液混合,
3 2 4
有 AgCrO 沉淀产生
2 4
C.向 AgCl 的悬浊液中滴加饱和 NaBr 溶液不能得到黄色 AgBr
D.向 100 mL 0.02mol/L 的 NaSO 溶液中加入 100mL 0.02mol/L 的 AgNO 溶
2 4 3
液,有白色沉淀生成
【解答】
A.对于结构相似的物质,溶度积常数越小,则溶解度越小,而组成、结构不相
似的物质,不能根据溶度积常数大小比较溶解性,故 A 错误;
B.由离子的浓度可知,(2×10﹣3)2×(2×10﹣3)=8×10﹣9>Ksp=1.12×10﹣12,
所以有 AgCrO 沉淀产生,故 B 正确;
2 4
C.由表格中的 Ksp 可知,1.8×10﹣10>8.5×10﹣17,则 AgI 的溶度积比 AgCl 小,
所以向 AgCl 的悬浊液中滴加 NaI 的饱和溶液可以得到黄色 AgI 悬浊液,故 C 错
误;
D.由离子浓度可知,0.01×(0.01)2=10﹣6<Ksp=1.4×10﹣5,则没有白色沉淀
生成,故 D 错误;
故选 B.第 8页(共 12页)13.下表是 3 种物质的溶解度(20℃),下列说法正确的是( ) ☆☆☆☆
物质 MgCl Mg(OH) MgCO
2 2
3
溶解度(g/100g) 74 0.00084 0.01
A.已知 MgCO 的 K =6.82×10﹣6,则所有含有固体 MgCO 的溶液中,都有 c(Mg2+)
3 sp 3
=c(CO 2﹣),且 c(Mg2+)•c(CO 2﹣)=6.82×10
﹣6
3 3
B.用石灰水处理含有 Mg2+和 HCO ﹣的硬水,发生反应的离子方程式:
3
Mg2++2HCO ﹣+2Ca2++4OH﹣═2CaCO↓+Mg(OH)↓+2HO
3 2 2
3
C.将表中 3 种物质与水混合,加热蒸干、灼烧,最终的固体产物不相同
D.除去粗盐中含有的 MgCl 杂质,最佳除杂试剂为 NaCO 溶液
2 2 3
【解答】
A.MgCO 的 K =6.82×l0﹣6,则 K (MgCO)=c(Mg2+)•c(CO 2﹣)=6.82×10﹣6,
3 sp sp 3
3
由于 Mg2+、CO 2﹣的浓度相互有影响,当含有其他镁离子或碳酸根离子的混合溶液
3
中,c(Mg2+)、c(CO 2﹣)不一定相同,故 A 错误;
3
B.用石灰水处理含有 Mg2+、HCO ﹣硬水,氢氧化镁溶解度小于碳酸镁,反应生成
3
氢氧化镁沉淀,发生反应的离子方程式为:
Mg +4OH
2+
+2HCO ﹣+2Ca ﹣═2CaCO↓+Mg(OH)↓+2HO,故 B 正确;
2+ 3 2 2
3
C.HCl 易挥发,氯化镁溶液蒸干得到 Mg(OH),灼烧得到 MgO;Mg(OH) 蒸干
2 2
灼烧得到 MgO;MgCO 溶液加热得到 Mg(OH),灼烧得到 MgO,所以将表中三种
3 2
物质与水混合,加热、灼烧,最终所得的固体产物相同,故 C 错误;
D.碳酸镁是微溶于水的物质,除去粗盐中含有的 MgCl 杂质,加入为 NaCO 溶液
2 2 3
不能除净,最佳的除杂试剂为 NaOH 溶液,故 D 错误;
故选 B.
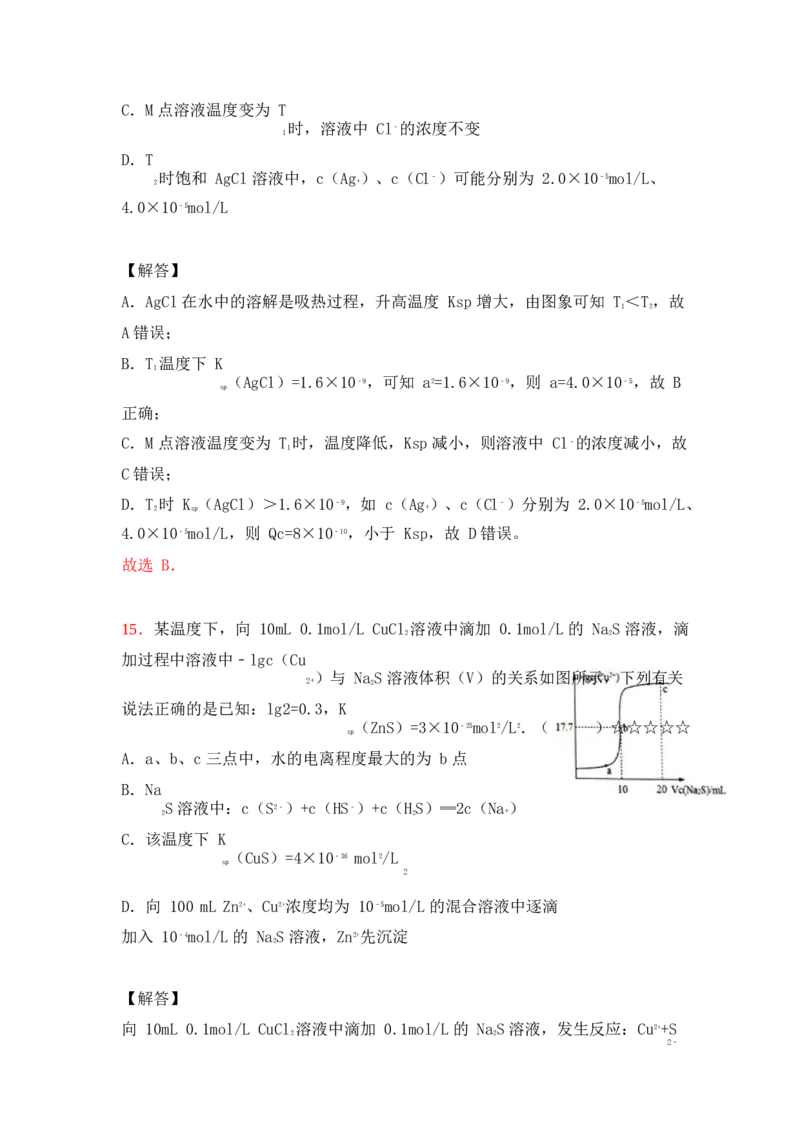
14.已知 AgCl 在水中的溶解是吸热过程.不同温度下,AgCl 在水中的沉淀溶解
平衡曲线如图所示.己知 T
温度下 K (AgCl)=1.6×10﹣9,下列说法正确的是
1 sp
( ) ☆☆☆☆☆
A.T>T
12
B.a=4.0×10
﹣5
第 9页(共 12页)C.M 点溶液温度变为 T
时,溶液中 Cl﹣的浓度不变
1
D.T
时饱和 AgCl 溶液中,c(Ag)、c(Cl﹣)可能分别为 2.0×10﹣5mol/L、
2 +
4.0×10﹣5mol/L
【解答】
A.AgCl 在水中的溶解是吸热过程,升高温度 Ksp 增大,由图象可知 T<T,故
1 2
A 错误;
B.T 温度下 K
1
(AgCl)=1.6×10﹣9,可知 a2=1.6×10﹣9,则 a=4.0×10﹣5,故 B
sp
正确;
C.M 点溶液温度变为 T 时,温度降低,Ksp 减小,则溶液中 Cl﹣的浓度减小,故
1
C 错误;
D.T 时 K (AgCl)>1.6×10﹣9,如 c(Ag)、c(Cl﹣)分别为 2.0×10﹣5mol/L、
2 sp +
4.0×10﹣5mol/L,则 Qc=8×10﹣10,小于 Ksp,故 D 错误。
故选 B.
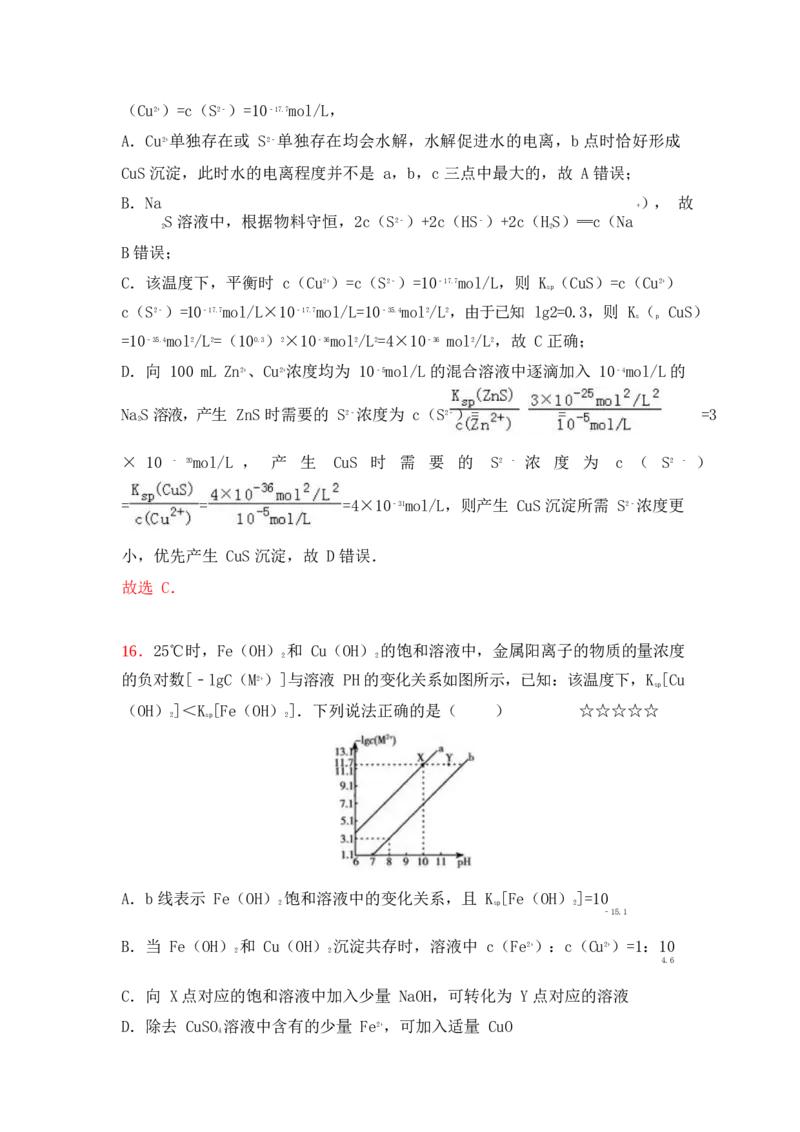
15.某温度下,向 10mL 0.1mol/L CuCl 溶液中滴加 0.1mol/L 的 NaS 溶液,滴
2 2
加过程中溶液中﹣lgc(Cu
)与 NaS 溶液体积(V)的关系如图所示,下列有关
2+ 2
说法正确的是已知:lg2=0.3,K
(ZnS)=3×10﹣25mol2/L2.( )☆☆☆☆☆
sp
A.a、b、c 三点中,水的电离程度最大的为 b 点
B.Na
S 溶液中:c(S2﹣)+c(HS﹣)+c(HS)═2c(Na)
2 2 +
C.该温度下 K
(CuS)=4×10﹣36 mol2/L
sp
2
D.向 100 mL Zn2+、Cu2+浓度均为 10﹣5mol/L 的混合溶液中逐滴
加入 10﹣4mol/L 的 NaS 溶液,Zn2+先沉淀
2
【解答】
向 10mL 0.1mol/L CuCl 溶液中滴加 0.1mol/L 的 NaS 溶液,发生反应:Cu2++S
2 2
2﹣⇌
CuS↓,Cu2+单独存在或 S2﹣单独存在均会水解,水解促进水的电离,b 点溶液
时滴加 NaS 溶液的体积是 20mL,此时恰好生成 CuS 沉淀,CuS 存在沉淀溶解平
2
衡:CuS(s)
⇌
Cu2+(aq)+S2﹣(aq),已知此时﹣lgc(Cu2+)=17.7,则平衡时 c
第 10页(共 12页)(Cu2+)=c(S2﹣)=10﹣17.7mol/L,
A.Cu2+单独存在或 S2﹣单独存在均会水解,水解促进水的电离,b 点时恰好形成
CuS 沉淀,此时水的电离程度并不是 a,b,c 三点中最大的,故 A 错误;
B.Na ), 故
+
S 溶液中,根据物料守恒,2c(S2﹣)+2c(HS﹣)+2c(HS)═c(Na
2 2
B 错误;
C.该温度下,平衡时 c(Cu2+)=c(S2﹣)=10﹣17.7mol/L,则 K (CuS)=c(Cu2+)
sp
c(S2﹣)=10﹣17.7mol/L×10﹣17.7mol/L=10﹣35.4mol2/L2,由于已知 lg2=0.3,则 K( CuS)
s p
=10﹣35.4mol2/L2=(100.3)2×10﹣36mol2/L2=4×10﹣36 mol2/L2,故 C 正确;
D.向 100 mL Zn2+、Cu2+浓度均为 10﹣5mol/L 的混合溶液中逐滴加入 10﹣4mol/L 的
NaS 溶液,产生 ZnS 时需要的 S2﹣浓度为 c(S2﹣)= = =3
2
× 10 ﹣ 20mol/L , 产 生 CuS 时 需 要 的 S2 ﹣ 浓 度 为 c ( S2 ﹣ )
= = =4×10﹣31mol/L,则产生 CuS 沉淀所需 S2﹣浓度更
小,优先产生 CuS 沉淀,故 D 错误.
故选 C.
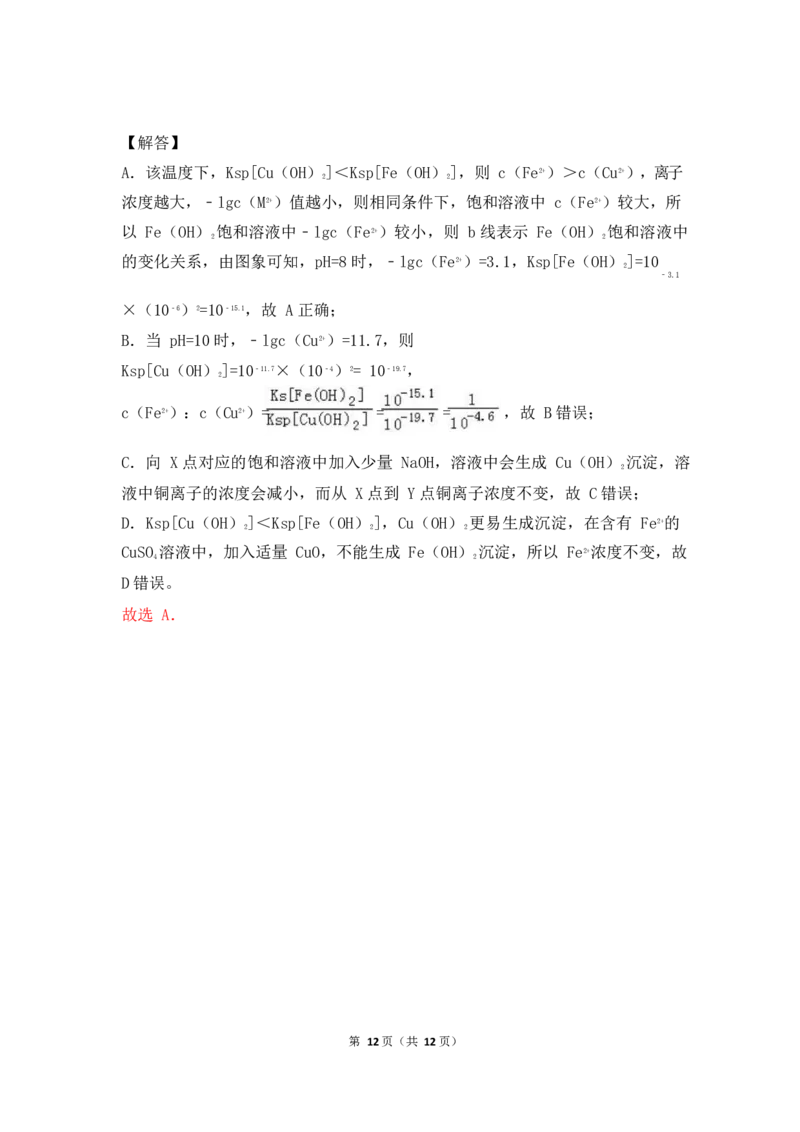
16.25℃时,Fe(OH) 和 Cu(OH) 的饱和溶液中,金属阳离子的物质的量浓度
2 2
的负对数[﹣lgC(M2+)]与溶液 PH 的变化关系如图所示,已知:该温度下,K [Cu
sp
(OH)]<K [Fe(OH)].下列说法正确的是( ) ☆☆☆☆☆
2 sp 2
A.b 线表示 Fe(OH) 饱和溶液中的变化关系,且 K [Fe(OH)]=10
2 sp 2
﹣15.1
B.当 Fe(OH) 和 Cu(OH) 沉淀共存时,溶液中 c(Fe2+):c(Cu2+)=1:10
2 2
4.6
C.向 X 点对应的饱和溶液中加入少量 NaOH,可转化为 Y 点对应的溶液
D.除去 CuSO 溶液中含有的少量 Fe2+,可加入适量 CuO
4第 11页(共 12页)【解答】
A.该温度下,Ksp[Cu(OH)]<Ksp[Fe(OH)],则 c(Fe2+)>c(Cu2+),离子
2 2
浓度越大,﹣lgc(M2+)值越小,则相同条件下,饱和溶液中 c(Fe2+)较大,所
以 Fe(OH) 饱和溶液中﹣lgc(Fe2+)较小,则 b 线表示 Fe(OH) 饱和溶液中
2 2
的变化关系,由图象可知,pH=8 时,﹣lgc(Fe2+)=3.1,Ksp[Fe(OH)]=10
2
﹣3.1
×(10﹣6)2=10﹣15.1,故 A 正确;
B.当 pH=10 时,﹣lgc(Cu2+)=11.7,则
Ksp[Cu(OH)]=10﹣11.7×(10﹣4)2= 10﹣19.7,
2
c(Fe2+):c(Cu2+)= = = ,故 B 错误;
C.向 X 点对应的饱和溶液中加入少量 NaOH,溶液中会生成 Cu(OH) 沉淀,溶
2
液中铜离子的浓度会减小,而从 X 点到 Y 点铜离子浓度不变,故 C 错误;
D.Ksp[Cu(OH)]<Ksp[Fe(OH)],Cu(OH) 更易生成沉淀,在含有 Fe2+的
2 2 2
CuSO 溶液中,加入适量 CuO,不能生成 Fe(OH) 沉淀,所以 Fe2+浓度不变,故
4 2
D 错误。
故选 A.
第 12页(共 12页)