文档内容
一、选择题
1.(2019·河南中原名校第一次质量考评)二十四节气是中国历法的独特创造。四月农谚:
“雷雨肥田”“雨生百谷”描述的都是节气谷雨。下列元素在自然界中的转化与“雷雨肥
田”有关的是( )
A.K B.N
C.P D.C
解析:选B。“雷雨肥田”的意思是在放电条件下N 和O 反应生成NO,NO与O 反应
2 2 2
生成NO ,NO 与水反应生成HNO,HNO 随雨水降落与土壤中的物质反应生成硝酸盐,硝
2 2 3 3
酸盐作为氮肥被农作物吸收,B项正确。
2.(2019·汕头高三一模)化学与生产、生活息息相关。下列说法中正确的是( )
A.SO 、CO、NO 都是可形成酸雨的气体
2 2 2
B.农业施肥作业时,草木灰(有效成分为KCO)不能与NH Cl混合使用
2 3 4
C.地沟油不宜食用,可以分馏提取汽油,做汽车的燃料
D.向牛奶中加入果汁会产生沉淀,是因为发生了酸碱中和反应
解析:选B。SO 和NO 都是可形成酸雨的气体,CO 不能形成酸雨,但能形成温室效应,
2 2 2
A项错误;KCO 为强碱弱酸盐,NH Cl为强酸弱碱盐,草木灰与NH Cl混合使用时,CO与
2 3 4 4
NH发生相互促进的水解反应生成NH ,降低肥效,B项正确;地沟油的主要成分为油脂,汽
3
油的主要成分为烃,C项错误;牛奶中含有蛋白质,果汁能使蛋白质变性而沉淀,D项错误。
3.(2019·全国名校第二次大联考)下列由相关实验现象推出的结论正确的是( )
A.NH Cl和NH HCO 受热都能分解,说明可以用加热NH Cl和NH HCO 固体的方法
4 4 3 4 4 3
制氨
B.向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定含有SO
3 2
C.Fe与稀硝酸、稀硫酸反应均有气泡产生,说明Fe与两种酸均发生置换反应
D.NH 遇到浓盐酸产生白烟,说明二者发生反应生成白色固体
3
解析:选D。NH Cl受热分解生成氨和氯化氢,冷却后二者又重新结合生成NH Cl,不能
4 4
制备氨,NH HCO 受热分解生成氨、二氧化碳和水,制得的氨中混有二氧化碳,不适合制备
4 3
氨,A项错误;向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,在酸性条件下NO具有强
3 2
氧化性,会把SO氧化成SO,故不能说明原溶液中一定含有SO,也可能含有SO,B项错误;
Fe与稀硝酸、稀硫酸反应均有气泡产生,前者是由于稀硝酸的强氧化性,后者是由于Fe与稀
硫酸发生置换反应,C项错误;NH 遇到浓盐酸产生白烟,说明二者发生反应生成白色固体氯
3
化铵,D项正确。
4.(2019·临沂高三统考)下列制取NH 并验证其还原性、收集并进行尾气处理的装置和
3
原理均正确的是( )解析:选B。氯化铵受热分解生成氨和氯化氢,但在试管口又重新化合生成氯化铵,得不
到氨,A项错误;氨具有还原性,氯气具有强氧化性,二者能发生氧化还原反应,又因为氨密
度小于空气,氯气密度大于空气,所以长口通入NH ,短口通入Cl,可以使其充分反应,装置
3 2
和原理均正确,B项正确;氨密度小于空气,收集时应该是短口进、长口出,C项错误;氨极易
溶于水,倒置的漏斗插入水中,不能防倒吸,D项错误。
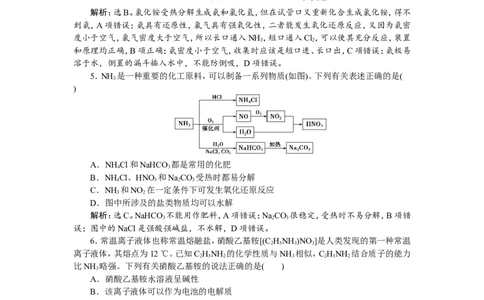
5.NH 是一种重要的化工原料,可以制备一系列物质(如图)。下列有关表述正确的是(
3
)
A.NH Cl和NaHCO 都是常用的化肥
4 3
B.NH Cl、HNO 和NaCO 受热时都易分解
4 3 2 3
C.NH 和NO 在一定条件下可发生氧化还原反应
3 2
D.图中所涉及的盐类物质均可以水解
解析:选C。NaHCO 不能用作肥料,A项错误;NaCO 很稳定,受热时不易分解,B项错
3 2 3
误;图中的NaCl是强酸强碱盐,不水解,D项错误。
6.常温离子液体也称常温熔融盐,硝酸乙基铵[(C HNH )NO ]是人类发现的第一种常温
2 5 3 3
离子液体,其熔点为12 ℃。已知C HNH 的化学性质与NH 相似,C HNH 结合质子的能力
2 5 2 3 2 5 2
比NH 略强。下列有关硝酸乙基铵的说法正确的是( )
3
A.硝酸乙基铵水溶液呈碱性
B.该离子液体可以作为电池的电解质
C.(C HNH )NO 能与氢氧化钠反应产生NH
2 5 3 3 3
D.相同温度下,相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液相比,前者的pH小
解析:选B。A项,硝酸乙基铵是强酸弱碱盐,水解显酸性;B项,(C HNH )NO 为离子液
2 5 3 3
体,能导电;C项,C HNH 的化学性质与NH 相似,(C HNH )NO 能与NaOH反应生成
2 5 2 3 2 5 3 3
C HNH ;D项,C HNH 结合质子的能力比NH 略强,说明相同物质的量浓度的C HNH 的
2 5 2 2 5 2 3 2 5 2
水溶液的碱性比氨水的强,因而相同物质的量浓度的硝酸乙基铵溶液的水解程度比硝酸铵
溶液小,则相同温度下,相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液相比,前者的pH
大。
7.将充有40 mL NO 和NO混合气体的试管倒置于盛水的水槽中,充分反应后试管中剩
2
下20 mL气体,则原混合气体中NO 和NO的体积比为( )
2A.2∶1 B.1∶3
C.3∶1 D.1∶1
解析:选C。3NO +HO===2HNO +NO ΔV
2 2 3
3 1 2
30 mL 20 mL
V(NO)=40 mL-30 mL=10 mL, V(NO )∶V(NO)=30 mL∶10 mL=3∶1。
2
8.(2019·青岛一中第一次月考)将11.2 g的Mg、Cu混合物完全溶解于足量的硝酸中,收
集反应产生的X气体。再向所得溶液中加入足量的NaOH溶液,产生21.4 g沉淀。根据题意
推断气体X的成分可能是( )
A.0.6 mol NO
B.0.1 mol NO、0.2 mol NO 和0.05 mol NO
2 2 4
C.0.2 mol NO 和0.1 mol NO
2 2 4
D.0.3 mol NO 和0.3 mol NO
2
解析:选B。根据题意n(NO)=n(OH-)==0.6 mol,则金属离子为0.3 mol,转移电子的物
质的量为0.6 mol。若生成0.6 mol NO,氮元素得电子的物质的量为0.6 mol×(5-2)=1.8
mol,A错误;若生成0.1 mol NO、0.2 mol NO 和0.05 mol N O ,氮元素得电子数为0.1
2 2 4
mol×(5-2)+0.2 mol×(5-4)+0.05 mol×(5-4)×2=0.6 mol,B正确;若生成0.2 mol NO
2
和0.1 mol NO,氮元素得电子的物质的量为(0.2+0.1×2) mol×(5-4)=0.4 mol,C错误;若
2 4
生成0.3 mol NO 和0.3 mol NO,氮元素得电子的物质的量为0.3 mol×(5-4)+0.3 mol×(5
2
-2)=1.2 mol,D错误。
9.(2019·南昌高三一模)某稀溶液中含4 mol KNO 和2.5 mol HSO ,向其中加入1.5 mol
3 2 4
铁,充分反应后产生的NO气体在标准状况下的体积为( )
A.36 L B.28 L
C.22.4 L D.11.2 L
解析:选B。题中发生反应的离子方程式为Fe+NO+4H+===NO↑+Fe3++2HO、2Fe3+
2
+Fe===3Fe2+,n(NO)=4 mol,n(H+)=5 mol,n(Fe)=1.5 mol,由此可知NO和Fe过量,以H+
的物质的量为基准进行计算,可得产生的NO的物质的量为1.25 mol,标准状况下的体积为
28 L。
10.铜和铁的合金7.2 g完全溶于稀硝酸,若反应中硝酸被还原只产生NO气体,在反应
后的溶液中加入足量的氢氧化钠溶液,最终生成12.3 g沉淀。则在标准状况下产生的NO气
体的体积为( )
A.1.12 L B.2.24 L
C.3.36 L D.1.68 L
解析:选B。两种金属单质最终生成氢氧化物时增加的质量实际上是OH-的质量,OH-
的物质的量与金属跟硝酸反应时失去的电子的物质的量相等,n(e-)=n(OH-)=(12.3 g-7.2
g)÷17 g/mol=0.3 mol,根据HNO――→NO,可知n(NO)=0.1 mol,故在标准状况下产生的
3
NO气体的体积为2.24 L。
二、非选择题
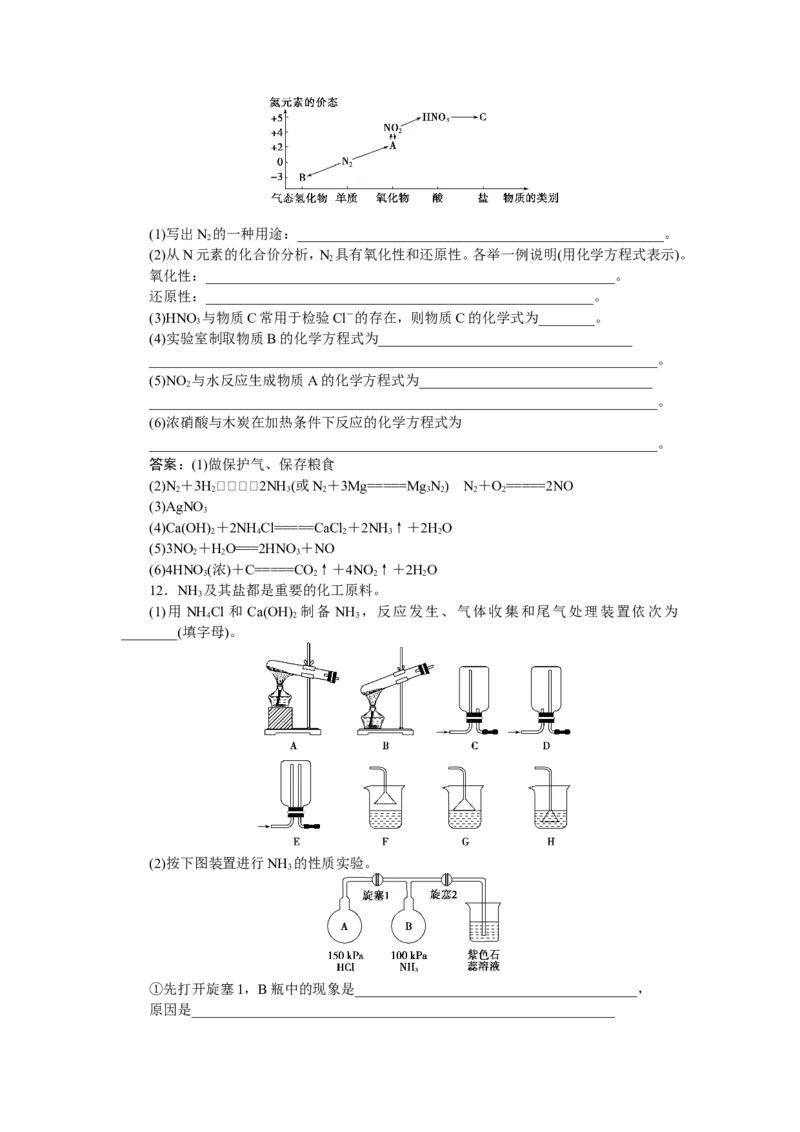
11.(教材改编题)如图是氮元素的几种价态与物质类别的对应关系,回答下列问题:(1)写出N 的一种用途:____________________________________________________。
2
(2)从N元素的化合价分析,N 具有氧化性和还原性。各举一例说明(用化学方程式表示)。
2
氧化性:__________________________________________________________。
还原性:_______________________________________________________。
(3)HNO 与物质C常用于检验Cl-的存在,则物质C的化学式为________。
3
(4)实验室制取物质B的化学方程式为____________________________________
________________________________________________________________________。
(5)NO 与水反应生成物质A的化学方程式为_________________________________
2
________________________________________________________________________。
(6)浓硝酸与木炭在加热条件下反应的化学方程式为
________________________________________________________________________。
答案:(1)做保护气、保存粮食
(2)N +3H2NH (或N+3Mg=====MgN) N+O=====2NO
2 2 3 2 3 2 2 2
(3)AgNO
3
(4)Ca(OH) +2NH Cl=====CaCl +2NH ↑+2HO
2 4 2 3 2
(5)3NO +HO===2HNO +NO
2 2 3
(6)4HNO(浓)+C=====CO↑+4NO ↑+2HO
3 2 2 2
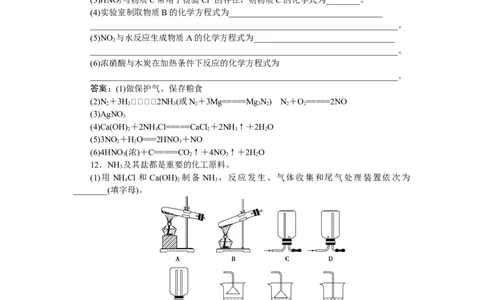
12.NH 及其盐都是重要的化工原料。
3
(1)用 NH Cl 和 Ca(OH) 制备 NH ,反应发生、气体收集和尾气处理装置依次为
4 2 3
________(填字母)。
(2)按下图装置进行NH 的性质实验。
3
①先打开旋塞1,B瓶中的现象是________________________________________,
原因是____________________________________________________________________________________________________________________________________。
稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是___________________________________________
________________________________________________________________________。
解析:(1)固固加热制备气体,应选用A为发生装置;NH 密度比空气小,应选用C收集气
3
体;NH 极易溶于水,为防止倒吸,应选用G进行尾气处理。
3
(2)①A瓶中压强比B瓶中压强大,打开旋塞1,HCl气体进入B瓶并与NH 反应生成
3
NH Cl,B瓶中产生白烟。②反应后B瓶中压强减小,关闭旋塞1,打开旋塞2,烧杯中的紫色
4
石蕊溶液倒吸入B瓶,因为B瓶中得到的溶液显酸性,所以溶液变红色。
答案:(1)A、C、G
(2)①有白烟出现 因A瓶中HCl气体压强大,所以HCl进入B瓶,与NH 发生反应,生
3
成白色NH Cl固体颗粒 ②紫色石蕊溶液进入B瓶,溶液变红色
4
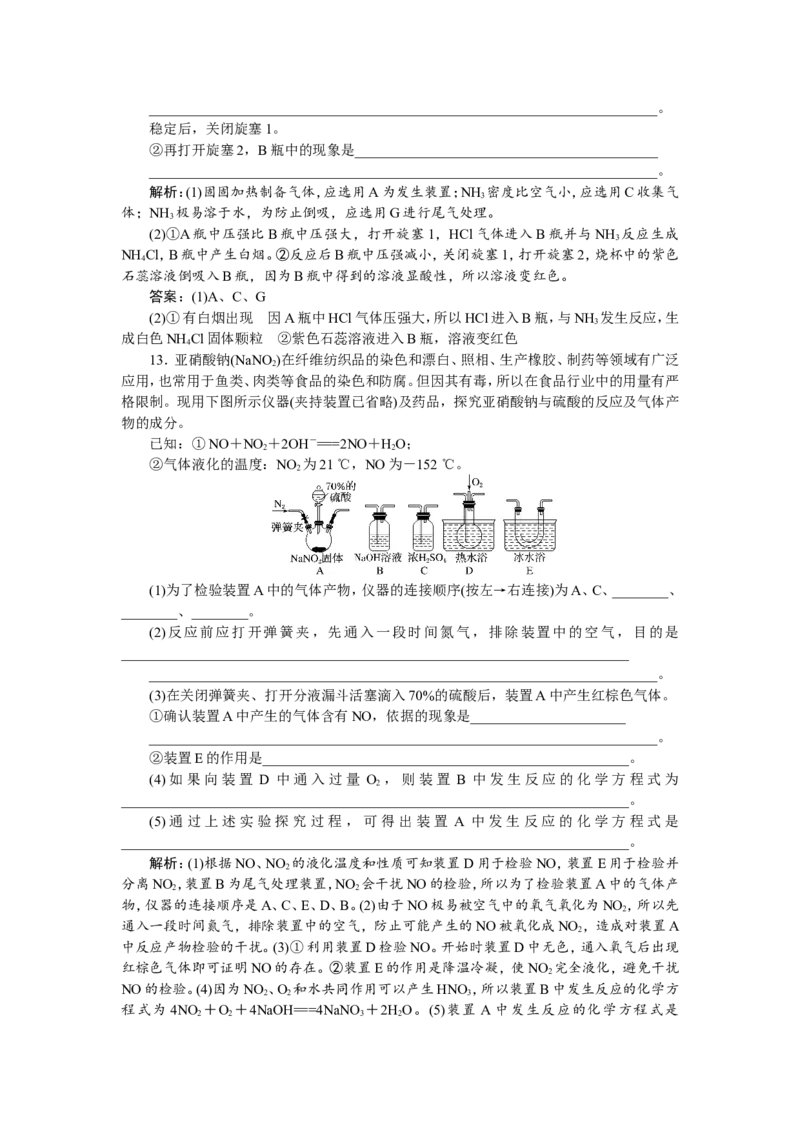
13.亚硝酸钠(NaNO )在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛
2
应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业中的用量有严
格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸的反应及气体产
物的成分。
已知:①NO+NO +2OH-===2NO+HO;
2 2
②气体液化的温度:NO 为21 ℃,NO为-152 ℃。
2
(1)为了检验装置A中的气体产物,仪器的连接顺序(按左→右连接)为A、C、________、
________、________。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是
________________________________________________________________________
________________________________________________________________________。
(3)在关闭弹簧夹、打开分液漏斗活塞滴入70%的硫酸后,装置A中产生红棕色气体。
①确认装置A中产生的气体含有NO,依据的现象是______________________
________________________________________________________________________。
②装置E的作用是____________________________________________________。
(4)如果向装置 D 中通入过量 O ,则装置 B 中发生反应的化学方程式为
2
________________________________________________________________________。
(5)通过上述实验探究过程,可得出装置 A 中发生反应的化学方程式是
________________________________________________________________________。
解析:(1)根据NO、NO 的液化温度和性质可知装置D用于检验NO,装置E用于检验并
2
分离NO ,装置B为尾气处理装置,NO 会干扰NO的检验,所以为了检验装置A中的气体产
2 2
物,仪器的连接顺序是A、C、E、D、B。(2)由于NO极易被空气中的氧气氧化为NO ,所以先
2
通入一段时间氮气,排除装置中的空气,防止可能产生的NO被氧化成NO ,造成对装置A
2
中反应产物检验的干扰。(3)①利用装置D检验NO。开始时装置D中无色,通入氧气后出现
红棕色气体即可证明NO的存在。②装置E的作用是降温冷凝,使NO 完全液化,避免干扰
2
NO的检验。(4)因为NO 、O 和水共同作用可以产生HNO,所以装置B中发生反应的化学方
2 2 3
程式为 4NO +O +4NaOH===4NaNO +2HO。(5)装置 A 中发生反应的化学方程式是
2 2 3 22NaNO +HSO ===Na SO +NO ↑+NO↑+HO。
2 2 4 2 4 2 2
答案:(1)E D B
(2)防止可能产生的NO被氧化成NO ,造成对A中反应产物检验的干扰
2
(3)①装置D中通入氧气后出现红棕色气体 ②冷凝,使NO 完全液化
2
(4)4NO +O+4NaOH===4NaNO +2HO
2 2 3 2
(5)2NaNO +HSO ===Na SO +NO ↑+NO↑+HO
2 2 4 2 4 2 2