文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练12 14道选择题+主观有机题
完卷时间:40分钟
答案速查
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C D D B B A B A C D B D D A
可能用到的相对原子质量:H-1 O-16 Na-23 S-32 Cl-35.5 Fe-56
一、选择题(共42分,只有1个正确选项)
1.我国早在“十二五”期间就增加了“脱硝”这一节能减排约束性硬指标。“脱硝”中的
“硝”是指
A. B. C. D.
【答案】C
【解析】脱硝是指将尾气中的氮氧化物转化为氮气和水蒸气的过程,故“硝”是指氮氧化
物,故选C。
2.已知NaBiO 制MnO 的离子方程式为5NaBiO+2Mn2++14H+=2MnO +5Na++5Bi3++7HO,下列
3 3 2
说法错误的是
A.上述反应需要在硫酸酸化的环境中进行
B.HO的VSEPR模型为:
2
C.基态Bi3+的价电子排布式为6s2
D.用浓盐酸溶解NaBiO 的离子方程式为BiO +2Cl-+6H+=Cl↑+Bi3++3HO
3 2 2
【答案】D
【解析】A.上述反应需要消耗 ,即需要在强酸性环境下进行,由于硝酸有强氧化性,
盐酸中 还原性比 强,均会影响该反应的发生,因此最适宜用硫酸酸化,A正确;
B.HO的中心原子O的价层电子对数为 ,O原子的杂化类型为 ,因此
2HO的VSEPR模型为四面体形,B正确;C.Bi位于第六周期第ⅤA族,基态 的价层电
2
子排布式为 ,C正确;D.用浓盐酸溶解NaBiO 固体时, 与 发生氧化还原反
3
应,生成 和 ,反应的离子方程式为: ,
D错误;故选D。
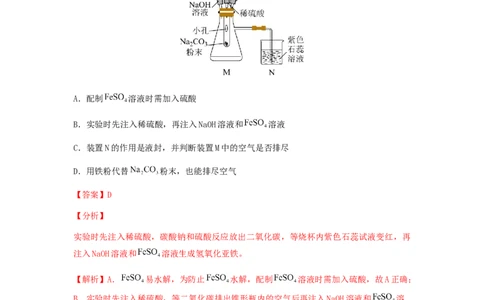
3.一种制备 的改进装置如图所示,下列说法错误的是
A.配制 溶液时需加入硫酸
B.实验时先注入稀硫酸,再注入NaOH溶液和 溶液
C.装置N的作用是液封,并判断装置M中的空气是否排尽
D.用铁粉代替 粉末,也能排尽空气
【答案】D
【分析】
实验时先注入稀硫酸,碳酸钠和硫酸反应放出二氧化碳,等烧杯内紫色石蕊试液变红,再
注入NaOH溶液和 溶液生成氢氧化亚铁。
【解析】A. 易水解,为防止 水解,配制 溶液时需加入硫酸,故A正确;
B.实验时先注入稀硫酸,等二氧化碳排出锥形瓶内的空气后再注入NaOH溶液和 溶
液生成氢氧化亚铁,故B正确;C.烧杯内紫色石蕊试液变红,说明锥形瓶内空气完全排出,
同时装置N可以防止空气进入锥形瓶,故C正确;D.氢气的密度比空气小,用铁粉代替
粉末,不能排尽空气,故D错误;选D。
4.科研人员开发了一种生产药物中间体三氟甲苯的方法:设 为阿伏加德罗常数的值,已知三氟乙酸的pKa=0.23,下列叙述正确的是
A.1mol三氟甲苯中碳碳双键数目为3
B.氢气和二氧化碳组成的混合物共1mol ,其中氢、氧原子总数为2
C.生成22.4L 时,需消耗1mol苯
D.1L 1 三氟乙酸溶液中, 的数目为
【答案】B
【解析】A.1个三氟甲苯分子中,苯环上的碳碳键是介于单键和双键之间一种特殊共价键,
分子中不存在碳碳双键,碳碳双键数目为0 N,A错误;B.氢气为双原子分子,二氧化碳
A
的分子组成为CO,含有2个氧原子,1mol 和 组成的混合物中不管比例如何,氢、
2
氧原子总数都是2N,B正确;C.生成22.4L 时,未明确气体所处状况,无法计算需消
A
耗苯的量,C错误;D.由三氟乙酸的pKa=0.23可知,三氟乙酸为弱酸,1L 1 三氟
乙酸溶液中, 的数目小于N,D错误;故选B。
A
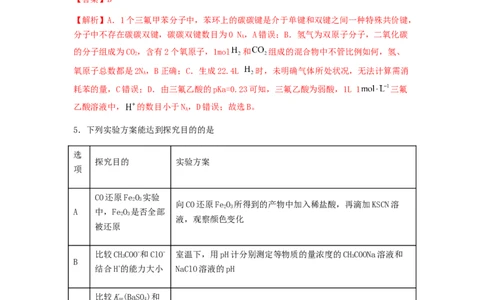
5.下列实验方案能达到探究目的的是
选
探究目的 实验方案
项
CO还原FeO 实验
2 3
向CO还原FeO 所得到的产物中加入稀盐酸,再滴加KSCN溶
2 3
A 中,FeO 是否全部
2 3
液,观察颜色变化
被还原
比较CHCOO-和ClO- 室温下,用pH计分别测定等物质的量浓度的CHCOONa溶液和
3 3
B
结合H+的能力大小 NaClO溶液的pH
比较K(BaSO)和
sp 4
将BaSO 粉末和NaCO 饱和溶液混合,充分振荡,静置,取少量
4 2 3
C K (BaCO)的相对
sp 3
上层清液,滴加盐酸和BaCl 溶液,观察是否有沉淀产生
2
大小
检验某有机物是否 取少许该有机物滴入盛有银氨溶液的试管中水浴加热,观察试
D
为醛类 管中是否有银镜产生
A.A B.B C.C D.D
【答案】B【解析】A.向CO还原FeO 所得到的产物中加入稀盐酸,再滴加KSCN溶液,如果溶液变
2 3
为血红色,表明FeO 没有全部被还原,如果溶液不变色,并不能说明FeO 全部被还原,
2 3 2 3
因为生成的Fe能将Fe3+还原为Fe2+,故A错误;B.室温下,用pH计分别测定等物质的量
浓度的CHCOONa溶液和NaClO溶液的pH,后者的pH大,表明后者溶液中c(OH-)大,溶液
3
的碱性强,ClO-的水解程度比CHCOO-大,从而说明ClO-结合H+的能力比CHCOO-强,故B正
3 3
确;C.将BaSO4粉末和NaCO 饱和溶液混合,充分振荡,静置,取少量上层清液,滴加盐
2 3
酸和BaCl 溶液,虽然有气泡和沉淀产生,但并不能说明K(BaSO)比K (BaCO)大,因为
2 sp 4 sp 3
使用的是NaCO 饱和溶液,故C错误;D.能发生银镜反应的物质不一定是醛类物质,只要
2 3
含有醛基即可,比如葡萄糖、甲酸、甲酸甲酯等,故D错误;故选B。
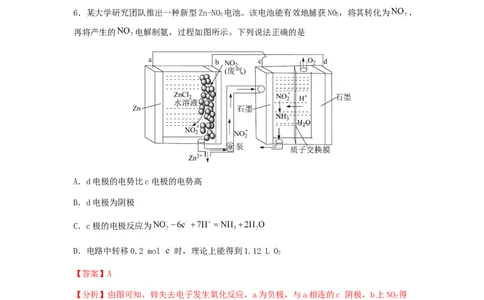
6.某大学研究团队推出一种新型Zn-NO 电池。该电池能有效地捕获NO,将其转化为 ,
2 2
再将产生的 电解制氨,过程如图所示。下列说法正确的是
A.d电极的电势比c电极的电势高
B.d电极为阴极
C.c极的电极反应为
D.电路中转移0.2 mol 时,理论上能得到1.12 L O
2
【答案】A
【分析】由图可知,锌失去电子发生氧化反应,a为负极,与a相连的c 阴极,b上NO 得
2
到电子,变为 ,b为正极,与b相连的d为阳极。
【解析】A.c 为阴极,d为阳极,d电极的电势比c电极的电势高,故A正确;B.由上述
分析可知,d为阳极,故B错误;C.c极为阴极, 得到电子转化为NH,电极反应为:
3
+6e−+7H+=NH+2HO,故C错误;D.d为阳极,电极反应式为:2HO−4e−=
3 2 2
O↑+4H+,电路中转移0.2mole-时,理论上能得到0.05molO,标况下的体积为
2 2
0.05mol×22.4mol/L=1.12L,D选项中并未说明是标况,此时无法得知O 的体积,故D错
2
误。答案选A。
7.日光灯中用到的某种荧光粉的主要成分为 。已知:X、Y、Z和W为原子
序数依次增大的前20号元素,W为金属元素,基态X原子s轨道上的电子数和p轨道上的
电子数相等,基态X、Y、Z原子的未成对电子数之比为2∶1∶3,下列说法正确的是
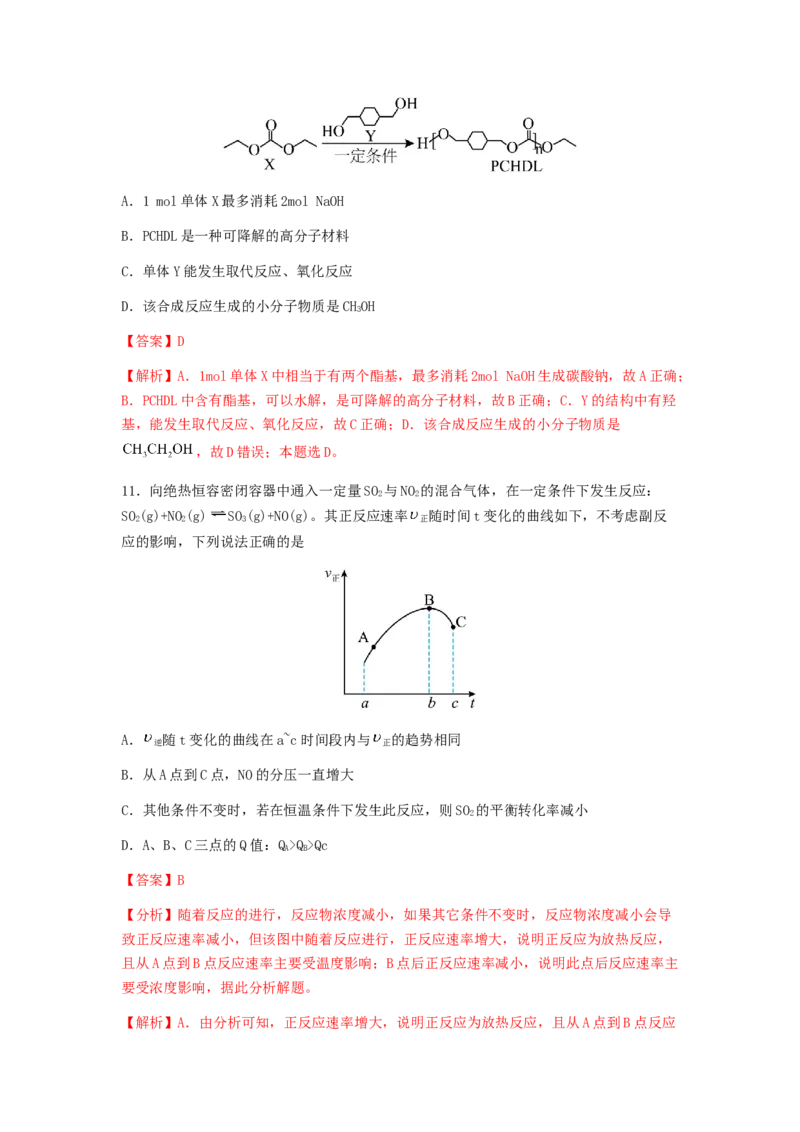
A.电负性:YQ>Qc
A B
【答案】B
【分析】随着反应的进行,反应物浓度减小,如果其它条件不变时,反应物浓度减小会导
致正反应速率减小,但该图中随着反应进行,正反应速率增大,说明正反应为放热反应,
且从A点到B点反应速率主要受温度影响;B点后正反应速率减小,说明此点后反应速率主
要受浓度影响,据此分析解题。
【解析】A.由分析可知,正反应速率增大,说明正反应为放热反应,且从A点到B点反应速率主要受温度影响;B点后正反应速率减小,说明此点后反应速率主要受浓度影响;而A
到C点过程中生成物浓度一直在增大,即逆反应速率一直在增大,则 随t变化的曲线在
逆
a~c时间段内与 的趋势不相同,A错误;B.由分析可知,正反应速率增大,说明正反应
正
为放热反应,而反应前后气体的总物质的量保持不变,从A点到C点,容器的压强由于温
度上升而增大,NO的物质的量也一直在增多,故NO的分压一直增大,B正确;C.由分析
可知,正反应速率增大,说明正反应为放热反应,其他条件不变时,若在恒温条件下发生
此反应,相当于降低温度,则上述反应化学平衡将向正向移动,则SO 的平衡转化率增大,
2
C错误;D.由分析可知,由A到C过程中反应一直在向正向进行,即SO、NO浓度在增大,
3
而SO、NO 的浓度在减小,故Q= ,A、B、C三点的Q值:Q<Q<Qc,D错误;
2 2 A B
故答案为:B。
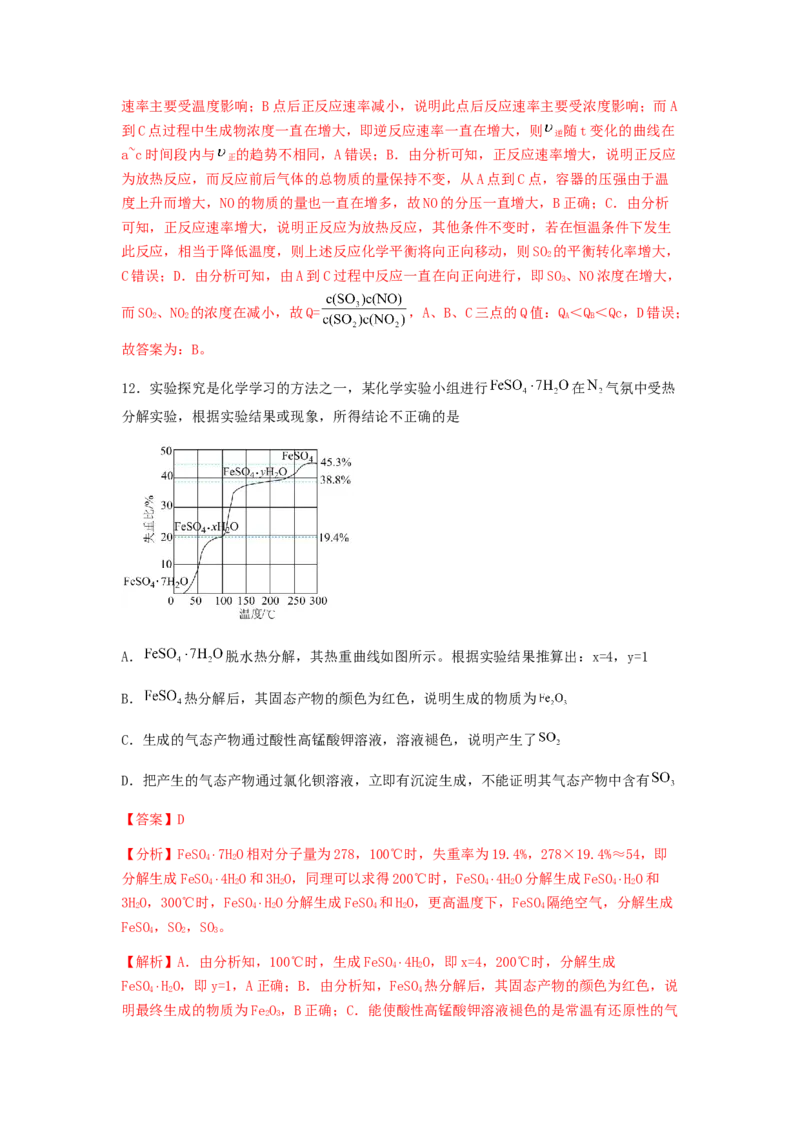
12.实验探究是化学学习的方法之一,某化学实验小组进行 在 气氛中受热
分解实验,根据实验结果或现象,所得结论不正确的是
A. 脱水热分解,其热重曲线如图所示。根据实验结果推算出:x=4,y=1
B. 热分解后,其固态产物的颜色为红色,说明生成的物质为
C.生成的气态产物通过酸性高锰酸钾溶液,溶液褪色,说明产生了
D.把产生的气态产物通过氯化钡溶液,立即有沉淀生成,不能证明其气态产物中含有
【答案】D
【分析】FeSO 4⋅7H
2
O相对分子量为278,100℃时,失重率为19.4%,278×19.4%≈54,即
分解生成FeSO 4⋅4H
2
O和3H
2
O,同理可以求得200℃时,FeSO 4⋅4H
2
O分解生成FeSO 4⋅H
2
O和
3H
2
O,300℃时,FeSO 4⋅H
2
O分解生成FeSO
4
和H
2
O,更高温度下,FeSO
4
隔绝空气,分解生成
FeSO,SO,SO。
4 2 3
【解析】A.由分析知,100℃时,生成FeSO 4⋅4H
2
O,即x=4,200℃时,分解生成
FeSO 4⋅H
2
O,即y=1,A正确;B.由分析知,FeSO
4
热分解后,其固态产物的颜色为红色,说
明最终生成的物质为FeO,B正确;C.能使酸性高锰酸钾溶液褪色的是常温有还原性的气
2 3体,反应中可能生成的有还原性的气体只有SO,故生成的气态产物通过酸性高锰酸钾溶液,
2
溶液褪色,说明产生了SO,C正确;D.把产生的气态产物通过氯化钡溶液,立即有沉淀
2
生成,因为SO 无法和氯化钡溶液反应得到硫酸钡沉淀,故可以说明其气态产物中含有
2
SO,故D错误;本题选D。
3
13.近年来有多个关于超高压下新型晶体的形成与结构的研究报道。 晶体在
的高压下和 反应,可以形成一种新型晶体,其立方晶胞如图所示(大球为
,小球为 ),下列叙述不正确的是
A.晶胞中,原子分数坐标 为(0,0,0),B为( ,0, ),则C的原子分数坐标为(0,
, )
B.晶胞中, 构成的多面体包含20个三角形的面
C.晶胞中,与 最近且等距的 有12个
D.已知晶胞参数为 ,阿伏加德罗常数的值为 ,则该晶体的密度 ×1030g/cm3
【答案】D
【解析】A.由晶胞结构可知,晶胞中位于顶点的A和位于体对角线上的B的原子分数坐标
分别为(0,0,0)、( ,0, ),则晶胞的边长为1,位于面上的C的原子分数坐标为
(0, , ),故A正确;B.由晶胞结构可知,晶胞中氯原子构成的多面体共有12个顶点,
每个顶点为5个三角形所共有,则每个三角形平均占有的顶点石墨为3× ,所以多面体包
含三角形的面的数目为 =20,故B正确;C.由晶胞结构可知,晶胞中位于顶点的钠原
子与位于面对角线上的氯原子距离最近,则晶胞中与钠原子距离最近的氯原子个数为12,
故C正确;D.由晶胞结构可知,晶胞中位于顶点和体心的钠原子个数为8× +1=2,位于面上的氯原子个数为12× =6,则晶胞的化学式为NaCl,设晶体的密度为dg/cm3,由晶
3
胞的质量公式可得: =(10—10a)3d,解得d= ×1030g/cm3,故D错误;故选D。
14.常温下,向某浓度的HA溶液中加入NaOH固体,保持溶液的体积和温度不变,测得pH
与 、 、 的变化关系如图所示。下列说法不正确的是
A.常温下, 的电离平衡常数 为
B.a点时,
C.a点→b点过程中,水的电离程度增大
D.NaHA溶液中
【答案】A
【分析】向某浓度HA溶液中加入NaOH(s),则HA不断减少,A2-不断增加, 且
2 2
比值减少,则-lgc(HA)减少、-lgc(A2-)增大、 减少且可以减少到0,故上升
2
的曲线是 -lgc(A2-),下降且与横坐标相交的是 ,另一条下降的曲线是-
lgc(HA)。
2【解析】A.当pH为5.3时, =0,此时,c(HA-)=c(A2-);当pH等于3.05
时,-lgc(HA)等于-lgc(A2-),即c(HA)=c(A2-);又因为K = ,K =
2 2 a1 a2
则K K = ,则K =10-0.8,A错误;B.a点时,电荷守恒
a1 a2 a1
为c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),pH=3.05,则c(H+)=10-3.05mol/L,c(OH-)=10-
10.95 mol/L,又因为c(A2-)= c(HA),所以c(Na+)+10-3.05-10-10.95=2c(A2-)+c(HA-),故
2
,B正确;C.a点→b点过程中,c(HA)逐渐减小,HA
2 2
的电离抑制水的电离,则该过程中水的电离程度增大,C正确;D.在NaHA溶液,由于HA-
即存在电离又存在水解,所以c(Na+)>c(HA-);因为K =10-6.1,水解常数K=
a2 b
,故水解程度小于电离程度,即c(HA)