文档内容
第八篇 化学实验
专项 57 滴定实验操作与计算
酸碱中和滴定是高中选择性必修《化学反应原理》中一个重要的定量实验,既可以考查学生实验操作
的技能,也可以考查学生数据分析处理的能力,酸碱中和滴定实验是发展学生化学学科核心素养的一个良
好载体。中和滴定的拓展应用是近几年高考试题的创新题型,主要类型有沉淀滴定和氧化还原滴定。考查
角度主要有:①滴定管的使用问题、②滴定指示剂的选择、③滴定终点的现象判断、④定量计算问题、⑤
滴定误差分析。
1.(2022•山东卷)实验室用基准NaCO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐
2 3
酸滴定NaCO 标准溶液。下列说法错误的是( )
2 3
A.可用量筒量取25.00 mL Na CO 标准溶液置于锥形瓶中
2 3
B.应选用配带塑料塞的容量瓶配制NaCO 标准溶液
2 3
C.应选用烧杯而非称量纸称量NaCO 固体
2 3
D.达到滴定终点时溶液显橙色
【答案】A
【解析】根据中和滴定过程批示剂选择原则,以盐酸滴定NaCO 标准溶液,选甲基橙为指示剂,则
2 3
应利用盐酸滴定碳酸钠,即将NaCO 标准溶液置于锥形瓶中,将待测盐酸置于酸式滴定管中,滴定终点时
2 3
溶液由黄色变为橙色。A项,量筒的精确度为0.1 mL,不可用量简量取NaCO 标准溶液,应该用碱式滴定
2 3
管或移液管量取25.00 mL Na CO 标准溶液置于锥形瓶中,A错误;B项,NaCO 溶液显碱性,盛放
2 3 2 3
NaCO 溶液的容器不能用玻璃塞,以防碱性溶液腐蚀玻璃产生有粘性的硅酸钠溶液而将瓶塞粘住,故应选
2 3
用配带塑料塞的容量瓶配制NaCO 标准溶液,B正确;C项,NaCO 有吸水性且有一定的腐蚀性,故应选
2 3 2 3
用烧杯而非称量纸称量NaCO 固体,C正确;D项,NaCO 溶液显碱性,甲基橙滴入NaCO 溶液中显黄
2 3 2 3 2 3
色,当滴入最后一滴盐酸时,溶液由黄色突变为橙色且半分钟之内不变色即为滴定终点,故达到滴定终点
时溶液显橙色,D正确;故选A。
2.(2022•广东选择性考试)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电离平衡密切相关。25℃时,HAc的K=1.75×105=10-4.76。
a
(1)配制 的HAc溶液,需 溶液的体积为_______mL。
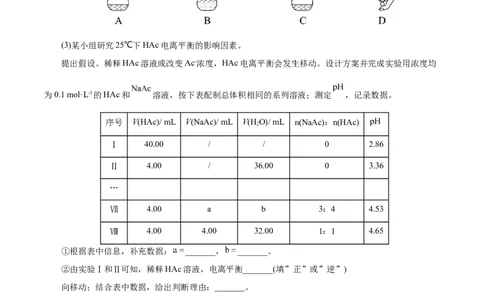
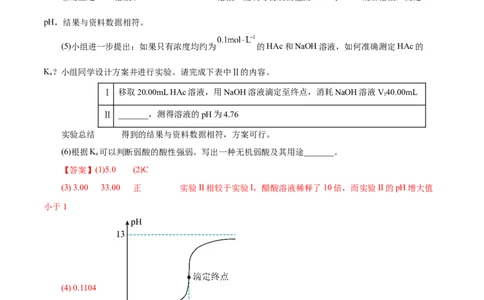
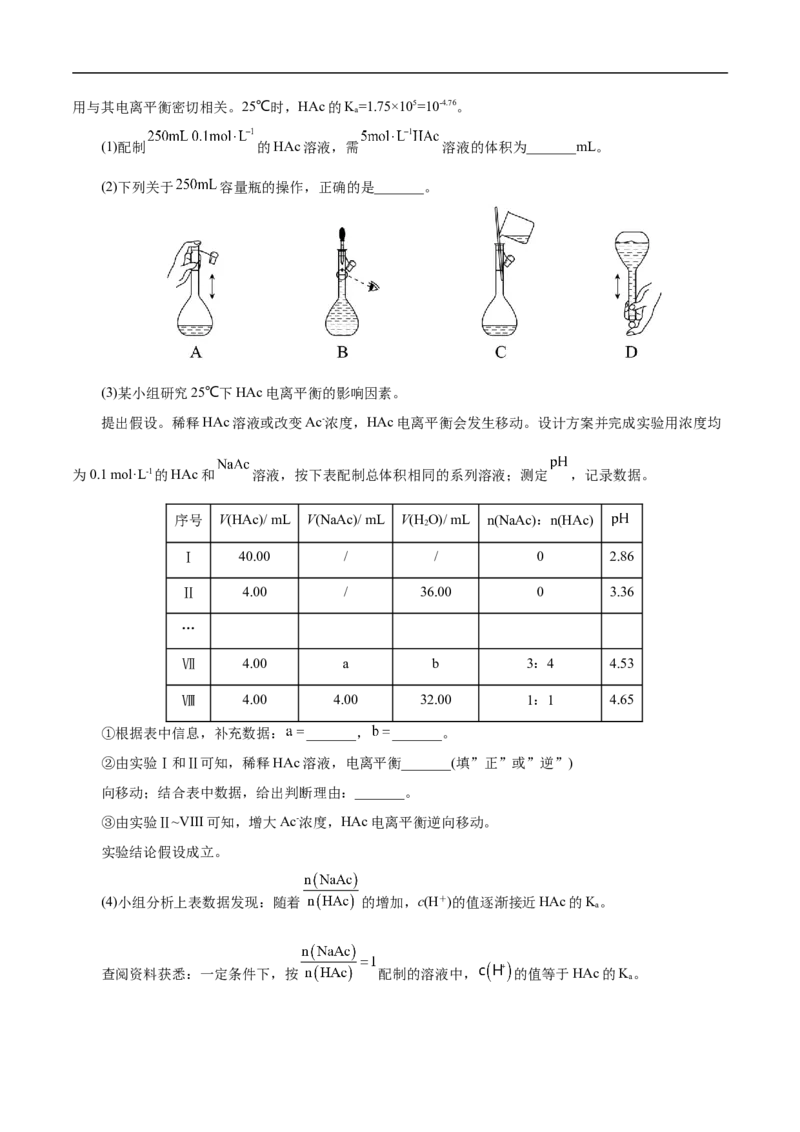
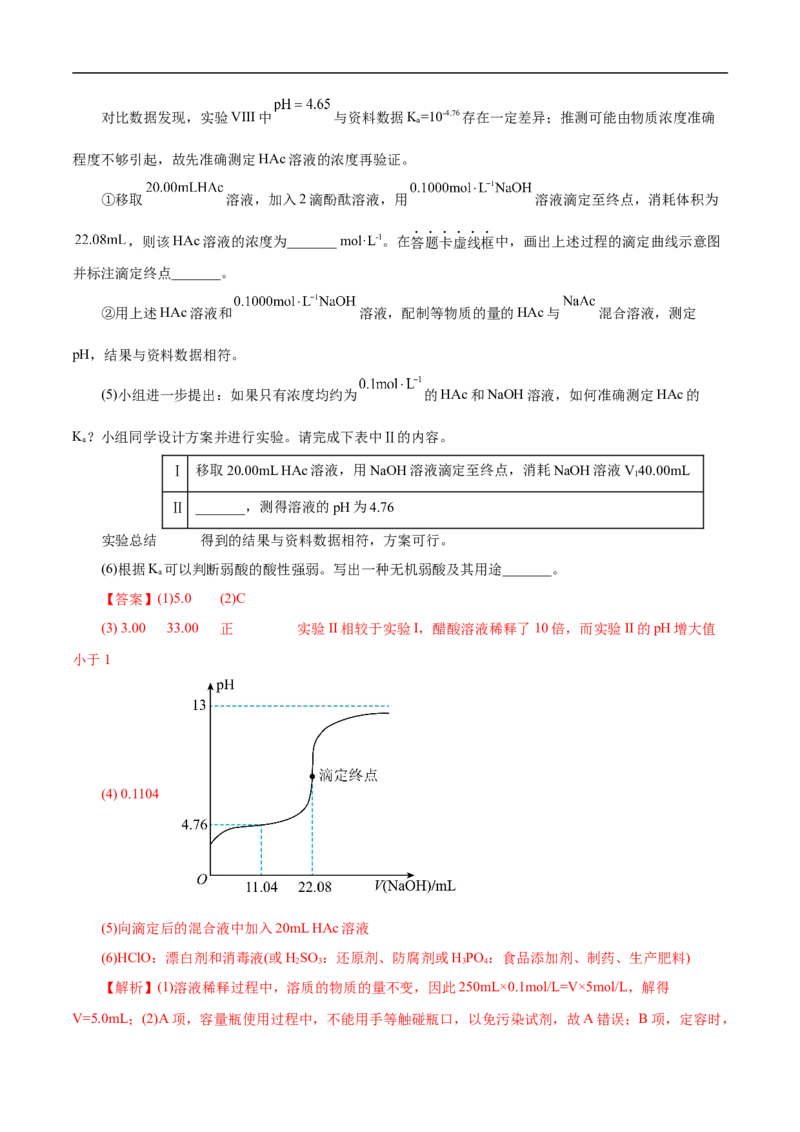
(2)下列关于 容量瓶的操作,正确的是_______。
(3)某小组研究25℃下HAc电离平衡的影响因素。
提出假设。稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。设计方案并完成实验用浓度均
为0.1 mol·L-1的HAc和 溶液,按下表配制总体积相同的系列溶液;测定 ,记录数据。
序号 V(HAc)/ mL V(NaAc)/ mL V(H O)/ mL n(NaAc):n(HAc)
2
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
…
Ⅶ 4.00 a b 3:4 4.53
Ⅷ 4.00 4.00 32.00 1:1 4.65
①根据表中信息,补充数据: _______, _______。
②由实验Ⅰ和Ⅱ可知,稀释HAc溶液,电离平衡_______(填”正”或”逆”)
向移动;结合表中数据,给出判断理由:_______。
③由实验Ⅱ~VIII可知,增大Ac-浓度,HAc电离平衡逆向移动。
实验结论假设成立。
(4)小组分析上表数据发现:随着 的增加,c(H+)的值逐渐接近HAc的K。
a
查阅资料获悉:一定条件下,按 配制的溶液中, 的值等于HAc的K。
a对比数据发现,实验VIII中 与资料数据K=10-4.76存在一定差异;推测可能由物质浓度准确
a
程度不够引起,故先准确测定HAc溶液的浓度再验证。
①移取 溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为
,则该HAc溶液的浓度为_______ mol·L-1。在答题卡虚线框中,画出上述过程的滴定曲线示意图
并标注滴定终点_______。
②用上述HAc溶液和 溶液,配制等物质的量的HAc与 混合溶液,测定
pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为 的HAc和NaOH溶液,如何准确测定HAc的
K?小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
a
Ⅰ 移取20.00mL HAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液V40.00mL
1
Ⅱ _______,测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。
(6)根据K 可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途_______。
a
【答案】(1)5.0 (2)C
(3) 3.00 33.00 正 实验II相较于实验I,醋酸溶液稀释了10倍,而实验II的pH增大值
小于1
(4) 0.1104
(5)向滴定后的混合液中加入20mL HAc溶液
(6)HClO:漂白剂和消毒液(或HSO :还原剂、防腐剂或HPO :食品添加剂、制药、生产肥料)
2 3 3 4
【解析】(1)溶液稀释过程中,溶质的物质的量不变,因此250mL×0.1mol/L=V×5mol/L,解得
V=5.0mL;(2)A项,容量瓶使用过程中,不能用手等触碰瓶口,以免污染试剂,故A错误;B项,定容时,视线应与溶液凹液面和刻度线“三线相切”,不能仰视或俯视,故B错误;C项,向容量瓶中转移液体,
需用玻璃棒引流,玻璃棒下端位于刻度线以下,同时玻璃棒不能接触容量瓶口,故C正确;D项,定容完
成后,盖上瓶塞,将容量瓶来回颠倒,将溶液摇匀,颠倒过程中,左手食指抵住瓶塞,防止瓶塞脱落,右
手扶住容量瓶底部,防止容量瓶从左手掉落,故D错误;综上所述,正确的是C项。(3)①实验VII的溶液
中n(NaAc):n(HAc)=3:4,V(HAc)=4.00mL,因此V(NaAc)=3.00mL,即a=3.00,,由实验I可知,溶液最
终的体积为40.00mL,因此V(H O)=40.00mL-4.00mL-3.00mL=33.00mL,即b=33.00;②实验I所得溶液的
2
pH=2.86,实验II的溶液中c(HAc)为实验I的 ,稀释过程中,若不考虑电离平衡移动,则实验II所得溶
液的pH=2.86+1=3.86,但实际溶液的pH=3.36<3.86,说明稀释过程中,溶液中n(H+)增大,即电离平衡正
向移动;(4)(i)滴定过程中发生反应:HAc+NaOH=NaAc+H O,由反应方程式可知,滴定至终点时,
2
n(HAc)=n(NaOH),因此22.08mL×0.1mol/L=20.00mL×c(HAc),解得c(HAc)=0.1104mol/L;(ii)滴定过程中,
当V(NaOH)=0时,c(H+)= ≈ mol/L=10-2.88mol/L,溶液的pH=2.88,当V(NaOH)=11.04mL时,
n(NaAc)=n(HAc),溶液的pH=4.76,当V(NaOH)=22.08mL时,达到滴定终点,溶液中溶质为NaAc溶液,
Ac-发生水解,溶液呈弱碱性,当NaOH溶液过量较多时,c(NaOH)无限接近0.1mol/L,溶液pH接近13,
因此滴定曲线如图: 。(5)向20.00mL的HAc溶液中加入
VmL NaOH溶液达到滴定终点,滴定终点的溶液中溶质为NaAc,当 时,溶液中c(H+)的值等
1于HAc的K ,因此可再向溶液中加入20.00mL HAc溶液,使溶液中n(NaAc)=n(HAc);(6)不同的无机弱酸
a
在生活中应用广泛,如HClO具有强氧化性,在生活中可用于漂白和消毒,HSO 具有还原性,可用作还
2 3
原剂,在葡萄酒中添加适量HSO 可用作防腐剂,HPO 具有中强酸性,可用作食品添加剂,同时在制药、
2 3 3 4
生产肥料等行业有广泛用途。
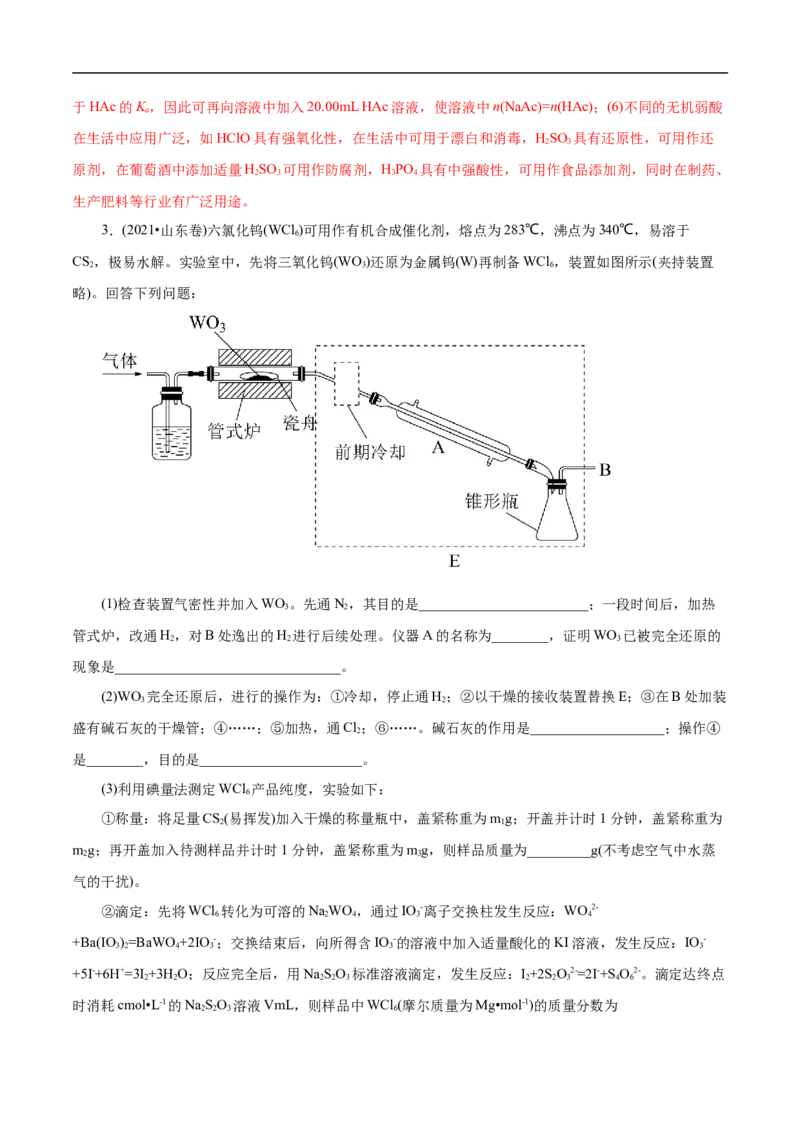
3.(2021•山东卷)六氯化钨(WCl )可用作有机合成催化剂,熔点为283℃,沸点为340℃,易溶于
6
CS,极易水解。实验室中,先将三氧化钨(WO)还原为金属钨(W)再制备WCl,装置如图所示(夹持装置
2 3 6
略)。回答下列问题:
(1)检查装置气密性并加入WO。先通N,其目的是________________________;一段时间后,加热
3 2
管式炉,改通H,对B处逸出的H 进行后续处理。仪器A的名称为________,证明WO 已被完全还原的
2 2 3
现象是________________________________。
(2)WO 完全还原后,进行的操作为:①冷却,停止通H;②以干燥的接收装置替换E;③在B处加装
3 2
盛有碱石灰的干燥管;④……;⑤加热,通Cl;⑥……。碱石灰的作用是___________________;操作④
2
是________,目的是_______________________。
(3)利用碘量法测定WCl 产品纯度,实验如下:
6
①称量:将足量CS(易挥发)加入干燥的称量瓶中,盖紧称重为mg;开盖并计时1分钟,盖紧称重为
2 1
mg;再开盖加入待测样品并计时1分钟,盖紧称重为mg,则样品质量为_________g(不考虑空气中水蒸
2 3
气的干扰)。
②滴定:先将WCl 转化为可溶的NaWO,通过IO -离子交换柱发生反应:WO2-
6 2 4 3 4
+Ba(IO )=BaWO +2IO -;交换结束后,向所得含IO -的溶液中加入适量酸化的KI溶液,发生反应:IO -
3 2 4 3 3 3
+5I-+6H+=3I +3H O;反应完全后,用NaSO 标准溶液滴定,发生反应:I+2S O2-=2I-+S O2-。滴定达终点
2 2 2 2 3 2 2 3 4 6
时消耗cmol•L-1的NaSO 溶液VmL,则样品中WCl(摩尔质量为Mg•mol-1)的质量分数为
2 2 3 6________________。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗NaSO 溶液的体
2 2 3
积将______ (填“偏大”“偏小”或“不变”),样品中WCl 质量分数的测定值将_____ (填“偏大”“偏
6
小”或“不变”)。
【答案】(1)排除装置中的空气 直形冷凝管 淡黄色固体变为银白色
(2)吸收多余氯气,防止污染空气;防止空气中的水蒸气进入E 再次通入N 排除装置中的H
2 2
(3)①( m +m- 2m ) ② % 不变 偏大
3 1 2
【解析】(1)用H 还原WO 制备W,装置中不能有空气,所以先通N,其目的是排除装置中的空气;
2 3 2
由仪器构造可知仪器A的名称为直形冷凝管;WO 为淡黄色固体,被还原后生成W为银白色,所以能证
3
明WO 已被完全还原的现象是淡黄色固体变为银白色;(2) 由信息可知WCl 极易水解,W与Cl 反应制取
3 6 2
WCl 时,要在B处加装盛有碱石灰的干燥管,防止空气中的水蒸气进入E中,所以碱石灰的作用其一是吸
6
收多余氯气,防止污染空气;其二是防止空气中的水蒸气进入E;在操作⑤加热,通Cl 之前,装置中有多
2
余的H,需要除去,所以操作④是再次通入N,目的是排除装置中的H;(3) ①根据分析,称量时加入足
2 2 2
量的CS,盖紧称重为mg,由于CS 易挥发,开盖时要挥发出来,称量的质量要减少,开盖并计时1分钟,
2 1 2
盖紧称重mg,则挥发出的CS 的质量为(m - m )g,再开盖加入待测样品并计时1分钟,又挥发出(m - m )g
2 2 1 2 1 2
的CS,盖紧称重为mg,则样品质量为:mg+2(m- m )g-m g=( m +m- 2m )g;②滴定时,根据关系式:
2 3 3 1 2 1 3 1 2
WO2-~2IO -~6I ~12 SO2-,样品中n(WCl )=n(WO 2-)= n(S O2-)= cV 10-3mol,m(WCl )= cV 10-
4 3 2 2 3 6 4 2 3 6
3mol Mg/mol= g,则样品中WCl 的质量分数为: 100%=
6
%;根据测定原理,称量时,若加入待测样品后,开盖时间超过1分钟,挥发的CS 的质量增大,m 偏小,
2 3
但WCl 的质量不变,则滴定时消耗NaSO 溶液的体积将不变,样品中WCl 质量分数的测定值将偏大。
6 2 2 3 6
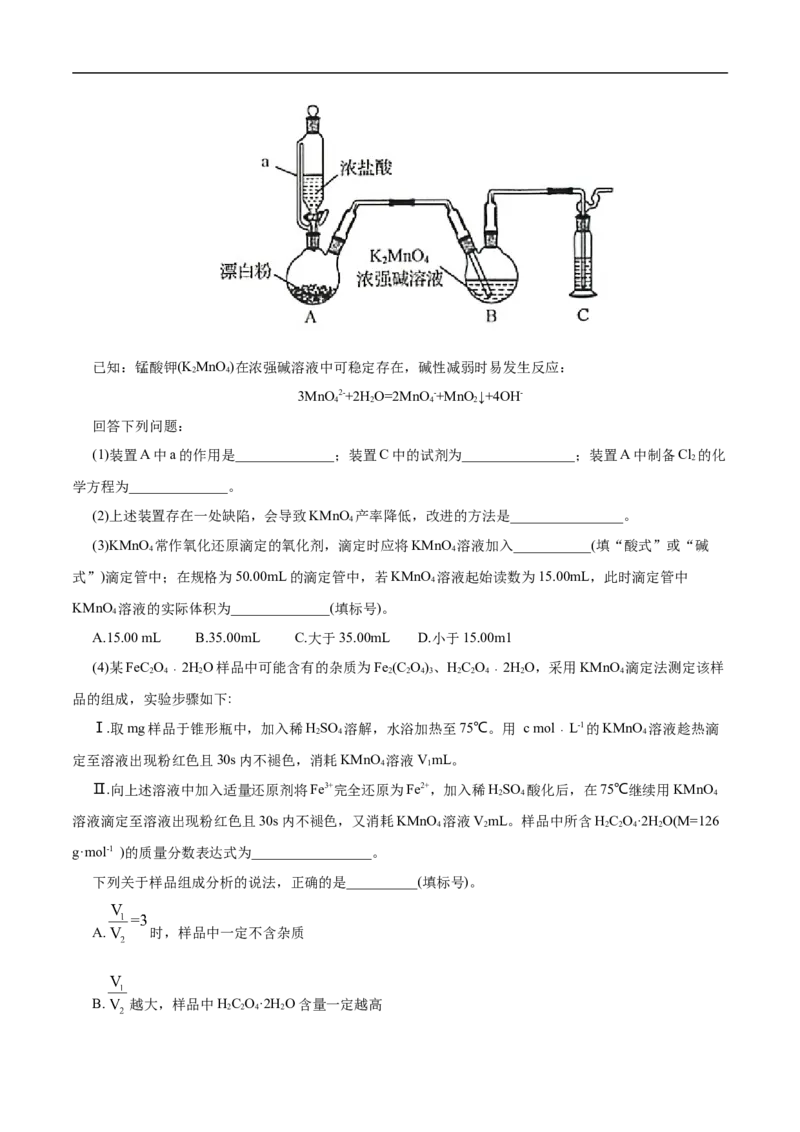
4.(2020•山东卷)某同学利用Cl 氧化KMnO 制备KMnO 的装置如下图所示(夹持装置略):
2 2 4 4已知:锰酸钾(K MnO )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
3MnO 2-+2H O=2MnO -+MnO↓+4OH-
4 2 4 2
回答下列问题:
(1)装置A中a的作用是______________;装置C中的试剂为________________;装置A中制备Cl 的化
2
学方程为______________。
(2)上述装置存在一处缺陷,会导致KMnO 产率降低,改进的方法是________________。
4
(3)KMnO 常作氧化还原滴定的氧化剂,滴定时应将KMnO 溶液加入___________(填“酸式”或“碱
4 4
式”)滴定管中;在规格为50.00mL的滴定管中,若KMnO 溶液起始读数为15.00mL,此时滴定管中
4
KMnO 溶液的实际体积为______________(填标号)。
4
A.15.00 mL B.35.00mL C.大于35.00mL D.小于15.00m1
(4)某FeC O﹒2HO样品中可能含有的杂质为Fe (C O)、HC O﹒2HO,采用KMnO 滴定法测定该样
2 4 2 2 2 4 3 2 2 4 2 4
品的组成,实验步骤如下:
Ⅰ.取mg样品于锥形瓶中,加入稀HSO 溶解,水浴加热至75℃。用 c mol﹒L-1的KMnO 溶液趁热滴
2 4 4
定至溶液出现粉红色且30s内不褪色,消耗KMnO 溶液VmL。
4 1
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀HSO 酸化后,在75℃继续用KMnO
2 4 4
溶液滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO 溶液VmL。样品中所含HC O·2H O(M=126
4 2 2 2 4 2
g·mol-1 )的质量分数表达式为_________________。
下列关于样品组成分析的说法,正确的是__________(填标号)。
A. 时,样品中一定不含杂质
B. 越大,样品中HC O·2H O含量一定越高
2 2 4 2C.若步骤I中滴入KMnO 溶液不足,则测得样品中Fe元素含量偏低
4
D.若所用KMnO 溶液实际浓度偏低,则测得样品中Fe元素含量偏高
4
【答案】(1)平衡气压,使浓盐酸顺利滴下 NaOH溶液
Ca(ClO) +4HCl=CaCl +2Cl↑+2H O
2 2 2 2
(2)在装置A、B之间加装盛有饱和食盐水的洗气瓶
(3)酸式 C (4) BD
【解析】(1)装置A为恒压分液漏斗,它的作用是平衡气压,使浓盐酸顺利滴下,C的作用是吸收反应
不完的Cl,可用NaOH溶液吸收,Ca(ClO) 和浓盐酸在A中发生归中反应产生Cl,反应的化学方程式为
2 2 2
Ca(ClO) +4HCl=CaCl +2Cl↑+2H O;(2)锰酸钾在浓强碱溶液中可稳定存在,碱性减弱时易发生3MnO 2-
2 2 2 2 4
+2H O=2MnO -+MnO↓+4OH-,一部分MnO 2-转化为了MnO ,导致最终KMnO 的产率低,而浓盐酸易挥
2 4 2 4 2 4
发,直接导致B中NaOH溶液的浓度减小,故改进措施是在装置A、B之间加装盛有饱和食盐水的洗气瓶
吸收挥发出来的HCl;(3)高锰酸钾有强氧化性,强氧化性溶液加入酸式滴定管,滴定管的“0”刻度在上,
规格为50.00mL的滴定管中实际的体积大于(50.00-15.00)mL,即大于35.00mL;(4)设FeC O·2H O的物质
2 4 2
的量为xmol,Fe (C O) 的物质的量为ymol,HC O·2H O的物质的量为zmol,步骤I中草酸根和Fe2+均被
2 2 4 3 2 2 4 2
氧化,结合得失电子守恒有:2KMnO ~5H C O(C O2-),KMnO ~5Fe2+,所以 ,
4 2 2 4 2 4 4
步骤II中Fe2+被氧化,由KMnO ~5Fe2+可知, ,联立二个方程解得:z=2.5(cV-
4 1
3V)×10-3,所以HC O·2H O的质量分数= = 。
2 2 2 4 2
关于样品组成分析如下:A项, 时,HC O·2H O的质量分数= =0,样品
2 2 4 2
中不含HC O·2H O,由 和 可知,y≠0,样品中含
2 2 4 2Fe (C O) 杂质,A错误;B项, 越大,由HC O·2H O的质量分数表达式可知,其含量一定越大,B
2 2 4 3 2 2 4 2
正确;C项,Fe元素的物质的量= ,若步骤I中KMnO 溶液不足,则步骤I中
4
有一部分Fe2+没有被氧化,不影响V 的大小,则cV×10-3不变,则对于测得Fe元素的含量无影响,C错误;
2 2
D项,结合C可知:若KMnO 溶液浓度偏低,则消耗KMnO 溶液的体积V、V 均偏大,Fe元素的物质的
4 4 1 2
量偏大,则测得样品中Fe元素含量偏高,D正确。
3.酸碱中和滴定实验
实验仪器: pH 计、酸式滴定管、碱式滴定管、锥形瓶、烧杯、滴定管夹、量筒、铁架台 。
实验药品:标准液、待测液、指示剂。
实验步骤:
(1)查:检查两滴定管是否漏水和堵塞;
(2)洗: 先用蒸馏水洗涤两滴定管,然后用所要盛装的酸碱润洗 2 ~ 3 遍 ;
(3)盛、调:分别将酸、碱溶液注入酸、碱滴定管中,使液面位于滴定管刻度“0”以上2~3厘米处,
并将滴定管固定在滴定管夹上,然后赶走滴定管内部气泡,调节滴定管中液面高度处于某一刻度,并记下
读数。
(4)取:从碱式滴定管中放出25.00 mL氢氧化钠溶液于锥形瓶中,滴入2滴酚酞试液,将锥形瓶置于酸
式滴定管下方,并在瓶底衬一张白纸。
(5)滴定:左手控制酸式滴定管活塞,右手拿住锥形瓶瓶颈,边滴入盐酸,边不断摇动锥形瓶,眼睛始
终注意锥形瓶内溶液颜色变化。
(6)记:当看到加一滴盐酸时,锥形瓶中溶液红色突变为无色时,停止滴定,且半分钟内不恢复原来的
颜色,准确记下盐酸读数,并准确求得滴定用去的盐酸体积。
(7)算:整理数据进行计算。根据c =计算。
B
1.沉淀滴定法
(1)概念:沉淀滴定法是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的反应很多,但符合条件
的却很少,实际上应用最多的是银量法,即利用Ag+与卤素离子的反应来测定Cl-、Br-、I-浓度。
(2)原理:沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应的生成物的溶解度要比
滴定剂与指示剂反应的生成物的溶解度小,否则不能用这种指示剂。如用AgNO 溶液滴定溶液中Cl-的含
3
量时常以CrO为指示剂,这是因为AgCl比Ag CrO 更难溶。
2 4
2.氧化还原滴定法
(1)原理:以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴定一些本身并没有还原性或氧化性,但能与某些还原剂或氧化剂反应的物质。
(2)试剂:常见的用于滴定的氧化剂有KMnO 、KCr O 等。常见的用于滴定的还原剂有亚铁盐、草酸、
4 2 2 7
维生素C等。
(3)指示剂:氧化还原滴定法的指示剂有三类:①氧化还原指示剂。②专用指示剂,如在碘量法滴定中,
可溶性淀粉溶液遇碘标准溶液变蓝。③自身指示剂,如高锰酸钾标准溶液滴定草酸时,滴定终点现象为溶
液由无色变为浅红色。
1.K[Fe(C O)]·3H O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。测定三草酸合铁酸钾中铁的
3 2 4 3 2
含量。
①称量m g样品于锥形瓶中,溶解后加稀HSO 酸化,用c mol·L-1 KMnO 溶液滴定至终点。滴定终点
2 4 4
的现象是___________________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加
稀HSO 酸化,用c mol·L-1 KMnO 溶液滴定至终点,消耗KMnO 溶液V ml。该晶体中铁的质量分数的表
2 4 4 4
达式为________________________________。
2.烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选用如下检测方法。
x
将v L气样通入适量酸化的HO 溶液中,使NO 完全被氧化为NO −,加水稀释至100.00 mL。量取
2 2 x 3
20.00 mL该溶液,加入v mL c mol·L−1 FeSO 标准溶液(过量),充分反应后,用c mol·L−1 KCr O 标准
1 1 4 2 2 2 7
溶液滴定剩余的Fe2+,终点时消耗v mL。(已知:2NO+3H O=2H++2NO–+2H O)
2 2 2 3 2
(1)滴定过程中发生下列反应:3Fe2++NO−+4H+=NO↑+3Fe3++2H O
3 2
Cr O2− + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H O,则气样中NO 折合成NO 的含量为______mg·m−3。
2 7 2 x 2
(2)判断下列情况对NO 含量测定结果的影响(填“偏高” 、“偏低”或“无影响 ”)若缺少采样步骤
x
③,会使测试结果___________。若FeSO 标准溶液部分变质,会使测定结果___________。
4
3.测定KFeO 产品纯度。称取KFeO 产品0.2100g于烧杯中,加入足量的强碱性亚铬酸盐溶液,反
2 4 2 4
应后再加稀硫酸调节溶液呈强酸性,配成250mL溶液,取出25.00mL放入锥形瓶,用0.010 00 mol·L-1的
(NH ) Fe(SO ) 溶液滴定至终点,重复操作 2 次,平均消耗标准溶液 30.00mL[已知:Cr(OH)+
4 2 4 2
FeO===Fe(OH) ↓+CrO+OH-,2CrO+2H+===Cr O+HO,Cr O+6Fe2++14H+===6Fe3++2Cr3++
3 2 2 2
7HO]。则KFeO 产品的纯度为______%(保留1位小数)。
2 2 4
4.称取1.40g二氧化锰样品(含杂质),加入2.68g草酸钠(Na C O)固体,再加入足量的稀硫酸并加热
2 2 4
(杂质不参与反应),充分反应后冷却,将所得溶液转移到100mL容量瓶中用蒸馏水稀释至刻线,从中取出
20.00mL,用 0.0200mol/L 高锰酸钾溶液进行滴定,滴定三次,消耗高锰酸钾溶液体积的平均值为
17.30mL。
(1)写出MnO 溶解反应的离子方程式 。
2
(2)产品的纯度为 。
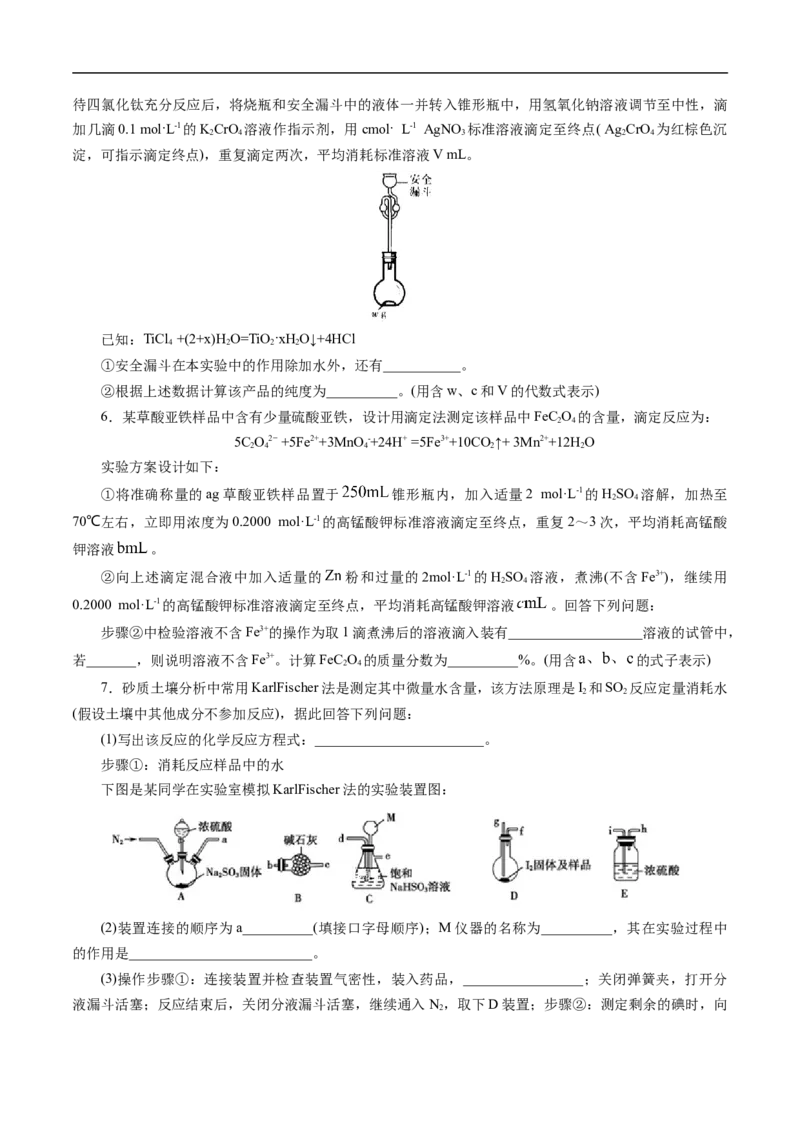
5.利用如图所示装置测定产品纯度:称取w g TiCl 产品进行实验,向安全漏斗中加入适量蒸馏水,
4待四氯化钛充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,用氢氧化钠溶液调节至中性,滴
加几滴0.1 mol·L-1的KCrO 溶液作指示剂,用cmol· L-1 AgNO 标准溶液滴定至终点( Ag CrO 为红棕色沉
2 4 3 2 4
淀,可指示滴定终点),重复滴定两次,平均消耗标准溶液V mL。
已知:TiCl +(2+x)H O=TiO·xHO↓+4HCl
4 2 2 2
①安全漏斗在本实验中的作用除加水外,还有___________。
②根据上述数据计算该产品的纯度为__________。(用含w、c和V的代数式表示)
6.某草酸亚铁样品中含有少量硫酸亚铁,设计用滴定法测定该样品中FeC O 的含量,滴定反应为:
2 4
5C O2− +5Fe2++3MnO -+24H+ =5Fe3++10CO ↑+ 3Mn2++12H O
2 4 4 2 2
实验方案设计如下:
①将准确称量的ag草酸亚铁样品置于 锥形瓶内,加入适量2 mol·L-1的HSO 溶解,加热至
2 4
70℃左右,立即用浓度为0.2000 mol·L-1的高锰酸钾标准溶液滴定至终点,重复2~3次,平均消耗高锰酸
钾溶液 。
②向上述滴定混合液中加入适量的 粉和过量的2mol·L-1的HSO 溶液,煮沸(不含Fe3+),继续用
2 4
0.2000 mol·L-1的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液 。回答下列问题:
步骤②中检验溶液不含Fe3+的操作为取1滴煮沸后的溶液滴入装有___________________溶液的试管中,
若_______,则说明溶液不含Fe3+。计算FeC O 的质量分数为__________%。(用含 的式子表示)
2 4
7.砂质土壤分析中常用KarlFischer法是测定其中微量水含量,该方法原理是I 和SO 反应定量消耗水
2 2
(假设土壤中其他成分不参加反应),据此回答下列问题:
(1)写出该反应的化学反应方程式:________________________。
步骤①:消耗反应样品中的水
下图是某同学在实验室模拟KarlFischer法的实验装置图:
(2)装置连接的顺序为a__________(填接口字母顺序);M仪器的名称为__________,其在实验过程中
的作用是__________________________。
(3)操作步骤①:连接装置并检查装置气密性,装入药品,_________________;关闭弹簧夹,打开分
液漏斗活塞;反应结束后,关闭分液漏斗活塞,继续通入N,取下D装置;步骤②:测定剩余的碘时,向
2反应后的D装置加入蒸馏水,过滤,充分洗涤滤渣,并合并洗涤液和滤液,将其配成250.00mL溶液,取
25.00mL用0.20mol·L-1NaSO 标准液滴定剩余的碘单质,已知反应如下:2SO +I=S O +2I-。
2 2 3 2 2 4
(4)Na SO 标准液应装在________(填“酸式”“碱式”)滴定管中;上述操作中,合并洗涤液和滤液的
2 2 3
目的是________________________________。
(5)滴定实验重复四次得到数据如下:
实验 1 2 3 4
消耗的标准液的体积/mL 18.37 20.05 19.95 20.00
①若实验开始时,向D装置中加入10.00g土壤样品和10.16gI(已知I 过量),则样品土壤中水的含量为
2 2
________%(计算结果保留小数点后一位)。
②若NaSO 标准液已部分氧化变质,则水含量测定结果将________(填“偏高”“偏低”或“不变”)。
2 2 3
8.(2023届·内蒙古达拉特旗第一中学高三开学考试)酸碱中和滴定是一种重要的化学分析手段,回答
下列问题:
I.某班学生通过实验测定酸碱滴定曲线,实验用品包括0.1mol/LHCl溶液、0.1mol/LNaOH溶液、蒸馏
水、pH计、酸式滴定管、碱式滴定管、滴定管架(铁架台和蝴蝶夹)、锥形瓶。甲、乙、丙3组同学用锥形
瓶取体积为20.00mL的溶液,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、
c所示。
(1)滴定时选用的滴定管为____(选填“酸式”或“碱式”)滴定管,在装入标准溶液前需要对滴定管进
行的操作为____。
(2)在图中的三条滴定曲线中,较为准确的是____。
II.在实际操作过程中,由于甲基橙指示剂的变色不敏锐,难以判断滴定终点,需在其中加入少量的
“惰性染料”靛蓝二磺酸钠,其固定颜色与甲基橙的可变颜色进行叠加(变色范围不变),形成“酸色”为
紫色、过渡色为浅灰色、“碱色”为绿色的混合指示剂。已知室温下0.10mol/LNH Cl溶液的,若以甲基橙
4
-靛蓝二磺酸钠为指示剂,用0.20mol/L盐酸滴定20.00mL同浓度的氨水,则:
(3)NH Cl溶液显酸性的原因是____(用离子方程式表示)。
4
(4)判断滴定终点的现象是____。
(5)若多组实验中所用盐酸的体积均略大于20.00mL,原因是____。
9.(2022·河南省商丘市名校联考)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO ·(NH )CO·2H O作原料制备。制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法
3 4 2 3 2
分析产品中Cl-的含量,称取6.1000g产品用适量硝酸溶解,经稀释等步骤最终配得500mL的溶液。
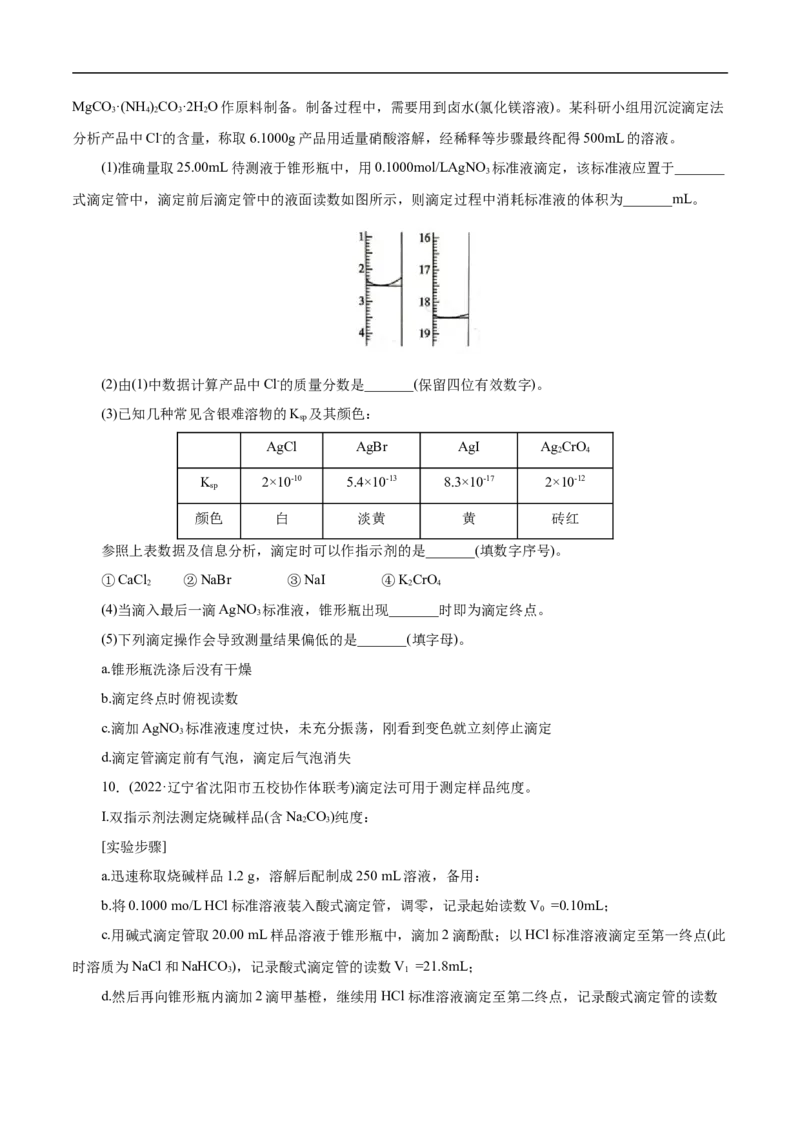
(1)准确量取25.00mL待测液于锥形瓶中,用0.1000mol/LAgNO 标准液滴定,该标准液应置于_______
3
式滴定管中,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为_______mL。
(2)由(1)中数据计算产品中Cl-的质量分数是_______(保留四位有效数字)。
(3)已知几种常见含银难溶物的K 及其颜色:
sp
AgCl AgBr AgI Ag CrO
2 4
K 2×10-10 5.4×10-13 8.3×10-17 2×10-12
sp
颜色 白 淡黄 黄 砖红
参照上表数据及信息分析,滴定时可以作指示剂的是_______(填数字序号)。
①CaCl ②NaBr ③NaI ④KCrO
2 2 4
(4)当滴入最后一滴AgNO 标准液,锥形瓶出现_______时即为滴定终点。
3
(5)下列滴定操作会导致测量结果偏低的是_______(填字母)。
a.锥形瓶洗涤后没有干燥
b.滴定终点时俯视读数
c.滴加AgNO 标准液速度过快,未充分振荡,刚看到变色就立刻停止滴定
3
d.滴定管滴定前有气泡,滴定后气泡消失
10.(2022·辽宁省沈阳市五校协作体联考)滴定法可用于测定样品纯度。
I.双指示剂法测定烧碱样品(含NaCO)纯度:
2 3
[实验步骤]
a.迅速称取烧碱样品1.2 g,溶解后配制成250 mL溶液,备用:
b.将0.1000 mo/L HCl标准溶液装入酸式滴定管,调零,记录起始读数V =0.10mL;
0
c.用碱式滴定管取20.00 mL样品溶液于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此
时溶质为NaCl和NaHCO ),记录酸式滴定管的读数V =21.8mL;
3 1
d.然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,记录酸式滴定管的读数V =23.50mL。
2
(1)滴定至第一终点的过程中,发生反应的离子方程式为_______。
(2)判断滴定至第二终点的现象是溶液由_______色变为橙色。
(3)样品中NaOH的质量分数 _______%(计算结果保留小数点后1位)。
(4)下列操作会导致测得的NaOH质量分数偏高的是_______(填字母序号)。
a.滴定前有气泡,滴定至第一终点时气泡消失
b.达到第一终点前,锥形瓶中有气泡产生
c.第一终点后继续滴定时,锥形瓶中有少许液体溅出
d.记录酸式滴定管读数V 时,仰视标准液液面
2
II.测定三草酸合铁酸钾K[Fe(C O)]·3H O中铁的含量:
3 2 4 3 2
第一步,称量m g样品于锥形瓶中,溶解后加稀HSO 酸化,用c mol/L KMnO 溶液滴定至终点,消
2 4 4
耗KMnO 溶液V mL。
4 1
第二步,向上述溶液中加入过量锌粉将Fe3+转化为Fe2+,过滤、洗涤,将滤液及洗涤液全部收集到锥
形瓶中。加稀HSO 酸化,用c mol/L KMnO 溶液滴定至终点,消耗KMnO 溶液V mL。
2 4 4 4 2
(5)该晶体中铁的质量分数的表达式是_______。
11.(2022·四川省雅安市质检)用氧化还原滴定法可以测定市售双氧水中过氧化氢的浓度(单位g∙L−1),
实验过程包括标准溶液的准备和滴定待测溶液。
I.准备KMnO 标准溶液
4
a.配制100.00mLKMnO 溶液备用;
4
b.准确称取NaC O 基准物质3.35g(0.025mol),配制成250.00mL标准溶液。取出25.00mL于锥形瓶
2 2 4
中,加入适量3 mol∙L−1硫酸酸化后,用待标定的KMnO 溶液滴定至终点,记录数据,计算KMnO 溶液的
4 4
浓度。
II.滴定主要步骤
a.取待测双氧水10.00mL于锥形瓶中;
b.锥形瓶中加入30.00mL蒸馏水和30.00mL3 mol∙L−1硫酸,然后用已标定的KMnO 溶液(0.1000
4
mol∙L−1)滴定至终点;
c.重复上述操作两次,三次测定的数据如表:
组别 1 2 3
消耗标准溶液体积(mL) 25.00 25.02 24.98
d.数据处理。请回答下列问题:
(1)将称得的NaC O 配制成250.00mL标准溶液,所使用的仪器除烧杯和玻璃棒外还有___。
2 2 4
(2)标定KMnO 溶液时,能否用稀硝酸调节溶液酸度____(填“能”或“不能”),简述理由___。写出
4
标定过程中发生反应的离子方程式____。
(3)滴定待测双氧水时,标准溶液应装入____滴定管,滴定至终点的现象是____。
(4)计算此双氧水的浓度为____g∙L−1。
(5)误差分析:在第II步滴定主要步骤中,下列操作会使双氧水浓度测定结果偏高的是____。A.锥形
瓶洗净后用双氧水润洗
B.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
C.观察读数时,滴定前仰视,滴定后俯视
D.振荡锥形瓶时部分液体溅出