文档内容
专项训练 热重曲线的计算
一、单选题
1.W、X、Y是三种短周期主族元素且分别位于三个周期,X和Y位于同一主族且原
子序数存在2倍关系。 (M=278g/mol)的热重曲线(空气中加热)如图所示。
下列说法不正确的是
A.X和Y的简单氢化物稳定性:X>Y
B.W和金属钠形成的化合物为离子化合物
C.热重曲线的第1、2、3个拐点失去的都是
D.最终曲线Q所得到的物质为
2.化合物 是分析化学中重要的基准物质,其中X、Y、Z、T
分别位于三个短周期,原子序数依次增加;T与Z同主族;常温下 为气体,其分
子的总电子数为奇数;W为常见的金属元素,在该化合物中W离子的价层电子排布式
为 。在惰性气体氛围中该物质的热重曲线如图所示。下列说法错误的是
A.简单离子半径:T>Y>Z
B.W元素位于元素周期表的d区
C.简单气态氢化物的稳定性:Z>Y
资料收集整理【淘宝店铺:向阳百分百】D.580℃热分解后得到的固体化合物是WZ
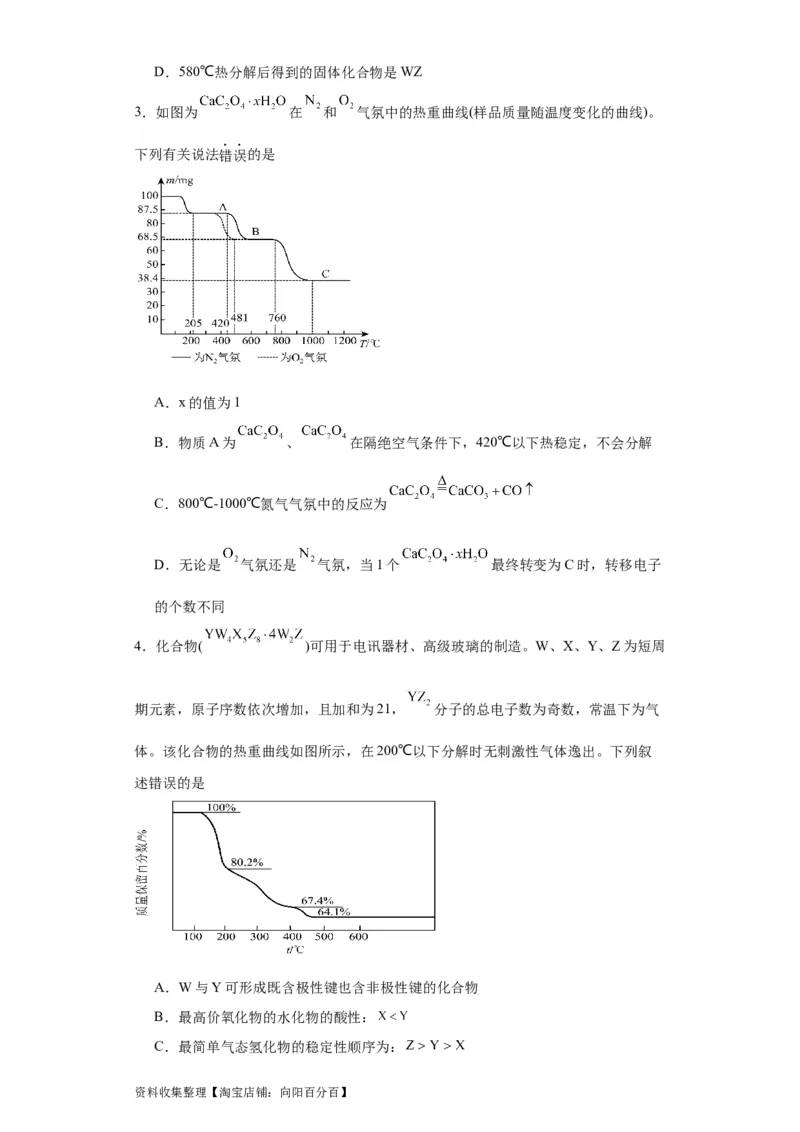
3.如图为 在 和 气氛中的热重曲线(样品质量随温度变化的曲线)。
下列有关说法错误的是
A.x的值为1
B.物质A为 、 在隔绝空气条件下,420℃以下热稳定,不会分解
C.800℃-1000℃氮气气氛中的反应为
D.无论是 气氛还是 气氛,当1个 最终转变为C时,转移电子
的个数不同
4.化合物( )可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
期元素,原子序数依次增加,且加和为21, 分子的总电子数为奇数,常温下为气
体。该化合物的热重曲线如图所示,在200℃以下分解时无刺激性气体逸出。下列叙
述错误的是
A.W与Y可形成既含极性键也含非极性键的化合物
B.最高价氧化物的水化物的酸性:
C.最简单气态氢化物的稳定性顺序为:
资料收集整理【淘宝店铺:向阳百分百】D.100~200℃阶段热分解的化学方程式为:
5.8.34g FeSO •7H O(相对分子质量:278)样品受热脱水过程的热重曲线(样品质量随温
4 2
度变化的曲线)如图所示,下列说法正确的是
A.温度为78℃时固体物质M的化学式为FeSO •5H O
4 2
B.温度为159℃时固体物质N的化学式为FeSO •2H O
4 2
C.在隔绝空气条件下,N得到P的化学方程式为FeSO •2H O FeSO +2H O
4 2 4 2
D.取适量380℃时所得的样品P,隔绝空气加热至650℃得到一种固体物质Q,同
时有两种无色气体生成,Q的化学式为Fe O
2 3
6. 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,
取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用
盐酸将其恰好完全溶解,得到 溶液和4.48L(标准状况)黄绿色
气体。下列说法错误的是
A.290℃时,若固体中只含有两种元素,则为
B.400℃时,
C.500℃时,固体中氧元素质量分数约为26.6%
D.生成的黄绿色气体可用于工业上生产“84”消毒液
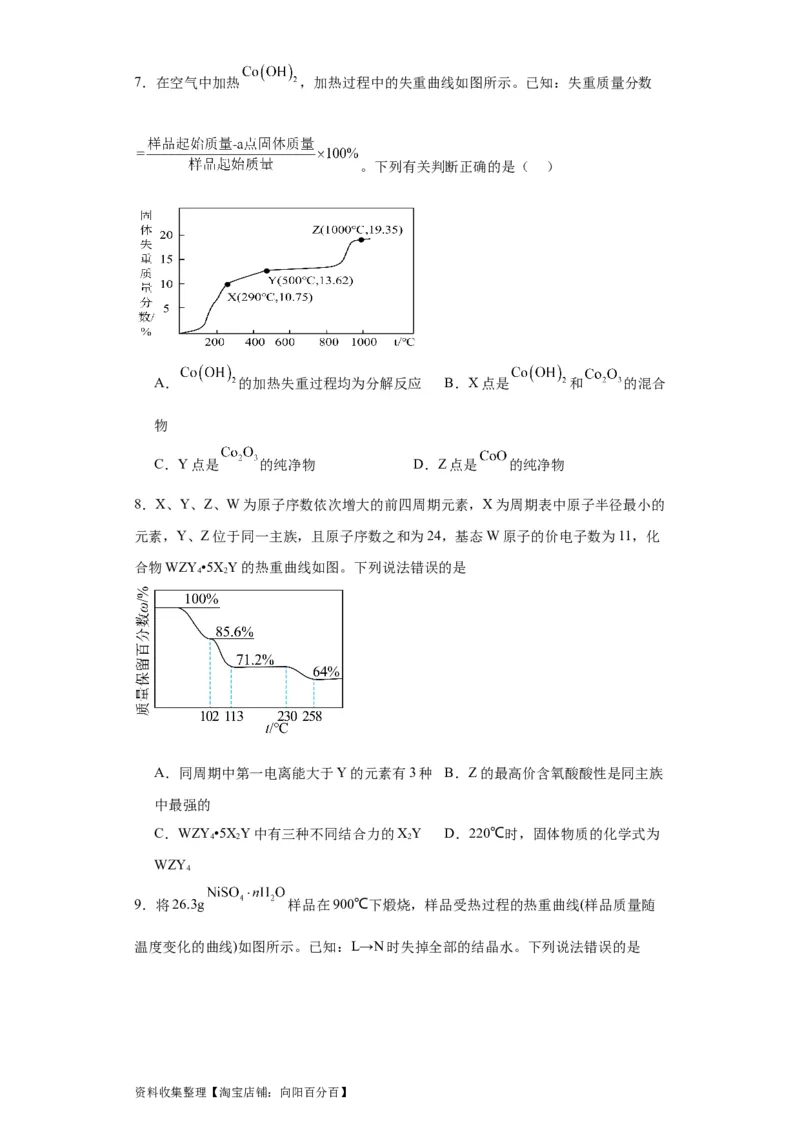
资料收集整理【淘宝店铺:向阳百分百】7.在空气中加热 ,加热过程中的失重曲线如图所示。已知:失重质量分数
。下列有关判断正确的是( )
A. 的加热失重过程均为分解反应 B.X点是 和 的混合
物
C.Y点是 的纯净物 D.Z点是 的纯净物
8.X、Y、Z、W为原子序数依次增大的前四周期元素,X为周期表中原子半径最小的
元素,Y、Z位于同一主族,且原子序数之和为24,基态W原子的价电子数为11,化
合物WZY •5X Y的热重曲线如图。下列说法错误的是
4 2
A.同周期中第一电离能大于Y的元素有3种 B.Z的最高价含氧酸酸性是同主族
中最强的
C.WZY •5X Y中有三种不同结合力的XY D.220℃时,固体物质的化学式为
4 2 2
WZY
4
9.将26.3g 样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随
温度变化的曲线)如图所示。已知:L→N时失掉全部的结晶水。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.
B.固体M的化学式为
C.生成固体P时,样品的失重率约为71.5%
D.固体Q的化学式为NiO
10. 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。W、X、Y、Z
为元素周期表前20号元素,已知W、X形成的化合物种类最多,Y原子最外层电子数
是其电子层数3倍,人体血液中缺乏Z离子易造成肌肉抽搐, 热分解可制
备ZY,该化合物的热重曲线如图所示。下列叙述不正确的是
A.150℃~200℃阶段热分解失去
B.400℃~600℃热分解后生成固体化合物
C.W、Y可形成具有杀菌消毒作用的化合物
D.化合物 具有还原性和强酸性
11.硝酸钬可用作科研试剂等。4.41g 受热分解过程的热重曲线(晶体
质量随温度变化的曲线)如图所示。
资料收集整理【淘宝店铺:向阳百分百】已知 中 。下列说法错误的是
A. 中n值为5
B.M点物质的化学式为
C.已知Q点物质的化学式为 ,则M→Q过程的其他产物为
和NO
D.P点氧化物的化学式为
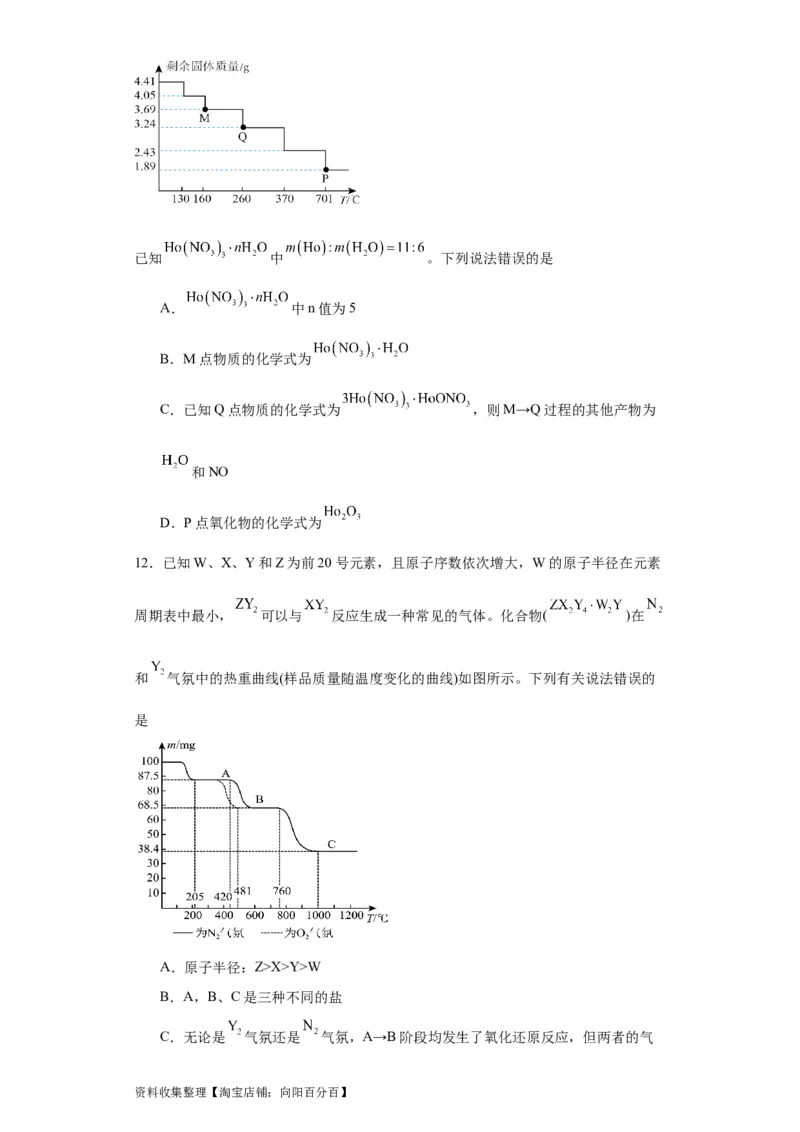
12.已知W、X、Y和Z为前20号元素,且原子序数依次增大,W的原子半径在元素
周期表中最小, 可以与 反应生成一种常见的气体。化合物( )在
和 气氛中的热重曲线(样品质量随温度变化的曲线)如图所示。下列有关说法错误的
是
A.原子半径:Z>X>Y>W
B.A,B、C是三种不同的盐
C.无论是 气氛还是 气氛,A→B阶段均发生了氧化还原反应,但两者的气
资料收集整理【淘宝店铺:向阳百分百】态产物不同
D.在酸性 溶液中加入少量A固体样品时,溶液褪色且有少量气泡产生
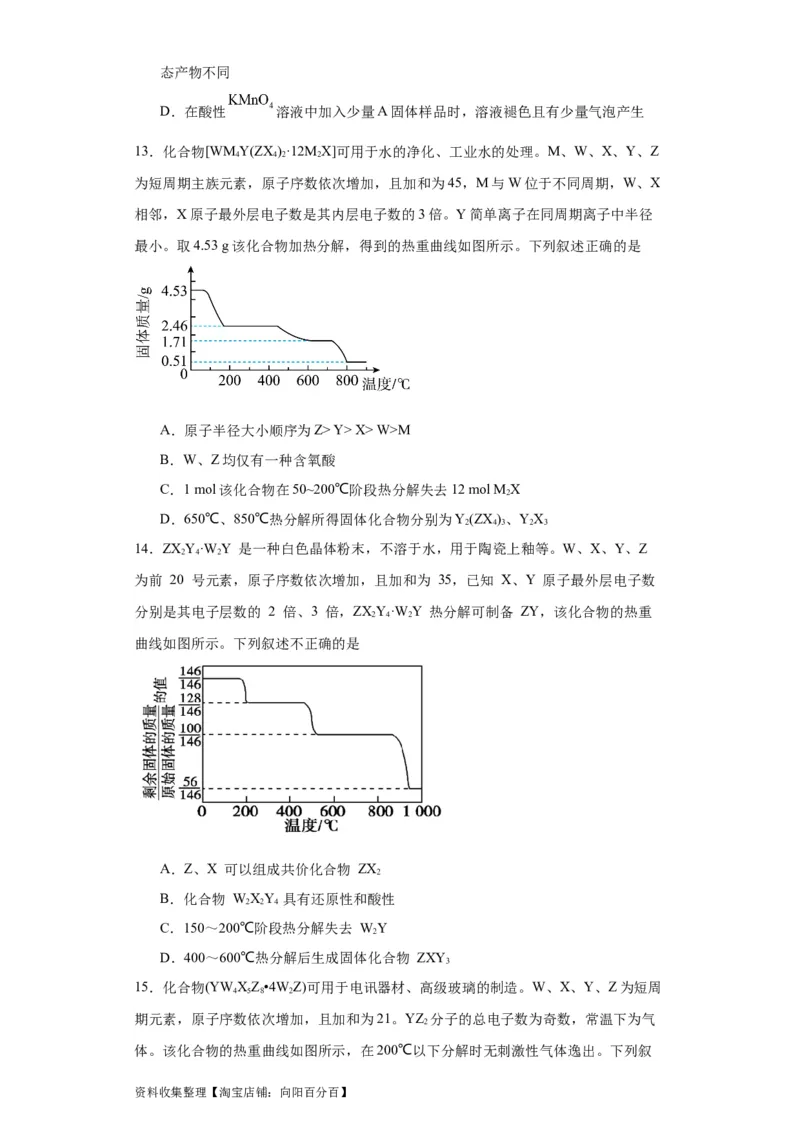
13.化合物[WMY(ZX )·12M X]可用于水的净化、工业水的处理。M、W、X、Y、Z
4 4 2 2
为短周期主族元素,原子序数依次增加,且加和为45,M与W位于不同周期,W、X
相邻,X原子最外层电子数是其内层电子数的3倍。Y简单离子在同周期离子中半径
最小。取4.53 g该化合物加热分解,得到的热重曲线如图所示。下列叙述正确的是
A.原子半径大小顺序为Z> Y> X> W>M
B.W、Z均仅有一种含氧酸
C.1 mol该化合物在50~200℃阶段热分解失去12 mol M X
2
D.650℃、850℃热分解所得固体化合物分别为Y(ZX)、YX
2 4 3 2 3
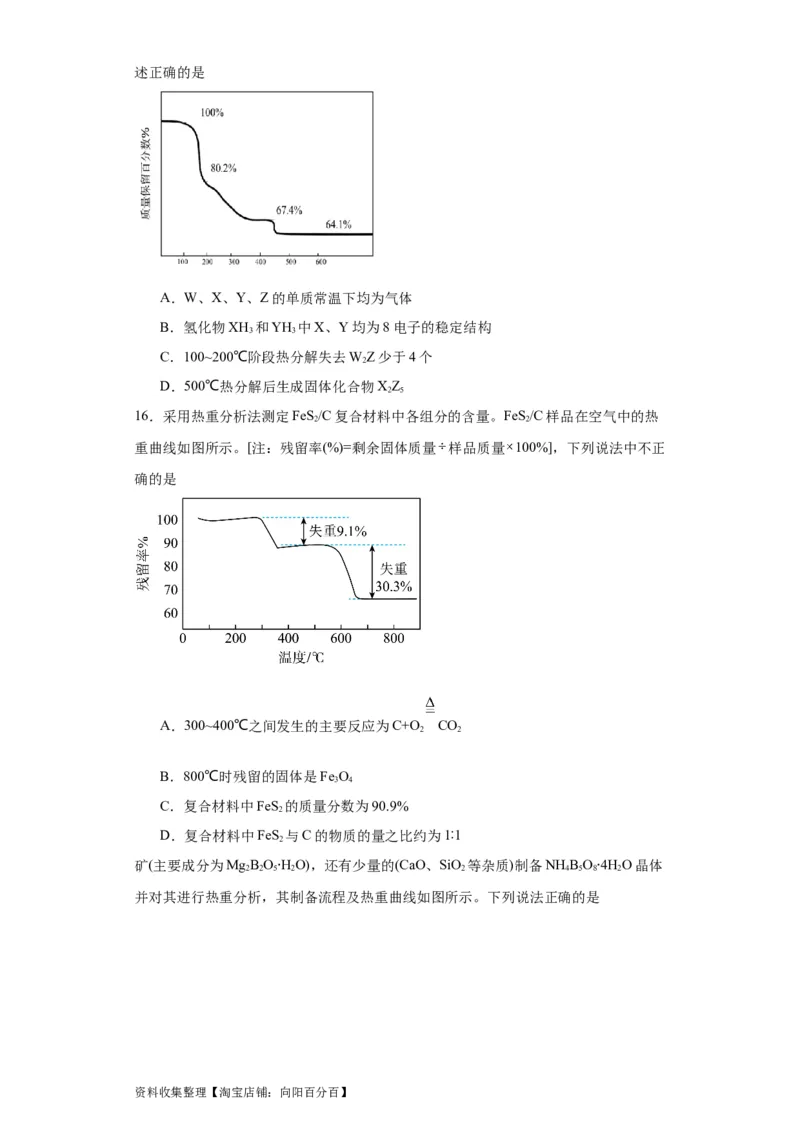
14.ZXY·W Y 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。W、X、Y、Z
2 4 2
为前 20 号元素,原子序数依次增加,且加和为 35,已知 X、Y 原子最外层电子数
分别是其电子层数的 2 倍、3 倍,ZXY·W Y 热分解可制备 ZY,该化合物的热重
2 4 2
曲线如图所示。下列叙述不正确的是
A.Z、X 可以组成共价化合物 ZX
2
B.化合物 WXY 具有还原性和酸性
2 2 4
C.150~200℃阶段热分解失去 WY
2
D.400~600℃热分解后生成固体化合物 ZXY
3
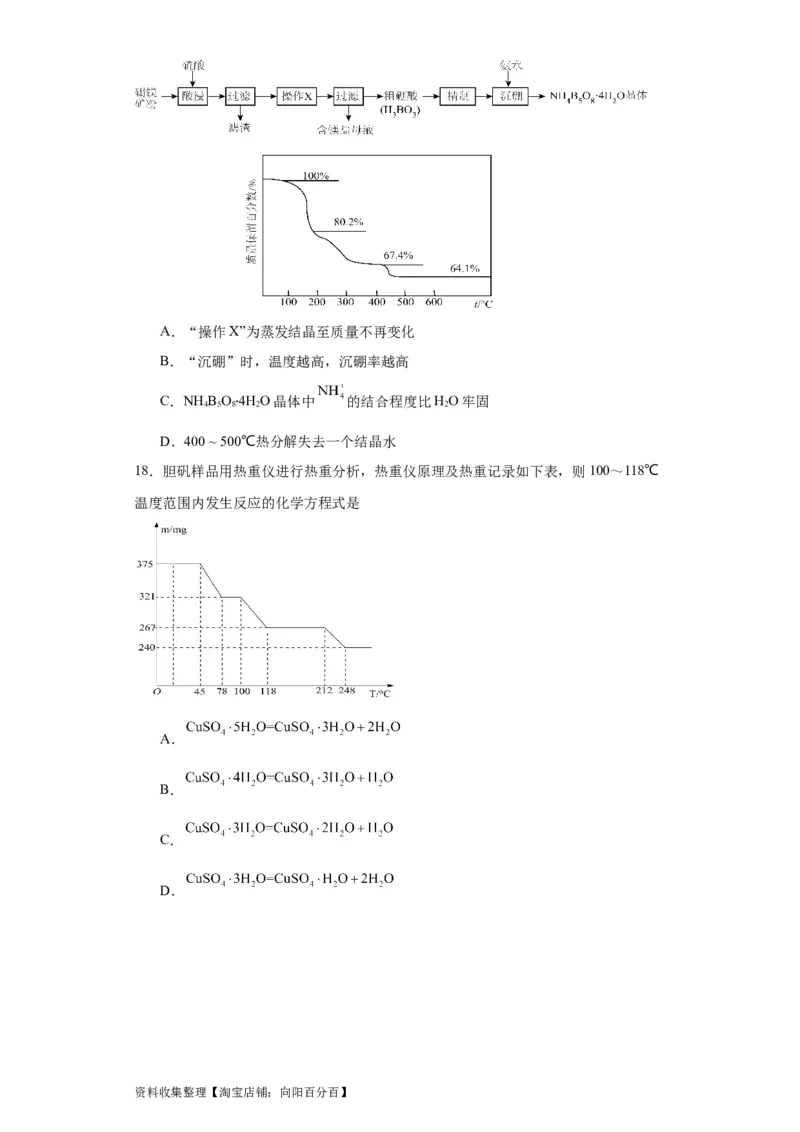
15.化合物(YW XZ•4WZ)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
4 5 8 2
期元素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数,常温下为气
2
体。该化合物的热重曲线如图所示,在200℃以下分解时无刺激性气体逸出。下列叙
资料收集整理【淘宝店铺:向阳百分百】述正确的是
A.W、X、Y、Z的单质常温下均为气体
B.氢化物XH 和YH 中X、Y均为8电子的稳定结构
3 3
C.100~200℃阶段热分解失去WZ少于4个
2
D.500℃热分解后生成固体化合物XZ
2 5
16.采用热重分析法测定FeS/C复合材料中各组分的含量。FeS/C样品在空气中的热
2 2
重曲线如图所示。[注:残留率(%)=剩余固体质量 样品质量 100%],下列说法中不正
确的是
A.300~400℃之间发生的主要反应为C+O CO
2 2
B.800℃时残留的固体是Fe O
3 4
C.复合材料中FeS 的质量分数为90.9%
2
D.复合材料中FeS 与C的物质的量之比约为1∶1
2
矿(主要成分为MgB O HO),还有少量的(CaO、SiO 等杂质)制备NH B O 4HO晶体
2 2 5 2 2 4 5 8 2
并对其进行热重分析,其∙ 制备流程及热重曲线如图所示。下列说法正确的是∙
资料收集整理【淘宝店铺:向阳百分百】A.“操作X”为蒸发结晶至质量不再变化
B.“沉硼”时,温度越高,沉硼率越高
C.NH B O 4HO晶体中 的结合程度比HO牢固
4 5 8 2 2
∙
D.400 ~ 500℃热分解失去一个结晶水
18.胆矾样品用热重仪进行热重分析,热重仪原理及热重记录如下表,则100~118℃
温度范围内发生反应的化学方程式是
A.
B.
C.
D.
资料收集整理【淘宝店铺:向阳百分百】