文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题03 离子共存、离子检验和推断
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
离子共存、离子检验和推断也是历年高考考查的重要内容。
预计2025年高考对这部分内容的考查,选择题仍主要涉及离子共存、离子的检验与推断三个角度,题
目考查内容主要是元素化合物的性质、化学过程的解释。
因此,在复习时要注意离子不能共存的各种类型,特别是氧化还原、双水解不能共存的情况。离子检
验和推断要考察全面,牢记重要的离子反应、检验方法。
1.(2024·重庆·高考真题)常温下,下列各组离子在指定溶液中能大量共存的是
A.氨水中: B.稀硫酸中:
C. 溶液中: D. 溶液中:
2.(2024·江西·高考真题)白色固体样品X,可能含有AgNO、NH NO 、BaCl 、KCl、NaSO 、
3 4 3 2 2 3
NaCO、Al O 之中的几种或全部。在三个烧杯中各加入适量X。分别加入足量以下三种试剂并微热使之
2 3 2 3
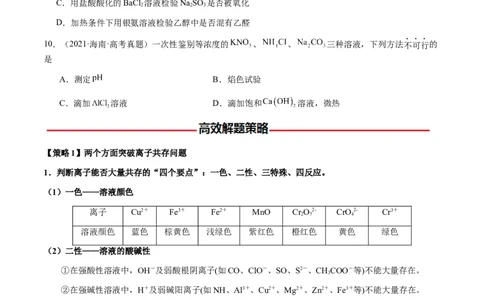
充分反应,实验记录为:
编号 试剂 反应后的不溶物 生成的气体
Ⅰ 蒸馏水 白色 无色、有刺激性气味
Ⅱ 稀盐酸 白色 无色、无味
Ⅲ NaOH溶液 无不溶物 无色、有刺激性气味
依据实验现象,下列说法正确的是
A.可能含Al O B.含BaCl C.含NaSO D.不含KCl
2 3 2 2 3
3.(2024·宁夏四川·高考真题)四瓶无色溶液 ,它们之间的反应关系
如图所示。其中a、b、c、d代表四种溶液,e和g为无色气体,f为白色沉淀。下列叙述正确的是A.a呈弱碱性
B.f可溶于过量的b中
C.c中通入过量的e可得到无色溶液
D.b和d反应生成的沉淀不溶于稀硝酸
4.(2024·浙江·高考真题)在溶液中能大量共存的离子组是
A. B.
C. D.
5.(2022·天津·高考真题)25℃时,下列各组离子中可以在水溶液中大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
6.(2022·重庆·高考真题)下列操作中,不会影响溶液中K+、Al3+、Fe3+、Ba2+、Cl-、NO 等离子大量共
存的是
A.加入ZnSO B.加入Fe粉 C.通入NH D.通入CO
4 3 2
7.(2022·湖北·高考真题)下列各组离子在给定溶液中能大量共存的是
A.在 氨水中:
B.在 氯化钠溶液中:
C.在 醋酸溶液中:
D.在 硝酸银溶液中:
8.(2022·全国·高考真题)某白色粉末样品,可能含有 、 、 和 。取少量
样品进行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加 溶液有沉淀生成。该样品中确定存在的是
A. B.
C. D.
9.(2023·辽宁·高考真题)下列鉴别或检验不能达到实验目的的是
A.用石灰水鉴别NaCO 与NaHCO
2 3 3
B.用KSCN溶液检验FeSO 是否变质
4
C.用盐酸酸化的BaCl 溶液检验NaSO 是否被氧化
2 2 3
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
10.(2021·海南·高考真题)一次性鉴别等浓度的 、 、 三种溶液,下列方法不可行的
是
A.测定 B.焰色试验
C.滴加 溶液 D.滴加饱和 溶液,微热
【策略1】两个方面突破离子共存问题
1.判断离子能否大量共存的“四个要点”:一色、二性、三特殊、四反应。
(1)一色——溶液颜色
离子 Cu2+ Fe3+ Fe2+ MnO Cr O2- CrO2- Cr3+
2 7 4
溶液颜色 蓝色 棕黄色 浅绿色 紫红色 橙红色 黄色 绿色
(2)二性——溶液的酸碱性
①在强酸性溶液中,OH-及弱酸根阴离子(如CO、ClO-、SO、S2-、CHCOO-等)不能大量存在。
3
②在强碱性溶液中,H+及弱碱阳离子(如NH、Al3+、Cu2+、Mg2+、Zn2+、Fe3+等)不能大量存在。
③如HCO、HS-、HSO、HPO、HPO等,在强酸性或强碱性溶液中均不能大量存在。
2
(3)三特殊——三种特殊情况:
①AlO与HCO不能大量共存:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
②“NO+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO等还原性的离子发生氧化还原反应而不能
大量共存。
③NH与CHCOO-、CO,Mg2+与HCO等组合中,虽然两种离子都能水解且水解相互促进,但总的水
3
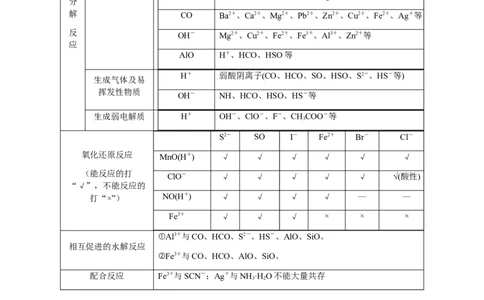
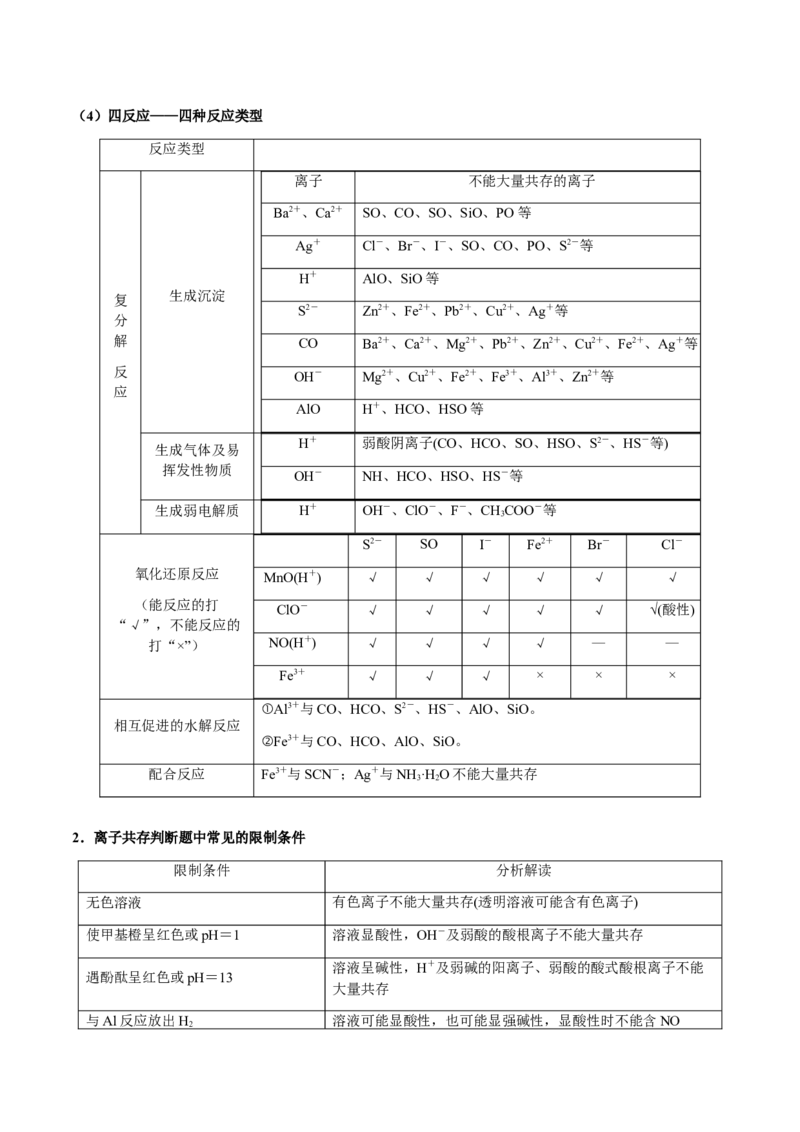
解程度仍很小,它们在溶液中仍能大量共存。(4)四反应——四种反应类型
反应类型
离子 不能大量共存的离子
Ba2+、Ca2+ SO、CO、SO、SiO、PO等
Ag+ Cl-、Br-、I-、SO、CO、PO、S2-等
H+ AlO、SiO等
生成沉淀
复
S2- Zn2+、Fe2+、Pb2+、Cu2+、Ag+等
分
解 CO Ba2+、Ca2+、Mg2+、Pb2+、Zn2+、Cu2+、Fe2+、Ag+等
反 OH- Mg2+、Cu2+、Fe2+、Fe3+、Al3+、Zn2+等
应
AlO H+、HCO、HSO等
H+ 弱酸阴离子(CO、HCO、SO、HSO、S2-、HS-等)
生成气体及易
挥发性物质
OH- NH、HCO、HSO、HS-等
生成弱电解质 H+ OH-、ClO-、F-、CHCOO-等
3
S2- SO I- Fe2+ Br- Cl-
氧化还原反应 MnO(H+) √ √ √ √ √ √
(能反应的打 ClO- √ √ √ √ √ √(酸性)
“√”,不能反应的
打“×”) NO(H+) √ √ √ √ — —
Fe3+ √ √ √ × × ×
①Al3+与CO、HCO、S2-、HS-、AlO、SiO。
相互促进的水解反应
②Fe3+与CO、HCO、AlO、SiO。
配合反应 Fe3+与SCN-;Ag+与NH ·H O不能大量共存
3 2
2.离子共存判断题中常见的限制条件
限制条件 分析解读
无色溶液 有色离子不能大量共存(透明溶液可能含有色离子)
使甲基橙呈红色或pH=1 溶液显酸性,OH-及弱酸的酸根离子不能大量共存
溶液呈碱性,H+及弱碱的阳离子、弱酸的酸式酸根离子不能
遇酚酞呈红色或pH=13
大量共存
与Al反应放出H 溶液可能显酸性,也可能显强碱性,显酸性时不能含NO
2由水电离出的c(H+)=1×10-13 mol·L-
溶液可能显酸性,也可能显碱性
1
通入足量的CO(或NH ) 溶液呈酸性(或碱性)
2 3
因发生氧化还原反应而不能大量共存 能发生氧化还原反应的氧化性离子和还原性离子不能大量共存
“一定”“可能”还是“不能”大量
确定是“可能性”还是“肯定性”
共存
说明该溶液呈酸性[稀释的是溶质,溶质c(H+)减小,而c(OH
加水稀释,减小
-)增大]
某溶液的lg =12 该溶液呈酸性
【策略2】牢记常见离子检验的特征反应及注意事项
(1)常见阳离子的检验
【易错提醒】阳离子检验的注意事项
NaOH溶液可以同时鉴别出若干种阳离子,包括Al3+、Fe3+、Fe2+、Cu2+、NH、Mg2+等多种离子,在阳
离子鉴别中,NaOH溶液是一种应用较广的试剂。若先使用NaOH溶液(必要时可加热)检验出几种离子,
再用其他方法鉴别用NaOH溶液鉴别不出来的离子,整个问题可以较快解决。
(2)常见阴离子的检验【易错提醒】阴离子检验的注意事项
①AgNO 溶液与稀硝酸、BaCl 溶液与稀盐酸这两组试剂,可以鉴别出若干种阴离子,是阴离子鉴别最
3 2
常用的试剂组合。一般说来,若待检的若干种离子中有SO,最好先用BaCl 溶液和盐酸这组试剂,检出包
2
括SO在内的一些离子,其他离子再用AgNO 溶液与稀硝酸等去鉴别。
3
②为了检验某盐中含SO或CO,可以直接加酸(非氧化性酸,如盐酸),根据放出气体的气味等特征现
象判断气体是CO 或SO ,进而确定物质中含CO或SO。
2 2
③灵活运用阴离子检验的知识,有时可以解决某些阳离子的鉴别问题。例如,在一定条件下,可考虑
用卤素离子(如Cl-)检出Ag+,用SO检出Ba2+。
【策略3】坚持“四项基本原则”突破离子推断
1.离子推断的“四项基本原则”
(1)肯定原则:根据实验现象推出溶液中肯定存在或肯定不存在的离子(记住几种常见的有色离子:Fe2
+、Fe3+、Cu2+、MnO、CrO、Cr O)。
2
(2)互斥原则:在肯定某些离子存在的同时,结合离子共存规律,否定一些离子的存在(注意题目中的隐
含条件,如酸性、碱性、指示剂的颜色变化、与铝反应产生H、水的电离情况等)。
2
(3)电中性原则:溶液呈电中性,溶液中有阳离子,必有阴离子,且溶液中阳离子所带正电荷总数与阴
离子所带负电荷总数相等(这一原则可帮助我们确定一些隐含的离子)。
(4)进出原则:通常是在实验过程中使用,是指在实验过程中反应生成的离子或引入的离子对后续实验
的干扰。
2.电荷守恒在定量型离子推断试题中的应用
离子定量推断试题常根据离子的物质的量(或浓度)定量推断最后一种离子的存在:如果多种离子共
存,且只有一种离子的物质的量未知,可以用电荷守恒来确定最后一种离子是否存在,即阳离子所带的正
电荷总数等于阴离子所带的负电荷总数。1.(2025高三上·辽宁·模拟预测)下列有关实验的叙述正确的是
A.配制 溶液,用托盘天平称取 固体
B.向某溶液中加入 溶液,有白色沉淀生成,说明原溶液中一定含有
C.把红热的木炭加入浓硝酸中,有红棕色气体生成,该现象能证明碳与浓硝酸发生了反应
D.将足量的 通入 溶液中充分反应,取反应后溶液,滴加酸性 溶液,
溶液紫色褪去,证明反应生成了
2.(2024·广东深圳·一模)将下列离子: 、 、 、 、 、 、 、 、 、
、 、 按可能大量共存的情况,把它们全部分成 、 两组,而且每组中都含有不少于两种阳
离子和两种阴离子。下列离子不会同在一组的是
A. 、 B. 、 C. 、 D. 、
3.(2025高三上·福建·模拟预测)某白色固体混合物由 中的两种组成,进行
如下实验:
①混合物溶于水,得到澄清透明溶液;
②做焰色试验,透过蓝色钴玻璃可观察到火焰的颜色呈紫色;
③向溶液中加碱溶液,产生白色沉淀。
根据实验现象可判断其组成为
A. B.
C. D.
4.(2025高三上·湖北·模拟预测)某溶液中只可能含有 、 、 、 、 、 、 、
中的若干种离子,离子浓度均为 。某同学进行了如下实验,下列说法正确的是
A.原溶液中存在 、 、 、
B.原溶液中含有 、不含
C.沉淀 中含有
D.滤液 中大量存在的阳离子有 、 和5.(2025高三上·宁夏·模拟预测)某无色溶液可能含有等物质的量的下列某些离子: 、 、 、
、 、 、 ,取溶液分别进行如下实验:①加入 酸化的 溶液产生白色沉淀;
②加入锌粉,有气泡生成;③加入适量 粉末产生白色沉淀。下列说法正确的是
A.由①、②可知该无色溶液中一定有 、 ,可能有
B.该无色溶液中可能有
C.该无色溶液中一定有 、 、 和
D.实验③发生反应的离子方程式只有:
6.(2025高三上·黑龙江哈尔滨·模拟预测)常温下,在下列给定条件的各溶液中,一定能大量共存的离子
组是
A.电解 溶液后的溶液中: 、 、 、
B.使甲基橙呈红色的溶液中: 、 、 、
C.澄清透明溶液中: 、 、 、
D.由水电离产生的 的溶液: 、 、 、
7.(2025高三上·福建泉州·模拟预测)常温下,下列各组粒子在指定溶液中一定能大量共存的是
A.澄清透明溶液:
B.由水电离出 为 的溶液:
C.使甲基橙变红色的溶液:
D.通入足量 的溶液:
8.(2025高三上·浙江·模拟预测)下列说法正确的是
A.能使酚酞变红的溶液中可大量存在 、 、 、
B.由水电离的 的溶液中能大量存在 、 、 、
C. 溶液中不能大量共存 、 、 、
D.某卤代烃中滴加 的乙醇溶液后加热,滴入稀硝酸酸化后再滴入几滴 溶液无白色沉
淀,则该卤代烃中不含
9.(2024·辽宁沈阳·模拟预测)某无色溶液Y可能含有中的几种离子,溶液中阳离子浓度相同。为了确定其组成,某同学进行了如下实验(假设气体均全部逸出,
忽略 的分解)。下列说法不正确的是
A.溶液Y中一定不存在
B.溶液Y中一定含有 ,且
C.溶液Y中肯定存在
D.溶液Y中可能存在 ,为确定其是否存在,可取溶液1通过焰色试验验证
10.(2024·安徽·一模)常温下,下列各组离子在指定溶液中能大量共存的是
A.与铝反应产生 的溶液中: 、 、 、
B.新制氯水中: 、 、 、
C.使酚酞变红的溶液中: 、 、 、
D.加入 固体的溶液中: 、 、 、
11.(2024·四川德阳·一模) (铁铵矾)是分析化学中的重要试剂。下列有关1mol·L-1
溶液的叙述正确的是
A.该溶液中, 、 和 可以大量共存
B.该溶液与0.5mol·L-1 溶液相比,
C.可分别用NaOH浓溶液、KSCN溶液检验该溶液中的 和
D.向该溶液滴入 溶液恰好使 完全沉淀的离子方程式为:
12.(2024·全国·模拟预测)常温下,下列各组离子在指定溶液中能够大量共存的是
A.氨水中: 、 、 、 B.HClO溶液中: 、 、 、
C. 溶液中: 、 、 、 D. 溶液中: 、 、 、13.(2024·江苏南京·模拟预测)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液中:Fe3+、Mg2+、 、Cl-
B. =106的溶液中: 、K+、 、
C.碱性溶液中:ClO-、S2-、 、Na+
D.与Al反应能放出H 的溶液中:Fe2+、K+、 、
2
14.(2025·四川·一模)常温常压下,下列指定条件的各组离子一定能大量共存的是
A.透明的溶液中: 、 、 、
B.在酒精中: 、 、 、
C.溶有 的水溶液中: 、 、 、
D.由水电离出 为 的溶液中: 、 、 、
15.(2025·宁夏陕西·模拟预测)下列名组离子在水溶液中可以大量共存的是
A. B.
C. D.
16.(2025高一上·湖南怀化·模拟预测)某无色溶液可能含有等物质的量的下列某些离子中的一种或几
种: 、 、 、 、 、 、 ,取溶液分别进行如下实验:
①加入 酸化的 溶液产生白色沉淀;
②加入锌粉,有气泡生成;
③加入适量 粉末产生白色沉淀。
下列说法正确的是
A.该无色溶液中一定没有 ,可能有
B.由①、②可知该溶液可能有
C.该无色溶液中一定有 、 、 和
D.实验③发生反应的离子方程式只有:
17.(2025高三上·天津·模拟预测)某无色溶液中可能含有 、 、 、 ,加入铝粉后,只产生 ,探究该无色溶液中离子大量共存情况。
(1)加入铝粉产生 ,说明铝具有 (填“氧化性”或“还原性”)。
(2)某同学分析:若 大量存在,则 就不能大量存在。设计实验如下:
i.实验初始,未见明显现象
ii.过一会儿,出现气泡,液面上方呈浅棕色
iii.试管变热,溶液沸腾
①盐酸溶解 薄膜的离子方程式是: 。
②根据现象ii,推测溶液中产生了NO,为进一步确认,进行实验:
实验1 将湿润KI-淀粉试纸置于空气中 未变蓝
实验2 用湿润KI-淀粉试纸检验浅棕色气体试纸 变蓝
a.浅棕色气体是 (化学式)
写出生成浅棕色气体的化学方程式 。
b.实验1的目的是 。
(3)再假设:若 大量存在, 也可能不能大量存在。重新设计实验:
i.实验初始,未见明显现象
ii.过一会儿,出现气泡,有刺激性气味
对“刺激性气味”气体,进行如下实验:用湿润KI-淀粉试纸检验,未变蓝;用蘸有浓盐酸的玻璃棒接近
该气体出现白烟。该气体是 (化学式);产生该气体的离子方程式 。
(4)实验结果证实: 有一定的氧化性,能氧化铝单质,产生含氮化合物(填序号)。
a.只在酸性环境中 b.只在碱性环境中 c.在酸性或碱性环境中均
结论:该无色溶液一定能大量存在的是 (离子符号)。
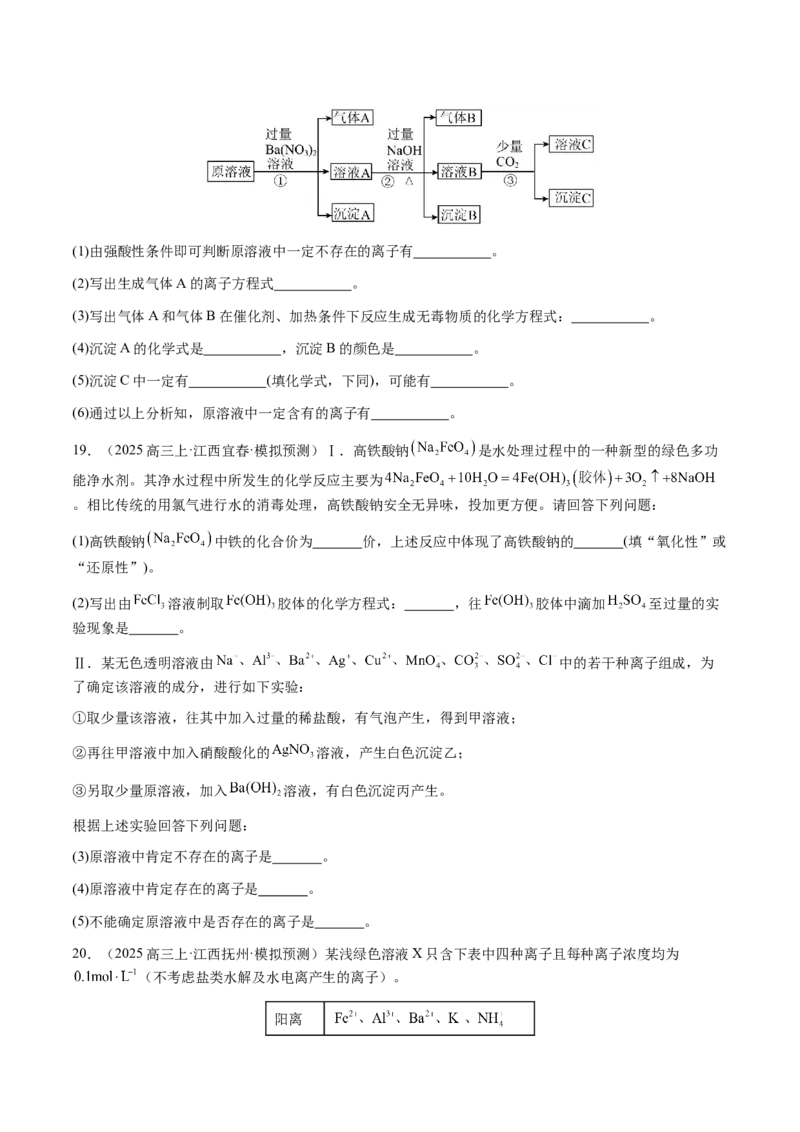
18.(2025高三上·辽宁·模拟预测)某强酸性稀溶液中可能存在
中的若干种,现取适量该溶液进行如下实验:(1)由强酸性条件即可判断原溶液中一定不存在的离子有 。
(2)写出生成气体A的离子方程式 。
(3)写出气体A和气体B在催化剂、加热条件下反应生成无毒物质的化学方程式: 。
(4)沉淀A的化学式是 ,沉淀B的颜色是 。
(5)沉淀C中一定有 (填化学式,下同),可能有 。
(6)通过以上分析知,原溶液中一定含有的离子有 。
19.(2025高三上·江西宜春·模拟预测)Ⅰ.高铁酸钠 是水处理过程中的一种新型的绿色多功
能净水剂。其净水过程中所发生的化学反应主要为
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠 中铁的化合价为 价,上述反应中体现了高铁酸钠的 (填“氧化性”或
“还原性”)。
(2)写出由 溶液制取 胶体的化学方程式: ,往 胶体中滴加 至过量的实
验现象是 。
Ⅱ.某无色透明溶液由 中的若干种离子组成,为
了确定该溶液的成分,进行如下实验:
①取少量该溶液,往其中加入过量的稀盐酸,有气泡产生,得到甲溶液;
②再往甲溶液中加入硝酸酸化的 溶液,产生白色沉淀乙;
③另取少量原溶液,加入 溶液,有白色沉淀丙产生。
根据上述实验回答下列问题:
(3)原溶液中肯定不存在的离子是 。
(4)原溶液中肯定存在的离子是 。
(5)不能确定原溶液中是否存在的离子是 。
20.(2025高三上·江西抚州·模拟预测)某浅绿色溶液X只含下表中四种离子且每种离子浓度均为
(不考虑盐类水解及水电离产生的离子)。
阳离子
阴离
子
为了确定X组成,进行如下实验:
序号 操作及现象
Ⅰ 取适量溶液X于试管①中,加入足量NaOH溶液,共热,实验过程中无刺激性气味的气体产生
Ⅱ 取适量溶液X于试管②中,滴加足量的稀硫酸,产生无色气泡
Ⅲ 实验Ⅱ结束后,继续向试管②中滴加 溶液,产生白色沉淀
回答下列问题:
(1)根据溶液颜色及实验Ⅰ现象可以排除 种离子存在。
(2)实验Ⅱ中产生无色气泡的离子方程式为 。
(3)根据实验Ⅲ现象, (填“能”或“不能”)确定溶液X中有 存在,理由是 。
(4)根据实验可知,X中含有的四种离子为 (填离子符号)。
(5) 容易转化成 ,其主要原因是 (从结构角度分析);请设计实验检验 溶液中的
是否被氧化为 : (写出操作、现象和结论)。