文档内容
专题 04 氧化还原反应
目 录
01 氧化还原反应基本概念
02 氧化还原反应的基本规律及应用
03 氧化还原反应方程式的书写与配平
01 氧化还原反应基本概念
1.下列物质的应用涉及氧化还原反应的是( )
A.利用氢氟酸刻蚀玻璃 B.利用活性炭由红糖制备白糖
C.煅烧石灰石制备生石灰 D.应用漂白粉对环境进行消杀
2.(2023·湖南省高三联考)《本草纲目》中记载:“(火药)乃焰硝(KNO)、硫黄、杉木炭所合,以为烽
3
燧铳机诸药者。”火药燃烧爆炸时发生的反应为S+2KNO +3C KS+N↑+3CO ↑。下列有关说法错误的
3 2 2 2
是( )
A.氧化产物与还原产物的物质的量之比为3:2
B.反应每转移6mol电子,则能生成11.2LN
2
C.该反应过程有极性键、非极性键和离子键的形成
D.该反应中分别被S和硝酸钾氧化的碳原子数之比为1:5
3.(2023·重庆市渝中高三调研)氧和氟都是非金属性很强的元素,可形成一系列性质活泼的氟氧化合
物,如:OF 、OF、OF、OF、OF、OF。其中OF 可以发生反应:HS+4OF═SF +2HF+4O,关于
2 2 2 3 2 4 2 5 2 6 2 2 2 2 2 2 6 2
此反应,下列说法正确的是( )
A.氧气是氧化产物
B.OF 既是氧化剂又是还原剂
2 2
C.若生成2.24LHF,则转移0.4mol电子
D.氧化剂与还原剂的物质的量之比为4∶14.(2024·浙江省七彩阳光新高考研究联盟三联考)关于反应3SiO+6C+2N Si N+6CO,下列说法
2 2 3 4
正确的是( )
A.SiO 既不是氧化剂,也不是还原剂
2
B.生成33.6L CO,转移3N 电子
A
C.Si N 是氧化产物
3 4
D.6g C中含有的共价键数目为一定为N
A
5.(2023·浙江省Z20名校联盟高三第三次联考)汽车发生剧烈碰撞时,安全气囊中迅速发生反应:
10NaN +2KNO =K O+5Na O+16N↑。下列说法正确的是
3 3 2 2 2
A.该反应中KNO 是还原剂
3
B.氧化产物与还原产物的物质的量之比为15∶1
C.若设计成原电池,KNO 在负极上反应
3
D.每转移1mol e-,可生成2.24LN
2
6.(2023·浙江省东阳市高三5月模拟考试)关于反应3Cu S+16H++4NO-=6Cu2++4NO↑+3S↓+8H O,下
2 3 2
列说法不正确的是( )
A.该反应体现了HNO 的强氧化性和酸性
3
B.反应生成22.4L(标况下)NO气体时转移3mol电子
C.该反应中氧化产物只有S
D.若设计成原电池,Cu S作为负极材料
2
7.(2023·浙江省临海、新昌两地高三适应性考试5月模考)关于反应
2NaNH +N O=NaN +NaOH+NH ,下列说法正确的是( )
2 2 3 3
A.NaN 溶液通入CO 可以得到HN (酸性与醋酸相当)
3 2 3
B.氧化剂和还原剂的物质的量之比为2:1
C.NaN 既是还原产物又是氧化产物
3
D.生成1molNaN ,共转移4mol电子
3
02 氧化还原反应的基本规律及应用
1. 现有下列三个氧化还原反应:
①2FeCl +2KI===2FeCl +2KCl+I
3 2 2
②2FeCl +Cl===2FeCl
2 2 3
③2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
若某溶液中含有Fe2+、Cl-和I-,要除去I-而不氧化Fe2+和Cl-,可以加入的试剂是( )
A.Cl B.KMnO C.FeCl D.HCl
2 4 3
2.将SO 气体不断通人Fe (SO ) 溶液中,溶液颜色逐渐变浅,最后至浅绿色,然后往溶液中滴加
2 2 4 3
KCr O 溶液,溶液又变成棕黄色(还原产物为Cr3+),则下列有关说法错误的是( )
2 2 7
A.氧化性:Cr O2->Fe3+>SO
2 7 2B.标准状况下,若有6.72LSO 参加反应,则最终能消耗0.1molKCr O
2 2 2 7
C.通入SO 时反应的离子方程式为:SO +2Fe3++2H O= SO 2-+2Fe2++4H+
2 2 2 4
D.随着上述操作的进行,溶液的酸性越来越强
3.(2024·福建福州八县协作校高三期中)KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,
3
该方法第一步反应为6I +11KClO + 3H O 6KH(IO) + 5KCl + 3Cl ↑。下列说法错误的是( )
2 3 2 3 2 2
A.产生22.4L(标准状况) Cl 时,反应中转移20mol e-
2
B.可用石灰乳吸收反应产生的Cl 制备漂白粉
2
C.反应中氧化剂和还原剂的物质的量之比为6:11
D.可用酸化的淀粉碘化钾试纸检验Cl 的存在
2
4.(2023·天津高三模拟)汽车剧烈碰撞时,安全气囊中发生反应10NaN +2KNO =K O+5Na O+16N↑。
3 3 2 2 2
若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
A.生成42.0LN (标准状况) B.有0.25molKNO 被氧化
2 3
C.转移电子的物质的量为1.25mol D.被还原的N原子的物质的量为3.75mol
5.KMnO 是常用的消毒剂和氧化剂。已知相关化学反应如下:
4
①向含KOH的KMnO 溶液中通入Cl 制备KMnO :2KMnO +Cl=2KMnO +2KCl
2 4 2 4 2 4 2 4
②实验室制Cl:2KMnO +16HCl=2KCl+2MnCl +5Cl↑+8H O
2 4 2 2 2
③测定废水中Mn2+:2MnO -+3Mn2++2H O=5MnO ↓+4H+,下列有关说法错误的是( )
4 2 2
A.MnO -+的氧化性一定比Cl 的氧化性强
4 2
B.物质氧化性与酸碱性有关,pH越低,氧化性越强
C.③中生成2mol还原产物时转移6mol电子
D.若转移电子数相等,则①中KMnO 与②中KMnO 的质量之比为5∶1
4 4
6.高铁酸钾是一种高效多功能的新型非氯绿色消毒剂,主要用于饮用水处理。工业上制备KFeO 的
2 4
方法是向KOH溶液中通入氯气,然后再加入Fe(NO ) 溶液:①Cl+KOH→KCl+KC1O+KClO +H O(未配
3 3 2 3 2
平);②2Fe(NO )+3KC1O+10KOH=2K FeO+6KNO +3KCl+5H O。下列说法不正确的是( )
3 3 2 4 3 2
A.KFeO 在杀菌消毒过程中还可以净水
2 4
B.反应①中每消耗2molKOH,吸收标准状况下22.4LCl (忽略Cl 和水的反应)
2 2
C.若反应①中n(ClO-):n(ClO -)=5:1,则氧化剂与还原剂的物质的量之比为3:5
3
D.若反应①的氧化产物只有KC1O,则得到0.2molKFeO 时最少消耗0.3molC1
2 4 2
7.(2023·河南省重点高中高三联考)白磷(P )有毒,实验时若皮肤接触到白磷,应立即用稀CuSO 溶液
4 4
清洗,发生两个反应:
反应①为P 和CuSO 反应生成Cu、HPO 和HSO ;
4 4 3 4 2 4
反应②为11P+60CuSO+96H O=20Cu P+24HPO +60H SO 。
4 4 2 3 3 4 2 4
下列说法正确的是( )
A.在反应①和②中,P 只作还原剂
4
B.反应①中氧化产物与还原产物的物质的量之比为5∶2C.若P 反应完全且转化为HPO 的转化率是80%,理论上反应①和②消耗P 的物质的量之比为
4 3 4 4
14∶11
D.用稀CuSO 溶液清洗后,应再使用NaOH溶液清洗
4
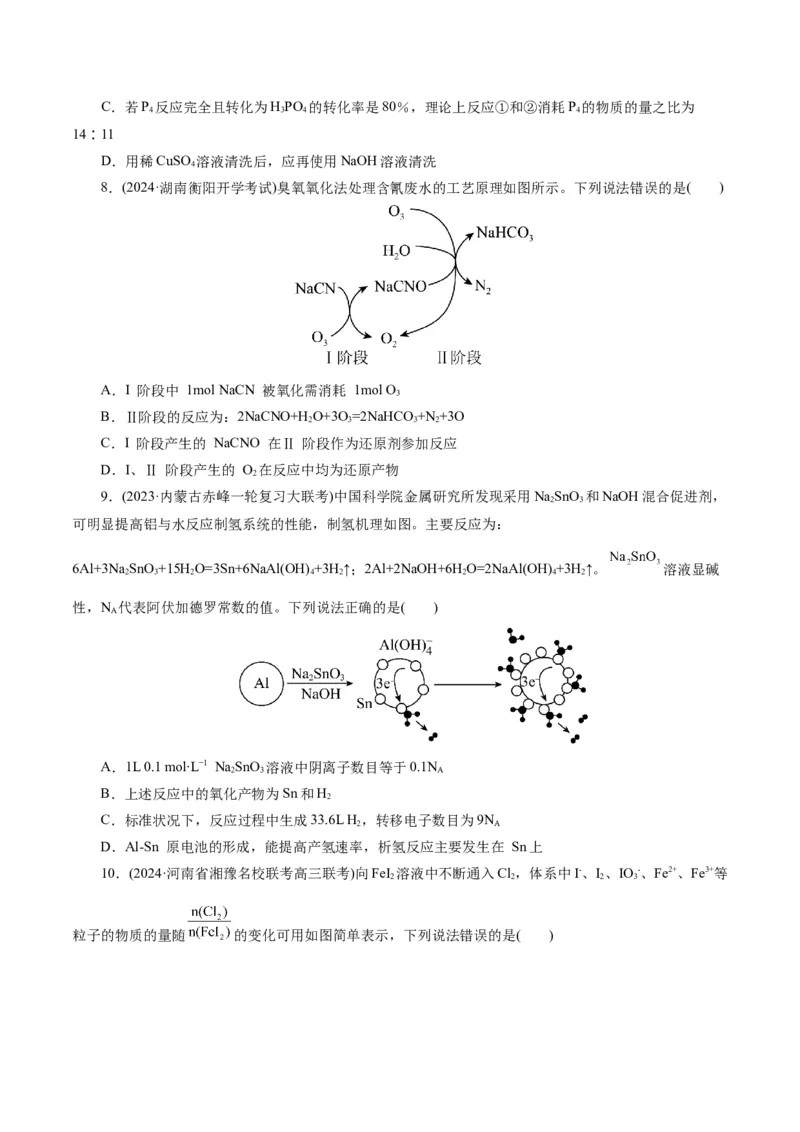
8.(2024·湖南衡阳开学考试)臭氧氧化法处理含氰废水的工艺原理如图所示。下列说法错误的是( )
A.I 阶段中 1mol NaCN 被氧化需消耗 1mol O
3
B.Ⅱ阶段的反应为:2NaCNO+H O+3O=2NaHCO+N +3O
2 3 3 2
C.I 阶段产生的 NaCNO 在Ⅱ 阶段作为还原剂参加反应
D.I、Ⅱ 阶段产生的 O 在反应中均为还原产物
2
9.(2023·内蒙古赤峰一轮复习大联考)中国科学院金属研究所发现采用NaSnO 和NaOH混合促进剂,
2 3
可明显提高铝与水反应制氢系统的性能,制氢机理如图。主要反应为:
6Al+3Na SnO +15H O=3Sn+6NaAl(OH) +3H ↑;2Al+2NaOH+6H O=2NaAl(OH) +3H ↑。 溶液显碱
2 3 2 4 2 2 4 2
性,N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.1L 0.1 mol∙L−1 Na SnO 溶液中阴离子数目等于0.1N
2 3 A
B.上述反应中的氧化产物为Sn和H
2
C.标准状况下,反应过程中生成33.6L H ,转移电子数目为9N
2 A
D.Al-Sn 原电池的形成,能提高产氢速率,析氢反应主要发生在 Sn上
10.(2024·河南省湘豫名校联考高三联考)向FeI 溶液中不断通入Cl,体系中I-、I、IO -、Fe2+、Fe3+等
2 2 2 3
粒子的物质的量随 的变化可用如图简单表示,下列说法错误的是( )A.A线表示n(I-)的变化
B.D线对应的反应的离子方程式为2Fe2++Cl=2Cl-+2Fe3+
2
C.形成IO 时,反应的离子方程式为5Cl+I +12OH-=2IO +6H O+10Cl-
2 2 2
D.当 =1.2时,反应的离子方程式为2Fe2++10I-+6Cl=5I +2Fe3++12Cl-
2 2
11.(2024·重庆高三调研考试)工业生产中除去电石浆(主要含CaO)中的 并制取硫酸盐的流程如下图
所示。下列说法正确的是( )
A.过程Ⅰ中被氧化的微粒为MnO 2-
3
B.在酸性条件下,氧化性: O>SO2->MnO 2-
2 2 3 3
C.经过过程Ⅱ后,溶液的碱性增强
D.若消耗56LO,理论上除去S2-的质量为16g
2
03 氧化还原反应方程式的书写与配平
1.NaNO 是一种食品添加剂,它能致癌。酸性KMnO 溶液与NaNO 反应的化学方程式是:MnO+
2 4 2
NO+→Mn2++NO+HO。下列叙述中正确的是( )
2
A.该反应中NO被还原 B.反应过程中溶液的pH减小
C.生成1 mol NaNO 需消耗0.4 mol KMnO D.中的粒子是OH-
3 4
2.(2023·浙江省诸暨市高三适应性考试)关于反应CHCHOH+Cr O2-+H++H O→CH COOH+ Cr(H O) 3+
3 2 2 7 2 3 2 6
(未配平),下列说法不正确的是( )
A.生成1mol CHCOOH,转移6mol电子 B.CHCOOH是氧化产物
3 3
C.该反应类型属于氧化还原反应 D.Cr(H O) 3+的配体中形成配位键的原子是O
2 6
3.ClO-可用于处理含CN-的废水,处理过程中体系存在ClO-、CN-、N、Cl-、HCO -、HO六种物质。
2 3 2
下列有关说法正确的是( )
A.ClO-是氧化剂,N 是氧化产物之一
2
B.反应配平后氧化剂与还原剂的化学计量数之比为3:2
C.若生成标准状况下2.24 L N ,则转移电子0.2 mol
2D.含CN-的废水也可用Cr O2-处理
2 7
4.已知下列实验事实:① Cr O 固体既能溶于 KOH 溶液得到 KCrO 溶液,又能溶于硫酸得到
2 3 2
Cr (SO ) 溶液;②将KCr O 溶液滴加到淀粉KI溶液中,溶液变蓝;③向KCrO 溶液中滴加HO 溶液,再
2 4 3 2 2 7 2 2 2
酸化,可得KCr O 溶液。下列判断不正确的是( )
2 2 7
A.化合物KCrO 中Cr为+3价 B.实验①证明Cr O 是两性氧化物
2 2 3
C.实验②证明氧化性:Cr O>I D.实验③证明HO 既有氧化性又有还原性
2 2 2 2
5.用酸性KMnO 溶液处理硫化亚铜(Cu S)和二硫化亚铁(FeS )的混合物时,发生反应I:MnO -+
4 2 2 4
Cu S+H+→Cu2++SO2-+Mn2++H O (未配平)和反应II:MnO -+ FeS +H+→Fe3++SO2-+Mn2++H O(未配平)。下列
2 4 2 4 2 4 2
说法正确的是( )
A.反应I中Cu S既是氧化剂又是还原剂
2
B.反应I中每生成1molSO 2-,转移电子的物质的量为10mol
4
C.反应II中氧化剂与还原剂的物质的量之比为
D.若反应I和反应II中消耗的KMnO 的物质的量相同,则反应I和反应II中消耗的还原剂的物质的
4
量之比为
6.(2023·辽宁省朝阳市一模)已知反应:aFeSO+ bNa O= cNa FeO+2Na O+ dNa SO +eO ↑,a=2。下
4 2 2 2 4 2 2 4 2
列关于该反应的说法错误的是( )
A.NaFeO 可以对水体进行杀菌消毒、净化 B.NaO 在该反应中既是氧化剂又是还原剂
2 4 2 2
C.3a=b D.每生成1mol Na FeO,转移4mol电子
2 4
7.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO -+4H++3e-
3
=NO↑+2HO,已知KMnO 、NaCO、FeO、Fe (SO ) 四种物质中的一种物质能使上述还原过程发生。
2 4 2 3 2 4 3
(1)写出并配平该氧化还原反应的方程式: 。
(2)反应中硝酸体现了 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
8.已知高锰酸钾(硫酸酸化)溶液和草酸(H C O)溶液可以发生氧化还原反应。请回答下列问题:
2 2 4
(1)该反应中的还原剂是________(填化学式)。
(2)写出该反应的化学方程式:____________________。
(3)反应转移了0.4 mol电子,则参加反应的HSO 的物质的量为________mol。
2 4
(4)高锰酸钾(硫酸酸化)溶液和草酸溶液的反应可用于测定血钙的含量。方法是取2 mL血液用蒸馏水稀
释后,向其中加入足量草酸铵晶体[化学式为(NH )C O],反应生成CaC O 沉淀,将沉淀用稀硫酸溶解后
4 2 2 4 2 4
得到HC O,再用KMnO 溶液滴定。
2 2 4 4
①稀硫酸溶解CaC O 沉淀的化学方程式是___________________________。
2 4
②用KMnO 溶液滴定HC O 时,判断滴定终点的方法是_______________________。
4 2 2 4
③若消耗了1.0×10-4 mol·L-1的KMnO 溶液20.00 mL,则100 mL该血液中含钙________ g。
4