文档内容
专题 04 氧化还原反应
2020年高考真题
加热
1.【2020年7月浙江选考】反应MnO +4HCl(浓) ¿MnCl +Cl ↑+2H O 中,氧化产物与还原产物的物
2 2 2 2
¿
质的量之比是( )
A.1:2 B.1:1 C.2:1 D.4:1
2.【2020山东(新高考)】下列叙述不涉及氧化还原反应的是
A.谷物发酵酿造食醋 B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒 D.大气中NO 参与酸雨形成
2
2020届高考模拟试题
3.(浙江省金华十校2020届高三4月模拟考试)下列变化中,气体被还原的是
A.水蒸气使 CuSO 固体变蓝 B.氯气使浅绿色 FeC1 溶液变黄
4 2
C.H 使灼热CuO 固体变红 D.氨气使A1Cl 溶液产生白色沉淀
2 3
4.(北京市顺义区2020届高三第一次模拟)常温下,向 溶液中滴加少量 溶液,反应原理
如图所示。关于该反应过程的说法正确的是
A.该反应过程中, 是 是 B.当有 生成时,转移 电子
C.在 分解过程中,溶液的 逐渐降低 D. 的氧化性比 强,还原性比 弱
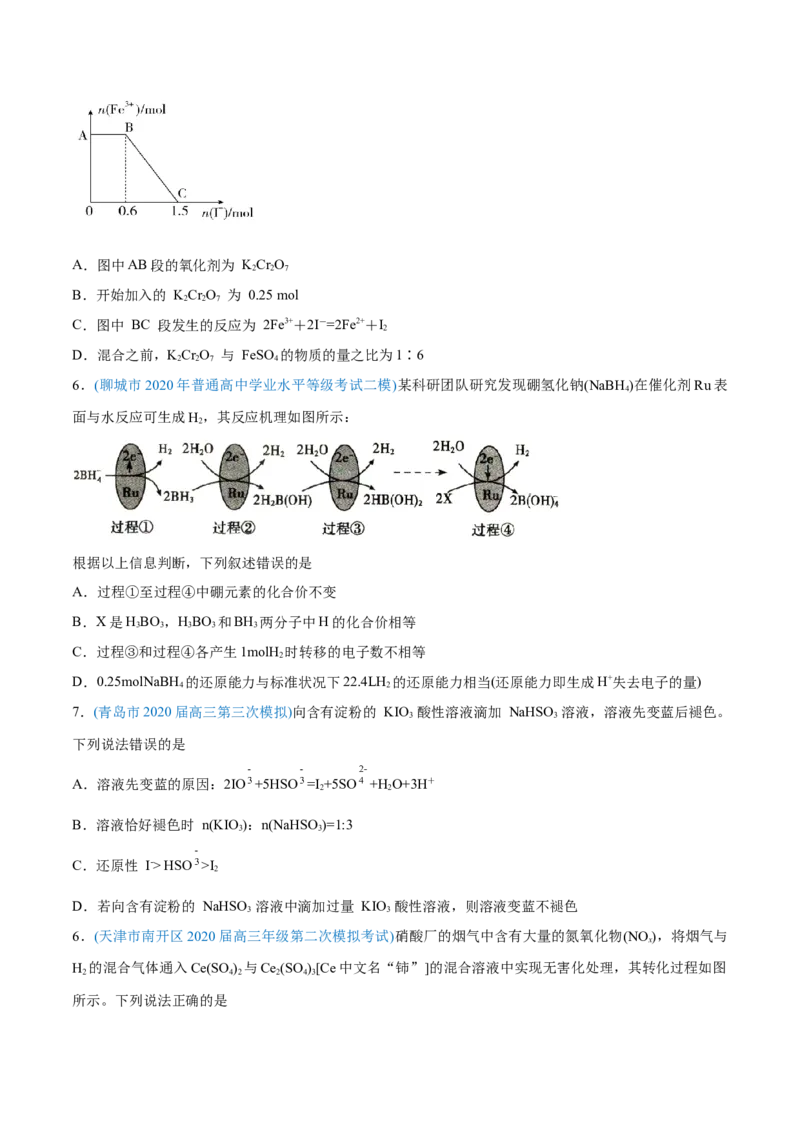
5.(2020届济南市实验中学高三下学期2月份阶段检测)已知酸性 KCr O 溶液可与 FeSO 溶液反应生成
2 2 7 4
Fe3+和 Cr3+。现将硫酸酸化的 KCr O 溶液与 FeSO 溶液混合,充分反应后再向所得溶液中加入KI溶
2 2 7 4
液,混合溶液中Fe3+的物质的量随加入的 KI 的物质的量的变化关系如图所示,下列不正确的是A.图中AB段的氧化剂为 KCr O
2 2 7
B.开始加入的 KCr O 为 0.25 mol
2 2 7
C.图中 BC 段发生的反应为 2Fe3++2I-=2Fe2++I
2
D.混合之前,KCr O 与 FeSO 的物质的量之比为1∶6
2 2 7 4
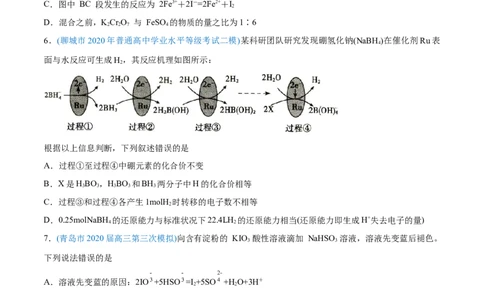
6.(聊城市2020年普通高中学业水平等级考试二模)某科研团队研究发现硼氢化钠(NaBH )在催化剂Ru表
4
面与水反应可生成H,其反应机理如图所示:
2
根据以上信息判断,下列叙述错误的是
A.过程①至过程④中硼元素的化合价不变
B.X是HBO,HBO 和BH 两分子中H的化合价相等
3 3 3 3 3
C.过程③和过程④各产生1molH 时转移的电子数不相等
2
D.0.25molNaBH 的还原能力与标准状况下22.4LH 的还原能力相当(还原能力即生成H+失去电子的量)
4 2
7.(青岛市2020届高三第三次模拟)向含有淀粉的 KIO 酸性溶液滴加 NaHSO 溶液,溶液先变蓝后褪色。
3 3
下列说法错误的是
A.溶液先变蓝的原因:2IO +5HSO =I +5SO +H O+3H+
2 2
B.溶液恰好褪色时 n(KIO ):n(NaHSO)=1:3
3 3
C.还原性 I-> HSO >I
2
D.若向含有淀粉的 NaHSO 溶液中滴加过量 KIO 酸性溶液,则溶液变蓝不褪色
3 3
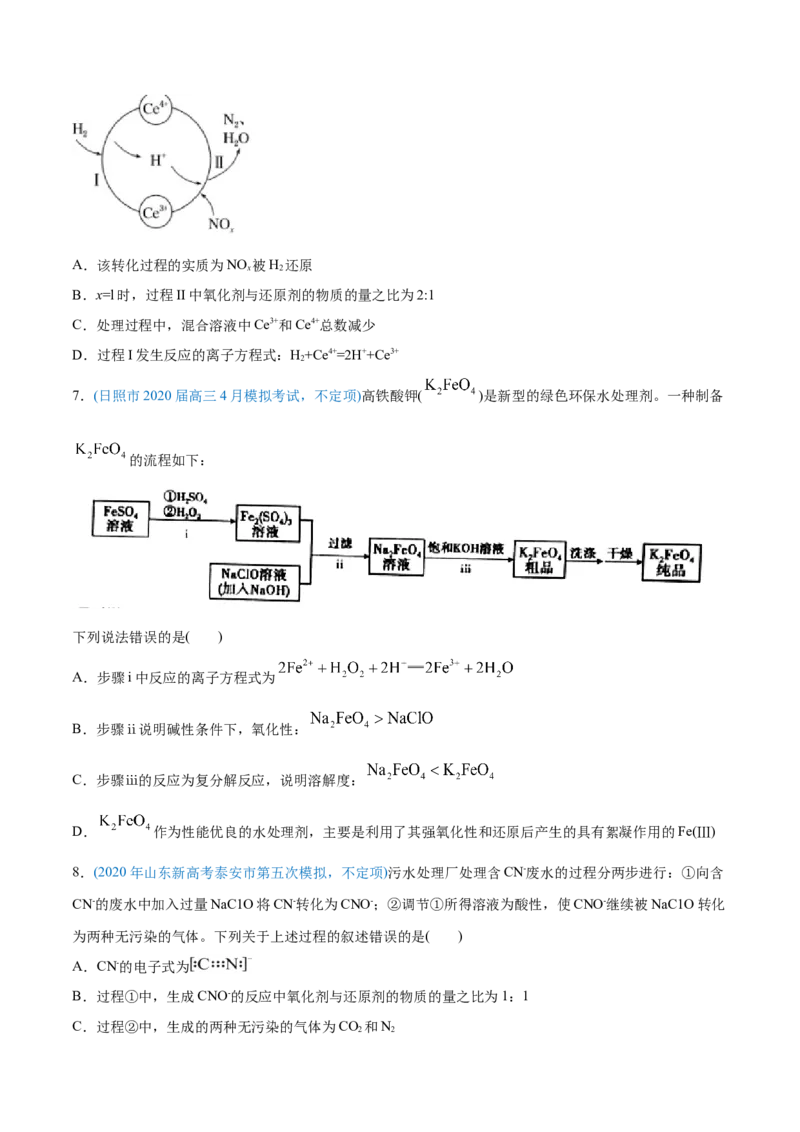
6.(天津市南开区2020届高三年级第二次模拟考试)硝酸厂的烟气中含有大量的氮氧化物(NO),将烟气与
x
H 的混合气体通入Ce(SO) 与Ce (SO )[Ce中文名“铈”]的混合溶液中实现无害化处理,其转化过程如图
2 4 2 2 4 3
所示。下列说法正确的是A.该转化过程的实质为NO 被H 还原
x 2
B.x=l时,过程II中氧化剂与还原剂的物质的量之比为2:1
C.处理过程中,混合溶液中Ce3+和Ce4+总数减少
D.过程I发生反应的离子方程式:H+Ce4+=2H++Ce3+
2
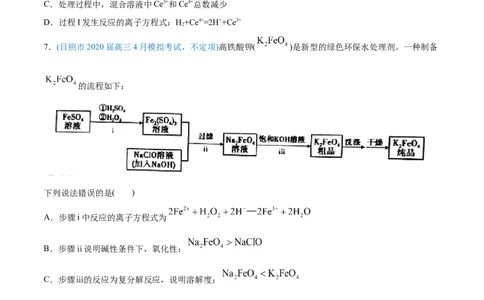
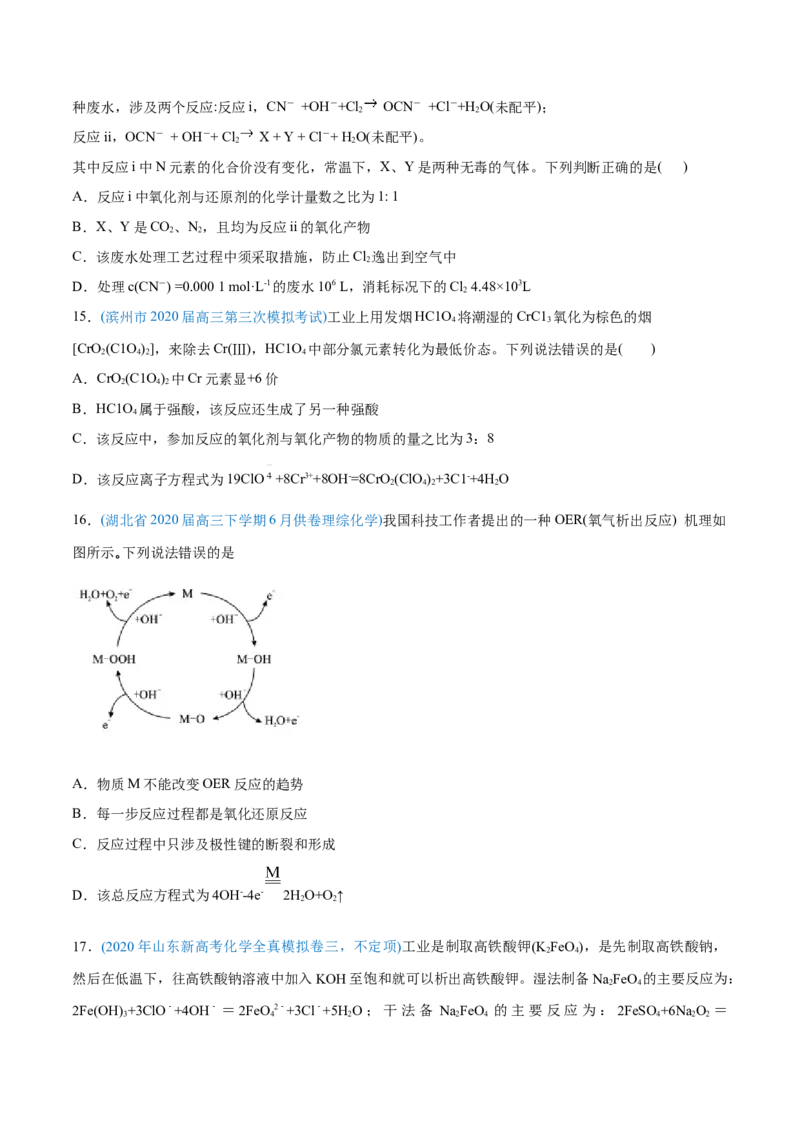
7.(日照市2020届高三4月模拟考试,不定项)高铁酸钾( )是新型的绿色环保水处理剂。一种制备
的流程如下:
下列说法错误的是( )
A.步骤i中反应的离子方程式为
B.步骤ⅱ说明碱性条件下,氧化性:
C.步骤ⅲ的反应为复分解反应,说明溶解度:
D. 作为性能优良的水处理剂,主要是利用了其强氧化性和还原后产生的具有絮凝作用的Fe(Ⅲ)
8.(2020年山东新高考泰安市第五次模拟,不定项)污水处理厂处理含CN-废水的过程分两步进行:①向含
CN-的废水中加入过量NaC1O将CN-转化为CNO-;②调节①所得溶液为酸性,使CNO-继续被NaC1O转化
为两种无污染的气体。下列关于上述过程的叙述错误的是( )
A.CN-的电子式为
B.过程①中,生成CNO-的反应中氧化剂与还原剂的物质的量之比为1:1
C.过程②中,生成的两种无污染的气体为CO 和N
2 2D.氧化性:CNO->C1O-
9.(2020年山东新高考烟台市适应性练习一,不定项)《环境科学》刊发了我国科研部门采用零价铁活化过
硫酸钠(Na SO,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示(SO
2 2 8
·、·OH表示自由基)。设阿伏加德罗常数的值为N 。下列叙述错误的是( )
A
A.过硫酸钠中-2价氧与-1价氧的个数比为3:1
B.若56gFe参加反应,共有1.5N 个SO2−被还原
A 2 8
C.碱性条件下硫酸根自由基发生反应的方程式为SO -·+OH-=SO2-+·OH
4 4
D.pH越小,越有利于去除废水中的正五价砷
10.(2020年山东新高考烟台市适应性练习一,不定项)用KMnO 酸性溶液处理硫化亚铜(Cu S)和二硫化亚
4 2
铁(FeS )的混合物时,发生的反应Ⅰ: +Cu S+H+→Cu2++ +Mn2++H O(未配平)和反应Ⅱ:
2 2 2
+FeS +H+→Fe3++ +Mn2++H O(未配平)。下列说法正确的是( )
2 2
A.反应Ⅰ中Cu S既是氧化剂又是还原剂
2
B.反应Ⅰ中每生成1mol ,转移电子的物质的量为10mol
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为1:3
D.若反应Ⅰ和反应Ⅱ中消耗的KMnO 的物质的量相同,则反应Ⅰ和反应Ⅱ中消耗的还原剂的物质的量之
4
比为3:2
11.(北京市海淀区2020届高三二模)金属铬常用于提升特种合金的性能。工业上以铬铁矿(主要成份为
FeO·Cr O,含有少量Al O)为原料制备金属铬的流程如下图。下列说法不正确的是( )
2 3 2 3A.①中需持续吹入空气作氧化剂 B.②中需加入过量稀硫酸
C.③中发生了置换反应 D.溶液A为橙色
12.(山东省实验中学2020届高三下学期打靶模拟考试)高锰酸钾(KMnO)是一种常用的氧化剂。不同条件
4
下高锰酸钾可发生如下反应: +5e-+8H+→Mn2++4H O; +3e-+2H O→MnO +4OH-; +e
2 2 2
-→ 。高锰酸钾溶液与硫化亚铁有如下反应:
FeS+KMnO +H SO →KSO +MnSO +Fe (SO )+S+H O(未配平)。下列有关说法正确的是
4 2 4 2 4 4 2 4 3 2
A.由上面的反应可知,高锰酸根离子( )反应后的产物与溶液的酸碱性有关
B.高锰酸钾溶液可代替二氧化锰用来制取Cl,氧化剂和还原剂物质的量之比为1:8
2
C.在高锰酸钾溶液与硫化亚铁的反应中,反应前后固体的质量减少了2.8g,则硫元素与高锰酸钾之间转
移的电子数为0.15N
A
D.高锰酸钾溶液也可与双氧水发生反应,其中双氧水是氧化剂
13.(日照市2020届高三 4月模拟考试) 是一种红色固体,常用作示温涂料。制备反应为:
。下列说法正确的是( )
A.上述反应的产物 中,Hg的化合价为
B.上述反应中Hg元素与Cu元素均被还原
C.上述反应中生成 时,转移的电子数为
D.由以上信息可推知:可发生反应
14.(山东师范大学附属中学2020届高三6月份模拟,不定项)氰化物是剧毒物质,传统生产工艺的电镀废
水中含一定浓度的CN-,无害化排放时必须对这种废水进行处理。 可采用碱性条件下的Cl 氧化法处理这
2种废水,涉及两个反应:反应i,CN- +OH-+Cl OCN- +Cl-+H O(未配平);
2 2
反应ii,OCN- + OH-+ Cl X + Y + Cl-+ H O(未配平)。
2 2
其中反应i中N元素的化合价没有变化,常温下,X、Y是两种无毒的气体。下列判断正确的是( )
A.反应i中氧化剂与还原剂的化学计量数之比为1: 1
B.X、Y是CO、N,且均为反应ii的氧化产物
2 2
C.该废水处理工艺过程中须采取措施,防止Cl 逸出到空气中
2
D.处理c(CN-) =0.000 1 mol·L-1的废水106 L,消耗标况下的Cl 4.48×103L
2
15.(滨州市2020届高三第三次模拟考试)工业上用发烟HC1O 将潮湿的CrC1 氧化为棕色的烟
4 3
[CrO (C1O)],来除去Cr(Ⅲ),HC1O 中部分氯元素转化为最低价态。下列说法错误的是( )
2 4 2 4
A.CrO(C1O) 中Cr元素显+6价
2 4 2
B.HC1O 属于强酸,该反应还生成了另一种强酸
4
C.该反应中,参加反应的氧化剂与氧化产物的物质的量之比为3:8
D.该反应离子方程式为19ClO +8Cr3++8OH-=8CrO (ClO )+3C1-+4H O
2 4 2 2
16.(湖北省2020届高三下学期6月供卷理综化学)我国科技工作者提出的一种OER(氧气析出反应) 机理如
图所示。下列说法错误的是
A.物质M不能改变OER反应的趋势
B.每一步反应过程都是氧化还原反应
C.反应过程中只涉及极性键的断裂和形成
D.该总反应方程式为4OH--4e- 2HO+O↑
2 2
17.(2020年山东新高考化学全真模拟卷三,不定项)工业是制取高铁酸钾(K FeO),是先制取高铁酸钠,
2 4
然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。湿法制备NaFeO 的主要反应为:
2 4
2Fe(OH) +3ClO﹣+4OH﹣=2FeO2﹣+3Cl﹣+5H O;干法备 NaFeO 的主要反应为:2FeSO +6Na O =
3 4 2 2 4 4 2 22NaFeO+2Na SO +O ↑。下列有关说法不正确的是( )
2 4 2 4 2
A.湿法和干法制备中,生成1molNa FeO 转移电子数目相同
2 4
B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小
C.干法制备的主要反应中NaO 是氧化剂
2 2
D.KFeO 处理水时,既能杀菌消毒,生成的Fe(OH) 胶体还能吸附水中的悬浮杂质
2 4 3
18.(日照市2020届高三校际联合考试化学试题,不定项)由一种阳离子与两种酸根阴离子组成的盐称为混
盐 。 向 混 盐 NaSO 中 加 入 足 量 稀 硫 酸 , 发 生 反 应 :
4 2 3
。下列说法正确的是( )
A.NaSO 的水溶液显碱性
4 2 3
B.1mol Na SO 中共含离子数为5N
4 2 3 A
C.上述反应中,每产生3molS,转移电子的物质的量为6mol
D.CaOCl 也可称为混盐,向CaOCl 中加入足量稀硫酸会有Cl 产生
2 2 2
19.(泰安市肥城市2020届高三适应性训练,不定项)铅的冶炼大致过程如下:
①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O 2PbO+2SO ;
2 2
③制粗铅:PbO +C Pb +CO↑;PbO+CO Pb+CO。
2
下列说法错误的是( )
A.浮选法富集方铅矿的过程,属于物理变化
B.将lmolPbS冶炼成Pb,理论上至少需要12g碳
C.方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO
D.焙烧过程中,每生成lmolPbO转移6mol电子
20.(山东省2020届普通高中学业水平等级考试模拟卷三,不定项)偏二甲肼[(CH )N—NH]与 NO 是常
3 2 2 2 4
用的火箭推进剂,火箭发射时常出现红棕色气体,发生的化学反应如下:
①(CH)N—NH(1)+2NO(1) = 2CO (g)+3N(g)+4HO(g) H<0
3 2 2 2 4 2 2 2 1
△
②NO(1) 2NO (g) H>0
2 4 2 2
△
下列说法不正确的是 ( )
A.反应①中,NO 为氧化剂
2 4
B.反应①中,生成1mo1CO 时,转移16mo1e-
2
C.由反应②推断:加压、降温是获得液态 NO 的条件
2 4D.温度升高,反应①的化学反应速率减小、反应②的化学反应速率增大