文档内容
1.以氯酸钠等为原料制备亚氯酸钠的工艺流程如下,下列说法错误的是
A.NaClO 在发生器中作氧化剂
3
B.吸收塔中1mol HO 得到2mol电子
2 2
C.吸收塔中温度不宜过高,会导致HO 的分解
2 2
D.从“母液”中可回收的主要物质是NaSO
2 4
【答案】B
2.下表各组物质之间通过一步反应就能实现如图所示转化的是( )
选项 a b c m
A N NO HNO O
[来源:学,科,网] 2[来源:学。科。网Z。X。X。K] [来源:学科网][来源:学§科§网Z§X§X§K] 3 2[来源:学科网ZXXK]
B NaCO NaHCO NaOH CO
2 3 3 2
C HS S SO O
2 2 2
D Fe FeCl FeCl Cl
2 3 2
【答案】C
【解析】A.氮气和硝酸不反应,氮气和氧气反应生成NO,NO和氧气、水反应生成硝酸,所以不能实现转化,
选项A错误;B.碳酸钠和二氧化碳反应生成碳酸氢钠,碳酸氢钠和二氧化碳不反应,碳酸钠溶液和二氧化碳
反应生成碳酸钠,所以不能实现转化,选项B错误;C、硫化氢与氧气反应生成单质硫,硫与氧气反应生成二
氧化硫,二氧化硫与硫化氢发生归中反应生成硫单质,各组物质之间可通过一步反应实现,选项C正确;D、
铁与氯化铁反应生成氯化亚铁,铁与氯气反应生成氯化铁而不是氯化亚铁,氯化亚铁与氯气反应生成氯化铁,
所以不能实现转化,选项D错误。
3.非金属元素的一些氧化物会导致环境污染,以下非金属元素的氧化物与其引起的环境问题及主要来源对应正确的是( )
选项 氧化物 环境问题 主要来源
A CO 酸雨 化石燃料的燃烧
2
B SO 光化学烟雾 工厂废气的排放
2
C NO 温室效应 汽车尾气的排放
2
D CO CO中毒 汽车尾气和化石燃料的不完全燃烧
【答案】D
4.用如图所示装置进行实验,下列对实验现象的解释不合理的是
①中试剂 ①中现象 解释
A 品红溶液 溶液褪色 SO 具有漂白性
2
B NaSiO 溶液 产生胶状沉淀 酸性:HSO >H SiO
2 3 2 3 2 3
C 酸性KMnO 溶液 紫色褪去 SO 具有还原性
4 2
D 酸性Ba(NO ) 溶液 生成白色沉淀 SO 2-与Ba2+生成BaSO 沉淀
3 2 3 3
【答案】D
【解析】A项、二氧化硫具有漂白性,能和有色物质反应生成无色物质而使品红溶液褪色,该实验体现二氧化
硫漂白性,故A正确;B项、亚硫酸酸性强于硅酸,向NaSiO 溶液通入二氧化硫气体,反应生成白色胶状硅
2 3
酸沉淀,故B正确;C项、二氧化硫能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,该实验体现二氧
化硫还原性,故C正确;D项、将SO 通入Ba(NO )溶液,酸性条件下硝酸将二氧化硫氧化生成硫酸,硫酸与
2 3 2硝酸钡反应,有白色沉淀硫酸钡生成,故D错误。
5.下图是氮元素的循环示意图,下列说法不正确的是
A. 均由氮气经氧化反应得到
B.氮素化肥的生产属于人工固氮
C.循环中氮元素发生氧化、还原反应
D.尿素及动植物的遗体一定含氮元素
【答案】A
6.将X气体通入BaCl 溶液,未见沉淀生成,然后通入Y气体,有沉淀生成。X、Y不可能是
2
选项 X Y
A SO NO
2 2
B SO HS
2 2
C NH SO
3 2
D Cl CO
2 2
【答案】D
【解析】A.二氧化氮与二氧化硫在溶液中反应生成硫酸根离子,然后与氯化钡反应生成硫酸钡白色沉淀,故不
选A;B.硫化氢与二氧化硫反应生成硫沉淀和水,故不选B;C.氨气与二氧化硫反应生成亚硫酸铵,然后与氯
化钡溶液反应生成亚硫酸钡白色沉淀,故不选C;D.氯气、二氧化碳与氯化钡溶液之间均不反应,不会有沉淀生成,故选D。
7.某同学设计如下微型实验装置用以验证SO 的性质,通过分析实验,下列结论表达不正确的是( )
2
A.a棉球褪色,验证SO 具有漂白性
2
B.b棉球褪色,验证SO 具有酸性氧化物的性质
2
C.c棉球蓝色褪去,验证SO 具有还原性
2
D.只能用烧碱溶液吸收尾气
【答案】D
8.常温下单质硫主要以S 形式存在。加热时,S 会转化为S、S、S 等。当温度达到750 ℃时,硫蒸气主要以
8 8 6 4 2
S 形式存在(占92%)。下列说法中正确的是
2
A.S 转化为S、S、S 属于物理变化
8 6 4 2
B.不论哪种硫分子,完全燃烧时都生成二氧化硫
C.S、S、S、S 都是硫元素形成的单质,为同种物质
2 4 6 8
D.把硫单质在空气中加热到750℃即得S
2
【答案】B
【解析】A.物理变化是没有新物质生成的变化,S、S、S、S 是不同的物质微粒,S 转化为S、S、S 属于化学
8 6 4 2 8 6 4 2
变化,A错误;B.不论哪种硫分子,由于组成元素都是只有硫元素,所以燃烧产物都是二氧化硫,B正确;
C.S 、S、S、S 是硫元素形成的不同单质,由于每一个分子中含有的S原子个数不同,所以它们为同素异形体,
2 4 6 8
不是同种物质,C错误;D.硫单质在空气中加热时,硫单质会和氧气之间发生反应,不会得到纯净的硫单质,
D错误。
9.已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白
色烟环。下列关于物质甲、乙的判断正确的是A.甲是浓氨水,乙是浓硫酸 B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸 D.甲是浓硫酸,乙是浓氨水
【答案】C
10.研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物——光化学烟雾,其中某些反
应过程如图所示。下列说法不正确的是
A.整个过程中O 作催化剂
3
B.反应III的方程式为O+O===O
2 3
C.光化学烟雾中含甲醛、乙醛等刺激性物质
D.反应I、反应Ⅱ均属于氧化还原反应
【答案】A
【解析】A、催化剂:反应前后质量和性质不发生改变,根据过程,O 只参与反应,没有O 的生成,因此O 不是
3 3 3
催化剂,故A说法错误;B、根据过程,反应III:O和O 参与反应,生成O,即反应 方程式为O+O=O,故B
2 3 2 3
说法正确;C、根据反应过程,反应Ⅱ生成甲醛和乙醛,因此光化学烟雾中含有甲醛和乙醛等刺激性物质,故
C说法正确;D、反应I:O+3NO=3NO ,存在化合价的变化,属于氧化还原反应,反应Ⅱ丙烯与O 发生反应
3 2 3
生成甲醛和乙醛,发生氧化还原反应,故D说法正确。
11.SO 通过下列工艺流程可制化工业原料HSO 和清洁能源H。
2 2 4 2下列说法中正确的是
A.电解槽中也可以用铁电极代替石墨作为阳极
B.原电池中负极的电极反应为:SO +2H O+4e-=SO2-+4H+
2 2 4
C.该工艺流程用总反应的化学方程式表示为:SO Br +2H O=2HBr+HSO
2+ 2 2 2 4
D.该生产工艺的优点Br 被循环利用,原电池产生的电能可充分利用,还能获得清洁能源
2
【答案】D
12.ClO 和NaClO 均具有漂白性,工业上用ClO 气体制NaClO 的工艺流程如图所示。
2 2 2 2
下列说法不正确的是
A.步骤a的操作包括过滤、洗涤和干燥
B.吸收器中生成NaClO 的离子方程式:2ClO +H O=2C1O -+O ↑+2H+
2 2 2 2 2 2
C.工业上可将ClO 制成NaClO 固体,便于贮存和运输
2 2
D.通入空气的目的是驱赶出ClO ,使其被吸收器充分吸收
2
【答案】B
【解析】A. 步骤a中,由溶液得到NaClO 固体,进行的操作为:过滤、洗涤和干燥,A正确;B. 吸收器中发生反
2
应:2ClO +2NaOH+HO═2NaClO+O+2HO,离子方程式为: 2ClO +2OH−+HO=2ClO -+O +2HO,B错误;
2 2 2 2 2 2 2 2 2 2 2 2
C. 固体比气体便于贮存和运输,工业上可将ClO 制成NaClO 固体,C正确;D. 反应结束后,发生器中仍有少
2 2
量ClO ,用空气可以将其排出,确保其在吸收器中被充分吸收,D正确。
2
13.水玻璃(Na SiO 溶液)广泛应用于耐火材料、洗涤剂生产等领域,是一种重要的工业原料。如图是用稻壳
2 3
灰(SiO:65%~70%、C:30%~35%)制取水玻璃的工艺流程:
2下列说法正确的是( )
A.原材料稻壳灰价格低廉,且副产品活性炭有较高的经济价值
B.操作A与操作B完全相同
C.该流程中硅元素的化合价发生改变
D.反应器中发生的复分解反应为SiO+2NaOH===Na SiO+HO
2 2 3 2
【答案】A
14.超临界状态下的CO 流体溶解性与有机溶剂相似,可提取中药材的有效成分,工艺流程如下。下列说法错
2
误的是( )
A.浸泡时加入乙醇有利于中草药有效成分的浸出
B.升温、减压的目的是实现CO 与产品分离
2
C.高温条件下更有利于超临界CO 萃取
2
D.CO 流体萃取中药材具有无溶剂残留、绿色环保等优点
2
【答案】C
【解析】A. 乙醇是常用的有机溶剂,中草药有效成分易溶在乙醇中,因此浸泡时加入乙醇有利于中草药有效
成分的浸出,A错误;B. 气体的溶解度随温度升高、压强减小而减小,所以升温、减压的目的是实现CO 与
2
产品分离,B正确;C. 根据流程图可知降温、加压更有利于超临界CO 萃取,C错误;D. 二氧化碳没有毒,
2
容易分离,因此CO 流体萃取中药材具有无溶剂残留、绿色环保等优点,D正确。
2
15.碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(含有质量分数为8%的TeO 、少量Ag、Au)
2为原料制备单质碲的一种工艺流程如下,(已知TeO 微溶于水,易溶于强酸和强碱),下列有关说法不正确的
2
是
A.将阳极泥研磨、反应适当加热都有利于提高“碱浸”的速率和效率
B.“碱浸”时发生主要反应的离子方程式为TeO +2OH-=TeO 2-+H O
2 3 2
C.“沉碲”时为使碲元素沉淀充分,应加入过量的硫酸
D.若提取过程碲元素的回收率为90%,则处理1kg这种阳极泥最少需通入标准状况下SO 20.16L
2
【答案】C
16.氰[(CN) ]的化学性质与卤素(X )很相似,化学上称之为拟卤素,其氧化性介于Br 和I 之间,下列有关反
2 2 2 2
应方程式不正确的是
A.(CN) 和NaOH溶液反应:(CN) +2OH— CN—+CNO—+HO
2 2 2
B.向KCN溶液中加入碘水:I+2KCN 2KI+(CN)
2 2
C.在NaI和KCN混合溶液中通入少量Cl:Cl+2I— 2Cl—+I
2 2 2
D.NaOH和HCN反应:NaOH+HCN NaCN+HO
2
【答案】B17.已知NH 和HCl都是能用来做喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH 和HCl气体,
3 3
进行如图所示实验(两烧瓶内充满溶液且不考虑溶质的扩散)。下列说法错误的是
A.NH 和HCl分别形成蓝色、红色喷泉
3
B.制备干燥的NH 和HCl,所需的干燥剂分别是碱石灰、浓硫酸
3
C.若烧瓶中改为NO ,则所得溶液溶质的物质的量浓度与前两者不同
2
D.去掉装置中的胶头滴管,改为单孔塞,也可引发喷泉
【答案】C
【解析】A.氨气和氯化氢都是极易溶于水的气体,氨气溶于水显碱性,遇到石蕊试液变蓝色,氯化氢溶于水显
酸性遇到石蕊试液变红色,NH 和HCl分别形成蓝色、红色喷泉,A正确;B.氨气是碱性气体,氯化氢是酸性
3
气体,制备干燥的NH 和HCl,所需的干燥剂分别是碱石灰、浓硫酸,B正确;C.设二氧化氮体积为1L,根据
3
反应方程式:3NO +H O=2HNO +NO,可知反应产生硝酸物质的量n(HNO)= ,溶液的体
2 2 3 3
积为HNO 的体积,所以HNO 的物质的量浓度c(HNO )= =0.0446mol/L,设氨气或
3 3 3氯化氢体积为1L,氨气和氯化氢气体形成喷泉实验形成的溶液浓度=
=0.0446mol/L,若改为NO 气体,所得溶液溶质的物质的量浓度与前两者相同,C错误;D.去掉装置中的胶头
2
滴管,改为单孔塞,用双手捂住烧瓶,待导气管气泡冒出后,冷却烧瓶会引发喷泉,D正确。
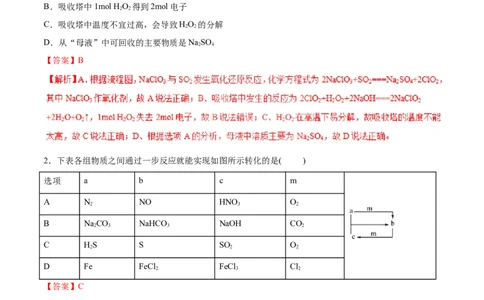
18.下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO,不一定说明木炭与浓硝酸发生了反应
2
【答案】B
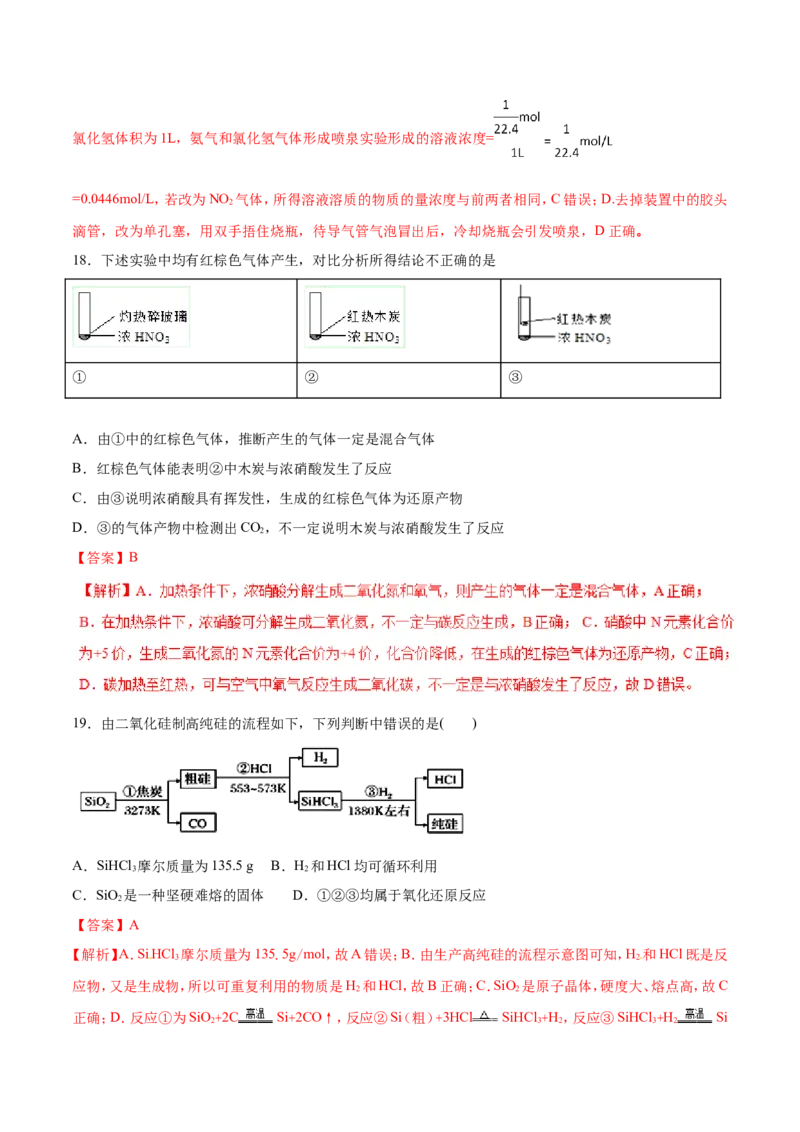
19.由二氧化硅制高纯硅的流程如下,下列判断中错误的是( )
A.SiHCl 摩尔质量为135.5 g B.H 和HCl均可循环利用
3 2
C.SiO 是一种坚硬难熔的固体 D.①②③均属于氧化还原反应
2
【答案】A
【解析】A.SiHCl 摩尔质量为135.5g/mol,故A错误;B.由生产高纯硅的流程示意图可知,H 和HCl既是反
3 2
应物,又是生成物,所以可重复利用的物质是H 和HCl,故B正确;C.SiO 是原子晶体,硬度大、熔点高,故C
2 2
正确;D.反应①为SiO+2C Si+2CO↑,反应②S(i 粗)+3HCl SiHCl +H,反应③SiHCl +H Si
2 3 2 3 2(粗)+3HCl,三个方程式中元素的化合价均发生变化,均属于氧化还原反应,D正确。
20.练江整治已刻不容缓,其中以印染工业造成的污染最为严重。某工厂拟综合处理含NH + 废水和工业废气
4
(主要含N、CO、SO 、NO、CO),设计了如下工业流程:
2 2 2
下列说法错误的是
A.气体I中主要含有的气体有N、NO、CO
2
B.X在反应中作氧化剂,可通入过量的空气
C.处理含NH +废水时,发生离子方程式是:NH ++NO-=N ↑+2H O
4 4 2 2 2
D.捕获剂所捕获的气体主要是CO
【答案】B
21.经过多方努力,郑州市的空气质量有明显改善。造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾
气处理装置可以减少有害尾气的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如
下图所示。下列说法错误的是A.NO 是该过程的中间产物
2
B.汽车尾气的主要污染成分为CO和NO
C.NO和O 必须在催化剂表面才能反应
2
D.该催化转化的总反应方程式:2NO+O+4CO 4CO+N
2 2 2
【答案】C
22.将一定物质的量的NaCO、NaHCO 组成的混合物溶于水,配成1L溶液,取出50mL溶液,然后滴加一定
2 3 3
物质的量浓度的盐酸与它反应,得到的图象如下,下列说法正确的是
A.标注 NaCl的直线代表产生的CO 的物质的量
2
B.原混合物中NaCO 与NaHCO 的物质的量之比为1:2
2 3 3
C.盐酸的浓度是0.05 mol/L
D.盐酸加到150mL时,放出CO 气体2.24L(标准状况下)
2
【答案】C
【解析】A、0~50mL时发生的反应为:NaCO+HCl=NaCl+NaHCO ,没有CO 产生,故A错误;B、从图中(0,
2 3 3 2
2.5)看出,原混合物中NaCO 与NaHCO 的物质的量之比为1:1,故B错误;C、由图可知50mL溶液中碳酸
2 3 3
钠完全转化为碳酸氢钠和氯化钠时,消耗盐酸的体积为50mL,由NaCO+HCl=NaCl+NaHCO 可知:n
2 3 3
(Na CO)=n(HCl)=0.0025mol,c(HCl)=0.0025mol÷0.05L=0.05mol·L-1,故C正确; D、50~150mL时,发生
2 3
反应为:NaHCO +HCl=NaCl+H O+CO↑,可知n(CO)=n(HCl)=100×10-3L×0.05mol·L-1×22.4L·mol-
3 2 2 2
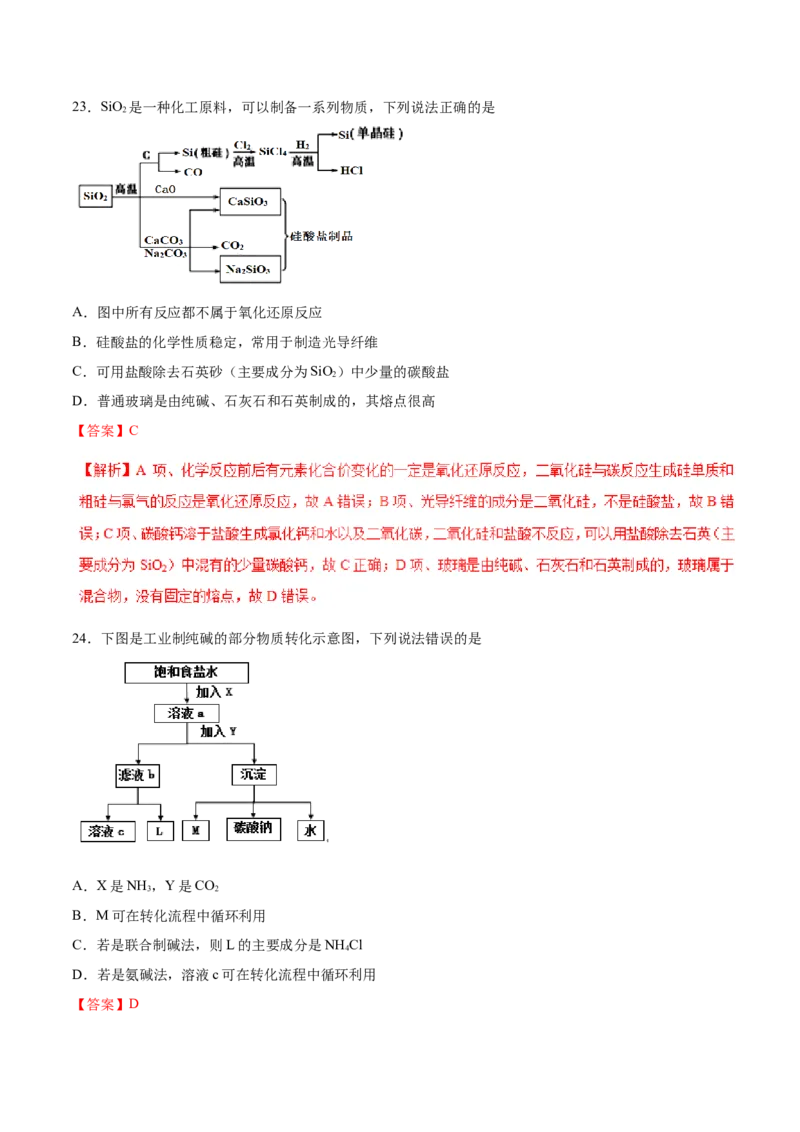
1=0.112L=112mL,故D错误。23.SiO 是一种化工原料,可以制备一系列物质,下列说法正确的是
2
A.图中所有反应都不属于氧化还原反应
B.硅酸盐的化学性质稳定,常用于制造光导纤维
C.可用盐酸除去石英砂(主要成分为SiO)中少量的碳酸盐
2
D.普通玻璃是由纯碱、石灰石和石英制成的,其熔点很高
【答案】C
24.下图是工业制纯碱的部分物质转化示意图,下列说法错误的是
A.X是NH ,Y是CO
3 2
B.M可在转化流程中循环利用
C.若是联合制碱法,则L的主要成分是NH Cl
4
D.若是氨碱法,溶液c可在转化流程中循环利用
【答案】D【解析】A.联合制碱法与氨碱法其原理都是NH +CO +H O+NaCl(饱和)=NaHCO ↓+NHCl,
3 2 2 3 4
2NaHCO NaCO+H O+CO↑,NH 极易溶于水且溶液呈弱碱性,再通入CO 使之更多地转化为HCO -,
3 2 3 2 2 3 2 3
故工业上可先向饱和食盐水中通入NH 后再通入CO 制NaHCO ,所以X是NH ,Y是CO,故A正确;B.图
3 2 3 3 2
中的沉淀为碳酸氢钠,碳酸氢钠受热分解2NaHCO NaCO+H O+CO↑,M为二氧化碳,二氧化碳是反应
3 2 3 2 2
的原料同时也是反应的副产物,可以循环利用,故B正确;C.若是联碱法,其滤液是含有氯化铵和氯化钠的
溶液,第二个过程是从含有氯化铵和氯化钠的滤液中结晶沉淀出氯化铵晶体,由于氯化铵在常温下的溶解度
比氯化钠要大,低温时的溶解度则比氯化钠小,而且氯化铵在氯化钠的浓溶液里的溶解度要比在水里的溶解
度小得多,所以在低温条件下,向滤液中加入细粉状的氯化钠,并通入氨气,可以使氯化铵单独结晶沉淀析出,
经过滤、洗涤和干燥即得氯化铵产品,所以L的主要成分是氯化铵,故C正确;D.先使氨气X通入饱和食盐
水中而成氨盐水,再通入二氧化碳Y生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,含有氯化铵的滤液b与
石灰乳混合加热,CaO+H O=Ca(OH) ,2NH Cl+Ca(OH) CaCl +2NH↑+2H O,所放出的氨气L可回收循环
2 2 4 2 2 3 2
使用,故D错误。
25.下图是进行气体性质实验的常用装置,下列对有关实验现象的描述中,不正确的是
A.若水槽中盛有水,试管中盛满SO ,可看到试管中液面上升
2
B.若水槽中盛有水,试管中盛满NO ,可看到试管中液面上升并充满试管
2
C.若水槽中盛有水(滴有酚酞),试管中是NH ,可看到试管内液面上升并呈红色
3
D.若水槽中盛有NaOH溶液,试管中是Cl,可看到试管内液面上升,黄绿色褪去
2
【答案】B