文档内容
专题 08 氧化还原反应
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 氧化还原反应的相关概念及其表示方法
考点二 氧化性、还原性强弱的比较
考点三 氧化还原反应的基本规律及应用
考点四 氧化还原反应的配平与计算
考点一 氧化还原反应的相关概念及其表示方法
1.(2023·浙江温州·乐清市知临中学校考二模)已知反应:
,下列说法正确的是
A. 是氧化剂,生成 过程中被氧化
B. 既是氧化产物又是还原产物
C.氧化剂与还原剂的物质的量之比为
D.反应中 参加反应,共转移 电子
【答案】D
【解析】A.Cu元素的化合价降低,故 是氧化剂,生成 过程中被还原发生还原反应,故A错
误;B.Cu、P元素的化合价均降低,则生成的 是还原产物,故B错误;C.Cu、P元素的化合价降
低,则5molP 、60mol 有0升高到+5价,6mol P 是还原剂,氧化剂与还原剂的物质的量之比为
4 4
65:6,故C错误;D.消耗60mol ,反应转移120mole-,消耗1mol ,转移2mole-,故D正确。
答案为D。
2.(2023·广东·高三学业考试)使用交叉分类法可从不同角度认识化学反应。下列反应既属于化合反应,
又属于氧化还原反应的是
A.Cl+H O=HCl+HClO B.2NaO+2H O=4NaOH+O ↑
2 2 2 2 2 2
C.3NO +H O=2HNO +NO D.4Fe(OH) +O +2H O=4Fe(OH)
2 2 3 2 2 2 3
【答案】D
【分析】根据反应特点及特征分析判断。
【解析】A.该反应中反应物有2种,生成物也有2种,因此反应不属于化合反应,A错误;B.该反应中
反应物有2种,生成物也有2种,因此反应不属于化合反应,B错误;C.该反应中反应物有2种,生成物
也有2种,因此反应不属于化合反应,C错误;D.该反应中反应物有3种,生成物只有1种,反应基本类
型属于化合反应,且在反应过程中Fe、O元素的化合价发生了变化,因此反应又属于氧化还原反应,D正
1
原创精品资源学科网独家享有版权,侵权必究!确;故合理选项是D。
3.(2023·海南省直辖县级单位·嘉积中学校考一模)氮循环是全球生物地球化学循环的重要组成部分,全
球每年通过人类活动新增的“活性”氮导致全球氮循环的严重失衡,并引起水体的富营养化、水体酸化、
温室气体排放等一系列环境问题。海洋生物参与氮循环的过程如图所示。下列叙述不正确的是
A.图中5个反应中包含4个氧化还原反应
B.1 mol NH 与1 mol NH 所含电子数相等
3
C.反应④中NH OH作还原产物
2
D.反应③和⑤生成等量N 时,反应⑤转移的电子数少
2
【答案】D
【解析】A.反应①中NH 的N和H的化合价均未发生变化,反应②中NH OH的N的化合价由-1降低
2
为-2,反应③中NH 的N的化合价由-2升高为0价,反应④中的NO 的N化合价由+3价降低为-1价,反
2 4
应⑤中的NO 的N化合价由+3价降低为0价,共有4个氧化还原反应,故A说法正确;B.1molNH 与
1molNH 均含有10mol电子,故B说法正确;C.反应④中的NO 的N化合价由+3价降低为-1价
3
(NH OH),NH OH作还原产物,故C说法正确;D.反应③中NH 的N的化合价由-2升高为0价,反应⑤
2 2 2 4
中的NO 的N化合价由+3价降低为0价,生成等量氮气时,反应⑤转移电子数多,故D说法错误;答案
为D。
4.(2023·浙江金华·浙江省丽水中学校联考一模)高铜酸钾KCuO (Cu为+3价)可由反应
2
2CuO+2KO =O ↑+2KCuO 制备得到,下列说法正确的是
2 2 2
A.KO 只发生还原反应 B.0.2molCuO被氧化时,反应共转移了0.3mol电子
2
C.CuO既是氧化剂又是还原剂 D.该反应的氧化产物只有KCuO
2
【答案】B
【解析】A.由题干反应方程式:2CuO+2KO =O ↑+2KCuO 可知,反应中KO 中的O部分由- 价变为0
2 2 2 2
价,部分由- 价变为-2价,即KO 既发生还原反应又发生还原反应,A错误;B.由题干反应方程式:
2
2CuO+2KO =O ↑+2KCuO 可知,反应中转移电子数为:3e-,故0.2molCuO被氧化时,反应共转移了
2 2 2
0.3mol电子,B正确;C.由题干反应方程式:2CuO+2KO =O ↑+2KCuO 可知,反应中CuO中Cu的化合
2 2 2
价由+2价升高到+3价,故CuO只是还原剂,被氧化,C错误;D.由题干反应方程式:
2CuO+2KO =O ↑+2KCuO 可知,从O的化合价可知O 为氧化产物,从Cu的化合价可知KCuO 为氧化产
2 2 2 2 2
物,故该反应的氧化产物有KCuO 和O,D错误;故答案为:B。
2 25.(2023·浙江杭州·校联考模拟预测)超氧化钾( )在加热条件下可以将 氧化,该反应的化学方程
式如下: ,则下列说法不正确的是
A.该反应中化合价升高的元素是O和Cu
B. 既是氧化产物,又是还原产物
C.当反应中转移的电子数为 时,有 被氧化
D.标准状况下,生成 时,被还原的超氧化钾( )为
【答案】C
【分析】 中,Cu化合价由+2价升高到+3价, 中O的化合价由- 价一部
分升高为0价,一部分降低到-2价,2molCuO参加反应,一共转移3mol电子;
【解析】A.根据分析可知,该反应中化合价升高的元素是O和Cu,选项A正确;B.Cu化合价由+2价
升高到+3价,O元素部分由- 价降为-2价, 既是氧化产物,又是还原产物,选项B正确;C.反
应 中,共转移3mol电子,故当反应中转移的电子数为 时,有
被氧化,选项C错误;D. 中O的化合价由- 价一部分长高为0价,一部分降低到-2价,
比例为1:1,标准状况下,生成 时,即0.1mol,被还原的超氧化钾( )为 ,选项D正确;
答案选C。
6.(2023·上海·统考模拟预测)聚合氯化铝用于城市给排水净化。氧化铝法制取无水三氯化铝的反应如下:
(1)标出上述反应的电子转移方向和数目 。
(2)写出该反应的平衡常数表达式: 。
(3)Al原子核外有 种不同能量的电子。
聚合氯化铝(PAC)是一种介于 和 之间的水溶性无机高分子聚合物,PAC的水解过程中会有一
种聚合稳定态物质 称为 , 对水中胶体和颗粒物具有高度电中和桥联作
用,是净水过程中的重要物质。
(4) Al 在水解过程中会产生[Al(OH) ]+、[Al(OH)]2+等产物,写出[Al(OH)]2+水解的离子方程式 。
13 2
(5) 溶液与NaOH溶液反应,若参与反应的铝离子最终全部转化生成 ,则理论上参与反应的
与 的物质的量之比是
(6)使用 净水时应控制pH在6.8~8.02之间,否则净水效果不佳。请结合使用 水解净化水时铝元素
存在的形态,分析在强酸性和强碱性环境时净水效果差的原因。【答案】(1) 或
(2)
(3)5
(4)Al(OH)2++H O Al(OH) +H+
2
(5)13∶32
(6)如果是强酸性,抑制Al3+水解,如果是强碱,Al元素以AlO 形式存在
【解析】(1)该反应中C为还原剂,氯气为氧化剂,3molC参与反应转移6mol电子,单线桥表示形式为
或用双线桥的形式表示
;故答案为 或
;
(2)根据平衡常数的数学表达式,K= ;故答案为 ;
(3)基态Al原子核外电子排布式为1s22s22p63s23p1,有1s、2s、2p、3s、3p,有5种不同能量的电子;故
答案为5;
(4)Al(OH)2+水解的方程式为:Al(OH)2++H O Al(OH) +H+,故答案为Al(OH)2++H O Al(OH)
2 2
+H+;
(5)理论上完全转化,发生的离子方程式为13Al3++32OH-+8H O=[AlOAl (OH) (H O) ]7+,参与Al3+与
2 4 12 24 2 12
OH-的物质的量之比为13∶32;故答案为13∶32;
(6)如果是强酸性,抑制Al3+水解,不能得到Al ,如果是强碱,Al元素以AlO 形式存在,也不能得到
13
Al ;故答案为如果是强酸性,抑制Al3+水解,如果是强碱,Al元素以AlO 形式存在。
13
考点二 氧化性、还原性强弱的比较
1.(2023·海南·海南中学校联考一模) 是一种常用的消毒剂,可通过反应制取,下列有关说法正确的是
A.还原性:
B.每消耗 ,转移 电子
C.氧化剂与还原剂的物质的量之比为2∶1
D.若该反应通过原电池来实现,则 是负极产物
【答案】C
【解析】A. 反应中,SO 是还原剂、ClO 是还原产物,还原性
2 2
,故A错误;B.SO 中S元素化合价由+4升高为+6,每消耗 ,转移 电子,故B
2
错误;C.NaClO 中Cl元素化合价降低,NaClO 是氧化剂,SO 中S元素化合价升高,SO 是还原剂,氧
3 3 2 2
化剂与还原剂的物质的量之比为2∶1,故C正确;D.若该反应通过原电池来实现,负极发生氧化反应,
正极发生还原反应,则 是正极产物,故D错误;选C。
2.(2023·山东滨州·统考二模)氧化还原电对的标准电极电势( )可用来比较相应氧化剂的氧化性强弱,
相关数据(酸性条件)如下。
氧化还原电对(氧
电极反应式 /V
化剂/还原剂)
0.77
0.54
1.36
1.07
1.84
下列分析错误的是
A.氧化性:
B.向 溶液滴加 溶液,反应的离子方程式为
C.向淀粉KI溶液中滴加 溶液,溶液变蓝色
D.向含有KSCN的 溶液中滴加少量氯水,溶液变红色
【答案】B
【解析】A.标准电极电势越大,对应氧化剂的氧化性越强,氧化性: ;故A正确;
B. 的氧化性低于 ,所以不能通过 氧化 得到 ;所以不会发生反应,故B错误;C. 的氧化性高于 ,向淀粉KI溶液中滴加 溶液,得到 ,溶液变蓝色;故C正确;D.氧化
性大小为 ,所以氯水氧化 ,溶液变红,故D正确;故答案选B。
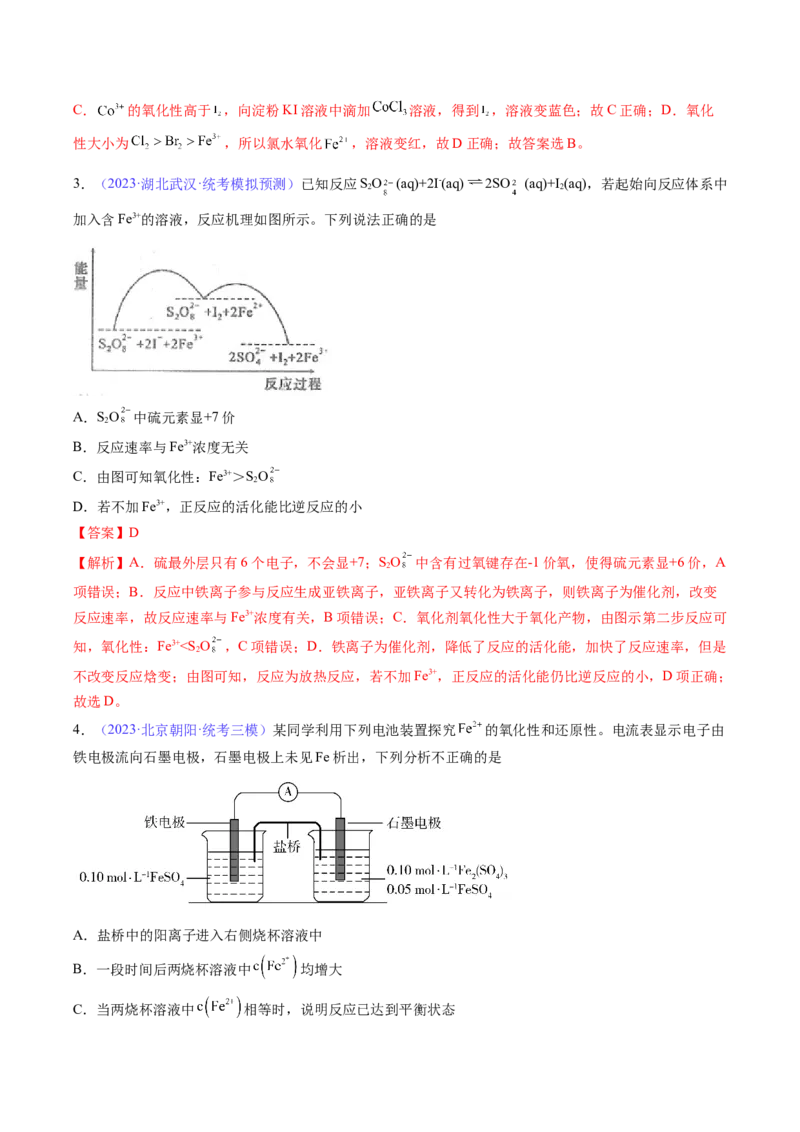
3.(2023·湖北武汉·统考模拟预测)已知反应SO (aq)+2I-(aq) 2SO (aq)+I (aq),若起始向反应体系中
2 2
加入含Fe3+的溶液,反应机理如图所示。下列说法正确的是
A.SO 中硫元素显+7价
2
B.反应速率与Fe3+浓度无关
C.由图可知氧化性:Fe3+>SO
2
D.若不加Fe3+,正反应的活化能比逆反应的小
【答案】D
【解析】A.硫最外层只有6个电子,不会显+7;SO 中含有过氧键存在-1价氧,使得硫元素显+6价,A
2
项错误;B.反应中铁离子参与反应生成亚铁离子,亚铁离子又转化为铁离子,则铁离子为催化剂,改变
反应速率,故反应速率与Fe3+浓度有关,B项错误;C.氧化剂氧化性大于氧化产物,由图示第二步反应可
知,氧化性:Fe3+氧化产物,氧
化剂>还原剂,可得出氧化性: ,D项正确;答案选C。
考点三 氧化还原反应的基本规律及应用
1.(2023·浙江·校联考一模)NaH PO 为正盐,关于化学反应NaH PO +4AgNO +2H O=4Ag+HPO
2 2 2 2 3 2 3 4
+NaNO +3HNO 。下列说法不正确的是
3 3
A.氧化产物是HPO
3 4
B.该反应氧化剂与还原剂的物质的量之比为4∶1
C.此条件下氧化性:Ag+>H PO
3 4
D.该反应的离子方程式为 +4Ag++H O=4Ag+HPO +H+
2 3 4
【答案】D
【分析】NaH PO 为正盐即可电离生成Na+和 ,银元素由+1价降到0价,磷元素由+1价升高到+5价。
2 2【解析】A.由分析知,磷元素化合价升高,即HPO 属于氧化产物,A正确;B.结合分析知,NaH PO
3 4 2 2
为还原剂,4AgNO 为氧化剂,得失电子守恒知氧化剂和还原剂物质的量之比为4∶1,B正确;C.氧化剂
3
的氧化性大于氧化产物的氧化性,即氧化性Ag+>H PO ,C正确;D.离子方程式为
3 4
,D错误;故选D。
2.(2023·山东济宁·统考二模) 去除酸性废水中 的反应机理如图所示(图中“HS·”为自由
基)。下列说法错误的是
A.X的化学式为
B.HS·反应活性较强,不能稳定存在
C.步骤III反应中氧化剂与还原剂的物质的量比为8∶1
D.步骤IV除砷的方程式为
【答案】C
【解析】A.SO 经过“途径I”的除砷过程可描述为,SO 与氢离子在紫外线照射条件下可以生成
2 2
HS·,两个HS·可以结合生成HS,HS 分解得到S 和HS,HS与HAsO 发生反应生成As S,X的化学
2 2 2 2 8 2 2 3 3 2 3
式为 ,故A正确;B.HS·反应活性较强,在强酸性或强碱性溶液中均不能大量存在,故B正确;C.
步骤III反应中HS 分解得到S 和HS,方程式为:8HS=S +8H S,S元素化合价由-1价上升到0价,又
2 2 8 2 2 2 8 2
由-1价下降到-2价,HS 既是氧化剂也是还原剂,氧化剂与还原剂的物质的量比为1∶1,故C错误;D.
2 2
步骤IV中,HS与HAsO 发生反应生成As S,方程式为: ,故D正确;
2 3 3 2 3
故选C。
3.(2023·浙江·校联考三模)工业上以镉铁矿(主要成分为 、 、Fe和 )为原料制备分析试剂
的流程如图[ 可溶于水]:
下列说法不正确的是
A.酸浸过程既有氧化还原反应,也有非氧化还原反应
B. 是还原镉步骤的还原剂,溶液中 可能将其氧化为
C.若氧化步骤有气泡生成,说明酸性条件下 也能氧化
D.沉镉后的滤液仍会残留少量的 ,排放前需进一步回收处理以防污染环境【答案】C
【分析】镉铁矿加入稀硫酸酸浸,得到滤渣1主要成分为 等,滤液加入甲醇还原镉,再加入双氧水氧
化,调节pH得到滤渣2,加入碳酸钾溶液沉镉,去掉滤液,得到的碳酸镉加入溴酸转化,蒸发结晶得到
;
【解析】A.酸浸过程 、 与稀硫酸发生复分解反应生成盐和水,属于非氧化还原反应,Fe与硫
酸反应生成硫酸亚铁和氢气属于氧化还原反应,选项A正确;B. 是还原镉步骤的还原剂,溶液中
可能将其氧化为 , 转化为 ,选项B正确;C.气泡可能是 等催化下双氧水的分解
产生的,选项C不正确;D.镉为重金属,沉镉后的滤液仍会残留少量的 ,排放前需进一步回收处理
以防污染环境,选项D正确;答案选C。
4.(2023·河北·张家口市宣化第一中学校联考二模)通过电氧化合成法可制备特殊高价金属化合物高铜酸
钠(化学式为NaCuO )。关于该物质的推测,下列有关说法正确的是
2
A.NaCuO 具有强还原性
2
B.NaCuO 与浓盐酸反应产生O
2 2
C.电氧化合成时,在阴极上Cu2+失电子得到NaCuO
2
D.NaCuO 与氢气反应可能有紫红色固体生成
2
【答案】D
【解析】A.NaCuO 中铜元素的化合价为+3价,不稳定,容易得到电子,表现强氧化性,A错误;B.
2
NaCuO 具有强氧化性,浓盐酸有还原性,二者会发生氧化还原反应生成黄绿色刺激性其为的气体氯气,B
2
错误;C.NaCuO 中铜元素的化合价为+3价,故电氧化合成时,Cu2+在阳极上失电子得到NaCuO ,C错
2 2
误;D.氢气具有还原性,NaCuO 具有强氧化性,氢气可将NaCuO 还原产生紫红色的单质铜,D正确;
2 2
故选D。
5.(2023·浙江·校联考模拟预测)超氧化钾 在加热条件下可以将 氧化成 Ⅲ 的化合物,化
学方程式如下: ,则下列说法正确的是
A. 既是氧化剂,又是还原剂
B. 只是氧化产物
C.当反应中转移的电子数为 时,则有 被氧化
D.标准状况下,生成 时,被还原的超氧化钾 为
【答案】C
【分析】分析方程式 可知, 中的O元素的化合价 由部分升高为氧气
中的 价,被氧化,部分转化为 , 中O为 价, 为 价,故氧气为氧化产物,
即是氧化产物也是还原产物。【解析】A.该反应中 中 的化合价由 价升高为 价, 被氧化,为还原剂, 的中O化合
价由 价部分升高为 价,部分降低为 价,既有升高,又有降低, 既是氧化剂又是还原剂,选项
A错误;B. 中 的化合价由 价升高为 价,化合价升高被氧化,是氧化产物,而部分氧的化
合价又由 价降低为 价,化合价降低被还原,故又是还原产物,选项B错误;C.根据方程式分析可
知,当反应中转移的电子数为 时,则有 被氧化,选项C正确;D.标准状况下,生成
时,即 时,根据方程式可知,参与反应的超氧化钾 为 ,但 中只有一半
是被还原的,另一半被氧化,故被还原的超氧化钾 为 ,选项D错误;答案选C。
考点四 氧化还原反应的配平与计算
1.(2023·浙江绍兴·统考二模)汽车剧烈碰撞时,安全气囊中发生反应 10NaN + 2KNO = K O + 5Na O
3 3 2 2
+ 16N ↑,下列有关说法不正确的是
2
A.NaN 为还原剂
3
B.生成 1mol N,转移 0.625N 个电子
2 A
C.氧化产物与还原产物的物质的量之比为 1:15
D.该反应过程有极性键、非极性键和离子键的断裂或形成
【答案】C
【分析】由方程式可知,反应中,叠氮化钠中的氮元素化合价升高被氧化,叠氮化钠为反应的还原剂,硝
酸钾中氮元素化合价降低被还原,硝酸钾是反应的氧化剂,氮气即是氧化产物也是还原产物。
【解析】A.由分析可知,反应中,叠氮化钠中的氮元素化合价升高被氧化,叠氮化钠为反应的还原剂,
故A正确;B.由方程式可知,反应生成16mol氮气时转移10mol电子,则生成1mol氮气时,反应转移电
子数目为 ×N mol—1=0.625N ,故B正确;C.由分析可知,反应中,叠氮化钠为反应的还原剂,
A A
硝酸钾是反应的氧化剂,氮气即是氧化产物也是还原产物,由方程式可知,叠氮化钠和硝酸钾的物质的量
比为10:2,则氧化产物与还原产物的物质的量之比为10×3:2=15:1,故C错误;D.叠氮化钠是含有离
子键和非极性键的离子化合物,硝酸钾是含有离子键和极性键的离子化合物,氧化钾、氧化钠是含有离子
键的离子化合物,氮气是含有非极性键的非金属单质,所以反应过程有极性键、非极性键和离子键的断裂
或形成,故D正确;故选C。
2.(2023·广东梅州·统考二模)为了获得良好的草酸酯加氢的催化效果,通常需要保持铜催化剂中Cu0和
Cu+的组成相对稳定,将C 作为电子缓冲剂,通过中性碳团簇(C )与负离子(C )的切换可有效地稳定铜催
60 60
化剂中Cu0和Cu+的比例。下列说法正确的是
A.C 是新型化合物
60
B.当1molC 转变为C 时,失去60mol电子
60
C.当C 转变为C 时,铜催化剂中Cu0和Cu+的个数比减小
60
D.草酸酯催化加氢过程中,需要不断补充C
60【答案】C
【解析】A. 是单质,不是化合物,A项错误;B. 是一个由60个C原子构成的分子, 转
变为 时,得到 电子,B项错误;C. 转变为 时,得到电子,则铜催化剂中部分 失去电子
变成 ,两者个数比减小,C项正确;D.题干中 是电子缓冲剂,通过 与 的切换起作用,不用
补充 ,D项错误;故选C。
3.(2023·辽宁沈阳·东北育才学校校考模拟预测)2.28 g铜镁合金完全溶解于75 mL密度为1.40 g/mL、质
量分数为63%的浓硝酸中,得到 和 的混合气体1680 mL(标准状况),向反应后的溶液中加入l.0
mol/L NaOH溶液,当金属离子全部沉淀时,得到3.81 g沉淀,下列说法正确的是
A.该合金中,镁的物质的量为0.03 mol
B. 和 混合气体的平均相对分子质量约为55.2
C.得到3.81 g沉淀时,加入NaOH溶液的体积为900 mL
D.该浓硝酸中 的物质的量浓度为12.0 mol/L
【答案】B
【分析】设铜、镁的物质的量分别为x、y,则①64x+24y=2.28,②98x+58y=3.81,解得x=0.03mol,
y=0.015 mol,混合气体的物质的量= ,设NO、NO 的物质的量分别为a、b,根据
2 4 2
氧化还原反应中得失电子数相等:2×(0.03+0.015)=2a+b,a+b=0.075,则a=0.015mol,b=0.06mol,
c(HNO )= ,硝酸的物质的量n(HNO)=14.0
3 3
mol/L×75mL÷1000=1.05mol。
【解析】A.由分析可知,该合金中,镁的物质的量为0.015 mol,A错误;B. 和 混合气体的摩
尔质量约= ,其平均相对分子质量约为55.2,B正确;C.沉淀达最大时,
溶液中只有硝酸钠,根据原子守恒:n(NaOH)=n(HNO )-(2a+b)=1.05mol-0.09mol=0.96mol,氢氧化钠溶
3
液体积为960mL,C错误;D.c(HNO )= , D错误;故选B。
3
4.(2023秋·江苏南通·高三如皋市第一中学开学考试)根据提供的情境书写指定反应的方程式。
(1)通过如图转化可回收废旧锂电池电极材料 (难溶于水)中钴元素和锂元素。
写出反应1的离子方程式: 。
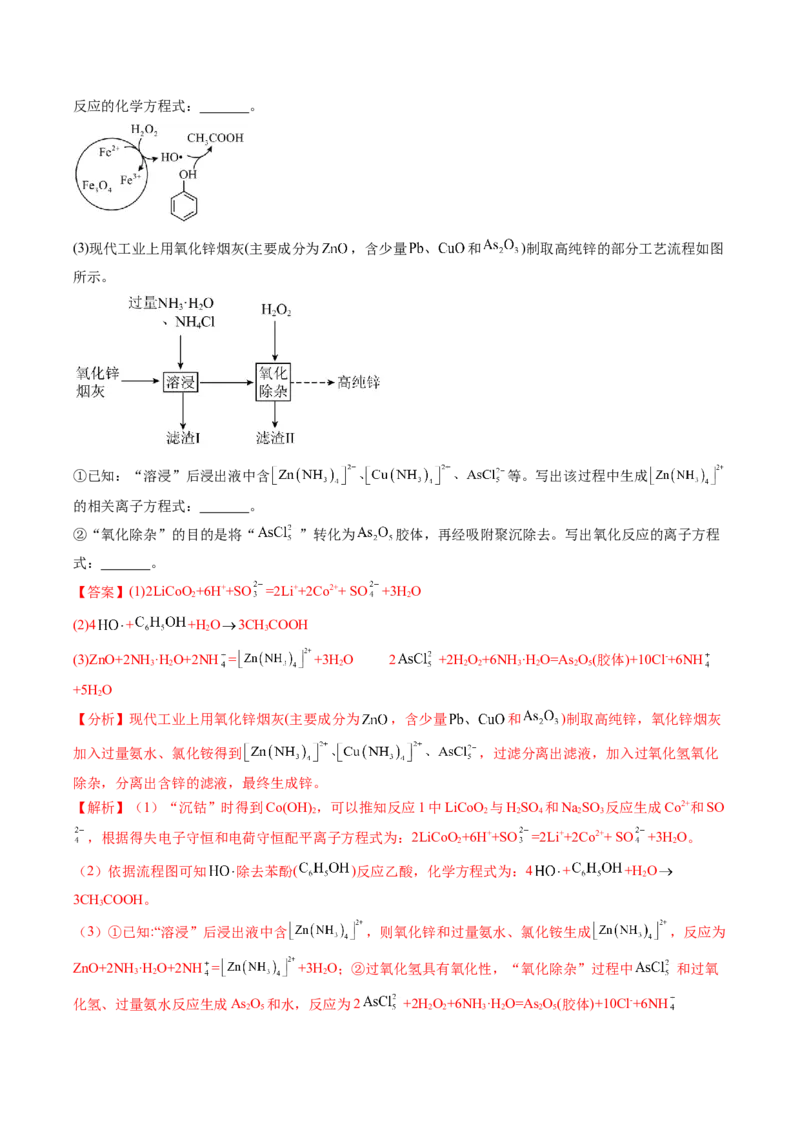
(2)活性自由基 可有效除去废水中的苯酚等有机污染物,原理如图所示。写出 除去苯酚( )反应的化学方程式: 。
(3)现代工业上用氧化锌烟灰(主要成分为 ,含少量 和 )制取高纯锌的部分工艺流程如图
所示。
①已知:“溶浸”后浸出液中含 等。写出该过程中生成
的相关离子方程式: 。
②“氧化除杂”的目的是将“ ”转化为 胶体,再经吸附聚沉除去。写出氧化反应的离子方程
式: 。
【答案】(1)2LiCoO +6H++SO =2Li++2Co2++ SO +3H O
2 2
(2)4 + +H O 3CHCOOH
2 3
(3)ZnO+2NH ·H O+2NH = +3H O 2 +2H O+6NH·H O=As O(胶体)+10Cl-+6NH
3 2 2 2 2 3 2 2 5
+5H O
2
【分析】现代工业上用氧化锌烟灰(主要成分为 ,含少量 和 )制取高纯锌,氧化锌烟灰
加入过量氨水、氯化铵得到 ,过滤分离出滤液,加入过氧化氢氧化
除杂,分离出含锌的滤液,最终生成锌。
【解析】(1)“沉钴”时得到Co(OH) ,可以推知反应1中LiCoO 与HSO 和NaSO 反应生成Co2+和SO
2 2 2 4 2 3
,根据得失电子守恒和电荷守恒配平离子方程式为:2LiCoO +6H++SO =2Li++2Co2++ SO +3H O。
2 2
(2)依据流程图可知 除去苯酚( )反应乙酸,化学方程式为:4 + +H O
2
3CHCOOH。
3
(3)①已知:“溶浸”后浸出液中含 ,则氧化锌和过量氨水、氯化铵生成 ,反应为
ZnO+2NH·H O+2NH = +3H O;②过氧化氢具有氧化性,“氧化除杂”过程中 和过氧
3 2 2
化氢、过量氨水反应生成As O 和水,反应为2 +2H O+6NH·H O=As O(胶体)+10Cl-+6NH
2 5 2 2 3 2 2 5+5H O。
2
5.(2023·浙江·校联考三模)某钾盐X含有4种前四周期元素,某兴趣小组进行了如下探究实验:
其中固体A为两种盐组成的混合物,并且两种盐含有相同的阴离子;气体F是由气体B与气体Ⅰ组成的混
合物,且只含有两种元素;黑色固体G是一种磁性物质;所有气体体积均已换算成标况下数据,请回答下
列问题:
(1)X的组成元素为K、 、 、 ,X的化学式为 。
(2)写出固体D真空加热分解的化学方程式 。
(3)写出溶液C与足量酸性 溶液反应的离子方程式 。
(4)设计实验检验溶液J中 以外的阳离子 。
【答案】(1)Fe C O K [Fe(C O)]
3 2 4 3
(2)FeC O FeO+CO↑+CO ↑
2 4 2
(3)5C O +2MnO +16H+=2Mn2++10CO ↑+8H O
2 2 2
(4)取少量溶液J于试管中,滴加KSCN溶液,若溶液变红,说明存在Fe3+;另取少量溶液J于试管中,滴
加K[Fe(CN) ]溶液,若产生蓝色沉淀,说明存在Fe2+
3 6
【分析】黑色固体G是一种磁性物质,则G为四氧化三铁,1.55g四氧化三铁中铁元素的物质的量为
×3≈0.02mol,由铁原子个数守恒可知,1.44g黑色固体E中铁原子的质量为0.02mol×56g/
mol=1.12g,由质量守恒定律可知,E中氧原子的物质的量为 =0.02mol,则E为氧化亚铁;气
体F是由气体B与气体Ⅰ组成的混合物,且只含有两种元素,由B能与澄清石灰水反应生成白色固体H可
知,气体B为二氧化碳、气体F为一氧化碳、白色固体H为碳酸钙,则固体D受热分解生成氧化亚铁、一
氧化碳和二氧化碳,由质量守恒定律可知,D发生分解反应生成二氧化碳的质量为2.88g—1.44g—
×28g/mol=0.88g,由原子个数守恒可知,D中铁原子的物质的量为0.02mol、碳原子的物质的量
为 + =0.04mol、氧原子的物质的量为 =0.08mol,则D中
铁原子、碳原子和氧原子的物质的量比为0.02mol:0.04mol:0.08mol=1:2:4,化学式为FeC O;由固体
2 4
A为两种盐组成的混合物,并且两种盐含有相同的阴离子可知,溶液C为草酸钾溶液,由固体A的质量可知,草酸钾的物质的量为 =0.03mol,则固体X受热分解生成草酸钾、草酸亚铁和
二氧化碳,由原子个数守恒可知,X中钾原子和铁原子的个数比为0.03mol×2:0.02mol=3:1,由化合价代
数和为0可知,X的化学式为K[Fe(C O)]。
3 2 4 3
【解析】(1)由分析可知,X的化学式为K[Fe(C O)],含有的元素为钾元素、铁元素、碳元素和氧元素,
3 2 4 3
故答案为:Fe;C;O; K[Fe(C O)];(2)由分析可知,固体D真空加热分解发生的反应为草酸亚铁受
3 2 4 3
热分解生成氧化亚铁、一氧化碳和二氧化碳,反应的化学方程式为FeC O FeO+CO↑+CO ↑,故答案为:
2 4 2
FeC O FeO+CO↑+CO ↑;(3)由分析可知,溶液C为草酸钾溶液,草酸钾溶液与足量酸性高锰酸钾溶
2 4 2
液反应生成硫酸钾、硫酸锰、二氧化碳和水,反应的离子方程式为5C O +2MnO +16H+=2Mn2+
2
+10CO ↑+8H O,故答案为:5C O +2MnO +16H+=2Mn2++10CO ↑+8H O;(4)由分析可知,黑色固体D
2 2 2 2 2
为四氧化三铁,四氧化三铁与足量盐酸反应生成氯化铁、氯化亚铁和水,则溶液J为盐酸、氯化铁和氯化
亚铁的混合溶液,检验溶液中铁离子和亚铁离子的操作为取少量溶液J于试管中,滴加KSCN溶液,若溶
液变红,说明存在Fe3+;另取少量溶液J于试管中,滴加K[Fe(CN) ]溶液,若产生蓝色沉淀,说明存在
3 6
Fe2+,故答案为:取少量溶液J于试管中,滴加KSCN溶液,若溶液变红,说明存在Fe3+;另取少量溶液J
于试管中,滴加K[Fe(CN) ]溶液,若产生蓝色沉淀,说明存在Fe2+。
3 6