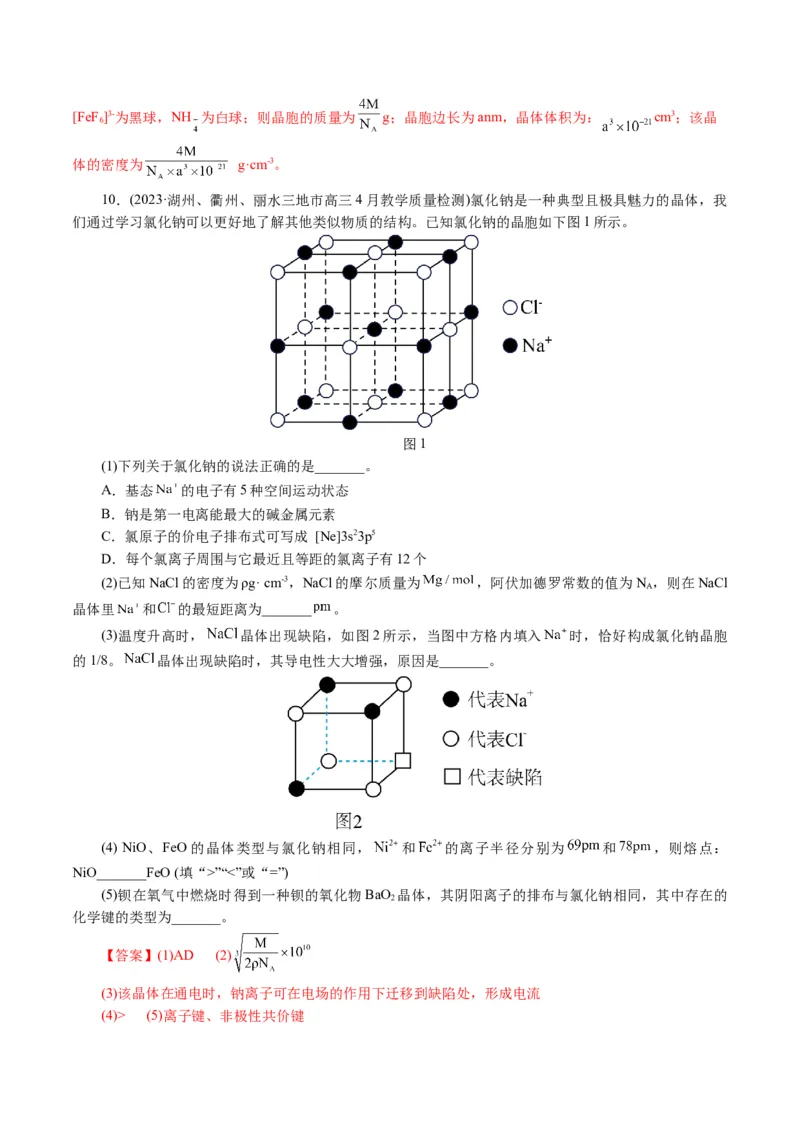
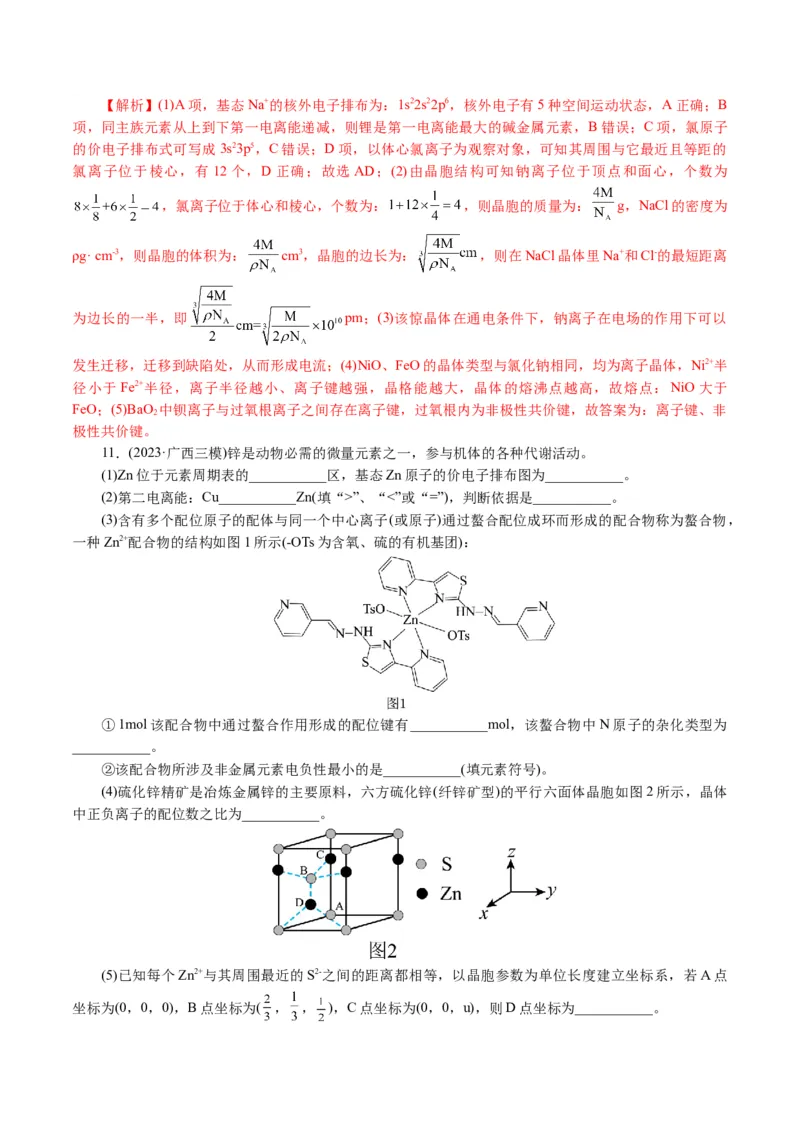
文档内容
专题 12 物质结构与性质综合(题型突破)
目 录
2
3
考点一 原子结构与性质 3
【真题研析·规律探寻】 3
解题技巧 13
【核心提炼·考向探究】 14
1.原子结构与化学键 14
2.原子核外电子排布的“三”规律 15
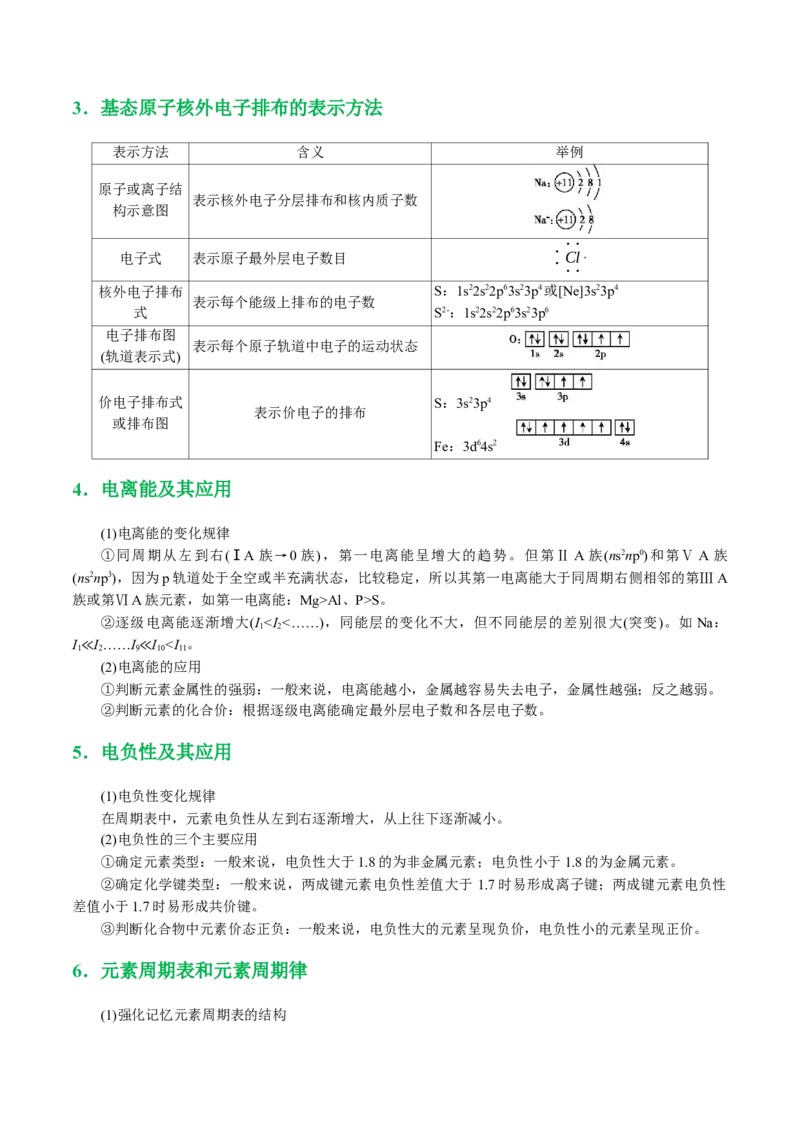
3.基态原子核外电子排布的表示方法 15
4.电离能及其应用 16
5.电负性及其应用 16
6.元素周期表和元素周期律 16
7.粒子半径大小比较规律 17
8.金属性、非金属性强弱的判断 17
【题型特训·命题预测】 18
题型一 原子核外电子排布 18
题型二 元素周期表与元素周期律 21
考点二 分子结构与性质 27
【真题研析·规律探寻】 27
解题技巧 31
1.键的极性与分子极性的关系 31
2.中心原子杂化类型和分子空间构型的相互判断 32
3.常见等电子体 32
【核心提炼·考向探究】 32
1.共价键 32
2.中心原子价层电子对数、杂化轨道类型与粒子的立体构型(ABm±型)
33
n
3.分子构型与分子极性的关系 33
4.三种作用力及其对物质性质的影响 33
5.配位化合物 34
6.超分子 34
【题型特训·命题预测】 34
题型一 共价键类型 34
题型二 分子的空间构型 36
题型三 分子间作用力 41
考点三 晶体的类型与性质比较 48【真题研析·规律探寻】 48
解题技巧 50
判断晶体类型的方法 50
【核心提炼·考向探究】 50
1.晶体与非晶体 50
2.晶体类型及性质的比较 51
3.物质熔、沸点高低的比较 51
【题型特训·命题预测】 52
考点四 晶体结构与性质 55
【真题研析·规律探寻】 55
解题技巧 61
晶体结构的相关计算 61
【核心提炼·考向探究】 62
1.常见原子晶体结构分析 62
2.常见分子晶体结构分析 62
3.常见离子晶体结构分析 63
4.常见金属晶体结构分析 64
【题型特训·命题预测】 64
考点五 物质结构与性质综合 73
【真题探析·规律探寻】 73
解题技巧 90
【题型特训·命题预测】 90
考点要求 考题统计 考情分析
【命题规律】
2023全国乙卷35(1)题,15分;2023浙江1月选考17(2)
《物质结构与性质》题目
题,10分;2023北京卷15(1)(2)题,10分;2022江苏卷
一般是以元素推断或某主
3题,3分;2022全国甲卷35(1)(2)题,15分;2022河北
族元素为背景,以“拼
卷17(1)(2)题,15分;2022湖南卷18(1)(2)题,15分;
盘”形式呈现,各小题之
2022 海南卷5题,2分;2022全国乙卷35(1)题,15
间相对独立,主要考查原
分;2022重庆卷18(1)(2)题,15分;2022北京卷15(1)(2)
原子结构与性质 子结构与性质、分子结构
(3)题,10分;2022海南卷19(1)(2)题,14分;2022广东
与性质、晶体结构与性
卷20(1)题,14分;2021湖北卷13题,3分;2021山东
质。试题背景新颖,注重
卷16(1)(2)题,12分;2022广东卷20(2)(3)题,14分;
体现科学新成果或新发
2021 海南卷19(1)(2)(3)题,14分;2021全国乙卷35(1) 现,更注重“结构决定性
题,15分;2021河北卷17(1)题,15分;2021湖南卷 质”思想的树立,考查空
18(1)题,15分 间想象能力。在原子结构部分主要命题点有电子排
布式或排布图的书写,电
离能、电负性大小的比较
与判断;在分子结构部分
2023山东卷3题,2分;2023北京卷10题,3分;2023
主要命题点有化学键类型
湖南卷4题,3分;2023湖北卷11题,3分;2023湖北
的判断,分子构型的判
卷9题,3分;2023浙江1月选考12题,3分;2023浙
断,中心原子杂化方式的
江6月选考17(2)题,10分;2023全国乙卷35(2)题,15
判断;在晶体结构部分主
分;2023山东卷16(2)题,12分;2023浙江1月选考 要命题点有晶体类型的判
17(1)题,3分;2023北京卷15(3)题,10分;2022海南 断,晶体结构的计算等。
卷11题,4分;2022湖北卷11题,3分;2022辽宁卷8 【命题预测】
题,3分;2022湖北卷10题,3分;2022山东卷5题,2 “物质结构与性质”
分子结构与性质 分;2022河北卷17(3)题,15分;2022湖南卷18(3)题, 模块的高考试题相对稳
15分;2022广东卷20(2)(4)(5)题,14分;2022全国乙卷 定,应抓住重点,明确考
点,辨别易错点,稳定和
35(2)题,15分; 2022全国甲卷35(3)题,15分;2022
创新是命题的特点,其命
海南卷19(3)题,14分;2022福建卷14题,10分;2022
题热点主要集中以下:(1)
山东卷16题,12分;2021湖北卷9题,3分;2021海南
原子结构与性质:基态原
卷10题,4分;2021河北卷17(3)(4)(5)(6)题,15分;
子核外电子排布、第一电
2021全国乙卷35(3)题,15分;2021全国甲卷35(1)(2)(3)
离能和电负性递变规律
题,15分;2021海南卷19(4)题,14分;2021山东卷19
等;(2)分子结构与性质:
题,12分;2021湖南卷18(2)题,15分;
共价键类型的判断、原子
2023山东卷5题,2分;2023北京卷1题,3分;2023
晶体的类型与性 轨道杂化类型、分子构型
全国新课标卷9题,6分;2022山东卷5题,2分;2022
质比较 判断等;(3)晶体结构与性
湖北卷7题,3分;质:晶体类型的判断、晶
体熔沸点高低的比较、氢
键对溶解性的影响、晶体
2023湖北卷15题,3分;2023湖南卷11题,4分;2023
密度和晶体参数的计算、
辽宁卷14题,3分;2023全国乙卷35(3)题,15分;
晶体空间利用率的计算
2023全国甲卷35题,15分;2023浙江1月选考17(3)
等。从题型上看,一般给
题,12分;2023浙江6月选考17(3)题,12分;2023山
出一定的知识背景,然后
东卷16(1)(3)题,12分;2023北京卷15(5)(6)题,15分;
设置3~4个小问题,每一
2022湖北卷9题,3分;2022山东卷15题,4分;2022
个小题考查相应的知识要
全国甲卷3(5)5题,15分;2022全国乙卷35(3)(4)题,15
点仍是今后命题的基本模
晶体结构与性质 分;2022重庆卷18(3)(4)题,15分;2022北京卷15(4)(5)
式。原子核外电子排布式
题,15分;2022湖南卷18(4)(5)(6)题,14分;2022广东
(价电子排布式)、杂化方
卷20(6)题,14分;2022江苏卷17(2)题,17分;2021湖
式、化学键类型、晶体结
北卷10题,3分;2023海南卷5题,2分;2021全国乙
构、配合物、电负性、电
卷35(4)题,15分;2021全国甲卷35(4)题,15分;2021
离能大小的比较、等电子
湖南卷18(3)题,14分;2021河北卷17(7)题,15分; 体知识是高考的热点。
2021广东卷19(6)题,14分;2021山东卷16(4)题,12
分;2021海南卷19(6)题,14分;
物质结构与性 质综合考点一 原子结构与性质
1.(2022•辽宁省选择性考试)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均
有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是( )
A.X能与多种元素形成共价键 B.简单氢化物沸点:
C.第一电离能: D.电负性:
【答案】B
【解析】短周期元素X、Y、Z、W、Q原子序数依次增大,W简单离子在同周期离子中半径最小,说
明W为第三周期元素Al。短周期元素的基态原子中有两个单电子,可分类讨论:①为第二周期元素时,
最外层电子排布为2s22p2或2s22p4,即C或O;②为第三周期元素时,最外层电子排布为3s23p2或3s23p4,
即Si或S。Q与Z同主族,结合原子序数大小关系可知,则X、Z、Q分别为C、O和S,则Y为N。A项,
X为C,能与多种元素(H、O、N、P、S等)形成共价键,A正确;B项,Z和Q形成的简单氢化物为HO
2
和HS,由于HO分子间能形成氢键,故HO沸点高于HS,B错误;C项,Y为N,Z为O,N的最外层
2 2 2 2
p轨道电子为半充满结构,比较稳定,故其第一电离能比O大,C正确;D项,W为Al,Z为O,O的电
负性更大,D正确;故选B。
2.(2021•山东卷)X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合
物能以[XY ]+[XY ]-的形式存在。下列说法错误的是( )
4 6
A.原子半径:X>Y B.简单氢化物的还原性:X>Y
C.同周期元素形成的单质中Y氧化性最强 D.同周期中第一电离能小于X的元素有4种
【答案】D
【解析】Y位于第三周期,且最高正价与最低负价的代数和为6,则Y是Cl元素,由X、Y形成的阴
离子和阳离子知,X与Y容易形成共价键,根据化合物的形式知X是P元素。A项,P与Cl在同一周期,
则P半径大,即X>Y,A项不符合题意;B项,两者对应的简单氢化物分别是PH 和HCl,半径是P3-
3
>Cl-,所以PH 的失电子能力强,还原性强,即X>Y,B项不符合题意;C项,同周期元素从左往右,金
3
属性减弱,非金属性增强,各元素对应的金属单质还原性减弱,非金属单质的氧化性增强,所以Cl 的氧
2
化性最强,C项不符合题意;D项,同一周期,从左到右,第一电离能呈现增大的趋势,第VA族元素的
第一电离能大于相邻元素的第一电离能;所以第三周期第一电离能从小到大依次为Na、Al、Mg、Si、S、
P、Cl,所以有5种,D项符合题意;故选D。
3.(2020•山东卷)短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数是其最高
能级电子数的2倍,Z可与X形成淡黄色化合物ZX,Y、W最外层电子数相同。下列说法正确的是( )
2 2
A.第一电离能:W>X>Y>Z B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z D.氢化物水溶液的酸性:Y>W
【答案】C
【解析】四种短周期主族元素,基态X原子的电子总数是其最高能级电子数的2倍,设若X为第二周
期元素原子,则X可能为Be或O,若X为第三周期元素原子,则均不满足题意,Z与X能形成ZX 的淡
2 2
黄色化合物,该淡黄色固体为NaO,则X为O元素,Z为Na元素;Y与W的最外层电子数相同,则Y
2 2
为F元素,W为Cl元素。A项,同一周期从左向右第一电离能总趋势为逐渐增大,同一主族从上到下第一
电离能逐渐减小,故四种元素中第一电离能从大到小的顺序为F>O>Cl>Na,A错误;B项,单质的氧化性越强,简单离子的还原性越弱,O、F、Cl三种元素中F 的氧化性最强O 的氧化性最弱,故简单离子的
2 2
还原性O2->Cl->F-,B错误;C项,电子层数越多简单离子半径越大,相同结构的离子,原子序数越大半
径越小,故四种元素中离子半径从大到小的顺序为Cl->O2->F->Na+,C正确;D项,F元素的非金属性强
于Cl元素,则形成氢化物后F原子束缚H原子的能力强于Cl原子,在水溶液中HF不容易发生电离,故
HCl的酸性强于HF,D错误;故选C。
4.(2023•浙江省6月选考,11)X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位
于同一周期,且只有X、 Y元素相邻。X基态原子核外有2个未成对电子,W原子在同周期中原子半径最
大。下列说法不正确的是( )
A.第一电离能: Y>Z>X
B.电负性: Z>Y>X>W
C.Z、W原子形成稀有气体电子构型的简单离子的半径:W<Z
D.WX 与水反应生成产物之一是非极性分子
2 2
【答案】A
【解析】X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,且只有
X、 Y元素相邻。X基态原子核外有2个未成对电子,则X为C,Y为N,Z为F,W原子在同周期中原
子半径最大,则W为Na。A项,根据同周期从左到右第一电离能呈增大趋势,但第IIA族大于第IIIA族,
第VA族大于第VIA族,则第一电离能: Z>Y>X,故A错误;B项,根据同周期从左到右电负性逐渐增
大,同主族从上到下电负性逐渐减小,则电负性:Z>Y>X>W,故B正确;C项,根据同电子层结构核
多径小,则Z、W原子形成稀有气体电子构型的简单离子的半径:W<Z,故C正确;D项,WX 与水反
2 2
应生成产物之一为乙炔,乙炔是非极性分子,故D正确。故选A。
5.(2023•全国新课标卷,9)一种可吸附甲醇的材料,其化学式为[C(NH )][B(OCH )]Cl,部分晶体结
2 3 4 3 4
构如下图所示,其中[C(NH )]+为平面结构。
2 3
下列说法正确的是( )
A.该晶体中存在N-H…O氢键
B.基态原子的第一电离能:
C.基态原子未成对电子数:
D.晶体中B、N和O原子轨道的杂化类型相同
【答案】A
【解析】A项,由晶体结构图可知,[C(NH )]+中的-NH 的H与[B(OCH )]-中的O形成氢键,因此,
2 3 2 3 4
该晶体中存在N-H…O氢键,A正确;B项,同一周期元素原子的第一电离能呈递增趋势,但是第ⅡA、
ⅤA元素的原子结构比较稳定,其第一电离能高于同周期的相邻元素的原子,因此,基态原子的第一电离
能从小到大的顺序为C< O < N,B不正确;C项,B、C、O、N的未成对电子数分别为1、2、2、3,因此,基态原子未成对电子数B①>②
B.电子排布属于基态原子(或离子)的是:①②
C.电离一个电子所需最低能量:①>②>③
D.得电子能力:①>②
【答案】(2)AB
【解析】(2)电子排布式分别为:①[Ne]3s23p2、②[Ne]3s23p1、③[Ne]3s23p14s1,可推知分别为基态Si原
子、基态Al原子、激发态Si原子;A项,根据微粒电子层数及各层电子数多少可推知,微粒半径:
③>①>②,A正确;B项,根据上述分析可知,电子排布属于基态原子(或离子)的是:①②,B正确;C项,
Si为非金属失电子能力比Al弱,电离一个电子所需最低能量:①>③>②,C错误;D项,非金属Si的得
电子能力强于金属Al,得电子能力:②>①,D错误;故选AB。
11.(2023•北京卷,15节选)硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根(S O2-)可看作是
2 3
SO 2-中的一个 原子被 原子取代的产物。
4
(1)基态 原子价层电子排布式是 。
(2)比较 原子和 原子的第一电离能大小,从原子结构的角度说明理由: 。
【答案】(1) 3s23p4
(2) I (O)>I (S),氧原子半径小,原子核对最外层电子的吸引力大,不易失去一个电子
1 1
【解析】(1)S是第三周期ⅥA族元素,基态S原子价层电子排布式为3s23p4;(2)S和O为同主族元素,
O原子核外有2个电子层,S原子核外有3个电子层,O原子半径小,原子核对最外层电子的吸引力大,不
易失去1个电子,即O的第一电离能大于S的第一电离能。
12.(2022•全国乙卷,35节选)卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列
问题:
(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)
a. 1s22s22p43s1 b. 1s22s22p43d2 c. 1s22s12p5 d. 1s22s22p33p2
【答案】(1) ad d
【解析】(1)F的原子序数为9,其基态原子电子排布式为1s22s22p5。a项,1s22s22p43s1,基态氟原子2p
能级上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;b项,1s22s22p43d2,核外共10个电子,
不是氟原子,b错误;c项,1s22s12p5,核外共8个电子,不是氟原子,c错误;d项,1s22s22p33p2,基态氟
原子2p能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,d正确;故选ad;而同一原子3p能级
的能量比3s能级的能量高,因此能量最高的是1s22s22p33p2,故选d。
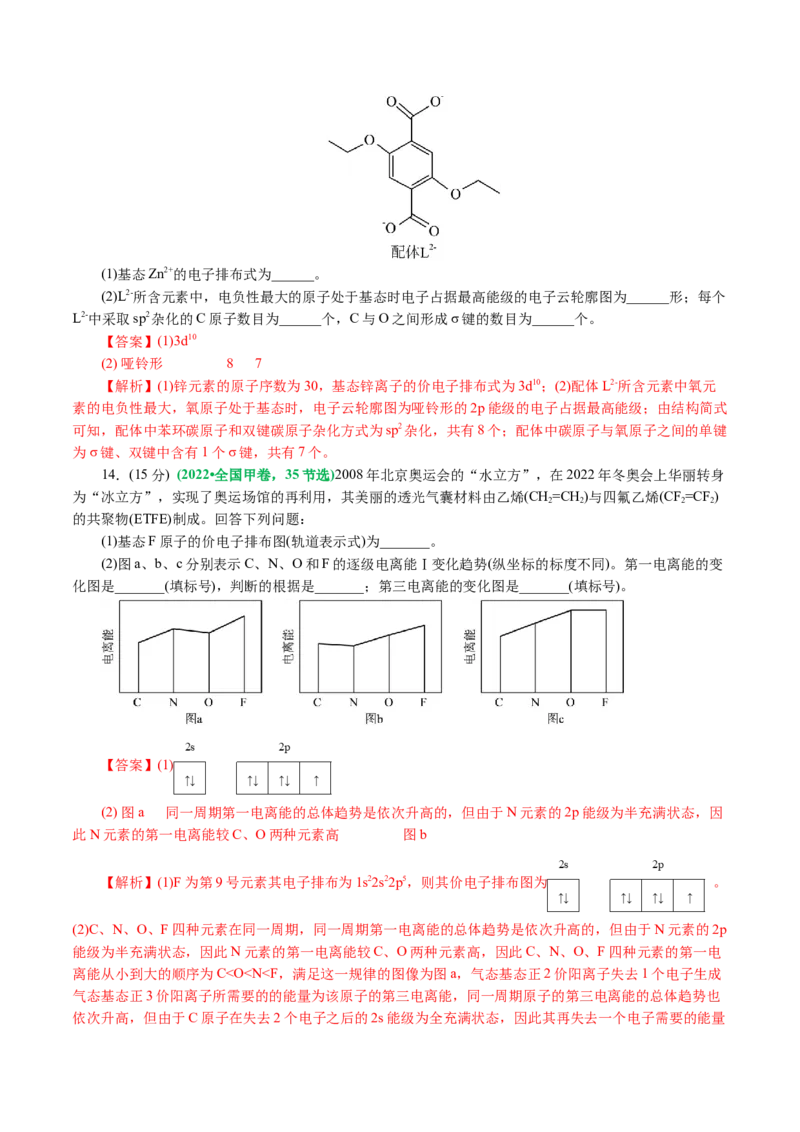
13.(2022•重庆卷,18节选)(15分)配位化合物X由配体L2-(如图)和具有正四面体结构的[Zn O]6+构成。
4(1)基态Zn2+的电子排布式为______。
(2)L2-所含元素中,电负性最大的原子处于基态时电子占据最高能级的电子云轮廓图为______形;每个
L2-中采取sp2杂化的C原子数目为______个,C与O之间形成σ键的数目为______个。
【答案】(1)3d10
(2) 哑铃形 8 7
【解析】(1)锌元素的原子序数为30,基态锌离子的价电子排布式为3d10;(2)配体L2-所含元素中氧元
素的电负性最大,氧原子处于基态时,电子云轮廓图为哑铃形的2p能级的电子占据最高能级;由结构简式
可知,配体中苯环碳原子和双键碳原子杂化方式为sp2杂化,共有8个;配体中碳原子与氧原子之间的单键
为σ键、双键中含有1个σ键,共有7个。
14.(15分) (2022•全国甲卷,35节选)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身
为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四氟乙烯(CF=CF )
2 2 2 2
的共聚物(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变
化图是_______(填标号),判断的根据是_______;第三电离能的变化图是_______(填标号)。
【答案】(1)
(2) 图a 同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因
此N元素的第一电离能较C、O两种元素高 图b
【解析】(1)F为第9号元素其电子排布为1s22s22p5,则其价电子排布图为 。
(2)C、N、O、F四种元素在同一周期,同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p
能级为半充满状态,因此N元素的第一电离能较C、O两种元素高,因此C、N、O、F四种元素的第一电
离能从小到大的顺序为C”“<”或“=”),原因是_______。
3 3
(2)富马酸亚铁(FeC HO)是一种补铁剂。富马酸分子的结构模型如图所示:
4 2 4
①富马酸分子中 键与 键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。
【答案】(1) [Ar] 3d104s24p4 6 > SeO 的空间构型为平面三角形,SeO2-的空间构型为三
3 3
角锥形
(2) 11:3 O>C>H>Fe
【解析】(1)①硒元素的原子序数为34,基态原子的电子排布式为[Ar] 3d104s24p4,故答案为:[Ar]
3d104s24p4;②由结构简式可知,乙烷硒啉的分子结构对称,分子中含有6种化学环境不同的碳原子;③三
氧化硒分子中硒原子的价层电子对数为3,孤对电子对数为0,分子的空间构型为平面三角形,键角为
120°,亚硒酸根离子中硒原子的价层电子对数为4,孤对电子对数为1,离子的空间构型为三角锥形,键角
小于120°;(2)①由球棍模型可知,富马酸的结构式为HOOCCH=CHCOOH,分子中的单键为σ键,双键中
含有1个σ键和1个π键,则分子中σ键和π键的数目比为11:3;②金属元素的电负性小于非金属元素,
则铁元素的电负性最小,非金属元素的非金属性越强,电负性越大,氢碳氧的非金属性依次增强,则电负
性依次增大,所以富马酸亚铁中四种元素的电负性由大到小的顺序为O>C>H>Fe。
19.(2022•广东选择性考试,20节选)硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域
具有重要应用。自我国科学家发现聚集诱导发光( )效应以来, 在发光材料、生物医学等领域引起
广泛关注。一种含 的新型 分子 的合成路线如下:
(1) Se与S同族,基态硒原子价电子排布式为_______。
【答案】(1)4s24p4【解析】(1)基态硫原子价电子排布式为3s23p4,Se与S同族,Se为第四周期元素,因此基态硒原子价
电子排布式为4s24p4。
15.(2021•山东卷,16节选)非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有________种。
(2)O、F、Cl电负性由大到小的顺序为____________;OF 分子的空间构型为_______;OF 的熔、沸
2 2
点_______ (填“高于”或“低于”)Cl O,原因是______________________。
2
【答案】(1)9 (2)F>O>Cl 角(V)形 低于 OF 和ClO都是分子晶体,结构相似,ClO的
2 2 2
相对分子质量大,ClO的熔、沸点高
2
【解析】(1)基态F原子共有9个核外电子,则每个电子都有对应的轨道和自旋状态,所以核外电子的
运动状态有9种;(2)电负性一定程度上相当于得电子能力,半径越小,得电子能力越强,电负性越大,半
径由小到大的顺序为F、O、Cl,所以电负性大小顺序为F>O>Cl;根据VSEPR理论有 ,去
掉2对孤对电子,知OF 分子的空间构型是角形;OF 和ClO都是分子晶体,结构相似,ClO的相对分子
2 2 2 2
质量大,ClO的熔、沸点高。
2
20.(2021•全国乙卷,35节选)过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中
有着广泛应用。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是_______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为 [Ar]3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
【答案】(1)AC
【解析】(1) A项,基态原子满足能量最低原理,Cr有24个核外电子,轨道处于半充满时体系总能量
低,核外电子排布应为[Ar]3d54s1,A正确;B项, Cr核外电子排布为[Ar]3d54s1,由于能级交错,3d轨道
能量高于4s轨道的能量,即3d电子能量较高,B错误;C项,电负性为原子对键合电子的吸引力,同周期
除零族原子序数越大电负性越强,钾与铬位于同周期,铬原子序数大于钾,故铬电负性比钾高,原子对键
合电子的吸引力比钾大,C正确; 故选AC。
21.(2021•湖南选择性考试,18节选)硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的电子排布图为 ,晶体硅和碳化硅熔点较高的是
(填化学式);
【答案】(1) ; SiC
【解析】(1)Si位于周期表中第3周期第ⅣA族,基态原子的价电子排布式为3s23p2,则基态Si原子的
价电子排布图为: ;晶体硅、碳化硅均属于原子晶体,原子半径:Si>C,键长:
C﹣Si<Si﹣Si,则键能:C﹣Si>Si﹣Si,所以熔点:碳化硅>晶体硅,晶体硅和碳化硅熔点较高的是
SiC。
22.(2021•河北选择性考试,17节选)KH PO 晶体具有优异的非线性光学性能。我国科学工作者制备
2 4
的超大KH PO 晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
2 4
(1)在KH PO 的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是___________(填离
2 4
子符号)。(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用- 表示,称
为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为____________。
【答案】(1)K+和P3- (2) 或
(3)在原子数目相同的条件下,N 比N 具有更低的能量,而P 比P 具有更低的能量,能量越低越稳定
2 4 4 2
【解析】(1)在KH PO 的四种组成元素各自所能形成的简单离子分别为H+ (或H-)、O2-、K+和P3-,其
2 4
中核外电子排布相同的是K+和P3-。(2)对于基态的磷原子,其价电子排布式为3s23p3,其中3s轨道的2个
电子自旋状态相反,自旋磁量子数的代数和为0;根据洪特规则可知,其3p轨道的3个电子的自旋状态相
同,因此,基态磷原子的价电子的自旋磁量子数的代数和为 或 。(3)根据表中的相关共价键的键能
可知,若6mol N形成类似白磷分子结构的N 分子,可以释放出的能量为193kJ6=1158kJ;若6mol N形成
4
N 分子,则可释放的能量为946kJ2=1892kJ,显然,形成N 分子放出的能量更多,故在N数目相同的条
2 2
件下,N 具有更低的能量,能量越低越稳定。同理,若6mol P形成P 分子,可以释放出的能量为
2 4
197kJ6=1182kJ;若6mol P形成P 分子,则可释放的能量为489kJ2=978kJ,显然,形成P 分子放出的能
2 4
量更多,故在P数目相同的条件下,P 具有更低的能量,能量越低越稳定。
4
23.(2021•广东选择性考试,19节选)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,
解毒剂化合物I可与氧化汞生成化合物Ⅱ。
(1)基态
硫原子价电子排布式为__________。
(2)H S、CH、HO的沸点由高到低顺序为__________。
2 4 2
(3)汞的原子序数为80,位于元素周期表第______周期第ⅡB族。
【答案】(1)3s23p4 (2)H O>HS>CH (3)六
2 2 4
【解析】(1)基态硫原子核外电子排布式为1s22s22p63s23p4,因此基态硫原子价电子排布式为3s23p4;
(2)H S、CH、HO均为分子晶体,HO分子间存在氢键,沸点较高,HS、CH 的分子间范德华力随相对
2 4 2 2 2 4
分子质量增大而增加,因此沸点由高到低顺序为:HO>HS>CH;(3)第六周期0族元素的原子序数为86,
2 2 4
因此第80号元素Hg位于第六周期第ⅡB族。
24.(2021•海南选择性考试,19节选) (14分)金属羰基配位化合物在催化反应中有着重要应用。
HMn(CO) 是锰的一种简单羰基配位化合物,其结构示意图如下。
5回答问题:
(1)基态锰原子的价层电子排布式为___________。
(2)配位化合物中的中心原子配位数是指和中心原子直接成键的原子的数目。HMn(CO) 中锰原子的配
5
位数为___________。
(3)第一电离能的大小:C___________O(填“大于”或“小于”)。
【答案】(1)3d54s2 (2)6 (3)小于
【解析】(1)Mn元素是第25号元素,其电子排布式为1s22s22p63s23p63d54s2,所以本问应填“3d54s2”;
(2)由题干图例所示,HMn(CO) 中Mn原子以配位键连接5个C原子,1个H原子,所以本问应填“6”;(3)
5
根据元素周期律,总体规律同一周期元素从左到右第一电离能依次增强,特殊规律同周期IIA族第一电离
能大于IIIA族,VA族第一电离能大于VIA族,C是IVA族,O是VIA族,不涉及特殊规律,所以本问应
填“小于”。
牢记单质或化合物具有“特性”的元素
(1)形成化合物种类最多的元素或对应单质是自然界中硬度最大的物质的元素:C。
(2)空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素:N。
(3)地壳中含量最多的元素或简单氢化物在通常情况下呈液态的元素:O。
(4)地壳中含量最多的金属元素或最高价氧化物及其对应水化物既能与强酸反应,又能与强碱反应的元
素:Al。
(5)最活泼的非金属元素或无正化合价的元素或无含氧酸的非金属元素或无氧酸可腐蚀玻璃的元素或气
态氢化物最稳定的元素或阴离子的还原性最弱的元素:F。
(6)(除放射性元素外)最活泼的金属元素或最高价氧化物对应水化物的碱性最强的元素或阳离子的氧化
性最弱的元素:Cs。
(7)焰色试验呈黄色的元素:Na;焰色试验呈紫色(透过蓝色钴玻璃观察)的元素:K;焰色试验呈绿色
的元素:Cu。
(8)单质密度最小的元素:H;单质密度最小的金属元素:Li。
(9)常温下单质呈液态的非金属元素:Br;常温下单质呈液态的金属元素:Hg。
(10)元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应的元素:N;元素的气态氢化
物和它的最高价氧化物对应的水化物能发生氧化还原反应的元素:S。
(11)单质为常见的半导体材料的元素:Si、Ge。
(12)气态氢化物能和它的氧化物在常温下反应生成该元素的单质的元素:S。
(13)单质在常温下能与水反应放出气体的短周期元素:Li、Na、F。
(14)若X是由短周期主族元素组成的二元化合物,0.01 mol·L-1 X溶液的pH=2,则X是HCl;若X是
由短周期主族元素组成的三元化合物,0.01 mol·L-1 X溶液的pH=2,则X是HNO 或HClO ;若X是由短
3 4
周期主族元素组成的三元化合物,0.005 mol·L-1 X溶液的pH=2,则X是HSO 。
2 4
1.原子结构与化学键
(1)微粒间“三个”数量关系中性原子:核电荷数=核内质子数=核外电子数=原子序数
阴离子:核外电子数=质子数+所带的电荷数
阳离子:核外电子数=质子数-所带的电荷数
(2)“四同”的判断方法——关键是抓住描述的对象
①同位素——原子,如
1 H、2 H、3
H。
1 1 1
②同素异形体——单质,如O 与O,金刚石与石墨,红磷与白磷。
2 3
③同系物——有机化合物,如CHCH、CHCHCH。
3 3 3 2 3
④同分异构体——化合物,如正戊烷与新戊烷。
(3)10e-、18e-微粒
10电子体和18电子体是元素推断题的重要突破口。
以Ne为中心记忆10电子体:
Ne
以Ar为中心记忆18电子体:
Ar
此外,由10电子体中的CH 、NH 、HO、HF失去一个H原子后的剩余部分如—CH 、—NH 、—
4 3 2 3 2
OH、—F等为9电子体,两两组合得到的物质如CHCH、CHOH、HO、NH、F 等为18电子体。
3 3 3 2 2 2 4 2
(4)化学键与化合物的关系
(5)规避化学键判断的易错点
①在离子化合物中一般既含有金属元素又含有非金属元素(铵盐除外);共价化合物一般只含有非金属
元素,但个别含有金属元素,如AlCl ;只含有非金属元素的化合物不一定是共价化合物,如铵盐。
3
②非金属单质只含共价键或不含化学键(稀有气体)。
③气态氢化物是共价化合物,只含共价键;而金属氢化物(如NaH)是离子化合物,含离子键。
④分子的稳定性与分子间作用力无关,而与分子内部化学键的强弱有关。
2.原子核外电子排布的“三”规律
能量最
原子核外电子总是先占据能量最低的原子轨道
低原理
泡利原理 每个原子轨道上最多只能容纳2个自旋状态相反的电子
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨
洪特规则
道,而且自旋状态相同3.基态原子核外电子排布的表示方法
表示方法 含义 举例
原子或离子结
表示核外电子分层排布和核内质子数
构示意图
··
电子式 表示原子最外层电子数目
·Cl·
·
··
核外电子排布 S:1s22s22p63s23p4或[Ne]3s23p4
表示每个能级上排布的电子数
式 S2-:1s22s22p63s23p6
电子排布图
表示每个原子轨道中电子的运动状态
(轨道表示式)
价电子排布式 S:3s23p4
表示价电子的排布
或排布图
Fe:3d64s2
4.电离能及其应用
(1)电离能的变化规律
①同周期从左到右(ⅠA 族→0 族),第一电离能呈增大的趋势。但第Ⅱ A 族(ns2np0)和第Ⅴ A 族
(ns2np3),因为p轨道处于全空或半充满状态,比较稳定,所以其第一电离能大于同周期右侧相邻的第Ⅲ A
族或第ⅥA族元素,如第一电离能:Mg>Al、P>S。
②逐级电离能逐渐增大(Ir(Mg)>r(Al)>r(Si)>r(P)>r(S)>r(Cl);r(O2-)>r(F-)>r(Na+)>r(Mg2+)>r(Al3+)。
“三看”核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。
例:r(Cl-)>r(Cl);r(Fe2+)>r(Fe3+)。
8.金属性、非金属性强弱的判断题型一 原子核外电子排布
1.下列说法正确的是( )
A.金属钠的焰色是黄色,它的产生与电子的跃迁吸收能量有关
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.氢原子核外只有一个电子,它产生的原子光谱中只有一根或明或暗的线
D.光谱分析就是利用原子光谱上的特征谱线来鉴定元素
【答案】D
【解析】A项,光的产生与与电子的跃迁释放能量有关,A错误;B项,能级和能层只是表明电子在
该处出现的概率大小,并不表示电子运动的位置,B错误;C项,氢原子核外只有一个电子,但它的激发
态存在多种情况,当电子跃迁回较低状态时释放能量,发出光线,故它产生的原子光谱中不会只有一根或
明或暗的线,C错误;D项,光谱分析就是利用原子光谱上的特征谱线来鉴定元素,D正确;故选D。
2.(2024·浙江省宁波市鄞州中学选考模拟)下列说法或有关化学用语的表达正确的是( )
A.能级能量大小关系:4f>5d
B.基态铜原子( Cu)的价层电子排布式:3d94s2
29
C.Ca处于激发态的电子排布式可能为:1s22s22p63s23p64p2
D.基态 的轨道表示式:
【答案】C
【解析】A项,由构造原理可知,4f的能力低于5d,故A错误;B项,铜元素的原子序数为29,基态
原子的价层电子排布式为3d104s1,故B错误;C项,钙元素的原子序数为20,基态原子的电子排布式为
1s22s22p63s23p64s2,则发态的电子排布式可能为1s22s22p63s23p64p2,故C正确;D项,钠元素的原子序数为
11,基态钠离子的电子排布式为1s22s22p6,轨道表示式为 ,故D错误;故选C。
3.(2023·湖南省衡阳市期末)磷灰石是制造磷肥和含磷化合物的最主要矿物原料,可表示为
Ca(PO )(F,Cl,OH)。下列有关化学用语或图示表达正确的是( )
5 4 3
A.OH-的电子式:
B.基态磷原子的最外层电子的轨道表示式:
C.基态Ca原子最高能级的电子云轮廓图:
D.中子数为20的氯原子:
【答案】B
【解析】A项,OH-的电子式为: ,故A错误;B项,基态磷原子的最外层电子的排布式为
3s23p3,其轨道表示式为: ,故B正确;C项,基态Ca原子最高能级为4s,其电子云轮廓图:,故C错误;D项,中子数为20的氯原子,质量数为17+20=37,该氯原子为: ,故D
错误。故选B。
4.(2023·安徽省黄山市期末)下列各项叙述中,正确的是( )
A.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同
B.价电子排布式为5s25p1的元素位于第五周期第ⅠA族,是s区元素
C.钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态
D. Cr原子的电子排布式是1s22s22p63s23p63d44s2
24
【答案】A
【解析】A项,所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同,A正确;B项,
价电子排布式为5s25p1的元素位于第五周期第IIIA族,是p区元素,B错误;C项,钠原子由
1s22s22p63s1→1s22s22p63p1时,原子吸收能量,由基态转化成激发态,C错误;D项, Cr原子的电子排布式
24
是1s22s22p63s23p63d54s1,D错误; 故选A。
5.(2023·广东省佛山市期末)人类对核外电子运动的认知不断进步。下列说法正确的是( )
A.电子在线性轨道上绕核运行
B.电子从激发态跃迁到基态时能产生吸收光谱
C. 、 、 轨道相互平行、能量相等
D.2s轨道比1s轨道大,其空间包含了 轨道
【答案】D
【解析】A项,电子在核外是在一个有形状的轨道空间内运动,A错误;B项,电子从激发态跃迁到
基态时能产生发射光谱,B错误;C项, 、 、 轨道相互垂直、能量相等,C错误;D项,2s轨
道比1s轨道大,其空间包含了1s轨道,D正确;故选D。
6.下列关于价电子排布为3s23p4的原子描述正确的是( )
A.它的元素符号为O
B.它的核外电子排布式为1s22s22p63s23p4
C.可以与H 化合生成液态化合物
2
D.其轨道表示式为
【答案】B
【解析】价电子排布为3s23p4的粒子,其基态原子核外电子排布式为1s22s22p63s23p4,其核外电子数为
16,为S元素, A错误, B正确;一定条件下,它可与H 生成气态化合物HS,C错误;S原子核外电子
2 2
排布遵循能量最低原理、泡利不相容原理、洪特规则,其轨道表示式为 ,D
错误。
7.X、Y、Z、W、P五种元素,其核电荷数依次增大。X基态原子核外只有三个能级,且各能级电子
数相等;Z原子的核外电子有8种运动状态;Z与W元素位于同一族;P原子核外有4个能层,最外层只
有1个电子,其余各层均排满电子。下列说法正确的是( )
A.Z、Y、X元素的第一电离能依次减小B.Y基态原子的轨道表示式:
C.P原子的价层电子排布为
D.P单质分别与Z、W单质反应,产物中P的化合价一定相同
【答案】B
【解析】X基态原子核外只有三个能级,且各能级电子数相等,为1s22s22p2,为C元素,Z原子的核
外电子有8种运动状态,Z为O原子,Y为N元素,Z与W元素位于同一族,W为S元素,P原子核外有
4个能层,最外层只有1个电子,其余各层均排满电子,为 ,为Cu元素。A项,Z为
O元素,Y为N元素,X为C元素,第一电离能的大小为:N>C>O,A错误;B项,Y为N元素,基态
原子的轨道表示式: ,B正确;C项,P为Cu元素,价层电子排布为: ,
C错误;D项,Cu和O 反应生成CuO,Cu元素的化合价为+2价,Cu和S反应生成Cu S,Cu元素的化合
2 2
价为+1价,D错误;故选B。
8.主族元素的原子可失去最外层电子形成阳离子,主族元素的原子也可得到电子填充在最外层形成
阴离子。下列各原子或离子的电子排布式错误的是( )
A.Ca2+ 1s22s22p63s23p6 B.F- 1s22s22p5 C.S 1s22s22p63s23p4 D.Ar 1s22s22p63s23p6
【答案】B
【解析】首先写出各原子的正确的电子排布式:Ca 1s22s22p63s23p64s2,F 1s22s22p5,S 1s22s22p63s23p4,
Ar 1s22s22p63s23p6,A中生成Ca2+失去了4s轨道上的2个电子,B中得1个电子进入2p轨道,电子排布为
1s22s22p6。
9.已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A.某元素原子的第二电子层电子排布图为
B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层上电子数为6
D.某元素的原子外围电子排布式为5s25p1
【答案】D
【解析】A中只能说明该元素的L层有8个电子,无法确定其在周期表中的位置;某些非金属元素有
多种化合价,+4价不一定是其最高化合价,无法确定;C中根据最外层电子数只能确定族序数,无法确
定周期数;D可确定该元素在第五周期第ⅢA族。
10.现有主族元素X、Y、Z,X原子的最外层电子排布式为ns1,Y原子M能层的p能级上有4个电
子,Z原子的最外层p能级上也有4个电子,且Z原子的核外电子数比Y原子少8个。由这三种元素组成
的化合物不可能是( )
A.XYZ B.XYZ C.XYZ D.XYZ
2 3 2 4 2 2 3 4
【答案】D
【解析】因为X原子的最外层电子排布式为ns1,故X位于ⅠA族,化合价为+1价;根据Y原子M
能层的p能级上有4个电子,可知其电子排布式为1s22s22p63s23p4,故Y为S;又因为Z原子的最外层p能
级上也有4个电子,说明Z和S为同一主族,又知Z原子的核外电子数比Y原子少8个,故Z为O。元素
X、Y、Z可以组成HSO 、NaSO 、KSO 等,A符合;也可以组成HSO 、NaSO 、KSO 等,B符合;
2 3 2 3 2 3 2 4 2 4 2 4
还可以组成NaSO、KSO 等,C符合。
2 2 3 2 2 3
11.(2023·江苏省南通市海安区高三期中)当汽车遭受一定碰撞力量以后,安全气囊中的物质会发生剧烈的反应:NaN +KNO =K O+Na O+N↑(未配平),生成大量气体。下列说法正确的是( )
3 3 2 2 2
A.半径大小:r(Na+)χ(O)
C.电离能大小:I1(Na)>I1(O) D.碱性强弱:KOH I (S) B.半径大小: r(Al3+)>r(Na+)
1 1
C.电负性大小: D.碱性强弱:Fe(OH) >NaOH
3
【答案】A
【解析】A项,同主族元素,从上到下元素的第一电离能依次减小,则氧元素的第一电离能大于硫元
素,故A正确;B项,电子层结构相同的离子,核电荷数越大,离子半径越小,则铝离子的离子半径小于
钠离子,故B错误;C项,元素的非金属性越强,电负性越大,氧元素的非金属性强于碳元素,则氧元素
的电负性大于碳元素,故C错误;D项,氢氧化钠是强碱,氢氧化铁是弱碱,则氢氧化钠的碱性强于氢氧
化铁,故D错误;故选A。
13.(2024·江苏常州市教育学会高三学业水平监测)铁系超导材料Fe-Sm-As-F-O中基态Sm原子的价电
子排布为 。下列说法正确的是( )
A.Sm位于元素周期表中的f区 B.Fe成为阳离子时先失去3d轨道电子
C.氢化物的稳定性:AsH > H O D.第一电离能:I(F)<I(O)
3 2 1 1
【答案】A
【解析】A项,基态Sm原子的价电子排布为4f26s2,4f轨道未充满,则Sm位于元素周期表中的f区,
A正确;B项,Fe的价层电子排布式为3d64s2,Fe生成阳离子时首先失去4s轨道上2个电子,再失去3d轨
道上的电子,B错误;C项,非金属性:O>P>As,非金属性越强,简单氢化物越稳定,则氢化物的稳定性:
AsH < H O,C错误;D项,F、O位于第二周期,第二周期从左向右第一电离能呈增大趋势,且F、O属
3 2
于VIIA、VIA族,则第一电离能: I(F)> I (O),D错误;故选A。
1 1
14.气态原子生成+1价气态阳离子所需要的能量称为第一电离能。元素的第一电离能是衡量元素金
属性强弱的一种尺度。下列有关说法不正确的是( )
A.元素的第一电离能越大,其金属性越弱
B.元素的第一电离能越小,其金属性越强
C.金属单质跟酸反应的难易,只跟该金属元素的第一电离能有关
D.金属单质跟酸反应的难易,除跟该金属元素的第一电离能有关外,还与该金属原子失去电子后在
水溶液里形成水合离子的变化有关
【答案】C
【解析】A项,元素的第一电离能越大,越难失电子,其金属性越弱,故A项正确;B项,元素的第
一电离能越小,越易失电子,其金属性越强,故B项正确;C项,第一电离能指的是气态原子的性质,而
金属单质跟酸反应是金属在水溶液中的活动性,故C项错误;D项,金属单质跟酸反应是金属在水溶液中的活动性,金属单质跟酸反应的难易,除跟该金属元素的第一电离能有关外,还与该金属原子失去电子后
在水溶液里形成水合离子的变化有关,故D项正确;故选C。
15.(2024·江苏泰州高三期中)X、Y、Z、W四种短周期主族元素,原子序数依次增大。X与Y相邻,
X基态原子核外有2个未成对电子;Z是元素周期表中电负性最大的元素。W原子在同周期中原子半径最
大。下列说法不正确的是( )
A.第一电离能:I(Y)> I (Z)> I (X)
1 1 1
B.最高价氧化物对应水化物的酸性:Y>X
C.Z、W的简单离子的半径: r( Z)>r(W)
D.简单气态氢化物的热稳定性:Z>Y
【答案】A
【解析】Z是元素周期表中电负性最大的元素,Z为F元素;W的原子序数大于Z,所以W是第三周
期元素,又因为W原子在同周期中原子半径最大,所以W为Na元素;X基态原子核外有2个未成对电子,
且X位于第二周期,所以X为C元素或O元素;又因为X与Y相邻,且Y的原子序数大于X,所以X只
能是C元素,Y是N元素。A项,同周期元素第一电离能随着原子序数增大有增大的趋势,所以第一电离
能:F>N>C,即I(Z)>I (Y)> I (X) ,A项错误;B项,N元素的最高价氧化物对应水化物为硝酸,C元
1 1 1
素的最高价氧化物对应水化物为碳酸,硝酸酸性大于碳酸,B项正确;C项,氟离子和钠离子的核外电子
排布相同,核电荷数大的离子半径小,氟离子的半径大于钠离子,C项正确;D项,非金属性越强,简单
气态氢化物的热稳定性越稳定,所以简单气态氢化物的热稳定性:F>N,D项正确;故选A。
16.已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。根据下表所列数据判断错误的是( )
元素 I I I I
1 2 3 4
X 500 4 600 6 900 9 500
Y 580 1 800 2 700 11 600
A.元素X的常见化合价是+1价
B.元素Y是第ⅢA族的元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第三周期,它可与冷水剧烈反应
【答案】D
【解析】根据表中提供的电离能的数据,可推断出X是第ⅠA族的元素,常见化合价是+1价,和氯
气化合形成XCl型的氯化物,Y是第ⅢA族的元素,选项A、B、C项均正确。当Y处于第三周期时,是
铝元素,不能和冷水反应,D项错误。故选D。
17.如表是同周期三种主族元素X、Y、Z的电离能数据(单位:kJ•mol-1)。下列判断错误的是( )
元素代号 I I I I
1 2 3 4
X 496 4562 6912 9543
Y 578 1817 2745 11575
Z 738 1451 7733 10540
A.X为第IA族元素 B. 的价电子排布式为ns2np1
C.Z位于元素周期表s区 D.金属性:X>Y>Z
【答案】D【解析】A项,根据表格中电离能的数据可知,X的I 较小,I 突增,故X的价电子数应为1,为第Ⅰ
1 2
A族元素,选项A正确;B项,Y的I、I、I 均较小,I 突增,则Y的价电子数为3,为第ⅢA族元素,
1 2 3 4
价电子排布或为 ,选项B正确;C项,Z的I、I 较小,I 突增,说明Z的价电子数为2,为第ⅡA
1 2 3
族元素,处于元素周期表s区,选项C正确;D项,三种元素处于同一周期,同一周期中元素金属性从左
向右依次减弱,故金属性:X>Z>Y,选项D错误;故选D。
18.四种常见元素基态原子的结构信息如下表。下列大小关系不一定正确的是( )
元素 X Y Z Q
价电子排
结构 有5个原子轨道填充有电子, 有8个不同运动 能级上
布式为
信息 有3个未成对电子 状态的电子 有2个电子
A.电负性: B.第一电离能:
C.单质的硬度: D.最高价含氧酸的酸性:
【答案】C
【解析】X由有5个原子轨道填充有电子,有3个未成对电子,可知X的核外电子排布式为
1s22s22p3,X为N;Y有8个不同运动状态的电子,则Y有8个核外电子,Y为O;Z的核外电子排布式为
1s22s22p2,则Z为C;Q的价电子排布式为 3d104s1,则Q为Cu。A项,同周期从左到右电负性依次增大,
则电负性O>N,A项正确;B项,N为半充满状态,比较稳定,第一电离能大于O,B项正确;C项,C
有多种同素异形体,比如金刚石、石墨等,石墨的硬度小于Cu,而金刚石的硬度大于Cu,C项不一定正
确;D项,N的最高价含氧酸为HNO,C的最高价含氧酸为HCO,酸性HNO>HCO,D项正确。故
3 2 3 3 2 3
选C。
19.(2023·湖南邵阳三模)金属M在潮湿的空气中会形成一层致密稳定的MZX•3M(XY) 薄膜。X、
3 2
Y、Z为短周期主族元素,X的原子序数是Y的8倍,X和Z同周期且X和Z基态原子的未成对电子数相
同,M是人体必需的微量元素之一。1molMZX 含有60mol质子。下列说法正确的是( )
3
A.原子半径:X>Z>Y
B.基态M原子的价层电子排布式为4s2
C.X、Y、Z三种元素的电负性:X>Z>Y
D.同周期元素中第一电离能比X大的有2种
【答案】C
【解析】X、Y、Z为短周期主族元素,X的原子序数是Y的8倍,推出Y为H元素,X为O元素;X
和Z同周期且基态X和Z的未成对电子数相同,则Z为C元素;金属M在潮湿的空气中会形成一层致密
稳定的MZX•3M(XY) ,1molMZX 含有60mol质子,M是人体的必需微量元素之一,为Zn元素;综上,
3 2 3
X为O、Y为H、Z为C、M为Zn。A项,电子层数越多半径越大,电子层数相同时,核电荷数越大,半
径越小;原子半径: Z(C)>X(O)>Y(H),A错误;B项,M为Zn,原子的价层电子排布式为3d104s2,B错
误;C项,同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,金属性
增强,非金属性逐渐减弱,元素电负性减弱;X、Y、Z三种元素的电负性:O>C>H,C正确;D项,同
一周期随着原子序数变大,第一电离能变大,N的2p轨道为半充满稳定状态,第一电离能大于同周期相邻
元素,X为O,同周期元素中第一电离能比O大的有N、F、Ne元素,所以有3种元素,D错误;故选
C。
20.短周期主族元素X、Y、Z、M、N的原子序数依次增大,其中基态Y原子s能级电子数是p能级
的两倍,Z和M位于同一主族,由上述五种元素形成的化合物可作离子导体,结构如图所示。下列说法正确的是( )
A.原子半径:M>Y>Z>X
B.非金属性:M>N,Y>Z
C.氢化物沸点:Z>N>M>Y
D.同周期中第一电离能小于Z的元素有4种
【答案】A
【解析】短周期主族元素X、Y、Z、M、N的原子序数依次增大,基态Y原子s能级电子数是p能级
的两倍,基态Y的电子排布为1s22s22p2,Y为C元素;根据结构图可知,X形成1对电子对,则X为H元
素,Z的原子序数比Y(C)大,且Z和M位于同一主族,则Z在第二周期,M、N在第三周期,若Z为N元
素,则M为P,由[MN ]-可得N为Cl元素;若Z为O元素,则M为S,N为Cl,不符合[MN ]-结构,因此Z
6 6
为N元素, M为P元素,N为Cl元素。A项,同周期原子序数越大原子半径越小,电子层数越多原子半
径越大,则原子半径:M(P)>Y(C)>Z(N)>X(H),A正确;B项,元素最高价含氧酸酸性越强,则元素的
非金属性越强,由酸性HClO>HNO>HPO >HCO 可知非金属性:N(Cl)>Z(N)>M(P)>Y(C),B错误;
4 3 3 4 2 3
C项,选项中没有说明是最简单的氢化物,Y为C元素,碳原子数目较大的烷烃是固态,Z为N元素,而
NH 为气态,则沸点Y>Z,C错误;D项,Z为N元素,同周期主族元素随原子序数增大第一电离能呈增
3
大趋势,但ⅡA、ⅤA元素高于同周期相邻元素,稀有气体第一电离能最大,N的2p能级处于半满稳定状
态,其第一电离能大于同周期相邻元素,则同周期中第一电离能小于N的有Li、Be、B、C、O共5种,D
错误;故选A。
21.(2023·浙江杭州联考)X、Y、Z、W、Q五种短周期元素,原子序数依次增大。X元素基态原子电
子排布式为 ,Y元素的第一电离能大于同周期相邻元素的第一电离能,Z元素基态原子2p轨道
有一个未成对电子,W元素基态原子s能级上的电子总数与p能级上电子总数相等,Q是地壳中含量最多
的金属元素。下列说法不正确的是( )
A.最高价氧化物对应水化物的碱性:
B.Y和原子序数为51的元素位于同一主族
C.同周期元素中Z的第一电离能最大
D.X、Q的氧化物、氢氧化物都有两性
【答案】C
【解析】X、Y、Z、W、Q五种短周期元素,原子序数依次增大,X元素基态原子电子排布式为
,n=2,则X为Be元素;Q是地壳中含量最多的金属元素,则Q为Al元素;Y元素的第一电离
能大于同周期相邻元素的第一电离能,Y位于IIA或VA族,且原子序数介于Be,O之间,则Y元素为N
元素,W元素基态原子s能级上的电子总数与p能级上电子总数相等,W原子核外电子排布式为
1s22s22p63s2,则W为Mg元素;Z元素基态原子2p轨道有一个未成对电子,且原子序数介于O、Al之间,
Z原子核外电子排布式为1s22s22p5,则Z为F元素。A项,金属性:BeW>Z
B.简单气态氢化物的热稳定性:W>Z
C.元素第一电离能:I(Y)>I (Z)>I (W)
1 1 1
D.最高价氧化物对应水化物的酸性:X>W
【答案】C
【解析】X、Y、Z、W、R属于元素周期表中前20号主族元素,且原子序数依次增大,X和Z的基态
原子的2p能级上各有两个未成对电子,分别为2p2、2p4,即X为C元素,Z为O,则Y为N元素;W与Z
同族,则W为S元素;R的最外层电子数与最内层电子数相等,即最外层电子数为2,且原子序数大于
16,则R为Ca元素,由上述分析可知,X、Y、Z、W、R分别为C、N、O、S、Ca元素。A项,S2-、
Ca2+的核外电子数均为18,二者核外电子排布相同,但Ca2+的质子数多,对最外层电子数的引力强,电子
Ca2+的半径小于S2-,即离子半径:S2- > Ca2+,O2-核外电子数均为10,小于S2-、Ca2+,所以正确排序为:
W>R> Z,A错误;B项,非金属性: O > S,非金属性越强,其简单气态氢化物的热稳定性越强,则热稳
定性:HO > HS,B错误;C项,N、O位于第二周期元素,但N原子的2p3结构属于半充满的稳定结构,
2 2
失去1个电子所需能量大,所以元素第一电离能: I(N) > I (O);O、S位于同一主族,O原子半径小,电
1 1
负性大,元素第一电离能: I(O) > I (S), C正确;D项,碳酸是弱酸,硫酸是强酸,即最高价氧化物对
1 1
应水化物的酸性: HSO > H CO,D错误;故选C。
2 4 2 3
23.(2024·福建厦门市松柏中学高三期中)已知A、B、C、D、E、G六种元素,原子序数依次增大。A
的简单气态氢化物能与其最高价含氧酸反应生成盐:B原子核外有两种形状的电子云,两种形状的电子云
轨道上电子数相等;C是短周期中原子半径最大的主族元素;D元素3p能级有两个空轨道;E是所在周期
电负性最大的元素:G是第四周期未成对电子数最多的元素
(1)G在元素周期表中第四周期、 族、 区;第二电离能: I(G) I(Mn) (填“>”或
2 2
“<”),原因是 。
(2)B、C、D、E四种元素形成的简单离子半径由小到大的顺序为 (填离子符号)。
(3)A与E形成的化合物的电子式为 。
(4)写出D的最高价氧化物对应水化物与C的最高价氧化物对应水化物反应的化学方程式 。
(5)写出A的最高价氧化物对应水化物的稀溶液与过量Fe反应的离子方程式 。
【答案】(1) VIB d > 根据核外电子排布,Cr失去一个电子后核外电子排布处于半充满
状态,再失去一个电子所需能量较多;Mn失去两个电子后核外电子排布处于半充满状态,失去第二个电
子所需能量相对于Cr较少
(2)Al3+<Na+<O2-<Cl-
(3)
(4)Al(OH) +NaOH=Na[Al(OH) ]
3 4(5)3Fe+8H++2NO-=3Fe2++2NO↑+4HO
3 2
【解析】A的简单气态氢化物能与其最高价含氧酸反应生成盐,则A为N元素;C是短周期中原子半
径最大的主族元素,则C为Na元素;B原子核外有两种形状的电子云,两种形状的电子云轨道上电子数
相等,则其原子核外电子排布:1s22s22p4,为O元素;D元素3p能级有两个空轨道,则核外电子排布:
1s22s22p63s23p1,为Al元素;E是所在周期电负性最大的元素,原子序数大于Al小于Cr,位于第第三周期,
则为Cl元素:G是第四周期未成对电子数最多的元素,则其核外电子排布:1s22s22p63s23p63d54s1,为Cr元
素。(1),G为Cr元素,原子序数为24,位于元素周期表第四周期第VIB族,处于d分区;Cr核外电子排
布:1s22s22p63s23p63d54s1,Mn核外电子排布:1s22s22p63s23p63d54s2,Cr失去一个电子后核外电子排布处于
半充满状态,再失去一个电子所需能量较多;Mn失去两个电子后核外电子排布处于半充满状态,失去第
二个电子所需能量相对于Cr较少,所以第二电离能: I(G)>I(Mn) ;(2)电子层数越多,离子半径越大;
2 2
电子层数相同,原子序数越大,离子半径越小,则离子半径:Al3+<Na+<O2-<Cl-;(3)A为N元素,E为
Cl元素,二者形成共价化合物NCl ,电子式 ;(4)Al的最高价氧化物对应水化物与
3
Na的最高价氧化物对应水化物反应的化学方程式:Al(OH) +NaOH=Na[Al(OH) ];(5)A为N元素,其最高
3 4
价氧化物对应水化物为HNO,硝酸稀溶液与过量铁反应生成硝酸亚铁,一氧化氮和水,离子方程式:
3
3Fe+8H++2NO-=3Fe2++2NO↑+4HO。
3 2
考点二 分子结构与性质
1.(2023•山东卷,3)下列分子属于极性分子的是( )
A.CS B.NF C.SO D.SiF
2 3 3 4
【答案】B
【解析】A项,CS 中C上的孤电子对数为 ×(4-2×2)=0,σ键电子对数为2,价层电子对数为2,CS
2 2
的空间构型为直线形,分子中正负电中心重合,CS 属于非极性分子,A项不符合题意;B项,NF 中N上
2 3
的孤电子对数为 ×(5-3×1)=1,σ键电子对数为3,价层电子对数为4,NF 的空间构型为三角锥形,分子
3
中正负电中心不重合,NF 属于极性分子,B项符合题意;C项,SO 中S上的孤电子对数为 ×(6-
3 3
3×2)=0,σ键电子对数为3,价层电子对数为3,SO 的空间构型为平面正三角形,分子中正负电中心重合,
3
SO 属于非极性分子,C项不符合题意;D项,SiF 中Si上的孤电子对数为 ×(4-4×1)=0,σ键电子对数为
3 4
4,价层电子对数为4,SiF 的空间构型为正四面体形,分子中正负电中心重合,SiF 属于非极性分子,D
4 4
项不符合题意;故选B。
2.(2023•北京卷,10)下列事实不能通过比较氟元素和氯元素的电负性进行解释的是( )
A. 键的键能小于Cl-Cl键的键能
B.三氟乙酸的K 大于三氯乙酸的K
a aC.氟化氢分子的极性强于氯化氢分子的极性
D.气态氟化氢中存在(HF) ,而气态氯化氢中是 分子
2
【答案】A
【解析】A项,F原子半径小,电子云密度大,两个原子间的斥力较强,F-F键不稳定,因此F-F键的
键能小于Cl-Cl键的键能,与电负性无关,A符合题意;B项,氟的电负性大于氯的电负性。F-C键的极性
大于Cl-C键的极性,使FC—的极性大于ClC—的极性,导致三氟乙酸的羧基中的羟基极性更大,更容易
3 3
电离出氢离子,酸性更强,B不符合题意;C项,氟的电负性大于氯的电负性,F-H键的极性大于Cl-H键
的极性,导致HF分子极性强于HCl,C不符合题意;D项,氟的电负性大于氯的电负性,与氟原子相连的
氢原子可以与另外的氟原子形成分子间氢键,因此气态氟化氢中存在(HF) ,D不符合题意;故选A。
2
3.(2023•湖北省选择性考试,9)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的
是
A.CH 和HO的VSEPR模型均为四面体 B.SO 2-和CO2-的空间构型均为平面三角形
4 2 3 3
C.CF 和SF 均为非极性分子 D.XeF 和XeO 的键角相等
4 4 2 2
【答案】A
【解析】A项,甲烷分子的中心原子的价层电子对为4,水分子的中心原子价层电子对也为4,所以他
们的VSEPR模型都是四面体,A正确;B项,SO 2-的孤电子对为1,CO2-的孤电子对为0,所以SO 2-的空
3 3 3
间构型为三角锥形,CO2-的空间构型为平面三角形,B错误,C项,CH 为正四面体结构,为非极性分子,
3 4
SF 中心原子有孤电子对,为极性分子,C错误;D项,XeF 和XeO 分子中,孤电子对不相等,孤电子对
4 2 2
越多,排斥力越大,所以键角不等,D错误;故选A。
4.(2023•浙江省1月选考,12)共价化合物Al Cl 中所有原子均满足8电子稳定结构,一定条件下可发
2 6
生反应: ,下列说法不正确的是( )
A.Al Cl 的结构式为 B.Al Cl 为非极性分子
2 6 2 6
C.该反应中NH 的配位能力大于氯 D.Al Br 比Al Cl 更难与 发生反应
3 2 6 2 6
【答案】D
【解析】A项,由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为
,故A正确;B项,由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分
子的结构式为 ,则双聚氯化铝分子为结构对称的非极性分子,故B正确;C项,由
反应方程式可知,氨分子更易与具有空轨道的铝原子形成配位键,配位能力大于氯原子,故C正确;D项,
溴元素的电负性小于氯元素,原子的原子半径大于氯原子,则铝溴键弱于铝氯键,所以双聚溴化铝的铝溴
键更易断裂,比双聚氯化铝更易与氨气反应,故D错误;故选D。
5.(2023•湖南卷,4)下列有关物质结构和性质的说法错误的是( )
A.含有手性碳原子的分子叫做手性分子
B.邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
C.酰胺在酸或碱存在并加热的条件下可发生水解反应
D.冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子
【答案】A【解析】A项,有手性异构体的分子被称为手性分子,当分子中存在两个或两个以上的手性碳原子时,
会出现内消旋体,这种含有内消旋体的分子不是手性分子,A错误;B项,邻羟基苯甲醛中含有分子内氢
键,分子内氢键可以降低物质的熔沸点,因此邻羟基苯甲醛的熔沸点低于对羟基苯甲醛的熔沸点,B正确;
C项,酰胺在酸性条件下反应生成羧基和氨基,在碱性条件下反应生成羧酸盐和氨气,二者均为水解反应,
C正确;D项,超分子是由两种或两种以上的分子通过分子间作用力形成的分子聚集体,冠醚(18-冠-6)的
空穴大小为260~320pm,可以适配K+(276pm)、Rb+(304pm),冠醚与离子之间以配位的形式结合,D正确;
故选A。
6.(2023•湖北省选择性考试,11)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是(
)
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 熔点:AlF (1040℃)远高于AlCl (178℃升华) 晶体类型
3 3
C 酸性:CFCOOH(pKa=0.23)远强于CHCOOH(pKa=4.76) 羟基极性
3 3
D 溶解度(20℃):NaCO(29g)大于NaHCO (8g) 阴离子电荷
2 3 3
【答案】D
【解析】A项,正戊烷和新戊烷形成的晶体都是分子晶体,由于新戊烷支链多,对称性好,分子间作
用力小,所以沸点较低,故A正确;B项,AlF 为离子化合物,形成的晶体为离子晶体,熔点较高,AlCl
3 3
为共价化合物,形成的晶体为分子晶体,熔点较低,则 AlF 熔点远高于AlCl ,故B正确;C项,由于电
3 3
负性F>H,C-F键极性大于C-H键,使得羧基上的羟基极性增强,氢原子更容易电离,酸性增强,故C正
确;D项,碳酸氢钠在水中的溶解度比碳酸钠小的原因是碳酸氢钠晶体中 HCO -间存在氢键,与晶格能大
3
小无关,即与阴离子电荷无关,故D错误;故选D。
7.(2022•湖北省选择性考试,11)磷酰三叠氮是一种高能分子,结构简式为O=P(N )。下列关于该分
3 3
子的说法正确的是( )
A.为非极性分子 B.立体构型为正四面体形
C.加热条件下会分解并放出N D.分解产物 的电子式为
2
【答案】C
【解析】A项,磷酰三叠氮分子不是对称结构,分子中的正负电荷重心是不重合的,是极性分子,A
项错误;B项,磷酰三叠氮分子含有三个P-N键及一个P=O双键,则立体构型为四面体构型,B项错误;
C项,磷酰三叠氮是一种高能分子,加热条件下会分解并放出N,C项正确;D项,NPO为共价化合物,
2
则电子式为 ,D项错误;故选C。
8.(2022•湖北省选择性考试,10)Be2+和Al3+的电荷与半径之比相近,导致两元素性质相似。下列说法
错误的是( )
A.Be2+与Al3+都能在水中与氨形成配合物
B.BeCl 和AlCl 的熔点都比MgCl 的低
2 3 2
C.Be(OH) 和Al(OH) 均可表现出弱酸性
2 3
D.Be和Al的氢化物都不能在酸中稳定存在
【答案】A
【解析】A项,Al3+半径小,不能容纳6个氮原子和它配位,则不能在水中与氨形成配合物,A项错误;B项,BeCl 和AlCl 属于分子晶体,而MgCl 属于离子晶体,则BeCl 和AlCl 的熔点都比MgCl 的低,B
2 3 2 2 3 2
项正确;C项,Be(OH) 和Al(OH) 均为两性氢氧化物,则均可表现出弱酸性,C项正确;D项,Be和Al
2 3
的氢化物与酸反应,生成对应的盐和氢气,则都不能在酸中稳定存在,D项正确;故选A。
9.(2022•辽宁省选择性考试,8)理论化学模拟得到一种N +离子,结构如图。下列关于该离子的说法
13
错误的是( )
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
【答案】B
【解析】A项,由N +的结构式可知,所有N原子均满足8电子稳定结构,A正确;B项,中心N原
13
子为sp3杂化,与中心N原子直接相连的N原子为sp2杂化,与端位N原子直接相连的N原子为sp杂化,
端位N原子为sp2杂化,则N原子的杂化方式有3种,B错误;C项,中心N原子为sp3杂化,则其空间结
构为四面体形,C正确;D项,N +中含叠氨结构( ),常温下不稳定,D正确;故选B。
13
10. (2022•海南选择性考试)关于NH 性质的解释合理的是( )
3
选
性质 解释
项
A 比PH 容易液化 NH 分子间的范德华力更大
3 3
B 熔点高于PH N-H键的键能比P-H大
3
C 能与Ag以配位键结合 NH 中氮原子有孤电子对
3
D 氨水中存在NH + NH ·H O是离子化合物
4 3 2
【答案】C
【解析】A项,NH 和PH 都属于同一主族是氢化物,分子晶体的沸点与其相对分子质量成正比,但
3 3
氨气中含有氢键, PH 不含氢键,氢键的存在导致氨气的沸点升高,故A错误;B项,NH 熔点高于
3 3
PH ,是因为氨气中含有氢键,氢键的存在导致氨气的熔点升高,不是N-H键的键能比P-H大,故B错误;
3
C项,NH 中氮原子有孤电子对,使Ag+和NH 以配位键结合形成[Ag(NH)]+,故C正确;D项,NH ·H O
3 3 3 2 3 2
是共价化合物,是弱碱,在水溶液中部分电离出NH +和OH-,故D错误;故选C。
4
11.(2022•山东卷,5)AlN、GaN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
键、 键。下列说法错误的是( )
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取sp3杂化 D.晶体中所有原子的配位数均相同
【答案】A
【解析】根据元素周期表,Al和Ga均为第ⅢA元素,N属于第ⅤA元素,结合题意AlN、GaN的成
键结构与金刚石相似,则其为共价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似,
AlN、GaN晶体中,N原子与其相邻的原子形成3个普通共价键和1个配位键。A项,因为AlN、GaN为
结构相似的共价晶体,由于Al原子的半径小于Ga,N—Al的键长小于N—Ga的,则N—Al的键能较大,键能越大则其对应的共价晶体的熔点越高,故GaN的熔点低于AlN,A说错误;B项,不同种元素的原子
之间形成的共价键为极性键,故两种晶体中所有化学键均为极性键,B说法正确;C项,金刚石中每个C
原子形成4个共价键(即C原子的价层电子对数为4),C原子无孤电子对,故C原子均采取sp3杂化;由于
AlN、GaN与金刚石互为等电子体,则其晶体中所有原子均采取sp3杂化,C说法正确;D项,金刚石中每
个C原子与其周围4个C原子形成共价键,即C原子的配位数是4,由于AlN、GaN与金刚石互为等电子
体,则其晶体中所有原子的配位数也均为4,D说法正确。故选A。
12.(2021•湖北选择性考试,9)下列有关N、P及其化合物的说法错误的是( )
A.N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B.N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C.NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3
D.HNO 的分子间作用力较小,可推断HNO 的熔点比HPO 的低
3 3 3 4
【答案】A
【解析】Cl、P的电负性差值大于Cl、N的电负性差值,三氯化氮、三氯化磷的空间结构都是三角锥
形,故三氯化氮的分子极性小于三氯化磷,A项错误;分子的稳定性与键能、键数目有关,N与N的π键
比P与P的强,可推断N≡N的稳定性比P≡P的高,B项正确;
NH 、PH 分子空间结构都是三角锥形,N、P原子价层孤电子对数都为1,杂化类型都是sp3,但是N
3 3
原子半径小于P,N的电负性大于P,NH 分子中成键电子对之间排斥力大于PH ,故NH 键角大于PH ,
3 3 3 3
C项正确;晶体熔点高低由构成晶体的微粒之间作用力大小决定,它们都是分子晶体,硝酸的相对分子质
量小于磷酸,HNO 分子间作用力小于HPO ,磷酸的熔点高于硝酸,D项正确。
3 3 4
1.键的极性与分子极性的关系
类型 实例 两个键之间的夹角 键的极性 分子的极性 空间构型
X H、N - 非极性键 非极性分子 直线型
2 2 2
XY HCl、NO - 极性键 极性分子 直线型
CO、CS 180° 极性键 非极性分子 直线型
2 2
XY (X Y) SO 120° 极性键 极性分子 三角形
2 2 2
HO、HS 104.5° 极性键 极性分子 V形
2 2
BF 120° 极性键 非极性分子 平面三角形
3
XY
3
NH 107.3° 极性键 非极性分子 三角锥形
3
XY CH、CCl 109.5° 极性键 非极性分子 正四面体
4 4 4
2.中心原子杂化类型和分子空间构型的相互判断
分子(A为中 中心原子杂 中心原子孤
分子构型 示例
心原子) 化方式 电子对数
sp 0 直线形 BeCl
2
AB sp2 1 V形 SO
2 2
sp3 2 V形 HO
2sp2 0 平面三角形 BF
3
AB
3 sp3 1 三角锥形 NH
3
AB sp3 0 正四面体形 CH
4 4
3.常见等电子体
粒子 通式 价电子总数 立体构型
CO、SCN-、NO、N、NO、COS、CS AX 16e- 直线形
2 2 2 2
CO、NO、SO AX 24e- 平面三角形
3 3
SO 、O、NO AX 18e- V形
2 3 2
SO、PO AX 32e- 正四面体形
4
PO、SO、ClO AX 26e- 三角锥形
3
CO、N、C AX 10e- 直线形
2
CH、NH AX 8e- 正四面体形
4 4
1.共价键
(1)分类
②配位键:形成配位键的条件是成键原子一方(A)能够提供孤电子对,另一方(B)具有能够接受孤电子
对的空轨道,可表示为A—B。
(2)σ键和π键的判断方法
共价单键为σ键,双键中有一个σ键和一个π键,三键中有一个σ键和两个π键。但注意配位键也属
于σ键,如1 mol [Cu(NH)]2+中所含σ键数目为16N 。
3 4 A
(3)大π键
①定义:大π键一般是三个或更多个原子间形成的,是未杂化轨道中原子轨道“肩并肩”重叠形成的
π键。
②表达式Πn
:m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。
m
Π6 Π4 O- Π6 Π4 Π4 O2- Π6
6 4 3 4 3 3 3 4
③示例: 、 ;CH CH—CH CH、 ;N 、 ;SO 、 ;O、 ;C 、 。
2 2 2 3
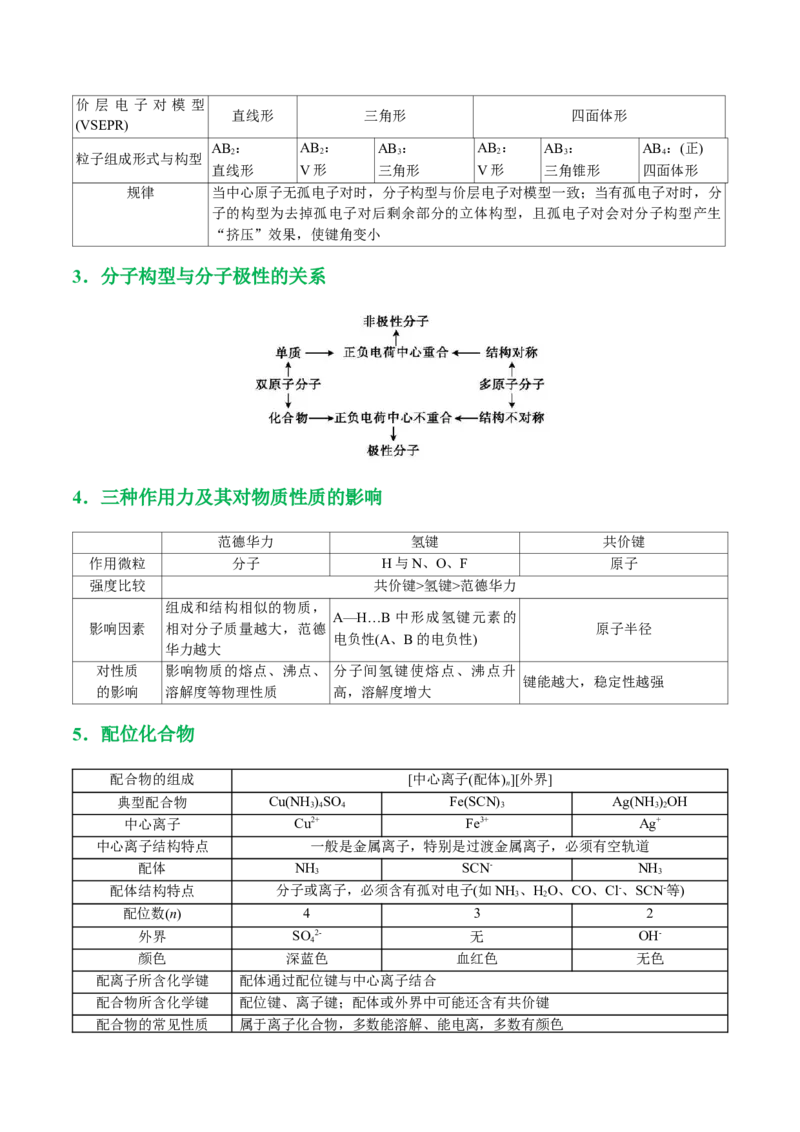
2.中心原子价层电子对数、杂化轨道类型与粒子的立体构型(ABm±型)
n
价层电子对数(杂化
2 3 4
轨道数)
杂化轨道类型 sp sp2 sp3价 层 电 子 对 模 型
直线形 三角形 四面体形
(VSEPR)
AB : AB : AB : AB : AB : AB :(正)
2 2 3 2 3 4
粒子组成形式与构型
直线形 V形 三角形 V形 三角锥形 四面体形
规律 当中心原子无孤电子对时,分子构型与价层电子对模型一致;当有孤电子对时,分
子的构型为去掉孤电子对后剩余部分的立体构型,且孤电子对会对分子构型产生
“挤压”效果,使键角变小
3.分子构型与分子极性的关系
4.三种作用力及其对物质性质的影响
范德华力 氢键 共价键
作用微粒 分子 H与N、O、F 原子
强度比较 共价键>氢键>范德华力
组成和结构相似的物质,
A—H…B 中形成氢键元素的
影响因素 相对分子质量越大,范德 原子半径
电负性(A、B的电负性)
华力越大
对性质 影响物质的熔点、沸点、 分子间氢键使熔点、沸点升
键能越大,稳定性越强
的影响 溶解度等物理性质 高,溶解度增大
5.配位化合物
配合物的组成 [中心离子(配体)][外界]
n
典型配合物 Cu(NH )SO Fe(SCN) Ag(NH)OH
3 4 4 3 3 2
中心离子 Cu2+ Fe3+ Ag+
中心离子结构特点 一般是金属离子,特别是过渡金属离子,必须有空轨道
配体 NH SCN- NH
3 3
配体结构特点 分子或离子,必须含有孤对电子(如NH 、HO、CO、Cl-、SCN-等)
3 2
配位数(n) 4 3 2
外界 SO 2- 无 OH-
4
颜色 深蓝色 血红色 无色
配离子所含化学键 配体通过配位键与中心离子结合
配合物所含化学键 配位键、离子键;配体或外界中可能还含有共价键
配合物的常见性质 属于离子化合物,多数能溶解、能电离,多数有颜色是过渡金属和一氧化碳配位形成的配合物,如四羰基镍[Ni(CO) ]。在许多有机
金属羰基配合物 4
化合物的合成反应中,金属羰基配合物常常作为这些反应的催化剂
二茂铁的结构为一个铁原子处在两个平行的环戊二烯的环之间。在固体状态
下,两个茂环相互错开成全错位构型,温度升高时则绕垂直轴相对转动。二茂
二茂铁
铁的化学性质稳定,类似芳香族化合物
6.超分子
(1)定义:有两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
注意:超分子定义中分子是广义的,其中包括离子。
(2)特征:分子识别和自组装。
题型一 共价键类型
1.(2023·陕西省宝鸡市期中)下列关于σ键和π键的说法中,不正确的是( )
A.N 分子中的π键为p-pπ键,π键不能绕键轴旋转
2
B.HCl分子中的σ键为s-sσ键
C.乙烯分子中σ键与π键的个数比为5:1
D.p轨道和p轨道之间既能形成π键,又能形成σ键
【答案】B
【解析】A项,氮气的结构式为N≡N,分子中含有三键含有1个σ键和2个π键,π键为p-p π键,π
键不能绕键轴旋转,A正确;B项,H只有1s电子,Cl的3p轨道上的电子与H的1s轨道电子以“头碰
头”方式重叠构建s-pσ键,B错误;C项,乙烯分子中含有一个碳碳双键,故π键的个数为1,σ键为5,
σ键与π键的个数比为5:1,C正确;D项,p和p轨道头对头能形成σ键、肩并肩能形成π键,所以p和
p轨道既能形成σ键又能形成π键,D正确;故选B。
2.(2023·河北省石家庄市期末)下列有关共价键的说法错误的是( )
A.HO 中只有σ键没有π键
2 2
B.所有σ键的强度都比π键的大
C.卤化氢中H-F键的键能最大
D.键长和键角的数值可通过晶体的X射线衍射实验获得
【答案】B
【解析】A项,HO 分子中只有单键,则只有σ键没有π键,A正确;B项,σ键的强度不一定比π键
2 2
的大,如氮气分子中σ键的强度都比π键的小,B错误;C项,H-F的键长是卤化氢中最短的,则H-F的键
能是卤化氢中最大的,C正确;D项,通过晶体X射线衍射实验可以测定分子结构中的键长和键角的数值,
键角是描述分子立体结构的重要参数,D正确;故选B。
3.( 2023·甘肃省武威市期中)下列说法中正确的是( )
A.π键比σ键重叠程度大,形成的共价键稳定
B.两个原子之间形成共价键时,最多有一个σ键
C.气体单质中,一定有σ键,可能有π键D.CO 分子中有一个σ键,二个π键
2
【答案】B
【解析】A项,σ键是头碰头的重叠,π键是肩并肩的重叠,一般σ键比π键重叠程度大,σ键比π键
稳定,A 错误;B项,两个原子间形成单键时,只能形成1个σ键,两个原子之间形成双键时,含有一个
σ键和一个π键,两个原子之间形成三键时,含有一个σ键和2个π键,B正确;C项,单原子分子中没有
共价键,如稀有气体分子中不存在共价键,C错误;D项,CO 分子中含有两个碳氧双键,即有2个σ键,
2
2个π键,D错误;故选B。
4.(2023·四川省成都·市联考)下列关于共价键的说法正确的是( )
A.HO和HO 分子内的共价键均是s-pσ键
2 2 2
B.N 分子内的共价键电子云形状均是镜面对称
2
C.H、Cl、HCl分子内的σ键均无方向性
2 2
D.共价化合物一定含σ键,可能含π键
【答案】D
【解析】A项,HO 分子内的共价键还有p-p σ键,故A错误;B项,N 分子内的共价键包括σ键和π
2 2 2
键,所以其电子云形状既有镜面对称也有轴对称,故B错误;C项,Cl、HCl分子内的σ键均有方向性,
2
故C错误;D项,共价化合物一定含σ键,可能含π键,比如氢气只有含σ键,而氧气、氮气含有σ键,
也含有π键,故D正确。故选D。
题型二 分子的空间构型
5.(2024·山东临沂市高三教学质量检测)下列每组分子的中心原子杂化方式和空间构型均相同的是(
)
A.BF、NF B.XeF 、PCl C.CS、HCN D.SO 、OF
3 3 2 5 2 2 2
【答案】C
【解析】A项,BF 中B原子为sp2杂化,为平面三角形,NF 中N原子为sp3杂化,为三角锥形,A错
3 3
误;B项,XeF 中Xe原子为sp3d2杂化,PCl 中P原子为sp3d杂化,B错误;C项,CS 中C原子为sp杂化,
2 5 2
HCN中C原子为sp杂化,且空间构型都为直线形,C正确;D项,SO 中S原子为sp2杂化,OF 中O原子
2 2
为sp3杂化,D错误;故选C。
6.下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
A.PCl 中P原子sp3杂化,为三角锥形 B.BCl 中B原子sp2杂化,为平面三角形
3 3
C.CS 中C原子sp杂化,为直线形 D.HS分子中,S为sp杂化,为直线形
2 2
【答案】D
【解析】PCl 分子中P原子形成3个σ键,孤对电子数为-3=1,为sp3杂化,三角锥形,A正确;
3
BCl 分子中B原子形成3个σ键,孤对电子数为-3=0,为sp2杂化,平面三角形,B正确;CS 分子中C
3 2
原子形成2个σ键,孤对电子数为-2=0,为sp杂化,直线形,C正确;HS分子中,S原子形成2个σ键,
2
孤对电子数为-2=2,为sp3杂化,V形,D错误。
7.有几种阴离子的信息如下:
阴离子 ClO - ClO - M ClO-
4 3
中心元素化合价 +5 +3 +1
中心原子杂化类型 sp3 sp3
下列推断不正确的是( )A.ClO -和CO2-的价电子总数相同 B.M的化学式为ClO -
3 3 2
C.ClO -、ClO-中氯原子的杂化类型都为sp3 D.M的空间结构为V形
3
【答案】A
【解析】A项,ClO -和CO2-的价电子总数分别为7+3×6+1=26、4+3×6+2=24,不相同,A项错误;
3 3
B项,M中Cl元素的化合价是+3价,杂化轨道类型是sp3,因此M的化学式为ClO -,B项正确;C项,
2
ClO -中价层电子对数是 =4,ClO-中价层电子对数是 =4,因此氯原子的杂
3
化类型都为sp3,C项正确;D项,M中价层电子对数是 =4,含有2对孤对电子,所以空
间结构为V形,D项正确;故选A。
8.根据杂化轨道理论和价层电子对互斥模型,判断下列分子或离子的空间结构正确的是( )
选项 分子或离子 中心原子杂化方式 价层电子对互斥模型 分子或离子的空间结构
A SO sp 直线形 直线形
2
B HCHO sp2 平面三角形 三角锥形
C NF sp2 四面体形 平面三角形
3
D
NH+
sp3 正四面体形 正四面体形
4
【答案】B
【解析】SO 分子中心原子杂化方式为sp2,价层电子对互斥模型为平面三角形,含有一对孤电子对,
2
分子的空间结构为V形,A错误;HCHO分子中心原子杂化方式为sp2,价层电子对互斥模型为平面三角
形,没有孤电子对,分子的空间结构为平面三角形,B错误;NF 分子中心原子杂化方式为sp3,价层电子
3
对互斥模型为四面体形,含有一对孤电子对,分子的空间结构为三角锥形,C错误;NH+
的中心原子杂化
4
方式为sp3,价层电子对互斥模型为正四面体形,没有孤电子对,离子的空间结构为正四面体形,D正确。
故选B。
9.(2024·江苏常州市教育学会高三学业水平监测)NaNH 易被O 氧化,与HO反应放出NH ,需在N
2 2 2 3 2
保护下储存。下列说法正确的是( )
A.NaNH 中N元素的化合价为-2 B.键能大小:O<N
2 2 2
C.NH 分子的VSEPR模型为 D.键角大小:HO>NH
3 2 3
【答案】B
【解析】A项,NaNH 中N元素的化合价为-3,故A错误;B项,氮气比氧气更稳定,因此键能O<
2 2
N,故B正确;C项,NH 分子的VSEPR模型为正四面体,图示是氨气的分子空间构型,故C错误;D项,
2 3
HO和NH 中心原子的杂化方式都是sp3,但前者比后者多一对孤对电子,键角更小,故D错误;故选B。
2 3
10.(2024·天津河北高三期中)硫元素与氯元素可形成SCl 、SCl 两种化合物,两种物质中各原子均满
2 2 2
足最外层8电子稳定结构。下列说法错误的是( )
A.硫元素与氯元素均属于p区元素
B.SCl 与SCl 分子中共价键的类型不完全相同
2 2 2
C.SCl 中S的化合价为 价
2 2
D.SCl 分子中的硫原子采取sp3杂化
2
【答案】C
【解析】A项,硫元素和氯元素分别为ⅥA族和ⅦA族元素,均属于p区元素,A正确;B项,SCl
2结构为Cl-S-Cl,SCl 结构为Cl-S-S-Cl,SCl 中共价键均为极性键,SCl 中除了极性键还有非极性键,B
2 2 2 2 2
正确;C项,S的非金属性弱于Cl,因此S显正价,SCl 中S为+1价,C错误;D项,SCl 中S原子价层
2 2 2
电子对数为2+ =4,采用sp3杂化,D正确;故选C。
11.(2023·海南省琼海市嘉积中学高三期中)氯元素有多种化合价,可形成ClO、Cl-、ClO-、ClO -、
2 2
ClO -、ClO -等微粒。下列说法错误的是( )
3 4
A.ClO -、ClO -、ClO -中Cl原子的杂化方式相同
2 3 4
B.基态Cl原子核外电子的空间运动状态有9种
C.键角:ClO ->ClO ->ClO -
2 3 4
D.ClO的空间构型为V形
2
【答案】C
【解析】A项,ClO -的结构式为: ,ClO -的结构式为: ,ClO -的结构
2 3 4
式为 ,VSEPR模型均为四面体,因此Cl的杂化方式都是sp3,A正确;B项,量子力学把电
子在原子核外的一个空间运动状态称为一个原子轨道,基态Cl原子的核外电子排布式为:1s22s22p63s23p5,
s能级各有一个轨道,p能级各有3个轨道,共9个轨道。因此基态Cl原子的核外电子的空间运动状态有9
种,B正确;C项,三种离子的Cl原子均为sp3杂化,ClO -空间结构呈V形,键角为105 ,ClO -空间结
2 3
构呈三角锥形,键角为107 ,ClO -空间结构呈四面体形,键角为109 28 ,键角关系为:ClO -<ClO -<
4 2 3
ClO -,C错误;D项,ClO中心原子为O原子,杂化方式为sp3,结构式为 ,因此空间构
4 2
型为形,D正确;故选C。
12.乙二胺四乙酸又叫EDTA,是化学中一种良好的配合剂,形成的配合物又叫螯合物。 在配
合滴定中经常用到,一般是测定金属离子的含量。已知:EDTA配离子结构如图。下列叙述错误的是(
)
A.EDTA中氮原子杂化方式sp3
B.M元素可以是Cu、 或
C.M元素的配位数是6
D.EDTANa-Fe(III)的化学键有:σ键、配位键、π键和离子键【答案】B
【解析】A项,根据该配离子结构,氮原子成四个单键(有1个配位键),属于杂化方式sp3,故A正确;
B项,依图可知,M的配位数为6,而Cu的配位数为4,故B项错误;C项,根据该配离子结构,M元素
的配位数是6,故C正确;D项,EDTANa-Fe(III)是离子化合物,含有离子键;阴离子是复杂离子,含有共
价单键、共价双键,单键为σ键、双键含σ键、π键,铁离子含有空轨道,与之结合的氮原子、氧原子含
有孤电子对,与铁离子形成配位键,故D正确;故选B。
13.(2024·江西景德镇乐平中学高三月考)下列有关C、N、O三种元素及其相关化合物的结构与性质
说法错误的是( )
A.第一电离能:CH SO >H PO
4 2 4 3 4
【答案】C
【解析】A项,液态氟化氢中存在氢键,所以氟化氢的沸点比氯化氢高,A项正确;B项,CH、
4
CO、BF 都是含有极性键的非极性分子,B项正确;C项,[Cu(NH )]2+中含有极性键、配位键,C项错误;
2 3 3 4
D项,非羟基氧原子数目越多酸性越强,而在HClO 中有3个非羟基氧原子,HSO 中有2个非羟基氧原子,
4 2 4
HPO 中有1个非羟基氧原子,所以酸性强弱的顺序为:HClO>H SO >H PO ,D项正确;故选C。
3 4 4 2 4 3 4
19.关于CS、SO 、NH 三种物质的说法中正确的是( )
2 2 3
A.CS 在水中的溶解度很小,是由于其属于极性分子
2
B.SO 和NH 均易溶于水,原因之一是它们都是极性分子
2 3
C.CS 为非极性分子,所以在三种物质中熔沸点最低
2
D.NH 在水中溶解度很大只是由于NH 分子有极性
3 3
【答案】B
【解析】根据“相似相溶”原理,水是极性分子,CS 是非极性分子,SO 和NH 都是极性分子,故A
2 2 3
项错误、B项正确;由于CS 常温下是液体,SO 和NH 常温下是气体,故C项错误;NH 在水中溶解度很
2 2 3 3
大,除了由于NH 分子有极性外,还因为NH 分子和HO分子之间可以形成氢键,故D项错误。故选B。
3 3 2
20.(2024·湖北武汉第十一中·高三月考)下列关于物质的结构或性质的描述及解释都正确的是( )
A.键角:HO+>HO,是由于HO+中O上孤电子对数比HO分中O上的少
3 2 3 2
B.沸点:对羟基苯甲醛>邻羟基苯甲醛,是由于对羟基苯甲醛分子间范德华力更强
C.溶解度:O 在水中溶解度比在CCl 中溶解度更大,是由于O 是弱极性分子
3 4 3
D.酸性:CHClCOOH>CHCOOH,是由于CHClCOOH的羧基中羟基极性更小
2 3 2
【答案】A【解析】A项,随着孤电子对数增多,成键电子对与成键电子对之间的斥力减小,键角也减小, HO
2
的孤电子对数= ,HO+的孤电子对数= ,所以键角大小为HO+>HO,A正确;B项,
3 3 2
沸点:对羟基苯甲醛>邻羟基苯甲醛,是因为对羟基苯甲醛形成分子间氢键,邻羟基苯甲醛形成分子内氢
键,所以对羟基苯甲醛分子间作用力较大,熔沸点也较高,B错误;C项,臭氧是V型结构,极性分子,
根据相似相溶原理,臭氧在水中溶解度比在CCl 中溶解度更小,C错误;D项,Cl的电负性大于H,电负
4
性越大,形成共价键的极性越强,因此,C-Cl的极性大于C-H的极性,导致CHClCOOH的羧基中的羟基
2
极性更大,更容易电离出氢离子,酸性CHClCOOH>CHCOOH,D错误;故选A。
2 3
21.离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1-乙基-3-甲基咪唑四氟硼酸盐离
子液体结构如图所示,下列相关叙述错误的是( )
A.该离子液体中C、N杂化方式均有sp2和sp3两种
B.阴离子呈正四面体形,存在共价键和配位键
C.阳离子中σ键数目是π键数目的10倍
D.该离子液体与水能够形成氢键
【答案】C
【解析】A项,该离子液体中根据C原子接的化学键有1个双键判断应采用的是sp2杂化,还有碳原子
接的是四个单键,判断采用的是sp3杂化。N原子接的有1个双键判断是sp2杂化,另一个N原子接的都是
单键判断是sp3,故A正确;B项,阴离子BF-中的B原子采用sp3杂化,根据VSEPR模型判断空间构型是
4
正四面体。根据杂化理论判断B原子中有空轨道,F-有孤对电子,故还含有配位键,故B正确;C项,根
据单键是σ键,双键是π键判断该物质中含有σ键是19个,π键2,σ键数目不是π键数目的10倍。故C
错误;D项,该物质中含有电负性大的N和F原子故能与水中的氢原子形成氢键,故D正确。
22.[Zn(CN) ]2-在水溶液中可与HCHO发生反应生成[Zn(HO) ]2+和HOCH CN,下列说法错误的是(
4 2 4 2
)
A.Zn2+基态核外电子排布式为[Ar]3d10
B.1mol HCHO分子中含有σ键的数目为1.806×1024
C.HOCH CN分子中碳原子轨道的杂化类型是sp3
2
D.[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键,结构可表示为
4
【答案】C
【解析】A项,Zn原子序数为30,位于ⅡB族,所以,Zn2+基态核外电子排布式为[Ar]3d10,A正确;
B项,1分子HCHO含2个C-H键和1个C=O键,共有3个σ键,所以,1molHCHO分子中含有σ键的物
质的量为3mol,数目为1.806×1024,B正确;C项,HOCH CN分子中与羟基相连的C为sp3杂化,-CN(-
2
C≡N)中的C为sp杂化,C错误;D项,[Zn(CN) ]2-中Zn2+与CN-的C原子形成配位键,Zn为sp3杂化,配
4
位原子形成正四面体,所以,[Zn(CN) ]2-结构可表示为 ,D正确;故选C。
423.(2024·江苏南京南京师大附中高三月考)氧及其化合物具有广泛用途。O 是常用的氧化剂,C H 的
2 2 2
燃烧热为 ,氧炔焰产生的高温可用于焊接金属。O 可用于水处理,pH约为8时,O 可与
3 3
CN-反应生成HCO -、N 和O。C H18OH可用于研究酯化反应的机理。CaO可用于烟气(含N、O、CO、
3 2 2 2 5 2 2 2
SO 等)脱硫。HO 是一种绿色氧化剂,电解NH HSO 饱和溶液产生的(NH )SO 经水解可制得HO。下列
2 2 2 4 4 4 2 2 8 2 2
物质结构与性质或物质性质与用途具有对应关系的是( )
A.N 分子中含共价三键,N 的沸点比O 的低
2 2 2
B.HO 分子之间形成氢键,可与水任意比例互溶
2 2
C.O 具有氧化性,可作为燃料电池的氧化剂
2
D.O 的溶解度比O 大,可用于饮用水消毒杀菌
3 2
【答案】C
【解析】A项,N 相对分子质量大于O,即N 范德华力大于O,所以N 的沸点比O 的高,故A错
2 2 2 2 2 2
误;B项,HO 可与水任意比例互溶,是因为HO 与水分子间形成氢键,故B错误;C项,O 具有氧化性,
2 2 2 2 2
可作为燃料电池的氧化剂,故C正确;D项,O 可用于饮用水消毒杀菌是因为其具有氧化性,与溶解性无
3
关,故D错误;故选C。
24.(2024·山东菏泽·统考二模)胍( )是一元强碱,分子构型为平面型,其盐酸盐(
)是核酸检测液的主要成分。下列说法错误的是( )
A.胍中C杂化方式为sp2,胍中N杂化方式为sp2、sp3
B.胍具有很强的吸湿性
C.胍的熔点低于胍盐
D.胍盐中含有的化学键均为极性键
【答案】D
【解析】A项,胍中C杂化方式为sp2,胍分子 中①号氮原子形成2个σ 键且有1个孤
电子对,为sp2杂化、②号和③号氮原子形成3个σ键且有1个孤电子对,为sp3杂化,A正确;B项,胍
中氮原子存在一对孤对电子,可以和水分子形成氢键,具有很强的吸湿性,B正确;C项,胍为分子晶体,
其盐为离子晶体,胍熔点低于胍盐,C正确;D项,H和H之间形成的化学键为非极性键,D错误;故选
D。
25.(2024·山东菏泽高三期中)我国科学家发现“杯酚”能与 形成超分子,从而识别 和 。下
列说法错误的是( )A.溶剂甲苯属于极性分子,而氯仿属于非极性分子
B.操作①是过滤:操作③是蒸馏
C.“杯酚”和甲苯分子中均存在大π键
D.“杯酚”能与C 形成分子间作用力
60
【答案】A
【解析】A项,甲苯是苯中的一个氢原子被甲基取代是极性分子,而氯仿不是正四面体属于极性分子,
故A错误;B项,甲苯将C 溶解,而超分子不能溶解因此操作①是过滤:氯仿溶解了杯酚释放C 操作③
70 60
是蒸馏,故B正确;C项,杯酚和甲苯分子都有苯环结构,都存在大π键,故C正确;D项,C 可以“装
60
进”杯酚中形成超分子,杯酚”能与C 形成分子间作用力,故D正确;故选A。
60
26.(2024·山东潍坊市五县区高三阶段监测)不同空腔尺寸的葫芦 可以通过形成超分
子从气体或溶液中识别不同分子并选择性吸附,对位取代的苯的衍生物恰好可以进入葫芦[6]脲(结构如
图所示)的空腔。下列说法正确的是( )
A.葫芦脲可以吸附进入空腔的所有分子
B.葫芦[6]脲是超分子且能发生丁达尔效应
C.葫芦[6]脲形成的超分子中分子间存在范德华力、氢键
D.可装入对甲基苯甲酸体现了超分子的“分子识别”功能
【答案】D
【解析】A项,由题给信息可知,只有对位取代的苯的衍生物恰好可以进入葫芦[6]脲的空腔,故A
错误;B项,葫芦[6]脲是超分子,属于纯净物,不能发生丁达尔效应,故B错误;C项,氢键是电负性
大的原子与氢原子形成共价键,这个氢原子与另外电负性大的原子形成,葫芦[6]脲形成的超分子间不
存在氢键,故C错误;D项,由题给信息可知,对位取代的苯的衍生物恰好可以进入葫芦[6]脲的空腔,
则可装入对甲基苯甲酸,体现了超分子的“分子识别”功能,故D正确;故选D。
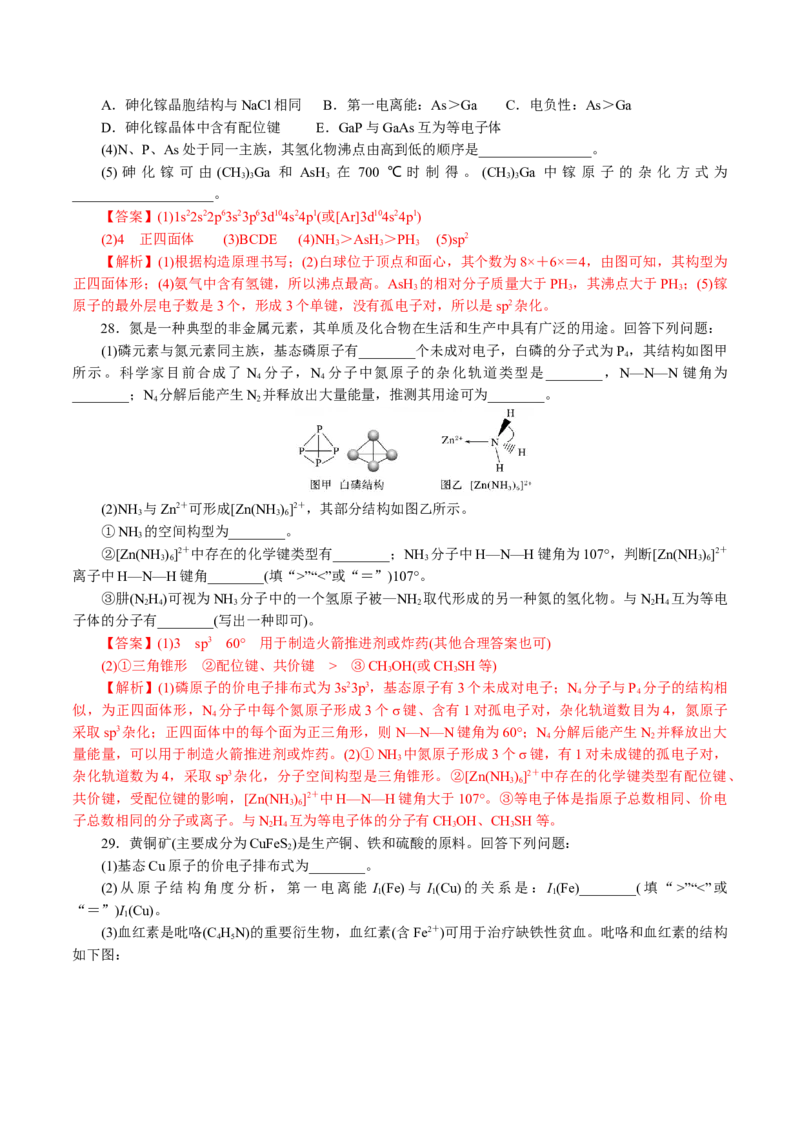
27.目前市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主。
砷化镓的晶胞结构如图。试回答:
(1)镓的基态原子的电子排布式是______________。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为______,与同一个镓原子相连的
砷原子构成的空间构型为________________。
(3)下列说法正确的是________(填字母)。A.砷化镓晶胞结构与NaCl相同 B.第一电离能:As>Ga C.电负性:As>Ga
D.砷化镓晶体中含有配位键 E.GaP与GaAs互为等电子体
(4)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是________________。
(5) 砷 化 镓 可 由 (CH)Ga 和 AsH 在 700 ℃ 时 制 得 。 (CH)Ga 中 镓 原 子 的 杂 化 方 式 为
3 3 3 3 3
____________________。
【答案】(1)1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1)
(2)4 正四面体 (3)BCDE (4)NH >AsH >PH (5)sp2
3 3 3
【解析】(1)根据构造原理书写;(2)白球位于顶点和面心,其个数为8×+6×=4,由图可知,其构型为
正四面体形;(4)氨气中含有氢键,所以沸点最高。AsH 的相对分子质量大于PH ,其沸点大于PH ;(5)镓
3 3 3
原子的最外层电子数是3个,形成3个单键,没有孤电子对,所以是sp2杂化。
28.氮是一种典型的非金属元素,其单质及化合物在生活和生产中具有广泛的用途。回答下列问题:
(1)磷元素与氮元素同主族,基态磷原子有________个未成对电子,白磷的分子式为P ,其结构如图甲
4
所示。科学家目前合成了 N 分子,N 分子中氮原子的杂化轨道类型是________,N—N—N 键角为
4 4
________;N 分解后能产生N 并释放出大量能量,推测其用途可为________。
4 2
(2)NH 与Zn2+可形成[Zn(NH )]2+,其部分结构如图乙所示。
3 3 6
①NH 的空间构型为________。
3
②[Zn(NH )]2+中存在的化学键类型有________;NH 分子中H—N—H键角为107°,判断[Zn(NH )]2+
3 6 3 3 6
离子中H—N—H键角________(填“>”“<”或“=”)107°。
③肼(N H)可视为NH 分子中的一个氢原子被—NH 取代形成的另一种氮的氢化物。与NH 互为等电
2 4 3 2 2 4
子体的分子有________(写出一种即可)。
【答案】(1)3 sp3 60° 用于制造火箭推进剂或炸药(其他合理答案也可)
(2)①三角锥形 ②配位键、共价键 > ③CHOH(或CHSH等)
3 3
【解析】(1)磷原子的价电子排布式为3s23p3,基态原子有3个未成对电子;N 分子与P 分子的结构相
4 4
似,为正四面体形,N 分子中每个氮原子形成3个σ键、含有1对孤电子对,杂化轨道数目为4,氮原子
4
采取sp3杂化;正四面体中的每个面为正三角形,则N—N—N键角为60°;N 分解后能产生N 并释放出大
4 2
量能量,可以用于制造火箭推进剂或炸药。(2)①NH 中氮原子形成3个σ键,有1对未成键的孤电子对,
3
杂化轨道数为4,采取sp3杂化,分子空间构型是三角锥形。②[Zn(NH )]2+中存在的化学键类型有配位键、
3 6
共价键,受配位键的影响,[Zn(NH )]2+中H—N—H键角大于107°。③等电子体是指原子总数相同、价电
3 6
子总数相同的分子或离子。与NH 互为等电子体的分子有CHOH、CHSH等。
2 4 3 3
29.黄铜矿(主要成分为CuFeS)是生产铜、铁和硫酸的原料。回答下列问题:
2
(1)基态Cu原子的价电子排布式为________。
(2)从原子结构角度分析,第一电离能 I(Fe)与 I(Cu)的关系是:I(Fe)________(填“>”“<”或
1 1 1
“=”)I(Cu)。
1
(3)血红素是吡咯(C HN)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构
4 5
如下图:①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为________。
②1 mol吡咯分子中所含的σ键总数为________个。分子中的大π键可用Π表示,其中m代表参与形
成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为________。
③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为________(填化学式)。
④血液中的O 是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的 Fe2+与O 是通过
2 2
________键相结合的。
(4)黄铜矿冶炼铜时产生的SO 可经过SO →SO →HSO 途径形成酸雨。SO 的空间构型为________。
2 2 3 2 4 2
HSO 的酸性强于HSO 的原因是________________________________。
2 4 2 3
【答案】(1)3d104s1 (2)>
(3)①sp2 ②10N Π ③CHI(Cu)。(3)①已知吡咯中的氮原子及与其相连的原子均在同一平面内且为平面
1 1
三角形,则吡咯分子中N原子的杂化类型为sp2。②根据分子结构可知1 mol吡咯分子中有8 mol单键、2
mol 双键,所以所含的σ键总数为10N ;吡咯环分子中形成大π键的原子数为5个;氮原子中未参与成键
A
的电子为1对,碳碳原子间除了形成σ键外,还有4个碳分别提供1个电子形成π键,共有电子数为6,所
以吡咯环中的大π键应表示为Π。③CH 分子间无氢键,沸点最低,而NH 、HO分子间均含氢键,由于
4 3 2
氧原子的电负性大于氮原子,所以HO分子间氢键较强,水的沸点最高;因此,三种氢化物的沸点由低到
2
高的顺序为CH离子晶体>分子晶体,如:金刚石>NaCl>Cl ;金属晶体>分子晶
2
体,如:Na>Cl 。(金属晶体熔、沸点有的很高,如钨、铂等,有的则很低,如汞等)
2
原子晶体 →→,如:金刚石>石英>晶体硅
离子晶体 一般地说,阴阳离子的电荷数越多,离子半径越小,离子键越强,晶格能越大,熔、沸点就越高。如:MgO>MgCl ,NaCl>CsCl
2
金属离子半径越小,离子所带电荷数越多,其形成的金属键越强,金属单
金属晶体
质的熔、沸点就越高,如Al>Mg>Na
①分子间作用力越大,物质的熔、沸点越高;具有分子间氢键的分子晶体
熔、沸点反常的高。如HO>HTe>HSe>HS
2 2 2 2
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如
SnH >GeH >SiH>CH
4 4 4 4
分子晶体
③组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔沸
点越高,如CO>N
2
在同分异构体中,一般支链越多,熔、沸点越低,如正戊烷>异戊烷>新
戊烷
1.(2024·江苏常州高三期中)我国自主研发的“深地一号”为进军万米深度提供核心装备。制造钻头
用的金刚石为( )
A.共价晶体 B.离子晶体 C.分子晶体 D.金属晶体
【答案】A
【解析】制造钻头用的金刚石是碳原子之间以4个共价键结合形成正四面体结构,这种结构向空间扩
展,就形成立体网状结构,属于共价晶体,故合理选项是A。
2.下表所列物质的晶体类型全部正确的一组是( )
共价晶体 离子晶体 分子晶体
A 氯化硅 磷酸 单质硫
B 单晶硅 碳酸氢铵 白磷
C 金刚石 尿素 冰
D 铁 烧碱 冰醋酸
【答案】B
【解析】A项,SiCl 、HPO 、单质硫均为分子晶体;C项,尿素属于分子晶体;D项,铁属于金属晶
4 3 4
体。
3.下列晶体分类中正确的是( )
选项 离子晶体 共价晶体 分子晶体 金属晶体
A NH Cl Ar C H O 生铁
4 6 12 6
B HSO Si S Hg
2 4
C CHCOONa SiO I Fe
3 2 2
D Ba(OH) 石墨 普通玻璃 Cu
2
【答案】C
【解析】A项中,Ar是分子晶体而不是共价晶体;B项中,HSO 属于分子晶体而不是离子晶体;D
2 4
项中,石墨属于混合型晶体而不是共价晶体,普通玻璃不是晶体。
4.下列晶体分类中正确的一组是( )
选项 离子晶体 原子晶体 分子晶体A NaOH Ar SO
2
B HSO 石墨 S
2 4
C CHCOONa 水晶
3
D Ba(OH) 金刚石 玻璃
2
【答案】C
【解析】A项,固态Ar为分子晶体;B项,HSO 为分子晶体、石墨是混合型晶体;D项,玻璃是非
2 4
晶体。
5.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
A.SO 和SiO B.CO 和HO C.NaCl和HCl D.CCl 和KCl
3 2 2 2 4
【答案】B
【解析】A中SO 为分子晶体、S—O键是共价键,SiO 为共价晶体;B中CO 、HO都是分子晶体,
3 2 2 2
C—O键、O—H键均为共价键;C中NaCl为离子晶体,阴、阳离子靠离子键结合在一起,HCl为分子晶
体,H—Cl键为共价键;D中CCl 为分子晶体,C—Cl键为共价键,KCl为离子晶体。
4
6.下列关于冰晶体、干冰晶体、金刚石晶体的说法正确的是( )
A.冰晶体中只存在范德华力和氢键两种作用力
B.沸点:金刚石>干冰>冰
C.冰晶体中的氧原子和金刚石中的碳原子均可形成四面体结构
D.干冰晶体中每个CO 周围距离相等且最近的CO 有10个
2 2
【答案】C
【解析】冰晶体中还存在H—O共价键,A错误;金刚石是共价晶体,冰、干冰是分子晶体,所以金
刚石的沸点最高,由于冰中存在氢键,其沸点比干冰高,B错误;冰晶体中1个O原子与邻近的4个O原
子可形成四面体结构,金刚石中1个C原子与邻近的4个C原子可形成正四面体结构,C正确;干冰晶体
中每个CO 周围距离相等且最近的CO 有12个,D错误。
2 2
7.下列每组物质发生状态变化所克服的微粒间的相互作用属同种类型是
A.食盐和蔗糖的熔化 B.白磷和硫的熔化
C.氯化铵固体和干冰受热后的气化 D.氧化镁和金属镁的熔化
【答案】B
【解析】食盐为离子晶体,熔化时克服的是离子键,蔗糖为分子晶体,熔化时克服的是分子间作用力,
二者不同,A错误;白磷和硫都是分子晶体,熔化时克服的是分子间作用力,二者相同,B正确;氯化铵
为离子晶体,受热易分解,分解时克服的是离子键和共价键,干冰为分子晶体,升华时克服的是分子间作
用力,二者不同,C错误;氧化镁为离子晶体,熔化时克服的是离子键,金属镁为金属晶体,熔化时克服
的是金属键,二者不同,D错误。
8.下列各物质中,按熔点由高到低的顺序排列正确的是( )
A.CH>SiH >GeH>SnH B.KCl>NaCl>MgCl >MgO
4 4 4 4 2
C.Rb>K>Na>Li D.金刚石>Si>钠
【答案】D
【解析】晶体熔点的高低取决于构成该晶体的结构粒子间作用力的大小。A项物质均为结构相似的分
子晶体,其熔点取决于分子间作用力的大小,一般来说,结构相似的分子晶体,相对分子质量越大者分子
间作用力也越大,故A项各物质熔点应为逐渐升高的顺序;B项物质均为离子晶体,离子晶体熔点高低取
决于离子键键能的大小,一般来说,离子的半径越小,电荷越多,离子键的键能就越强,故B项各物质熔点也应为升高顺序;C项物质均为同主族的金属晶体,其熔点高低取决于金属键的强弱,而金属键键能与
金属原子半径成反比,与价电子数成正比,碱金属原子半径依Li~Cs的顺序增大,价电子数相同,故熔点
应是Li最高,Cs最低;D项,原子晶体的熔点取决于共价键的键能,后者则与键长成反比,金刚石C—C
键的键长更短些,所以金刚石的熔点比硅高,原子晶体的熔点一般比金属晶体的熔点高。
9.下面的叙述不正确的是( )
A. 晶胞空间利用率:金属铜>金属镁>金属钾>金属钋
B. 硬度由大到小:金刚石>碳化硅>晶体硅
C.晶体熔点由低到高:CH<SiH<GeH <SnH
4 4 4 4
D. 晶格能由大到小:NaF>NaCl>NaBr>NaI
【答案】A
【解析】A项,金属钾的空间利用率是68%,Po的空间利用率是52%,金属铜和金属镁的空间利用率
都是74%,因此不同金属的空间利用率大小关系为金属铜=金属镁>金属钾>金属钋,A项符合题意; B项,
三种晶体都是共价晶体,由于共价键的键长Si-Si>Si-C>C-C,共价键的键长越短,原子间形成的共价键结
合的就越牢固,晶体的硬度就越大,所以晶体硬度由大到小:金刚石>碳化硅>晶体硅,B项不符合题意;
C项,这几种物质都是分子晶体,分子间通过分子间作用力结合,由于分子间作用力随物质相对分子质量
的增大而增大,分子间作用力越大,克服分子间作用力使物质熔化需要的能量就越高,所以物质的熔点由
低到高:CHNaCl>NaBr>NaI,D项不符合题意;故选A。
10.(2023·浙江省浙南名校联盟高三第二次联考)冠醚是一类具有特殊性质的有机化合物最大的特点就
是能与正离子,尤其是与碱金属离子络合,二苯并—18—冠醚—6与 或 作用可表示为
下列说法不正确的( )
A.冠醚与碱金属离子间的作用力可能为非共价键作用力
B.冠醚与碱金属离子络合后形成化合物得到的晶体是离子晶体
C.冠醚络合哪种阳离子取决于O与阳离子的配位能力
D.通过冠醚将阳离子溶入有机溶剂是根据相似相溶的原理
【答案】C
【解析】A项,冠醚与碱金属离子以配位键形成超分子,则冠醚与碱金属离子间的作用力不是共价键,
是配位键,故A正确;B项,冠醚与碱金属离子络合形成的配离子与配合物中的阴离子形成离子化合物,
得到的晶体是离子晶体,故B正确;C项,冠醚络合哪种阳离子取决于空穴与阳离子的配位能力,不同大
小的空穴适配不同大小的碱金属离子,故C错误;D项,冠醚最主要的特点是与碱金属离子形成稳定的络
合物,则冠醚可以将阳离子溶入有机溶剂是利用了相似相溶的原理,故D正确;故选C。考点四 晶体结构与性质
1.(2023•辽宁省选择性考试,14)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞
是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的
是( )
A.图1晶体密度为 g∙cm-3 B.图1中O原子的配位数为6
C.图2表示的化学式为LiMg OCl Br D.Mg2+取代产生的空位有利于Li+传导
2 x 1-x
【答案】C
【解析】A项,根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的
质量为 g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密度为 g÷(a3×10-
30cm3)= g/cm3,A项正确;B项,图1晶胞中,O位于面心,与O等距离最近的Li有6个,
O原子的配位数为6,B项正确;C项,根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,
Cl或Br:4× =1,Mg的个数小于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br ,C
x 1-x
项错误;D项,进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明 Mg2+取代产生的空
位有利于Li+的传导,D项正确;故选C。
2.(2023•湖北省选择性考试,15)镧La和H可以形成一系列晶体材料LaH ,在储氢和超导等领域具有
n
重要应用。LaH 属于立方晶系,晶胞结构和参数如图所示。高压下,LaH 中的每个H结合4个H形成类
n 2
似CH 的结构,即得到晶体LaH 。下列说法错误的是( )
4 x
A.LaH 晶体中La的配位数为8
2B.晶体中H和H的最短距离:LaH >LaH
2 x
C.在LaH 晶胞中,H形成一个顶点数为40的闭合多面体笼
x
D.LaH 单位体积中含氢质量的计算式为
x
【答案】C
【解析】A项,由LaH 的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中心各有1个H
2
原子,若以顶点La研究,与之最近的H原子有8个,则La的配位数为8,故A正确;B项,由LaH 晶胞
x
结构可知,每个H结合4个H形成类似CH 的结构,H和H之间的最短距离变小,则晶体中H和H的最短
4
距离: LaH >LaH ,故B正确;C项,由题干信息可知,在LaH 晶胞中,每个H结合4个H形成类似
2 x x
CH 的结构,这样的结构有8个,顶点数为4 8=32,且不是闭合的结构,故C错误;D项,1个LaH 晶胞
4 x
中含有5 8=40个H原子,含H质量为 g,晶胞的体积为(484.0 10-10cm)3=(4.84 10-8)3cm3,则LaH 单
x
位体积中含氢质量的计算式为 ,故D正确;故选C。
3.(2023•湖南卷,11)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为a
pm。阿伏加德罗常数的值为N 。下列说法错误的是( )
A
A.晶体最简化学式为KCaB C
6 6
B.晶体中与 最近且距离相等的Ca2+有8个
C.晶胞中B和C原子构成的多面体有12个面
D.晶体的密度为
【答案】C
【解析】A项,根据晶胞结构可知,其中K个数:8× =1,其中Ca个数:1,其中B个数:12×
=6,其中C个数:12× =6,故其最简化学式为KCaB C ,A正确;B项,根据晶胞结构可知,K+位于晶
6 6
胞体心,Ca位于定点,则晶体中与K+最近且距离相等的Ca2+有8个,B正确;C项,根据晶胞结构可知,
晶胞中B和C原子构成的多面体有14个面,C错误;D项,根据选项A分析可知,该晶胞最简化学式为
KCaB C ,则1个晶胞质量为: ,晶胞体积为a3×10-30cm3,则其密度为 ,D正确;
6 6故选C。
4.(2022•湖北省选择性考试,9)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法
错误的是( )
A.Ca2+的配位数为6 B.与 距离最近的是K+
C.该物质的化学式为KCaF D.若 换为Cl-,则晶胞棱长将改变
3
【答案】B
【解析】A项,Ca2+配位数为与其距离最近且等距离的F-的个数,如图所示,Ca2+位于体心,F-位于面
心,所以Ca2+配位数为6,A正确;B项,F-与K+的最近距离为棱长的 ,F-与Ca2+的最近距离为棱长的
,所以与F-距离最近的是Ca2+,B错误;C项,K+位于顶点,所以K+个数= =1,F-位于面心,F-个数
= =3,Ca2+位于体心,所以Ca2+个数=1,综上,该物质的化学式为KCaF ,C正确;D项,F-与Cl-半径
3
不同,替换后晶胞棱长将改变,D正确;故选B。
5.(2022•山东卷,15)Cu Se是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的
2-x
组成变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是( )
A.每个Cu Se晶胞中Cu2+个数为x
2-x
B.每个NaSe晶胞完全转化为Cu Se晶胞,转移电子数为8
2 2-x
C.每个NaCuSe晶胞中0价Cu原子个数为1-x
D.当NaCu Se转化为NaCuSe时,每转移 电子,产生(1-x)mol原子
y 2-x
【答案】D
【解析】A项,由Cu Se晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,位于体内的
2-x
铜离子和亚铜离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化
合价代数和为0可得2a+b=4×2,解得a=4x,故A错误;B项,由NaSe转化为Cu Se的电极反应式为
2 2-x
NaSe-e-+(2-x)Cu=Cu Se+Na+,由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,则每个
2 2-x
晶胞中含有4个NaSe,转移电子数为4,故B错误;C项,由NaCuSe晶胞结构可知,位于顶点和面心的
2硒离子个数为8× +6× =4,则每个晶胞中含有4个NaCuSe,晶胞中0价铜而个数为(4-4x),故C错误;
D项,由题意可知,NaCu Se转化为NaCuSe的电极反应式为NaCu Se+(1-y) e-+ Na+=NaCuSe+(1-x)Cu,
y 2-x y 2-x
所以每转移(1-y)电子,产生(1-x)mol铜,故D正确;故选D。
6.(2021•湖北选择性考试,10)某立方晶系的锑钾(Sb-K)合金可作为钾离子电池的电极材料,图a为
该合金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是( )
A.该晶胞的体积为 B.K和Sb原子数之比为3:1
C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 pm
【答案】B
【解析】该晶胞的边长为a×1010 cm,故晶胞的体积为(a×1010 cm)3=a3×1030 cm3,A项错误;该晶胞
中K的个数为12×+9=12,Sb的个数为8×+6×=4,故K和Sb原子个数之比为3:1,B项正确;以面心
处Sb为研究对象,与Sb最邻近的K原子数为8,C项错误;K和Sb的最短距离为晶胞体对角线长度的,
即 pm,D项错误。
7.(2021•海南选择性考试,5) SF 可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。
6
有关SF 的说法正确的是( )
6
A.是非极性分子 B.键角 都等于90°
C. 与 之间共用电子对偏向S D. 原子满足8电子稳定结构
【答案】A
【解析】A项,结构对称、正负电荷重心重合的分子为非极性分子,SF 分子呈正八面体结构,S 原子
6
位于正八面体的中心,该分子结构对称、正负电荷重心重合,所以为非极性分子,A正确;B项,SF 是结
6
构对称、正负电荷重心重合的分子,故键角 不都等于90°,B错误;C项,由于F的电负性比S的大,
S与F之间共用电子对偏向F,C错误;D项,中心元素价电子数+化合价的绝对值=8时该分子中所有原子
都达到8电子稳定结构,但氢化物除外,该化合物中S元素化合价+价电子数=6+6=12,则S原子不是8电
子稳定结构,D错误;故选A。
8.(2023•全国乙卷,35节选) (3)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有_______个Mg;该物质化学式为_______,B-B最近距离为
_______。
【答案】(3) 1 MgB
2
【解析】(3)由硼镁化合物的晶体结构可知Mg位于正六棱柱的顶点和面心,由均摊法可以求出正六棱
柱中含有 个Mg,由晶胞沿c轴的投影图可知本题所给晶体结构包含三个晶胞,则晶胞中
Mg的个数为1;晶体结构中B在正六棱柱体内共6个,则该物质的化学式为MgB ;由晶胞沿c轴的投影
2
图可知,B原子在图中两个正三角形的重心,该点到顶点的距离是该点到对边中点距离的2倍,顶点到对
边的垂线长度为 ,因此B-B最近距离为 。
9.(2023•浙江省1月选考,17节选) (10分) (3)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是
___________,该化合物的化学式为___________。
【答案】(3)共价晶体 SiP
2
【解析】(3)Si与P形成的某化合物晶体的晶胞如图可知,原子间通过共价键形成的空间网状结构,形
成共价晶体;根据均摊法可知,一个晶胞中含有 个Si,8个P,故该化合物的化学式为
SiP。
2
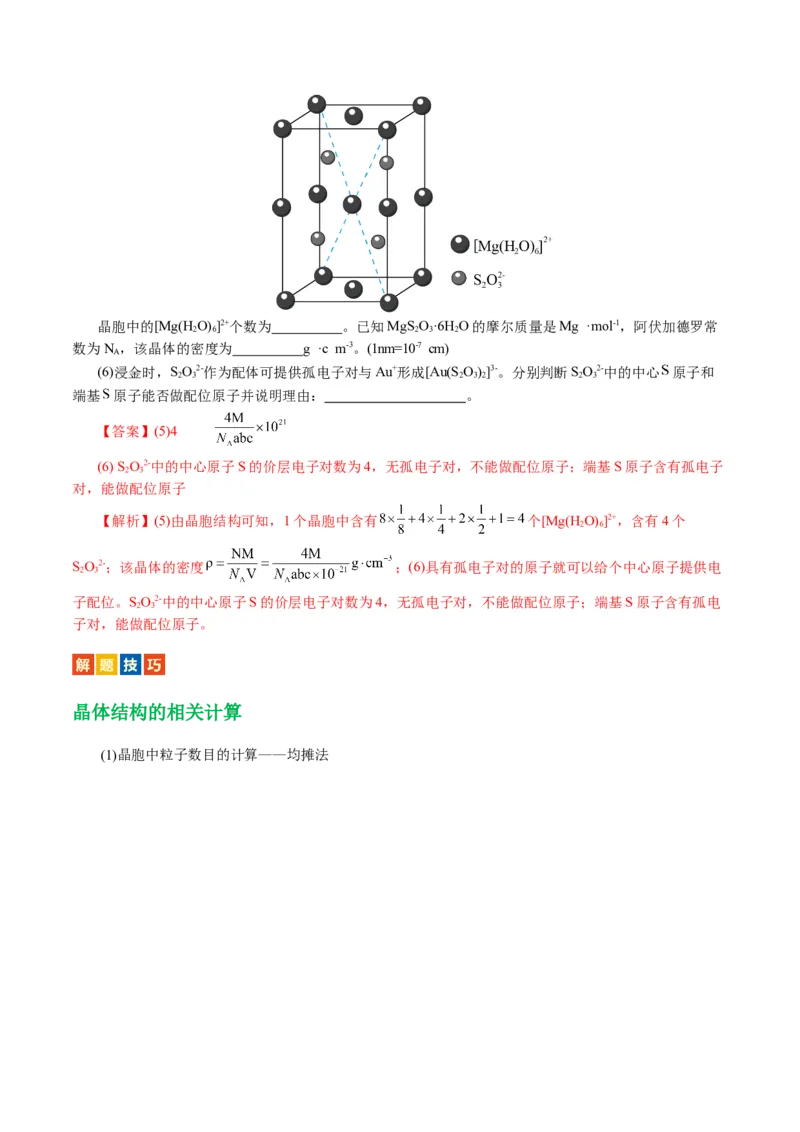
10.(10分)(2023•北京卷,15节选) (5) MgS O·6H O的晶胞形状为长方体,边长分别为a nm、b nm、c
2 3 2
nm,结构如图所示。晶胞中的[Mg(H O) ]2+个数为 。已知MgS O·6H O的摩尔质量是Mg ·mol-1,阿伏加德罗常
2 6 2 3 2
数为N ,该晶体的密度为 g ·c m-3。(1nm=10-7 cm)
A
(6)浸金时,SO2-作为配体可提供孤电子对与Au+形成[Au(SO)]3-。分别判断SO2-中的中心 原子和
2 3 2 3 2 2 3
端基 原子能否做配位原子并说明理由: 。
【答案】(5)4
(6) S O2-中的中心原子S的价层电子对数为4,无孤电子对,不能做配位原子;端基S原子含有孤电子
2 3
对,能做配位原子
【解析】(5)由晶胞结构可知,1个晶胞中含有 个[Mg(H O) ]2+,含有4个
2 6
SO2-;该晶体的密度 ;(6)具有孤电子对的原子就可以给个中心原子提供电
2 3
子配位。SO2-中的中心原子S的价层电子对数为4,无孤电子对,不能做配位原子;端基S原子含有孤电
2 3
子对,能做配位原子。
晶体结构的相关计算
(1)晶胞中粒子数目的计算——均摊法立方体中粒子周围粒子的个数判断
(2)晶体微粒与M、ρ之间的关系
若1个晶胞(立方晶胞)中含有x个微粒,则1 mol该晶胞中含有x mol 微粒,其质量为xM g(M为微粒
的相对分子质量);又1个晶胞的质量为ρa3 g(a3为晶胞的体积),则1 mol晶胞的质量为ρa3N g,因此有
A
xM=ρa3N 。
A
(3)金属晶体中体心立方堆积、面心立方堆积中的几组公式(设棱长为a)
①面对角线长=a。
②体对角线长=a。
③体心立方堆积4r=a(r为原子半径)。
④面心立方堆积4r=a(r为原子半径)。
(4)空间利用率=。
1.常见原子晶体结构分析
晶体 晶体结构 结构分析
(1)每个碳与相邻4个碳以共价键结合,形成正四面体结构,键角均为109°28′
(2)每个金刚石晶胞中含有8个碳原子,最小的碳环为6元环,并且不在同一
金刚石
平面(实际为椅式结构),碳原子为sp3杂化
(3)每个碳原子被12个六元环共用,每个共价键被6个六元环共用,一个六元原子半径(r)与边
环实际拥有 个碳原子
长(a)的关系:
(4)C原子数与C—C键数之比为1∶2,12g金刚石中有2 mol共价键
a=8r (5)密度= (a为晶胞边长,N A 为阿伏加德罗常数)
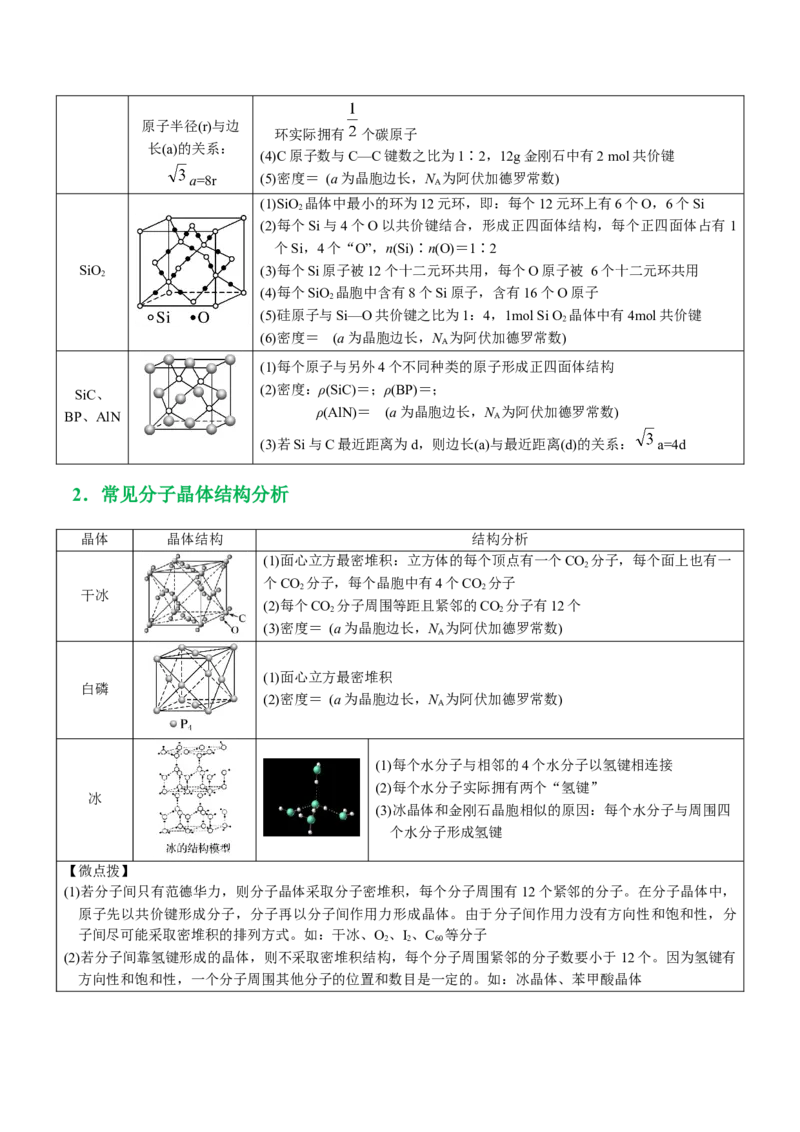
(1)SiO 晶体中最小的环为12元环,即:每个12元环上有6个O,6个Si
2
(2)每个Si与4个O以共价键结合,形成正四面体结构,每个正四面体占有1
个Si,4个“O”,n(Si)∶n(O)=1∶2
SiO (3)每个Si原子被12个十二元环共用,每个O原子被 6个十二元环共用
2
(4)每个SiO 晶胞中含有8个Si原子,含有16个O原子
2
(5)硅原子与Si—O共价键之比为1:4,1mol Si O 晶体中有4mol共价键
2
(6)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)每个原子与另外4个不同种类的原子形成正四面体结构
(2)密度:ρ(SiC)=;ρ(BP)=;
SiC、
BP、AlN
ρ(AlN)= (a为晶胞边长,N
A
为阿伏加德罗常数)
(3)若Si与C最近距离为d,则边长(a)与最近距离(d)的关系: a=4d
2.常见分子晶体结构分析
晶体 晶体结构 结构分析
(1)面心立方最密堆积:立方体的每个顶点有一个CO 分子,每个面上也有一
2
个CO 分子,每个晶胞中有4个CO 分子
2 2
干冰
(2)每个CO 分子周围等距且紧邻的CO 分子有12个
2 2
(3)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)面心立方最密堆积
白磷
(2)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)每个水分子与相邻的4个水分子以氢键相连接
(2)每个水分子实际拥有两个“氢键”
冰
(3)冰晶体和金刚石晶胞相似的原因:每个水分子与周围四
个水分子形成氢键
【微点拨】
(1)若分子间只有范德华力,则分子晶体采取分子密堆积,每个分子周围有12个紧邻的分子。在分子晶体中,
原子先以共价键形成分子,分子再以分子间作用力形成晶体。由于分子间作用力没有方向性和饱和性,分
子间尽可能采取密堆积的排列方式。如:干冰、O、I、C 等分子
2 2 60
(2)若分子间靠氢键形成的晶体,则不采取密堆积结构,每个分子周围紧邻的分子数要小于 12个。因为氢键有
方向性和饱和性,一个分子周围其他分子的位置和数目是一定的。如:冰晶体、苯甲酸晶体3.常见离子晶体结构分析
晶体 晶体结构 结构分析
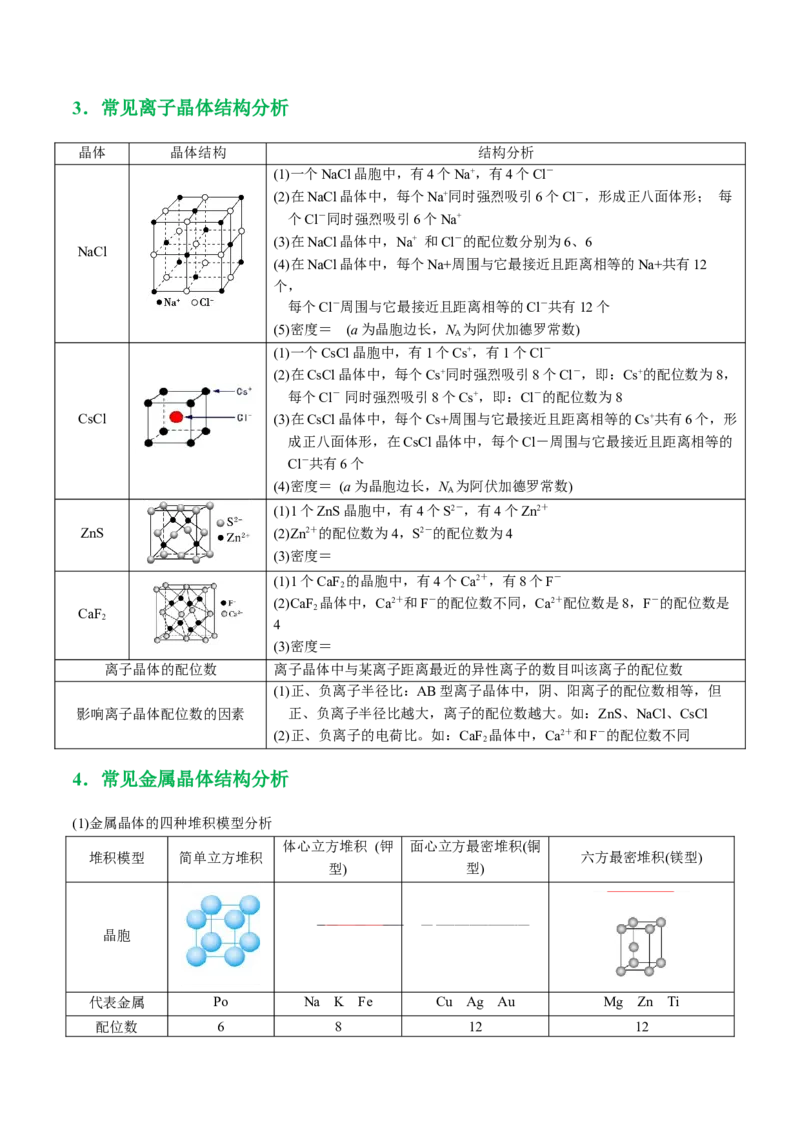
(1)一个NaCl晶胞中,有4个Na+,有4个Cl-
(2)在NaCl晶体中,每个Na+同时强烈吸引6个Cl-,形成正八面体形; 每
个Cl-同时强烈吸引6个Na+
(3)在NaCl晶体中,Na+ 和Cl-的配位数分别为6、6
NaCl
(4)在NaCl晶体中,每个Na+周围与它最接近且距离相等的Na+共有12
个,
每个Cl-周围与它最接近且距离相等的Cl-共有12个
(5)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)一个CsCl晶胞中,有1个Cs+,有1个Cl-
(2)在CsCl晶体中,每个Cs+同时强烈吸引8个Cl-,即:Cs+的配位数为8,
每个Cl- 同时强烈吸引8个Cs+,即:Cl-的配位数为8
CsCl (3)在CsCl晶体中,每个Cs+周围与它最接近且距离相等的Cs+共有6个,形
成正八面体形,在CsCl晶体中,每个Cl-周围与它最接近且距离相等的
Cl-共有6个
(4)密度= (a为晶胞边长,N 为阿伏加德罗常数)
A
(1)1个ZnS晶胞中,有4个S2-,有4个Zn2+
ZnS (2)Zn2+的配位数为4,S2-的配位数为4
(3)密度=
(1)1个CaF 的晶胞中,有4个Ca2+,有8个F-
2
(2)CaF 晶体中,Ca2+和F-的配位数不同,Ca2+配位数是8,F-的配位数是
CaF 2
2
4
(3)密度=
离子晶体的配位数 离子晶体中与某离子距离最近的异性离子的数目叫该离子的配位数
(1)正、负离子半径比:AB型离子晶体中,阴、阳离子的配位数相等,但
影响离子晶体配位数的因素 正、负离子半径比越大,离子的配位数越大。如:ZnS、NaCl、CsCl
(2)正、负离子的电荷比。如:CaF 晶体中,Ca2+和F-的配位数不同
2
4.常见金属晶体结构分析
(1)金属晶体的四种堆积模型分析
体心立方堆积 (钾 面心立方最密堆积(铜
堆积模型 简单立方堆积 六方最密堆积(镁型)
型) 型)
晶胞
代表金属 Po Na K Fe Cu Ag Au Mg Zn Ti
配位数 6 8 12 12晶胞占有的原
1 2 4 6或2
子数
原子半径(r)与
立方体边长为 a=2r a=4r a=4r ——
(a)的关系
1.(2024·吉林长春东北师大附中模拟)氮化铬的晶胞结构如图所示,A点分数坐标为(0,0,0)。氮化
铬的晶体密度为dg/cm3,摩尔质量为M g/mol,晶胞参数为anm,N 代表阿伏加德罗常数的值。下列说法
A
正确的是( )
A.铬原子的价电子排布式为
B.Cr原子位于N原子构成的四面体空隙中
C.距离Cr原子最近的Cr原子有8个
D.
【答案】D
【解析】A项,已知Cr是24号元素,根据洪特规则及特例可知,基态铬原子价层电子排布式为
3d54s1,A错误;B项,由题干晶胞示意图可知,Cr原子位于N原子构成的八面体空隙中,B错误;C项,
由题干晶胞示意图可知,距离体心的Cr原子最近的Cr原子位于棱心,共有12个,C错误;D项,由题干
晶胞示意图可知,N原子位于顶点和面心,个数为8× +6× =4,Cr原子位于棱心和体心,个数为12×
+1=4,晶胞质量为 g,晶胞体积为(a×10-7)3cm3,根据ρ= 可得,dgcm-3= ,则a=
⋅
,D正确;故选D。
2.(2024·吉林长春高三质量监测模)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方
晶胞参数为 。设N 为阿伏加德罗常数的值。下列说法错误的是( )
AA.晶体的最简化学式为KCaB C
6 6
B.晶体中与 最近且距离相等的 有4个
C.晶胞中B和C原子构成的多面体有14个面
D.晶体的密度为
【答案】B
【解析】A项,根据均摊法,K原子处在晶胞顶点,个数为 =1,Ca原子处在体心,个数为1个,
B原子在晶胞每个面上有2个,则个数为12 =6,C原子每个面上有2个,个数为12 =6,则晶胞的最
简化学式为KCaB C ,故A正确;B项,K原子处在晶胞顶点,Ca原子处在晶胞体心,1个K原子同时被
6 6
8个晶胞共有,则晶体中与K+最近且距离相等的Ca2+有8个,故B错误;C项,晶胞中B和C原子构成的
多面体,同一个面上的B和C原子构成的面总共有6个,晶胞每个顶点对应1个B和C原子构成的面,总
共有8面,合起来6+8=14,故C正确;D项,晶胞的质量为 ,晶胞的
体积为v=a3 10-30cm3,则晶胞密度为 ,故D正确;答案B。
3.(2024·江西景德镇市高三第一次质量检测联考)KIO 晶体具有钙钛矿型的立方结构,其一种晶胞如
3
图所示,其中顶点为K,晶胞边长为a pm,下列说法正确的是( )
A.碘氧键的键长为
B.距离K最近的O有12个
C.KIO 的另一种晶胞图中,若I在顶点,则O在体心
3
D.晶体密度
【答案】B【解析】根据均摊原则,顶点原子数 、体心原子数为1、面心原子数 ,顶点为K,根
据化学式KIO ,可知体心为I、面心为O。A项,体心为I、面心为O,碘氧键的键长为晶胞边长的一半,
3
碘氧键的键长为 ,故A错误;B项,顶点为K、面心为O,所以距离K最近的O有12个,故B正确;
C项,KIO 的另一种晶胞图中,若I在顶点,则O在棱心,故C错误;D项,晶体密度
3
,故D错误;选B。
4.(2024·重庆渝中高三期中)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立
方体(图1),在进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是(
)
A.图1中O 原子的配位数为8 B.图1 晶体密度为
C.图2 表示的化学式为LiMgOCl Br D.Mg2+取代产生的空位有利于Li⁺传导
x 1-x
【答案】A
【解析】A项,图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,A符
合题意;B项,根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的质量
为 g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密度为 g÷(a3×10-30cm3)=
,B不符合题意;C项,根据均摊法,图2中Li:1,Mg或空位为8× =2,O:2×
=1,Cl或Br:4× =1,Mg的个数小于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br
x 1-
,C不符合题意;D项,进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代
x
产生的空位有利于Li+的传导,D不符合题意;故选A。
5.(2024·河南高三联考)Fe CuN晶胞结构如图所示,若晶胞参数为apm,N 表示阿伏加德罗常数的
x y A
值。下列说法错误的是( )A.
B.B.若以N为顶点建立晶胞,则Fe位于棱心的位置
C.相邻两铁原子间最短距离为
D.晶体密度为
【答案】D
【解析】A项,晶胞中Cu个数为 ,Fe个数为 ,N个数为1,则 ,故A正确;
B项,若以N为顶点建立晶胞,则Fe位于棱心的位置,按照均摊法棱心位置Fe原子数为3个,故B正确;
C项,相邻两铁原子间最短距离为 的棱长,即 ,故C正确;D项,晶体密度等于晶胞质量除
以晶胞体积,其中晶胞体积为 ,晶胞的质量为 ,晶体的密度为
,故D错误;故选D。
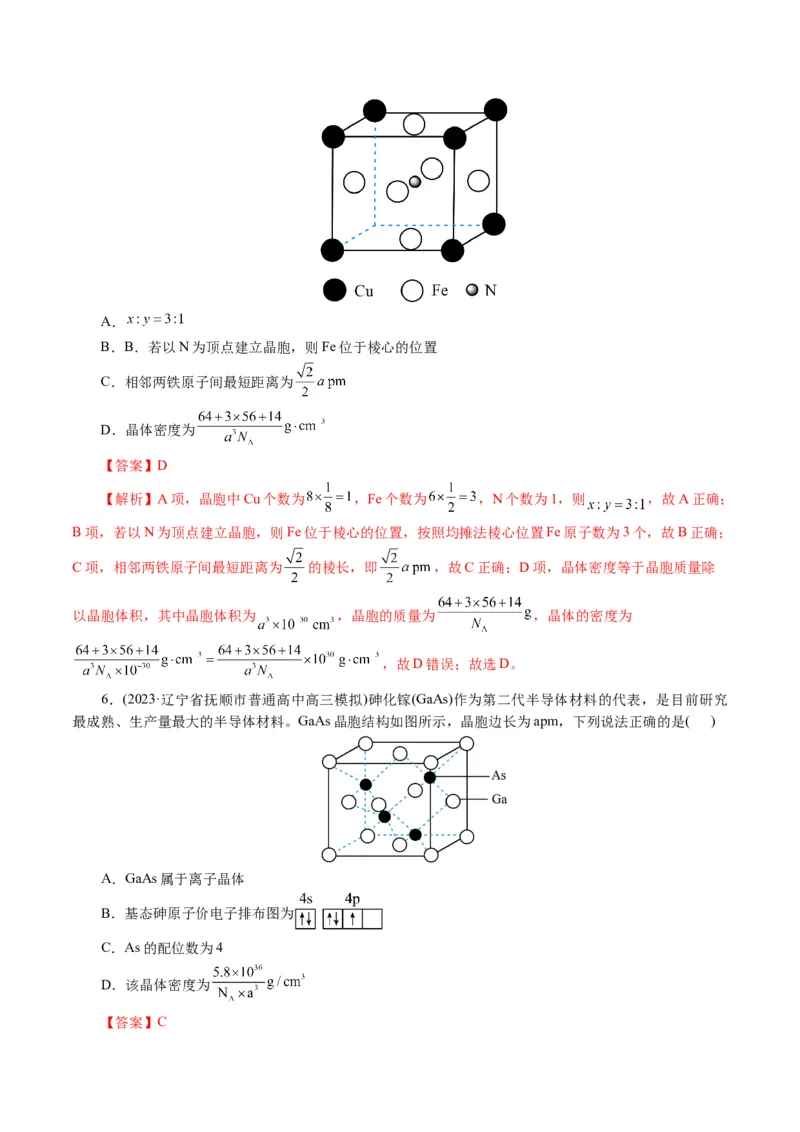
6.(2023·辽宁省抚顺市普通高中高三模拟)砷化镓(GaAs)作为第二代半导体材料的代表,是目前研究
最成熟、生产量最大的半导体材料。GaAs晶胞结构如图所示,晶胞边长为apm,下列说法正确的是( )
A.GaAs属于离子晶体
B.基态砷原子价电子排布图为
C.As的配位数为4
D.该晶体密度为
【答案】C【关键能力】宏观辨识与微观探析
【解析】A项,根据题中GaAs晶胞结构图,可知该晶胞含有Ga原子和As原子,微粒间的作用力是
共价键,属于共价晶体,A错误;B项,砷元素的质子数为33,依据构造原理写出核外电子排布式为
[Ar]4s24p3,价电子排布式为4s24p3,则价电子排布图为 ,B错误;C项,由GaAs晶胞结构
图,可知与砷原子距离最近的镓原子的个数为4,则As的配位数为4,C正确;D项,根据GaAs晶胞结构
图,可得出位于晶体内部的砷原子的个数为4,位于顶点和面心的镓原子个数为 ,设晶体的
密度为dg/cm3,则 ,D错误;故选C。
7.锌与硫所形成化合物晶体的晶胞如图所示。下列判断错误的是( )
A.Zn位于元素周期表的d区 B.该晶胞中Zn2+和S2-数目相等
C.S2-位于Zn2+构成的四面体空隙中 D.氧化锌的熔点高于硫化锌
【答案】A
【解析】A项,Zn的价电子排布式为:3d104s2,故Zn位于元素周期表ds区,A错误;B项,由图可
知,Zn2+位于顶点和面心,个数为 ,S2-位于体内,其个数为4,则离子数目相同,B正确;C
项,由图可知每个S2-周围有4个Zn2+,C正确;D项,同类型的离子晶体中,离子半径越小,晶格能越大,
因氧离子半径小于硫离子半径,则氧化锌的晶格能大于硫化锌,D正确。故选A。
8.(2024·江西省部分高中学校高三联考)某课题组用过渡金属碳化物(Co ZnC)合成了具有催化活性位点
3
的钴单质催化剂。下列叙述正确的是( )
已知:①Co ZnC中,C位于晶胞内部,且图1和图3晶胞中原子总数相等;
3
②N 代表阿伏加德罗常数的值,Co晶胞的底边长和高均为2apm,宽为apm。
A
A.1个 晶胞中含5个原子
B.1个 晶胞的质量为C.上述晶胞涉及的元素位于周期表2个区
D.钴晶体的密度为
【答案】D
【解析】A项,1个Co ZnC晶胞中含12个Co、4个Zn和4个C,A项错误;B项,N 个
3 A
晶胞的质量为 ,B项错误;C项,题中所述晶胞涉及Co、Zn、C
三种元素,分别位于d区、ds区和p区,C项错误;D项,钴晶体晶胞的质量为 ,晶胞体积为:
,钴晶体的密度为 ,故D正确;故选D。
9.近期,我国科技工作者合成了一种高质量的纳米棒发光材料,其晶胞结构如图所示,晶胞的边长
a。下列说法错误的是( )
A.与Cs+距离最近I-个数为12 B.Pb2+的配位数为6
C.Pb2+与Cs+间最短距离为 D.该物质的化学式为CsPbI
3
【答案】C
【解析】A项,Cs+位于晶胞顶点,I-位于面心,1个晶胞中有3个面心I-离顶点Cs+最近,1个顶点周围
可以放8个晶胞,而面心I-又被两个晶胞共用,故1个Cs+周围最近的I-有 个,A正确;B项,
Pb2+位于体心,其周围6个面心I-离其最近,故Pb2+配位数为6,B正确;C项,Pb2+与Cs+最短距离为体对
角线的一半,面对角线长度= ,则体对角线= ,则Pb2+与Cs+最短距离为 ,C错误;
D项,该晶胞中含Cs+= 个,含Pb2+1个,含I-= 个,三者之比为1:1:3,故该物质化学式为:
CsPbI ,D正确;故选C。
3
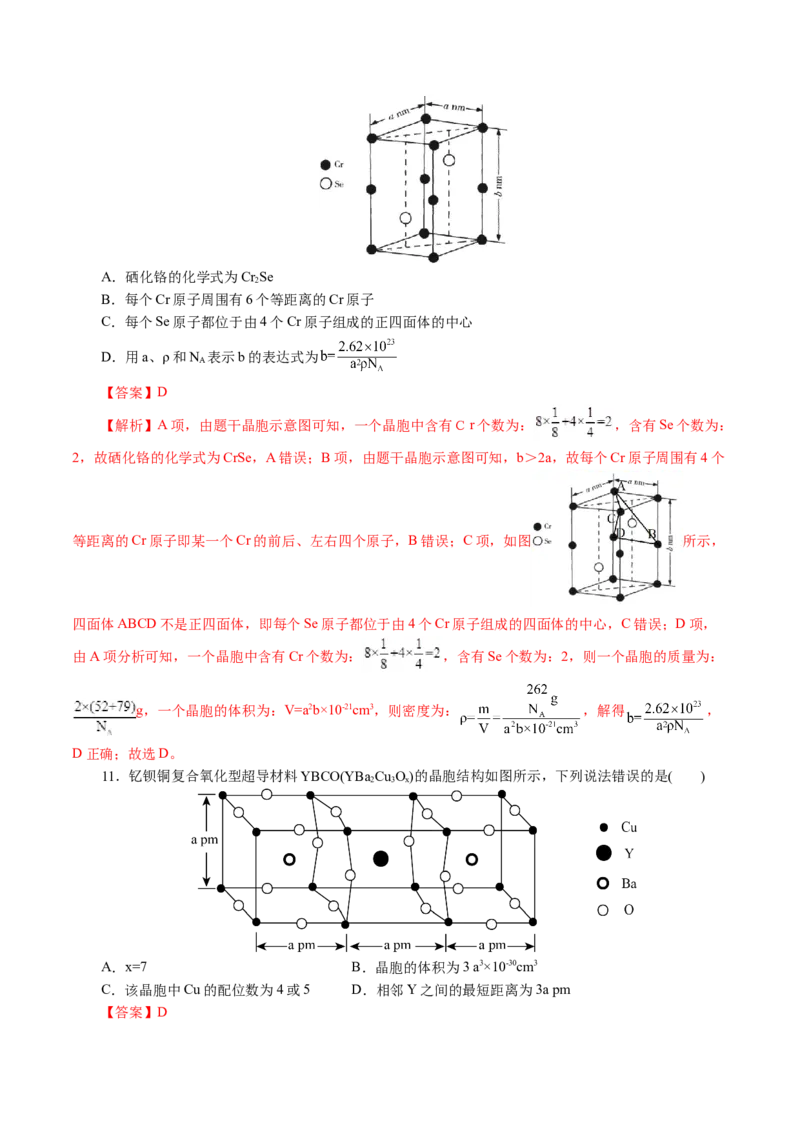
10.已知硒化铬的晶胞结构如图所示,晶胞参数为anm和bnm(晶胞棱边夹角均为90°),密度为
ρg·cm-3,设阿伏加德罗常数的值为N 。下列说法正确的是( )
AA.硒化铬的化学式为Cr Se
2
B.每个Cr原子周围有6个等距离的Cr原子
C.每个Se原子都位于由4个Cr原子组成的正四面体的中心
D.用a、ρ和N 表示b的表达式为
A
【答案】D
【解析】A项,由题干晶胞示意图可知,一个晶胞中含有Cr个数为: ,含有Se个数为:
2,故硒化铬的化学式为CrSe,A错误;B项,由题干晶胞示意图可知,b>2a,故每个Cr原子周围有4个
等距离的Cr原子即某一个Cr的前后、左右四个原子,B错误;C项,如图 所示,
四面体ABCD不是正四面体,即每个Se原子都位于由4个Cr原子组成的四面体的中心,C错误;D项,
由A项分析可知,一个晶胞中含有Cr个数为: ,含有Se个数为:2,则一个晶胞的质量为:
g,一个晶胞的体积为:V=a2b×10-21cm3,则密度为: ,解得 ,
D正确;故选D。
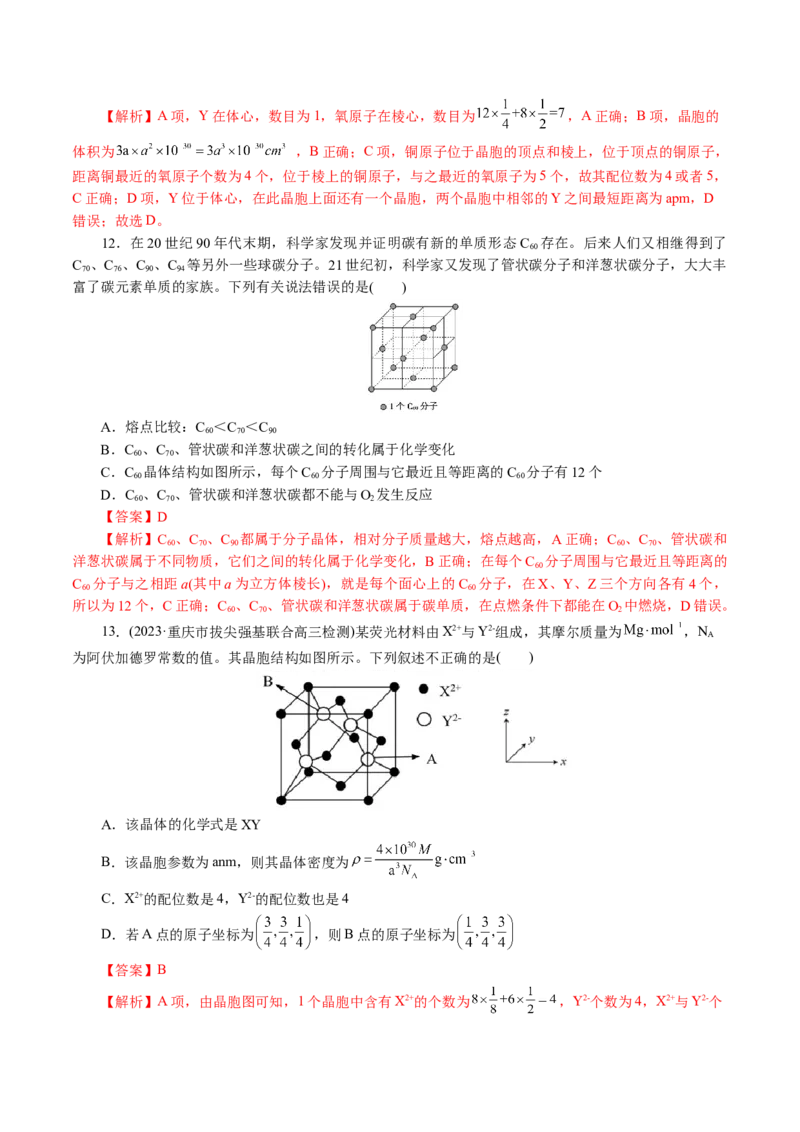
11.钇钡铜复合氧化型超导材料YBCO(YBa Cu O)的晶胞结构如图所示,下列说法错误的是( )
2 3 x
A.x=7 B.晶胞的体积为3 a3×10-30cm3
C.该晶胞中Cu的配位数为4或5 D.相邻Y之间的最短距离为3a pm
【答案】D【解析】A项,Y在体心,数目为1,氧原子在棱心,数目为 ,A正确;B项,晶胞的
体积为 ,B正确;C项,铜原子位于晶胞的顶点和棱上,位于顶点的铜原子,
距离铜最近的氧原子个数为4个,位于棱上的铜原子,与之最近的氧原子为5个,故其配位数为4或者5,
C正确;D项,Y位于体心,在此晶胞上面还有一个晶胞,两个晶胞中相邻的Y之间最短距离为apm,D
错误;故选D。
12.在20世纪90年代末期,科学家发现并证明碳有新的单质形态C 存在。后来人们又相继得到了
60
C 、C 、C 、C 等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰
70 76 90 94
富了碳元素单质的家族。下列有关说法错误的是( )
A.熔点比较:C <C <C
60 70 90
B.C 、C 、管状碳和洋葱状碳之间的转化属于化学变化
60 70
C.C 晶体结构如图所示,每个C 分子周围与它最近且等距离的C 分子有12个
60 60 60
D.C 、C 、管状碳和洋葱状碳都不能与O 发生反应
60 70 2
【答案】D
【解析】C 、C 、C 都属于分子晶体,相对分子质量越大,熔点越高,A正确;C 、C 、管状碳和
60 70 90 60 70
洋葱状碳属于不同物质,它们之间的转化属于化学变化,B正确;在每个C 分子周围与它最近且等距离的
60
C 分子与之相距a(其中a为立方体棱长),就是每个面心上的C 分子,在X、Y、Z三个方向各有4个,
60 60
所以为12个,C正确;C 、C 、管状碳和洋葱状碳属于碳单质,在点燃条件下都能在O 中燃烧,D错误。
60 70 2
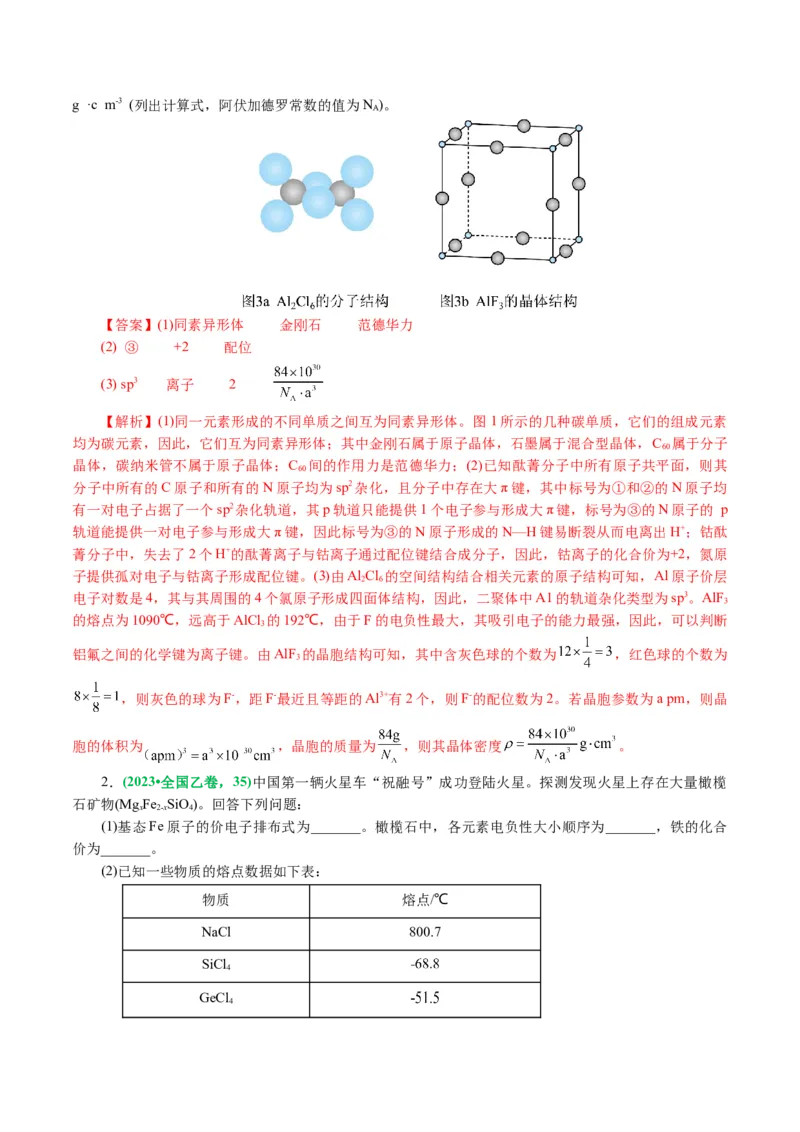
13.(2023·重庆市拔尖强基联合高三检测)某荧光材料由X2+与Y2-组成,其摩尔质量为 ,N
A
为阿伏加德罗常数的值。其晶胞结构如图所示。下列叙述不正确的是( )
A.该晶体的化学式是XY
B.该晶胞参数为anm,则其晶体密度为
C.X2+的配位数是4,Y2-的配位数也是4
D.若A点的原子坐标为 ,则B点的原子坐标为
【答案】B
【解析】A项,由晶胞图可知,1个晶胞中含有X2+的个数为 ,Y2-个数为4,X2+与Y2-个数比为1:1,因此该晶体的化学式是XY,故A项正确;B项,1个晶胞中含有4个XY,即1个晶胞的质
量为 ,晶胞体积为 ,因此晶体密度 ,故B项错误;C项,由图可
知,距离X2+最近且等距的Y2-有4个,距离Y2-最近且等距的X2+有4个,故C项正确;D项,若A点的原
子坐标为 ,则原点位于左下前X2+的顶点,该晶胞自下至上可分为4层(X2+-Y2--X2+-Y2--X2+),同理
从左至右也可分为4层(X2+-Y2--X2+-Y2--X2+),因此B点的原子坐标为 ,故D项正确;故选B。
考点五 物质结构与性质综合
1.(2023•全国甲卷,35)将酞菁—钴钛—三氯化铝复合嵌接在碳纳米管上,制得一种高效催化还原二
氧化碳的催化剂。回答下列问题:
(1)图1所示的几种碳单质,它们互为_______,其中属于原子晶体的是_______,C 间的作用力是
60
_______。
(2)酞菁和钴酞菁的分子结构如图2所示。
酞菁分子中所有原子共平面,其中 轨道能提供一对电子的 原子是_______(填图2酞菁中 原子的
标号)。钴酞菁分子中,钴离子的化合价为_______,氮原子提供孤对电子与钴离子形成_______键。
(3)气态AlCl 通常以二聚体Al Cl 的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型
3 2 6
为_______。AlF 的熔点为 ,远高于AlCl 的 ,由此可以判断铝氟之间的化学键为_______键。
3 3
AlF 结构属立方晶系,晶胞如图3b所示,F-的配位数为_______。若晶胞参数为 ,晶体密度ρ=_______
3g ·c m-3 (列出计算式,阿伏加德罗常数的值为N )。
A
【答案】(1)同素异形体 金刚石 范德华力
(2) ③ +2 配位
(3) sp3 离子 2
【解析】(1)同一元素形成的不同单质之间互为同素异形体。图 1所示的几种碳单质,它们的组成元素
均为碳元素,因此,它们互为同素异形体;其中金刚石属于原子晶体,石墨属于混合型晶体,C 属于分子
60
晶体,碳纳米管不属于原子晶体;C 间的作用力是范德华力;(2)已知酞菁分子中所有原子共平面,则其
60
分子中所有的C原子和所有的N原子均为sp2杂化,且分子中存在大π键,其中标号为①和②的N原子均
有一对电子占据了一个sp2杂化轨道,其p轨道只能提供1个电子参与形成大π键,标号为③的N原子的 p
轨道能提供一对电子参与形成大π键,因此标号为③的N原子形成的N—H键易断裂从而电离出H+;钴酞
菁分子中,失去了2个H+的酞菁离子与钴离子通过配位键结合成分子,因此,钴离子的化合价为+2,氮原
子提供孤对电子与钴离子形成配位键。(3)由Al Cl 的空间结构结合相关元素的原子结构可知,Al原子价层
2 6
电子对数是4,其与其周围的4个氯原子形成四面体结构,因此,二聚体中A1的轨道杂化类型为sp3。AlF
3
的熔点为1090℃,远高于AlCl 的192℃,由于F的电负性最大,其吸引电子的能力最强,因此,可以判断
3
铝氟之间的化学键为离子键。由AlF 的晶胞结构可知,其中含灰色球的个数为 ,红色球的个数为
3
,则灰色的球为F-,距F-最近且等距的Al3+有2个,则F-的配位数为2。若晶胞参数为a pm,则晶
胞的体积为 ,晶胞的质量为 ,则其晶体密度 。
2.(2023•全国乙卷,35)中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄
石矿物(MgFe SiO)。回答下列问题:
x 2-x 4
(1)基态Fe原子的价电子排布式为_______。橄榄石中,各元素电负性大小顺序为_______,铁的化合
价为_______。
(2)已知一些物质的熔点数据如下表:
物质 熔点/℃
NaCl 800.7
SiCl
4
GeCl
4SnCl
4
Na与Si均为第三周期元素,NaCl熔点明显高于 SiCl ,原因是_______。分析同族元素的氯化物
4
SiCl 、GeCl 、SnCl 熔点变化趋势及其原因_______。SiCl 的空间结构为_______,其中Si的轨道杂化形式
4 4 4 4
为_______。
(3)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如下所
示,晶胞中含有_______个Mg;该物质化学式为_______,B-B最近距离为_______。
【答案】(1) 3d64s2 O>Si>Fe>Mg +2
(2) 钠的电负性小于硅,氯化钠为离子晶体,而SiCl 为分子晶体 随着同族元素的电子层数的增
4
多,其熔点依次升高,其原因是:SiCl 、GeCl 、SnCl 均形成分子晶体,分子晶体的熔点由分子间作用力
4 4 4
决定,分子间作用力越大则其熔点越高;随着其相对分子质量增大,其分子间作用力依次增大 正四
面体 sp3
(3) 1 MgB
2
【解析】(1)Fe为26号元素,基态Fe原子的价电子排布式为3d64s2。元素的金属性越强,其电负性越
小,元素的非金属性越强则其电负性越大,因此,橄榄石(MgFe SiO)中,各元素电负性大小顺序为O>
x 2-x 4
Si>Fe>Mg;因为MgFe SiO 中Mg、Si、O的化合价分别为+2、+4和-2,x+2-x=2,根据化合物中各元
x 2-x 4
素的化合价的代数和为0,可以确定铁的化合价为+2。(2)Na与Si均为第三周期元素,NaCl熔点明显高于
SiCl ,原因是:钠的电负性小于硅,氯化钠为离子晶体,其熔点较高;而SiCl 为分子晶体,其熔点较低。
4 4
由表中的数据可知,SiCl 、GeCl 、SnCl 熔点变化趋势为:随着同族元素的电子层数的增多,其熔点依次
4 4 4
升高,其原因是:SiCl 、GeCl 、SnCl 均形成分子晶体,分子晶体的熔点由分子间作用力决定,分子间作
4 4 4
用力越大则其熔点越高;随着其相对分子质量增大,其分子间作用力依次增大。SiCl 的空间结构为正四面
4
体,其中Si的价层电子对数为4,因此Si的轨道杂化形式为sp3。(3)由硼镁化合物的晶体结构可知Mg位
于正六棱柱的顶点和面心,由均摊法可以求出正六棱柱中含有 个Mg,由晶胞沿c轴的投影
图可知本题所给晶体结构包含三个晶胞,则晶胞中Mg的个数为1;晶体结构中B在正六棱柱体内共6个,
则该物质的化学式为MgB ;由晶胞沿c轴的投影图可知,B原子在图中两个正三角形的重心,该点到顶点
2
的距离是该点到对边中点距离的 2 倍,顶点到对边的垂线长度为 ,因此 B-B 最近距离为
。
3.(2023•浙江省1月选考,17改编)硅材料在生活中占有重要地位。
请回答:
(1) Si(NH ) 分子的空间结构(以Si为中心)名称为________,分子中氮原子的杂化轨道类型是_______。
2 4
Si(NH ) 受热分解生成Si N 和NH ,其受热不稳定的原因是________。
2 4 3 4 3(2)由硅原子核形成的三种微粒,电子排布式分别为:①[Ne]3s23p2、②[Ne]3s23p1、③[Ne]3s23p14s1,有
关这些微粒的叙述,正确的是___________。
A.微粒半径:③>①>②
B.电子排布属于基态原子(或离子)的是:①②
C.电离一个电子所需最低能量:①>②>③
D.得电子能力:①>②
(3)Si 与 P 形成的某化合物晶体的晶胞如图。该晶体类型是___________,该化合物的化学式为
___________。
【答案】(1)四面体 sp3
Si周围的NH 基团体积较大,受热时斥力较强[Si(NH ) 中Si-N键键能相对较小];产物中气态分子数
2 2 4
显著增多(熵增)
(2)AB (3)共价晶体 SiP
2
【解析】(1)Si(NH ) 分子可视为SiH 分子中的4个氢原子被—NH (氨基)取代形成的,所以Si(NH ) 分
2 4 4 2 2 4
子中Si原子轨道的杂化类型是sp3,分子的空间结构(以Si为中心)名称为四面体;氨基(-NH )氮原子形成3
2
个σ键,含有1对孤对电子,N原子杂化轨道数目为4,N原子轨道的杂化类型是sp3;Si周围的NH 基团
2
体积较大,受热时斥力较强 Si(NH ) 中Si-N键能相对较小];产物中气态分子数显著增多(熵增),故
2 4
Si(NH ) 受热不稳定,容易分解生成Si N 和NH ;(2)电子排布式分别为:①[Ne]3s23p2、②[Ne]3s23p1、
2 4 3 4 3
③[Ne]3s23p14s1,可推知分别为基态Si原子、基态Al原子、激发态Si原子;A项,根据微粒电子层数及各
层电子数多少可推知,微粒半径:③>①>②,A正确;B项,根据上述分析可知,电子排布属于基态原子
(或离子)的是:①②,B正确;C项,Si为非金属失电子能力比Al弱,电离一个电子所需最低能量:
①>③>②,C错误;D项,非金属Si的得电子能力强于金属Al,得电子能力:②>①,D错误;故选AB;
(3)Si与P形成的某化合物晶体的晶胞如图可知,原子间通过共价键形成的空间网状结构,形成共价晶体;
根据均摊法可知,一个晶胞中含有 个Si,8个P,故该化合物的化学式为SiP。
2
4.(2023•山东卷,16改编)卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1) -405℃时,F 与冰反应生成HOF利HF。常温常压下,HOF为无色气体,固态HOF的晶体类型为
2
_____,HOF水解反应的产物为_____(填化学式)。
(2) Cl O中心原子为Cl,Cl O中心原子为 ,二者均为 形结构,但ClO 中存在大 键 。ClO
2 2 2 2
中Cl原子的轨道杂化方式_____;为O-Cl-O键角_____Cl-O-Cl键角(填“>”“ <”或“=”)。比较ClO 与
2
Cl O中Cl-O键的键长并说明原因_____。
2
(3)一定条件下,CuCl 、K和F 反应生成 和化合物 。已知 属于四方晶系,晶胞结构如图所示
2 2
(晶胞参数 ),其中 化合价为 。上述反应的化学方程式为_____。若阿伏加德罗
常数的值为 ,化合物 的密度 _____ (用含 的代数式表示)。【答案】(1)分子晶体 HF 、HO 和O
2 2 2
(2) sp2 > ClO 分子中Cl-O键的键长小于Cl O中Cl-O键的键长,其原因是:ClO 分子中既
2 2 2
存在σ键,又存在大π键,原子轨道重叠的程度较大,因此其中Cl-O键的键长较小,而Cl O只存在普通
2
的σ键
(3) CuCl +4K+2F=KCuF+2KCl
2 2 2 4
【解析】(1)常温常压下,HOF为无色气体,则HOF的沸点较低,因此,固态HOF的晶体类型为分子
晶体。HOF分子中F显-1价,其水解时结合HO电离的H+生成HF,则OH+结合HO电离的OH-,两者反
2 2
应生成HO ,HO 不稳定,其分解生成O ,因此,HOF水解反应的产物为HF 、HO 和O 。(2)ClO 中心
2 2 2 2 2 2 2 2 2
原子为Cl,Cl O中心原子为O,二者均为V形结构,但ClO 中存在大π键( )。由ClO 中存在 可以推
2 2 2
断,其中Cl原子只能提供1对电子,有一个O原子提供1个电子,另一个O原子提供1对电子,这5个电
子处于互相平行的p轨道中形成大π键,Cl提供孤电子对与其中一个O形成配位键,与另一个O形成的是
普通的共价键(σ键,这个O只提供了一个电子参与形成大π键), Cl的价层电子对数为3,则 原子的轨
道杂化方式为sp2;Cl O中心原子为O,根据价层电子对的计算公式可知 ,因此,O的杂化
2
方式为sp3;根据价层电子对互斥理论可知,n =4时,价电子对的几何构型为正四面体,n =3时,价电子
对的几何构型平面正三角形,sp2杂化的键角一定大于sp3的,因此,虽然ClO 和Cl O均为V形结构,但
2 2
O-Cl-O键角大于Cl-O-Cl键角,孤电子对对成键电子对的排斥作用也改变不了这个结论。ClO 分子中Cl-O
2
键的键长小于Cl O中Cl-O键的键长,其原因是:ClO 分子中既存在σ键,又存在大π键,原子轨道重叠
2 2
的程度较大,因此其中Cl-O键的键长较小,而Cl O只存在普通的σ键。(3)一定条件下,CuCl、K和F 反
2 2 2
应生成KCl和化合物X。已知X属于四方晶系,其中Cu化合价为+2。由晶胞结构图可知,该晶胞中含有
黑球的个数为 、白球的个数为 、灰色球的个数为 ,则X中含有3
种元素,其个数比为1:2:4,由于其中Cu化合价为+2、F的化合价为-1、K的化合价为+1,根据化合价代
数和为0,可以推断X为KCuF ,上述反应的化学方程式为CuCl +4K+2F= KCuF+2KCl。若阿伏加德罗
2 4 2 2 2 4
富数的值为 N ,晶胞的质量为 ,晶胞的体积为 ,化合物 X 的密度
A
。
5. (2023•浙江省6月选考,17改编)氮的化合物种类繁多,应用广泛。请回答:
(1)基态N原子的价层电子排布式是___________。
(2)与碳氢化合物类似,N、H两元素之间也可以形成氮烷、氮烯。
①下列说法不正确的是___________。
A.能量最低的激发态N原子的电子排布式:1s22s12p33s1
B.化学键中离子键成分的百分数:CaN>MgN
3 2 3 2
C.最简单的氮烯分子式:NH
2 2
D.氮烷中N原子的杂化方式都是sp3
②氮和氢形成的无环氨多烯,设分子中氮原子数为n,双键数为m,其分子式通式为______。
③给出H+的能力:NH _______[ CuNH ]2+ (填“>”或“<”),理由是___________。
3 3
(3)某含氮化合物晶胞如图,其化学式为___________,每个阴离子团的配位数(紧邻的阳离子数)为
___________。
【答案】(1)2s22p3
(2)① A ②NH ( ,m为正整数) ③< ④[CuNH ]2+形成配位键后,由于Cu对电子
n n+2−2m 3
的吸引,使得电子云向铜偏移,进一步使氮氢键的极性变大,故其更易断裂
(3) ①CaCN ②6
2
【解析】(1)N核电荷数为7,核外有7个电子,基态N原子电子排布式为1s22s22p3,则基态N原子的
价层电子排布式是2s22p3;(2)①A项,能量最低的激发态N原子应该是2p能级上一个电子跃迁到3s能级,
其电子排布式:1s22s22p23s1,故A错误;B项,钙的金属性比镁的金属性强,则化学键中离子键成分的百
分数:CaN >MgN ,故B正确;C项,氮有三个价键,最简单的氮烯即含一个氮氮双键,另一个价键与
3 2 3 2
氢结合,则其分子式:NH ,故C正确;D项,氮烷中N原子有一对孤对电子,有三个价键,则氮原子的
2 2
杂化方式都是sp3,故D正确;故选A。②氮和氢形成的无环氨多烯,一个氮的氮烷为NH ,两个氮的氮烷
3
为NH ,三个氮的氮烷为NH ,四个氮的氮烷为NH ,设分子中氮原子数为n,其氮烷分子式通式为
2 4 3 5 4 6
NH ,根据又一个氮氮双键,则少2个氢原子,因此当双键数为m,其分子式通式为NH ( ,
n n+2 n n+2−2m
m为正整数);③[CuNH ]2+形成配位键后,由于Cu对电子的吸引,使得电子云向铜偏移,进一步使氮氢键
3
的极性变大,故其更易断裂,因此给出H+的能力:NH <[CuNH ]2+;(3)钙个数为 ,
3 3
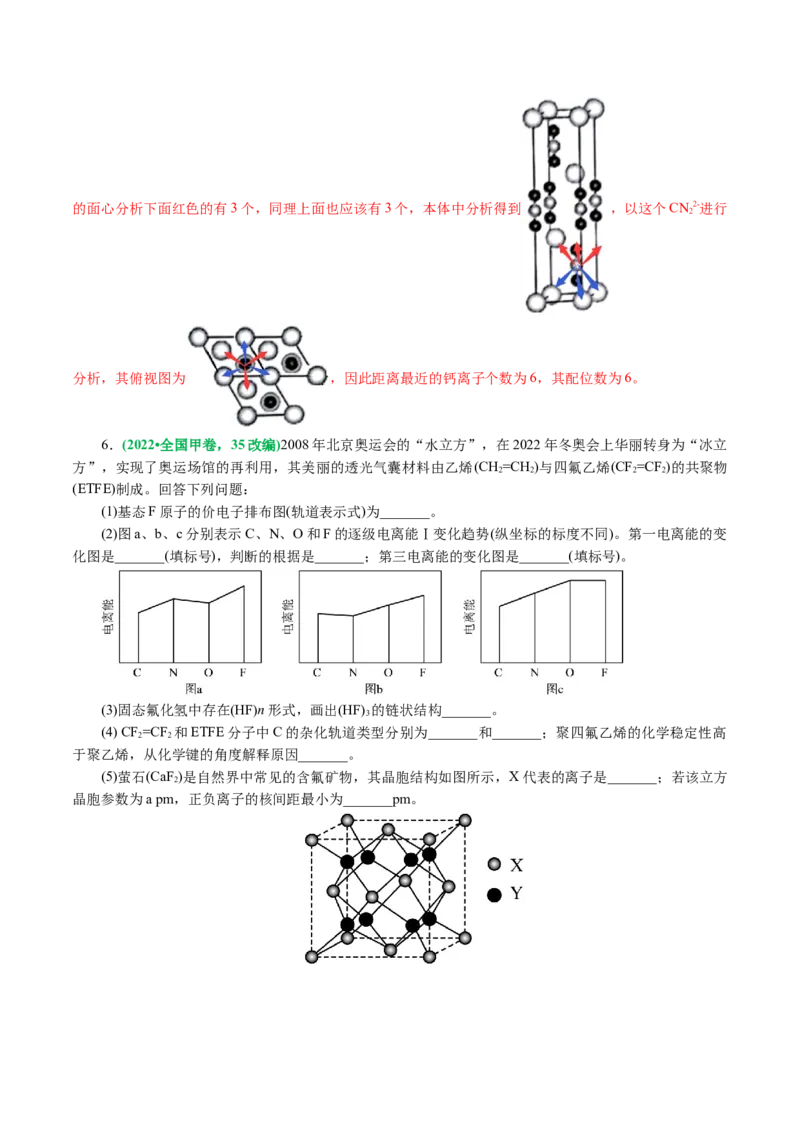
CN2-个数为 ,则其化学式为CaCN ;根据六方最密堆积图 ,以上面
2 2的面心分析下面红色的有3个,同理上面也应该有3个,本体中分析得到 ,以这个CN2-进行
2
分析,其俯视图为 ,因此距离最近的钙离子个数为6,其配位数为6。
6.(2022•全国甲卷,35改编)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立
方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四氟乙烯(CF=CF )的共聚物
2 2 2 2
(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变
化图是_______(填标号),判断的根据是_______;第三电离能的变化图是_______(填标号)。
(3)固态氟化氢中存在(HF)n形式,画出(HF) 的链状结构_______。
3
(4) CF =CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯的化学稳定性高
2 2
于聚乙烯,从化学键的角度解释原因_______。
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______;若该立方
2
晶胞参数为a pm,正负离子的核间距最小为_______pm。【答案】(1)
(2) 图a 同一周期第一电离能的总体趋势是依次升高的,但由于 N元素的2p能级为半充满状态,因
此N元素的第一电离能较C、O两种元素高 图b
(3)
(4) sp2 sp3 C-F键的键能大于聚乙烯中C-H的键能,键能越大,化学性质越稳定
(5) Ca2+ a pm
【解析】根据基态原子的电子表示式书写价电子排布式;根据电离能的排布规律分析电离能趋势和原
因;根据氢键的表示方法书写(HF) 的结构;根据键能影响物质稳定性的规律分析两种物质的稳定性差异;
3
根据均摊法计算晶胞中各粒子的个数,判断粒子种类。(1)F为第9号元素其电子排布为1s22s22p5,则其价
电子排布图为 。(2)C、N、O、F四种元素在同一周期,同一周期第一电离能的
总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因此N元素的第一电离能较C、O两种元
素高,因此C、N、O、F四种元素的第一电离能从小到大的顺序为C一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,形成的C-Cl键的键
长越短
(3) CsCl CsCl为离子晶体,ICl为分子晶体
(4)电解质
【解析】(1)F的原子序数为9,其基态原子电子排布式为1s22s22p5。a项,1s22s22p43s1,基态氟原子2p
能级上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;b项,1s22s22p43d2,核外共10个电子
不是氟原子,b错误;c项,1s22s12p5,核外共8个电子,不是氟原子,c错误;d项,1s22s22p33p2,基态氟
原子2p能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,d正确;故选ad;而同一原子3p能级
的能量比 3s 能级的能量高,因此能量最高的是 1s22s22p33p2,故选 d。(2)①一氯乙烯的结构式为
,碳为双键碳,采取sp2杂化,因此C的一个sp2杂化轨道与Cl的3p 轨道形成C-Clσ键。
x
②C的杂化轨道中s成分越多,形成的C-Cl键越强,C-Cl键的键长越短,一氯乙烷中碳采取sp3杂化,一
氯乙烯中碳采取sp2杂化,一氯乙炔中碳采取sp杂化,sp杂化时p成分少,sp3杂化时p成分多,因此三种
物质中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>一氯乙炔,同时Cl参与形成的大π键越多,形成的C-Cl
键的键长越短,一氯乙烯中Cl的3p 轨道与C的2p 轨道形成3中心4电子的大π键( ),一氯乙炔中Cl
x x
的3p 轨道与C的2p 轨道形成2套3中心4电子的大π键( ),因此三种物质中C-Cl键键长顺序为:一
x x
氯乙烷>一氯乙烯>一氯乙炔。(3)CsICl 发生非氧化还原反应,各元素化合价不变,生成无色晶体和红棕色
2液体,则无色晶体为CsCl,红棕色液体为ICl,而CsCl为离子晶体,熔化时,克服的是离子键,ICl为分
子晶体,熔化时,克服的是分子间作用力,因此CsCl的熔点比ICl高。(4)由题意可知,在电场作用下,
Ag+不需要克服太大阻力即可发生迁移,因此α-AgI晶体是优良的离子导体,在电池中可作为电解质;每个
晶胞中含碘离子的个数为8× +1=2个,依据化学式AgI可知,银离子个数也为2个,晶胞的物质的量n=
mol= mol,晶胞体积V=a3pm3=(504×10-12)3m3,则α-AgI晶体的摩尔体积V = = =
m
m3/mol。
8.(2022•海南省选择性考试,19改编)以Cu O、ZnO等半导体材料制作的传感器和芯片具有能耗低、
2
效率高的优势。回答问题:
(1)基态O原子的电子排布式_______,其中未成对电子有_______个。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______。
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原
子共平面,所有N原子的杂化轨道类型相同,均采取_______杂化。邻苯二甲酸酐( )和邻苯二甲酰
亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是_______。
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为 4的配离子,Zn与氨水反应的离子方程式为
_______。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小
于Zn-O键,原因是_______。
(6)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。 为
所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶
胞的底面_______、_______。【答案】(1) 1s22s22p4或[He]2s22p4 2
(2)自由电子在外加电场中作定向移动
(3) sp2 两者均为分子晶体,后者能形成分子间氢键,使分子间作用力增大,熔点更高
(4)Zn+4NH+2H O=[Zn(NH )]2++2OH-+H ↑
3 2 3 4 2
(5)电负性O>N,O对电子的吸引能力更强,Zn和O更易形成离子键
(6) ▱cdhi ▱bcek
【解析】(1)O为8号元素,其基态O原子核外有8个电子,因此基态O原子的电子排布式为1s22s22p4
或[He]2s22p4,其2p轨道有2个未成对电子,即O原子有2个未成对电子;(2)由于金属的自由电子可在外
加电场中作定向移动,因此Cu、Zn等金属具有良好的导电性;(3)根据结构式可知,N原子均形成双键,
故N原子的杂化方式均为sp2,由于邻苯二甲酸酐和邻苯二甲酰亚胺均为分子晶体,而后者能形成分子间
氢键,使分子间作用力增大,因此熔点更高;(4)金属Zn与氨水反应可生成[Zn(NH )](OH) 和H ,反应的
3 4 2 2
离子方程式为Zn+4NH +2H O=[Zn(NH )]2++2OH-+H ↑;(5)由于电负性O>N,O对电子的吸引能力更强,
3 2 3 4 2
Zn和O更易形成离子键,因此Zn—N键中离子键成分的百分数小于Zn—O键;(6)根据晶胞示意图,一个
晶胞中8个O原子位于晶胞的顶点,1个O原子位于晶胞体内,4个Zn原子位于晶胞的棱上,1个Zn原子
位于晶胞体内,棱上的3个Zn原子和体内的Zn原子、O原子形成四面体结构,则于其相邻的晶胞与该晶
胞共用bc和cd,则相邻的两个晶胞的底面为▱cdhi和▱bcek。
9 . (2022• 山 东 卷 , 16 改 编 ) 研 究 笼 形 包 合 物 结 构 和 性 质 具 有 重 要 意 义 。 化 学 式 为
Ni(CN)x·Zn(NH )y·zC H 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶
3 6 6
胞。晶胞参数为 。回答下列问题:
(1)基态Ni原子的价电子排布式为_______,在元素周期表中位置为_______。
(2)晶胞中N原子均参与形成配位键,Ni2+与Zn2+的配位数之比为_______;x:y:z=_______;晶胞中
有d轨道参与杂化的金属离子是_______。(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的π 6大π键、则吡啶
6
中N原子的价层孤电子对占据_______(填标号)。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
(4)在水中的溶解度,吡啶远大于苯,主要原因是①_______,②_______。
(5) 、 、 的碱性随N原子电子云密度的增大而增强,其中
碱性最弱的是_______。
【答案】(1) 3d84s2 第4周期第VIII族 (2) 2:3 2:1:1 Zn2+ (3)D
(4) 吡啶能与HO分子形成分子间氢键 吡啶和HO均为极性分子相似相溶,而苯为非极性分
2 2
子
(5)
【解析】(1)已知Ni是28号元素,故基态Ni原子的价电子排布式为:3d84s2,在周期表中第四横行第
10纵列即位于第4周期第VIII族;(2)由题干晶胞示意图可知,一个晶胞中含有Ni2+个数为: =1,
Zn2+个数为: =1,含有CN-为: =4,NH 个数为: =2,苯环个数为: =2,则该晶胞的
3
化学式为:Ni(CN) ·Zn(NH )·2C H ,且晶胞中每个N原子均参与形成配位键,Ni2+周围形成的配位键数目
4 3 2 6 6
为:4,Zn2+周围形成的配位键数目为:6,则Ni2+与Zn2+的配位数之比,4:6=2:3;x:y:z=4:2:2=2:
1:1;由以上分析可知,Ni2+的配位数为4,则Ni2+采用sp3杂化,而Zn2+的配位数为6,Zn2+采用sp3d2杂化,
即晶胞中有d轨道参与杂化的金属离子是Zn2+;(3)吡啶( )替代苯也可形成类似的笼形包合物。已知
吡啶中含有与苯类似的π 6大π键,则说明吡啶中N原子也是采用sp2杂化,杂化轨道只用于形成σ键和存
6
在孤电子对,则吡啶中N原子的价层孤电子对占据sp2杂化轨道,故选D;(4)已知苯分子为非极性分子,
HO分子为极性分子,且吡啶中N原子上含有孤电子对能与HO分子形成分子间氢键,从而导致在水中的
2 2
溶解度,吡啶远大于苯;(5)已知-CH 为推电子基团,-Cl是吸电子基团,则导致N原子电子云密度大小顺
3
序为: > > ,结合题干信息可知,其中碱性最弱的为: 。
10.(2022•北京卷,15改编)FeSO ·7H O失水后可转为FeSO ·H O,与FeS 可联合制备铁粉精(Fe O)
4 2 4 2 2 x y
和HSO 。
2 4
I. FeSO ·H O结构如图所示。
4 2(1) Fe2+价层电子排布式为___________。
(2)比较SO 2-和HO分子中的键角大小并给出相应解释:___________。
4 2
(3)H O与Fe2+、SO 2-和HO的作用分别为___________。
2 4 2
II.FeS 晶胞为立方体,边长为 ,如图所示。
2
(4)①与Fe2+紧邻的阴离子个数为___________。
②晶胞的密度为 ___________ 。
(5)以FeS 为燃料,配合FeSO ·H O可以制备铁粉精(Fe O)和HSO 。结合图示解释可充分实现能源和
2 4 2 x y 2 4
资源有效利用的原因为___________。
【答案】(1)3d6
(2) SO2-的键角大于HO,SO 2-中S原子的价层电子对数为4、孤对电子对数为0,离子的空间构型为
4 2 4
正四面体形,HO分子中O原子的价层电子对数为4、孤对电子对数为2,分子的空间构型为V形
2
(3)配位键、氢键 (4) 6 ×1021
(5)由图可知,FeS 与O 生成Fe O 的反应为放热反应,FeSO ·H O分解生成Fe O 的反应为吸热反应,
2 2 x y 4 2 x y
放热反应放出的热量有利于吸热反应的进行,有利于反应生成的SO 与HO反应生成HSO
3 2 2 4
【解析】(1)铁元素的原子序数为26,基态亚铁离子的价电子排布式为3d6;
(2)硫酸根离子中硫原子的价层电子对数为4、孤对电子对数为0,离子的空间型为正四面体形,水分
子中氧原子的价层电子对数为4、孤对电子对数为2,分子的空间构型为V形,所以硫酸根离子的键角大
于水分子;(3)由图可知,具有空轨道的亚铁离子与水分子中具有孤对电子的氧原子形成配位键,硫酸根离子与水分子间形成氢键;(4)①由晶胞结构可知,晶胞中位于顶点的亚铁离子与位于棱上的阴离子S 离子
间的距离最近,则亚铁离子紧邻的阴离子个数为6;②由晶胞结构可知,晶胞中位于顶点和面心的亚铁离
子个数为8× +6× =4,位于棱上和体心的S 离子个数为12× +1=4,设晶体的密度为dg/cm3,由晶胞的
质量公式可得: ==10—21a3d,解得d= ×1021;(5)由图可知,FeS 与O 生成Fe O 的反应
2 2 x y
为放热反应,FeSO ·H O分解生成Fe O 的反应为吸热反应,放热反应放出的热量有利于吸热反应的进行,
4 2 x y
有利于反应生成的SO 与HO反应生成HSO ,所以以FeS 为燃料,配合FeSO ·H O可以制备铁粉精和
3 2 2 4 2 4 2
HSO 可充分实现能源和资源有效利用。
2 4
11.(2022•湖南选择性考试,18改编)铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料
等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态 原子的核外电子排布式为 [Ar]_______;
②该新药分子中有_______种不同化学环境的C原子;
③比较键角大小:气态SeO 分子_______ SeO 2-离子(填“>”“<”或“=”),原因是_______。
3 3
(2)富马酸亚铁(FeC HO)是一种补铁剂。富马酸分子的结构模型如图所示:
4 2 4
①富马酸分子中 键与 键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化 H ,将N3-转化为
2
NH -,反应过程如图所示:
2
①产物中N原子的杂化轨道类型为_______;
②与NH -互为等电子体的一种分子为_______(填化学式)。
2(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为_______;
②Fe原子的配位数为_______;
③该晶胞参数 、 。阿伏加德罗常数的值为N ,则该晶体的密度为_______ g· cm-3
A
(列出计算式)。
【答案】(1) [Ar] 3d104s24p4 6 > SeO 的空间构型为平面三角形,SeO2-的空间构型为三
3 3
角锥形
(2) 11:3 O>C>H>Fe (3) sp3杂化 HO
2
(4) KFe Se 4
2 2
【解析】(1)①硒元素的原子序数为34,基态原子的电子排布式为[Ar] 3d104s24p4,故答案为:[Ar]
3d104s24p4;②由结构简式可知,乙烷硒啉的分子结构对称,分子中含有6种化学环境不同的碳原子;③三
氧化硒分子中硒原子的价层电子对数为 3,孤对电子对数为0,分子的空间构型为平面三角形,键角为
120°,亚硒酸根离子中硒原子的价层电子对数为4,孤对电子对数为1,离子的空间构型为三角锥形,键角
小于120°;(2)①由球棍模型可知,富马酸的结构式为HOOCCH=CHCOOH,分子中的单键为σ键,双键中
含有1个σ键和1个π键,则分子中σ键和π键的数目比为11:3;②金属元素的电负性小于非金属元素,
则铁元素的电负性最小,非金属元素的非金属性越强,电负性越大,氢碳氧的非金属性依次增强,则电负
性依次增大,所以富马酸亚铁中四种元素的电负性由大到小的顺序为 O>C>H>Fe;(3)①由结构简式可
知,产物中氮原子的价层电子对数为4,原子的杂化方式为sp3杂化;②水分子和氨基阴离子的原子个数都
为3、价电子数都为8,互为等电子体;(4)①由平面投影图可知,晶胞中位于顶点和体心的钾原子个数为
8× +1=2,均位于棱上和面上的铁原子和硒原子的个数为 12× +2× =4,则超导材料最简化学式为
KFe Se ;②由平面投影图可知,位于棱上的铁原子与位于面上的硒原子的距离最近,所以铁原子的配位数
2 2
为4;③设晶体的密度为dg/cm3,由晶胞的质量公式可得: =abc×10—21×d,解得d=
。
12.(2022•广东选择性考试,20改编)硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来, 在发光材料、生物医学等领域引起
广泛关注。一种含 的新型 分子 的合成路线如下:
(1) Se与S同族,基态硒原子价电子排布式为_______。
(2)H Se的沸点低于HO,其原因是_______。
2 2
(3)关于I~III三种反应物,下列说法正确的有_______。
A.I中仅有 键
B.I中的Se-Se键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有sp与sp2
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______。
(5)硒的两种含氧酸的酸性强弱为HSeO_______ H SeO(填“>”或“<”)。研究发现,给小鼠喂食适量
2 4 2 3
硒酸钠(Na SeO)可减轻重金属铊引起的中毒。SeO2-的立体构型为_______。
2 4 4
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于
加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图 1,
沿x、y、z轴方向的投影均为图2。
①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为_______ (列
出计算式,N 为阿伏加德罗常数的值)。
A
【答案】(1)4s24p4
(2)两者都是分子晶体,由于水存在分子间氢键,沸点高
(3)BDE
(4)O、Se
(5)> 正四面体形
(6) K SeBr
2 6
【解析】(1)基态硫原子价电子排布式为3s23p4,Se与S同族,Se为第四周期元素,因此基态硒原子价电子排布式为4s24p4;(2) H Se的沸点低于HO,其原因是两者都是分子晶体,由于水存在分子间氢键,沸
2 2
点高;(3)A项,I中有 键,还有大π键,故A错误;B项,Se−Se是同种元素,因此I中的Se−Se键为非
极性共价键,故B正确;C项,烃都是难溶于水,因此II难溶于水,故B错误;D项,II中苯环上的碳原
子和碳碳双键上的碳原子杂化类型为sp2,碳碳三键上的碳原子杂化类型为sp,故D正确;E.根据同周期
从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,因此I~III含有的元素中,O电负性最大,故
E正确;故选BDE。(4)根据题中信息IV中O、Se都有孤对电子,碳、氢、硫都没有孤对电子;(5)根据非
羟基氧越多,酸性越强,因此硒的两种含氧酸的酸性强弱为 HSeO >HSeO 。SeO2-中Se价层电子对数为
2 4 2 3 4
,其立体构型为正四面体形;(6)①根据晶胞结构得到K有8个, 有
,则X的化学式为KSeBr ;②设X的最简式的式量为 ,晶体密度为 ,设晶胞参
2 6
数为anm,得到 ,解得 ,X中相邻K之间的最短距离为晶
胞参数的一半即 。
1.(2024·浙江省金华市十校选考模拟考试)钛被称为继铁、铝之后的第三金属。其单质及化合物用途广
泛。请回答:
(1)基态Ti原子的电子排布式为 ,其价电子中不同自旋状态的电子数之比为 。
(2)钛酸钡/氧化锌纳米纤维可以催化降解水中的亚甲基蓝等有机污染物。
①亚甲基蓝在水中的溶解度 其在乙醇中的溶解度(填“大于”或“小于”)。
②下列有关说法正确的是 。
A.光照使钛酸钡/氧化锌纳米纤维的电子被激发,形成原子发射光谱
B.亚甲基蓝中C原子的杂化方式:sp3、sp2C.亚甲基蓝阳离子组成元素的电负性大小为:S>N>C>H
D.SO 2-和SO 2-的价层电子空间构型均为四面体
4 3
(3)钛酸钡晶体的晶胞结构如图所示。
①与Ba原子最近且等距离的O原子有 个。
②如果将晶胞转换为Ti原子为顶点的形式(见下图),请在图中用“○”画出O原子的位置 。
【答案】(1) [Ar]3d24s2 3∶1或1∶3
(2) 大于 BD
(3) 12
【解析】(1)钛元素的原子序数为22,基态原子的电子排布式为[Ar]3d24s2,其价电子3d24s2,根据基态
原子电子排布规则,不同自旋状态的电子数之比为3∶1;(2)①由亚甲基蓝的结构图可知,亚甲蓝为盐,具
有一定的极性,根据相似相溶原理,亚甲基蓝在水里溶解度大于在乙醇中的溶解度;②A项,光照使催化
剂的电子被激发,该过程吸收能量,形成的原子光谱为吸收光谱,故A错误;B项,亚甲基蓝中环上的所
有碳原子都形成3个键和1个键,价层电子对数为3,为sp2杂化,甲基上C原子的杂化方式:sp3,故B正
确;C项,根据同周期主族元素的电负性由左向右逐渐增大,同主族元素的电负性由上向下逐渐减小,电
负性大小顺序为N>S>C>H,故C错误;D项,SO 2-中价层电子对数为4+ =4,SO 2-中价层电
4 3
子对数为3+ =4,价层电子空间构型均为四面体,故D正确;故选BD;(3)①以顶点Ba原子为
研究对象,由BaTiO3的晶胞可知,距离钡原子最近的氧原子的个数为 =12;②根据均摊法,1个晶胞
中Ba:8× =1,Ti:1,O:6× =3,若将晶胞转换为Ti原子为顶点,则O2-位于晶胞的棱心,对应结构如
图所示: 。2.(2024·浙江省宁波市高三选考模拟考试)第ⅢA和第ⅤA元素可形成多种化合物。请回答:
(1)基态B原子核外电子占据的最高能级符号是 ,基态As原子的价层电子排布式是
。
(2)①固体储氢材料氨硼烷BH·NH ,其结构和乙烷相似,下列有关说法正确的是 。
3 3
A.氨硼烷中B原子的杂化方式为sp2
B.相同条件下在水中的溶解度:氨硼烷>乙烷
C.元素B、N的第一电离能均高于相邻元素
D. 是硼原子能量最低的激发态
②BF 形成的化合物中配位键的强度:BF·N(CH )Cl BF·N(CH )Cl (填“>”、“<”或“=”),
3 3 3 2 3 3 2
理由是 。
(3)一种含Ga化合物晶胞如图甲,三个晶胞围成一个六棱柱,如图乙,该化合物的化学式为
,每个N原子周围距离最近的N原子数目为 。
【答案】(1) 2p 4s24p3
(2) B > Cl电负性大,N(CH )Cl中Cl原子多,使N电子云密度降低,N的孤电子对不易给
3 2
出与BF 形成配位键,即形成的配位键稳定性低
3
(3) GaN 12
【解析】(1)基态B原子核外电子排布:1s22s22p1,占据的最高能级符号2p;As原子序数33,基态As
原子与的价层电子排布式4s24p3;(2)①A项,氨硼烷BH·NH ,其结构和乙烷相似,则氨硼烷中B原子的
3 3
杂化方式为sp3,A错误;B项,氨硼烷分子与水分子间可形成氢键,所以相同条件下在水中的溶解度:氨
硼烷>乙烷,B正确;C项,N原子核外电子排布处于半充满稳定结构,第一电离能高于相邻元素;B核外
电子排布:1s22s22p1,第一电离能不高于相邻元素,C错误;D项, 2s能级未排
满电子,不是硼原子能量最低的激发态,D错误;故选B;②Cl电负性大,N(CH )Cl 中Cl原子多,使N
3 2
电子云密度降低,N的孤电子对不易给出与BF 形成配位键,即形成的配位键稳定性低;(3)均摊法计算可
3
知Ga原子与N原子个数比为1:1,则其化学式:GaN;距离每个N原子距离最近的N原子数目为12。
3.(2024·浙江省温州市普通高中高三一模)2023年8月1日起,我国对镓(Ga)等相关物项实施出口管制。
Ga与B、Al处于同一主族。请回答:
(1)基态Ga原子的价电子排布图: ;
(2)①硼的氢化物叫硼烷(B H )。如B H (乙硼烷-6)、B H (丁硼烷-10)等。下列说法不正确的是
n m 2 6 4 10
;
A.B原子由 需吸收能量B.B H 的结构式:
2 6
C.同周期相邻元素的电负性大小:Be<B<C
D.B H 与C≡O反应生成HBCO,HBCO分子中 键与 键数目之比为:5:2
2 6 3 3
②氮和硼形成的化合的BN,与C 互为等电子体,通常存在石墨型与金刚石型两种结构,可发生如下
2
转化: 。两类化合物中B原子的杂化方式分别为: ;
金刚石型的BN的硬度大于金刚石,原因是 ;
③B H 极易发生水解生成HBO 和H,请写出反应的化学方程式: ;
n m 3 3 2
(3)Ga与N形成的化合物是一种重要的半导体材料,晶体的部分结构如图。
①Ga的配位数为: ;
②下列所示为图1所对应晶胞的是: 。
A. B. C. D.
【答案】(1)
(2) AB sp2、sp3 金刚石型BN为共价晶体,B-N的键能大于金刚石中C-C键能,所有硬度更大
或
(3) 4 A
【解析】(1)基态 Ga 原子的价电子排布图: ;(2)① A 项,B 原子由
, 与 能量相同,不需吸收能量,故 A 错误;B 项,B H 的结构式:
2 6
,故B错误;C项,同周期元素电负性从左到右逐渐增强,所以同周期相邻元素的电负性大小:Be<B<C,故C正确;D项,B H 与C≡O反应生成HBCO,HBCO分子中含4个共价单
2 6 3 3
键和1个三键,则键与π键数目之比为:5:2,故D正确;故选AB;②氮和硼形成的化合的BN,与C 互
2
为 等 电 子 体 , 通 常 存 在 石 墨 型 与 金 刚 石 型 两 种 结 构 , 可 发 生 如 下 转 化 :
。 类比混合型晶体石墨,石墨中每个中心原子
直接与其它3个原子相连,属于sp2杂化; 类比共价晶体金刚石,每个C原子直接与其余
4个C相连,属于sp3杂化;金刚石型的BN的硬度大于金刚石,原因:金刚石型BN为共价晶体,B-N的
键能大于金刚石中C-C键能,所有硬度更大;③B H 极易发生水解生成HBO 和H ,反应的化学方程式:
n m 3 3 2
或 ;(3)①根据晶体结构图可知,
直接与Ga相连的N有4个,则Ga的配位数为4;②晶胞是晶体结构的基本单元,根据晶胞与晶体间关系
可知,为图1所对应晶胞的是 ,故选A。
4.(2024·山东临沂市高三教学质量检测)X、Q、Y、Z、W、M、R、T是原子半径依次增大的前四周
期元素,基态R原子核外电子有9种空间运动状态,并有2个单电子;基态 的d轨道半充满。由上述元
素中的六种组成的一种化合物常作为“相转移催化剂”被广泛应用于有机合成中,其结构简式如图Ⅰ所示。
回答下列问题:
(1)基态R原子的价电子排布式为 的,第一电离能小于R的同周期元素有 种。
(2)XZY 的结构如图Ⅱ所示,分子中存在大π键(π4),比较键长:① ②(填“>”“<”或“=”),理
3 3
由是 。
(3)ZXMX 分子中M原子的杂化方式为 ,熔点比WX (填“高”或“低”);TY 中T
3 3 2 6 5
的化合价为 ,且含有4个 价的Y,则该分子中 键与 键的个数比为 。
(4)53号元素A的电负性与W近似相等,WQA水解反应的产物为 。
3
【答案】(1)3s23p4 4
(2)> 硝酸中端基2个氧原子参与形成大π键,原子轨道重叠程度大,使N-O键键长变短
(3)sp3 高 7:1
(4)CHF 、HIO
3
【解析】X、Q、Y、Z、W、M、R、T是原子半径依次增大的前四周期元素,基态R原子核外电子有9种空间运动状态,有9个原子轨道,并有2个单电子,则核外有16个电子,R是S元素;基态T+的d轨
道半充满,T是Cr元素。X、Q、Y、Z、W、M原子半径依次增大,X能形成1个共价键,X是H元素;Y
形成2个共价键,Y是O元素; W形成4个共价键,W是C元素;Z形成4个共价键带1个正电荷、M形
成4个共价键带1个负电荷,Z是N元素、M是B元素,则Q是F元素。(1)R是S元素,基态R原子的价
电子排布式为3s23p4,第一电离能小于S的同周期元素有Na、Mg、Al、Si,共4种。(2)硝酸中端基2个氧
原子参与形成大π键,原子轨道重叠程度大,使N-O键键长变短,所以键长①>②。(3)NH BH 分子中B原
3 3
子形成4个σ键,B原子杂化方式为sp3;NH BH 分子间能形成氢键,熔点比C H 高;CrO 中Cr的化合价
3 3 2 6 5
为+6,且含有4个-1价的O,则CrO 的结构式为 ,该分子中σ键与π键的个数比为7:1。
5
(4)53号元素I的电负性与C近似相等,由于F原子电负性大,所以CFI中I显正价,所以水解反应的产物
3
为CHF 、HIO。
3
5.(2024·宁夏石嘴山平罗中学高三期中)a、b、c、d、e、f、g七种元素,是原子序数依次增大的前四
周期的元素。有关信息如下,请回答以下问题:
a a能形成一种硬度最大的固体单质
b 在同周期元素中,b的基态原子未成对电子数最多
c c元素基态原子的电子排布式为1s22s22p4
d d基态原子的 ; ; ;
e e基态原子核外3p轨道半满
f f在周期表中第11纵行
g g基态原子最外层电子数为2
(1)f的元素名称为 ,位于元素周期表的 区。
(2)e的基态原子中能量最高的电子所占的轨道形状是 ,其电子云在空间有 个
伸展方向。
(3)d基态原子的价层电子的轨道表示式为 ,某X元素在元素周期表中位置处于d元素的左
上角对角线处,它们具有部分相似的性质,请写出该X元素组成的单质与氢氧化钠溶液反应的化学方程式
。
(4)a的最高价氧化物的电子式 。
(5)元素f基态原子的第二电离能 元素g基态原子的第二电离能(填“>”、“<”或“=”),原
因是 。
【答案】(1) 铜 ds (2) 纺锤体或哑铃形 3
(3) Be+2NaOH=Na BeO+H ↑
2 2 2
(4)
(5) > Cu+核外价电子排布为3d10全充满结构,比Zn+的3d104s1稳定,Cu+更难失去电子,故Cu的
第二电离能大于Zn的第二电离能【解析】由题干信息可知,a、b、c、d、e、f、g七种元素,是原子序数依次增大的前四周期的元素,
a能形成一种硬度最大的固体单质,故a为C,在同周期元素中,b的基态原子未成对电子数最多,故b为
N,c元素基态原子的电子排布式为1s22s22p4,则c为O,d基态原子的 ; ;
; ,该元素第3电离能比第4电离能小得多,故d为Al,e基态原子核外3p
轨道半满,即[Ne]3s23p3,则e为P,f在周期表中第11纵行,则f为Cu,g基态原子最外层电子数为2,故
g为Zn。(1),f为Cu,则f的元素名称为铜,铜位于元素周期表的ds区;(2)由分析可知,e为P,P的核外
电子排布式为:[Ne]3s23p3,故e的基态原子中能量最高的电子所占的轨道为p能级,故其形状是纺锤体或
哑铃形,其电子云在空间有3个相互垂直的伸展方向;(3)由分析可知,d为Al,是13号元素,故d基态原
子的价层电子的轨道表示式为 ,某X元素在元素周期表中位置处于d元素的左上
角对角线处,它们具有部分相似的性质,则X为Be,根据Al与NaOH溶液反应可知该X元素组成的单质
与氢氧化钠溶液反应的化学方程式为:Be+2NaOH=Na BeO+H ↑;(4)a为C,故a的最高价氧化物为CO,
2 2 2 2
其电子式为: ;(5)由分析可知,f为Cu,g为Zn,则Cu+核外价电子排布为3d10全充满结
构,比Zn+的3d104s1稳定,Cu+更难失去电子,故Cu的第二电离能大于Zn的第二电离能。
6.(2024·山东菏泽·高三统考期中)铁系元素(铁、钴、镍)构成了丰富的物质世界,其形成的物质在生
产生活中用途广泛。回答下列问题:
(1)基态Ni2+的单电子数目为 。
(2) [Co(NH )Cl]Cl 中含有的 键数目为 ,NH 分子与Co3+形成配合物后H-N-H键角
3 5 2 3
(填“变大”“变小”或“不变”)。
(3)[Co(N )(NH )]SO 中配体N-的空间结构为 ,N、O原子的第二电离能与第一电离能差
3 3 5 4 3
值相比更大的是 (填元素符号)。
(4)一种铁基超导材料晶胞结构如图a所示,铁原子沿z轴方向的投影如图b所示。该材料的化学式为
,已知体心与顶点的 原子有着相同的化学环境,晶胞中 原子1分数坐标为(0,0,0.628),则 原子
2的分数坐标为 ,体心 原子与 原子1之间的距离为 。
【答案】(1)2 (2) 21N 变大 (3) 直线形 O
A
(4)CaFe As (0.5,0.5,0.872) pm
2 2
【解析】(1)基态Ni2+的价层电子为:3d8,未成对电子数为2;(2) [Co(NH )Cl]Cl 中有6个配位键,配
3 5 2体NH 中有3个σ键,因此中共有6+5×3=21个σ键,1mol [Co(NH )Cl]Cl 中有21N 个σ键;配位后没有
3 3 5 2 A
了孤对电子,因此键角变大;(3)N -与二氧化碳是等电子体,空间构型为直线形,N最高能级电子排布为
3
2p3半充满较为稳定,N的第一电离能大于O,由于氧电离一个后形成半充满结构,故第二电离能O大于
N,所以差值更大的是O;(4)由均摊法:一个晶胞中Ca数目为 、Fe数目为 、As数目为
,则该材料的化学式为CaFe As ;晶胞中As原子(1) 分数坐标为(0,0,0.628),已知体心与顶
2 2
点的Ca原子有着相同的化学环境,体心Ca坐标为(0.5,0.5,0.5)则As原子1与体心Ca在z轴上的坐标差
为0.628-0.5=0.128,则As原子2的z轴上距离顶面的坐标差为0.128,故As原子2的z轴上坐标为1-0.128
=0.872,故As原子2的分数坐标为(0.5,0.5,0.872),与底面平行的体心Ca所在平面和As原子1的距离
为0.128cpm,体心Ca原子与As原子1所在的z轴距离为 ,则体心Ca原子与As原子1之间的距
离为 pm。
7.(2024·河北沧州市部分高中高三联考)非金属氮的化合物在生产、生活和科研中应用广泛。回答下
列问题:
(1)基态N原子核外电子的空间运动状态有 种;第二周期元素中,第一电离能介于B和N之间的
元素有 种。
(2)气态NO 的分子结构为 ,而固态NO 则由一种直线形的阳离子X与一种
2 5 2 5
平面正三角形的阴离子Y构成,X的化学式为 ,Y的离域π键可表示为 。
(3) 和 可形成如图所示的配合物离子,其中铁的一个配体为茂环阴离子(C H-),该配体以π电
5 5
子参与配位,其中与 的单电子数相同的同周期元素有 种,配合物离子中与铁形成配位键的电子
共有 个,S元素的杂化方式为 。
(4)甲乙酮肟( )是一种重要有机合成活性试剂。其中, 键与 键夹
角 (填“<”“>”或“=”) 键与 键夹角。
(5)氮化锂晶体中存在锂、氮原子共同组成的锂、氮层,锂原子以石墨晶体中的碳原子方式排布,N原子处在六元环的中心,同层中锂、氮的原子个数比为 ;设氮化锂晶体中,同层N-N间距为apm,层
与层间距为bpm,该物质的密度为 g ·c m-3(用含a、b的式子表示)。
【答案】(1) 5 3 (2)NO +
2
(3) 3 12 sp3 (4)>
(5) 2:1
【解析】(1)N是7号元素,核外7个电子占据了5个原子轨道,有5种空间运动状态;第二周期元素
中,第一电离能介于B和N之间的元素有:Be、C、O共3种。(2)固态NO 则由一种直线形的阳离子X与
2 5
一种平面正三角形的阴离子Y构成,X的化学式为NO +,Y的化学式为NO -,NO -的中心原子氮原子的价
2 3 3
层电子对数为 ,杂化方式为sp2,参与形成离域π键的电子包括每个氧原子上的一个电
子和氮原子上的两个电子,还有得到的一个电子共 6个电子,则Y的离域π键可表达 ;(3)Ni是28号元
素,Ni2+是Ni原子失去最外层2个电子形成的,核外电子排布式是1s22s22p63s23p63d8,Ni2+有2个未成对电
子,同周期有2个未成对电子的元素还有T i、Ge、Se共3种;铁的一个配体为茂环阴离子(C H-),该配体
5 5
以π电子参与配位,C H-离子中大π键是 ,再加上2个S和1个C各提供2个电子,配合物离子中与铁
5 5
形成配位键的电子共有12个;S原子形成3个共价键,S原子上还有一对孤电子对,故S原子杂化类型为
sp3杂化;(4) 中C=N的C、N均采用sp2杂化,但N原子有1对孤电子对,C原子
没有孤电子对,由于孤电子对与成键电子对的斥力大于成键电子对之间的斥力,所以C=N键与C-C角大于
C=N键与N-O键夹角;(5)根据石墨晶体结构可知1个Li原子被3个六元环共用,所以1个六元环中含有
个Li原子,而N原子处于六元环中心,所以其个数为 1,则同层中锂、氮的原子个数比为2 :
1;根据均摊法,晶胞中N原子(黑球)的个数为 ,Li原子的个数为 ,所以晶胞的质量
为 ;底面为菱形,边长为 apm,底面积为 ,高为 bpm,则晶胞的体积为
,所以密度 。
8.(2024·辽宁·高三校联考期中)配合物在工农业生产中有广泛应用。
(1)铁的一种配合物的化学式为 ,配体Htrz为三氮唑( )。
①基态Fe2+与Fe3+中未成对的电子数之比为 。②元素H、O、C、N电负性从小到大的顺序为 。
③阴离子ClO -的键角 ClO -的键角(填“等于”“大于”或“小于”)。
4 3
④配体三氮唑( )中配位原子是 ,碳原子的杂化方式为 。
⑤三氮唑沸点为260℃,与其结构类似的环戊二烯沸点为42.5℃,三氮唑沸点明显偏高的原因是
。
(2)钴蓝晶胞结构如下图所示,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其化学式为
;N 为阿伏加德罗常数的值,钻蓝晶体的密度为 g ·c m-3(列计算式)。
A
【答案】(1) ①4∶5 ②HS。O和S为同主族元素,电子层数S>O,原子半径S>O,原子核对最外层电子的吸
引作用O>S a c(H+)较大,F-与H+结合形成HF,c(F-)降低,不易与Fe3+形成[FeF ]3-
6
(3)abe [FeF ]3-
6
【解析】(1)Fe为26号元素,基态Fe原子的价层电子轨道表示式为 ;
(2)①第一电离能O>S。O和S为同主族元素,电子层数S>O,原子半径S>O,原子核对最外层电子的吸引
作用O>S; ②a项,(NH )SO 能将Fe2+氧化为Fe3+,结合组成和化合价可知(NH )SO 中有2个氧原子
4 2 2 8 4 2 2 8
为-2,可能含有“-O-O-”结构,因此具有强氧化性,故正确;b项,依据结构分析,(NH )SO 中硫元素的
4 2 2 8
化合价为+6价,故错误;c项,SO2-中“S-O-O”呈V形结构,不可能在同一条直线上,故错误;
2 8
(3)①[FeF ]3-与NH +之间存在离子键,NH +中存在N-H键为极性共价键;[FeF ]3-中存在配位键;②黑球位
6 4 4 6
于顶点和面心,个数为: ;白球位于棱心和体心,个数为: ;结合化学式可知:[FeF ]3-为黑球,NH 为白球;则晶胞的质量为 g;晶胞边长为anm,晶体体积为: cm3;该晶
6
体的密度为 g·cm-3。
10.(2023·湖州、衢州、丽水三地市高三4月教学质量检测)氯化钠是一种典型且极具魅力的晶体,我
们通过学习氯化钠可以更好地了解其他类似物质的结构。已知氯化钠的晶胞如下图1所示。
图1
(1)下列关于氯化钠的说法正确的是_______。
A.基态 的电子有5种空间运动状态
B.钠是第一电离能最大的碱金属元素
C.氯原子的价电子排布式可写成 [Ne]3s23p5
D.每个氯离子周围与它最近且等距的氯离子有12个
(2)已知NaCl的密度为ρg· cm-3,NaCl的摩尔质量为 ,阿伏加德罗常数的值为N ,则在NaCl
A
晶体里 和 的最短距离为_______ 。
(3)温度升高时, 晶体出现缺陷,如图2所示,当图中方格内填入 时,恰好构成氯化钠晶胞
的1/8。 晶体出现缺陷时,其导电性大大增强,原因是_______。
(4) NiO、FeO的晶体类型与氯化钠相同, 和 的离子半径分别为 和 ,则熔点:
NiO_______FeO (填“>”“<”或“=”)
(5)钡在氧气中燃烧时得到一种钡的氧化物BaO 晶体,其阴阳离子的排布与氯化钠相同,其中存在的
2
化学键的类型为_______。
【答案】(1)AD (2)
(3)该晶体在通电时,钠离子可在电场的作用下迁移到缺陷处,形成电流
(4)> (5)离子键、非极性共价键【解析】(1)A项,基态Na+的核外电子排布为:1s22s22p6,核外电子有5种空间运动状态,A正确;B
项,同主族元素从上到下第一电离能递减,则锂是第一电离能最大的碱金属元素,B错误;C项,氯原子
的价电子排布式可写成3s23p5,C错误;D项,以体心氯离子为观察对象,可知其周围与它最近且等距的
氯离子位于棱心,有12个,D正确;故选AD;(2)由晶胞结构可知钠离子位于顶点和面心,个数为
,氯离子位于体心和棱心,个数为: ,则晶胞的质量为: g,NaCl的密度为
ρg· cm-3,则晶胞的体积为: cm3,晶胞的边长为: ,则在NaCl晶体里Na+和Cl-的最短距离
为边长的一半,即 pm;(3)该惊晶体在通电条件下,钠离子在电场的作用下可以
发生迁移,迁移到缺陷处,从而形成电流;(4)NiO、FeO的晶体类型与氯化钠相同,均为离子晶体,Ni2+半
径小于Fe2+半径,离子半径越小、离子键越强,晶格能越大,晶体的熔沸点越高,故熔点:NiO大于
FeO;(5)BaO 中钡离子与过氧根离子之间存在离子键,过氧根内为非极性共价键,故答案为:离子键、非
2
极性共价键。
11.(2023·广西三模)锌是动物必需的微量元素之一,参与机体的各种代谢活动。
(1)Zn位于元素周期表的___________区,基态Zn原子的价电子排布图为___________。
(2)第二电离能:Cu___________Zn(填“>”、“<”或“=”),判断依据是___________。
(3)含有多个配位原子的配体与同一个中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物,
一种Zn2+配合物的结构如图1所示(-OTs为含氧、硫的有机基团):
①1mol该配合物中通过螯合作用形成的配位键有___________mol,该螯合物中N原子的杂化类型为
___________。
②该配合物所涉及非金属元素电负性最小的是___________(填元素符号)。
(4)硫化锌精矿是冶炼金属锌的主要原料,六方硫化锌(纤锌矿型)的平行六面体晶胞如图2所示,晶体
中正负离子的配位数之比为___________。
(5)已知每个Zn2+与其周围最近的S2-之间的距离都相等,以晶胞参数为单位长度建立坐标系,若A点
坐标为(0,0,0),B点坐标为( , , ),C点坐标为(0,0,u),则D点坐标为___________。【答案】(1) ds
(2) > 基态Cu+核外价电子为3d10,3d轨道为全满较稳定状态,不容易再失去一个电子;基态
Zn+核外价电子为3d104s1,4s轨道有1个电子,容易失去1个电子
(3) 4 sp2杂化、sp3杂化 H
(4)1:1
(5)( , , )
【解析】(1)Zn 为 30 号元素,位于元素周期表的 ds 区,基态 Zn 原子的价电子排布图为
;(2)基态Cu+核外价电子为3d10,3d轨道为全满较稳定状态,不容易再
失去一个电子;基态Zn+核外价电子为3d104s1,4s轨道有1个电子,容易失去1个电子形成锌离子;故第
二电离能:Cu>Zn;(3)①由螯合物定义和结构示意图可知,1mol该配合物中通过螯合作用形成的配位键有
4mol,该螯合物中环上N所在的环为平面结构,其杂化类型为 sp2杂化,-NH-中氮原子形成3个共价键且
存在1对孤电子对,为sp3杂化;②同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同
主族由上而下,金属性增强,非金属性逐渐减弱,元素电负性减弱;该配合物所涉及非金属元素电负性最
小的是氢元素H;(4)据“均摊法”,晶胞中含 个S、 个Zn,则化学式为ZnS,以B
点硫为例,其最近且相邻的锌为4个,结合化学式可知,晶体中正负离子的配位数之比为 4:4=1:1;(5)
由已知坐标可知,B点硫距离y轴距离为 ,则BC距离为 ,
BC距离等于BD距离,则D点在y轴上投影坐标为 ,结合B点坐标可知,D点在x、y轴上
投影坐标为 、 ,故D点坐标为( , , )。
12.(2023·北京市高三统考)铁( Fe)、镍( Ni)的单质及其化合物在医药、材料等领域有广泛的应用。
26 28
回答下列问题:
(1)基态Fe原子核外电子排布式为_______,Ni位于元素周期表的_______区。
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成
Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是_______。
(3)FeCl 常用作净水剂、刻蚀剂等。
3
① FeCl 的熔点(306℃)显著低于FeF 的熔点(1000℃)的原因是_______。
3 3
② FeCl 水溶液中Fe3+可水解生成双核阳离子[Fe (H O) (OH) ]4+,结构如下图,解释能够形成双核阳离
3 2 2 8 2
子的原因:_______。(4)镍白铜(铜镍合金)常用作海洋工程应用材料。某镍白铜合金的晶胞结构如图所示。
① 晶胞中铜原子与镍原子的原子个数比为_______ 。
②已知一定条件下晶胞的棱长为a cm,用N 表示阿伏加德罗常数的值,在该条件下该晶体的摩尔体
A
积为_______ m3·mol-1(用含a, N 的代数式表示)。
A
【答案】(1) 1s22s22p63s23p63d64S2 或 [Ar]3d64S2 d
(2)Fe3+的3d5半满状态更稳定
(3) FeCl 为分子晶体,熔点受分子间作用力影响,FeF 是离子晶体,熔点受离子键强弱的影响,离子
3 3
键强度比分子间作用力大得多 HO和OH-中的O原子提供孤电子对,Fe3+有空轨道能接受孤电子对,
2
形成配位键
(4) 1:3 N ·a3·10-6
A
【解析】(1)基态Fe原子核外电子排布式为1s22s22p63s23p63d64S2 或 [Ar]3d64S2;Ni是28号元素,其价
电子排布式为 3d84s2,其位于元素周期表的 d区;(2)从结构角度分析,Fe2+ 易被氧化成Fe3+的原因是
Fe3+的3d5半满状态更稳定;(3)①FeCl 的熔点(306℃)显著低于FeF 的熔点(1000℃)的原因是FeCl 为分子
3 3 3
晶体,熔点受分子间作用力影响,FeF 是离子晶体,熔点受离子键强弱的影响,离子键强度比分子间作用
3
力大得多;②形成双核阳离子的原因HO和OH- 中的O原子提供孤电子对,Fe3+ 有空轨道能接受孤电子
2
对,形成配位键;(4)①由晶胞图可知,Cu原子位于顶点,其个数为8× =1,Ni原子位于面心,其个数为
6× =3,则晶胞中铜原子与镍原子的原子个数比为1:3;②由①可知,该晶胞中含有1个Cu原子,含有3
个Ni原子,则1个晶胞含有1个CuNi ,其物质的量为 mol,1个晶胞的体积为 ,则该晶体
3
的摩尔体积为N ·a3·10-6 m3·mol-1。
A
13.(2023·陕西省“高考研究831重点课题项目“联盟学校第二次大联考)铁在史前就为人们所用。在
人类文明发展过程中,铁所起的作用是其他任何元素都不能比拟的。请回答下列问题:
(1)基态铁原子中,价电子电子云的伸展方向有_______ 种。
(2)五羰基合铁[Fe(CO) ]分解制铁晶体,反应过程中断裂和形成的化学键有_________ ( 填序号);
5
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键
F.范德华力
Fe(CO) 中各元素电负性的大小顺序是___________________。
5
(3)绿矾(FeSO ·7H O)结构如图。
4 2①HO分别与Fe2+、SO 2-的相互作用分别为_______________、_____________。
2 4
②比较SO 2-中的键角∠O−S−O________H O中的键角∠H−O−H。 (填“<” “>”或“=”)
4 2
(4)铁的化合物种类众多,其中 FeF 的熔点高于 1000°C,而 FeBr 的熔点只有 200°C,原因是
3 3
___________。
(5)铁的一种配位化合物(普鲁士蓝)中铁氰骨架结构如图(a)所所示,骨架为正六面体,K+位于骨架的正
六面体的空穴中,以平衡铁氰骨架的负电荷,则该钾盐的化学式为_____________________。
(6)一种锂电池的正极材料磷酸铁锂(LiFePO ) 的晶胞结构如上图(b)所示。其中Li+分别位于顶角、棱心、
4
面心,O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。磷酸铁锂晶
体的晶胞参数分别为anm、bnm,则磷酸铁锂晶体的摩尔体积V =____________ cm3·mol−1 (已知阿伏加德
m
罗常数为N ,晶体的摩尔体积是指单位物质的量晶体所占的体积)。
A
【答案】(1)6 (2) DE O>C>Fe
(3) 配位键 分子间氢键 >
(4)FeF 是离子晶体,FeBr 是分子晶体,离子晶体的熔点大于分子晶体,故 FeF 的熔点高于1000°C,
3 3 3
而FeBr 的熔点只有200°C
3
(5)KFe[Fe(CN) ] 或KFe (CN)
6 2 6
(6)
【解析】(1)基态铁原子中,价电子排布式为3d64s2,则价电子电子云的伸展方向有6种;(2)五羰基合
铁[Fe(CO) ]分解制铁晶体即Fe(CO) Fe+5CO,反应过程中断裂了配位键,形成了金属键,而CO中共价
5 5
键未发生断裂;根据同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,Fe(CO) 中各元
5
素电负性的大小顺序是O>C>Fe;(3)①根据图中信息HO与Fe2+的相互作用力为配位键,HO与SO 2-的
2 2 4
相互作用力为分子间氢键;②SO 2-立体构型为正四面体形,HO立体构型为“V”形,则 中的键角
4 2
∠O−S−O>HO中的键角∠H−O−H;(4)铁的化合物种类众多,其中FeF 的熔点高于1000°C,而FeBr 的
2 3 3
熔点只有200°C,原因是FeF 是离子晶体,FeBr 是分子晶体,离子晶体的熔点大于分子晶体,故FeF 的
3 3 3熔点高于1000°C,而FeBr 的熔点只有200°C;(5)根据图中信息该晶胞中铁离子有 ,亚铁离子有
3
,CN-有 ,Fe与CN-个数比为2:6,根据化合价代数和为0,则该钾盐的化学式为
KFe (CN) ;(6)根据图中信息得到晶胞中Li+个数为 ,则该晶胞中有4个LiFePO ,磷
2 6 4
酸 铁 锂 晶 体 的 晶 胞 参 数 分 别 为 anm 、 bnm , 则 磷 酸 铁 锂 晶 体 的 摩 尔 体 积
。
14.(2023·河南省普通高中高三适应性考试)磷、碳、氢等非金属及其化合物用途广泛。试回答下列问
题。
(1)白磷(P )在氯气中燃烧可生成PCl 和PCl 。
4 3 5
①形成 PCl 时,P 原子的一个 3s 电子激发入 3d 轨道后参与成键,该激发态的价电子排布式为
5
___________。
②研究表明,在加压条件下PCl 于148℃液化时能发生与水类似的自耦电离,形成一种能导电的熔体,
5
其电离方程式为 ___________ ,产生的阳离子的空间结构为___________;N和P都有+5价,但NCl 不存
5
在,从原子结构的角度分析其原因:___________。
(2)分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电
子数(如苯分子中的大π键可表示为 )。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π
键可表示为___________ ,一定在同一平面上的原子有___________个;乙醇显中性而苯酚显酸性的原因
是:在大π键中氧的p电子云向苯环转移,___________。
(3)镍镧合金(LaNi )具有很强的储氢能力,其晶胞结构如图所示,其中n=___________。 已知晶胞体积
n
为9.0 ×10 -29 m3,若储氢后形成LaNiH (氢进入晶胞空隙,晶胞体积不变),则氢在合金中的密度为
n 5.5
___________g·cm-3(保留1位小数)。
【答案】(1) 3s13p23d1 PCl PCl -+PCl - 正四面体形 P原子半径大,且有可以利用
5 6 4
的3d空轨道采取sp3d杂化,N原子半径小且没有可以利用的d空轨道
(2) 13 使O原子上的电子云密度降低,O、H间的结合力减弱,易离解出H+
(3) 5 0.1
【解析】(1)①磷元素的原子序数为15,价电子排布式为3s23p3,由形成五氯化磷时,磷原子的一个3s
电子激发入3d轨道后参与成键可知,激发态的价电子排布式为3s13p33d1;②由题意可知,五氯化磷发
生与水类似的自耦电离电离出PCl -和PCl -,电离方程式为PCl PCl -+PCl -,PCl -离子中价层电子对
6 4 5 6 4 4
数为4、孤对电子对数为0,则离子的空间结构为正四面体形;位于同一主族的磷原子的原子半径大于氮原
子,磷原子可以利用3d空轨道采取sp3d杂化与氯原子形成五氯化磷,而氮原子没有可以利用的d空轨道,所以N和P都有+5价,但NCl 不存在;(2)若苯酚羟基中的氧原子的杂化方式为sp2杂化,未参与杂化的2
5
个p电子与苯环上6个碳原子中未参与杂化的6个p电子形成 大π键,则分子中的13个原子一定在同一
平面上;乙醇显中性而苯酚显酸性的原因是在大 π键中氧原子的p电子云向苯环转移,使羟基中氧原子上
的电子云密度降低,氧原子和氢原子间的结合力减弱,易离解出氢离子;(3)由晶胞结构可知,晶胞中位于
面上和体心的镍原子个数为8× +1=5,由储氢后形成LaNiH 可知,晶胞中氢原子的质量为 g,则
n 5.5
氢在合金中的密度为 ≈0.1g/cm3。
15.(2023·山东省聊城市部分学校高三第三次学业质量联合检测)铜及其化合物在生产、生活中有广泛
应用。最近科学家开发出石墨炔调控 Cu 单原子电催化剂 实现 CO 还原制备 CH ,反应为
2 4
。
(1)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则绿色对应的波长为
___________(填标号)。
A.577~492nm B.597~577nm C.622~597nm
基态Cu原子的未成对电子占据原子轨道的形状为___________。
(2)①上述反应涉及的物质中,既含 键又含 键的非极性分子是___________(填分子式)。
②VSEPR模型和空间结构相同的分子有___________(填分子式)。
③在周期表中铜和锌相邻,第二电离能与第一电离能相差较大的是___________(填元素符号)。
(3) 催化剂如图所示。铜的配位数未为___________。N原子与直接连接的原子构成的空间结构是
___________。
(4)铜可形成多种配合物,如 、 等。 分子中 键角为
107°,在 中的 键角为109.5°,键角变大的原因是___________。
(5)最近我国科学家开发出一种高效储存、分离、提纯H 新材料,晶胞结构如图所示。已知:图(a)边
2
长为xpm,图(c)中高为ypm,Ca、Cu的原子半径分别为 、 ,设 为阿伏加德罗常数
的值。该晶胞中原子空间利用率为___________(注:晶胞中原子空间利用率等于原子总体积与晶胞体积之
比)。【答案】(1) A 球形
(2) CO CH 、CO Cu
2 4 2
(3) 4 三角锥形
(4)NH 分子中N原子的孤电子对进入Cu2+的空轨道与Cu2+形成配位键后,使得原孤电子对与成键电子
3
对间的排斥作用变成了成键电子对间的相互排斥,排斥作用减弱,因而键角变大
(5)
【解析】(1)橙色、黄色、绿色对应的波长分别为622~597nm、597~577nm、577~492nm,故选A;Cu
元素为29号元素,原子核外有29个电子,所以核外电子排布式为 ,未成对电子占
据的原子轨道为4s轨道,形状为球形。(2)①题给反应涉及的物质中,既含σ键,又含π键的非极性分子是
CO 。②VSEPR模型和空间结构相同的分子有CH 、CO 。③铜失去一个电子后变为 ,
2 4 2
锌失去一个电子后变为 ,铜失去一个电子后,3d轨道为全满稳定结构,故铜的第二
电离能与第一电离能相差较大。(3)由图可知铜的配位数为4,N原子采用 杂化,空间结构为三角锥形。
(4)由于NH 分子中N原子的孤电子对进入Cu2+的空轨道与Ca2+形成配位键后,使得原孤电子对与成键电子
3
对间的排斥作用变成了成键电子对间的相互排斥,排斥作用减弱,因而键角变大。(5)观察图(c)知,钙位于
六棱柱的顶点和上、下面心,铜位于面上和体内。1个晶胞含铜原子数为 ,含钙原子数为
,晶体的化学式为CaCu ;图(a)面积为 ,图(c)体积为 ,原子
3
空间利用率等于原子总体积与晶胞体积之比,即 。
16.(2023·浙江省Z20名校联盟高三第三次联考)氮及其化合物在医药化工领域应用十分厂泛。
I、配合物顺铂[Pt(NH )Cl]是临床使用的第一代铂类抗癌药物,其抗癌机理是在 转运蛋白的作用下,
3 2 2
顺铂进入人体细胞发生水解,生成的Pt(NH )(OH)Cl与DNA结合,破坏DNA的结构阻止癌细胞增殖,如
3 2
图所示:
请回答:
(1)基态N原子价层电子排布式为_______。
(2)鸟嘌呤分子中N原子杂化方式为_______。
(3) Pt(NH )Cl 中配体与铂(II)的结合能力:Cl-_______NH (填“>”或“<”)
3 2 2 3
(4)已知顺铂和反铂互为同分异构体,两者的结构和性质如下表。
顺铂 反铂结构
25℃时溶解度/g 0.2577 0.0366
①推测Pt(NH )Cl 中Pt的杂化轨道类型不是sp3,依据是_______。
3 2 2
②顺铂在水中的溶解度大于反铂的原因是_______。
II﹑(CH NH )PbI 是钙钛矿型太阳能电池的重要吸光材料,其晶胞结构如图所示,已知(CHNH )PbI 摩
3 3 3 3 3 3
尔质量为M g·molˉ1 ,晶胞边长为anm,N 为阿伏加德罗常数的值。
A
(5)中心小黑球的配位数为_______。
(6)(CH NH )PbI 晶体的密度为_______ g· cm-3。
3 3 3
【答案】(1)2s22p3
(2)sp2、sp3
(3)<
(4)Pt杂化类型如果是sp3,则Pt(NH )Cl 空间构型为四面体形,不会存在同分异构体 顺铂为极性
3 2 2
分子,反铂为非极性分子
(5)6
(6) 或
【解析】(1)基态N原子价层电子指的是最外层电子,即价层电子排布式为2s22p3;(2)根据鸟嘌呤的结
构简式,五元环、六元环共面,因此环上的N原子杂化类型为sp2,-NH 中N原子杂化类型为sp3;(3)NH
2 3
具有较强的电子捕获能力,可以与Pt形成更紧密的配位键,因此结合能力:Cl-<NH ;(4)①Pt(NH )Cl 中
3 3 2 2
Pt杂化类型如果是sp3,则Pt(NH )Cl 空间构型为四面体形,只有一种结构,不会存在同分异构体,因此
3 2 2
Pt的杂化类型不是sp3,Pt(NH )Cl 空间构型为平面四边形;②根据顺铂的结构,顺铂正负电荷中心不重合,
3 2 2
顺铂为极性分子,同理反铂为非极性分子,水是极性分子,根据“相似相溶”,顺铂在水中的溶解度大于
反铂;(5)根据晶胞图可知,中心小黑球周围由 6个白球,即小黑球的配位数为 6;(6)晶胞的质量为
g,晶胞的体积为(a×10-7)3cm3,则晶胞的密度为 g/cm3或 g/cm3。