文档内容
专题 17 物质结构与性质综合题
1.(2022·全国甲卷)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了
奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四氟乙烯(CF=CF )的共聚物(ETFE)制成。
2 2 2 2
回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
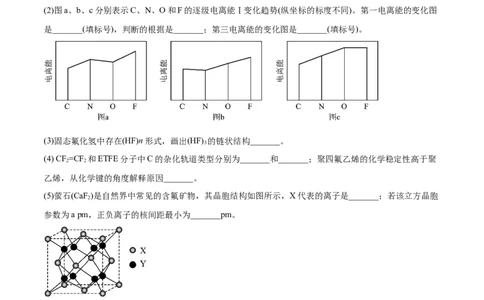
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图
是_______(填标号),判断的根据是_______;第三电离能的变化图是_______(填标号)。
(3)固态氟化氢中存在(HF)n形式,画出(HF) 的链状结构_______。
3
(4) CF =CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯的化学稳定性高于聚
2 2
乙烯,从化学键的角度解释原因_______。
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______;若该立方晶胞
2
参数为a pm,正负离子的核间距最小为_______pm。
2.(2022·全国乙卷)卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)
a. b. c. d.
(2)①一氯乙烯 分子中,C的一个_______杂化轨道与Cl的 轨道形成 _______键,并且Cl的 轨道与C的 轨道形成3中心4电子的大 键 。
②一氯乙烷 、一氯乙烯 、一氯乙炔 分子中, 键长的顺序是_______,理由:
(ⅰ)C的杂化轨道中s成分越多,形成的 键越强:(ⅱ)_______。
(3)卤化物 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______。解释X的熔
点比Y高的原因_______。
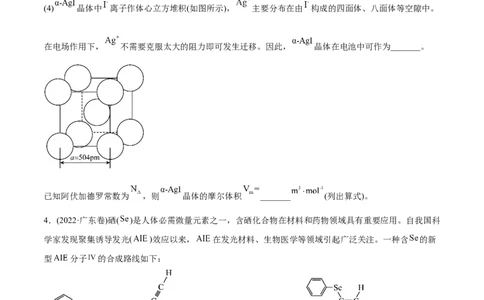
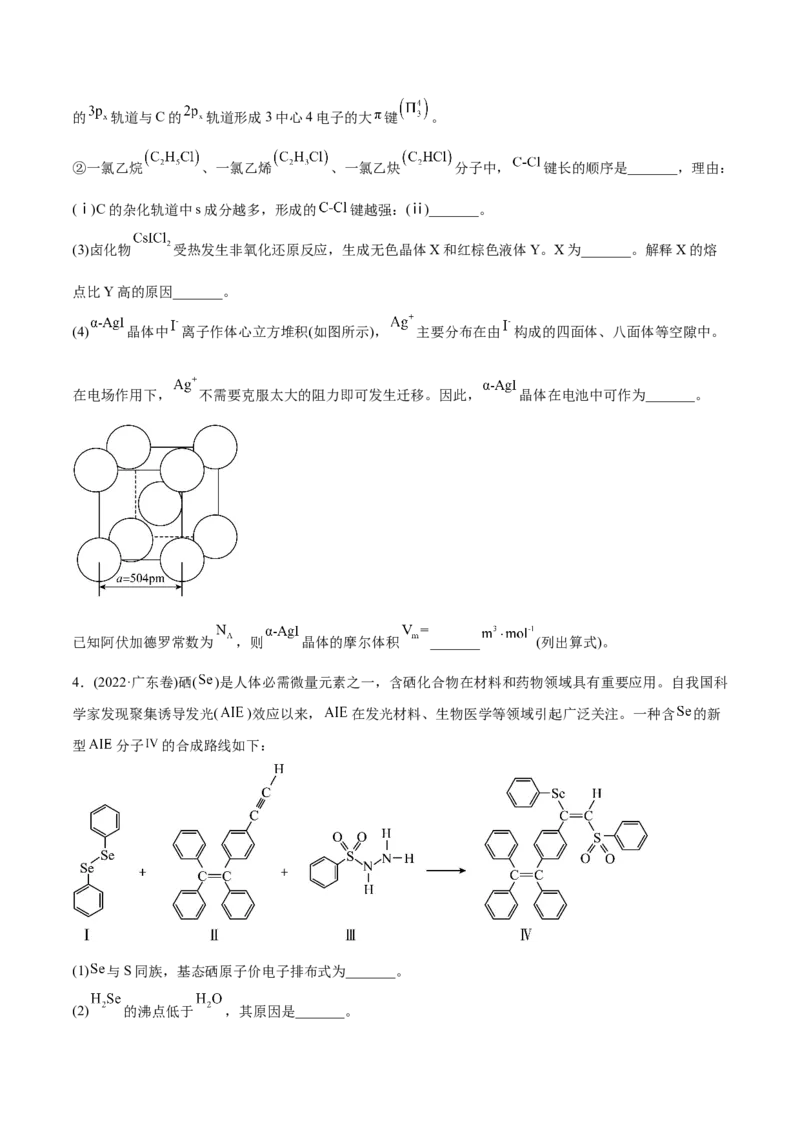
(4) 晶体中 离子作体心立方堆积(如图所示), 主要分布在由 构成的四面体、八面体等空隙中。
在电场作用下, 不需要克服太大的阻力即可发生迁移。因此, 晶体在电池中可作为_______。
已知阿伏加德罗常数为 ,则 晶体的摩尔体积 _______ (列出算式)。
4.(2022·广东卷)硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科
学家发现聚集诱导发光( )效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含 的新
型 分子 的合成路线如下:
(1) 与S同族,基态硒原子价电子排布式为_______。
(2) 的沸点低于 ,其原因是_______。(3)关于I~III三种反应物,下列说法正确的有_______。
A.I中仅有 键
B.I中的 键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______。
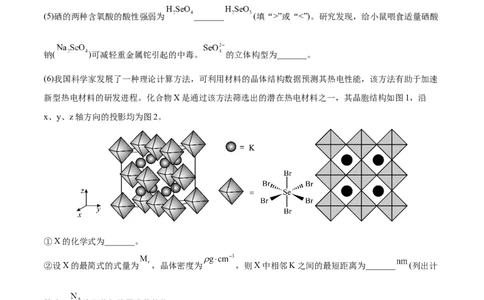
(5)硒的两种含氧酸的酸性强弱为 _______ (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸
钠( )可减轻重金属铊引起的中毒。 的立体构型为_______。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速
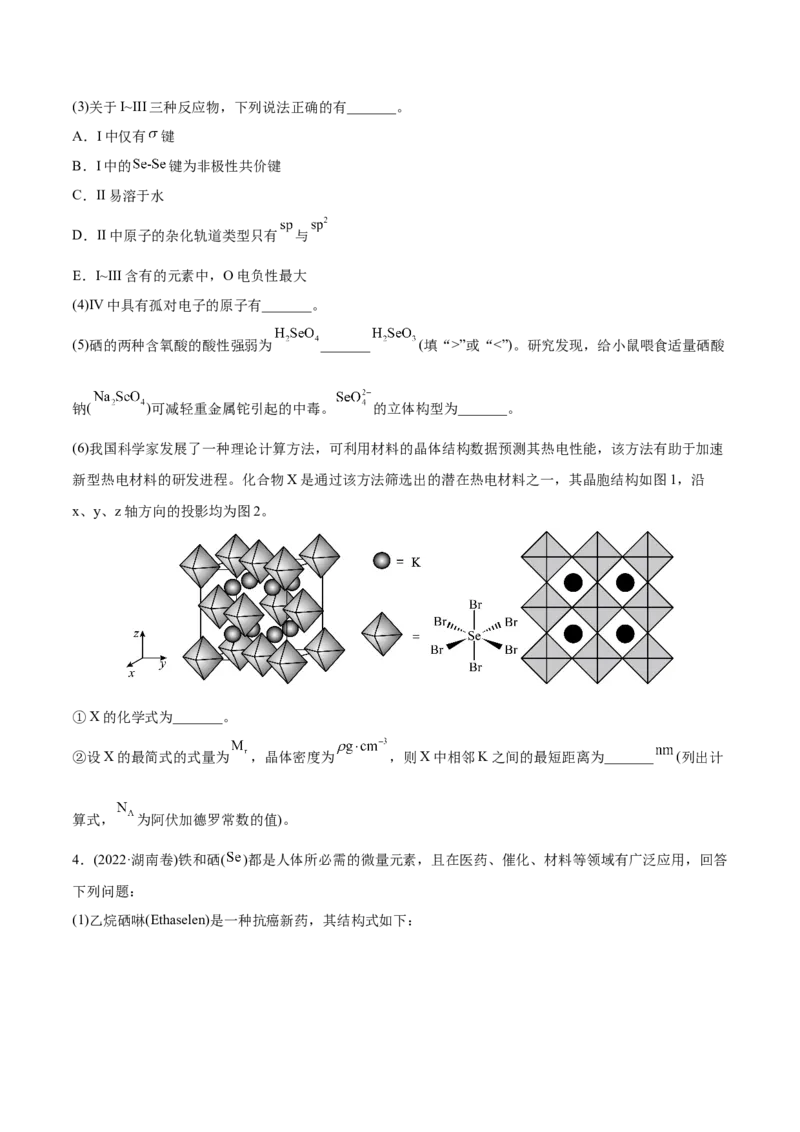
新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿
x、y、z轴方向的投影均为图2。
①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为_______ (列出计
算式, 为阿伏加德罗常数的值)。
4.(2022·湖南卷)铁和硒( )都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答
下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:①基态 原子的核外电子排布式为 _______;
②该新药分子中有_______种不同化学环境的C原子;
③比较键角大小:气态 分子_______ 离子(填“>”“<”或“=”),原因是_______。
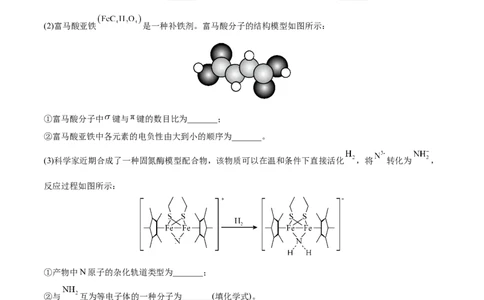
(2)富马酸亚铁 是一种补铁剂。富马酸分子的结构模型如图所示:
①富马酸分子中 键与 键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化 ,将 转化为 ,
反应过程如图所示:
①产物中N原子的杂化轨道类型为_______;
②与 互为等电子体的一种分子为_______(填化学式)。
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:①该超导材料的最简化学式为_______;
②Fe原子的配位数为_______;
③该晶胞参数 、 。阿伏加德罗常数的值为 ,则该晶体的密度为_______ (列出
计算式)。
1.(2022·陕西西安·二模)硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为_______。
(2)H SeO 的中心原子杂化类型是:_______, 的立体构型是_______。与 互为等电子体的分子
2 3
有_______(写一种物质的化学式即可)。
(3)H Se属于_______(填“极性”或“非极性”)分子;比较HSe与HO沸点高低,并说明原因:_______。
2 2 2
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为_______;若
该晶胞密度为ρg·cm-3,硒化锌的摩尔质量为Mg·mol-1,N 代表阿伏加德罗常数的值,则晶胞参数a为
A
_______。
2.(2022·陕西汉中·二模)主族元素N、F、Si、As、Se、Cl等的某些化合物对工农业生产意义重大,回答下
列问题:
(1)Si N 陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于_______晶体;
3 4SiCl 中Si采取的杂化类型为_______。
4
(2)O、F、Cl电负性由大到小的顺序为_______;OF 分子的空间构型为_______;OF 的熔、沸点低于
2 2
ClO,原因是_______。
2
(3)Se元素基态原子的原子核外电子排布式为_______;As的第一电离能比Se的第一电离能大的原因为
_______。
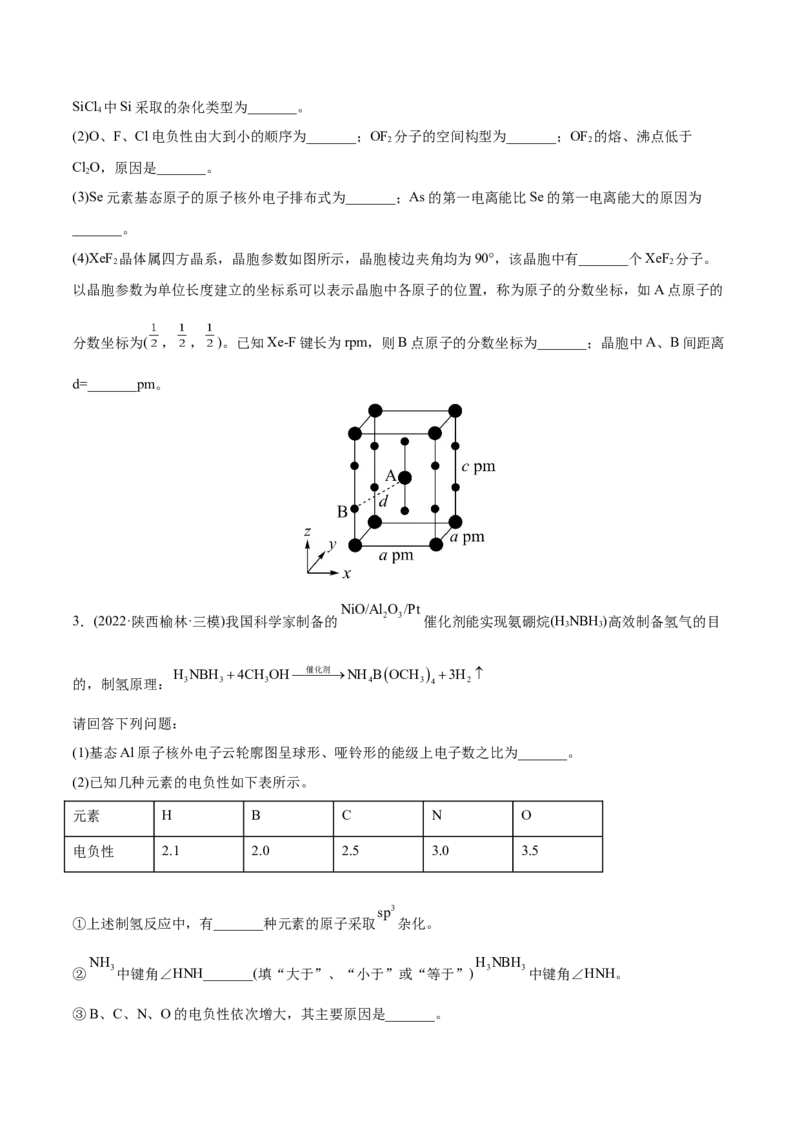
(4)XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______个XeF 分子。
2 2
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的
分数坐标为( , , )。已知Xe-F键长为rpm,则B点原子的分数坐标为_______;晶胞中A、B间距离
d=_______pm。
NiO/Al O /Pt
3.(2022·陕西榆林·三模)我国科学家制备的 2 3 催化剂能实现氨硼烷(H NBH )高效制备氢气的目
3 3
H NBH 4CH OH催化剂NH BOCH 3H
的,制氢原理: 3 3 3 4 3 4 2
请回答下列问题:
(1)基态Al原子核外电子云轮廓图呈球形、哑铃形的能级上电子数之比为_______。
(2)已知几种元素的电负性如下表所示。
元素 H B C N O
电负性 2.1 2.0 2.5 3.0 3.5
sp3
①上述制氢反应中,有_______种元素的原子采取 杂化。
NH H NBH
② 3中键角∠HNH_______(填“大于”、“小于”或“等于”) 3 3中键角∠HNH。
③B、C、N、O的电负性依次增大,其主要原因是_______。④在氨硼烷中,H—B键中H带部分_______(填“正”或“负”)电荷。
(3)某有机硼化合物的结构简式如图1所示,1mol该有机物中含_______molσ键。组成该有机物的第二周期
元素第一电离能由大到小的顺序为_______(填元素符号)。
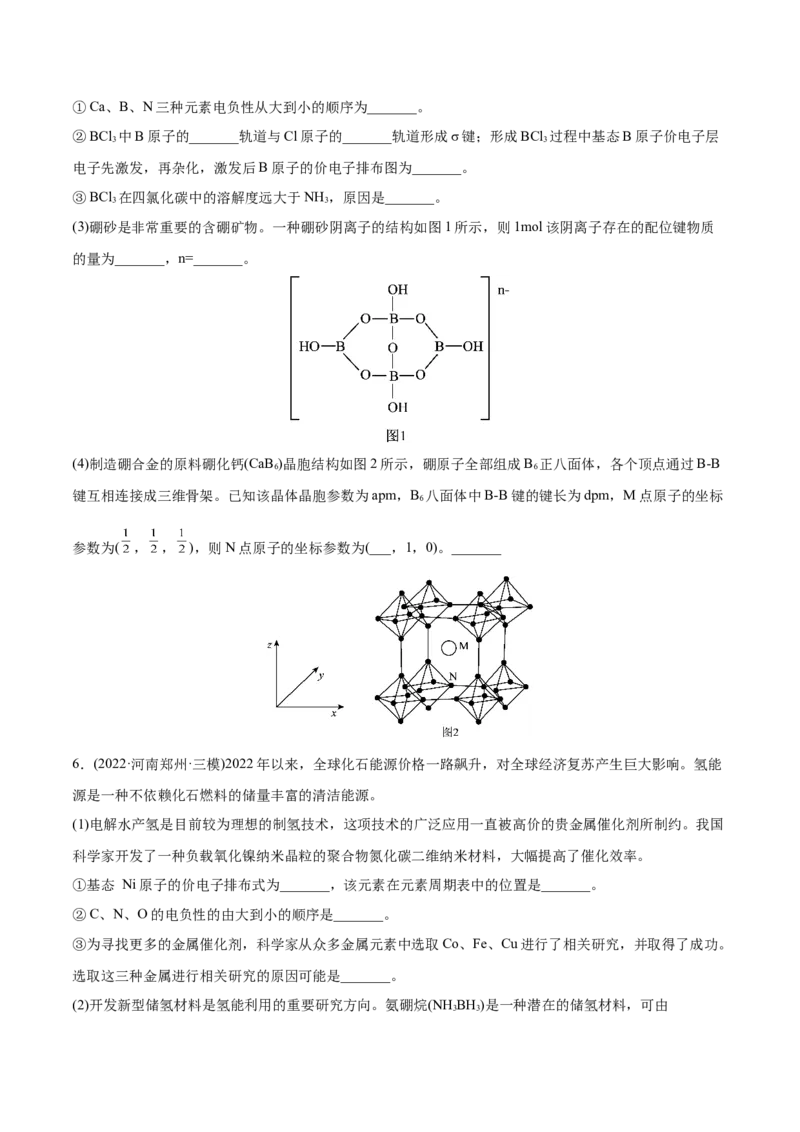
(4)化硼是一种新型无机非金属材料,晶胞结构如图2所示。以晶胞参数为单位长度建立坐标系,表示晶胞
中各原子的位置,称为原子坐标。a点磷原子的坐标为(0,0,0),b点磷原子的坐标为(1,1,0),则c点
硼原子的坐标为_______。
(5)四氢铝钠(NaAlH )是有机合成中重要的还原剂,晶胞结构如图3所示。
4
AlH AlH
① 4的空间构型为_______, 4的配位数为_______。
gcm-3
②已知N 为阿伏加德罗常数的值,晶体的密度为_______(用含a、N 的代数式表示) 。
A A
4.(2022·山西太原·二模)我国科学家研究了具有高稳定性的二维硼烯氧化物(B O)的超导电性。回答下列
m n
问题:
(1)第一电离能介于B、N之间的第二周期元素为_______(填元素符号)。
(2)①已知二维硼烯氧化物的部分结构如图所示,则该氧化物的化学式为_____,其中硼原子的杂化轨道类
型为_____。②键长和键角的数值可通过晶体的X射线衍射实验获得。经过该实验测定,二维硼烯氧化物中B-B键的键
长大于B-O键的键长,其原因是_______。
(3)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因_______。
(4)LiBH -LiI复合材料在低温下表现出较高的离子电导率。BH 离子中H的化合价为-1,其原因可能是
4
_______,BH 可以被PS 离子部分取代,PS 离子的空间结构为_______。
(5)Fe O 是电子导体,其导电率显著高于Fe O,这归因于Fe2+和Fe3+中心之间的电子交换。如图甲所示,
3 4 2 3
Fe O 晶体中,O2-围成正四面体空隙(如:1、3、6、7围成)和正八面体空隙(如:3、6、7、8、9、12围成),
3 4
Fe O 中有一半的Fe3+填充在正四面体空隙中, Fe2+和另一半 Fe3+填充在正八面体空隙中。则没有填充阳离
3 4
子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为_______。FeO 、Fe O 都具有与Fe O 相
2 3 3 4
似的立方堆积结构,氧化亚铁晶体的晶胞如图乙所示,已知:氧化亚铁晶体的密度为ρg·cm-3,N 代表阿
A
伏加德罗常数的值。在该晶体中,与Fe2+紧邻且等距离的Fe2+数目为_______ ;Fe2+与O2-的最短核间距为
_______cm(列出计算式)。
5.(2022·山西临汾·三模)总订单数已经超过1000架的国产大飞机C919预定在今年交付,其制造使用了较
多含硼材料(如硼纤维、氮化硼等),多项技术打破了外国垄断。
(1)原子的能量由核电荷数、电子数、_______三个因素共同决定;基态B原子的核外电子填充在_______个
轨道中。
(2)耐高温材料立方BN制备流程中用到NH 、BCl 和触媒剂Ca B N。
3 3 3 2 4①Ca、B、N三种元素电负性从大到小的顺序为_______。
②BCl 中B原子的_______轨道与Cl原子的_______轨道形成σ键;形成BCl 过程中基态B原子价电子层
3 3
电子先激发,再杂化,激发后B原子的价电子排布图为_______。
③BCl 在四氯化碳中的溶解度远大于NH ,原因是_______。
3 3
(3)硼砂是非常重要的含硼矿物。一种硼砂阴离子的结构如图1所示,则1mol该阴离子存在的配位键物质
的量为_______,n=_______。
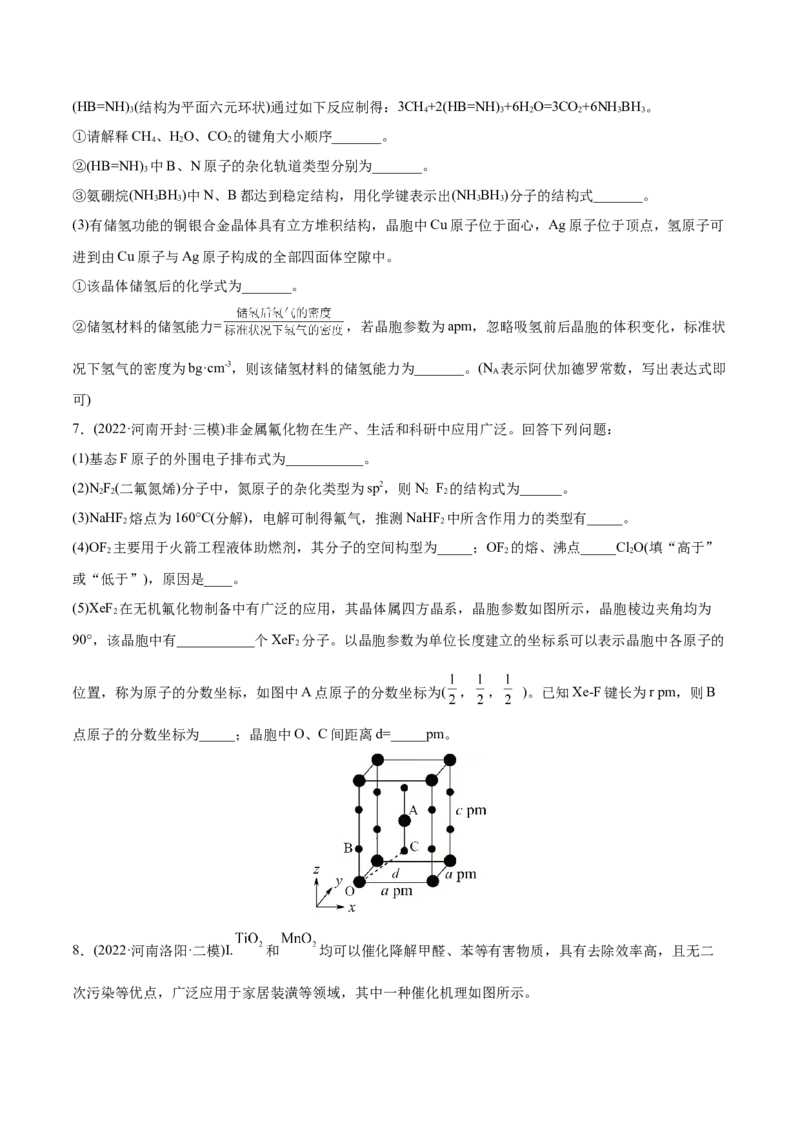
(4)制造硼合金的原料硼化钙(CaB )晶胞结构如图2所示,硼原子全部组成B 正八面体,各个顶点通过B-B
6 6
键互相连接成三维骨架。已知该晶体晶胞参数为apm,B 八面体中B-B键的键长为dpm,M点原子的坐标
6
参数为( , , ),则N点原子的坐标参数为(___,1,0)。_______
6.(2022·河南郑州·三模)2022年以来,全球化石能源价格一路飙升,对全球经济复苏产生巨大影响。氢能
源是一种不依赖化石燃料的储量丰富的清洁能源。
(1)电解水产氢是目前较为理想的制氢技术,这项技术的广泛应用一直被高价的贵金属催化剂所制约。我国
科学家开发了一种负载氧化镍纳米晶粒的聚合物氮化碳二维纳米材料,大幅提高了催化效率。
①基态 Ni原子的价电子排布式为_______,该元素在元素周期表中的位置是_______。
②C、N、O的电负性的由大到小的顺序是_______。
③为寻找更多的金属催化剂,科学家从众多金属元素中选取Co、Fe、Cu进行了相关研究,并取得了成功。
选取这三种金属进行相关研究的原因可能是_______。
(2)开发新型储氢材料是氢能利用的重要研究方向。氨硼烷(NH BH)是一种潜在的储氢材料,可由
3 3(HB=NH) (结构为平面六元环状)通过如下反应制得:3CH+2(HB=NH) +6H O=3CO+6NHBH。
3 4 3 2 2 3 3
①请解释CH、HO、CO 的键角大小顺序_______。
4 2 2
②(HB=NH) 中B、N原子的杂化轨道类型分别为_______。
3
③氨硼烷(NH BH)中N、B都达到稳定结构,用化学键表示出(NH BH)分子的结构式_______。
3 3 3 3
(3)有储氢功能的铜银合金晶体具有立方堆积结构,晶胞中Cu原子位于面心,Ag原子位于顶点,氢原子可
进到由Cu原子与Ag原子构成的全部四面体空隙中。
①该晶体储氢后的化学式为_______。
②储氢材料的储氢能力= ,若晶胞参数为apm,忽略吸氢前后晶胞的体积变化,标准状
况下氢气的密度为bg·cm-3,则该储氢材料的储氢能力为_______。(N 表示阿伏加德罗常数,写出表达式即
A
可)
7.(2022·河南开封·三模)非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子的外围电子排布式为___________。
(2)N F(二氟氮烯)分子中,氮原子的杂化类型为sp2,则N F 的结构式为______。
2 2 2 2
(3)NaHF 熔点为160°C(分解),电解可制得氟气,推测NaHF 中所含作用力的类型有_____。
2 2
(4)OF 主要用于火箭工程液体助燃剂,其分子的空间构型为_____;OF 的熔、沸点_____ClO(填“高于”
2 2 2
或“低于”),原因是____。
(5)XeF 在无机氟化物制备中有广泛的应用,其晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
2
90°,该晶胞中有___________个XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的
2
位置,称为原子的分数坐标,如图中A点原子的分数坐标为( , , )。已知Xe-F键长为r pm,则B
点原子的分数坐标为_____;晶胞中O、C间距离d=_____pm。
8.(2022·河南洛阳·二模)I. 和 均可以催化降解甲醛、苯等有害物质,具有去除效率高,且无二
次污染等优点,广泛应用于家居装潢等领域,其中一种催化机理如图所示。回答下列问题:
(1)基态Ti和Mn原子中未成对电子数之比为_______。
(2)CO 和·CHO中碳原子的杂化形式分别为_______、_______。
2
(3)HCHO的空间构型为_______。
(4)金属钛和锰可导电、导热,有金属光泽和延展性,这些性质都可以用理论解释。已知金属锰有多种晶型,
y型锰的面心立方晶胞俯视图符合下列_______(填编号)。
II.2019年诺贝尔化学奖授予三位化学家,以表彰其对研究开发锂离子电池作出的卓越贡献。 、聚
乙二醇、 、 和LiCl等可作锂离子聚合物电池的材料。
回答下列问题:
(5)Fe的基态原子的价电子排布式为_______。
(6)乙二醇(HOCHCHOH)的相对分子质量与丙醇(CHCHCHOH)相近,但沸点高出100℃,原因是_______。
2 2 3 2 2
III.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl ∙H O属
3 2
正交晶系(长方体形)。晶胞参数为0.72nm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有C1原子的分
布图和原子分数坐标。LiCl ∙H O的摩尔质量为 ,设 为阿伏加德罗常数的值。
3 2(7)该晶胞中Cl原子的数目为_______, 晶体的密度为_______ (列出计算表达式)。
9.(2022·云南昆明·一模)中子衍射实验证实:trans-[CO(NH CHCHNH )Cl]Cl·HCl·2H O晶体中仅存在3种
2 2 2 2 2
离子:X+和含钴的Y+和Cl—,不存在分子。Y+的结构如图所示。
回答下列问题:
(1)Co3+的价层电子排布式是_______,已知磁矩μ = (n表示未成对电子数),则Co3+的磁矩
B
μ =_______。
B
(2)Y+中的配体,提供孤电子对的原子是_______(填元素符号),Co3+的配位数是_______,X+是_______(填
离子符号)。
(3)Y+中N原子的杂化方式是_______,乙二胺(NH CHCHNH )与正丁烷的相对分子质量相近,比较两者的
2 2 2 2
沸点高低并解释原因_______。
(4)NO 、NO 、NO 的键角由大到小的顺序是_______。
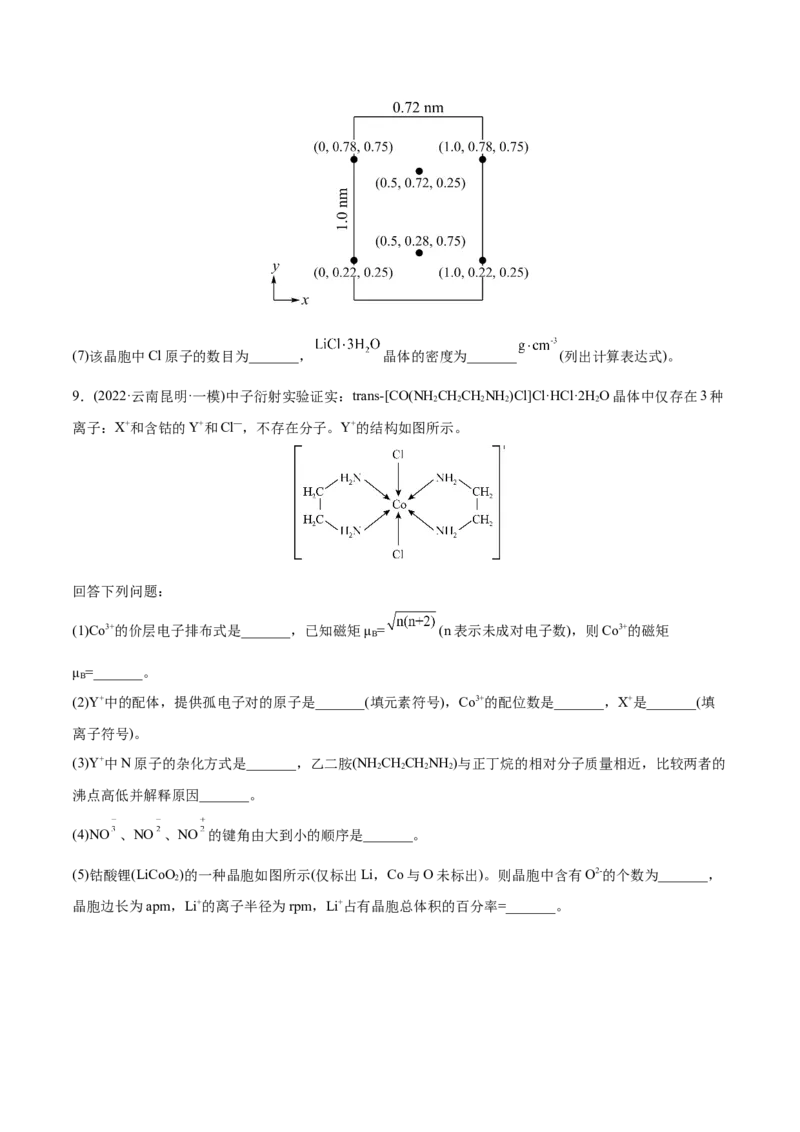
(5)钴酸锂(LiCoO )的一种晶胞如图所示(仅标出Li,Co与O未标出)。则晶胞中含有O2-的个数为_______,
2
晶胞边长为apm,Li+的离子半径为rpm,Li+占有晶胞总体积的百分率=_______。10.(2022·安徽马鞍山·三模)人类对第二周期的元素及化合物认识最早。
(1)第二周期的元素中,I(第一电离能)从大到小排前三位的是_______。
1
(2)人类合成的第一个稀有气体化合物是XeF+PtF ,PtF 中的键角有90°和180°两种。下列关于该化合物的
说法中正确的是_______。
A.熔化状态下不能导电
B.XeF+中所有原子都满足8电子稳定结构
C.用两个Cl替换F后,所得PtFCl 有两种结构
4 2
D.含有离子键、极性键、非极性键和配位键
(3)XeF+PtF 溶于水可生成Xe和HPtF ,写出反应的化学方程式。_______。
6
(4)解释HNO 和HNO 酸性强弱不同的原因_______。
3 2
(5)SCN—中C原子的杂化类型为_______, 其中含有两个相同的大π键,其形式为_______。(用π 表示,
n为原子数,m为电子数),检验Fe3+时,SCN—以 S原子配位不以N原子配位的原因是_______。
(6)如图,在NaCl的晶体中,Na+和Cl—互相占据对方的正八面体空隙,CaF 晶体中,F—占据由Ca2+构成的
2
所有正四面体空隙。钛镍合金具有形状记忆功能。某钛、镍原子个数比为2:1的合金的晶体结构为:镍原
子呈面心立方排列,钛原子填充在由镍原子围成的所有八面体空隙和一半的四面体空隙中,若最近的钛原
子和镍原子紧密接触,镍原子周围距离最近的钛原子数为_______; 钛原子和镍原子的半径分别为r 和
1
r,该晶体的空间利用率为_______(用含r的代数式表示,不必化简,空间利用率=晶胞中原子的总体积/晶
2
胞的体积)。
11.(2022·甘肃兰州·一模)我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划,太阳能电池板主要材料为单晶硅或多晶硅。
(1)与硅同主族的锗元素的价层电子排布式为____。
(2)NCl 、SiCl 、SCl 的键角由大到小的顺序为____,其中SCl 的分子构型为____。
3 4 2 2
(3)环戊基二乙基硅基乙炔分子结构为 ,分子中σ键和π键的个数比为____。
(4)碳与硅元素同主族,但形成的晶体性质却有不同。单晶硅不导电,但石墨能导电,石墨能够导电的原因
是____。
(5)SiC和单晶硅具有相似的晶体结构,但SiC熔点更高,其原因是____。
(6)晶胞中原子的位置通常可用原子分数坐标表示(原子分数坐标:将原子位置的坐标表示为晶胞棱长的分
数)。复杂结构的三维表示往往难以在二维图上绘制和解释,可以从晶胞的一个方向(通常选择晶胞的一个
轴的方向)往下看,某面心立方晶胞的投影图如图1所示。某种硫化硅晶体的晶胞结构的投影图如图2所示。
①该硫化硅晶体的化学式为____。
②在该晶胞中与S距离最近的Si的数目为____。
③若距离最近的Si和S的核间距为dnm,阿伏加德罗常数的值为N ,则该硫化硅晶体的密度为
A
____g·cm-3(列出算式即可)。