文档内容
化学综合实验
考向一 以无机物制备为主线的综合实验
1.有气体参与的物质制备综合题考向分析
2.物质制备型实验题的思维方法
1.[2023·河北,15(1)(2)(3)(4)(5)]配合物Na [Co(NO ) ](M=404 g·mol-1)在分析化学中用于K+的鉴定,其制
3 2 6
备装置示意图(夹持装置等略)如图,步骤如下:
①向三颈烧瓶中加入15.0 g NaNO 和15.0 mL热蒸馏水,搅拌溶解。
2②磁力搅拌下加入5.0 g Co(NO ) ·6H O,从仪器a加入50%醋酸7.0 mL。冷却至室温后,再从仪器b缓
3 2 2
慢滴入30%双氧水8.0 mL。待反应结束,滤去固体。
③在滤液中加入95%乙醇,静置40分钟。固液分离后,依次用乙醇、乙醚洗涤固体产品,称重。
已知:ⅰ.乙醇、乙醚的沸点分别是78.5 ℃、34.5 ℃;
ⅱ.NaNO 的溶解度数据如下表。
2
温度/℃ 20 30 40 50
溶解度/(g/
84.5 91.6 98.4 104.1
100 g H O)
2
回答下列问题:
(1)仪器a的名称是 ,使用前应 。
(2)Na [Co(NO ) ]中钴的化合价是 ,制备该配合物的化学方程式为 。
3 2 6
(3)步骤①中,用热蒸馏水的目的是 。
(4)步骤③中,用乙醚洗涤固体产品的作用是 。
(5)已知:2K++Na++[Co(NO ) ]3- K Na[Co(NO ) ]↓(亮黄色),足量KCl与1.010 g产品反应生
2 6 2 2 6
成0.872 g亮黄色沉淀,产品纯度为 %。
考向二 以有机物制备、提取、纯化为主线的综合实验
解有机物制备类实验题的思维模型
分析制备流程
(1)有机化合物易挥发,反应中通常采用冷凝回流装置,以减少有机物
的挥发,提高原料的利用率和产物的产率;
依据有机反应特 (2)有机反应通常都是可逆反应,且易发生副反应,因此常使价格较低
点作答 的反应物过量,以提高另一反应物的转化率和产物的产率,同时在实
验中需要控制反应条件,以减少副反应的发生;
(3)根据产品与杂质的性质差异,选择合适的分离、提纯方法
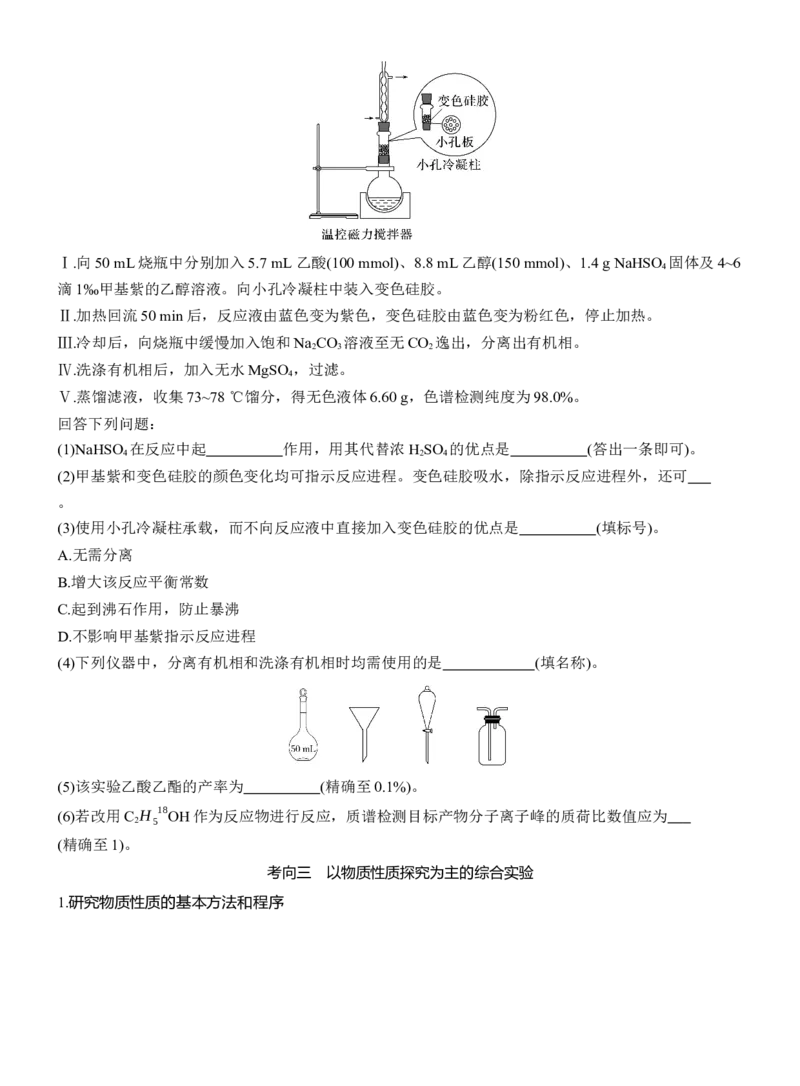
2.(2024·黑吉辽,17)某实验小组为实现乙酸乙酯的绿色制备及反应过程可视化,设计实验方案如下:Ⅰ.向50 mL烧瓶中分别加入5.7 mL 乙酸(100 mmol)、8.8 mL乙醇(150 mmol)、1.4 g NaHSO 固体及4~6
4
滴1‰甲基紫的乙醇溶液。向小孔冷凝柱中装入变色硅胶。
Ⅱ.加热回流50 min后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。
Ⅲ.冷却后,向烧瓶中缓慢加入饱和Na CO 溶液至无CO 逸出,分离出有机相。
2 3 2
Ⅳ.洗涤有机相后,加入无水MgSO ,过滤。
4
Ⅴ.蒸馏滤液,收集73~78 ℃馏分,得无色液体6.60 g,色谱检测纯度为98.0%。
回答下列问题:
(1)NaHSO 在反应中起 作用,用其代替浓H SO 的优点是 (答出一条即可)。
4 2 4
(2)甲基紫和变色硅胶的颜色变化均可指示反应进程。变色硅胶吸水,除指示反应进程外,还可
。
(3)使用小孔冷凝柱承载,而不向反应液中直接加入变色硅胶的优点是 (填标号)。
A.无需分离
B.增大该反应平衡常数
C.起到沸石作用,防止暴沸
D.不影响甲基紫指示反应进程
(4)下列仪器中,分离有机相和洗涤有机相时均需使用的是 (填名称)。
(5)该实验乙酸乙酯的产率为 (精确至0.1%)。
(6)若改用C H 18 OH作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为
2 5
(精确至1)。
考向三 以物质性质探究为主的综合实验
1.研究物质性质的基本方法和程序注意事项:
(1)若探究影响物质性质的因素,首先应确定变量,其次是“定多变一”,即其他因素不变,只改变一
种因素,看这种因素与探究的问题存在怎样的关系。
(2)多角度辩证地看问题
①研究反应物中各微粒的性质(即内因)。
②研究反应条件的影响(如温度、浓度、环境中的其他物质)。
2.物质性质综合实验探究题的审题思路
强化证据意识:
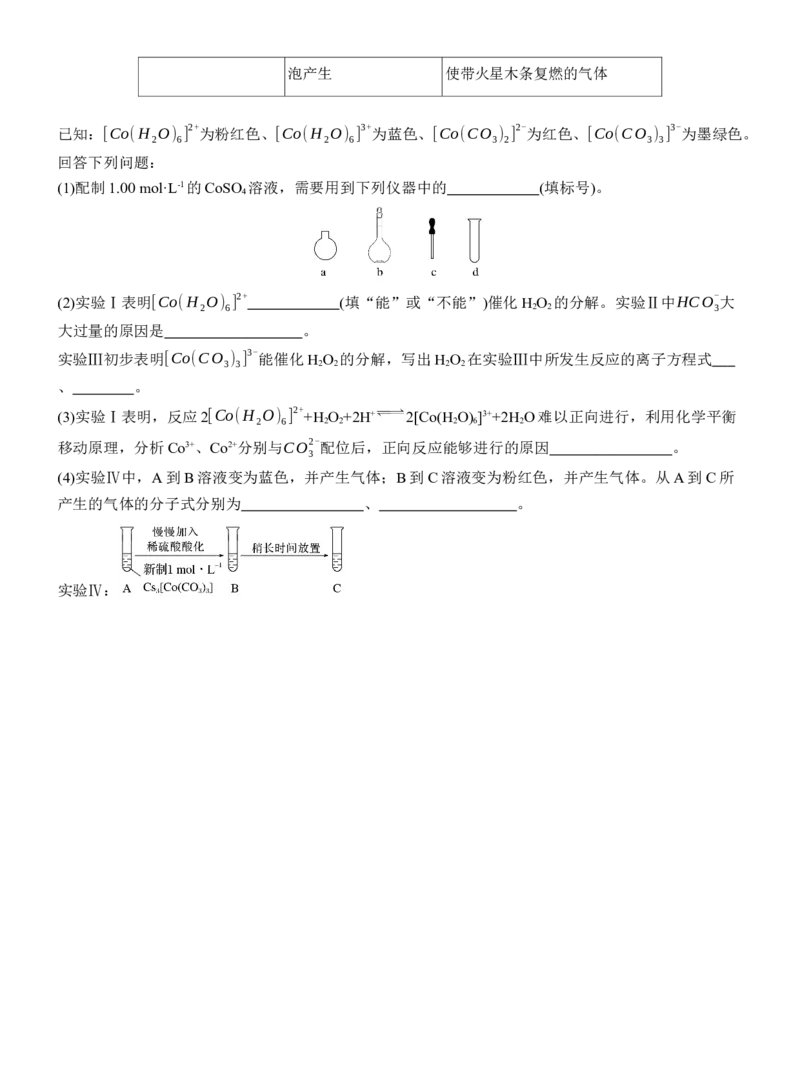
3.(2024·湖北,18)学习小组为探究Co2+、Co3+能否催化H O 的分解及相关性质,室温下进行了实验
2 2
Ⅰ~Ⅳ。
实验Ⅰ 实验Ⅱ 实验Ⅲ
无明显变化 溶液变为红色,伴有气 溶液变为墨绿色,并持续产生能泡产生 使带火星木条复燃的气体
已知:[Co(H O) ] 2+ 为粉红色、[Co(H O) ] 3+ 为蓝色、[Co(CO ) ] 2- 为红色、[Co(CO ) ] 3- 为墨绿色。
2 6 2 6 3 2 3 3
回答下列问题:
(1)配制1.00 mol·L-1的CoSO 溶液,需要用到下列仪器中的 (填标号)。
4
(2)实验Ⅰ表明[Co(H O) ] 2+ (填“能”或“不能”)催化H O 的分解。实验Ⅱ中HCO- 大
2 6 2 2 3
大过量的原因是 。
实验Ⅲ初步表明[Co(CO ) ] 3- 能催化H O 的分解,写出H O 在实验Ⅲ中所发生反应的离子方程式
3 3 2 2 2 2
、 。
(3)实验Ⅰ表明,反应2[Co(H O) ] 2+ +H O +2H+ 2[Co(H O) ]3++2H O难以正向进行,利用化学平衡
2 6 2 2 2 6 2
移动原理,分析Co3+、Co2+分别与CO2-配位后,正向反应能够进行的原因 。
3
(4)实验Ⅳ中,A到B溶液变为蓝色,并产生气体;B到C溶液变为粉红色,并产生气体。从A到C所
产生的气体的分子式分别为 、 。
实验Ⅳ:答案精析
考向一
精练高考真题
1.(1)分液漏斗 检漏 (2)+3
12NaNO +2Co(NO ) +H O +2CH COOH===2Na [Co(NO ) ]+4NaNO +2CH COONa+2H O (3)增加NaNO 的
2 3 2 2 2 3 3 2 6 3 3 2 2
溶解度
(4)加速产品干燥 (5)80
解析 (5)已知:2K++Na++[Co(NO ) ]3- K Na[Co(NO ) ]↓(亮黄色),足量KCl与1.010 g产品反
2 6 2 2 6
0.872
应生成0.872 g亮黄色沉淀,则n(K Na[Co(NO ) ])=n(Na [Co(NO ) ])= mol=0.002 mol,
2 2 6 3 2 6 436
0.808
m(Na [Co(NO ) ])=0.002 mol×404 g·mol-1=0.808 g,产品纯度为 ×100%=80%。
3 2 6 1.010
考向二
精练高考真题
2.(1)催化剂 无有毒气体二氧化硫产生 (2)吸收生成的水,使平衡正向移动,提高乙酸乙酯的产率
(3)AD (4)分液漏斗 (5)73.5% (6)90
解析 (1)乙酸、乙醇中加浓硫酸制乙酸乙酯时,浓硫酸的作用是催化剂和吸水剂,故本实验NaHSO 在反
4
应中起催化剂作用;浓硫酸还具有强氧化性和脱水性,用浓H SO 时可能发生副反应,且浓硫酸的还原产
2 4
物二氧化硫为有毒气体,用NaHSO 代替浓H SO 的优点是副产物少,可绿色制备乙酸乙酯,无有毒气体
4 2 4
二氧化硫产生。(3)若向反应液中直接加入变色硅胶,反应后需要过滤出硅胶,而使用小孔冷凝柱承载则无
需分离,故A正确;平衡常数只与温度有关,使用小孔冷凝柱承载不能增大该反应平衡常数,故B错误;
小孔冷凝柱承载并没有投入溶液中,不能起到沸石作用,不能防止暴沸,故C错误;由题中“反应液由蓝
色变为紫色,变色硅胶由蓝色变为粉红色”可知,若向反应液中直接加入变色硅胶,则变色硅胶由蓝色变
为粉红色,会影响观察反应液由蓝色变为紫色,使用小孔冷凝柱承载不影响甲基紫指示反应进程,故D正
确。(5)由反应CH COOH+CH CH OH CH COOCH CH +H O可知,100 mmol乙酸与150 mmol乙醇
3 3 2 3 2 3 2
反应时,乙醇过量,理论上可获得的乙酸乙酯的质量为0.1 mol×88 g·mol-1=8.8 g,该实验乙酸乙酯的产率
6.60 g×98.0%
为 ×100%=73.5%。(6)若改用C H 18 OH作为反应物进行反应:CH COOH+CH CH 18 OH
8.8 g 2 5 3 3 2
CH CO18OCH CH +H O,生成的乙酸乙酯的摩尔质量为90 g·mol-1,所以质谱检测目标产物分子离
3 2 3 2
子峰的质荷比数值应为90。
考向三
精练高考真题3.(1)bc (2)不能 吸收产生的H+,维持pH,促进反应正向进行
2Co2++10HCO-
+H O ===2[Co(CO ) ]3-
3 2 2 3 3
CO2-
+6H O+4CO ↑ 2H O 2H O+O ↑ (3)实验Ⅲ的现象表明,Co3+、Co2+分别与 3 配位时,
2 2 2 2 2 2
[Co(H O) ] 3+更易与CO2-反应生成[Co(CO ) ] 3- (该反应为快反应),导致[Co(H O) ] 2+几乎不能转化
2 6 3 3 3 2 6
为[Co(CO ) ] 2- ,这样使得[Co(H O) ] 3+ 的浓度减小的幅度远远大于[Co(H O) ] 2+ 减小的幅度,根据化
3 2 2 6 2 6
学平衡移动原理,减小生成物浓度能使化学平衡向正反应方向移动,因此,上述反应能够正向进行
(4)CO O
2 2
解析 实验Ⅰ中无明显变化,证明[Co(H O) ] 2+ 不能催化H O 的分解;实验Ⅱ中溶液变为红色,证明
2 6 2 2
[Co(H O) ] 2+ 易转化为[Co(CO ) ] 2- ;实验Ⅲ中溶液变为墨绿色,说明[Co(H O) ] 3+ 更易与CO2- 反应
2 6 3 2 2 6 3
生成[Co(CO ) ] 3- ,并且初步证明[Co(H O) ] 2+ 在HCO- 的作用下易被H O 氧化为[Co(CO ) ] 3- ;实
3 3 2 6 3 2 2 3 3
验Ⅳ中溶液先变蓝后变红,并且前后均有气体生成,证明在酸性条件下,[Co(CO ) ] 3- 易转化为
3 3
[Co(H O) ] 3+ ,[Co(H O) ] 3+ 氧化性强,可以把H O氧化为O 。(2)CoSO 溶液中存在大量的
2 6 2 6 2 2 4
[Co(H O) ] 2+ ,向其中加入30%的H O 后无明显变化,因此实验Ⅰ表明[Co(H O) ] 2+ 不能催化H O 的
2 6 2 2 2 6 2 2
分解。(4)实验Ⅳ中,A到B溶液变为蓝色,并产生气体,说明发生了[Co(CO ) ] 3- +6H++3H O===
3 3 2
[Co(H O) ] 3+ +3CO ↑;B到C溶液变为粉红色,并产生气体,说明发生了4[Co(H O) ] 3+ +2H O===4[Co
2 6 2 2 6 2
(H O) ]2++O ↑+4H+,因此从A到C所产生的气体的分子式分别为CO 和O 。
2 6 2 2 2