文档内容
专题九 水溶液中的离子平衡
必备知识 解读
一、弱电解质的电离(
弱电解质:包括 弱酸 、 弱碱 、极少数盐(如醋酸铅)、
两性氢氧化物、 水等。)
1.电离度
(1)概念
在一定条件下的弱电解质达到电离平衡时,已经电离的电解质分子数占原电解质总分
子数的分数。
(2)表示方法
α=×100%
也可表示为α=×100%
(3)影响因素
升高温度,电离平衡向右移动,电离度增大;
温度的影响
降低温度,电离平衡向左移动,电离度减小
当弱电解质溶液浓度增大时,电离度减小;
浓度的影响
当弱电解质溶液浓度减小时,电离度增大
2.电离常数
(1)概念:电离平衡的常数叫做电离常数。
(2)表达式
①对于一元弱酸HA:HA H++A-,电离常数K=。
a
②对于一元弱碱BOH:BOH B++OH-,电离常数K=。
b
(3)特点
多元弱酸各级电离常数的大小关系是K 1≫K 2≫K
3
,故其酸性取决于第一步电离。
(4)影响因素
内因:弱电解质本身的性质
外因:电离常数只与温度有关,升高温度,K值增大。
(5)意义
―→―→
如相同条件下常见弱酸的酸性强弱:
HCO>HSO>HPO>HF>HCOOH>CHCOOH>HCO>HS>HClO。
2 2 4 2 3 3 4 3 2 3 2
3.电离常数的四大应用
①判断弱酸(或弱碱)的相对强弱,电离常数越大,酸性(或碱性)越强。
②判断盐溶液的酸性(或碱性)强弱,电离常数越大,对应的盐水解程度越小,酸性(或碱
性)越弱。
③判断复分解反应能否发生,一般符合“强酸制弱酸”规律。④计算弱酸、弱碱溶液中的c(H+)、c(OH-)。有关电离平衡常数的计算(以弱酸HX为例)
已知c(HX)和电离平衡常数,求c(H+)。
HX H+ + X-
起始: c(HX) 0 0
平衡: c(HX)-c(H+) c(H+) c(X-)
则:K==
由于c(H+)的数值很小,可做近似处理:c(HX)-c(H+)≈c(HX),则c(H+)=,代入数值求
解即可。
稀溶液中、弱酸溶液中,c(H+)=,弱碱溶液中c(OH-)=。用来计算PH值。
4.电离度和电离常数的关系α≈或K≈cα2。
5.水电离的c(H+)或c(OH-)的计算
(1)任何情况下,中性溶液:c(H+)=c(OH-),常温下,中性溶液:c(H+)=c(OH-)=
1.0×10-7 mol·L-1。
(2)常温下,酸或碱抑制水的电离,水电离出的c (H+)=c(OH-)=<10-7 mol·L-1。当溶
水
液中的c总(H+)<10-7 mol·L-1时就是水电离出的c(H+),c (H+)=c总(H+),是
水
碱溶液;当溶液中的c(H+)>10-7 mol·L-1时,水电离出的c (H+)=c(OH-)=<10-
水
7 mol·L-1。如pH=2的硫酸中水电离出的c (H+)=c (OH-)==10-12 mol·L-1。
水 水
(3)常温下,可水解的盐促进水的电离,水电离的c(H+)或c(OH-)均大于10-7mol·L-1。盐
是不能电离出H+或OH-的,可水解的盐的溶液中H+和OH-都是水电离的。水电离的H+和
OH-应该是相等的,但是,盐溶液可以是酸性也可是碱性的,也就是说,盐溶液中,水
电离的H+和OH-又是不相等的,这是什么原因?
若给出的c(H+)>10-7 mol·L-1,即为水电离的c(H+),水解显酸性;若给出的c(H+)<10
-7 mol·L-1,就用10-14除以这个浓度即得水电离的c(OH-),水解显碱性;如pH=4
的NHCl中水电离出的c (H+)=10-4 mol·L-1。
4 水
二、水解规律及应用
1.实质
盐电离→→破坏水的电离平衡→水的电离程度增大―→c(H+)≠c(OH-)―→溶液呈碱性、
酸性或中性
2.盐类水解规律
(1)“谁弱谁水解,越弱越水解,谁强显谁性。”如酸性:HCN<CHCOOH,则相同条件下溶
3
液的碱性:NaCN>CHCOONa。
3
(2)弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
①若电离程度小于水解程度,溶液显碱性。如NaHCO 溶液中:HCO H++CO(次要),HCO
3+HO HCO+OH-(主要)。
2 2 3
②若电离程度大于水解程度,溶液显酸性。如NaHSO 溶液中:HSO H++SO(主要),HSO
3
+HO HSO+OH-(次要)。
2 2 3
(3)相同条件下的水解程度:正盐>相应酸式盐,如CO>HCO。
(4)相互促进水解的盐>单独水解的盐>水解相互抑制的盐。如 NH的水解:(NH)CO >
4 2 3
(NH)SO>(NH)Fe(SO)。
4 2 4 4 2 4 2
(5)FeCl 、NHCl、CHCOONa等溶液中由于自己不能电离出H+和OH-,它们的水溶液中
3 4 3
的H+和OH-都是由水电离出来的。能水解的离子都能破坏水的电离平衡。
3.盐类水解的一些应用
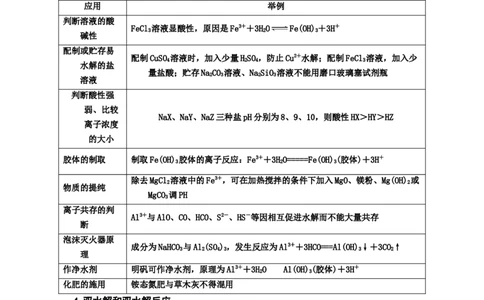
应用 举例
判断溶液的酸
FeCl 溶液显酸性,原因是Fe3++3HO Fe(OH)+3H+
3 2 3
碱性
配制或贮存易
配制CuSO 溶液时,加入少量HSO,防止Cu2+水解;配制FeCl 溶液,加入少
4 2 4 3
水解的盐
量盐酸;贮存NaCO 溶液、NaSiO 溶液不能用磨口玻璃塞试剂瓶
2 3 2 3
溶液
判断酸性强
弱、比较
NaX、NaY、NaZ三种盐pH分别为8、9、10,则酸性HX>HY>HZ
离子浓度
的大小
胶体的制取 制取Fe(OH) 胶体的离子反应:Fe3++3HO=====Fe(OH)(胶体)+3H+
3 2 3
除去MgCl 溶液中的Fe3+,可在加热搅拌的条件下加入MgO、镁粉、Mg(OH) 或
2 2
物质的提纯
MgCO 调PH
3
离子共存的判
Al3+与AlO、CO、HCO、S2-、HS-等因相互促进水解而不能大量共存
断
泡沫灭火器原
成分为NaHCO 与Al(SO),发生反应为Al3++3HCO===Al(OH)↓+3CO↑
3 2 4 3 3 2
理
作净水剂 明矾可作净水剂,原理为Al3++3HOAl(OH)(胶体)+3H+
2 3
化肥的施用 铵态氮肥与草木灰不得混用
4.双水解和双水解反应
熟记下列因双水解不能大量共存的离子组合
(1)Al3+与HCO、CO、AlO、SiO、HS-、S2-、ClO-。
(2)Fe3+与HCO、CO、AlO、SiO、ClO-。
(3)NH与SiO、AlO。
[特别提醒]
①NH与CHCOO-、HCO虽能发生双水解,但不能发生双水解反应,能大量共存。②Fe3+在
3
中性条件下已完全水解。
5.判断盐溶液蒸干时所得产物的5种类型(1)盐溶液水解生成难挥发性酸和酸根阴离子易水解的强碱盐,蒸干后一般得原物质,如
CuSO(aq)蒸干得CuSO(s);NaCO(aq)蒸干得NaCO(s)。Al(SO) 蒸干后得Al(SO)
4 4 2 3 2 3 2 4 3 2 4 3
(2)盐溶液水解生成易挥发性酸时,蒸干灼烧后一般得到对应的氧化物,如 AlCl(aq)蒸干
3
得Al(OH),灼烧得AlO。
3 2 3
(3)考虑盐受热时是否分解。Ca(HCO) 、NaHCO 、KMnO 、NHCl固体受热易分解,因此蒸干
3 2 3 4 4
灼烧后分别为Ca(HCO)―→CaCO(CaO);NaHCO―→NaCO ;KMnO―→KMnO 和MnO ;
3 2 3 3 2 3 4 2 4 2
NHCl―→NH↑+HCl↑。
4 3
(4)还原性盐在蒸干时会被O 氧化。如NaSO(aq)蒸干得NaSO(s)。
2 2 3 2 4
(5)弱酸的铵盐蒸干后无固体。如NHHCO、(NH)CO。
4 3 4 2 3
三、沉淀溶解平衡K
SP
1.溶度积和离子积
以AB(s) mAn+(aq)+nBm-(aq)为例
m n
溶度积 离子积
概念 沉淀溶解的平衡常数 溶液中有关离子浓度幂的乘积
符号 K Q
sp c
表达 K sp (A m B n )= c m ( A n + )· c n ( B m - ),式中的浓度都是平衡 Q c (A m B n )= c m ( A n + )· c n ( B m - ),
式 浓度 式中的浓度都是任意浓度
判断在一定条件下沉淀能否生成或溶解
①Q>K :溶液过饱和,有沉淀析出
c sp
应用
②Q=K :溶液饱和,处于平衡状态
c sp
③QC(H+)>C(CHCOO-)>C(OH-)
3 3 3
一元弱碱:NH.HO溶液:C(NH.HO)>C(OH-)>C(NH+)>C(H+)
3 2 3 2 4
2.弱酸酸式盐:
碱性酸式盐:如NaHCO 溶液:C(Na+)>C(HCO-)>C(OH-)>C(HCO)>C(CO2-)
3 3 2 3 3
酸性酸式盐:如NaHSO 溶液:C(Na+)>C(HSO-)>C(H+)>C(SO2-)>C(OH-)>C(HSO)
3 3 3 2 3
3.多元弱酸的正盐溶液:多元弱酸的酸根离子分步水解,水解程度逐级减弱。如在 Na CO
2 3
溶液中:c(Na+)>c(CO)>c(OH-)>c(HCO)>c(H+)。
类型二 两种电解质混合溶液中
(1) 等体积、等浓度的CHCOOH和CHCOONa溶液
3 3
(溶液呈酸性,说明CHCOOH电离程度大于CHCOO-水解程度):
3 3
c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+)>c(OH-)
3 3
(2) 等体积、等浓度的NHCl和NH·HO溶液(溶液呈碱性,说明NH·HO电离程度大于
4 3 2 3 2
NH+水解程度): c(NH+)>(Cl-)>c(NH·HO)>c(OH-)>c(H+)
4 4 3 2
(3) 等体积、等浓度的NaCN和HCN溶液(溶液呈碱性,说明CN-水解程度大于HCN电离程度):c(HCN)>(Na+)>c(CN-)>c(OH-)>c(H+)
(4)等体积、等浓度的NaCO 与NaHCO 混合溶液(CO2-一级水解远大于二级水解):
2 3 3 3
c(Na+)>c(HCO-)>C(CO2-)>C(OH-)>C(H+)
3 3
(5)向0.2 mol·L-1NaHCO 溶液中加入等体积0.1 mol·L-1
3
NaOH溶液:c(Na+)>c(HCO-)>c(CO2-)>c(OH-)>c(H+)
3 3
(6)向0.2 mol·L―1NHCl溶液中加入等体积0.1 mol·L-1
4
NaOH溶液,得到pH>7的溶液c(Cl-)>c(NH+)>c(Na+)>c(NH·HO)>c(OH-)
4 3 2
(7)0.2 mol·L-1HCl与0.1 mol·L-1NaAlO 溶液等体积混合:
2
c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-)
(8)0.1 mol·L-1CHCOONa溶液与0.1 mol·L-1HCl溶液等
3
体积混合:c(Na+)=c(Cl-)>C(H+)>c(CHCOO-)>c(OH-)
3
类型三 不同溶液中同一粒子浓度的比较
不同溶液要看溶液中其他离子对该离子的影响。
如在相同物质的量浓度的下列溶液中:①NH Cl;②CH COONH ;③NH HSO ,c(NH)
4 3 4 4 4
由大到小的顺序为③>①>②。
三、中和滴定中图像
1.酸碱中和滴定曲线分析
(1).滴定曲线上的特殊点的分析
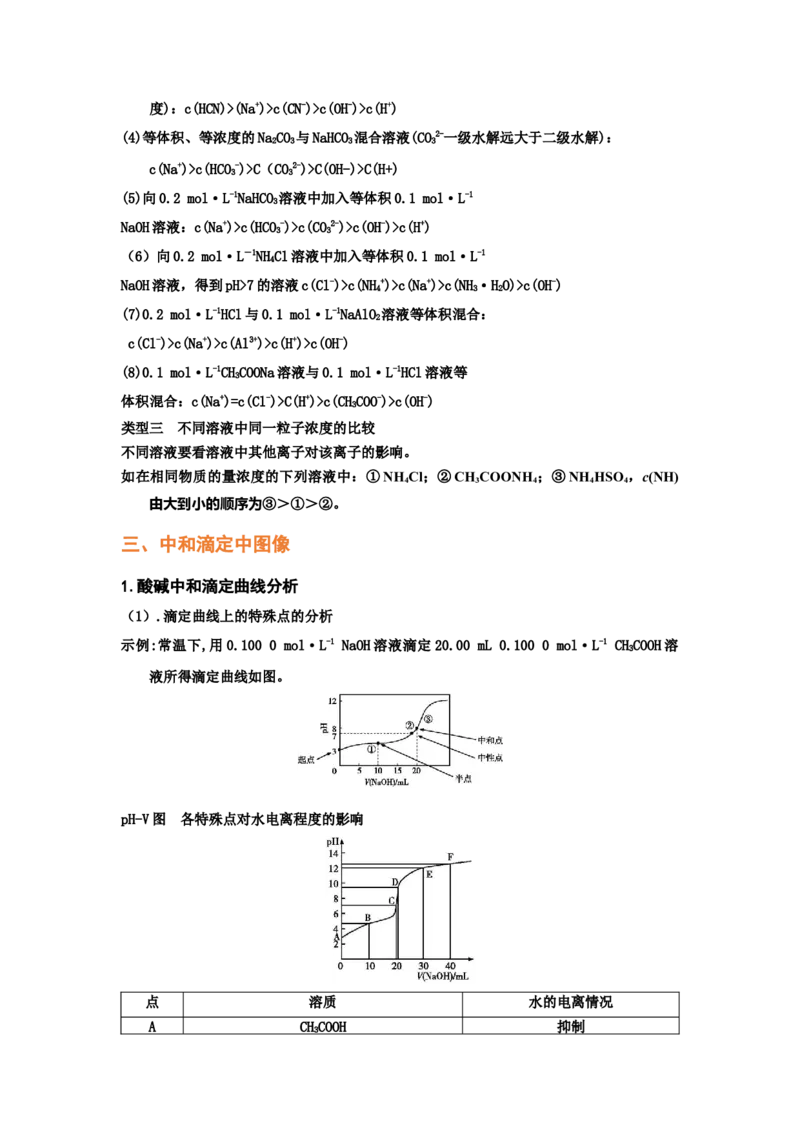
示例:常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 CHCOOH溶
3
液所得滴定曲线如图。
pH-V图 各特殊点对水电离程度的影响
点 溶质 水的电离情况
A CHCOOH 抑制
3B CHCOOH、CHCOONa 抑制
3 3
C CHCOOH、CHCOONa 正常电离
3 3
D CHCOONa 只促进
3
E CHCOONa、NaOH 抑制
3
F CHCOONa、NaOH 抑制
3
根据图中pH数据,图中A、B、C、D、E、F各点对应的溶液中水的电离程度大小图示如图:
pH-V图 各特殊点粒子浓度大小关系
点 溶质 离子浓度大小比较
A CHCOOH c(H+)>c(CHCOO-)>c(OH-)
3 3
CHCOOH、
3
B(1∶1) c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
CHCOONa
3
CHCOOH、
3
C(pH=7) c(CHCOO-)=c(Na+)>c(H+)=c(OH-)
3
CHCOONa
3
D CHCOONa c(Na+)>c(CHCOO-)>c(OH-)>c(H+)
3 3
E(2∶1) CHCOONa、NaOH c(Na+)>c(CHCOO-)>c(OH-)>c(H+)
3 3
F(1∶1) CHCOONa、NaOH c(Na+)>c(OH-)>c(CHCOO-)>c(H+)
3 3
2.正态分布曲线
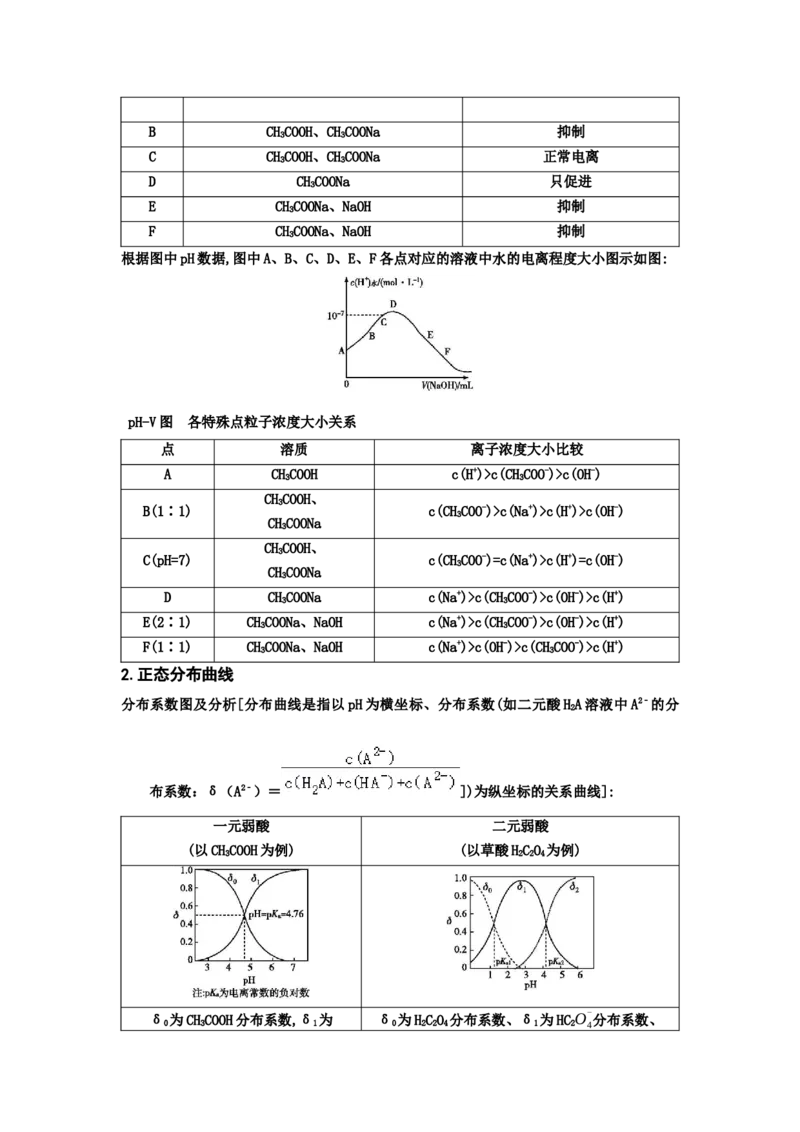
分布系数图及分析[分布曲线是指以pH为横坐标、分布系数(如二元酸HA溶液中A2﹣的分
2
布系数:δ(A2﹣)= ])为纵坐标的关系曲线]:
一元弱酸 二元弱酸
(以CHCOOH为例) (以草酸HCO 为例)
3 2 2 4
δ 为CHCOOH分布系数,δ 为 δ 为HCO 分布系数、δ
为HCO-
分布系数、
0 3 1 0 2 2 4 1 2 4CHCOO-分布系数 δ 为CO2- 分布系数
3 2 2 4
随着pH增大,溶质分子浓度不断减小,离子浓度逐渐增大,酸根离子增多。根据分布系数
可以书写一定pH时所发生反应的离子方程式
同一pH条件下可以存在多种溶质微粒。根据在一定pH的微粒分布系数和酸的浓度,就可
以计算各成分在该pH时的平衡浓度
3 . p H - - 分布系数 δ - - 滴加 NaO H 溶液体积 V
NaOH
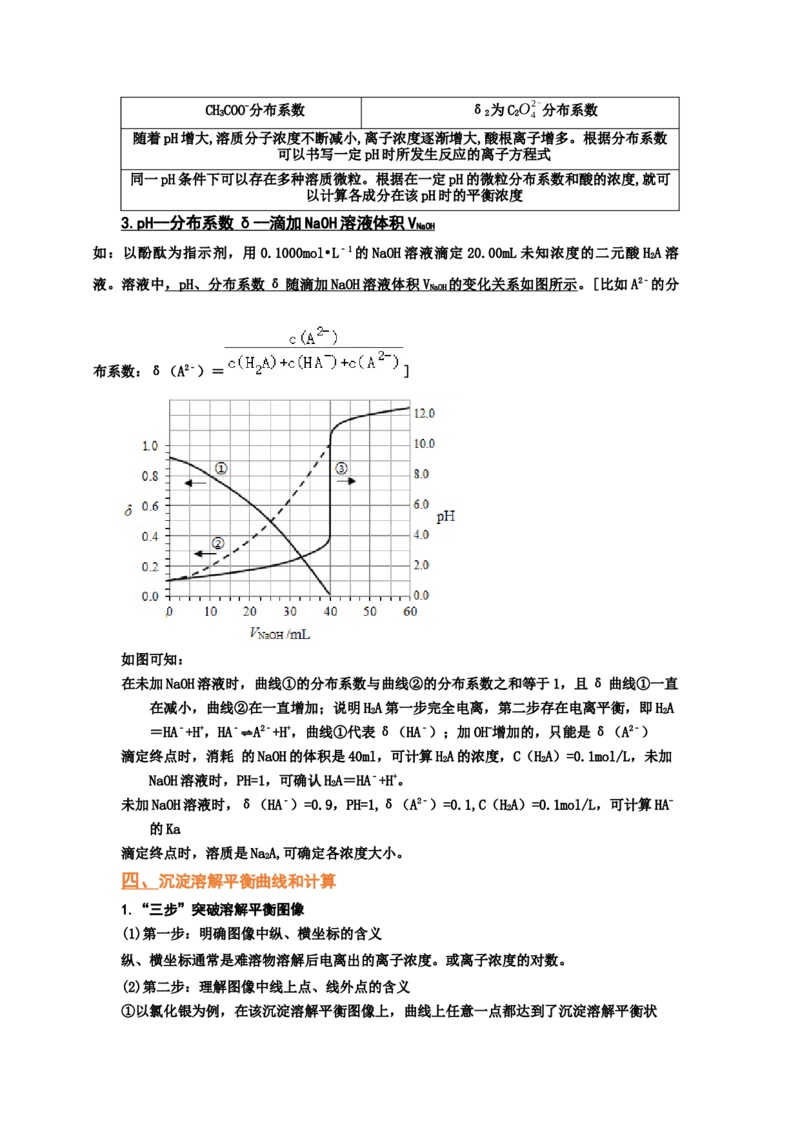
如:以酚酞为指示剂,用0.1000mol•L﹣1的NaOH溶液滴定20.00mL未知浓度的二元酸HA溶
2
液。溶液中 , pH 、分布系数 δ 随滴加 NaOH 溶液体积 V 的变化关系如图所示。[比如A2﹣的分
NaOH
布系数:δ(A2﹣)= ]
如图可知:
在未加NaOH溶液时,曲线①的分布系数与曲线②的分布系数之和等于1,且δ曲线①一直
在减小,曲线②在一直增加;说明HA第一步完全电离,第二步存在电离平衡,即HA
2 2
=HA﹣+H+,HA﹣ A2﹣+H+,曲线①代表δ(HA﹣);加OH-增加的,只能是δ(A2﹣)
⇌
滴定终点时,消耗 的NaOH的体积是40ml,可计算HA的浓度,C(HA)=0.1mol/L,未加
2 2
NaOH溶液时,PH=1,可确认HA=HA﹣+H+。
2
未加NaOH溶液时,δ(HA﹣)=0.9,PH=1,δ(A2﹣)=0.1,C(HA)=0.1mol/L,可计算HA-
2
的Ka
滴定终点时,溶质是NaA,可确定各浓度大小。
2
四、沉淀溶解平衡曲线和计算
1.“三步”突破溶解平衡图像
(1)第一步:明确图像中纵、横坐标的含义
纵、横坐标通常是难溶物溶解后电离出的离子浓度。或离子浓度的对数。
(2)第二步:理解图像中线上点、线外点的含义
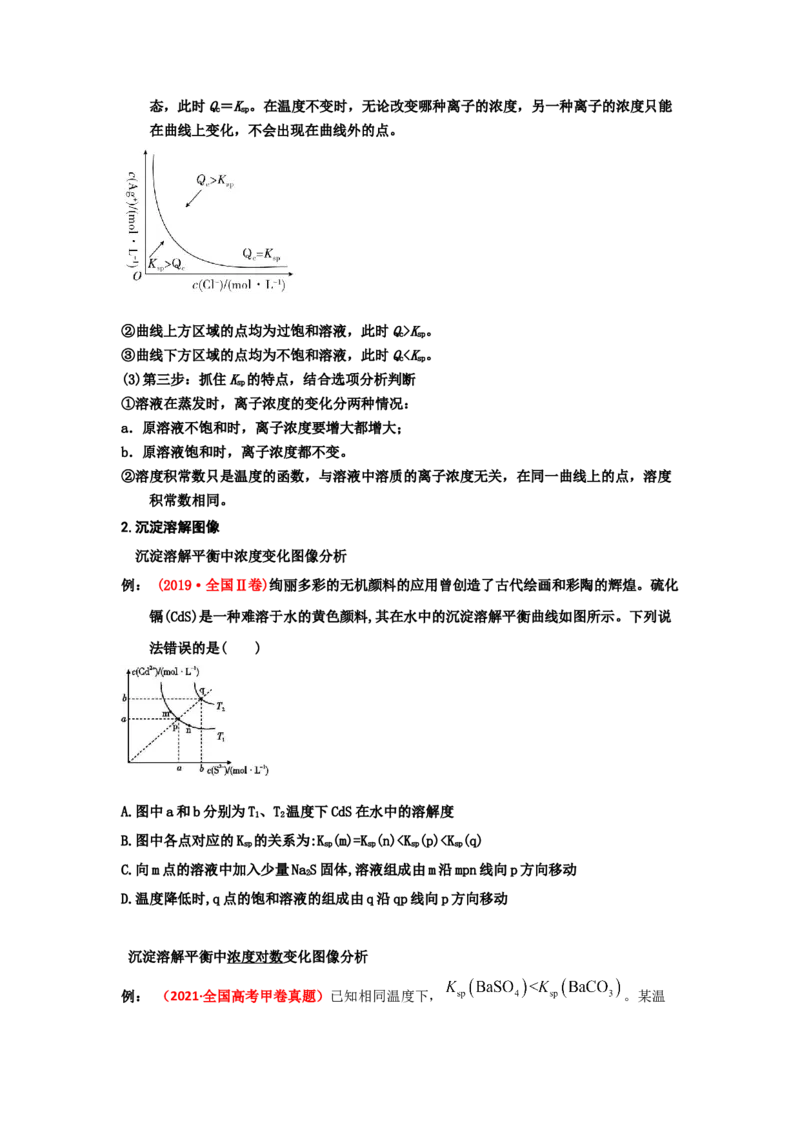
①以氯化银为例,在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解平衡状态,此时Q=K。在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能
c sp
在曲线上变化,不会出现在曲线外的点。
②曲线上方区域的点均为过饱和溶液,此时Q>K。
c sp
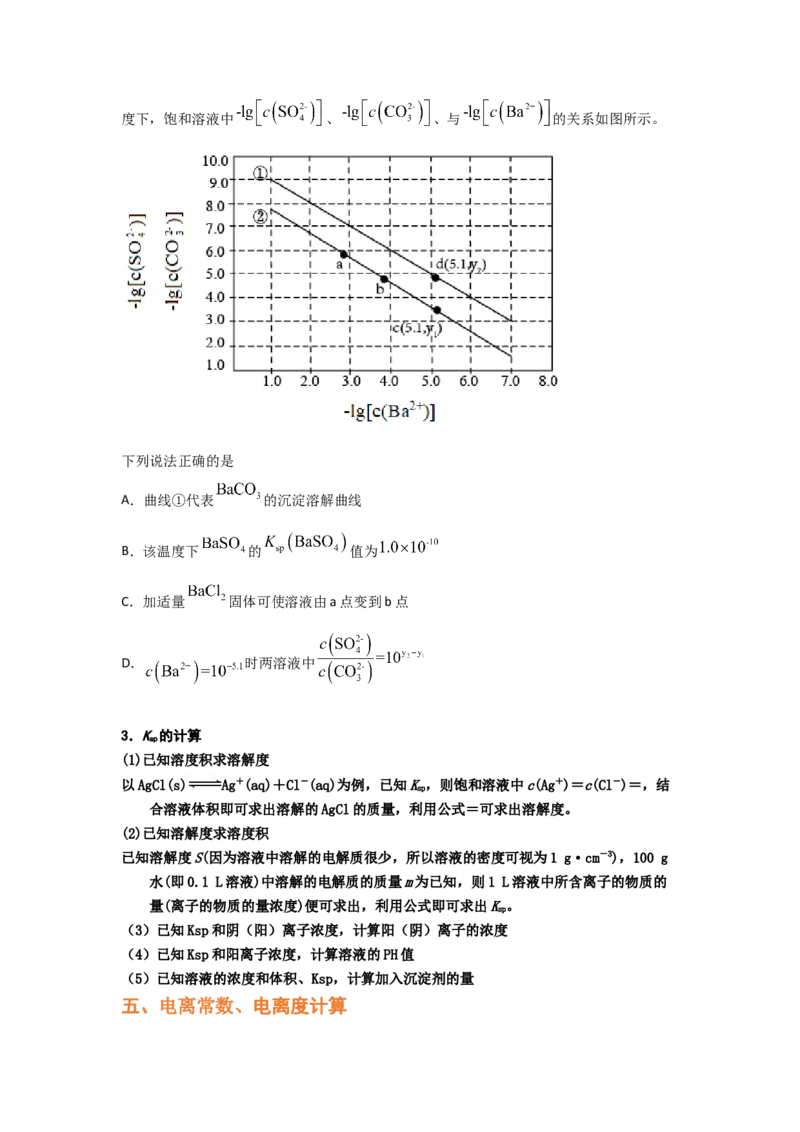
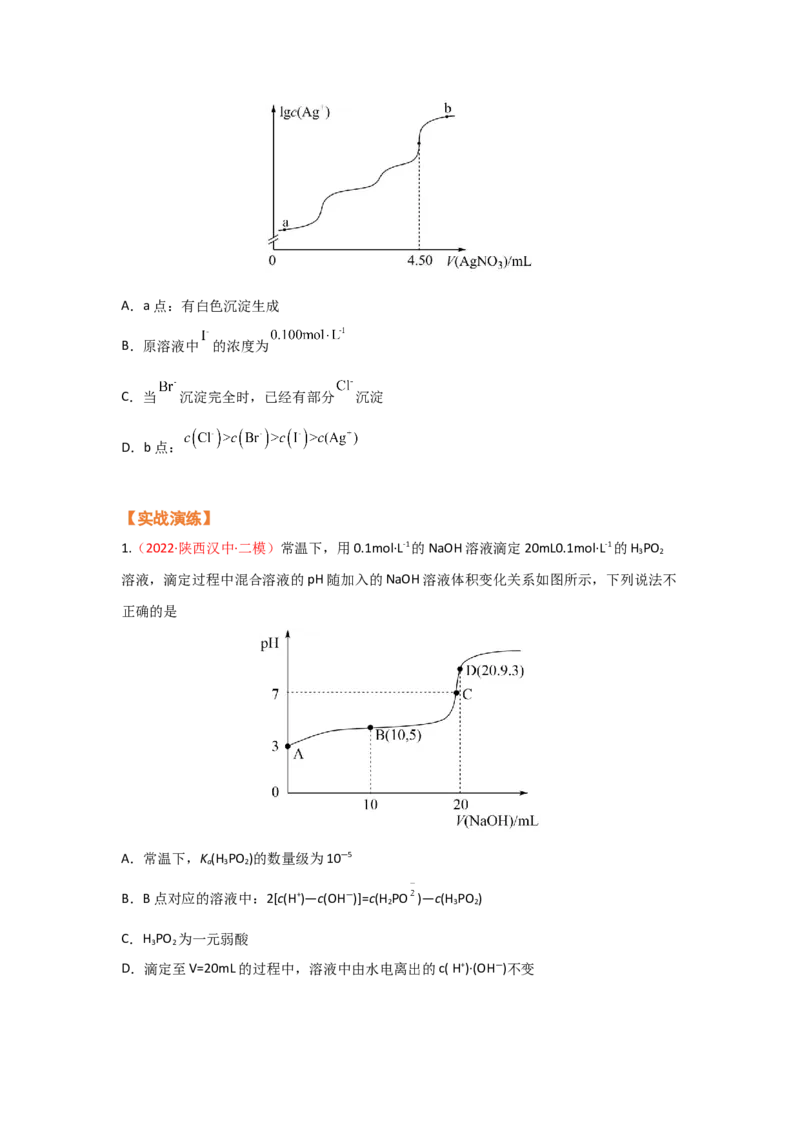
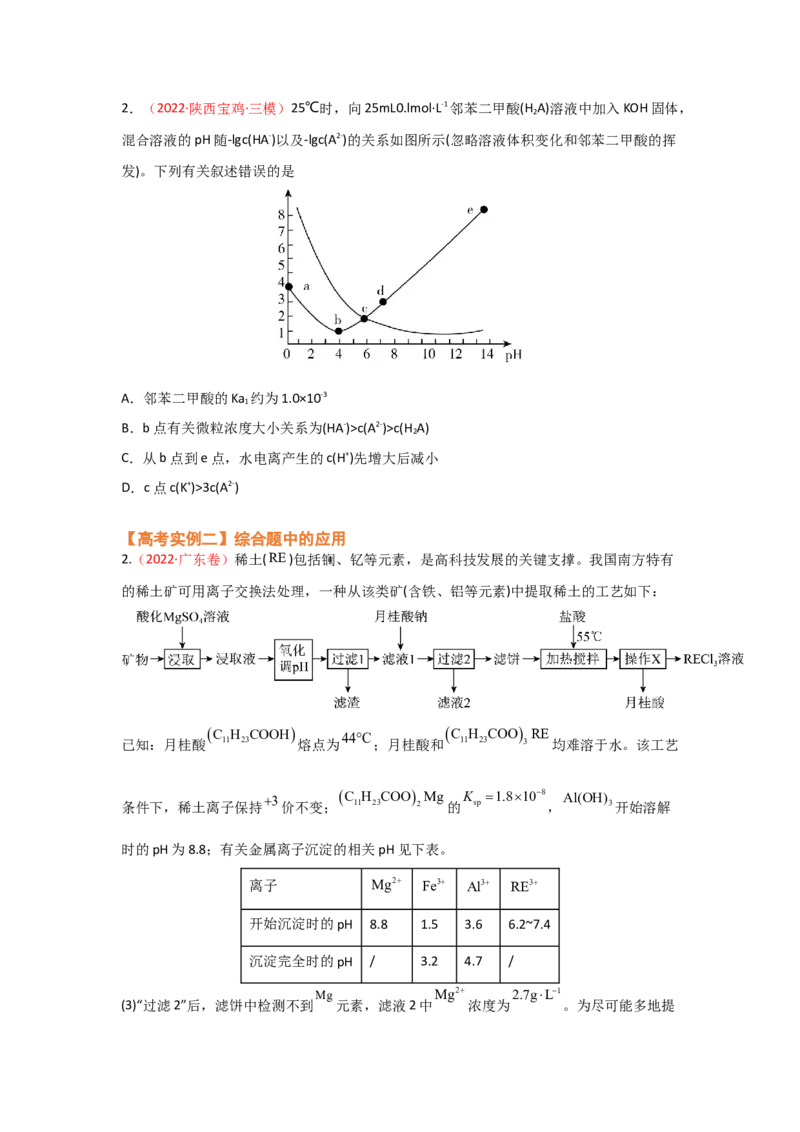
③曲线下方区域的点均为不饱和溶液,此时Qc(A2-)>c(H A)
2
C.从b点到e点,水电离产生的c(H+)先增大后减小
D.c点c(K+)>3c(A2-)
【高考实例二】综合题中的应用
2.(2022·广东卷)稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有
的稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
C H COOH 44C C H COO RE
已知:月桂酸 11 23 熔点为 ;月桂酸和 11 23 3 均难溶于水。该工艺
3 C H COO Mg K 1.8108 Al(OH)
条件下,稀土离子保持 价不变; 11 23 2 的 sp , 3开始溶解
时的pH为8.8;有关金属离子沉淀的相关pH见下表。
离子 Mg2 Fe3 Al3 RE3
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
Mg Mg2 2.7gL1
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提c
C H
COO-
取RE3,可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 11 23 低于
molL1
_______ (保留两位有效数字)。
【实战演练】
1.(2022·江西九江·二模)以碳酸锰铜矿(主要成分为MnCO 、CuCO ,还含有Fe O 、FeO
3 3 2 3
等杂质)为原料制备硫酸锰的一种工艺流程如下:
(2)加入MnCO 调节pH=3.3时可以将Fe3+转化为Fe(OH) 而除去,该反应的离子方程式为
3 3
_______。
(3)“沉铜"时,若滤液中c(Mn2+)=0.21mol·L-1,向其中缓慢通入氨气,为了使铜离子完全沉淀
而又避免生成Mn(OH) ,应控制pH的范围为_______。[已知:常温下,Ksp[Cu(OH) ]=1×10-
2 2
20,Ksp[Mn(OH) ]=2.1×10-13,离子浓度小于或等于10-5mol/L可视为沉淀完全]
2
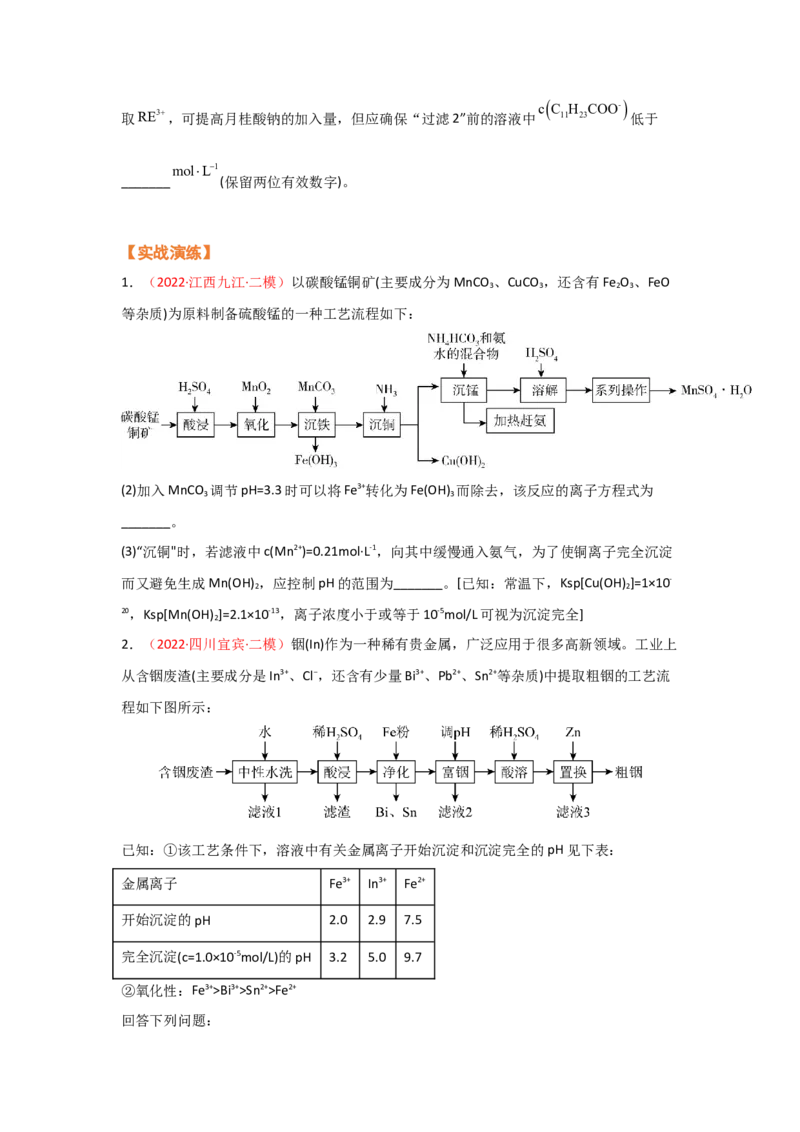
2.(2022·四川宜宾·二模)铟(In)作为一种稀有贵金属,广泛应用于很多高新领域。工业上
从含铟废渣(主要成分是In3+、Cl−,还含有少量Bi3+、Pb2+、Sn2+等杂质)中提取粗铟的工艺流
程如下图所示:
已知:①该工艺条件下,溶液中有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子 Fe3+ In3+ Fe2+
开始沉淀的pH 2.0 2.9 7.5
完全沉淀(c=1.0×10-5mol/L)的pH 3.2 5.0 9.7
②氧化性:Fe3+>Bi3+>Sn2+>Fe2+
回答下列问题:(1)“中性水洗”时,含铟废渣中金属阳离子转化为氢氧化物或氧化物。Sn2+转化为SnO的离
子方程式是_______,该过程需加入大量水并加热,目的是_______。
(2)“酸浸”时,得到对应的硫酸盐,则“滤渣”的主要成分是_______(填化学式)。
(3)“净化”时,生成Bi的离子方程式是_______。
(4)“富铟”时,“调pH”应控制的pH范围是_______。
(5)利用上述表格数据,计算In(OH) 的K =_______。
3 sp
(6)实验室检验“滤液2”中主要金属阳离子的方法是_______。