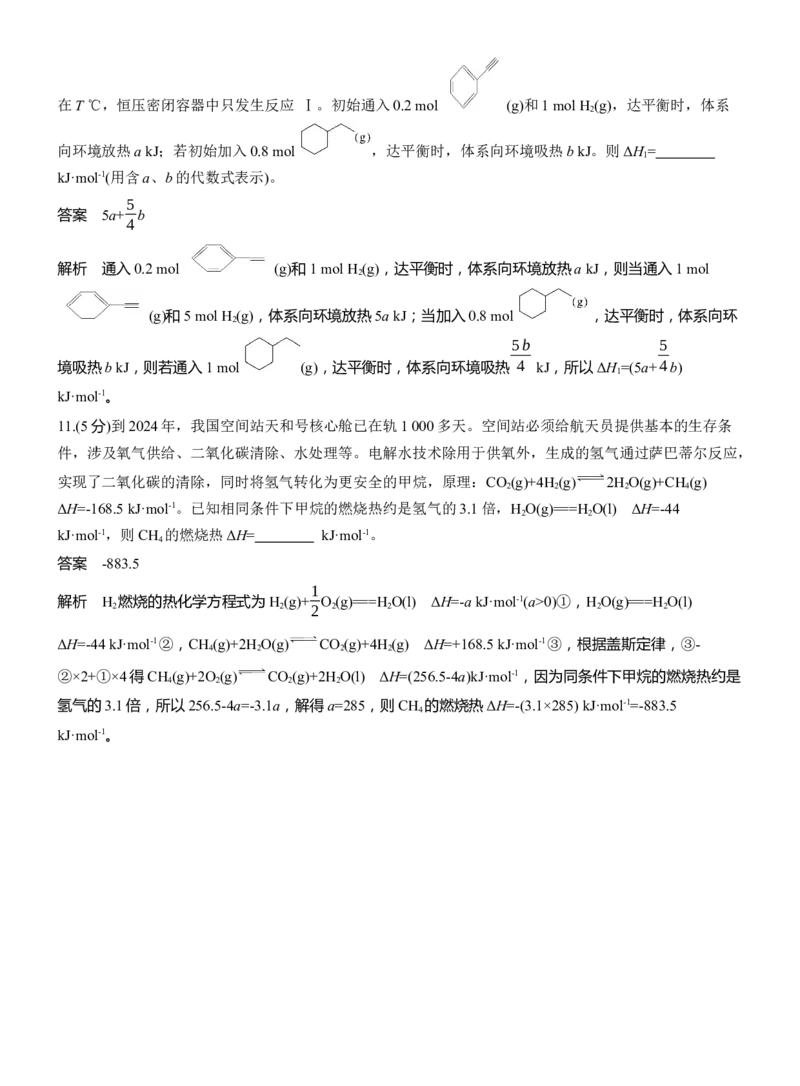文档内容
热化学方程式的书写与焓变的计算
1.计算反应热的方法
(1)根据物质能量的变化计算
①ΔH=E(生成物的总能量)-E(反应物的总能量)
②从活化能角度分析计算
ΔH=E(正反应的活化能)-E(逆反应的活化能)
a a
(2)根据键能数据计算
ΔH=E(反应物的键能总和)-E(生成物的键能总和)
(3)根据盖斯定律计算
①思维模型
②反应热计算技巧
同边加号异边负,焓的变化跟系数。
2.热化学方程式书写注意事项
(1)注意ΔH符号及单位:逆反应的反应热与正反应的反应热数值相等,但符号相反。
(2)注意热化学方程式中的化学计量数,如果化学计量数加倍,则ΔH也要加倍。
(3)注意物质的聚集状态:气体用“g”,液体用“l”,固体用“s”,溶液用“aq”。对于具有同素异形体
的物质,除了要注明聚集状态外,还要注明物质的名称。
(4)热化学方程式中可不写反应条件,不用“↑”和“↓”。
1.[2024·安徽,17(1)]C H 氧化脱氢反应:2C H (g)+O (g)===2C H (g)+2H O(g) ΔH =-209.8 kJ·mol-1
2 6 2 6 2 2 4 2 1
C H (g)+CO (g)===C H (g)+H O(g)+CO(g) ΔH =+178.1 kJ·mol-1
2 6 2 2 4 2 2
计算:2CO(g)+O (g)===2CO (g) ΔH = kJ·mol-1 。
2 2 3
答案 -566
解析 将两个反应依次标号为反应①和反应②,反应①-反应②×2可得目标反应,根据盖斯定律知
ΔH =ΔH -2ΔH =(-209.8 kJ·mol-1 -178.1 kJ·mol-1 ×2)=-566 kJ·mol-1 。
3 1 22.[2024·湖南,18(1)]丙烯腈(CH ==CHCN)是一种重要的化工原料。工业上以N 为载气,用TiO 作催化
2 2 2
剂生产CH ==CHCN的流程如下:
2
已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定;
②反应釜Ⅰ中发生的反应:
ⅰ:HOCH CH COOC H (g)―→CH ==CHCOOC H (g)+H O(g) ΔH
2 2 2 5 2 2 5 2 1
③反应釜Ⅱ中发生的反应:
ⅱ:CH ==CHCOOC H (g)+NH (g)―→CH ==CHCONH (g)+C H OH(g) ΔH
2 2 5 3 2 2 2 5 2
ⅲ:CH ==CHCONH (g)―→CH ==CHCN(g)+H O(g) ΔH
2 2 2 2 3
④在此生产条件下,酯类物质可能发生水解。
总反应HOCH CH COOC H (g)+NH (g)―→CH ==CHCN(g)+C H OH(g)+2H O(g) ΔH=
2 2 2 5 3 2 2 5 2
(用含ΔH 、ΔH 、和ΔH 的代数式表示)。
1 2 3
答案 ΔH +ΔH +ΔH
1 2 3
解析 根据盖斯定律,由反应ⅰ+反应ⅱ+反应ⅲ得HOCH CH COOC H (g)+NH (g)―→CH ==CHCN(g)
2 2 2 5 3 2
+C H OH(g)+2H O(g),故ΔH=ΔH +ΔH +ΔH 。
2 5 2 1 2 3
3.[2024·河北,17(1)①]硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:SO (g)+Cl (g)
2 2
SO Cl (g) ΔH=-67.59 kJ·mol-1。
2 2
若正反应的活化能为E kJ·mol-1,则逆反应的活化能E = kJ·mol-1(用含E 的代数式表示)。
正 逆 正
答案 E +67.59
正
解析 根据反应热与活化能E 和E 关系ΔH=E -E 可知,该反应的E =[E -(-67.59)]kJ·mol-1=(E
正 逆 正 逆 逆 正 正
+67.59) kJ·mol-1。
1 3
4.[2023·新课标卷,29(1)]根据图示数据计算反应 N (g)+ H (g)===NH (g)的ΔH= kJ·mol-1。
2 2 2 2 3
答案 -45解析 在化学反应中,断开化学键要消耗能量,形成化学键要释放能量,反应的焓变等于反应物的键能总
1 3
和与生成物的键能总和的差,因此,由图中数据可知,反应 N (g)+ H (g)===NH (g)的ΔH=(473+654-436-
2 2 2 2 3
397-339) kJ·mol-1=-45 kJ·mol-1。
5.[2023·湖南,16(1)]已知下列反应的热化学方程式:
21
①C H C H (g)+ O (g)===8CO (g)+5H O(g) ΔH =-4 386.9 kJ·mol-1
6 5 2 5 2 2 2 2 1
②C H CH==CH (g)+10O (g)===8CO (g)+4H O(g) ΔH =-4 263.1 kJ·mol-1
6 5 2 2 2 2 2
1
③H (g)+ O (g)===H O(g) ΔH =-241.8 kJ·mol-1
2 2 2 2 3
计算反应④C H C H (g) C H CH==CH (g)+H (g)的ΔH = kJ·mol-1。
6 5 2 5 6 5 2 2 4
答案 +118
解析 根据盖斯定律,将①-②-③可得C H C H (g) C H CH==CH (g)+H (g) ΔH =-4 386.9 kJ·mol-1-(-4
6 5 2 5 6 5 2 2 4
263.1 kJ·mol-1)-(-241.8 kJ·mol-1)=+118 kJ·mol-1。
6.[2023·河北,17(1)]已知:1 mol物质中的化学键断裂时所需能量如下表。
物质 N (g) O (g) NO(g)
2 2
能量/kJ 945 498 631
恒温下,将1 mol空气(N 和O 的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容
2 2
密闭容器中,假设体系中只存在如下两个反应:
ⅰ.N (g)+O (g) 2NO(g) K ΔH
2 2 1 1
ⅱ.2NO(g)+O (g) 2NO (g) K ΔH =-114 kJ·mol-1
2 2 2 2
ΔH = kJ·mol-1。
1
答案 +181
解析 ΔH =反应物总键能-生成物总键能=(945 kJ·mol-1+498 kJ·mol-1)-2×631 kJ·mol-1=+181 kJ·mol-1。
1
题型突破练 [分值:50 分]
1.(4分)(2023·广东湛江模拟)我国在二氧化碳催化加氢合成甲醇上取得了突破性进展,有关反应如下:
反应ⅰ:CO (g)+3H (g) CH OH(g)+H O(g) ΔH=-49.6 kJ·mol-1
2 2 3 2
反应ⅱ:CO (g)+H (g) CO(g)+H O(g) ΔH=+41 kJ·mol-1
2 2 2
CO(g)和H (g)合成CH OH(g)的热化学方程式为 。
2 3
答案 CO(g)+2H (g) CH OH(g) ΔH=-90.6 kJ·mol-1
2 3
2.(4分)实验室可用KClO 分解制取O ,KClO 受热分解的反应分两步进行:
3 2 3Ⅰ.4KClO (s)===3KClO (s)+KCl(s)
3 4
Ⅱ.KClO (s)===KCl(s)+2O (g)
4 2
已知:
1
①K(s)+ Cl (g)===KCl(s) ΔH=-437 kJ·mol-1
2 2
1 3
②K(s)+ Cl (g)+ O (g)===KClO (s) ΔH=-398 kJ·mol-1
2 2 2 2 3
1
③K(s)+ Cl (g)+2O (g)===KClO (s) ΔH=-433 kJ·mol-1
2 2 2 4
则反应4KClO (s)===3KClO (s)+KCl(s)的ΔH= kJ·mol-1。
3 4
答案 -144
1 1 3
解析 ①K(s)+ Cl (g)===KCl(s) ΔH=-437 kJ·mol-1;②K(s)+ Cl (g)+ O (g)===KClO (s) ΔH=-398
2 2 2 2 2 2 3
1
kJ·mol-1;③K(s)+ Cl (g)+2O (g)===KClO (s) ΔH=-433 kJ·mol-1,依据盖斯定律将①+③×3-②×4得到
2 2 2 4
4KClO (s)===3KClO (s)+KCl(s)的ΔH=-144 kJ·mol-1。
3 4
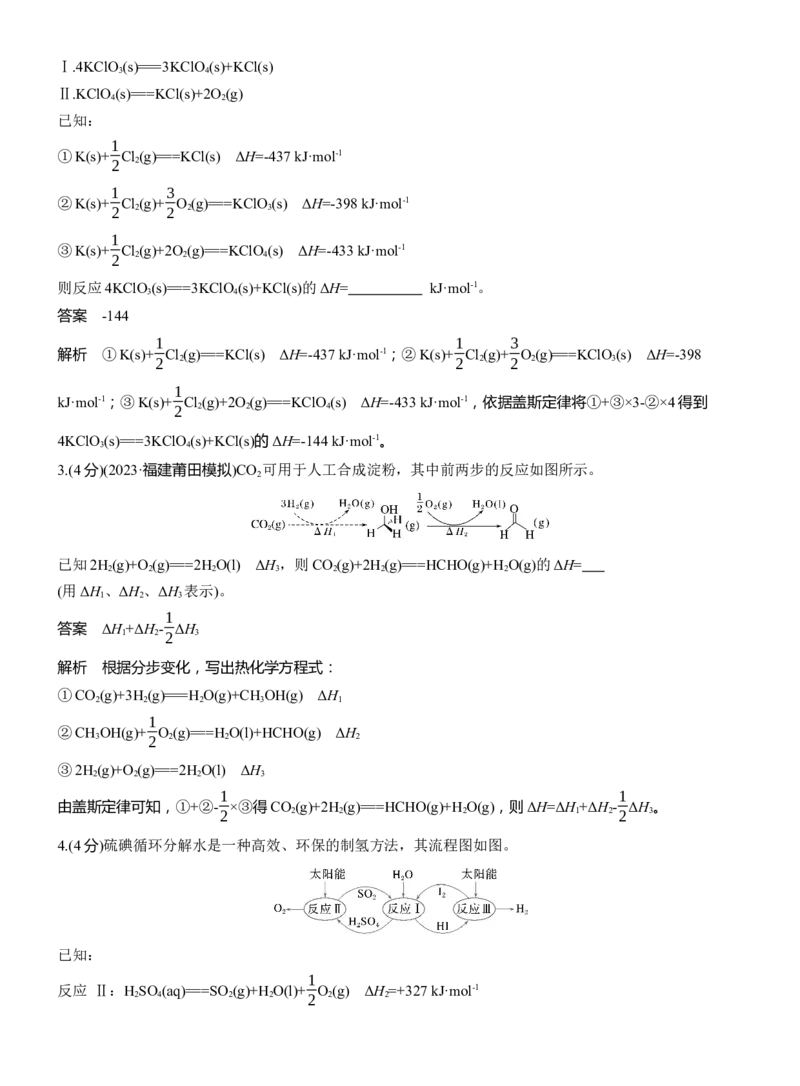
3.(4分)(2023·福建莆田模拟)CO 可用于人工合成淀粉,其中前两步的反应如图所示。
2
已知2H (g)+O (g)===2H O(l) ΔH ,则CO (g)+2H (g)===HCHO(g)+H O(g)的ΔH=
2 2 2 3 2 2 2
(用ΔH 、ΔH 、ΔH 表示)。
1 2 3
1
答案 ΔH +ΔH - ΔH
1 2 2 3
解析 根据分步变化,写出热化学方程式:
①CO (g)+3H (g)===H O(g)+CH OH(g) ΔH
2 2 2 3 1
1
②CH OH(g)+ O (g)===H O(l)+HCHO(g) ΔH
3 2 2 2 2
③2H (g)+O (g)===2H O(l) ΔH
2 2 2 3
1 1
由盖斯定律可知,①+②- ×③得CO (g)+2H (g)===HCHO(g)+H O(g),则ΔH=ΔH +ΔH - ΔH 。
2 2 2 2 1 2 2 3
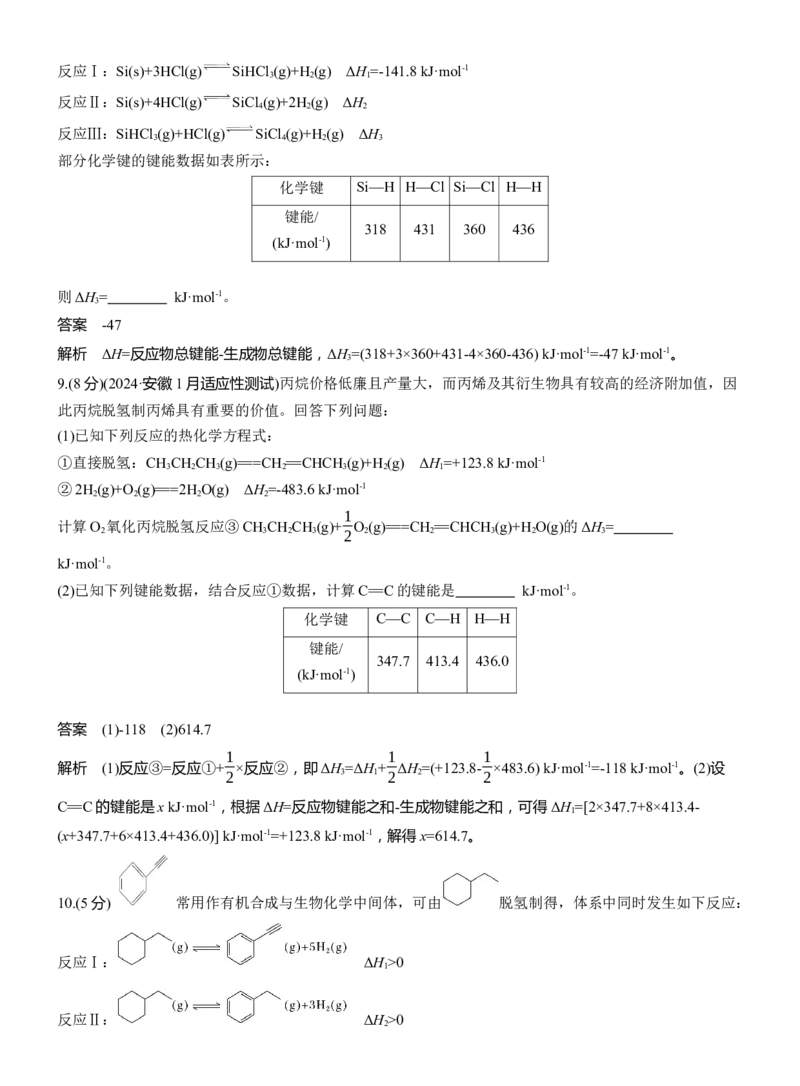
4.(4分)硫碘循环分解水是一种高效、环保的制氢方法,其流程图如图。
已知:
1
反应 Ⅱ:H SO (aq)===SO (g)+H O(l)+ O (g) ΔH =+327 kJ·mol-1
2 4 2 2 2 2 2反应 Ⅲ:2HI(aq)===H (g)+I (g) ΔH =+172 kJ·mol-1
2 2 3
反应 Ⅳ:2H O(l)===2H (g)+O (g) ΔH =+572 kJ·mol-1
2 2 2 4
则反应 Ⅰ :SO (g)+I (g)+2H O(l)===2HI(aq)+H SO (aq) ΔH= 。
2 2 2 2 4
答案 -213 kJ·mol-1
1
解析 根据盖斯定律,将Ⅳ× -Ⅱ-Ⅲ得反应SO (g)+I (g)+2H O(l)===2HI(aq)+H SO (aq) ΔH=-213
2 2 2 2 2 4
kJ·mol-1。
5.(4分)利用CO 与CH 制备合成气CO、H ,可能的反应历程如图所示:
2 4 2
说明:C(ads)为吸附性活性炭,E表示方框中物质的总能量(单位:kJ),TS表示过渡态。
制备合成气CO、H 总反应的热化学方程式为 。
2
答案 CH (g)+CO (g)===2CO(g)+2H (g) ΔH=(E -E ) kJ·mol-1
4 2 2 5 1
解析 根据ΔH=生成物总能量-反应物总能量,则ΔH=(E -E )kJ·mol-1。
5 1
6.(4分)异丁烷直接脱氢制备异丁烯,反应为CH CH(CH ) (g) CH ==C(CH ) (g)+H (g) ΔH。根据下列
3 3 2 2 3 2 2
键能数据,计算该反应的ΔH= kJ·mol-1。
化学键 C—C C==C C—H H—H
键能/
348 615 413 436
(kJ·mol-1)
答案 +123
解析 ΔH=反应物键能之和-生成物键能之和,除去异丁烷和异丁烯中相同的化学键,则反应的ΔH=(413×2
kJ·mol-1+348 kJ·mol-1)-615 kJ·mol-1-436 kJ·mol-1=+123 kJ·mol-1。
7.(4分)为了减缓温室效应,实现碳中和目标,可将CO 转化为甲醚、甲醇等产品。
2
CO 与H 制甲醚(CH OCH )的主要反应如下:
2 2 3 3
Ⅰ.CO (g)+H (g) CO(g)+H O(g) ΔH =+41.2 kJ·mol-1
2 2 2 1
Ⅱ.CO(g)+2H (g) CH OH(g) ΔH =-90.7 kJ·mol-1
2 3 2
Ⅲ.2CH OH(g) CH OCH (g)+H O(g) ΔH =-23.5 kJ·mol-1
3 3 3 2 3
则总反应2CO (g)+6H (g) CH OCH (g)+3H O(g)的ΔH= 。
2 2 3 3 2
答案 -122.5 kJ·mol-1
解析 由盖斯定律可知,反应Ⅰ×2+反应Ⅱ×2+反应Ⅲ可得2CO (g)+6H (g) CH OCH (g)+3H O(g)
2 2 3 3 2
ΔH=+41.2 kJ·mol-1×2-90.7 kJ·mol-1×2-23.5 kJ·mol-1=-122.5 kJ·mol-1。
8.(4分)三氯甲硅烷(SiHCl )是生产多晶硅的原料,工业合成SiHCl 体系中同时存在如下反应:
3 3反应Ⅰ:Si(s)+3HCl(g) SiHCl (g)+H (g) ΔH =-141.8 kJ·mol-1
3 2 1
反应Ⅱ:Si(s)+4HCl(g) SiCl (g)+2H (g) ΔH
4 2 2
反应Ⅲ:SiHCl (g)+HCl(g) SiCl (g)+H (g) ΔH
3 4 2 3
部分化学键的键能数据如表所示:
化学键 Si—H H—Cl Si—Cl H—H
键能/
318 431 360 436
(kJ·mol-1)
则ΔH = kJ·mol-1。
3
答案 -47
解析 ΔH=反应物总键能-生成物总键能,ΔH =(318+3×360+431-4×360-436) kJ·mol-1=-47 kJ·mol-1。
3
9.(8分)(2024·安徽1月适应性测试)丙烷价格低廉且产量大,而丙烯及其衍生物具有较高的经济附加值,因
此丙烷脱氢制丙烯具有重要的价值。回答下列问题:
(1)已知下列反应的热化学方程式:
①直接脱氢:CH CH CH (g)===CH ==CHCH (g)+H (g) ΔH =+123.8 kJ·mol-1
3 2 3 2 3 2 1
②2H (g)+O (g)===2H O(g) ΔH =-483.6 kJ·mol-1
2 2 2 2
1
计算O 氧化丙烷脱氢反应③CH CH CH (g)+ O (g)===CH ==CHCH (g)+H O(g)的ΔH =
2 3 2 3 2 2 2 3 2 3
kJ·mol-1。
(2)已知下列键能数据,结合反应①数据,计算C==C的键能是 kJ·mol-1。
化学键 C—C C—H H—H
键能/
347.7 413.4 436.0
(kJ·mol-1)
答案 (1)-118 (2)614.7
1 1 1
解析 (1)反应③=反应①+ ×反应②,即ΔH =ΔH + ΔH =(+123.8- ×483.6) kJ·mol-1=-118 kJ·mol-1。(2)设
2 3 1 2 2 2
C==C的键能是x kJ·mol-1,根据ΔH=反应物键能之和-生成物键能之和,可得ΔH =[2×347.7+8×413.4-
1
(x+347.7+6×413.4+436.0)] kJ·mol-1=+123.8 kJ·mol-1,解得x=614.7。
10.(5分) 常用作有机合成与生物化学中间体,可由 脱氢制得,体系中同时发生如下反应:
反应Ⅰ: ΔH >0
1
反应Ⅱ: ΔH >0
2在T ℃,恒压密闭容器中只发生反应 Ⅰ。初始通入0.2 mol (g)和1 mol H (g),达平衡时,体系
2
向环境放热a kJ;若初始加入0.8 mol ,达平衡时,体系向环境吸热b kJ。则ΔH =
1
kJ·mol-1(用含a、b的代数式表示)。
5
答案 5a+ b
4
解析 通入0.2 mol (g)和1 mol H (g),达平衡时,体系向环境放热a kJ,则当通入1 mol
2
(g)和5 mol H (g),体系向环境放热5a kJ;当加入0.8 mol ,达平衡时,体系向环
2
5b 5
境吸热b kJ,则若通入1 mol (g),达平衡时,体系向环境吸热 4 kJ,所以ΔH =(5a+4b)
1
kJ·mol-1。
11.(5分)到2024年,我国空间站天和号核心舱已在轨1 000多天。空间站必须给航天员提供基本的生存条
件,涉及氧气供给、二氧化碳清除、水处理等。电解水技术除用于供氧外,生成的氢气通过萨巴蒂尔反应,
实现了二氧化碳的清除,同时将氢气转化为更安全的甲烷,原理:CO (g)+4H (g) 2H O(g)+CH (g)
2 2 2 4
ΔH=-168.5 kJ·mol-1。已知相同条件下甲烷的燃烧热约是氢气的3.1倍,H O(g)===H O(l) ΔH=-44
2 2
kJ·mol-1,则CH 的燃烧热ΔH= kJ·mol-1。
4
答案 -883.5
1
解析 H 燃烧的热化学方程式为H (g)+ O (g)===H O(l) ΔH=-a kJ·mol-1(a>0)①,H O(g)===H O(l)
2 2 2 2 2 2 2
ΔH=-44 kJ·mol-1②,CH (g)+2H O(g) CO (g)+4H (g) ΔH=+168.5 kJ·mol-1③,根据盖斯定律,③-
4 2 2 2
②×2+①×4得CH (g)+2O (g) CO (g)+2H O(l) ΔH=(256.5-4a)kJ·mol-1,因为同条件下甲烷的燃烧热约是
4 2 2 2
氢气的3.1倍,所以256.5-4a=-3.1a,解得a=285,则CH 的燃烧热ΔH=-(3.1×285) kJ·mol-1=-883.5
4
kJ·mol-1。