文档内容
热化学方程式的书写与焓变的计算
1.计算反应热的方法
(1)根据物质能量的变化计算
①ΔH=E(生成物的总能量)-E(反应物的总能量)
②从活化能角度分析计算
ΔH=E(正反应的活化能)-E(逆反应的活化能)
a a
(2)根据键能数据计算
ΔH=E(反应物的键能总和)-E(生成物的键能总和)
(3)根据盖斯定律计算
①思维模型
②反应热计算技巧
同边加号异边负,焓的变化跟系数。
2.热化学方程式书写注意事项
(1)注意ΔH符号及单位:逆反应的反应热与正反应的反应热数值相等,但符号相反。
(2)注意热化学方程式中的化学计量数,如果化学计量数加倍,则ΔH也要加倍。
(3)注意物质的聚集状态:气体用“g”,液体用“l”,固体用“s”,溶液用“aq”。对于具有同素异形体
的物质,除了要注明聚集状态外,还要注明物质的名称。
(4)热化学方程式中可不写反应条件,不用“↑”和“↓”。
1.[2024·安徽,17(1)]C H 氧化脱氢反应:2C H (g)+O (g)===2C H (g)+2H O(g) ΔH =-209.8 kJ·mol-1
2 6 2 6 2 2 4 2 1
C H (g)+CO (g)===C H (g)+H O(g)+CO(g) ΔH =+178.1 kJ·mol-1
2 6 2 2 4 2 2
计算:2CO(g)+O (g)===2CO (g) ΔH = kJ·mol-1 。
2 2 3
2.[2024·湖南,18(1)]丙烯腈(CH ==CHCN)是一种重要的化工原料。工业上以N 为载气,用TiO 作催化
2 2 2
剂生产CH ==CHCN的流程如下:
2已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定;
②反应釜Ⅰ中发生的反应:
ⅰ:HOCH CH COOC H (g)―→CH ==CHCOOC H (g)+H O(g) ΔH
2 2 2 5 2 2 5 2 1
③反应釜Ⅱ中发生的反应:
ⅱ:CH ==CHCOOC H (g)+NH (g)―→CH ==CHCONH (g)+C H OH(g) ΔH
2 2 5 3 2 2 2 5 2
ⅲ:CH ==CHCONH (g)―→CH ==CHCN(g)+H O(g) ΔH
2 2 2 2 3
④在此生产条件下,酯类物质可能发生水解。
总反应HOCH CH COOC H (g)+NH (g)―→CH ==CHCN(g)+C H OH(g)+2H O(g) ΔH=
2 2 2 5 3 2 2 5 2
(用含ΔH 、ΔH 、和ΔH 的代数式表示)。
1 2 3
3.[2024·河北,17(1)①]硫酰氯常用作氯化剂和氯磺化剂,工业上制备原理如下:SO (g)+Cl (g)
2 2
SO Cl (g) ΔH=-67.59 kJ·mol-1。
2 2
若正反应的活化能为E kJ·mol-1,则逆反应的活化能E = kJ·mol-1(用含E 的代数式表示)。
正 逆 正
1 3
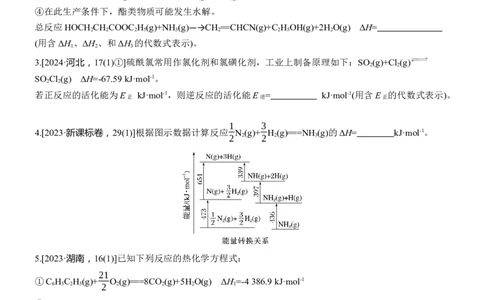
4.[2023·新课标卷,29(1)]根据图示数据计算反应 N (g)+ H (g)===NH (g)的ΔH= kJ·mol-1。
2 2 2 2 3
5.[2023·湖南,16(1)]已知下列反应的热化学方程式:
21
①C H C H (g)+ O (g)===8CO (g)+5H O(g) ΔH =-4 386.9 kJ·mol-1
6 5 2 5 2 2 2 2 1
②C H CH==CH (g)+10O (g)===8CO (g)+4H O(g) ΔH =-4 263.1 kJ·mol-1
6 5 2 2 2 2 2
1
③H (g)+ O (g)===H O(g) ΔH =-241.8 kJ·mol-1
2 2 2 2 3
计算反应④C H C H (g) C H CH==CH (g)+H (g)的ΔH = kJ·mol-1。
6 5 2 5 6 5 2 2 4
6.[2023·河北,17(1)]已知:1 mol物质中的化学键断裂时所需能量如下表。
物质 N (g) O (g) NO(g)
2 2
能量/kJ 945 498 631恒温下,将1 mol空气(N 和O 的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为V L的恒容
2 2
密闭容器中,假设体系中只存在如下两个反应:
ⅰ.N (g)+O (g) 2NO(g) K ΔH
2 2 1 1
ⅱ.2NO(g)+O (g) 2NO (g) K ΔH =-114 kJ·mol-1
2 2 2 2
ΔH = kJ·mol-1。
1答案精析
精练高考真题
1.-566
解析 将两个反应依次标号为反应①和反应②,反应①-反应②×2可得目标反应,根据盖斯定律知
ΔH =ΔH -2ΔH =(-209.8 kJ·mol-1-178.1 kJ·mol-1×2)=-566 kJ·mol-1。
3 1 2
2.ΔH +ΔH +ΔH
1 2 3
解析 根据盖斯定律,由反应ⅰ+反应ⅱ+反应ⅲ得HOCH CH COOC H (g)+NH (g) CH ==CHCN(g)
2 2 2 5 3 2
+C H OH(g)+2H O(g),故ΔH=ΔH +ΔH +ΔH 。
2 5 2 1 2 3
3.E +67.59
正
解析 根据反应热与活化能E 和E 关系ΔH=E -E 可知,该反应的E =[E -(-67.59)]kJ·mol-1=(E
正 逆 正 逆 逆 正 正
+67.59) kJ·mol-1。
4.-45
解析 在化学反应中,断开化学键要消耗能量,形成化学键要释放能量,反应的焓变等于反应物的键能总
1 3
和与生成物的键能总和的差,因此,由图中数据可知,反应 N (g)+ H (g)===NH (g)的ΔH=(473+654-436-
2 2 2 2 3
397-339) kJ·mol-1=-45 kJ·mol-1。
5.+118
解析 根据盖斯定律,将①-②-③可得C H C H (g) C H CH==CH (g)+H (g) ΔH =-4 386.9 kJ·mol-1-(-4
6 5 2 5 6 5 2 2 4
263.1 kJ·mol-1)-(-241.8 kJ·mol-1)=+118 kJ·mol-1。
6.+181
解析 ΔH =反应物总键能-生成物总键能=(945 kJ·mol-1+498 kJ·mol-1)-2×631 kJ·mol-1=+181 kJ·mol-1。
1