文档内容
专题八 能力提升检测卷
1.下列电离方程式书写正确的是
A. B.
C. D.
2.下列有关电解质、强电解质、弱电解质的分类正确的是
选项 A B C D
电解质 HO CO NaCl NaOH
2 2
强电解
盐酸 Ba(OH) HClO BaSO
质 2 4 4
弱电解
CHCOOH HO Cu(OH) 氨水
质 3 2 2
3.下列实验事实不能证明醋酸是弱电解质的是
A.用醋酸溶液做导电实验,灯泡很暗
B.常温下,测得0.1 mol·L-1醋酸溶液的c(H+)=10-4 mol·L-1
C.常温下,将c(H+)=0.1 mol·L-1的醋酸溶液稀释1 000倍测得c(H+)<10-4 mol·L-1
D.等c(H+)、等体积的盐酸和醋酸溶液中和碱时,醋酸中和碱的能力强
4.已知25℃时有关弱酸的电离平衡常数如下表:
弱酸化学式 CHCOOH HCN HCO
3 2 3
电离平衡常 1.75×10-5 6.2×10-10 K=4.5×10-7K=4.7×10-11
1 2
下列有关说法正确的是
A.等物质的量浓度的各溶液中c(H+)大小关系为CHCOOH溶液K (AgI)
sp sp21.已知某烧碱样品中含有NaCl杂质,为测定该样品中NaOH的质量分数,进行如下实验:
①称量1.00g样品溶于水配成250mL溶液:
②用碱式滴定管准确量取25.00mL所配溶液于锥形瓶中,滴加2—3滴指示剂:
③用 的标准盐酸滴定并重复三次,每次实验数据记录如下:
消耗盐酸的体积/mL
滴 定 序
待测液体积/mL
号
滴定前 滴定后
1 25.00 0.50 20.60
2 25.00 6.00 26.00
3 25.00 1.10 21.00
请回答下列问题:
(1)配制该溶液所需要的主要玻璃仪器为 。
(2)实验步骤②中所滴加的指示剂是 。
(3)滴定管装好溶液后,排除碱式滴定管胶管中气泡的方法是 。滴定过程中用左手控制
。(填仪器及部位),眼睛 ,直至滴定终点。
(4)判断达到滴定终点时的现象为 。
(5)若出现下列情况,导致测定结果偏高的是 (填序号)。
a.滴定前用蒸水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎使瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在链形瓶外
d.酸式滴定管中在滴定前有气泡,滴定后气泡消失
e.滴定前仰视读数,滴定后俯视读数
f.酸式滴定管在使用前没有用标准液润洗
(6)通过计算可知该烧碱样品的纯度为 。
22.回答下列问题:
(1)已知:HS:K =1.3×10﹣7 K =7.1×10−15; HCO:K =4.3×10﹣7 K =5.6×10−11;
2 a1 a2 2 3 a1 a2
CHCOOH:K=1.8×10﹣5 NH •H O:K=1.8×10﹣5。
3 a 3 2 b
①常温下,0.1 mol∙L−1NaS溶液和0.1 mol∙L−1NaCO 溶液,碱性更强的是 。
2 2 3
②25℃时,NaHCO 溶液的pH (填“大于”或“小于”)CHCOONa溶液的pH。
3 3
③NH HCO 溶液显 性。
4 3
(2)25℃时,HSO +H+的电离常数K=1.0×10−2,则该温度下NaHSO 的水解常数K=
2 3 a 3 h。
(3)能证明NaSO 溶液中存在 +H O +OH﹣水解平衡的事实是 (填字母,下同)。
2 3 2
A.滴入酚酞溶液变红,再加HSO 溶液红色褪去
2 4
B.滴入酚酞溶液变红,再加BaCl 溶液后产生沉淀且红色褪去
2
C.滴入酚酞溶液变红,再加氯水后红色褪去
(4)氯化铝水溶液呈 性(填“酸”、“中”、“碱”),把AlCl 溶液蒸干、灼烧后,得到的主要
3
固体产物是 。
(5)①写出1mol/L的NaH PO 溶液中的电荷守恒表达式: 。
2 4
②泡沫灭火器[里面装饱和NaHCO 溶液和Al (SO )]的工作原理: (用离子方程式
3 2 4 3
表示)。
23.完成下列问题
(1)常温时,0.1 mol·L-1NH Al(SO ) 溶液的pH=3。
4 4 2
①溶液中的K = (填数值),由水电离出的c(H+)= mol·L-1
W
②溶液中c( )+c(NH·H O) (填“>”“=”或“<”)c(Al3+)+c[Al(OH) ];2c( )-c( )-3c(Al3+)=
3 2 3
mol·L-1(填数值)。
③80 ℃时,0.1 mol·L-1NH Al(SO ) 溶液的pH小于3,分析导致pH随温度变化的原因是 。
4 4 2
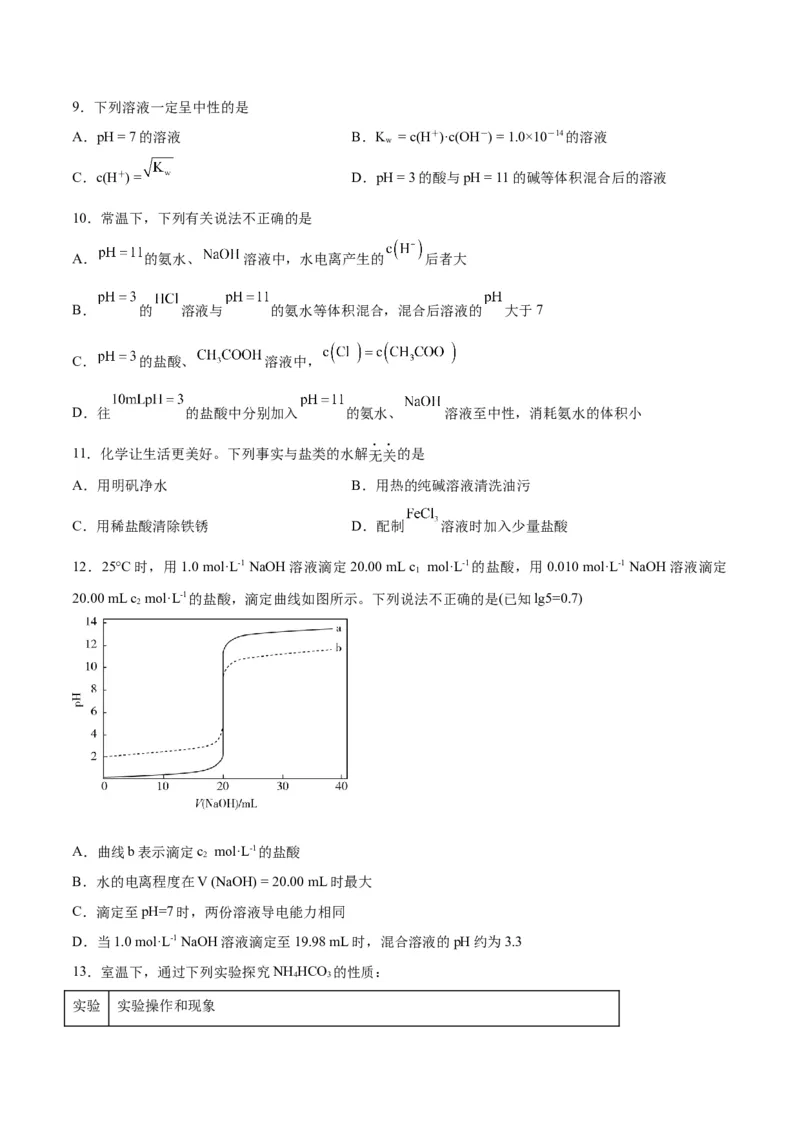
④常温时,向100 mL 0.1 mol·L-1NH HSO 溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液
4 4
体积的关系曲线如图所示。
ⅰ.图中a、b、c、d四点中水的电离程度最小的是 。
ⅱ.向NH HSO 溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为 。
4 4
(2)将常温下pH=13的NaOH溶液aL与pH=2的稀硫酸bL混合,若所得的混合溶液pH=11,则a∶b=
。
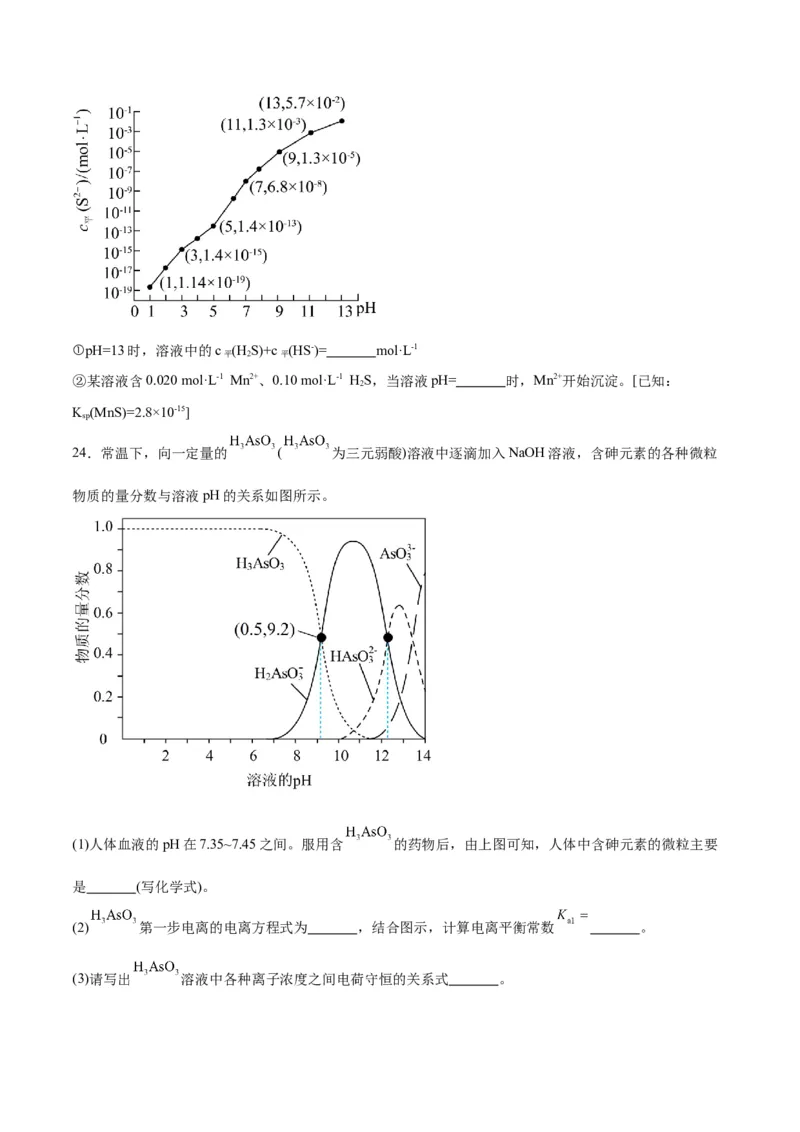
(3)25 ℃,在0.10 mol·L-1 HS溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c (S2-)
2 平
关系如图(忽略溶液体积的变化、HS的挥发)。
2①pH=13时,溶液中的c (H S)+c (HS-)= mol·L-1
平 2 平
②某溶液含0.020 mol·L-1 Mn2+、0.10 mol·L-1 HS,当溶液pH= 时,Mn2+开始沉淀。[已知:
2
K (MnS)=2.8×10-15]
sp
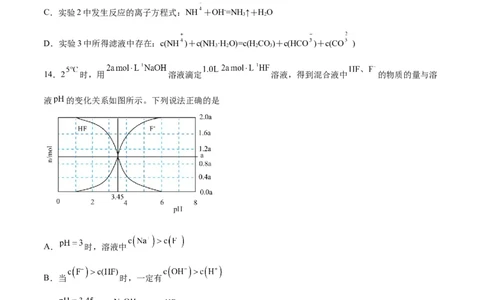
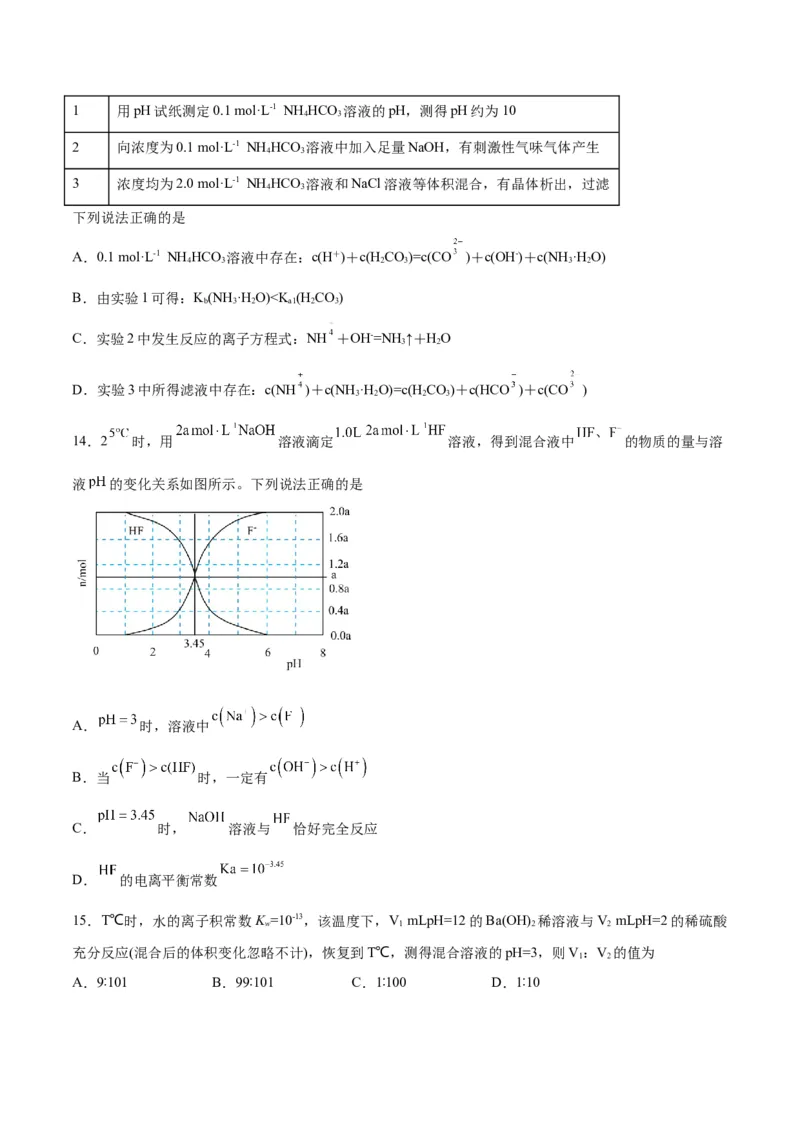
24.常温下,向一定量的 ( 为三元弱酸)溶液中逐滴加入NaOH溶液,含砷元素的各种微粒
物质的量分数与溶液pH的关系如图所示。
(1)人体血液的pH在7.35~7.45之间。服用含 的药物后,由上图可知,人体中含砷元素的微粒主要
是 (写化学式)。
(2) 第一步电离的电离方程式为 ,结合图示,计算电离平衡常数 。
(3)请写出 溶液中各种离子浓度之间电荷守恒的关系式 。(4)0.10mol/L的 溶液中, mol/L。
(5)写出 溶液中发生水解的离子方程式 。
(6)向含 的废水中加入适量氧化剂,再加入生石灰将砷元素转化为 沉淀。若要除去
,则溶液中的 至少为 mol/L。(已知:①当溶液中离子浓度 时,则该
离子被除尽;② )