文档内容
章末综合检测(十一) 物质结构与性质
一、选择题:本题包括5小题,每小题只有一个选项最符合题意。
1.(2020·山东威海一模)下列叙述错误的是( )
A.C H 分子中有π键
2 4
B.CH 的中心原子是sp3杂化
4
C.HCl和HI化学键的类型和分子的极性都相同
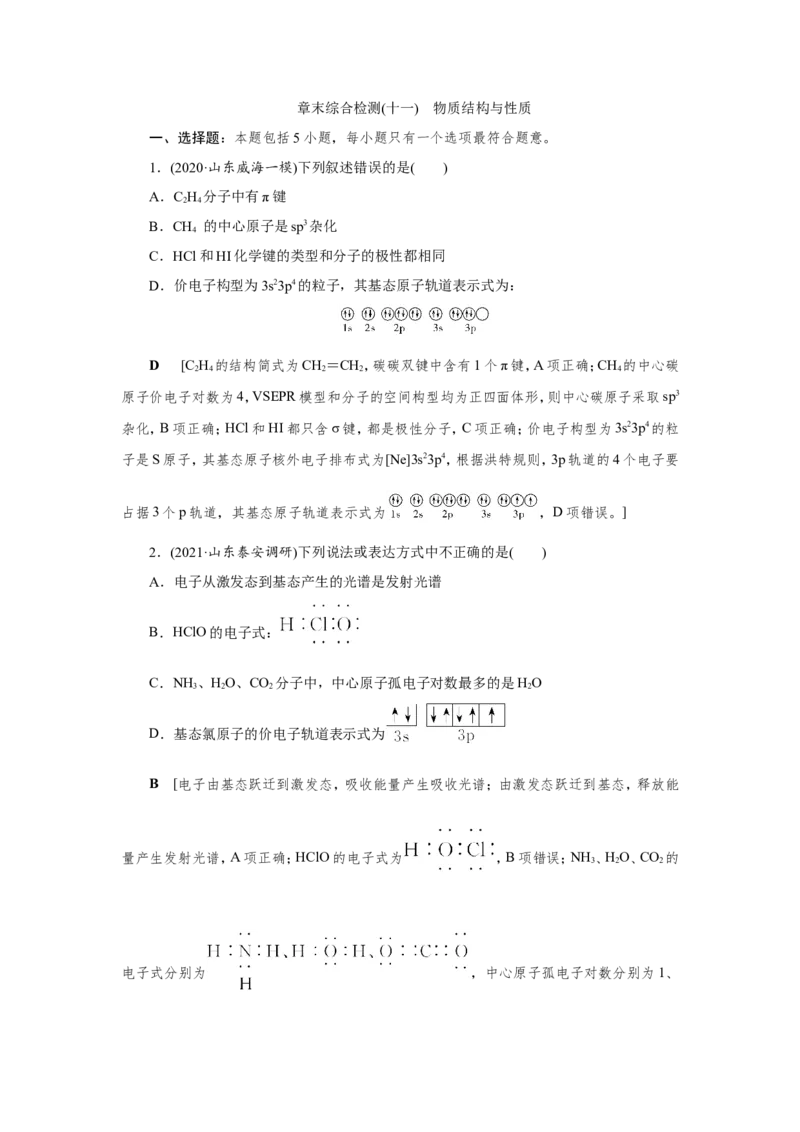
D.价电子构型为3s23p4的粒子,其基态原子轨道表示式为:
D [C H 的结构简式为CH=CH,碳碳双键中含有1个π键,A项正确;CH 的中心碳
2 4 2 2 4
原子价电子对数为4,VSEPR模型和分子的空间构型均为正四面体形,则中心碳原子采取sp3
杂化,B项正确;HCl和HI都只含σ键,都是极性分子,C项正确;价电子构型为3s23p4的粒
子是S原子,其基态原子核外电子排布式为[Ne]3s23p4,根据洪特规则,3p轨道的4个电子要
占据3个p轨道,其基态原子轨道表示式为 ,D项错误。]
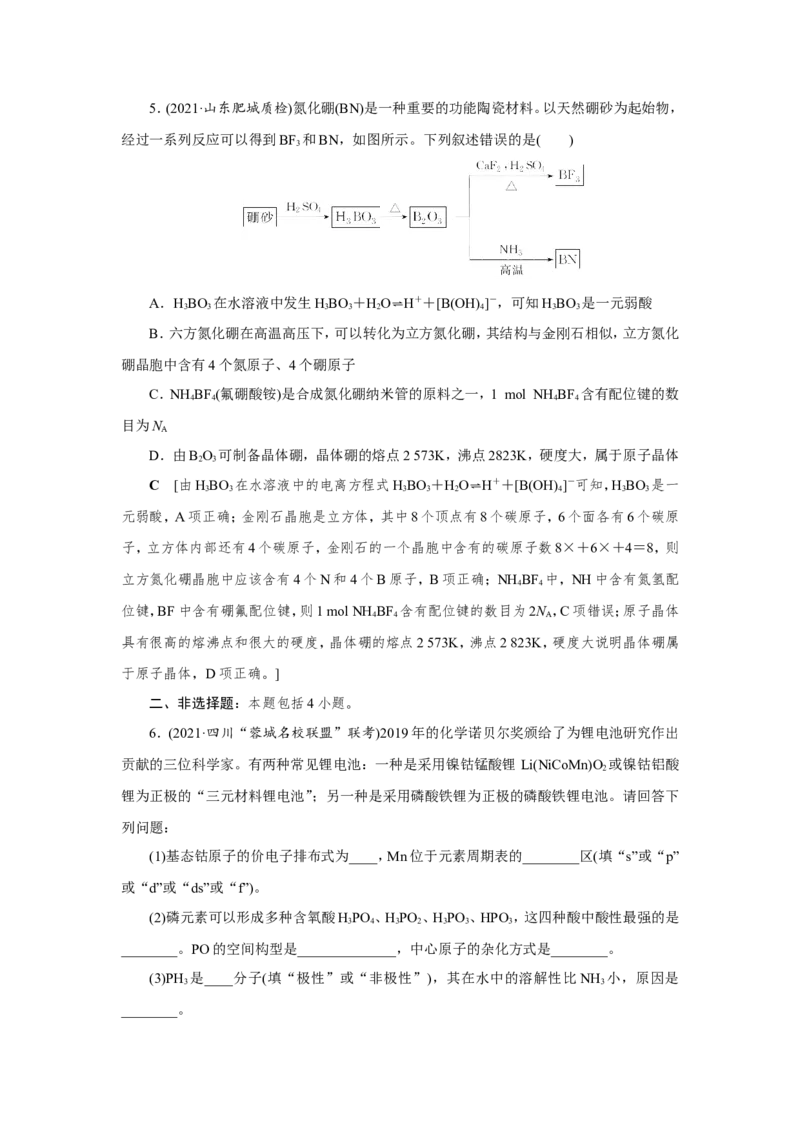
2.(2021·山东泰安调研)下列说法或表达方式中不正确的是( )
A.电子从激发态到基态产生的光谱是发射光谱
B.HClO的电子式:
C.NH 、HO、CO 分子中,中心原子孤电子对数最多的是HO
3 2 2 2
D.基态氯原子的价电子轨道表示式为
B [电子由基态跃迁到激发态,吸收能量产生吸收光谱;由激发态跃迁到基态,释放能
量产生发射光谱,A项正确;HClO的电子式为 ,B项错误;NH 、HO、CO 的
3 2 2
电子式分别为 ,中心原子孤电子对数分别为1、2、0,孤电子对数最多的是HO,C项正确;基态氯原子的价电子排布式为3s23p5,轨道表示式
2
为 ,D项正确。]
3.(2021·辽宁辽阳四校联考)镍的配合物常用于镍的提纯以及药物合成,如Ni(CO) 、
4
[Ni(CN) ]2-、[Ni(NH )]2+等。下列说法正确的是( )
4 3 6
A.CO与CN-结构相似,CO分子内σ键和π键个数之比为1∶2
B.[Ni(NH )]2+中含有非极性共价键和配位键
3 6
C.Ni2+的电子排布式为[Ar]3d10
D.CN-中C原子的杂化方式是sp2
A [CO与CN-结构相似,二者的成键方式相似,CO的分子结构为C≡O,分子内σ键
和π键个数之比为1∶2,A正确;[Ni(NH )]2+中含有极性共价键和配位键,不含非极性键,B
3 6
错误;基态Ni原子核外电子排布为[Ar]3d84s2,失去4s轨道的2个电子变成Ni2+,则Ni2+的
电子排布式为[Ar]3d8,C错误;CO与CN-结构相似,碳原子的成键方式相同,均采取sp杂化,
D错误。]
4.(2021·天津南开中学检测)有5种元素X、Y、Z、Q、T,基态X原子M能层p能级上有2
个未成对电子且无空轨道;Y原子的价电子构型为3d64s2;Z原子的L电子层的p能级上有一
个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半
充满。下列叙述不正确的是( )
A.X和Q形成的化合物为直线形
B.T和Z分别可与Q形成两种化合物
C.Y和X可形成化合物YX、YX
2
D.X和Z可形成非极性分子ZX
2
A [基态X原子M能层p能级上有2个未成对电子且无空轨道,则X的价电子排布式
为3s23p4,X是S;Y原子的价电子构型为3d64s2,则Y是Fe;Z原子的L电子层的p能级上有
一个空轨道,则Z的价电子排布式为2s22p2,Z是C;Q原子的L电子层的p能级上只有一对
成对电子,其价电子排布式为2s22p4,则Q是O;T原子的M电子层上p轨道半充满,其价电
子排布式为3s23p3,则T是P。S和O形成的化合物有SO 、SO ,前者是V形,后者是平面三
2 3
角形,A项错误;P、C分别可与O形成PO、PO、CO、CO 等化合物,B项正确;Fe和S可形
2 3 2 5 2
成化合物FeS、FeS,C项正确;ZX 是CS,C原子采取sp杂化,属于非极性分子,D项正确。]
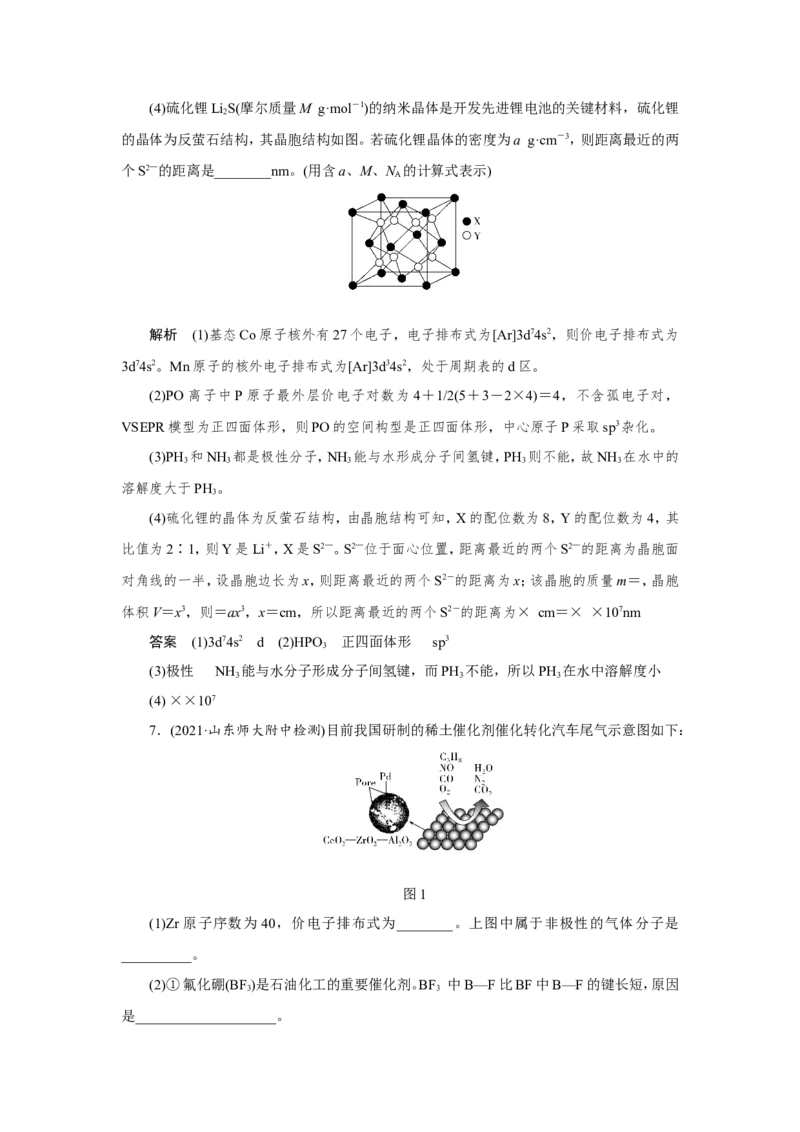
2 2 25.(2021·山东肥城质检)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,
经过一系列反应可以得到BF 和BN,如图所示。下列叙述错误的是( )
3
A.H
3
BO
3
在水溶液中发生H
3
BO
3
+H
2
O⇌H++[B(OH)
4
]-,可知H
3
BO
3
是一元弱酸
B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,立方氮化
硼晶胞中含有4个氮原子、4个硼原子
C.NH BF(氟硼酸铵)是合成氮化硼纳米管的原料之一,1 mol NH BF 含有配位键的数
4 4 4 4
目为N
A
D.由B O 可制备晶体硼,晶体硼的熔点2 573K,沸点2823K,硬度大,属于原子晶体
2 3
C [由H
3
BO
3
在水溶液中的电离方程式H
3
BO
3
+H
2
O⇌H++[B(OH)
4
]-可知,H
3
BO
3
是一
元弱酸,A项正确;金刚石晶胞是立方体,其中8个顶点有8个碳原子,6个面各有6个碳原
子,立方体内部还有4个碳原子,金刚石的一个晶胞中含有的碳原子数8×+6×+4=8,则
立方氮化硼晶胞中应该含有4个N和4个B原子,B项正确;NH BF 中,NH中含有氮氢配
4 4
位键,BF中含有硼氟配位键,则1 mol NH BF 含有配位键的数目为2N ,C项错误;原子晶体
4 4 A
具有很高的熔沸点和很大的硬度,晶体硼的熔点2 573K,沸点2 823K,硬度大说明晶体硼属
于原子晶体,D项正确。]
二、非选择题:本题包括4小题。
6.(2021·四川“蓉城名校联盟”联考)2019年的化学诺贝尔奖颁给了为锂电池研究作出
贡献的三位科学家。有两种常见锂电池:一种是采用镍钴锰酸锂 Li(NiCoMn)O 或镍钴铝酸
2
锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂为正极的磷酸铁锂电池。请回答下
列问题:
(1)基态钴原子的价电子排布式为____,Mn位于元素周期表的________区(填“s”或“p”
或“d”或“ds”或“f”)。
(2)磷元素可以形成多种含氧酸HPO 、HPO 、HPO 、HPO ,这四种酸中酸性最强的是
3 4 3 2 3 3 3
________。PO的空间构型是______________,中心原子的杂化方式是________。
(3)PH 是____分子(填“极性”或“非极性”),其在水中的溶解性比NH 小,原因是
3 3
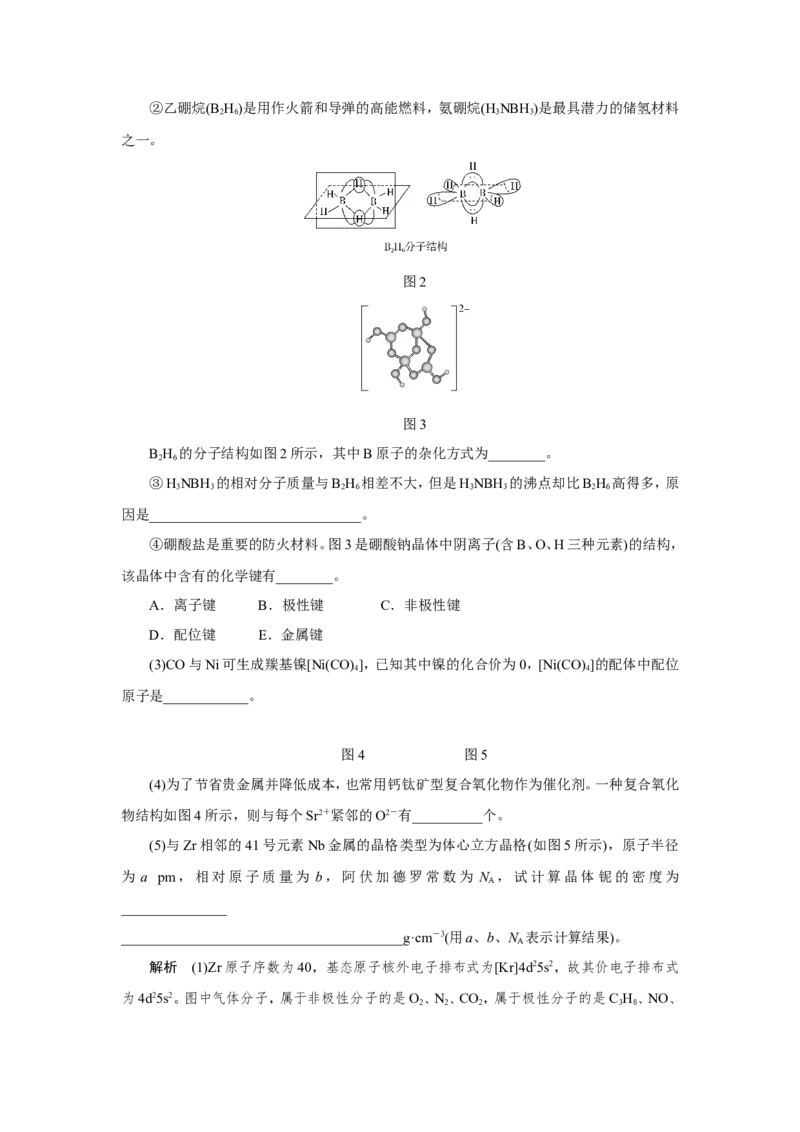
________。(4)硫化锂LiS(摩尔质量M g·mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂
2
的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为a g·cm-3,则距离最近的两
个S2—的距离是________nm。(用含a、M、N 的计算式表示)
A
解析 (1)基态Co原子核外有27个电子,电子排布式为[Ar]3d74s2,则价电子排布式为
3d74s2。Mn原子的核外电子排布式为[Ar]3d34s2,处于周期表的d区。
(2)PO离子中P原子最外层价电子对数为4+1/2(5+3-2×4)=4,不含孤电子对,
VSEPR模型为正四面体形,则PO的空间构型是正四面体形,中心原子P采取sp3杂化。
(3)PH 和NH 都是极性分子,NH 能与水形成分子间氢键,PH 则不能,故NH 在水中的
3 3 3 3 3
溶解度大于PH 。
3
(4)硫化锂的晶体为反萤石结构,由晶胞结构可知,X的配位数为8,Y的配位数为4,其
比值为2∶1,则Y是Li+,X是S2—。S2—位于面心位置,距离最近的两个S2—的距离为晶胞面
对角线的一半,设晶胞边长为x,则距离最近的两个S2-的距离为x;该晶胞的质量m=,晶胞
体积V=x3,则=ax3,x=cm,所以距离最近的两个S2-的距离为× cm=× ×107nm
答案 (1)3d74s2 d (2)HPO 正四面体形 sp3
3
(3)极性 NH 能与水分子形成分子间氢键,而PH 不能,所以PH 在水中溶解度小
3 3 3
(4) ××107
7.(2021·山东师大附中检测)目前我国研制的稀土催化剂催化转化汽车尾气示意图如下:
图1
(1)Zr原子序数为40,价电子排布式为________。上图中属于非极性的气体分子是
__________。
(2)①氟化硼(BF)是石油化工的重要催化剂。BF 中B—F比BF中B—F的键长短,原因
3 3
是____________________。②乙硼烷(B H)是用作火箭和导弹的高能燃料,氨硼烷(H NBH )是最具潜力的储氢材料
2 6 3 3
之一。
图2
图3
B H 的分子结构如图2所示,其中B原子的杂化方式为________。
2 6
③HNBH 的相对分子质量与B H 相差不大,但是HNBH 的沸点却比B H 高得多,原
3 3 2 6 3 3 2 6
因是______________________________。
④硼酸盐是重要的防火材料。图3是硼酸钠晶体中阴离子(含B、O、H三种元素)的结构,
该晶体中含有的化学键有________。
A.离子键 B.极性键 C.非极性键
D.配位键 E.金属键
(3)CO与Ni可生成羰基镍[Ni(CO) ],已知其中镍的化合价为0,[Ni(CO) ]的配体中配位
4 4
原子是____________。
图4 图5
(4)为了节省贵金属并降低成本,也常用钙钛矿型复合氧化物作为催化剂。一种复合氧化
物结构如图4所示,则与每个Sr2+紧邻的O2-有__________个。
(5)与Zr相邻的41号元素Nb金属的晶格类型为体心立方晶格(如图5所示),原子半径
为 a pm,相对原子质量为 b,阿伏加德罗常数为 N ,试计算晶体铌的密度为
A
_______________
________________________________________g·cm-3(用a、b、N 表示计算结果)。
A
解析 (1)Zr原子序数为40,基态原子核外电子排布式为[Kr]4d25s2,故其价电子排布式
为4d25s2。图中气体分子,属于非极性分子的是O、N、CO,属于极性分子的是C H、NO、
2 2 2 3 8CO、HO(g)。
2
(2)①BF 中B原子采用sp2杂化,BF中B原子采用sp3杂化,s轨道成分越多,电子云重
3
叠程度越大,键长越短。
②由B H 的分子结构可知,每个B原子形成4个单键,则B原子采取sp3杂化。
2 6
③HNBH 的相对分子质量与B H 相差不大,由于HNBH 分子间存在氢键,分子间作
3 3 2 6 3 3
用力更大,故HNBH 的沸点却比B H 高得多。
3 3 2 6
④硼酸钠晶体中存在离子键、极性键(H—O、B—O)、配位键(B←O),故答案选A、B、D。
(4)Sr2+位于晶胞的体心,O2-位于晶胞的棱中点,则与每个Sr2+紧邻的O2-有12个。
(5)金属Nb的晶格类型为体心立方晶格,则每个晶胞含有Nb原子数为1+×8=2个;相
对原子质量为b,阿伏加德罗常数为N ,则每个晶胞的质量为 g。原子半径为a pm,设晶胞
A
的棱长为x ,体对角线长度等于原子半径的4倍,则有x=4a pm,x=pm=×
10—10 cm,晶胞的体积为(×10—10 cm)3,故晶体铌的密度为(g)/(×10-10 cm)3=
g/cm3。
答案 (1)4d25s2 O、N、CO
2 2 2
(2)①BF 中B采用sp2杂化,BF中B采用sp3杂化,s轨道成分越多,电子云重叠程度越
3
大,键长越短(或BF 中除了σ键,还有()大π键)
3
②sp3 ③HNBH 分子间存在氢键,分子间作用力更大 ④A、B、D
3 3
(3)C(或碳) (4)12 (5)
8.(2020·山东济宁三模)氮、铬及其相关化合物用途非常广泛。回答下列问题:
(1)基态N原子的核外电子排布式为__________,Cr位于元素周期表第四周期________
族。
(2)Cr与K位于同一周期且最外层电子数相同,两种元素原子第一电离能的大小关系为
________;CrCl 的熔点(83 ℃)比CrF 的熔点(1 100 ℃)低得多,这是因为________________。
3 3
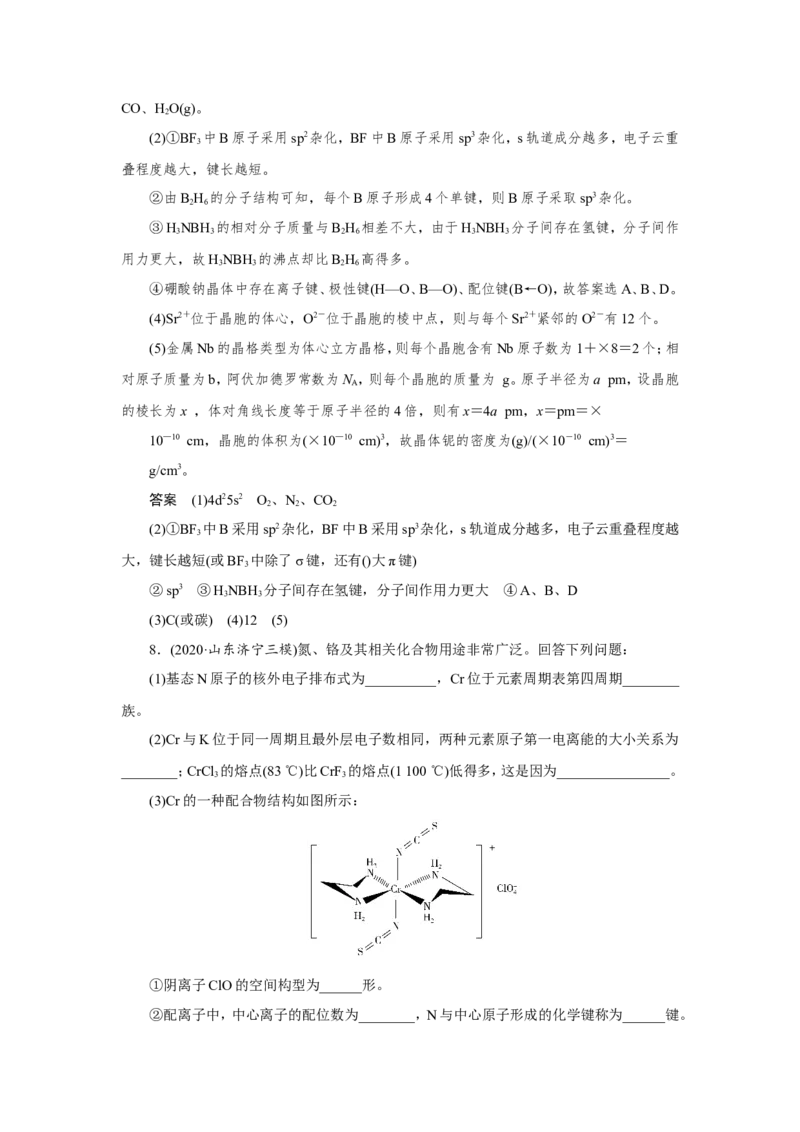
(3)Cr的一种配合物结构如图所示:
①阴离子ClO的空间构型为______形。
②配离子中,中心离子的配位数为________,N与中心原子形成的化学键称为______键。③配体HNCH CHNH (乙二胺)中碳原子的杂化方式是______,分子中三种元素电负性
2 2 2 2
从大到小的顺序为______。
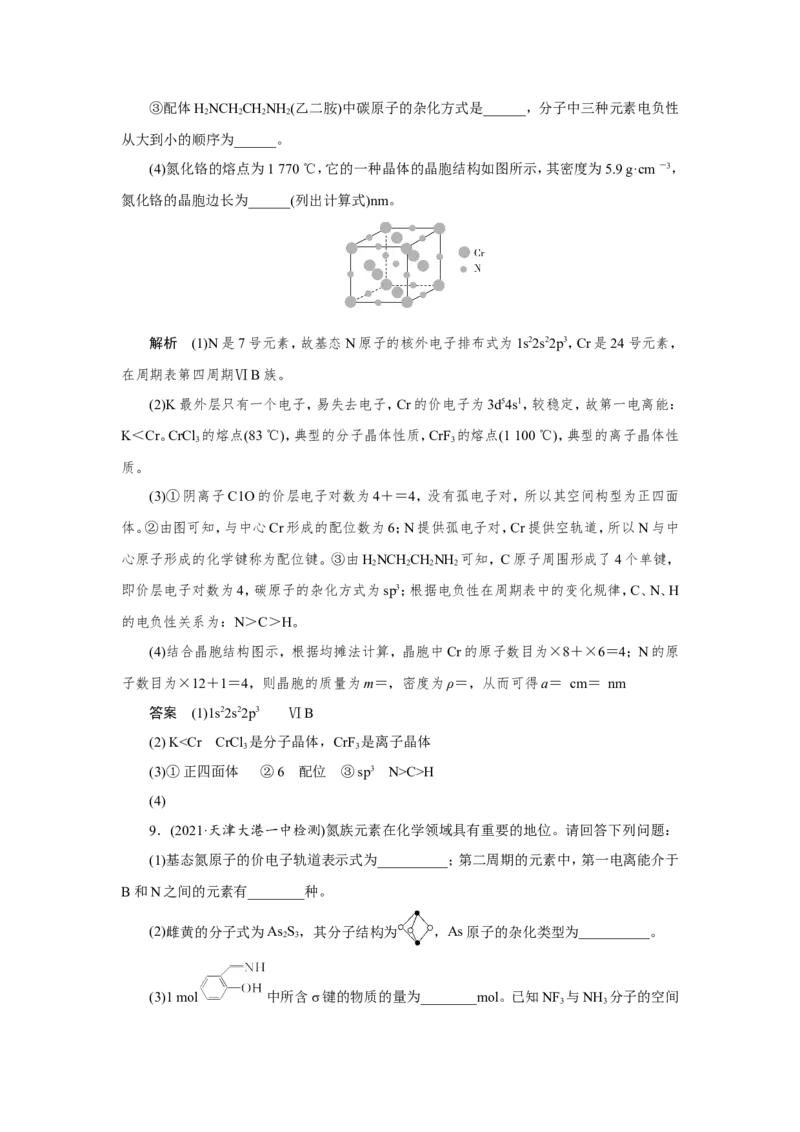
(4)氮化铬的熔点为1 770 ℃,它的一种晶体的晶胞结构如图所示,其密度为5.9 g·cm -3,
氮化铬的晶胞边长为______(列出计算式)nm。
解析 (1)N是7号元素,故基态N原子的核外电子排布式为1s22s22p3,Cr是24号元素,
在周期表第四周期ⅥB族。
(2)K最外层只有一个电子,易失去电子,Cr的价电子为3d54s1,较稳定,故第一电离能:
K<Cr。CrCl 的熔点(83 ℃),典型的分子晶体性质,CrF 的熔点(1 100 ℃),典型的离子晶体性
3 3
质。
(3)①阴离子C1O的价层电子对数为4+=4,没有孤电子对,所以其空间构型为正四面
体。②由图可知,与中心Cr形成的配位数为6;N提供孤电子对,Cr提供空轨道,所以N与中
心原子形成的化学键称为配位键。③由HNCH CHNH 可知,C原子周围形成了4个单键,
2 2 2 2
即价层电子对数为4,碳原子的杂化方式为sp3;根据电负性在周期表中的变化规律,C、N、H
的电负性关系为:N>C>H。
(4)结合晶胞结构图示,根据均摊法计算,晶胞中Cr的原子数目为×8+×6=4;N的原
子数目为×12+1=4,则晶胞的质量为m=,密度为ρ=,从而可得a= cm= nm
答案 (1)1s22s22p3 ⅥB
(2) KC>H
(4)
9.(2021·天津大港一中检测)氮族元素在化学领域具有重要的地位。请回答下列问题:
(1)基态氮原子的价电子轨道表示式为__________;第二周期的元素中,第一电离能介于
B和N之间的元素有________种。
(2)雌黄的分子式为As S,其分子结构为 ,As原子的杂化类型为__________。
2 3
(3)1 mol 中所含σ键的物质的量为________mol。已知NF 与NH 分子的空间
3 3构型都是三角锥形,但NF 不易与Cu2+形成配离子,原因是_____________________。
3
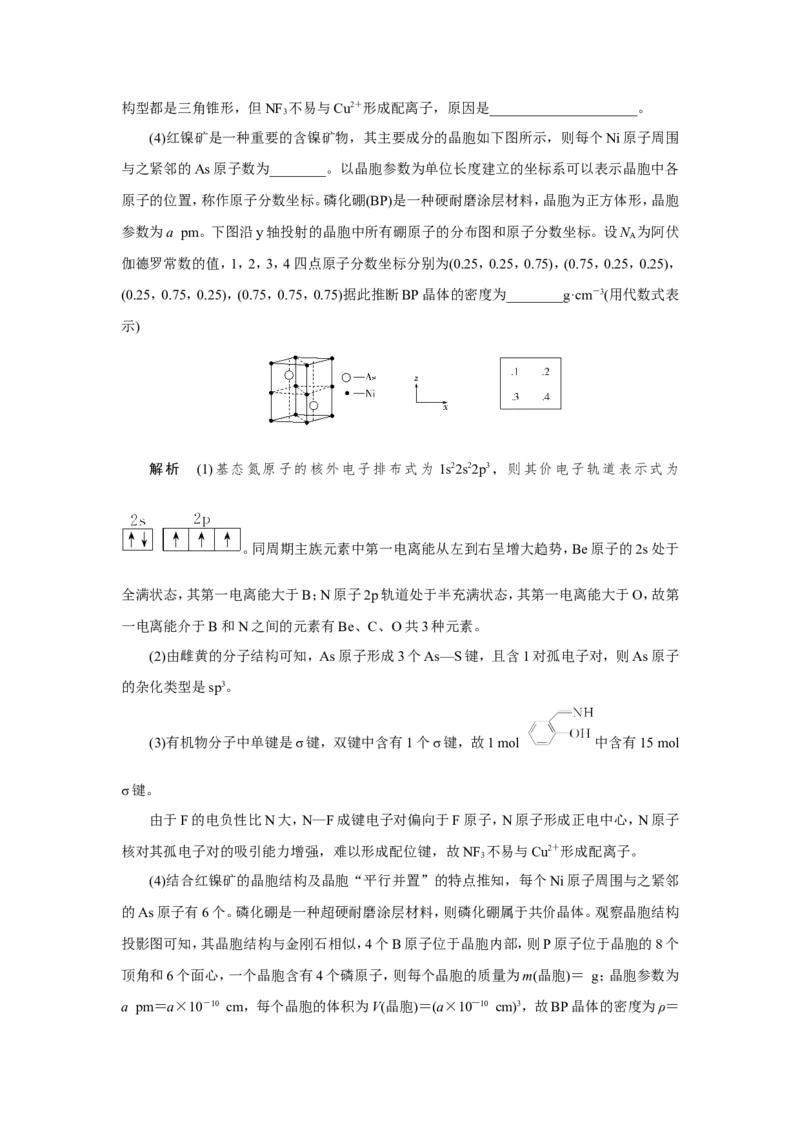
(4)红镍矿是一种重要的含镍矿物,其主要成分的晶胞如下图所示,则每个Ni原子周围
与之紧邻的As原子数为________。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各
原子的位置,称作原子分数坐标。磷化硼(BP)是一种硬耐磨涂层材料,晶胞为正方体形,晶胞
参数为a pm。下图沿y轴投射的晶胞中所有硼原子的分布图和原子分数坐标。设N 为阿伏
A
伽德罗常数的值,1,2,3,4四点原子分数坐标分别为(0.25,0.25,0.75),(0.75,0.25,0.25),
(0.25,0.75,0.25),(0.75,0.75,0.75)据此推断BP晶体的密度为________g·cm-3(用代数式表
示)
解析 (1)基态氮原子的核外电子排布式为 1s22s22p3,则其价电子轨道表示式为
。同周期主族元素中第一电离能从左到右呈增大趋势,Be原子的2s处于
全满状态,其第一电离能大于B;N原子2p轨道处于半充满状态,其第一电离能大于O,故第
一电离能介于B和N之间的元素有Be、C、O共3种元素。
(2)由雌黄的分子结构可知,As原子形成3个As—S键,且含1对孤电子对,则As原子
的杂化类型是sp3。
(3)有机物分子中单键是σ键,双键中含有1个σ键,故1 mol 中含有15 mol
σ键。
由于F的电负性比N大,N—F成键电子对偏向于F原子,N原子形成正电中心,N原子
核对其孤电子对的吸引能力增强,难以形成配位键,故NF 不易与Cu2+形成配离子。
3
(4)结合红镍矿的晶胞结构及晶胞“平行并置”的特点推知,每个Ni原子周围与之紧邻
的As原子有6个。磷化硼是一种超硬耐磨涂层材料,则磷化硼属于共价晶体。观察晶胞结构
投影图可知,其晶胞结构与金刚石相似,4个B原子位于晶胞内部,则P原子位于晶胞的8个
顶角和6个面心,一个晶胞含有4个磷原子,则每个晶胞的质量为m(晶胞)= g;晶胞参数为
a pm=a×10-10 cm,每个晶胞的体积为V(晶胞)=(a×10—10 cm)3,故BP晶体的密度为ρ=m(晶胞)/V(晶胞)=(g)/(a×10-10 cm)3= g·cm—3。
答案 (1) 3 (2)sp3
(3)15 F的电负性比N大,N—F成键电子对向F偏移,导致NF 中N原子核对其孤对
3
电子的吸引能力增强,难以形成配位键,故NF 不易与Cu2+形成配离子
3
(4)6