文档内容
专题突破卷 05 物质结构与性质 元素周期律(一)
——原子结构与性质 元素周期表、元素周期律
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列有关化学元素周期表的说法正确的是( )
A.元素周期表共有18列,所以共有18个族
B.ⅦA族元素的非金属性自上而下依次减弱
C.主族元素均呈现与其族数相同的最高化合价
D.第二周期主族元素的原子半径自左向右依次增大
2.一定量的锎(Cf)在医学上常用作治疗恶性肿瘤的中子源。下列有关锎的说法错误的是( )
A.Cf原子中,中子数为154
B.Cf原子中,质子数为98
C.Cf原子中,核外电子数为98
D.锎元素的相对原子质量为252
3. (2024·陕西西安模拟)下列化学用语表述错误的是( )
A.中子数为18的氯原子:Cl
B.基态N原子的价层电子排布图:
C.基态 Cu原子的电子排布式:
29
1s22s22p63s23p63d94s2
D.标准状况下,2.24 L C H 和N 的混合气体中含有的π键数为0.2N
2 2 2 A
4. (2024·天津南开区一模)科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复
轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子,这4个原子在生成数微秒后衰变
成第113号元素。第115号元素的一种核素为X。下列有关叙述错误的是( )
A.核素X的质量数为288
B.核素X的质量数与中子数之差为173
C.113号元素属于金属元素
D.155号元素的最高正化合价是+5
5.下列说法正确的是( )
①在氮原子中,质子数为7,而中子数不一定为7 ②O与O是不同的核素,因此分别由这两种原子构成
1
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司的分子化学性质不同 ③O 和O 互为同素异形体 ④Ti和Ti的质量数不同,属于两种元素 ⑤实际存在
2 3
的H、H、H、H+和H ,是氢的五种核素 ⑥H 、H 、H 互为同位素 ⑦稀土元素Sm与Sm 是同一种核
2 2 2 2
素
A.①⑥ B.②④ C.⑤⑦ D.①③
6.某元素的一种同位素X原子的质量数为A,它与2H原子组成2H X分子,此分子含N个中子,在a g
m
2H X中所含电子的物质的量是( )
m
A.(A-N+m)mol
B.(A-N)mol
C.(A-N+m)mol
D.(A-N+2m)mol
7.(2024·河北保定模拟)医学界通过用放射性14C来标记C ,发现C 的一种羧酸衍生物在特定条件下可通
60 60
过DNA来杀死细胞,从而抑制艾滋病(AIDS)。下列说法正确的是( )
A.C 与石墨互为同位素
60
B.14C的中子数与质子数相差2
C.常温下,C 易溶于氯化钠溶液
60
D.基态碳原子L层的轨道表示式为
8.(2024·江苏苏锡常镇四市调研一)一种超导材料中含 Cu、P、O、S等元素。下列说法正确的是
( )
A. 原子半径:r(P)>r(S)>r(O) B. 第一电离能:I(O)>I(S)>I(P)
1 1 1
C. 酸性强弱:HPO >H SO D. 基态Cu原子3d轨道上有9个电子
3 4 2 4
9.(2024·广东佛山一模)现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p2、②1s22s22p63s23p3、
③1s22s22p3、④1s22s22p5。下列有关比较正确的是( )
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
C.电负性:①>②>③>④
D.最高正化合价:④>③>②>①
10.已知X、Y、Z三种主族元素在元素周期表中的位置如图所示,设X的原子序数为a,则下列说法不正
确的是( )
A.Y与Z的原子序数之和可能为2a
B.Y的原子序数可能为a-17
C.Z的原子序数可能为a+31
2
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.X、Y、Z一定为短周期元素
11.下列实验不能达到实验目的的是( )
选项 实验操作 实验目的
A Cl、Br 分别与H 反应 比较氯、溴的非金属性强弱
2 2 2
B 向MgCl 、AlCl 溶液中分别通入氨 比较镁、铝的金属性强弱
2 3
测定相同物质的量浓度的NaCO、NaSO 的溶液
2 3 2 4
C 比较碳、硫的非金属性强弱
的pH
D Fe、Cu分别与稀盐酸反应 比较铁、铜的金属性强弱
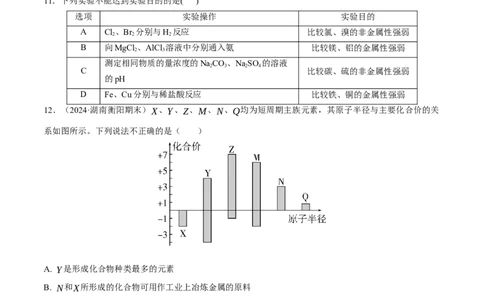
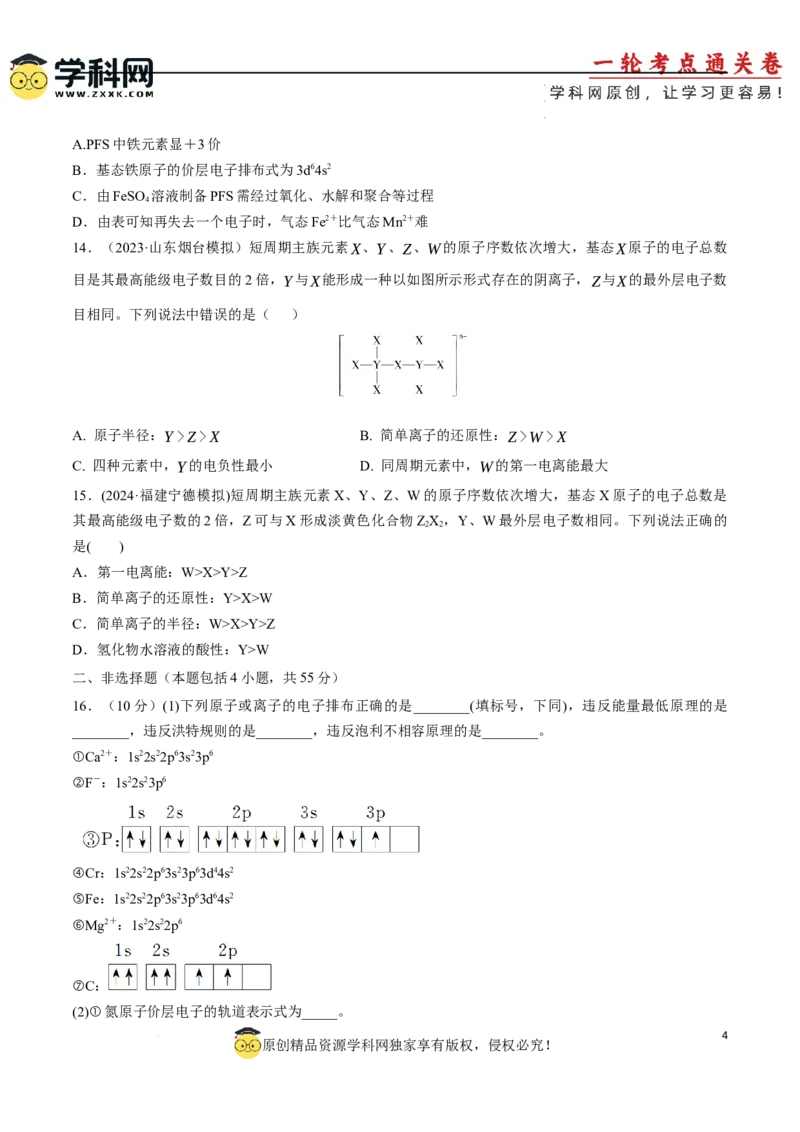
12.(2024·湖南衡阳期末)X、Y、Z、M、N、Q均为短周期主族元素,其原子半径与主要化合价的关
系如图所示。下列说法不正确的是( )
A. Y是形成化合物种类最多的元素
B. N和X所形成的化合物可用作工业上冶炼金属的原料
C. X、Z、N形成的简单离子半径最小的是X2−
D. 简单氢化物的稳定性:Z>M
13.现代污水处理工艺中常利用聚合铁在水体中形成絮状物,以吸附 Mn2+等重金属离子,聚合铁简称
PFS,化学式为 (n<5,m<10)。下列说法错误的是( )
m
元素 Mn Fe
I 717 762
1
电离能/
I 1 509 1 561
2
(kJ·mol-1)
I 3 248 2 957
3
3
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司A.PFS中铁元素显+3价
B.基态铁原子的价层电子排布式为3d64s2
C.由FeSO 溶液制备PFS需经过氧化、水解和聚合等过程
4
D.由表可知再失去一个电子时,气态Fe2+比气态Mn2+难
14.(2023·山东烟台模拟)短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数
目是其最高能级电子数目的2倍,Y与X能形成一种以如图所示形式存在的阴离子,Z与X的最外层电子数
目相同。下列说法中错误的是( )
A. 原子半径:Y>Z>X B. 简单离子的还原性:Z>W>X
C. 四种元素中,Y的电负性最小 D. 同周期元素中,W的第一电离能最大
15.(2024·福建宁德模拟)短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数是
其最高能级电子数的2倍,Z可与X形成淡黄色化合物ZX ,Y、W最外层电子数相同。下列说法正确的
2 2
是( )
A.第一电离能:W>X>Y>Z
B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z
D.氢化物水溶液的酸性:Y>W
二、非选择题(本题包括4小题,共55分)
16.(10分)(1)下列原子或离子的电子排布正确的是________(填标号,下同),违反能量最低原理的是
________,违反洪特规则的是________,违反泡利不相容原理的是________。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C:
(2)①氮原子价层电子的轨道表示式为_____。
4
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司②Co基态原子核外电子排布式为______。
③Fe3+基态核外电子排布式为______。
17.(14分)下面给出14种元素的电负性:
元素 Al B Be C Cl F Li
电负性 1.5 2.0 1.5 2.5 3.0 4.0 1.0
元素 Mg N Na O P S Si
电负性 3.0 0.9 3.5 2.1 2.5 1.8
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价
键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是________。
(2)通过分析电负性值变化规律,确定镁元素电负性的最小范围是________。
(3)判断下列物质是离子化合物还是共价化合物:
A.LiN B.BeCl
3 2
C.AlCl D.SiC
3
属于离子化合物的是________;
属于共价化合物的是________;
请设计一个实验方案证明上述所得到的结论:________。
(4)在P与Cl组成的化合物中,Cl元素显________(填“正”或“负”)价,理由是________。
18.(12分)现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子
序数依次增大。
A元素原子的核外p电子数比s电子数少3
B元素形成的物质种类繁多,其形成的一种固体单质工业上常用作
切割工具
C元素基态原子p轨道有3个未成对电子
D原子核外所有p轨道全充满或半充满
E在该周期中未成对电子数最多
F能形成红色(或砖红色)的FO和黑色的FO两种氧化物
2
某同学根据上述信息,完成下列各题。
(1)画出A基态原子的核外电子轨道表示式: 。
(2)B 基态原子的核外电子轨道表示式为 该同学所画的轨道表示式违背了
。
(3)D基态原子中能量最高的电子,其电子云在空间有 个伸展方向,呈 形。
(4)写出C原子的电子排布式: ;写出E原子的简化电子排布式: 。
5
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司(5)写出F元素原子的价层电子排布式: 。
19.(19分)X、Y、Z、W为元素周期表前四周期的元素,原子序数依次增大,X原子核外有6种不同运
动状态的电子,Y原子基态时的2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧
化物可作涂料;W位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
(1)X 在元素周期表中的位置是 ;Y的最高价氧化物对应水化物与Y的最简单气态氢化
物反应的化学方程式 。
(2)X、Y最简单气态氢化物的稳定性:X Y(填“大于”或“小于”)。
(3)Z原子核外电子排布式为 。
(4)W位于元素周期表的 区,与W处于同一周期且最外层电子数相同的元素的基态原子共有
种,这些元素分别为 (填元素符号)。
(5)在发生焰色试验时,W的4s电子会跃迁到4p轨道,写出此激发态W原子的价层电子排布式:
。
(6)与钛位于同一周期且含有相同未成对电子数的过渡元素为 (填元素符号)。
(7)基态砷原子N电子层中的成对电子与单电子的数量比为 。
6
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司