文档内容
专题突破卷 06 物质结构与性质
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列事实不能直接从原子结构角度解释的是
A.化合物ICl中I为+1价 B.第一电离能:N>O
C.熔点:纯铁>生铁 D.热稳定性:NH >PH
3 3
2.软钾镁矾(化学式为 )是一种重要的钾肥。下列说法正确的是
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
3.下列说法正确的是
A.碱性:Al(OH) >Mg(OH) B.硬度:晶体硅>金刚石
3 2
C.热稳定性:PH >NH D.酸性:CFCOOH > CCl COOH
3 3 3 3
4.下列化学用语表达正确的是
A. 的结构示意图为:
B.硼酸的电子式为:
C.原子核内有10个中子的氧原子:
D.基态铜原子的价层电子轨道表示式为:
5.近年来,光催化剂的研究是材料领域的热点。一种Ru配合物(如图所示)复合光催化剂可将 转化为
HCOOH。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.Ru配合物中第二周期元素的电负性:O>N>C
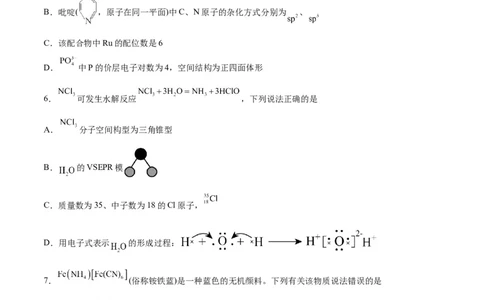
B.吡啶( ,原子在同一平面)中C、N原子的杂化方式分别为 、
C.该配合物中Ru的配位数是6
D. 中P的价层电子对数为4,空间结构为正四面体形
6. 可发生水解反应 ,下列说法正确的是
A. 分子空间构型为三角锥型
B. 的VSEPR模
C.质量数为35、中子数为18的Cl原子,
D.用电子式表示 的形成过程:
7. (俗称铵铁蓝)是一种蓝色的无机颜料。下列有关该物质说法错误的是
A.电负性:
B.铵铁蓝中铁元素有两种化合价
C. 中 的键角比 中的 的键角小
D.铵铁蓝中的配体是 ,该配体中的 键与 键之比是1:2
8.X、Y 、Z、W 、Q是原子序数依次增大的短周期主族元素。基态X原子核外有两个未成对电子,Y是
地壳中含量最高的元素 ,其中Z与X同族,W 与Y同族。下列说法正确的是
A.原子半径:Z>Y>X
资料收集整理【淘宝店铺:向阳百分百】B.XY 和ZY 中的键角:Y-X-Y>Y- Z- Y
2 2
C.气态氢化物的沸点:Z>X
D.氧化物对应水化物的酸性:Q> W
9.我国科学家用如图所示的阴离子的盐作水系锌离子电池的电解质溶液,显示了优良的循环性能。X、
Y、Z、W均为短周期元素且原子序数依次增大,其中X、Y、Z位于同一周期,Y、W核外最外层电子数
相等。下列叙述正确的是
A.简单离子半径大小顺序为W>Z>Y
B.每个阴离子中σ键与π键的数目之比为5:2
C.Y的简单氢化物的沸点高于W的简单氢化物,是因为Y的非金属性强于W
D.X和Z形成的简单化合物各原子最外层均满足8电子稳定结构
10.物质的结构决定性质,下列比较,不正确的是
A.碱性: 大于 ; 小于
B.热稳定性: 小于 ;金刚石大于硅晶体
C.沸点: 大于 ;正丁烷大于异丁烷
D.酸性: 大于 ; 大于
11.氮、砷元素为同主族元素。下列说法正确的是
A.基态As原子的电子排布式为[Ar]4s24p3
B.第一电离能:I(N)AsH
3 3
12.用氨水吸收硫酸工厂尾气中的 ,发生的反应为: 。下列说法
正确的是
资料收集整理【淘宝店铺:向阳百分百】A. 分子的空间结构呈V形
B. 的电子式为
C. 是非极性分子
D. 中的S原子的杂化轨道类型为 杂化
13.由铁及其化合物可制得FeSO ·7H O、FeCl 、KFeO 等化工产品,它们在生产、生活中具有广泛应用。
4 2 3 2 4
已知NO能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO 。高炉炼铁的反应为 Fe O(s)+3CO(g)=2Fe(s)
4 2 5 4 2 3
+3CO(g) ΔH=-23.5 kJ· mol-1。下列有关说法不正确的是
2
A.如图所示γFe的晶胞中,铁原子的配位数为12
B.配离子为[Fe(NO)(H O) ]2+,配位数为6
2 5
C.基态铁原子的核外电子排布式为1s22s22p63s23p63d74s1
D.该配合物中阴离子空间结构为正四面体形
14.W、X、Y、Z是原子序数依次增大的短周期主族元素。W是自然界中形成化合物最多的元素,其核外
电子有4种空间运动状态;X的简单氢化物与其最高价氧化物对应的水化物反应生成化合物甲;Y是短周
期主族中原子半径最大的元素;Z与Y处于同一周期,且Z元素所形成的简单单质常温常压下为气态。下
列说法正确的是
A.Y的第一电离能在四种元素中最小
B. 是含极性键的极性分子
C. 的中心原子的杂化轨道类型为
D. 晶胞中含 1 个 和一个
15.几种晶体的晶胞结构如图所示。已知: 、 均为立方晶胞。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.相同条件下,熔点:
B.另一种 晶胞结构中,当 处于体心时,则 处于棱心
C. 晶胞中a点原子坐标参数为 ,则b点原子坐标参数为
D.三种晶体中,Ca的配位数均为8
二、填空题(本题包括4小题,共55分)
16.(12分)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂
微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:
(1)铜位于周期表中 区。
(2)基态二价铜离子的电子排布式为 ,已知高温下Cu O比CuO更稳定,试从核外电子排布角
2
度解释 。
(3)硼核外电子的运动状态的概率密度分布可用 形象化描述。
(4)Fe3+的价电子排布图为 。
(5)N、O、Se三种元素中的第一电离能最大的为: 。
17.(15分)根据杂化轨道理论可以判断分子的空间结构,试根据相关知识填空:
(1)AsCl 分子的空间结构为 ,其中As的杂化轨道类型为 。
3
(2)CH COOH中C原子轨道杂化类型为 。
3
(3)一种有机化合物的结构简式为:
①该分子中有 个sp2杂化碳原子; 个sp3杂化碳原子;
资料收集整理【淘宝店铺:向阳百分百】②该分子中有 个sp2-sp3σ键; 个sp3-sp3σ键。
(4)SCN-与NO 的结构相同,微粒呈 形,中心原子都采取 杂化。
(5)CO 、NO 等微粒具有相同的原子个数,它们的价电子总数都是 ,空间结构呈 形,中心原
子都采取 杂化。
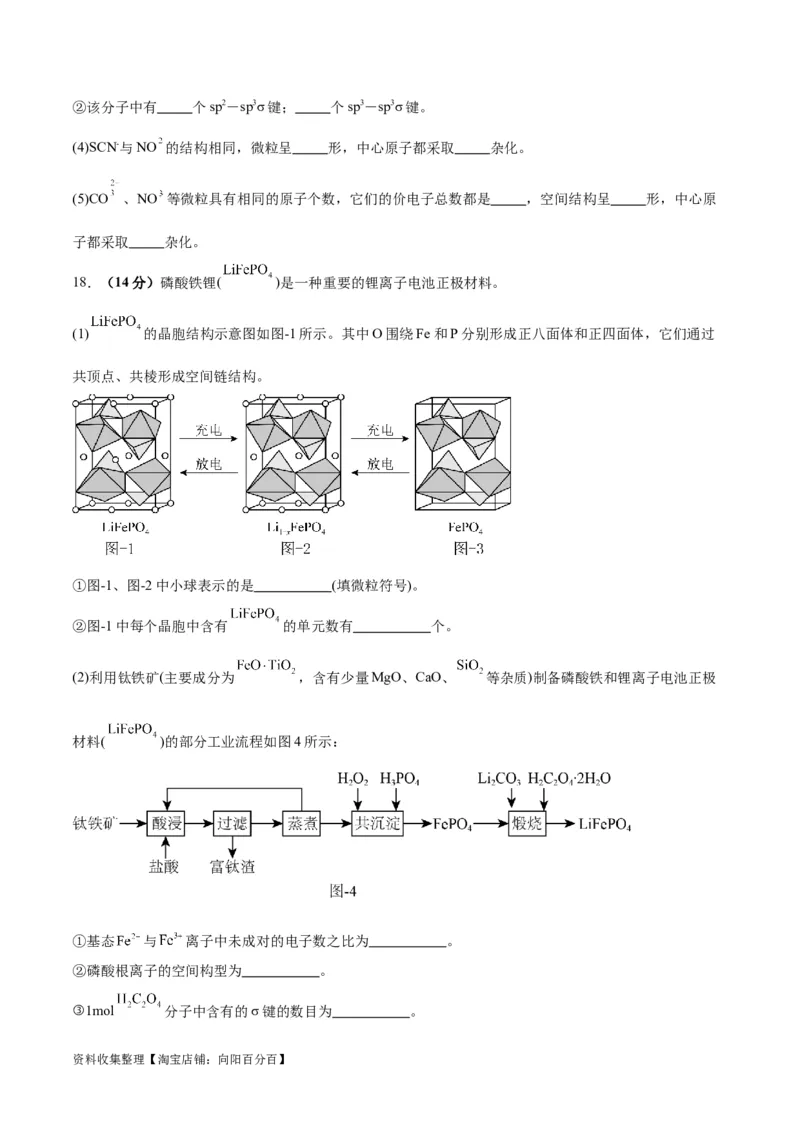
18.(14分)磷酸铁锂( )是一种重要的锂离子电池正极材料。
(1) 的晶胞结构示意图如图-1所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过
共顶点、共棱形成空间链结构。
①图-1、图-2中小球表示的是 (填微粒符号)。
②图-1中每个晶胞中含有 的单元数有 个。
(2)利用钛铁矿(主要成分为 ,含有少量MgO、CaO、 等杂质)制备磷酸铁和锂离子电池正极
材料( )的部分工业流程如图4所示:
①基态 与 离子中未成对的电子数之比为 。
②磷酸根离子的空间构型为 。
③1mol 分子中含有的σ键的数目为 。
资料收集整理【淘宝店铺:向阳百分百】④煅烧得到 的化学方程式为 。
⑤制备 的过程中,理论上所需17%双氧水与 的质量比为 。
19.(14分)最近我国学者研究得出三金属Fe-Co-Ni、硼的氧化物复合聚吡咯/rGO协同表现出最佳增强
电解析氧。回答下列问题:
(1)基态Fe2+的价层电子排布图为 ;基态Fe2+与Fe3+的未成对电子数之比为 ,第四电离能
I(Fe) (填“大于”或“小于”)I(Co)。
4 4
(2)硼的氧化物有α-B O、β-B O 及γ-B O 等。γ-B O 玻璃状氧化硼的结构如下图所示。
2 3 2 3 2 3 2 3
B属于 区元素,γ-B O 中硼原子的杂化方式是 。
2 3
(3)吡咯、呋喃及噻吩均是杂环化合物,它们的沸点如下:
吡咯 呋喃 噻吩
结构简式
沸点/℃ 131 31.36 84
①C、N、O的电负性由大到小的顺序为 。
②吡咯属于 晶体。
③沸点:吡咯>噻吩>呋喃,原因是 。
(4)NiFeGa是磁性形状记忆合金,晶胞参数为a pm。
2
设N 为阿伏加德罗常数的值,则晶体的密度为 g·cm-3(列出计算式)。
A
资料收集整理【淘宝店铺:向阳百分百】