文档内容
第三章 金属及其化合物
专题讲座(三) 热重分析中的物质成分的判断(精练)
完卷时间:50分钟
可能用到的相对原子质量:H1 C12 N14 O16 Mg12 Al27 S32 Ca40 V51 Cr52 Mn55 Fe65 Zn65 Ce140
pb207
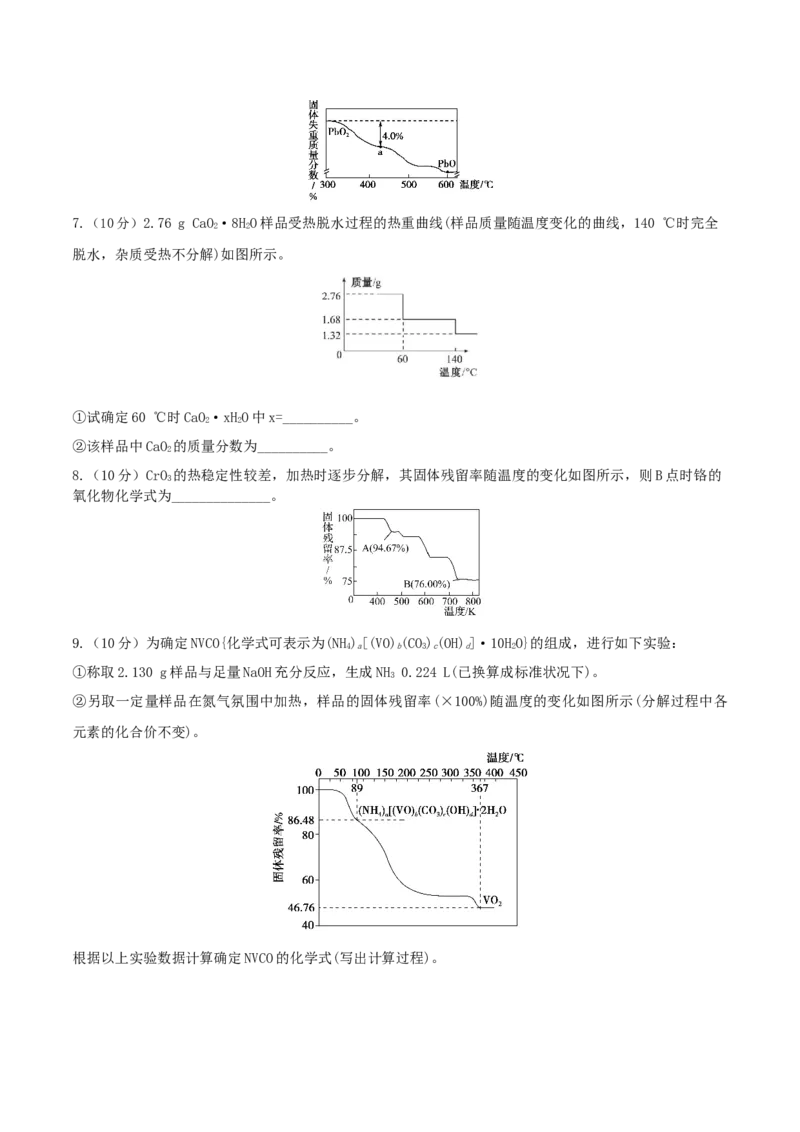
1.(10分)8.34 g FeSO·7HO(M=278 g·mol -1)样品受热脱水过程的热重曲线(样品质量随温度变化的曲
4 2
线)如图所示,下列说法正确的是( )
A.温度为78 ℃时,固体物质M的化学式为FeSO·5HO
4 2
B.温度为159 ℃时固体N的化学式为FeSO·2HO
4 2
C.在隔绝空气条件下,由N得到P的化学方程式为FeSO·HO FeSO+HO
4 2 4 2
D.取适量380 ℃时所得的样品P,隔绝空气加热至650 ℃,得到一种固体物质Q,同时有两种无色气体生成,Q
的化学式为FeO
3 4
2.(10分)将Ce(SO)·4HO(摩尔质量为404 g·mol-1)在空气中加热,样品的固体残留率(固体样品
4 2 2
的剩余质量/固体样品的起始质量×100%)随温度的变化如下图所示。
当固体残留率为70.3%时,所得固体可能为(填字母)。
A.Ce(SO) B.Ce(SO4) C.CeOSO
4 2 2 3 4
3.(10分)PbO 受热会随温度升高逐步分解。称取23.9 g PbO,将其加热分解,受热分解过程中固体质量
2 2
随温度的变化如图所示。A点与C点对应物质的化学式分别为__________、__________。
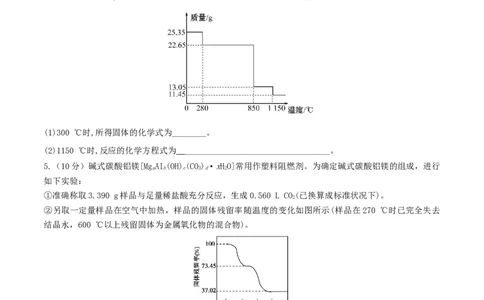
4.(10分)25.35 g MnSO·HO样品受热分解过程的热重曲线(样品质量随温度变化的曲线)如下图所示:
4 2
(1)300 ℃时,所得固体的化学式为________。
(2)1150 ℃时,反应的化学方程式为 __________________________________。
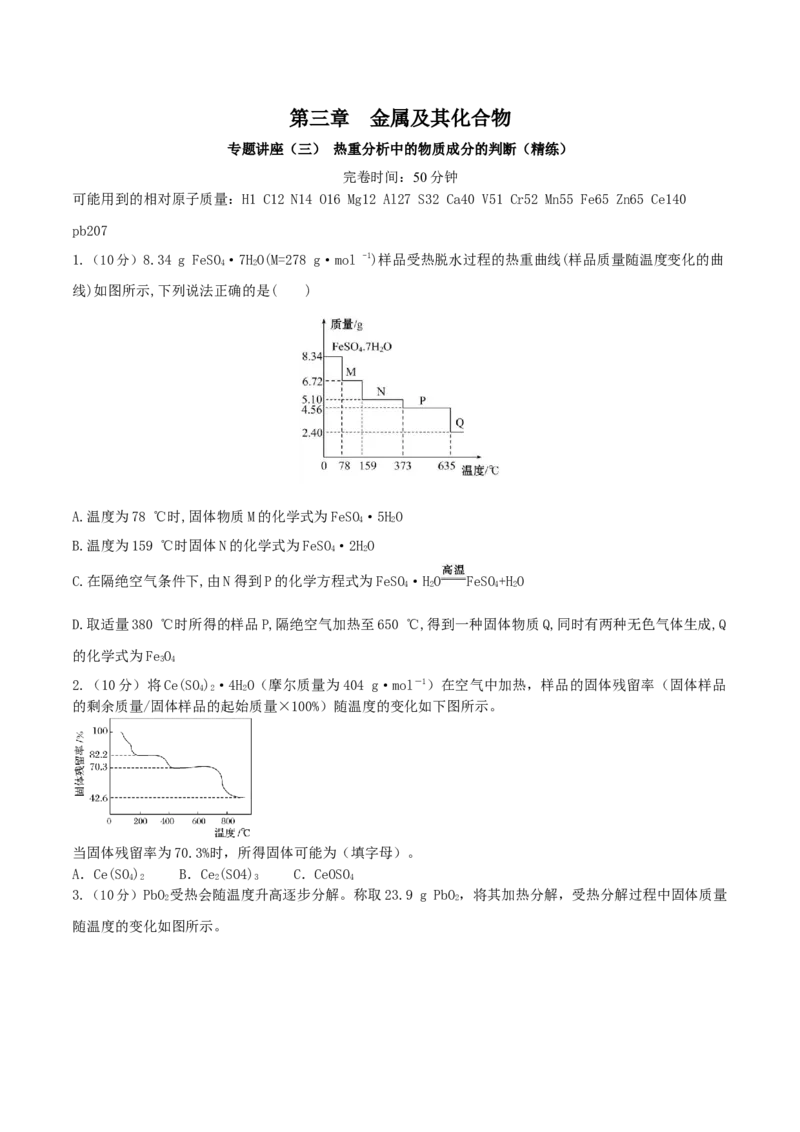
5.(10分)碱式碳酸铝镁[MgAl(OH)(CO)·xHO]常用作塑料阻燃剂。为确定碱式碳酸铝镁的组成,进行
a b c 3 d 2
如下实验:
①准确称取3.390 g样品与足量稀盐酸充分反应,生成0.560 L CO(已换算成标准状况下)。
2
②另取一定量样品在空气中加热,样品的固体残留率随温度的变化如图所示(样品在270 ℃时已完全失去
结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO)=________。
6.(10分)PbO 在加热过程发生分解的失重曲线如图所示,已知失重曲线上的 a点样品失重4.0%(即
2
×100%)的残留固体。若a点固体组成表示为PbO 或mPbO·nPbO,列式计算x值和m∶n值_________。
x 27.(10分)2.76 g CaO·8HO样品受热脱水过程的热重曲线(样品质量随温度变化的曲线,140 ℃时完全
2 2
脱水,杂质受热不分解)如图所示。
①试确定60 ℃时CaO·xHO中x=__________。
2 2
②该样品中CaO 的质量分数为__________。
2
8.(10分)CrO 的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示,则B点时铬的
3
氧化物化学式为______________。
9.(10分)为确定NVCO{化学式可表示为(NH)[(VO)(CO)(OH)]·10HO}的组成,进行如下实验:
4 a b 3 c d 2
①称取2.130 g样品与足量NaOH充分反应,生成NH 0.224 L(已换算成标准状况下)。
3
②另取一定量样品在氮气氛围中加热,样品的固体残留率(×100%)随温度的变化如图所示(分解过程中各
元素的化合价不变)。
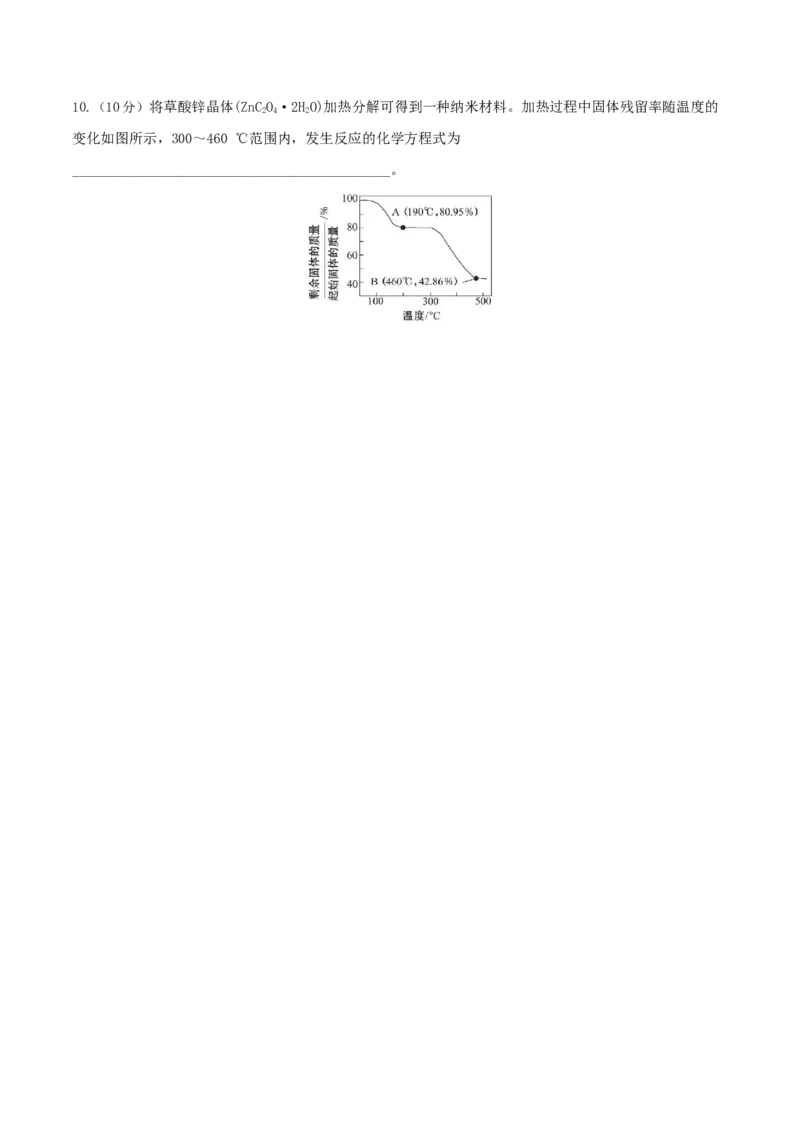
根据以上实验数据计算确定NVCO的化学式(写出计算过程)。10.(10分)将草酸锌晶体(ZnCO·2HO)加热分解可得到一种纳米材料。加热过程中固体残留率随温度的
2 4 2
变化如图所示,300~460 ℃范围内,发生反应的化学方程式为
_____________________________________________。