文档内容
第二章 化学物质及其变化
专题讲座(二) 整合有效信息书写陌生化学(离子)方程式 (精练)
完卷时间:50分钟
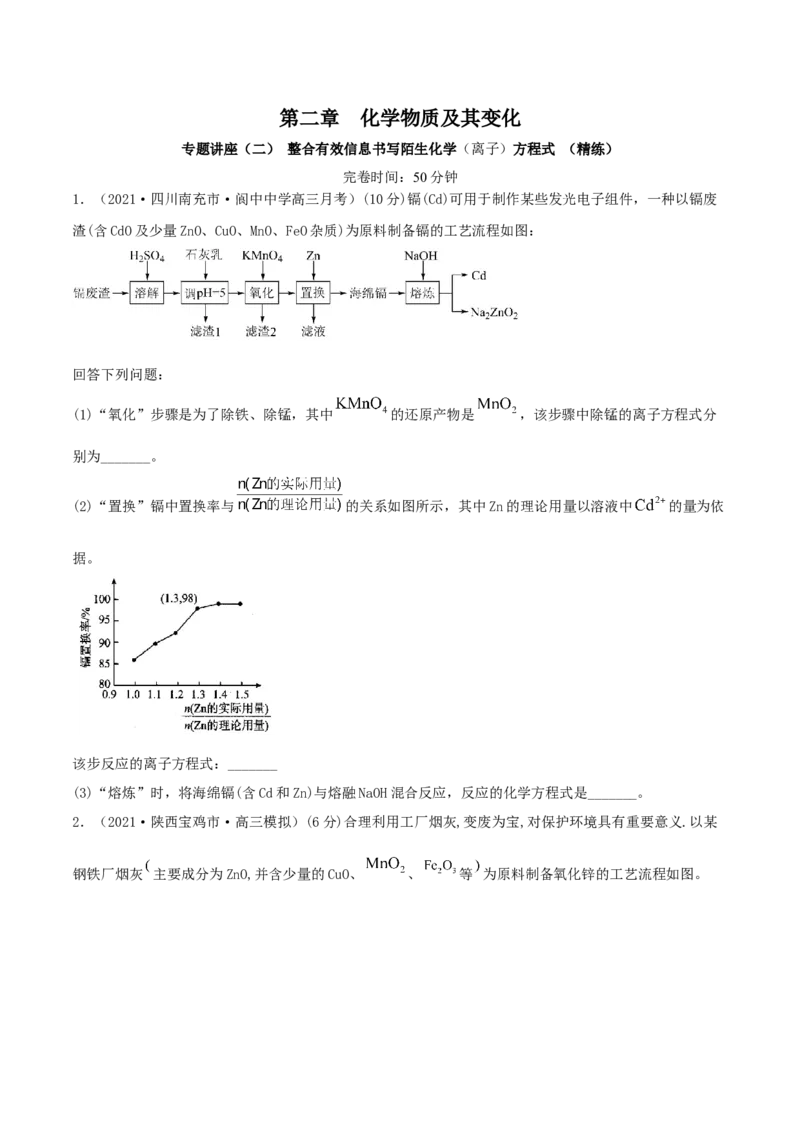
1.(2021·四川南充市·阆中中学高三月考)(10分)镉(Cd)可用于制作某些发光电子组件,一种以镉废
渣(含CdO及少量ZnO、CuO、MnO、FeO杂质)为原料制备镉的工艺流程如图:
回答下列问题:
(1)“氧化”步骤是为了除铁、除锰,其中 的还原产物是 ,该步骤中除锰的离子方程式分
别为_______。
(2)“置换”镉中置换率与 的关系如图所示,其中Zn的理论用量以溶液中 的量为依
据。
该步反应的离子方程式:_______
(3)“熔炼”时,将海绵镉(含Cd和Zn)与熔融NaOH混合反应,反应的化学方程式是_______。
2.(2021·陕西宝鸡市·高三模拟)(6分)合理利用工厂烟灰,变废为宝,对保护环境具有重要意义.以某
钢铁厂烟灰 主要成分为ZnO,并含少量的CuO、 、 等 为原料制备氧化锌的工艺流程如图。回答下列问题:
(1)“除杂”工序加入过量的A是一种金属,该反应的离子方程式为 _______ 。
(2)ZnO与 NHHCO 和NH·HO 的混合物三者在“浸取”反应时离子方程式为 _______ 。
4 3 3 2
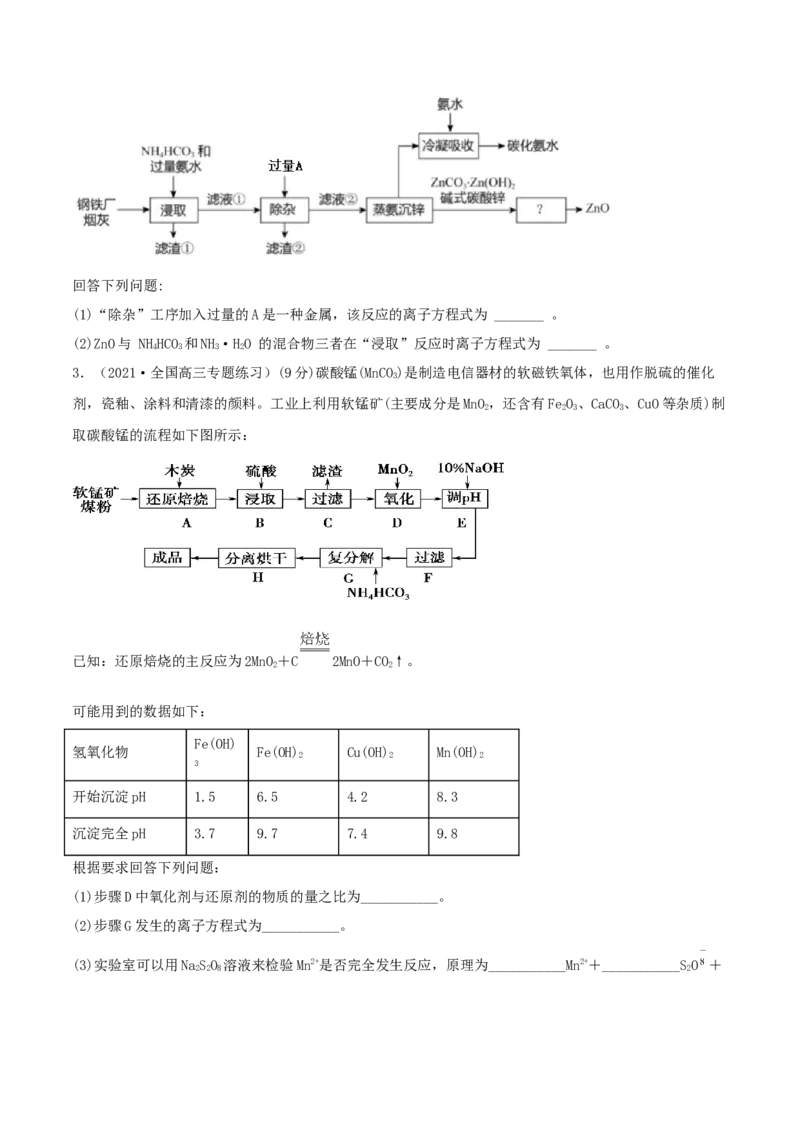
3.(2021·全国高三专题练习)(9分)碳酸锰(MnCO)是制造电信器材的软磁铁氧体,也用作脱硫的催化
3
剂,瓷釉、涂料和清漆的颜料。工业上利用软锰矿(主要成分是MnO,还含有FeO、CaCO、CuO等杂质)制
2 2 3 3
取碳酸锰的流程如下图所示:
已知:还原焙烧的主反应为2MnO+C 2MnO+CO↑。
2 2
可能用到的数据如下:
Fe(OH)
氢氧化物 Fe(OH) Cu(OH) Mn(OH)
2 2 2
3
开始沉淀pH 1.5 6.5 4.2 8.3
沉淀完全pH 3.7 9.7 7.4 9.8
根据要求回答下列问题:
(1)步骤D中氧化剂与还原剂的物质的量之比为___________。
(2)步骤G发生的离子方程式为___________。
(3)实验室可以用NaSO 溶液来检验Mn2+是否完全发生反应,原理为___________Mn2++___________SO +
2 2 8 2___________HO→___________H++___________SO +___________MnO 。试配平该离子方程式。
2
___________
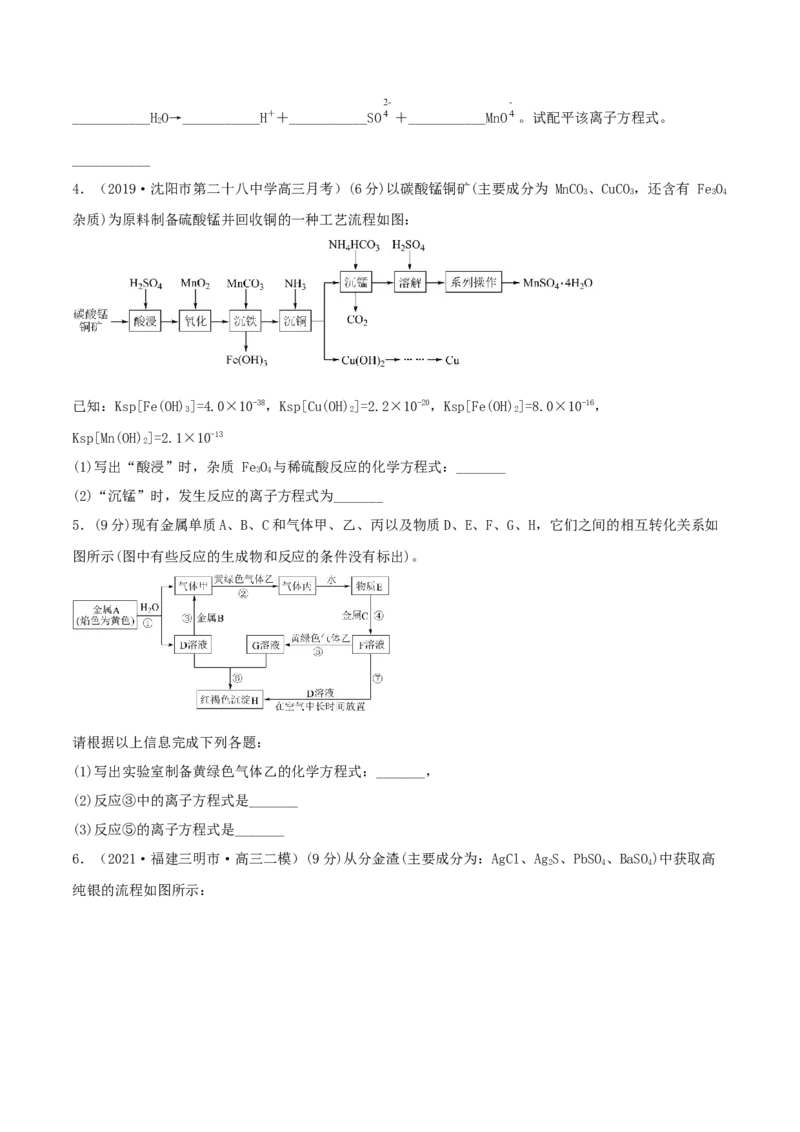
4.(2019·沈阳市第二十八中学高三月考)(6分)以碳酸锰铜矿(主要成分为 MnCO、CuCO,还含有 FeO
3 3 3 4
杂质)为原料制备硫酸锰并回收铜的一种工艺流程如图:
已知:Ksp[Fe(OH)]=4.0×10-38,Ksp[Cu(OH)]=2.2×10-20,Ksp[Fe(OH)]=8.0×10-16,
3 2 2
Ksp[Mn(OH)]=2.1×10-13
2
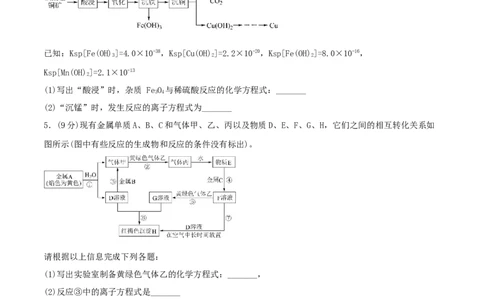
(1)写出“酸浸”时,杂质 FeO 与稀硫酸反应的化学方程式:_______
3 4
(2)“沉锰”时,发生反应的离子方程式为_______
5.(9分)现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如
图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:
(1)写出实验室制备黄绿色气体乙的化学方程式:_______,
(2)反应③中的离子方程式是_______
(3)反应⑤的离子方程式是_______
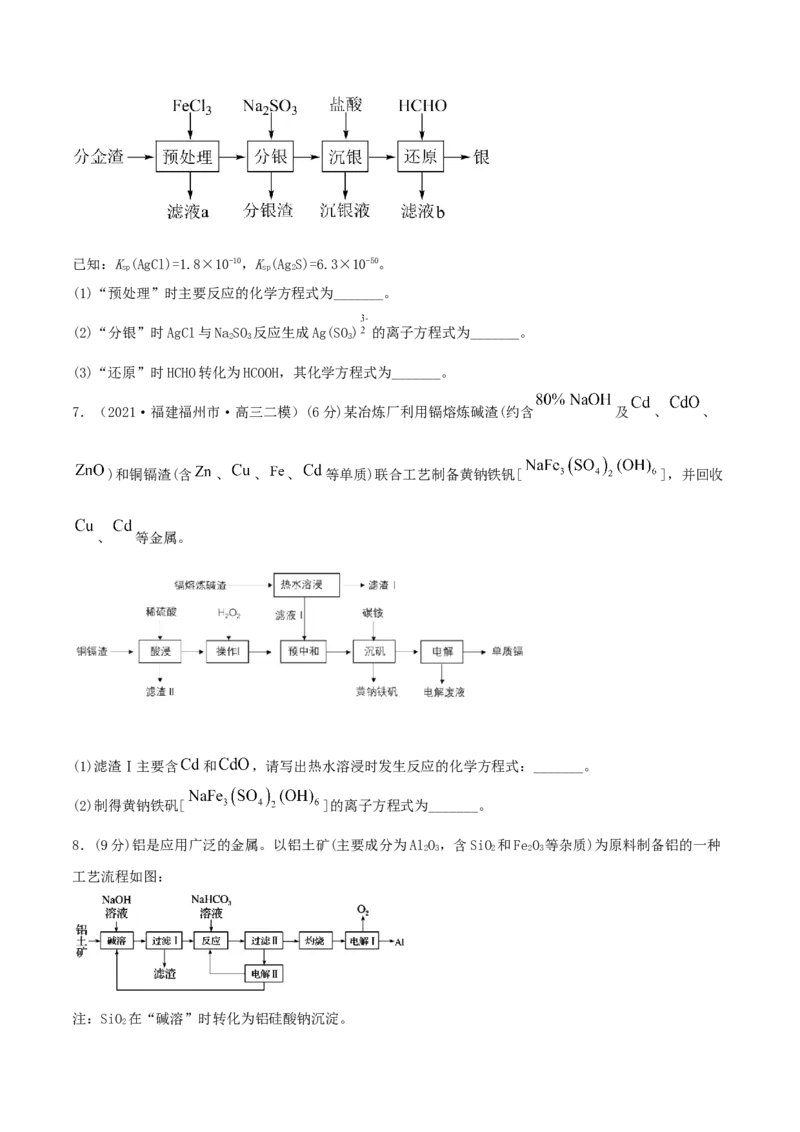
6.(2021·福建三明市·高三二模)(9分)从分金渣(主要成分为:AgCl、AgS、PbSO、BaSO)中获取高
2 4 4
纯银的流程如图所示:已知:K(AgCl)=1.8×10-10,K(AgS)=6.3×10-50。
sp sp 2
(1)“预处理”时主要反应的化学方程式为_______。
(2)“分银”时AgCl与NaSO 反应生成Ag(SO) 的离子方程式为_______。
2 3 3
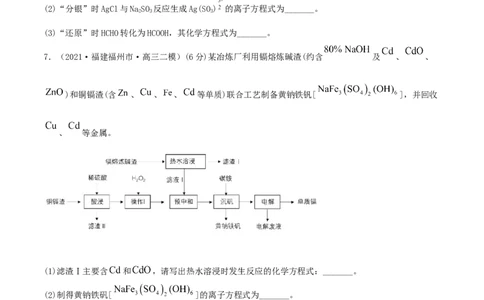
(3)“还原”时HCHO转化为HCOOH,其化学方程式为_______。
7.(2021·福建福州市·高三二模)(6分)某冶炼厂利用镉熔炼碱渣(约含 及 、 、
)和铜镉渣(含 、 、 、 等单质)联合工艺制备黄钠铁钒[ ],并回收
、 等金属。
(1)滤渣Ⅰ主要含 和 ,请写出热水溶浸时发生反应的化学方程式:_______。
(2)制得黄钠铁矾[ ]的离子方程式为_______。
8.(9分)铝是应用广泛的金属。以铝土矿(主要成分为AlO,含SiO 和FeO 等杂质)为原料制备铝的一种
2 3 2 2 3
工艺流程如图:
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
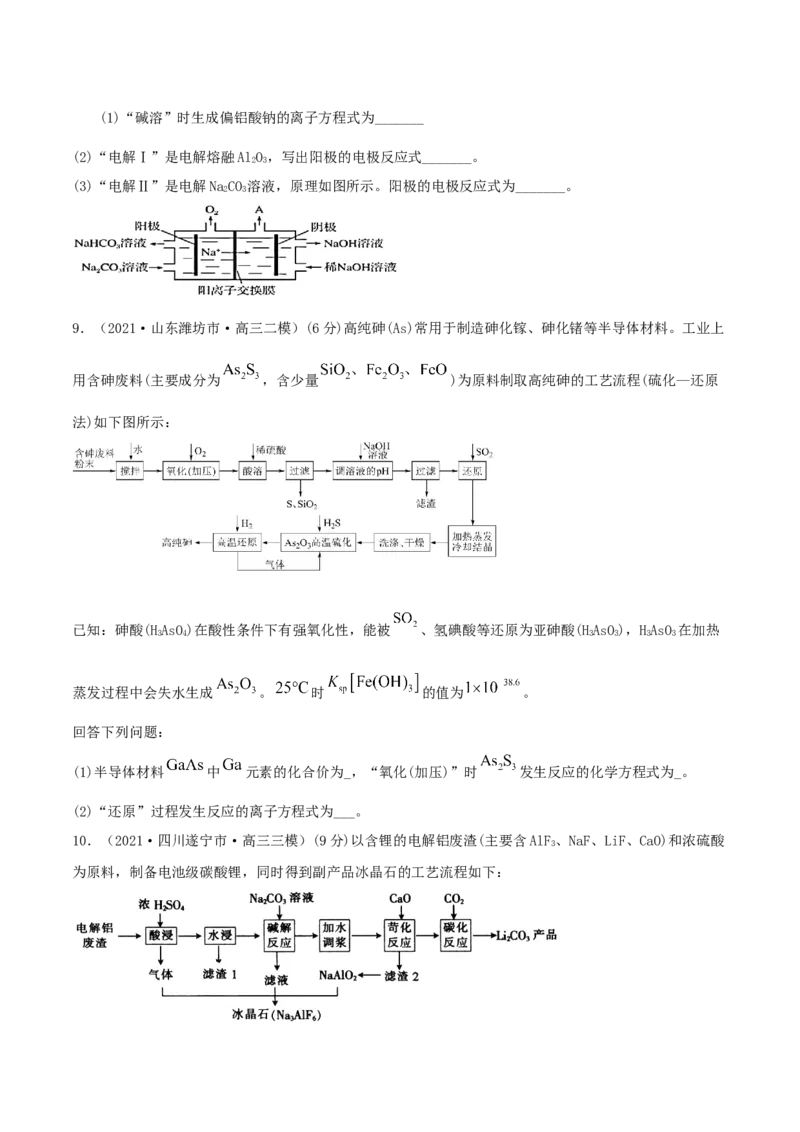
2(1)“碱溶”时生成偏铝酸钠的离子方程式为_______
(2)“电解Ⅰ”是电解熔融AlO,写出阳极的电极反应式_______。
2 3
(3)“电解Ⅱ”是电解NaCO 溶液,原理如图所示。阳极的电极反应式为_______。
2 3
9.(2021·山东潍坊市·高三二模)(6分)高纯砷(As)常用于制造砷化镓、砷化锗等半导体材料。工业上
用含砷废料(主要成分为 ,含少量 )为原料制取高纯砷的工艺流程(硫化—还原
法)如下图所示:
已知:砷酸(HAsO)在酸性条件下有强氧化性,能被 、氢碘酸等还原为亚砷酸(HAsO),HAsO 在加热
3 4 3 3 3 3
蒸发过程中会失水生成 。 时 的值为 。
回答下列问题:
(1)半导体材料 中 元素的化合价为_,“氧化(加压)”时 发生反应的化学方程式为_。
(2)“还原”过程发生反应的离子方程式为___。
10.(2021·四川遂宁市·高三三模)(9分)以含锂的电解铝废渣(主要含AlF、NaF、LiF、CaO)和浓硫酸
3
为原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如下:已知:LiOH易溶于水,LiCO 微溶于水。回答下列问题:
2 3
(1)碱解反应中,同时得到气体和沉淀,反应的离子方程式为___________。
(2)上述流程得到的副产品冰晶石的化学方程式___________
(3)电池级LiCO 可由高纯度LiOH转化而来。将电池级LiCO 和C、FePO 高温下反应,生成LiFePO 和一种
2 3 2 3 4 4
可燃性气体,该反应的化学方程式为___________。
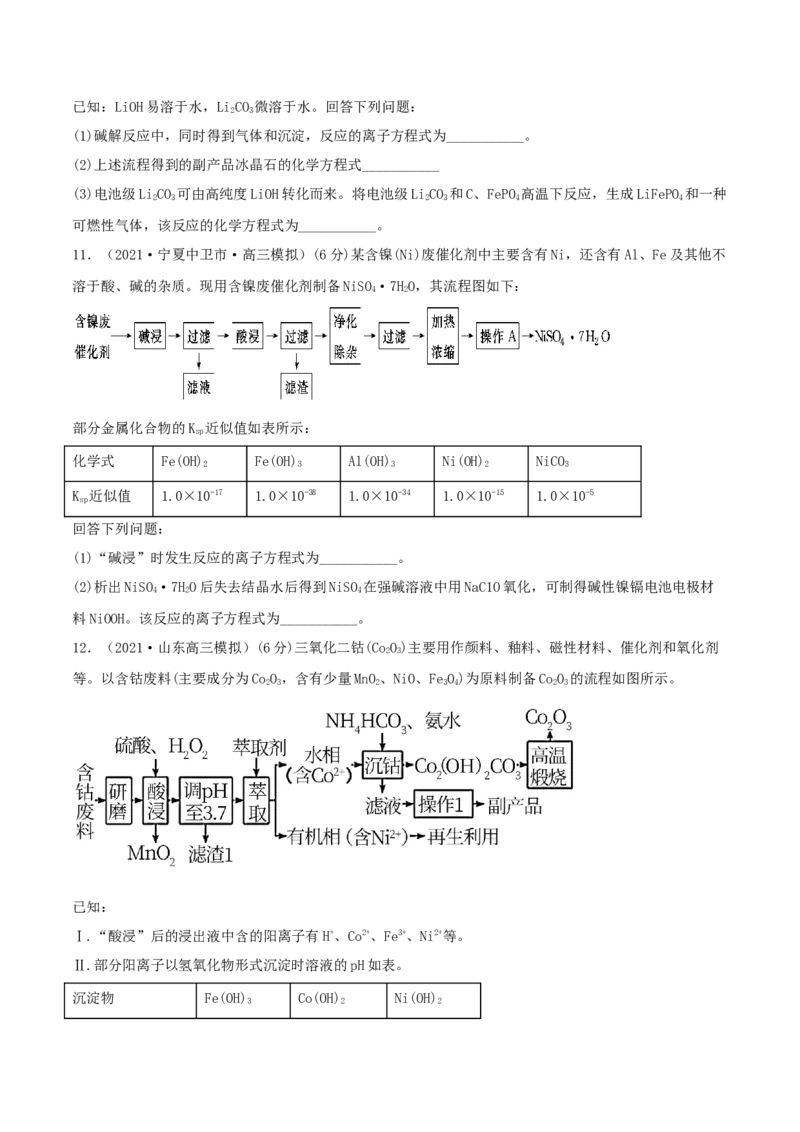
11.(2021·宁夏中卫市·高三模拟)(6分)某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Fe及其他不
溶于酸、碱的杂质。现用含镍废催化剂制备NiSO·7HO,其流程图如下:
4 2
部分金属化合物的K 近似值如表所示:
sp
化学式 Fe(OH) Fe(OH) Al(OH) Ni(OH) NiCO
2 3 3 2 3
K 近似值 1.0×10-17 1.0×10-38 1.0×10-34 1.0×10-15 1.0×10-5
sp
回答下列问题:
(1)“碱浸”时发生反应的离子方程式为___________。
(2)析出NiSO·7HO后失去结晶水后得到NiSO 在强碱溶液中用NaC1O氧化,可制得碱性镍镉电池电极材
4 2 4
料NiOOH。该反应的离子方程式为___________。
12.(2021·山东高三模拟)(6分)三氧化二钴(CoO)主要用作颜料、釉料、磁性材料、催化剂和氧化剂
2 3
等。以含钴废料(主要成分为CoO,含有少量MnO、NiO、FeO)为原料制备CoO 的流程如图所示。
2 3 2 3 4 2 3
已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
沉淀物 Fe(OH) Co(OH) Ni(OH)
3 2 2完全沉淀时的pH 3.7 9.0 9.2
①“酸浸”时发生的主要反应是___(写离子方程式)。
②写出高温煅烧时发生的化学反应方程式___。
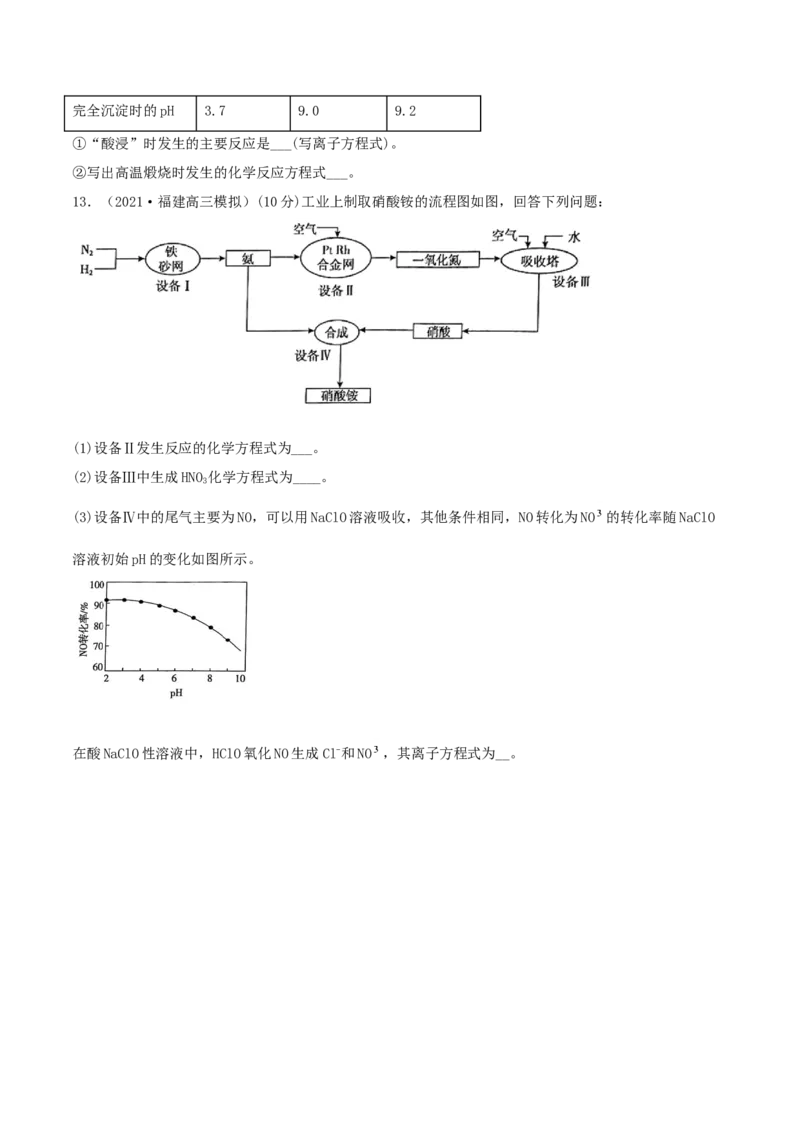
13.(2021·福建高三模拟)(10分)工业上制取硝酸铵的流程图如图,回答下列问题:
(1)设备Ⅱ发生反应的化学方程式为___。
(2)设备Ⅲ中生成HNO 化学方程式为____。
3
(3)设备Ⅳ中的尾气主要为NO,可以用NaClO溶液吸收,其他条件相同,NO转化为NO 的转化率随NaClO
溶液初始pH的变化如图所示。
在酸NaClO性溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为__。